芳香分子的反应
激活和去活化组织在亲电芳香取代反应
最后更新:2023年2月3日|
激活和去活化组织在亲电芳香取代反应
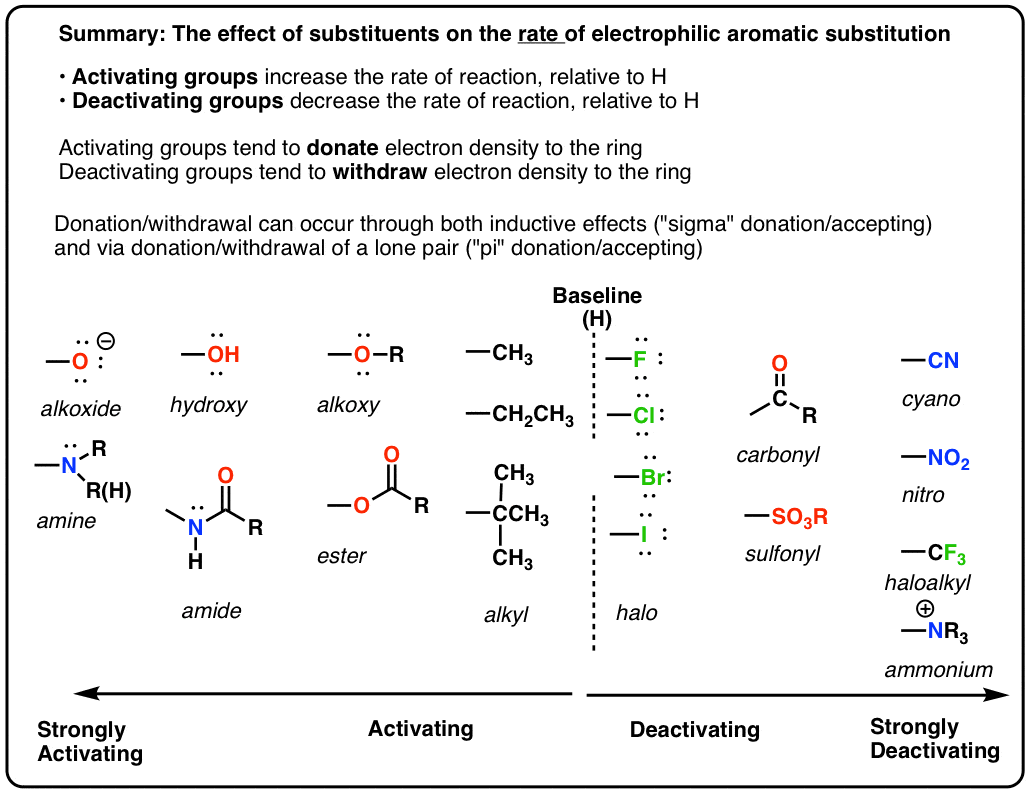
- 亲电芳香取代(EAS)反应的速率大大影响基团的环。多电子芳环,反应越快
- 组可以给出电子密度环使东亚峰会反应更快。
- 如果一个取代基的增加反应的速率相对于H叫做激活。如果它降低率相对于H安静下来。(这些利率需要通过实验测定)。
- 重要!或者和NR组2那似乎像他们应该安静下来,因为它们的电负性激活因为他们可以捐一个孤对电子环通过共振。
这篇文章有很多,所以这是一个快速指数:
表的内容
- 激活和去活化组
- 测量反应速率可以提供洞察机制
- “激活”和“去活化”组织——一个定义
- “σ”(σ)体和受体(或称为“感应效应”)
- π(π)体和受体(经常称为“共振”)
- 氧和氮含孤对高度激活时直接保税戒指
- 卤素(F, Cl, Br,我)去活化
- π受体组织强烈安静下来
- 一个表的激活和去活化组
- 总结:这告诉了我们什么亲电芳香取代的机制?
- 笔记
- (高级)引用和进一步阅读
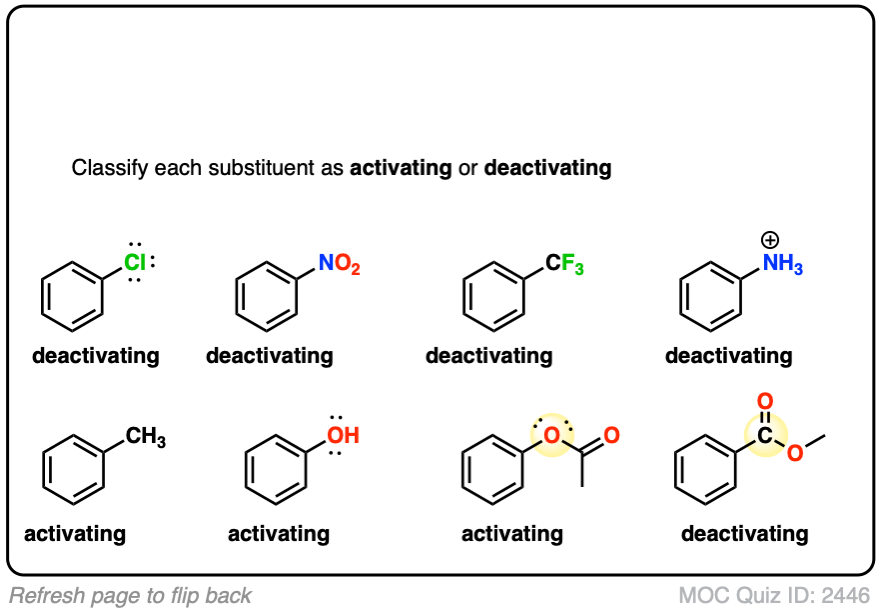
1。激活和去活化组
最后文章在本系列中我们介绍了亲电芳香取代。一般情况下: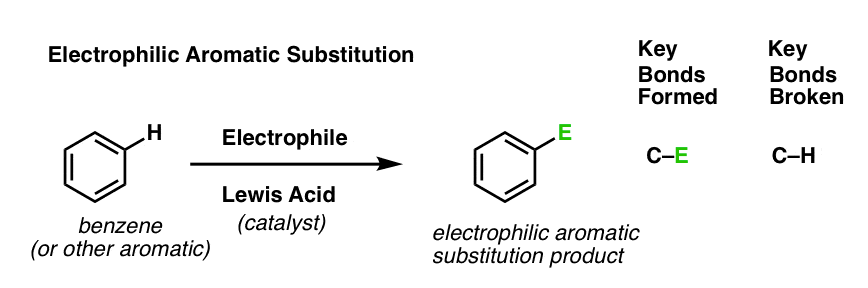
为什么这是一个取代反应,你问?因为我们形成和打破债券在同一个碳。我们形式一部(“E”是一个通用的术语“亲电子原子”)我们打破碳氢键。
(至于“E”的具体身份,我们提到的六个关键亲电芳香取代反应在过去的文章(溴化、氯化、硝化、sulfonylation傅克烷基化和傅克酰化),最终我们会详细深入。但现在还不是时候。]
如果的总结什么发生,下一个显而易见的问题是:如何它会发生吗?
换句话说,机理是什么?
义务pre-mechanism演讲:你不能确定化学反应的机制是通过逻辑推理从第一原则。当然,你可以猜测——甚至是好的!但最终测试机械的假设是符合实验,这通常涉及很多实验室工作。你教入门课程是tippy-topmost层冰山上的雪。我们给你最好的答案,回想起来看起来明显。你没有看到的是所有的失败,错误的结果,错误的假设发生沿道路确定正确的机制。然而,这些反应的机制,您将了解没有明显的发现者,谁是最聪明的和最好的化学家的时间。记住这一点。
2。测量反应速率可以提供洞察机制
确定机制而言,最好的工具之一在我们实验阿森纳是衡量的能力反应率。
通过测量效果的微小调整实验条件(如反应物的结构、温度、溶剂)时率,我们可以收集有用的见解如何运营“引擎盖下”的反应。
上述参数,改变基质(反应物)可能是最强大的方法来探测机制,因为它允许您调整负电子(亲核)或electron-poor(亲电)。
让我告诉你我的意思。
让我们随意挑选一个亲电芳香取代反应:硝化反应。
- 我们知道,通过添加硝酸和H2所以4,苯可以进行硝化形成硝基苯(c不打破碳氢键,形式2)
- 我们甚至可以测量这个反应的速率在给定温度、浓度和溶剂。
- 使用相同的实验条件我们可以测量时的反应速率甲苯(甲苯,C6H5CH3)是用作基质代替苯。
- 甲苯的硝化反应23倍比苯。(Ref 1]
- 使用相同的实验条件,我们也可以使用trifluoromethylbenzene (C6H5CF3)作为底物,测定反应速率。
- trifluoromethylbenzene的硝化反应40000年时间慢比苯(2.5×105)。
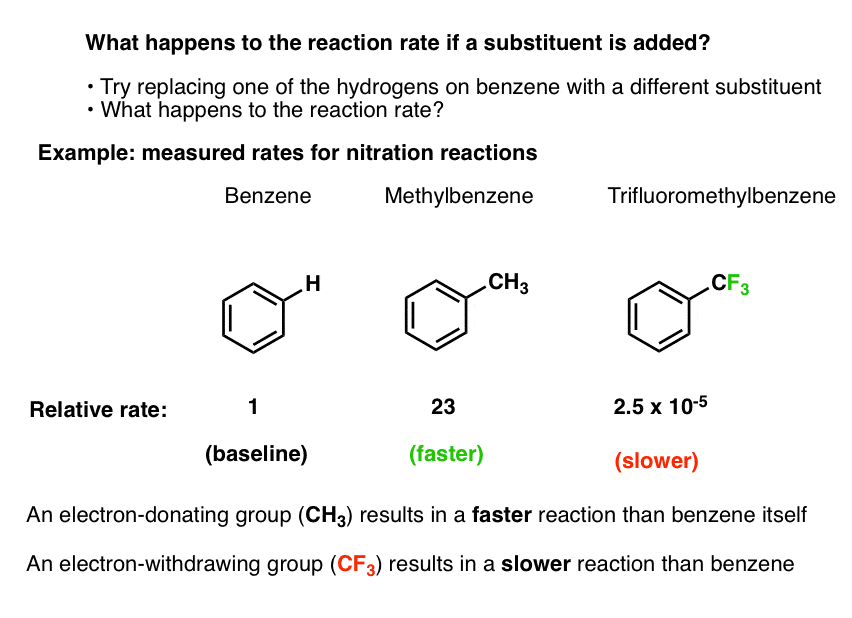
底线:如果我们交换一个氢甲基苯,反应更快。如果我们交换一个氢trifluoromethyl组,反应慢。
这种模式是一般为其他亲电芳香取代反应(氯化、溴化、傅克反应等)。
3所示。“激活”和“去活化”组织——一个定义
到一组吧激活那增加一个亲电芳香取代反应相对于氢。我们刚刚看到,CH3是一个完美的例子,一个激活组;当我们用一个氢苯CH3硝化反应的速率增加。
一个组才会安静下来,另一方面,减少一个亲电芳香取代反应相对于氢。trifluoromethyl集团CF3,大大降低了硝化速率时代替苯环上的氢。
这个定义最终是基于实验反应速率数据。它没有告诉我们为什么每一组加速或降低利率。“激活”和“去活化”只是指率上的每个取代基的影响,相对于H。
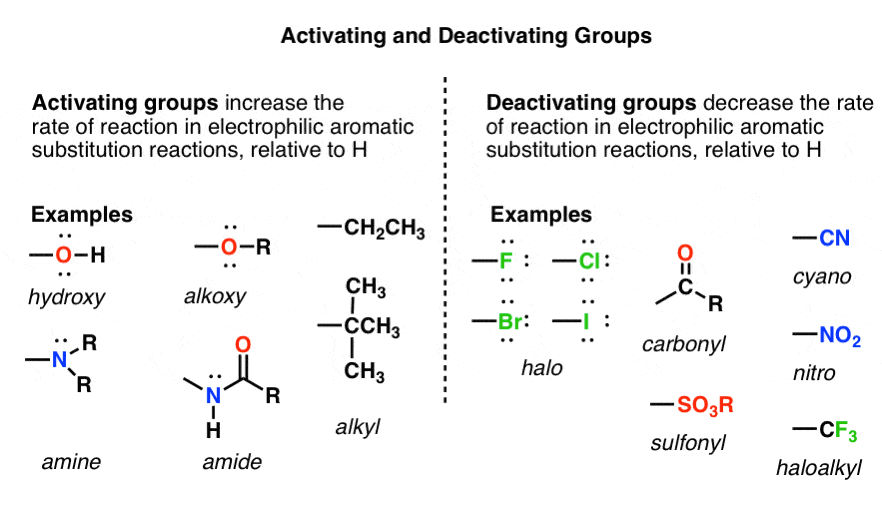
那么,好吧。为什么可能CH3提高反应的速率,CF3减少了吗?
4所示。“σ”(σ)体和受体(或称为“感应效应”)
让我们快速回想我们所知烷基团体(例如CH3)和haloalkyl团体(例如CF3),并试图解决这个问题。
在CH3,比氢碳原子的电负性更大(2.5)(2.2)。这意味着碳吸引多一点平等分享的电子密度与H共价键,导致部分负电荷(δ- - - - - -)碳和部分正电荷(δ+在氢)。这部分负电荷然后可以捐赠给一个相邻的原子。因此,我们倾向于认为CH3作为一个负电子的物种;一个电子- - - - - -捐赠。

在CF3电子在向相反的方向发展。三个高电负性(4.0)氟原子拉碳原子的电子密度(2.5),导致部分正电荷(δ+)碳。而不是捐赠电子密度,碳倾向接受(离开)从相邻原子的电子密度(这是熟悉的诱导效应)我们一般考虑CF3是一个electron-poor物种;一个电子受体。

因为这些操作仅通过电感的影响单键(“σ”或σ债券)这种行为有时被称为“σ捐赠”(CH3σ)或“接受”(CF3)。
这似乎是一个不错的假设
- 激活组电子基(相对于H)
- 去活化组织吸电子(相对于H)
5。π(π)体和受体(或称为“共振”)
σ捐赠和接受帮助我们理解的影响烷基组织亲电芳香取代反应。那么其他官能团呢?效果可能会说什么,羟基对硝化反应的速度吗?
测试时间。你认为-哦是吗激活(增加)或安静下来(减少)亲电芳香取代(如硝化)?猜测是好的!

基于我们刚才说的,这是完全可以理解的,如果你说,“安静下来”。毕竟,氧气是高电负性(3.4)通过感应,一把推开电子密度通过债券。换句话说,这是一个sigma-acceptor。
然而,事实是,哦,大大加快了速度,数量级比CH3所做的事。事实上我找不到好的率数据比较哦CH3因为在-哦,反应叫做,“扩散控制”。,大概的意思是:“当反应物接触亲电试剂,一个反应发生。”In other words, the –OH group is高度激活。
显然,这里别的必须除了氧气的诱导效应!
6。氧和氮含孤对高度激活时直接保税戒指
我们看到在我们的章在共振,羟基是优秀的π捐助者。氧原子上的孤可以形成一个π键和一个相邻原子含有一个可用的p轨道。
这种捐赠效果(或“共振”)必须大于electron-withdrawal通过感应效果,否则我们会观察到羟基都安静下来。
这同样适用于与孤氮组,如胺和酰胺(下图)。
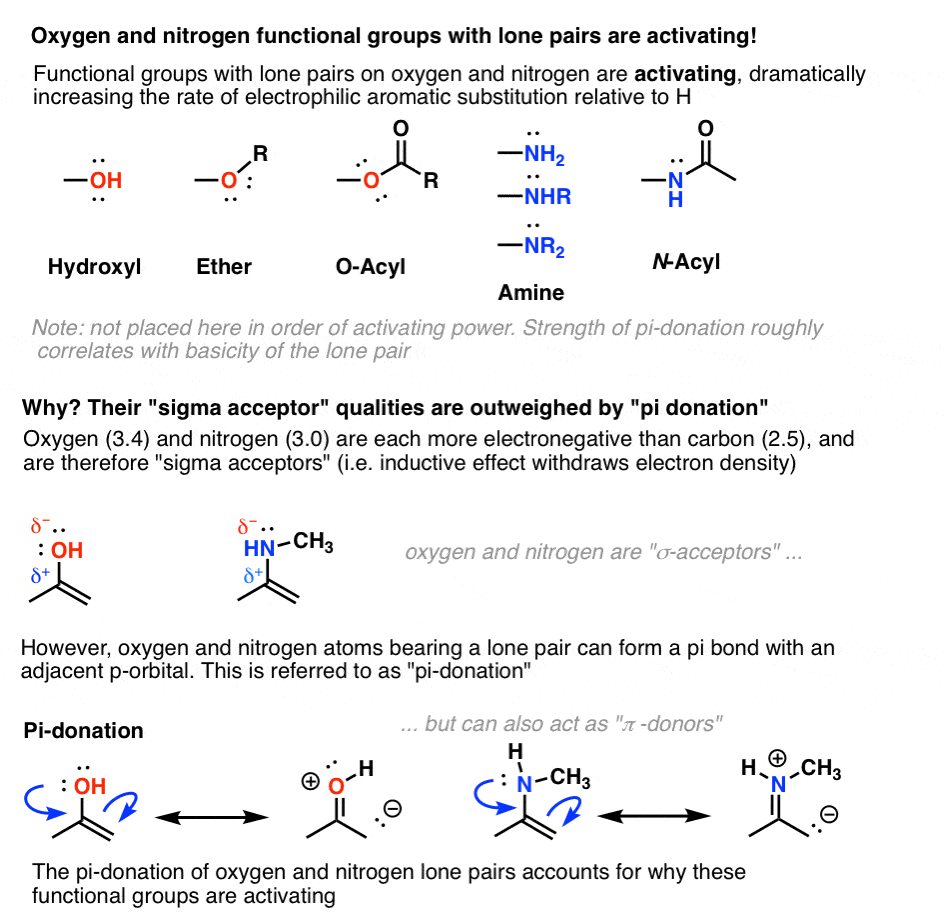
(一个测量的重要性pi-donation激活的本质胺在强酸性条件下他们的行为。如果氮孤对质子化了的与强酸或经历取代反应形成NR3+,pi-donation处于待发状态是不可能的,该组织变得强烈(见下表)。]
7所示。卤素(F, Cl, Br,我)去活化
并不是所有组π捐赠激活组织的能力。例如,卤素(F, Cl, Br,我)往往是安静下来。的亲电芳香取代反应氟苯、氯苯、溴苯和苯碘苯都比他们慢本身。在这些情况下,归纳影响(“σ接受”)似乎有更大的影响比任何pi-donation孤。(π捐赠<σ验收)。(为什么?]
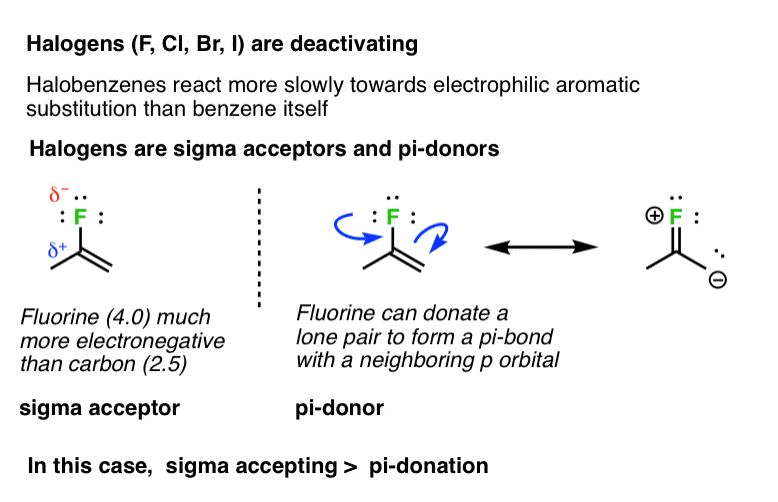
一个好的经验法则pi-donation能力是孤对的碱度。胺往往比氧更好的基地,这远比卤素更好的基地。
好吧。如果电子流在相反的方向呢?有相反的“π捐赠”?
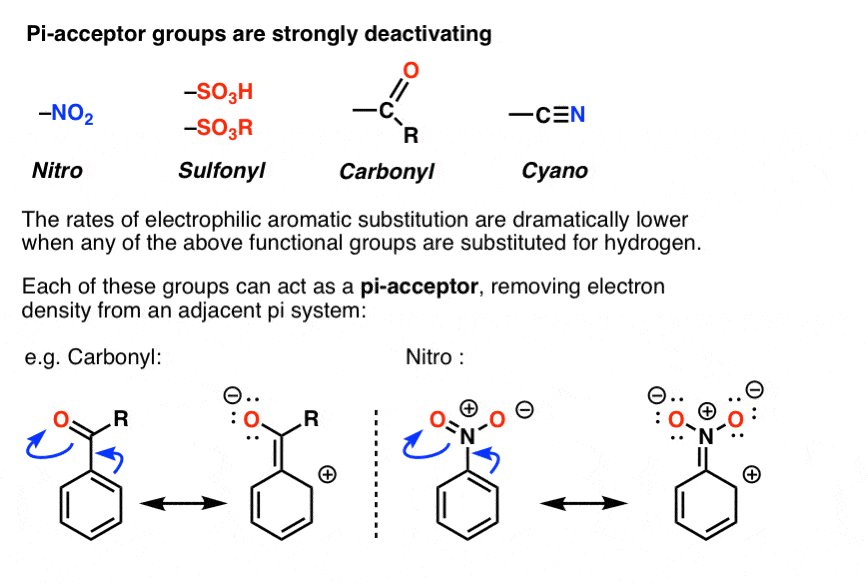
8。π受体组织强烈安静下来
是的!正如你可能已经知道的,相反的“pi-donor”是一个“π受体”。特定的官能团可以接受,而不是捐赠,从环π键,导致新孤对取代基原子。没有例子2,羰基组(C = O)、磺酰、含氰基的(CN)等等。这些组织是普遍安静下来,亲电芳香取代的速度放缓。
共振,可以画一个π键芳环的形成与atom绑定到环π键,从而形成一个新的孤对一个电负性原子的取代基。注意,这将导致一个正电荷的戒指!
那么,我们如何保持所有这些因素直接?
这是为什么我说的一个例子共振是最重要的关键概念为Org 2审查。在部分芳香化学卷土重来。
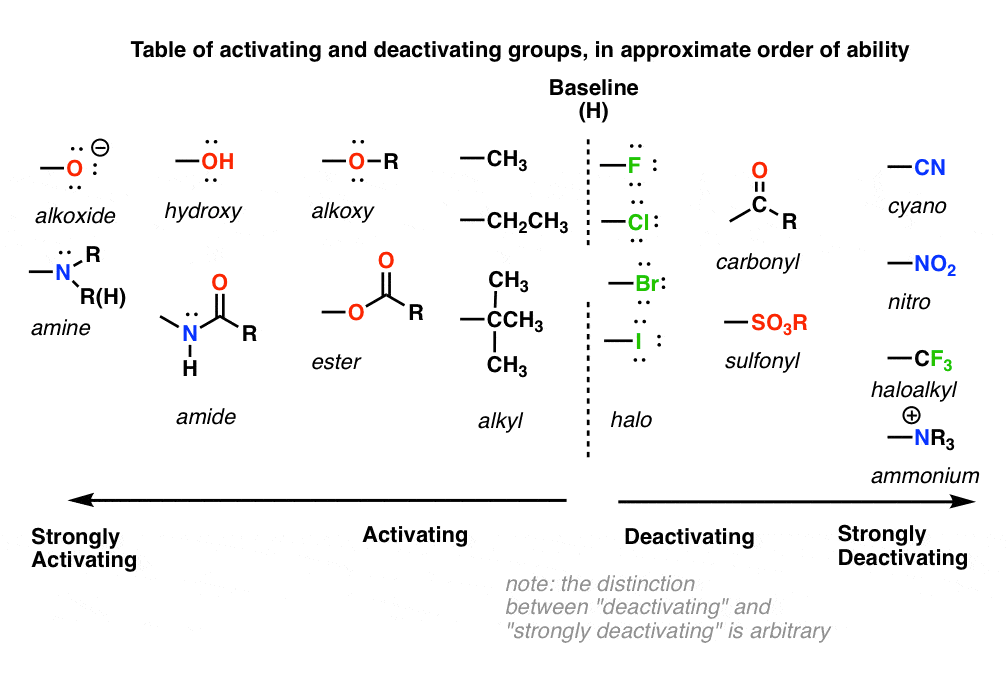
9。一个表的激活和去活化组
现在似乎正确的时间激活的大桌子,团体才会安静下来。很难准确排名以来,权力效果平均在几种类型的反应。
我建议五个主要“桶”,如下:
- 与孤氮和氧- - - - - -胺(NH2NHR, NR2),苯酚(OH)和它的共轭碱O- - - - - -很强的激活组由于pi-donation(共振)。烷氧基、酰胺、酯组少强烈激活。
- 烷基组-(没有电子撤回组)。适度激活通过诱导效应。
- 卤素——适度去活化。电子撤回(高电负性)自然比捐款通过孤对电子密度。
- 与π键原子的电负性组织——强烈安静下来。没有2CN,所以3H,赵,软木,羧基,作,CONH2。所有pi-acceptors。
- 电子撤回组没有π键或孤-强烈地安静下来。CF3CCl,3,NR3(+)。纯粹的诱导效应。
一旦你记住有点不合常理,O和N-bonded官能团与孤激活,和卤素都安静下来,其余相当简单。
最后一个单词。表“激活”和“安静下来”组织是有点像pK一个表。如何?我们可以评估影响的几个因素pKa,但最终测试的因素是更重要的是实验平衡常数的测量。同样,激活和去活化组,我们可以确定因素可能会或可能不会使某一组激活或去活化,但是最终,它的位置在图表中涉及到的实验测量反应率。
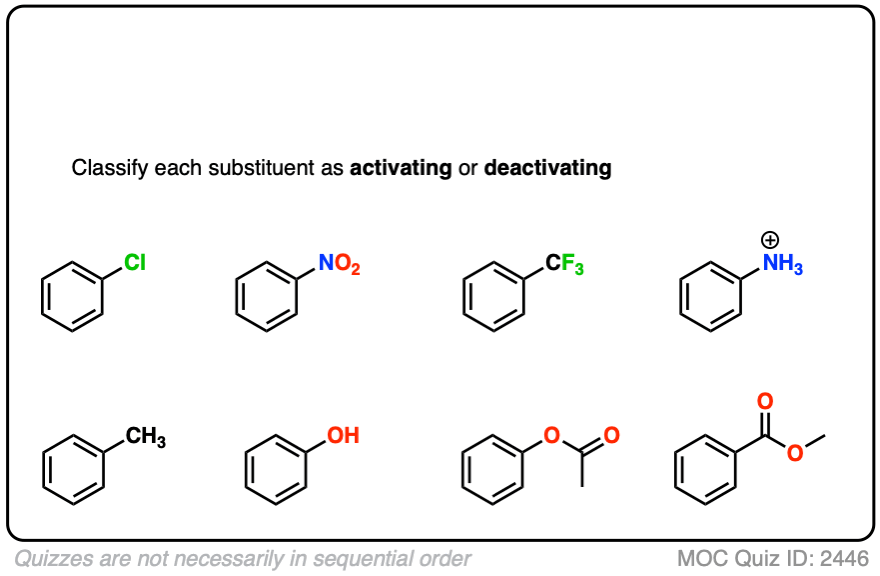 点击翻转
点击翻转
10。简介:这告诉了我们什么亲电芳香取代的机制?
好的。这一切告诉我们什么?
由于速度是如此敏感组是否电子捐赠或电子撤回(“电子效应”,如有机化学家可能很快总结)这将表明速率决定步骤是一个相当不稳定的形成electron-poor物种,如碳正离子。
记得CH3和CF3。你可能记得,碳正离子稳定性的顺序(三级>二级>主)是由于碳正离子稳定通过相邻烷基团体(例如CH3),相反,不稳定邻电子撤回团体(如CF3)。
同样地,稳定的碳正离子相邻原子可以给出孤对(如O, N)通过共振,也使π受体C = O等2,等等。
可能的第一步将是这样的:
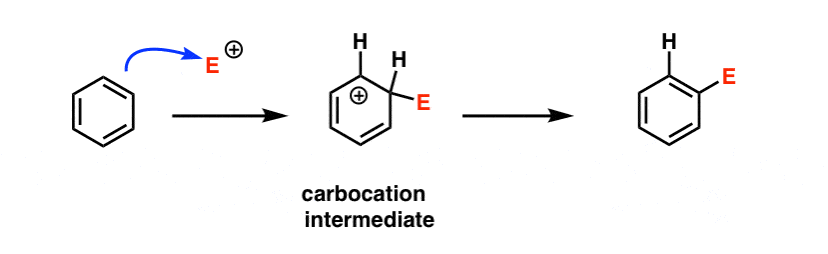
我们将进入亲电芳香取代的完整机制在接下来的帖子,但在奖金将填写额外的细节下面的主题。
在下一篇文章:亲电芳香取代:机制
笔记
1。(高级)没有氘同位素效应是在亲电芳香取代反应
在亲电芳香取代一个碳氢键坏了。调查的一个方法涉及碳氢键裂解的反应机制是使用氘(D)标签。在碳氢键断裂反应速率决定步骤(如。E2消除)碳氢键可以分手6 - 7倍c - d键。这被称为重氢同位素效应它是可以衡量的。
亲电芳香取代反应不显著氘同位素效应。(请注意这强烈表明,碳氢键断裂速率决定步骤。
2。碳正离子中间体已经被隔离,强烈支持拟议的机制
这是一个物种被观察到当1,3,5-trimethylbenzene(5 -三甲基苯)接受氟乙酯和三氟化硼在-80°C(这是一个傅克烷基化反应,顺便说一下)。
碳正离子中间体(称为一个“arenium离子”或“Wheland中间”是孤立的白色固体,熔点-15°C,并通过核磁共振光谱分析。
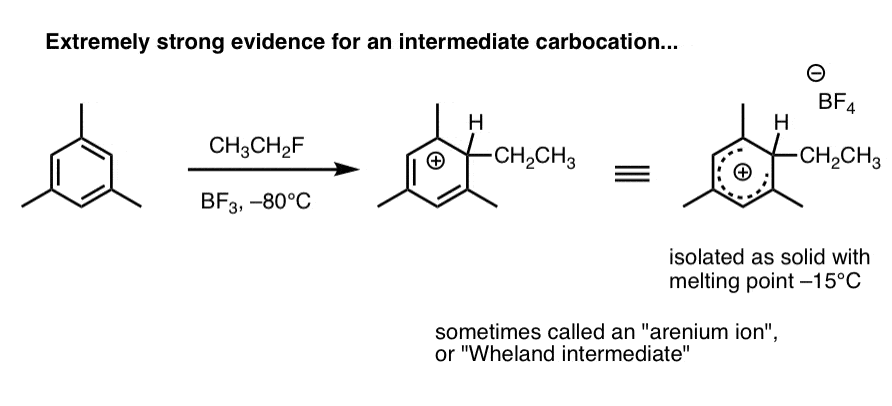
作为埃里克·雅各布森可能会说:”机制无法证明,但是…。”。(这几乎海豹交易)。我们将更详细地进入下一篇文章。
注2。为什么?有趣的是,氟是最卤素的激活。原因可能是重叠的孤对氟2 p轨道的p轨道碳要好得多(导致更强的π键)比捐赠的3 p(高)p轨道的氯、溴、碘。
注3。一个善意的谎言;确实有一些亲电芳香取代反应非常小的氘同位素效应,但我们不触及这个话题,nosiree。(分区效果,看到3月份的先进的有机化学,5日ed, p . 679)
(高级)引用和进一步阅读
如前所述,这对于所有类型的东亚峰会主题是有用的反应——傅克烷基化、酰化、卤化、硝化等。
- ——氯化苯胺。acylamido-group指导的影响
约瑟夫肯尼迪Previte奥尔顿和艾伦•埃德温Bradfield
j .化学。Soc。1927年,986 - 997
DOI:10.1039 / JR9270000986
早期论文讨论昊图公司/帕拉产品销售通过亲电氯化苯胺(一般65%帕拉/ 35%昊图公司)。不幸的是这篇文章没有数据比较的氯化苯。 - 一些亲电取代苯反应的动力学和机理
阿兰·e·Bradfield和Brynmor琼斯
法拉第Soc。1941年,37,726 - 743
DOI:10.1039 / TF9413700726
表我在这篇文章中包含部分因素对苯的硝化速率和相关化合物。氯苯和溴苯约1 - 3%苯反应,而苯甲酸乙酯明显的释放——这大约是0.1 -0.2%,反应苯!甲苯是40 - 50倍反应苯。 - 芳香卤素取代的动力学。第九部分。种苯的相对反应活性
p·w·罗伯逊,p . b . d . de la母马和b . e . Swedlund
j .化学。Soc。1953年,782 - 788
DOI:10.1039 / JR9530000782
Pg。783年在本文中包含的数据的卤化反应速率不同的苯衍生物。这个跨度取代基的极端激活(N, N-dimethylaniline1018倍比苯的反应处于待发状态!),取代基(硝基苯是106次活性低于苯)。 - 在芳香取代甲氧基的影响
p . b . d . de la母马和c·a·弗农
j .化学。Soc。1951年,1764 - 1767
DOI:10.1039 / JR9510001764
本文研究的影响- ome在亲电芳香取代(如苯甲醚和相关化合物与苯)。总的来说,苯甲醚是108倍比苯反应,因此,o / p选择性反应非常低。 - 利率的溴化苯甲醚和某些衍生品。部分因素为溴化反应速率。选择性的应用与取代苯甲醚的反应的关系
利昂·m .股票和赫伯特·c·布朗
美国化学学会杂志》上1960年,82年(8),1942 - 1947
DOI:1021 / ja01493a026
本文是一个更严格的溴化苯甲醚的诺贝尔奖得主的研究教授h·c·布朗。o / p苯甲醚的选择性是很高——溴化给1.6%o- - - 98.4%p-bromoanisole。苯甲醚的相对反应:苯还测量了1.79 x 109:1.00。本文还表明,s+测量值(亲电哈米特常量)这种方式可比哈米特值通过其他方法来衡量,而汉还值提供的一个很好的衡量取代基将如何影响东亚峰会的反应。 - 影响面向核指挥组织反应的芳香族替换。第二部分。甲苯的硝化
亚瑟Lapworth克里斯托弗•Kelk英格尔德尤金Rothstein,丹尼斯病房
j .化学。Soc。1931年,1959 - 1982
DOI:10.1039 / JR9310001959
这是第一篇论文引入“部分利率因素”这个词(通常用fpfof米)来表示一个特定位置的数量在一个取代苯苯相比可能或多或少的反应。表4显示了摘要,甲苯可以在1.2 - 10倍比苯的反应。 - 的影响烷基在亲电添加和替换
科恩,H。,HUGHES, E., JONES, M. and PEELING, M. G.
自然1952年,169年,291年
DOI:1038/169291a0
本文数据比较的硝化反应t丁苯和甲苯。T丁苯更p导演比甲苯(79.5%帕拉t-butylbenzene vs 40%帕拉对甲苯),这可能是因为空间(昊图公司方法被笨重-丁基)。 - 通过芳香系统极地的传播效果。第二部分。的硝化苄衍生品
j·r·诺尔斯,r·o·c·诺曼
j .化学。Soc。1961年,2938 - 2947
DOI:10.1039 / JR9610002938
j·r·诺尔斯后来成为哈佛大学教授专门从事酶学。动力学的知识,从做物理有机化学是适用于各种各样的领域!表2,很有趣,和表明,甲苯和苯的经验反应区别是25 x,这是今天在教科书。T-butylbenzene不如甲苯反应,但仍然15 x比苯的反应。 - 指导小组对核的影响反应在面向芳香替换。第四部分,halogenobenzenes的硝化反应
马乔里·l·鸟和克里斯托弗·k·英格尔德
j .化学。Soc。1938年,918年
DOI:10.1039 / JR9380000918
摘要表我表明,总体来说,氯苯和溴苯大约有2 - 3%活性在各种条件下苯对硝化。 - mononitrotoluenes的硝化反应的某些方面
j·g·Tillett
j .化学。Soc。1962年,5142 - 5148
DOI:10.1039 / JR9620005142
Pg。5148摘要显示,在硝基甲苯硝基胜出的退役工作性质在激活的甲基。有趣的是,在米硝基甲苯,元位置的硝基反应比其他职位,由于共振的影响。注意,这些化合物也常见爆炸TNT前兆! - 取代基的影响积极的波兰人芳香取代反应。第一部分的硝化anilinium硫酸离子在90 - 100%
玛德琳Brickman和j·h·Ridd
j .化学。Soc。1965年,6845 - 6851
DOI:10.1039 / JR9650006845 - 取代基的影响积极的波兰人芳香取代反应。第二部分。的硝化N-methylated anilinium离子
玛德琳Brickman、j·h·p·特利和j . h . Ridd
j .化学。Soc。1965年,6851 - 6857
DOI:10.1039 / JR9650006851
与苯胺,在东亚峰会非常被动和苯相比,anilinium离子(这很容易形成于酸性介质)是无效的。随着介质的酸度增加,的数量元产品苯胺硝化得到增加,表明通过anilinium离子(PhNH反应进行3+)。反应速率也随着酸度增加,减少的数量免费的苯胺的反应变得越来越低。 - 芳香取代反应。53岁。亲电硝化反应、卤化、酰化、烷基化(.alpha, .alpha .alpha.-trifluoromethoxy)苯
Takehiko大和乔治•a . Olah行长桥本约瑟夫·g·施Nirupam Trivedi,玻雷吉·辛格和朱迪斯·a·马克•Piteau Olah
美国化学学会杂志》上1987年,109年(12),3708 - 3713
DOI:10.1021 / ja00246a030
的ocf3取代基在本科化学课程并不常见,但用于药物化学。本文由诺贝尔奖得主乔治·a·Olah教授和他的妻子朱迪思,涵盖了导演PhOCF的效果和反应3在各种各样的东亚峰会的反应。总的来说,PhOCF3大约是3 - 10%,因反应的苯EAS VI-VIII(见表)。 - 量子力学的研究取向取代基的芳香分子
g . w . Wheland
美国化学学会杂志》上1942年,64年(4),900 - 908
DOI:10.1021 / ja01256a047
这个讨论的结构arenium在东亚峰会反应形成离子,也称为中心或Wheland中间,作者在这里第一次提出。 - 隔离的稳定的三氟化硼-氟化氢Methyl-benzenes复合物;络合阳离子的盐(或σ-Complex)傅克反应复合物的结构
OLAH G。,KUHN, S. & PAVLÁTH, A.
自然1956年,178年,693 - 694
DOI:1038/178693b0 - 三氟化的Benzotrifluoride-Nitryl Fluoride-Boron复杂
OLAH G。,没有SZKÓ, L. & PAVLÁTH, A.
自然1957年,179年,146 - 147
DOI:1038/179146b0 - 隔离的稳定Trifluoride-ethylfluoride硼和硼Trifluoride-formylfluoride复合物的甲苯:傅克反应机制
OLAH G。,KUHN, S.
自然1956年,178年,1344 - 1345
DOI:10.1038 / 1781344 a0
这些文件由诺贝尔奖得主教授g . a . Olah描述中间的隔离和表征离子(Wheland中间体)从各种亲电芳香取代反应,烷基化、硝化、甚至质子化作用(通过住宅4!) - 芳香取代量化处理指令的影响
利昂·m .股票,赫伯特·c·布朗
理论物理。Org。化学。1963年,135 - 154
DOI:10.1016 / s0065 - 3160 (08) 60277 - 4
这是一个非常全面的回顾,总结工作指导东亚峰会(如确定哪些群体的影响o / p -指挥vs。元导演,在多大程度上他们直接/禁用)。 - 稳定的碳正离子。CLXX。Ethylbenzenium离子和heptaethylbenzenium离子
乔治•a . Olah giusseppe梅西纳,罗伯特·j·矛和菲利普·w·威斯曼
美国化学学会杂志》上1975年,97年(14),4051 - 4055
DOI:1021 / ja00847a031
论述了benzenium离子的特性,这在东亚峰会中间体,heptaethylbenzenium离子的特性,是一种稳定的物种因为它缺乏一个质子,因此消除了与困难。 - 氟苯的异常反应亲电芳香取代和相关的现象
乔罗森塔尔和大卫·舒斯特尔
《化学教育2003年,80年(6),679年
DOI:1021 / ed080p679
一个非常有趣的纸,适合好奇的本科生,并讨论了大多数练习有机化学家会知道经验-氟苯一样反应苯在东亚峰会或傅克反应,这是反直觉的,当一个人认为电子效应。
我看不到解决一个取代基如烯烃…特别是c双连着另一个碳的苯环。这是由于共振才会安静下来吗?或激活因为共振不太可能给它产生一个不稳定的碳负离子?
如果亲电试剂*不*双键,你是正确的,一个正常的烯烃应该稍微激活,因为它可以作为π捐赠。
然而,一个问题是,烯烃的反应更容易比芳环的亲电试剂,所以他们常常试图亲电芳香取代中遭到破坏。试图氯化苯为例,最终将烯烃。
亲电芳香取代烯烃时可以与电子结合撤销集团如酯,这有助于使烯烃electron-poor。
有一个具体的例子你思考?
将p-methoxybenzenesulfonic酸经过弗里德尔工艺反应?
非常感谢…这个页面是一个概念清晰…。所有的解释做了一部分
你应该重写部分“卤化物竞争效应”对“亲电芳香指导组织”的维基百科页面
我将把这看作是一种恭维,史蒂文。谢谢
我刚刚发现这个博客,使化学这么简单和容易感谢这样一个神奇的博客
先生,激活和去活化组织定义了相对于氢。相对于氢真的是什么意思? ?
请帮我整理出来先生
测量与苯反应的速率。然后看看会发生什么当苯环上的氢速率不同的取代基取代了Cl, CH3、二氧化氮等。
哪个更反应在NR2 NHR氨基哦?
风扇先生…。!你们必须提供宝贵的材料复印件…我肯定打赌…。至少在印度,它将得到很多爱…
这个网站是一个转折。美妙的strait-forward解释。谢谢你!
你有一个错误在第一段:“傅克烷基化和傅克烷基化”两次,而不是酰化。
谢谢你,谢谢你的纠正!詹姆斯
烷氧基(或)是我组…
但它是激活和邻对位指导. .
请解释. .
此外,它的酸度增加或减少苯吗?
嗨,詹姆斯
是的CH3激活。我在网上一看,发现苯和甲苯的静电势图几乎是相同的吗?应该开得有更多的红圈的强度MB ikndicating有更大的电子密度?
如果你有2苯和MB Ep地图显示一个电子密度差对戒指请转发。
为什么他们看起来一样呢?我。e基于EP地图苯的反应性和MB应该类似反应的差异。当然这是在实验室中诞生!
化学教育工作者在新西兰
你好雷——而不是看潜在的地图我就看你能不能找到电子密度计算。不应该有巨大的差异,但将是足够重要的10 - 100倍增加率为烷基苯和苯本身。
哪个更deactivting CF3组b / w CN和
根据计算,CN是*比恶略*强电子撤回小组,在对位与电子密度为0.972和0.984的恶(0.957,更强的电子撤回组NO2)。看到j•Hehre, L。屏蔽罩,J.A.荡漾,j。化学。Soc 94:1496, 1972。https://pubs.acs.org/doi/abs/10.1021/ja00760a011
我仍然不明白为什么σ接受卤素超过π捐赠使他们安静下来吗?
这是一个简单的问题,但不是一个简单的问题回答。
卤素团体才会安静下来,因为π捐献导致保税(带正电)卤素的两倍。一个正电荷等原子的电负性是如此不稳定,它超过了“稳定”提供给arenium离子通过π电子的共振。因此,卤素集团是弱禁用。
不,正电荷也没有那么糟糕,因为它只是一个正式的正电荷,而不是导致正电荷不到一个完整的八隅体。卤素都安静下来的原因是,他们是高度的电负性,它从戒指中提取电子密度。氟更比氧气由于这个原因才会安静下来。时较重的卤素,问题不仅是电负性但也可怜的轨道重叠,难以形成π键2 p和3 p轨道(Cl)或2 p和4 p轨道(Br),因此π捐助者弱得多。
氧-哦组倾向于捐赠其孤对形成一个π键,但心脏的氧气组倾向于接受π电子。为什么?
在后一种情况下,该集团直接附着在芳环羰基(C = O),这是一个pi-acceptor。把它画出来,你就会看到。
为什么是烷氧基酰胺和酯组(在第一个类别-nitrogens&oxygens孤)? ? ?
如果原子直接与芳环是一个氧气,这将是一个邻对位导演,无论,氧气是酒精的一部分,醚或酯官能团。这同样适用于氮re:胺和酰胺。
如果的羰基酯直接附着在芳环,这是一个不同的故事。在这种情况下,它是一个元导演。
你在做一个了不起的工作。
谢谢你也爱不够。
真正令人惊叹!
好的,谢谢你停下来,Saatvik !
先生,如果我们进行亲电芳香2-methoxyphenol氯化(说与nc和PPh3S的主要产品是什么,为什么?
哦是更强的捐赠(对甲基)所以我希望看到氯化对位哦。
一个词:神奇的
神奇的网站。神奇的教程。神奇的博客。
你让这一切如此简单和容易理解。
非常感谢。
不能等到第二部分。与此同时,两个小的观察:
——文本在图1:“去活化组织倾向于退出电子密度环”,不应该是“环”?
——“溴化、氯化、硝化、sulfonylation傅克烷基化和傅克烷基化”——更改的最后一两个“酰化”。