二烯烃和MO理论
Diels-Alder反应
最后更新:2023年1月17日|
Diels-Alder反应是可怕的
今天我们将介绍一个反应我认为是最有用的和强大的有机化学反应在所有:Diels-Alder反应。
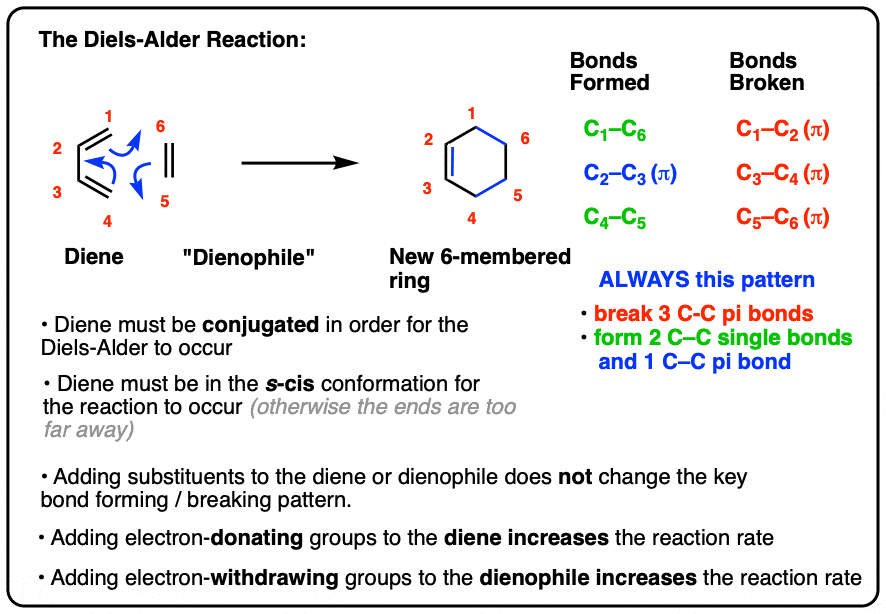
- Diels-Alder反应,二烯结合一个π键(通常称为“亲二烯体”)给一个新的六元环
- 两个碳碳σ键和碳碳(pi)债券形成,三个碳碳π键破碎的
- 为了让Diels-Alder反应发生,二烯必须共轭,必须的s -独联体构象
- Diels-Alder反应更快,当有一个吸电子集团的π键(“亲二烯体”)和电子捐赠组织二烯。
表的内容
- 化学家们一致同意:Diels-Alder反应是可怕的
- Diels-Alder反应
- 不要感到乏味的!
- Diels-Alder反应的基本模式
- Diels-Alder Arrow-Pushing机制
- 四个关键事情知道Diels-Alder反应
- 四个关键东西,第1部分:必须共轭二烯
- 四个关键的东西,第2部分:二烯必须在s-cis构象
- 四个关键的东西,第3部分:取代基二烯或亲二烯体不影响Bond-Forming / Bond-Breaking Diels-Alder的模式
- 四个关键的东西,第4部分。然而,取代基影响Diels-Alder的速率。率增加了EWG的亲二烯体和电子给体二烯
- 笔记
- 附录1:其他戒指尺寸呢?
- 附录2:三个壮观Diels-Alder反应的例子
- (高级)引用和进一步阅读
1。化学家们一致同意:Diels-Alder反应是可怕的
但不要带一些随机的博主的话语。这里有三个著名的化学家们对这个反应。

2。Diels-Alder反应
好的。你准备好看到了吗?
自己做好准备。
这里是:
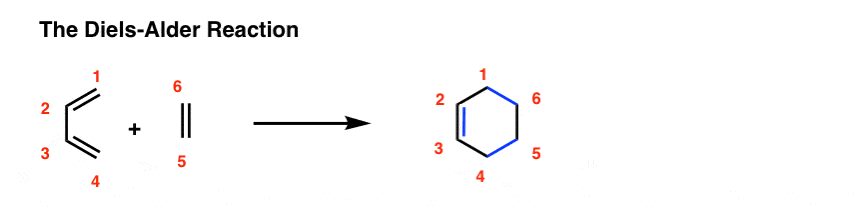
我的工作是做在这里,。
课结束了!
(滴麦克风)
3所示。不要感到乏味的!
…等。你不惊讶吗?你没有印象?你没有被风吹走的力与美这惊人的强大的过程?
神已经赦免了你。说实话,我有点感到乏味的时候学会了在大学生这个反应。(我也不是像我应该的印象应对重排时,在其最简单的形式,似乎毫无意义。狮子座Paquette的名义,我忏悔!]。
这是因为教师(包括我自己)倾向于从最无聊,简单,牵手的例子可能传达的主要模式,结果学生错过看到非常壮观的情况下。
所以,我想从这些复杂和非常漂亮的例子Diels-Alder…我们将开始,作为传统规定,在浅池。
(所以对于几ka-pow !Diels-Alder的例子,让您的一天,看到脚注-河豚毒素(岸,1972)。四环素[迈尔斯,2005)。iso- - - - - -Odoratin[纽豪斯,2017]
让我们来仔细看看这极其重要的反应。第一:
- 基本键形成/键被破坏模式
- 简单箭头推动机制
4所示。Diels-Alder反应的基本模式
汇集了Diels-Alder反应两部分组成。
- 我们所说的一部分”二烯”,这是由两个相邻(即。共轭π键。
- 第二个组件是被称为“亲二烯体”,也就是说“diene-loving”,至少有一个π键。
形式,债券和债券打破吗?
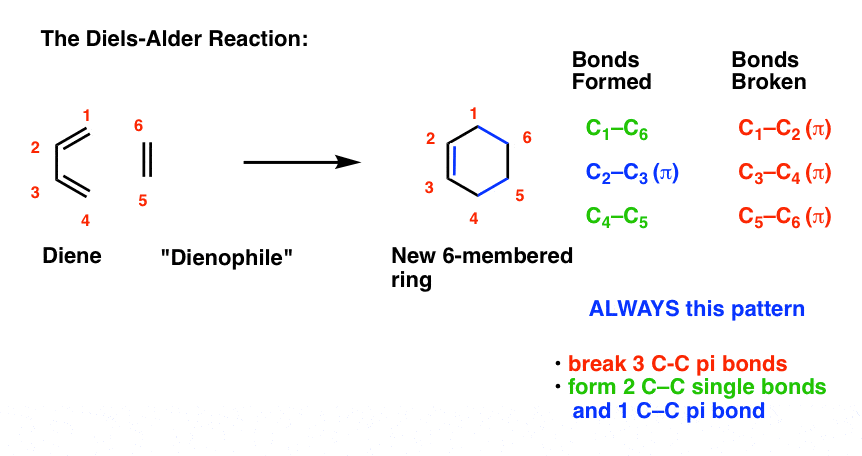
- 三个π键坏了。(C1- c2C3- c4C5- c6)请注意——这不是IUPAC编号,对我们来说只是跟踪每个碳簿记的目的。
- 两个新单债券形成(C1- c6C4- c5)
- 一个新π债券形成(C2- c3)。
注意这个关键模式,因为它重演,一遍又一遍。
事实上,每一个Diels-Alder我们学习将会遵循这种模式。
三个π键被打破;两个σ键和一个π键组成。每一个。单身。时间。
其结果是,一个新的六元环的形成。(每隔……。时间!)
5。Diels-Alder Arrow-Pushing机制
我通常倾向于推迟机制直到我们走过一些实验事实,但在这里我将做一个例外。
有两种方法可以吸引电子的流动(正确的):顺时针和逆时针。
这个流和三箭电子被描述,我贴上A, B, c .注意什么债券形式和休息在每个箭头。
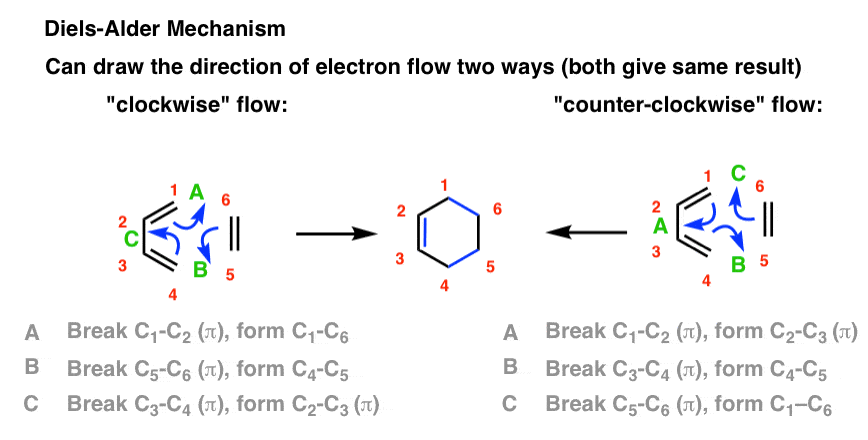
您应该能够看到三个碳碳π键坏了,和三个形成新的碳碳键(2碳碳σ键和一个碳碳π键)无论电子流动收益在顺时针或逆时针方向。
(题外话:到目前为止,几乎所有你见过有机化学中涉及到的反应亲核试剂和一个亲电试剂。电子总流的亲核试剂到亲电试剂。这引起了一个问题。如果电子流可以吸引任何一个方向,然后是什么亲核试剂和亲电试剂在这里吗?这是一个非常深奥的问题——一个我们还不会回答!]
6。四个关键事情知道Diels-Alder反应
看着电子流和债券形式和破坏的模式,让我们继续关于Diels-Alder一些非常基本的问题。
这里有四个要点:
7所示。四个关键东西,第1部分:必须共轭二烯
的二烯必须是参与Diels-Alder共轭反应。没有结合,没有Diels-Alder。所以当1,三丁基容易经历Diels-Alder反应,1,4戊二烯(下图)没有。
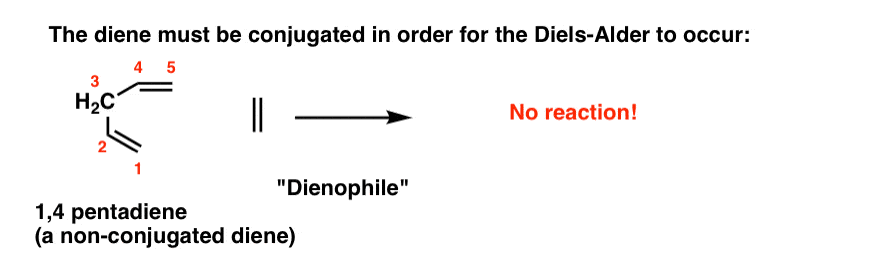
(如果您不清楚什么是“共轭二烯”,你可能会想访问这个帖子。)
8。四个关键的东西,第2部分:二烯必须在s-cis构象
是不够的π键二烯邻;两个碳碳π键必须采用构象他们在同一个平面上(即平)。
但即使这么做也不能充分的。二烯必须采用构象面向两个π键在哪里独联体中央碳碳单键为了Diels-Alder发生。换句话说,必须在s -二烯独联体构象!(点评:s-cis和s-trans]
例如,下面的Diels-Alder发生只有当丁二烯在s -独联体构象,从不在s -反式。
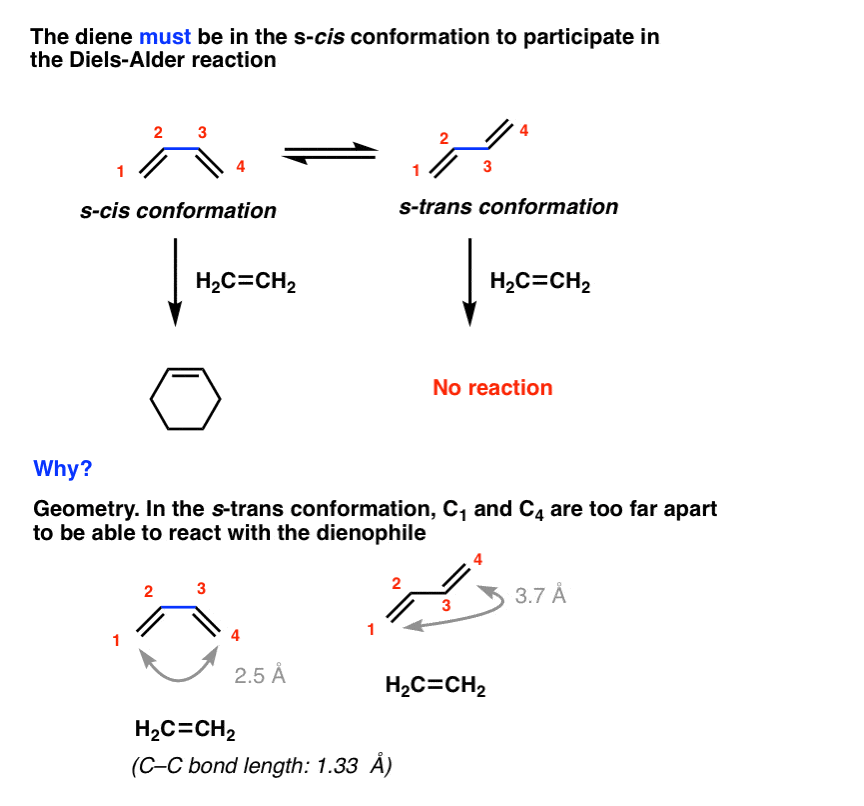
为什么?总之,几何。在这个年代- - - - - -反式构象,之间的差距的两端二烯(约3.7)无法弥合的亲二烯体(长约1.3)。这仅仅是可能的- - - - - -独联体构象。
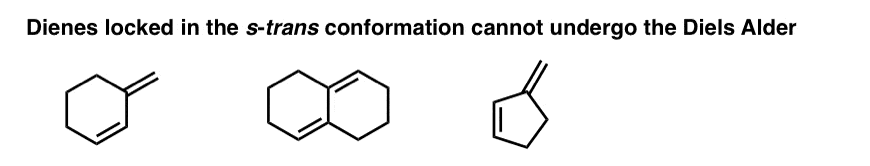
有很多例子的二烯烃在s -“锁定”反式构象,因为s -旋转独联体构象需要碳碳键的断裂。这些双烯Diels-Alder不能接受。
9。四个关键的东西,第3部分:取代基二烯或亲二烯体不影响Bond-Forming / Bond-Breaking Diels-Alder的模式
添加取代基对二烯或亲二烯体不影响bond-forming Diels-Alder / bond-breaking模式。
例如,让我们策略CH3颈- 1组(用红色)到与乙烯丁二烯和勾勒出相同的反应。
这是产品会是什么样子:
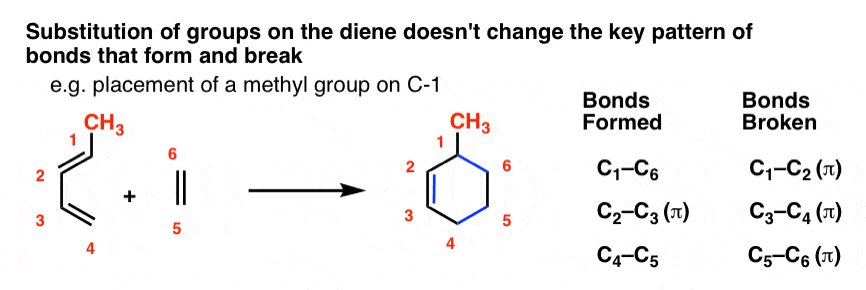
注意,债券形式和破坏的模式是一模一样的丁二烯本身!债券的模式不要求任何取代基打破,所以我们把他们都完好无损。
这同样适用于替换c - 2。债券形式和破坏的模式是相同的。
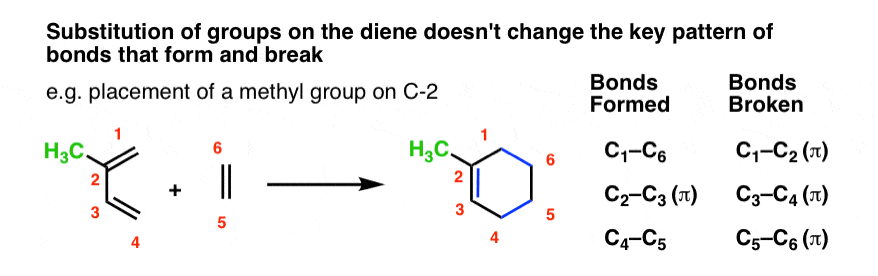
尽管它可能很难看到,这同样适用于更复杂的例子,其中一些是附录。上的所有额外的卷心菜二烯不会改变基本反应模式。
(取代基的主要并发症增加,正如我们将要看到的,是会计立体化学产品的一个主题,我们将在随后的帖子介绍。)
我们刚才说的二烯也适用于亲二烯体。取代基的亲二烯体不影响债券形成和破坏的主要模式。取代基来凑热闹而已。
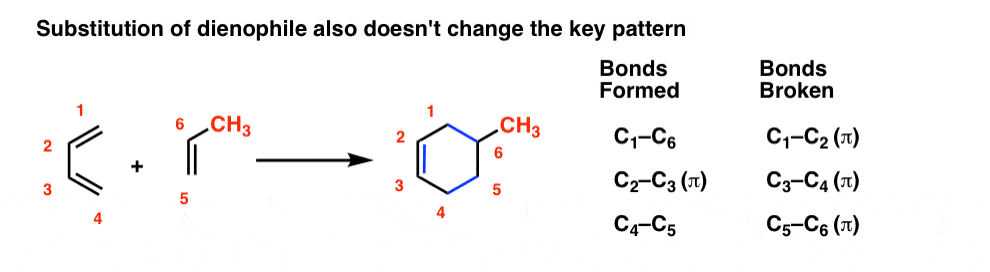
你可能会想:我们可以把替换二烯和亲二烯体吗?你说的没错这是同样的模式。
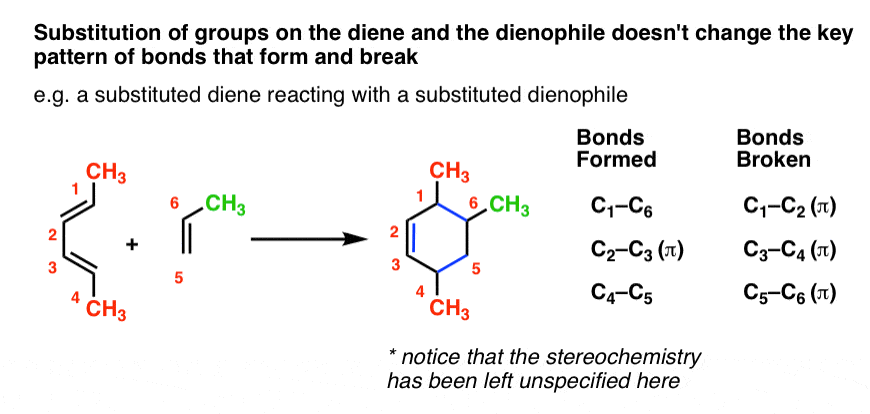
重复我的观点,让我说一遍。Diels-Alder要求的模式打破三个π键,形成两个单键和一个π键,导致六元环。任何债券取代基的二烯/亲二烯体不失。这些取代基保持完全相同。
10。四个关键的东西,第4部分。取代基影响Diels-Alder的速率。率增加了EWG的亲二烯体和电子给体二烯
取代基时不得改变Diels-Alder反应的基本模式,他们可以极大地影响其利率。
事实证明Diels-Alder是数量级的速度快如果亲二烯体上有一个吸电子集团(注意4]例如,更换一个氢与吸电子集团CN(乙烯腈在大约10)的结果5提高反应速率。(注5]。
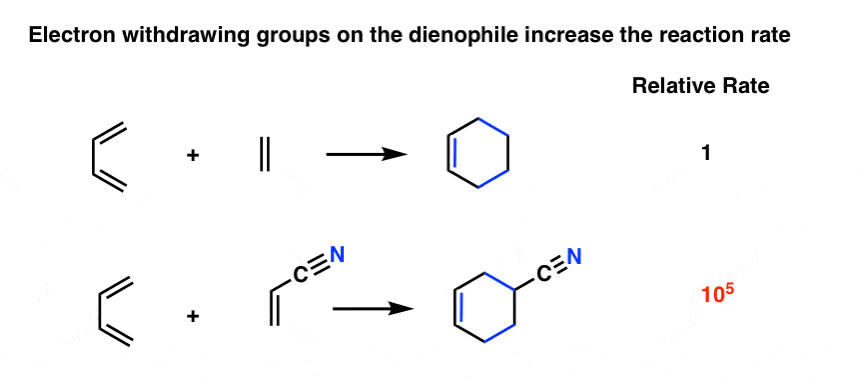
其他常见电子官能团,将加速撤军的一昼夜的桤木反应亲二烯体包括醛、酮酯类。简而言之,任何官能团共轭π键可以充当π受体将加速Diels-Alder反应与一个典型的二烯。
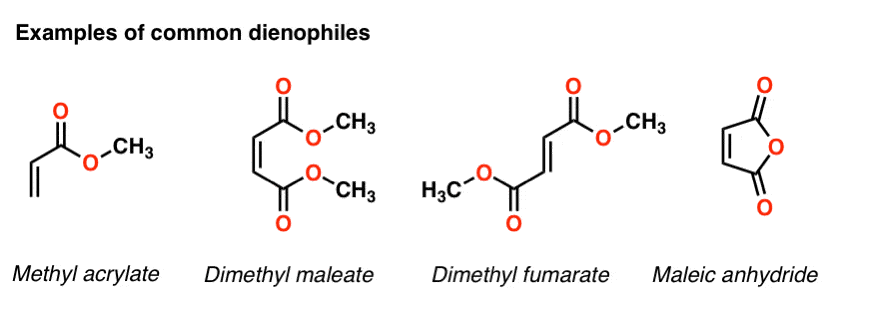
使二烯多电子也增加率。“富”,我的意思是任何取代基可以捐赠电子密度二烯。烷基组(如甲基、乙基)就是一个例子,也一样π捐助者如氧和氮。
例如,添加一个甲基丁二烯会增加反应速率的3倍到100多,根据亲二烯体(裁判]。
接下来:循环二烯烃和亲二烯体
许多学生斗争与图纸的产品Diels-Alder反应循环二烯烃和亲二烯体。我计划解决这一主题在这篇文章中,但是它太长了。下次我们将讨论。
感谢汤姆Struble援助与这篇文章。
笔记
注1出于我们的目的,我们将只讨论正常电子需求一昼夜的桤木的反应,和一个富二烯和一个electron-poor亲二烯体。然而,在是的例子Diels-Alder反应进行electron-poor二烯烃和负电子的亲二烯体。这些被称为电子逆需求一昼夜的阿尔德反应。
注2——这些数字实际上申请环戊二烯,不是丁二烯,但是相对利率应该是相似的。实验数据见凯莉和桑德博格(谷歌图书上641页)或直接从文学,在这里。(德国)
附录1:其他戒指尺寸呢?
几个“愚蠢”的问题的Diels-Alder实际上是好问题
1。这种类型的反应局限于“二烯”和“亲二烯体”,或可以用来制造其他尺寸的戒指吗?
好问题。到目前为止我们已经习惯看到高度紧张的亲核试剂与亲电试剂。
Diels-Alder是一个家庭的一部分的反应称为“pericyclic反应”,这两个反应组件是相对非极性和一般不通过碳正离子中间体等
具体来说,本身会使六元环和Diels-Alder反应只有六元环。二烯[4]电子组件和一个亲二烯体[2]电子组件需要反应发生。因此Diels-Alder通常被称为一个[4 + 2]环加成作用。
有其他类型的环加吗?是的——尽管他们不那么常见的或重要的[4 + 2]环加成反应。
例如,您可能想知道:如果没有二烯会怎样?可以两个烯烃共同构成一个四元环吗?
在同等条件下随着Diels-Alder(热),没有。
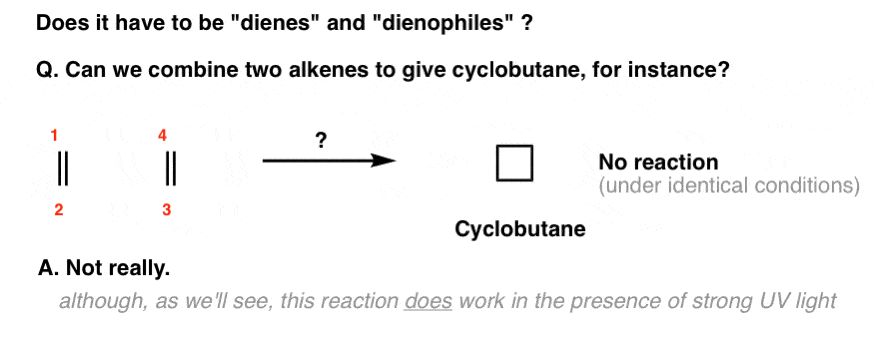
我们写了一个巨大的系列文章对的反应烯烃你没有看到这个反应。这是一个很好的理由。
然而,它是可能有两个烯烃结合成一个环丁烷,如果(只有)强烈的紫外线(UV)光。
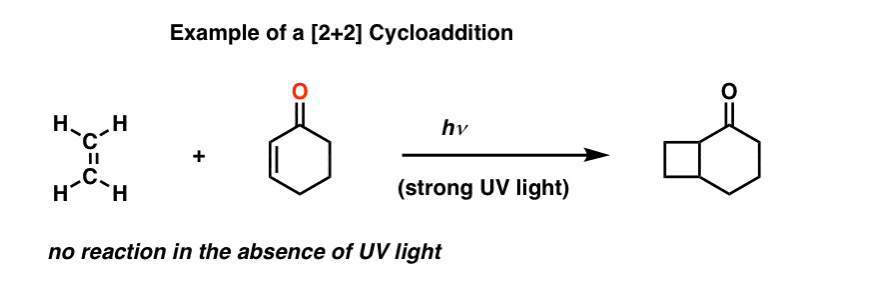
这就是所谓的[2 + 2]环加成作用。
为什么紫外线是需要的但不是Diels-Alder吗?好问题!这与轨道对称性,我们很快就会到达。
类似的:如果没有亲二烯体呢?两个二烯烃的反应吗?
在缺乏亲二烯体,加热二烯在相同条件下不给一个八元环(这将是一个4 + 4]环加成作用顺便说一下)。
什么实际上发生的是一个二烯结合烯烃在Diels-Alder反应,形成六元环。
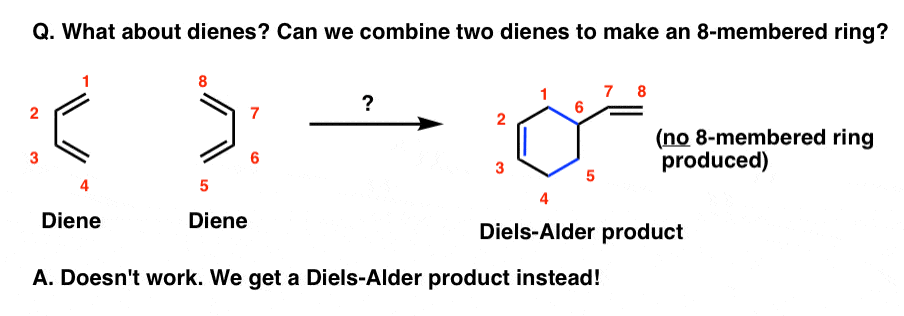
其他种类的“高阶”环加也被观察到,等(6 + 4),(6 + 8),甚至(14 + 2)环加成作用,但这些通常是罕见的和相当的例子,苍白的有用性[4 + 2]。
这里我想说的组合二烯+烯烃给一个六元环尤为重要和青睐。
2。亲二烯体需要是吗烯烃吗?
亲二烯体没有一个烯烃特别地;唯一的要求是,它包含一个π键。它也可以是一个炔烃为例。例如dimethylacetylene脱羧基(DMAD)是一个很好的亲二烯体,碳碳π键的断裂,后一个烯烃仍然存在。甚至N =π键可以参与Diels-Alder反应,只要连接到电子贫困群体,如diethylazodicarboxylate(死亡)。是的,有一个试剂叫死了。
此外有示例C = O债券参与Diels-Alder反应,尽管这进入的领域电子逆需求Diels-Alder反应,我们甚至还没有接近讨论话题。
附录2:三个壮观Diels-Alder反应的例子
高级的主题。
有无数的例子Diels-Alder反应用于天然产物的合成。我选择下面三个。
示例将复杂的初学者,他们。然而,关键我想锤家债券形成的模式,打破所有的这些反应并不比我们看到的模式不同的具有良好的丁二烯、乙烯。
大约需要三年的强化训练获得许可证准备河豚(河豚在日本)。这是为什么呢?因为,河豚的肝脏和其他选定的器官含有河豚毒素致命的神经毒素,它需要巨大的练习,学习如何准备鱼片没有污染的肉。
河豚毒素有非常复杂的结构。Yoshito岸的哈佛大学首先合成了河豚毒素在1972年使用Diels-Alder设置立体化学的核心六元环。
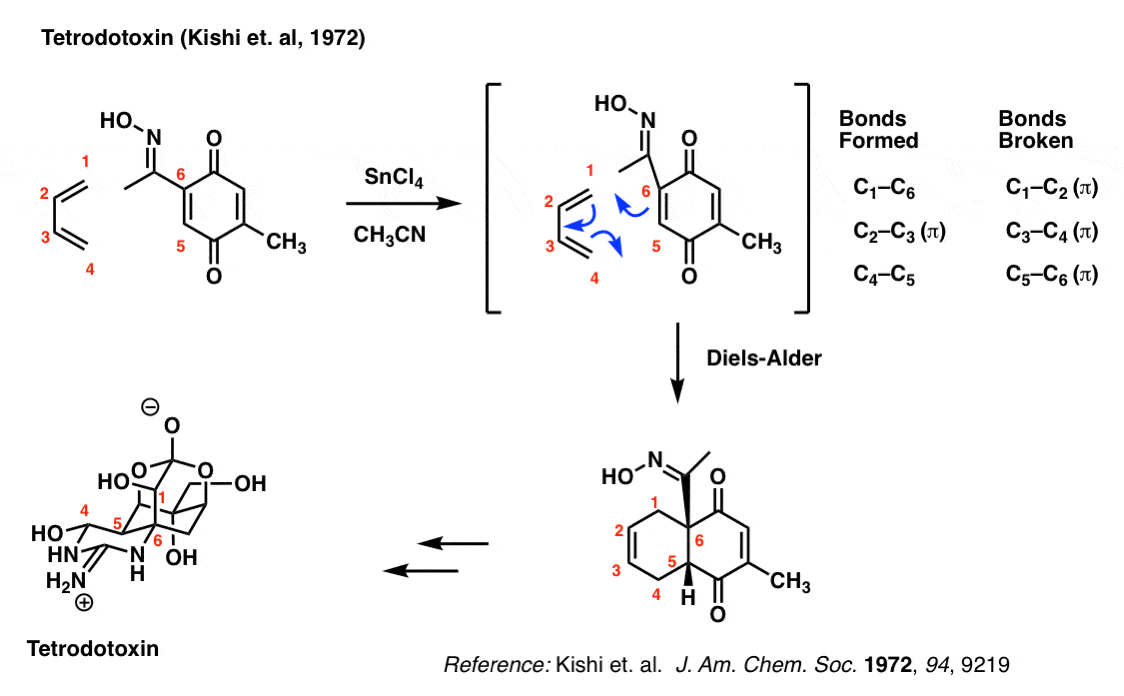
试着看过去的复杂性关注债券形式和休息在这里:你应该能够看到他们完全相同,形式和打破与乙烯丁二烯的反应。
Diels-Alder的重要性在于,它集c - 5的立体化学和其他碳(红色标签),并组成了一个叫做“凹”cis-decalin”结构,允许岸的小组随后将其余的手性中心的分子(7)。这个经典的战略,开创了伍德沃德,允许一次一项极其复杂的分子的合成,有很少的不对称合成的方法。
您可能想知道SnCl什么4是对的。这个路易斯酸催化丁二烯和亲二烯体之间的反应。不仅路易斯酸催化提高反应速度,但它也使它更有选择性。不是我们今天要进入主题。
也许你听说过抗生素四环素?哈佛大学的安德鲁·g·迈尔斯的研究小组开发了一个平台,各种各样的四环素抗生素的合成依赖于Diels-Alder反应。
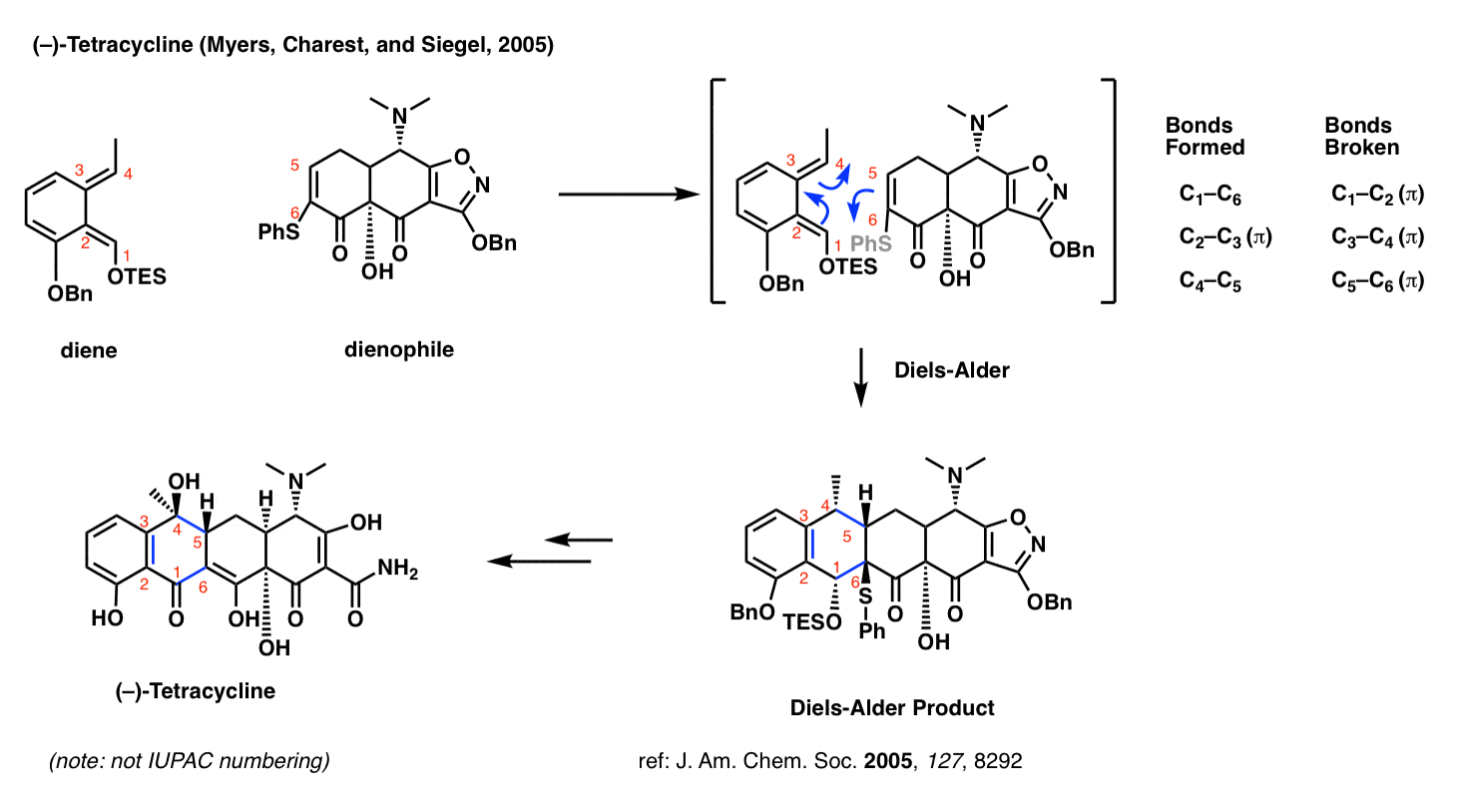
Diels-Alder之所以如此有用吗?两件事。首先,它集立体化学的c - 5 (IUPAC红色编号,而不是编号)。其次,更重要的是,一起Diels-Alder允许加入两个非常复杂的碎片在一种可预测的方法。
药物化学家通常使大量不同类似物的一种有前景的候选药物和测试它们在生理条件下,看看哪一个表现最好的。美丽的Diels-Alder四环素合成是策略收敛;可以使一个复杂的二烯和一个复杂的亲二烯体后期,然后把它们放在一起。
这种策略对四环素合成是一个上市公司的基础(Tetraphase目前治疗诊所。
iso-Odoratin(纽豪斯和Schuppe, 2017)
Diels-Alder不是一些发霉的老反应局限于背页的教科书。是目前很重要的一部分,尖端化学研究。只是为了证明这不是一些反应,埋在过去,这里有一个例子从今年1月的合成iso-odoratin(和其他分子)的蒂姆·纽豪斯在耶鲁大学。
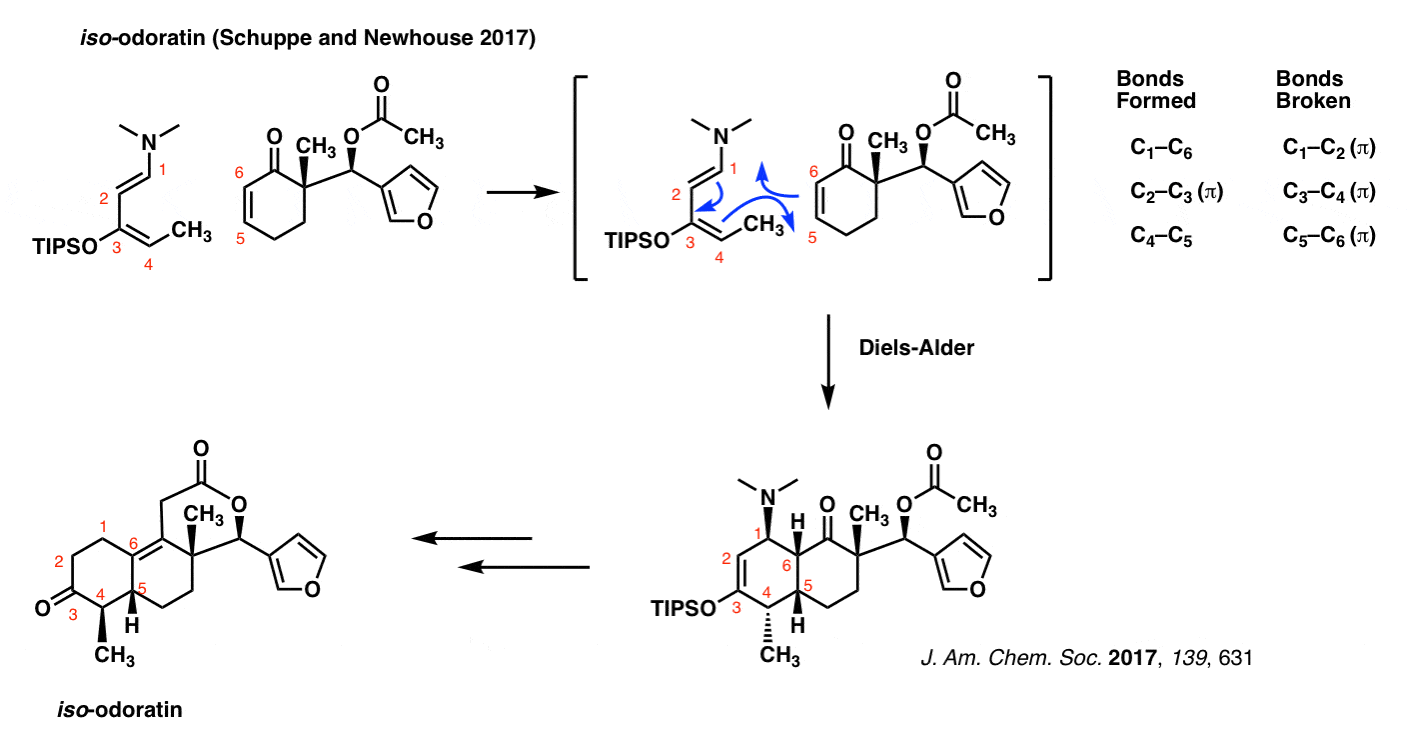
请注意,在前面的所有情况下的Diels-Alder,债券形式和破坏的模式是相同的。
本例中的二烯非常富,拥有一个氧和氮(强π捐助者!)直接连着π体系。
为什么不与c - 5和c - 4 c - 4债券与其他区域选择性,换句话说是一个很棒的问题。我们会解决这个问题。(参见:Diels-Alder反应区域选择性]
这催生了一个反应巨大的量的研究由于其通用性。这里列出的论文代表,但几乎不周详的工作已经完成。
- 在der Synthesen hydroaromatischen Reihe
奥托一昼夜的库尔特·阿尔德
Lieb。安。化学。1928年,460年(1),98 - 122
DOI:10.1002 / jlac.19284600106
这个反应命名它的发现,一昼夜的桤木,谁获得了1950年诺贝尔化学奖这项工作。在这篇文章中,他们声称他们的领土在应用他们的反应合成,总说“我们明确地准备自己开发的应用程序的反应我们解决这些问题”。 - Diels-Alder反应的机制
r·b·伍德沃德托马斯·j·卡茨
四面体1959年,5(1),70 - 89
DOI:10.1016 / 0040 - 4020 (59)80072 - 7
r·b·伍德沃德教授是一个传奇人物在有机化学中,并介绍了各种理论Diels-Alder反应的机制。 - Diels-alder反应与逆电子需求。二世。苯甲脒的反应与π-deficient heteroaromatic化合物
p . Figeys数学
春节。列托人。1981年,22(15),1393 - 1396
DOI:10.1016 / s0040 - 4039 (01) 90330 - 2
正常Diels-Alder反应所得最好当二烯负电子,亲二烯体electron-poor。然而,在某些情况下,相反的极性是可能的,这些被称为反应逆electron-demand Diels-Alder反应。 - 总共Diels-Alder反应合成
c . Nicolaou斯科特·a·斯奈德Tamsyn Montagnon,乔治·Vassilikogiannakis
Angew。化学。Int。。2002年,41(10)1668 - 1698
DOI:10.1002 / 1521 - 3773 (20020517)41:10 < 1668::AID-ANIE1668 > 3.0.CO; 2 z
教授k . c . Nicolaou(大米)是一个目前天然产物全合成的领导者,和本文综述了Diels-Alder反应在该领域的应用。 - 疏水性Diels-Alder加速度反应
达瑞尔·c·赖德奥特和罗纳德•布勒斯洛
美国化学学会杂志》上1980年,102年(26),7816 - 7817
DOI:10.1021 / ja00546a048
这份出版物教授‘(哥伦比亚)是重要的,因为它描述了一个锐意创新Diels-Alder的加速度反应速率时在水中进行。这归因于疏水效应,是一个熵的影响力量反应物更紧密地联系在一起。 - 有用的二烯Diels-Alder反应
Danishefsky和非
美国化学学会杂志》上1974年,96年(25),7807 - 7808
DOI:10.1021 / ja00832a031
介绍了合成和效用的功能化和活性二烯Diels-Alder反应。这个二烯现在通常被称为“Danishefsky二烯”创作者之后,美国教授Danishefsky(现在在哥伦比亚美国)。(值得注意的是,Danishefsky的博士生导师,教授彼得•耶茨做出了重要进展报告路易斯酸催化Diels-Alder] - 有机催化的新策略:第一高度拆分Organocatalytic一昼夜的−桤木的反应
凯特瑞·a·阿伦特克里斯托弗·j·波尔斯和大卫·w·c·麦克米伦
美国化学学会杂志》上2000年,122年(17),4243 - 4244
DOI:10.1021 / ja000092s
拆分Diels-Alder反应也有可能,一个活跃的研究领域。本文通过教授大卫·麦克米伦(现在普林斯顿)展示了一个如何使用organocatalysis实现一个拆分Diels-Alder通过手性iminium离子反应的中间体。 - 轨道对称性守恒
罗尔德·霍夫曼和罗伯特·b·伍德沃德
的化学研究1968年,1 (1),17-22
DOI:10.1021 / ar50001a003
这是一个极重要的论文。轨道对称性守恒允许一个预测pericyclic的立体化学反应(如Diels-Alder反应)。本文是一个伟大的介绍主题的创造者和介绍有关条款(同侧的,antarafacial synrotatory,顺旋,等等)。霍夫曼教授在1981年获得了诺贝尔化学奖这项工作,并与伍德沃德教授无疑也共享这一年(这是伍德沃德的第二个诺贝尔)如果他没有过早地去世了。 - 拆分,催化DIELS-ALDER反应:(1 s-endo) 3 - (BICYCLO [2.2.1] HEPT-5-EN-2-YLCARBONYL) 2-oxazolidinone
Pikul和e·j·科里
Org。Synth。1993年,71年,30
DOI:10.15227 / orgsyn.071.0030
这个过程由诺贝尔奖得主教授e·j·科里(哈佛)展示了一个不对称Diels-Alder反应的手性催化剂。
我们应该记住这个反应?反应进行的原因是什么?
作为一个初学者,我很幸运能够最终发现DA理论详细的反应。我不能感谢你才好。
非常感谢你们这些优秀的文章!他们帮助我比任何单一的学习工具我发现到目前为止——很好的内容! !
高兴你有帮助伊恩!让我知道如果你发现任何错误/错误。谢谢
为什么环辛二烯不接受桤木死去
这不是明显。相关研究:https://pubs.acs.org/doi/10.1021/acs.joc.5b00174
我只是想谢谢你。我在Orgo I我读所有分配的章节宗教,参加所有讲座、做所有课本的练习题,但仍难以理解正在向我解释什么。我来你的网站,如果你说我的语言。我明白了。我完全明白了。我欠你,我及格分数。谢谢你这么多!
亚历山德拉,我很高兴听到这个。感谢你的分享!
是6 + 4反应环庚三烯酮和环戊二烯之间给九元环不是一昼夜的桤木反应. .德雷克,还是Cookson Hudec和莫里森不正确吗?
这不是一个Diels-Alder反应。这是一个“高阶”环加成作用。“一昼夜的桤木”具体是指4 + 2例。如果Cookson你指的是原始报告,我相信这是在伍德沃德和霍夫曼广义选择规则。https://pubs.rsc.org/en/content/articlelanding/1966/c1/c19660000015 ! divAbstract
伍德沃德·霍夫曼预测6 + 4反应之前。什么时候成为“高阶”的反应。仅仅是单词。
我认错。他们确实选择规则,1965年出版。https://pubs.acs.org/doi/10.1021/ja01087a034。我相信伍德沃德分配肯胡克调查6 + 4环加他的毕业设计。不幸的选择heptatriene 6π组件的伍德沃德/胡克不是那么偶然的环庚三烯酮的选择你的研究小组。
谢谢你做的一切。帮助前医学院的学生随处可见
很高兴你有帮助,科比!
在第二部分,你国家的二烯必须s-cis构象否则Diels-Alder反应不会发生。然后,您显示1,三丁基在反式构象和说不发生反应。然而,不能1,三丁基反式排列独联体和经历一个反应?二烯不循环,所以它不是锁在反式postition。
至于二烯的立体化学,你写二烯必须在sigma-cis构象与亲二烯体发生反应。环的大小有什么效果的反应循环二烯锁在sigma-trans构象?
例如,[4 + 2]环加成反应3-methylenecyclohept-1-ene与亲二烯体之间symmetry-forbidden或允许吗?
亲爱的詹姆斯,
关于arrow-pushing机制,为什么箭头从二烯亲二烯体?我学会了,箭头表示电子的流动。如果亲二烯体electron-poor二烯是电子的,不应该被吸引的箭头?
别介意,詹姆斯。我意识到Diels-Alder反应是一个一步,协同机制,正如你提到的,电子可以顺时针或逆时针方向移动。
我有另一个问题。
如果我们丁二烯的乙烯反应,得到环己烯。新成立的双键作为亲二烯体,这可能与二烯反应了?(再一次得到一种聚合)
我知道亲二烯体最好应该EWG,但你说一个例子,乙烯methylgroup连接,所以它并不遥远。
最好的问候,
大卫