芳香分子的反应
亲电芳香取代:介绍
最后更新:2022年9月25日|
六个关键亲电芳香取代反应
- 在亲电芳香取代碳氢键坏了和新汉英债券(E作为一个亲电原子如氯、溴、N…)就形成了。
- 有六个关键的亲电芳香取代反应在大多数介绍有机化学课程:氯化,溴化,硝化反应,磺化,傅克烷基化,傅克酰化。
- 这些反应需要一个酸催化剂激活它,这样相对稳定的芳环会攻击它。
- 烯烃与亲电试剂反应给“加法”产品。所以苯比较如何?
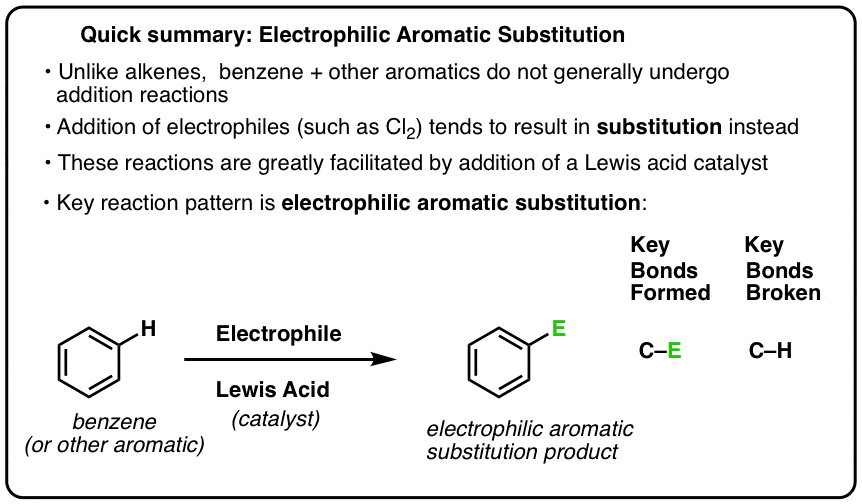
- 亲电芳香取代
- 路易斯酸加速亲电芳香取代反应的速率
- 的关键模式六个重要的亲电芳香取代反应
- 芳香氯化、溴化
- 芳香硝化、磺化
- 傅克烷基化和酰化
- 摘要:六个关键亲电芳香取代反应
- 测试你自己!
1。烯烃与亲电试剂反应给“加法”产品。所以苯比较如何?
当我们的反应烯烃前阵子,很多的反应!——我们发现绝大多数落入反应我们调用的类除了反应。这就是我们打破(相对较弱的)碳碳(pi)债券和形成两个新的碳单键。氯化烯烃与氯2是一个典型的例子:
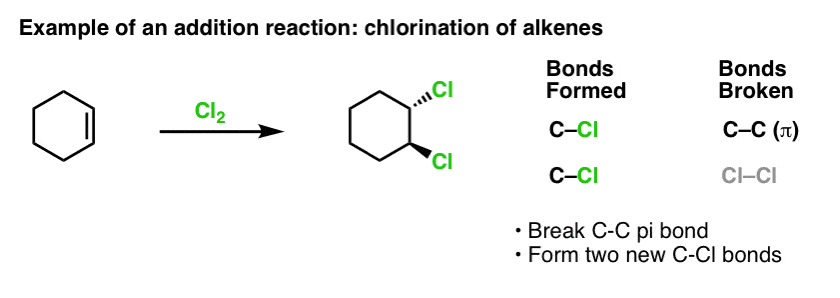
因为我们在苯的话题,很自然怀疑π键的芳香系统(如苯)比较在π键的反应烯烃,进而如何比较芳香族化合物的反应的反应烯烃。
我们已经看到,苯不寻常的稳定(36千卡每摩尔的共振能量)相对于我们期望理论“双键苯”,这肯定会导致我们预测,在芳香分子π键将反应较少,相对于烯烃。
您可能还记得,氢化苯本身就是异常困难。氢(H2)可以添加在大多数烯烃在催化量的精确划分钯碳(Pd / C),但你真的需要突破的奥尔德里奇品牌Whup-Ass®(如高温、高压的H2,延长反应时间)为了成功添加H2苯,相对于“典型”烯烃。
知道了这一点,我们预计会如何像Cl亲电试剂2或溴2与芳香族化合物如苯反应吗?
2。亲电芳香取代
我们的第一个猜想可能是苯与氯反应2给一个“添加”产品如下所示(虽然比“正常”的慢烯烃):
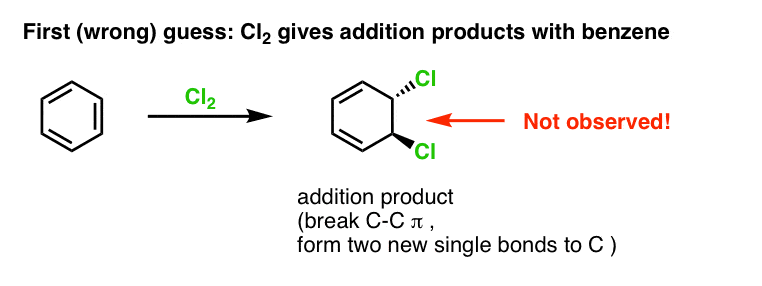
这不是我们观察的产品!
相反,如果你对苯Cl2你最终会(慢慢地)获得以下产品:氯苯。
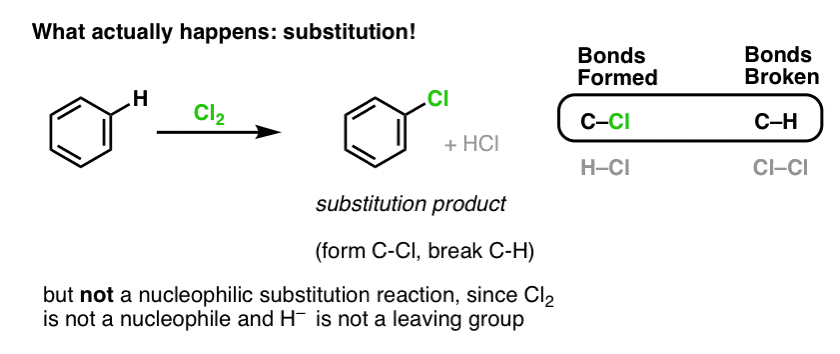
形成的债券和债券打破在这个反应?
我们成立了C-Cl摔断碳氢键。自从π键都完好无损,这是不一个加成反应。相反,这是一种替换反应,形式和打破债券在一个碳原子。
我们已经见过置换反应的一个例子,但这些亲核替换,亲核试剂(如RS- - - - - -)添加到一个烷基卤亲电试剂(例如R-Br)取代离去基团(Br- - - - - -这里)形成一个C-Nuc债券(c)和打破C-LG债券(C-Br这里)。
氯的反应也是如此2与苯同样一个亲核的取代反应吗?不!
Cl2是一个非常可怜的亲核试剂,反应作为给电子体只有强路易斯酸(例如AlCl3下面)。当结合相对温和亲核试剂比如在一个π键烯烃,它表现为一个亲电试剂(电子受体),我们看到在其反应烯烃。
氯的反应2与苯因此被称为一个亲电芳香取代(EAS):
3所示。路易斯酸加速亲电芳香取代反应的速率
氯的反应2与苯比脚趾甲快增长,但幅度不大(ref)(然而,更快更富芳烃如甲苯和苯酚)。所以坐在实验室里的周等待反应完成,我们可以添加一个“汤”试剂氯的反应性2使它成为一个更好的亲电试剂:一个催化剂换句话说。
添加一个好的像AlCl路易斯酸3或FeCl3就可以了。(还有很多其他的路易斯酸,还会做这项工作,但这是一个话题,当我们进入机制——不是今天)。更新:看到帖子机制
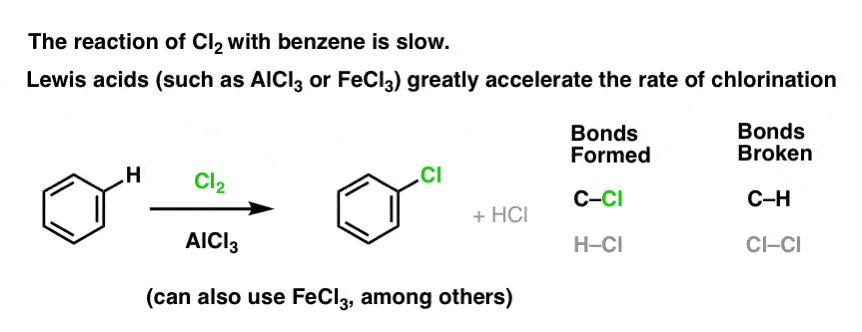
这是如何工作的呢?
从我们的醇系列你可能记得,醇(R-OH)可以诱导参与替换和消除反应如果强酸(形成R-OH补充道2+)。这是因为共轭酸总是更好的离去基团;H2O是一个较弱的基础,从而更好离去基团,比- - - - - -。乙醇本身永远不会与生理盐水给乙氯反应,因为由此产生的离去基团HO -太浓碱相对于Cl -反应进行的程度。但是如果我们转换酒精到它的共轭酸R-OH2+盐酸等强酸,反应可以进行,因为Cl- - - - - -是取代弱得多基地H2O。
它可以帮助认为H +削弱切断键,从而使碳附加到它更好亲电试剂。
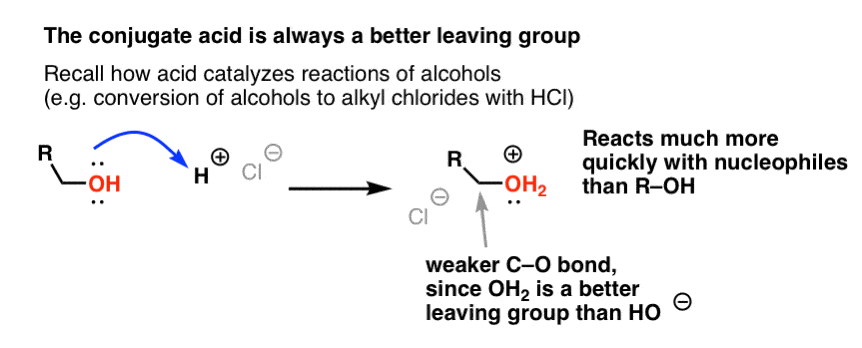
正如酸“素数”的碳哦组后续反应的羟基转化为其共轭酸,路易斯酸同样工作相同的魔法Cl2(和,我们将会覆盖所有的亲电芳香取代反应将涉及某种酸催化)。
在氯化消毒的情况下,路易斯酸(AlCl3从Cl,下文)接受一对电子2。这削弱了Cl-Cl键,使其变成一个更好的亲电试剂。攻击的亲核试剂在远端Cl不会Cl -解放,但甚至较弱的基础(,因此,更好离去基团)AlCl4(-)。
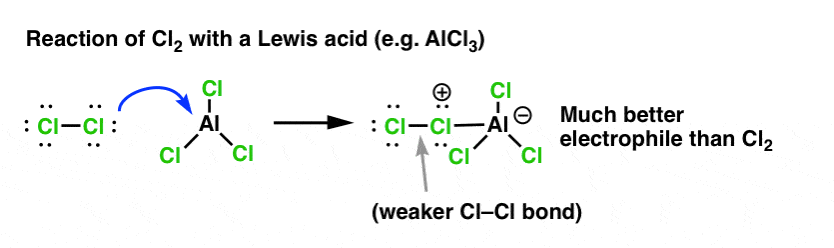
除了路易斯酸(召回,包括像H Brønsted酸吗2所以4)是一个常见的线程的6个关键亲电芳香取代通常覆盖在介绍有机化学。
4所示。的关键模式六个重要的亲电芳香取代反应
在本节中,我们将介绍这六个关键的亲电芳香取代反应,哪一组过渡到三双:
- 氯化、溴化
- 硝化和sulfonylation
- 傅克烷基化和傅克酰化
我们不打算进入机制。这里的重点是按照债券形式和休息,所以你看到的关键模式。
这里是:
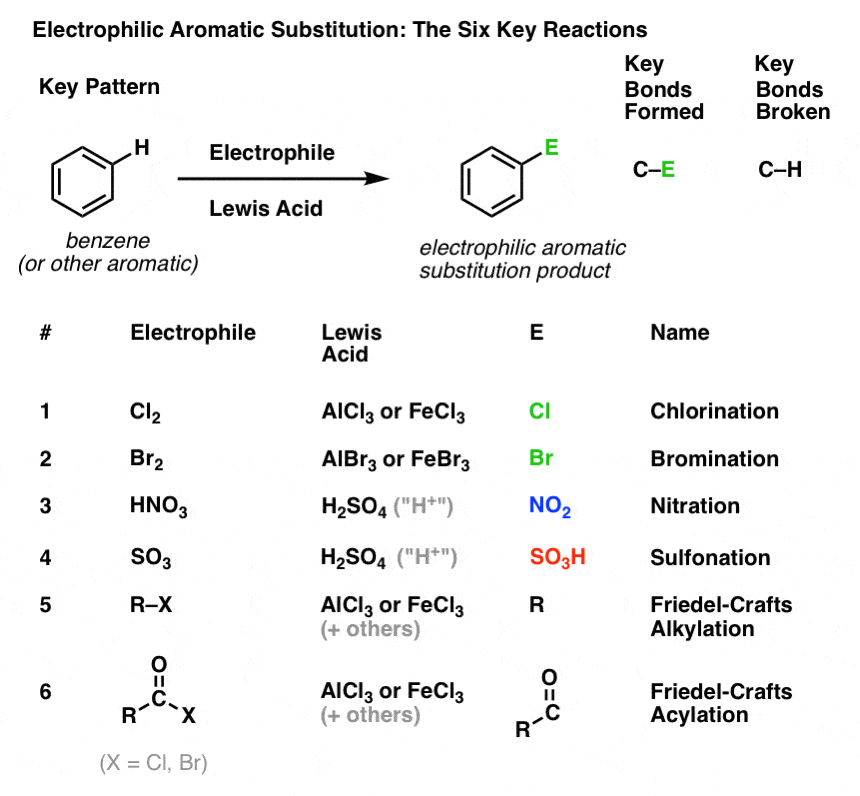
5。氯化、溴化的芳香分子
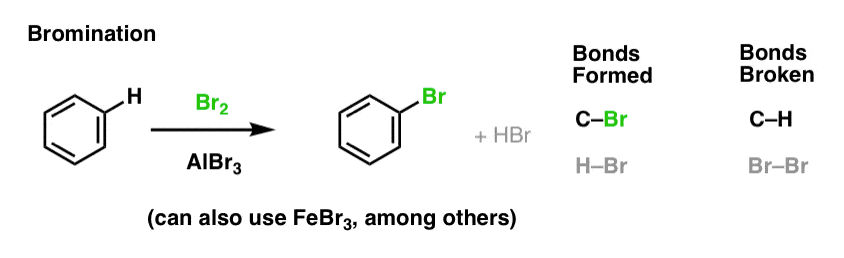
我们已经看到氯化(上图);溴化是非常相似的。由于溴2本身并不是一个足够强大亲电试剂与苯反应在一个合理的利率,我们使用诸如AlBr路易斯酸3或FeBr3加速反应。(使用AlBr3/ FeBr3而不是AlCl3/ FeCl3卤化物的避免一些“爬”,随后在文章中我们将会看到当我们进入机制)。
6。硝化、磺化芳香分子
硝化反应(更换H2集团)不是一个反应,我们看到在我们的部分烯烃,但它是一个受欢迎的反应与苯等芳香分子。这是甲苯的反应(甲苯)转化为2,4,6-trinitrotoluene。你可能更熟悉这个分子烈性炸药TNT。
硝化的替代H没有2用硝酸(HNO3)的来源2和硫酸(H2所以4)作为路易斯酸:
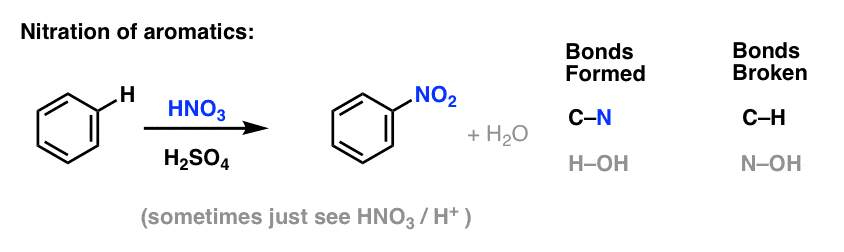
磺化(更换H3H组)也变成了一个有用的反应。它可以通过添加三氧化硫(这样执行3)在硫酸的存在(H2所以4)作为路易斯酸:
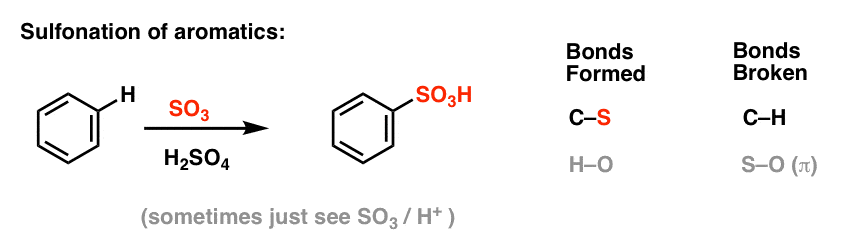
7所示。傅克烷基化和酰化
在上面的四个反应中,我们观察到C-Cl的形成,C-Br、碳氮和c。
也有可能形成碳碳键通过添加芳香分子烷基或酰卤化物在路易斯酸的存在。这些反应是众所周知的傅克反应后反应,发明家(反应可以追溯到1877年)。
在傅克烷基化,我们从一开始烷基卤化物等“r×”CH3CH2Cl AlCl等,然后添加一个路易斯酸3或FeCl3(还有许多其他的路易斯酸的工作,但这些是最常见的例子]。与氯2,路易斯酸加速卤素反应协调,削弱C-Cl债券,使它更好离去基团从而允许连接碳更容易受到亲核试剂。没有发生反应,而路易斯酸。
注意,这里我们形成碳碳和碳氢键。
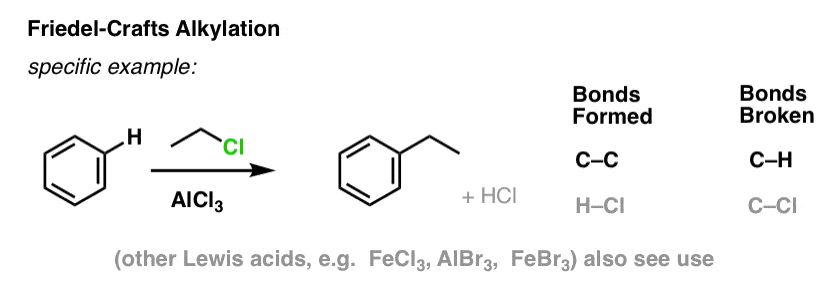
的傅克酰化是相似的,但我们从一个开始呢酰基卤化物。除了我们的路易斯酸导致的形成碳碳和碳氢键的破损。
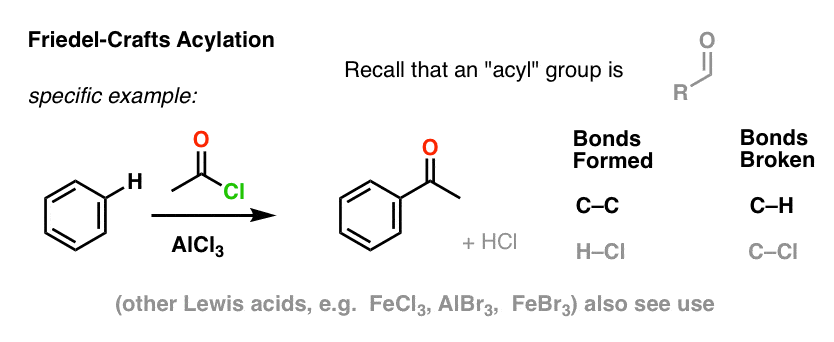
8。摘要:六个关键亲电芳香取代反应
我们已经展示了六个关键亲电芳香取代反应(氯化、溴化、硝化、sulfonylation傅克烷基化和酰化),他们都涉及碳氢键的断裂和形成汉英(“E”亲电试剂在问题)。
但知道债券形式,打破仅仅是个开始。
这里有一些问题,我们想知道这个问题的答案:
- 取代基对苯如何影响这个反应?例如,这些反应可能如何影响对甲苯如果我们执行他们吗?或苯酚?或氯苯吗?
- 如何电子基或吸电子取代基影响反应的速度?
- 与苯,只有一个mono-substituted产品可能形成。但是如果我们开始mono-substituted产品和做一个亲电芳香取代吗?最终取代基的哪里?
- 反应是如何工作的呢?我们如何解释的形成汉英和碳氢键的断裂?
- 以外的其他芳香组(苯)。怎么亲电芳香取代吡咯反应,吡啶、萘或其他团体比较?
在下一篇文章中,我们将讨论第一个问题:电子基、取代基吸电子的影响。我们会讨论激活和安静下来组。
在下一篇文章:激活和去活化组
感谢你的阅读!
许多感谢马修Knowe援助与这篇文章。
笔记
测试你自己!
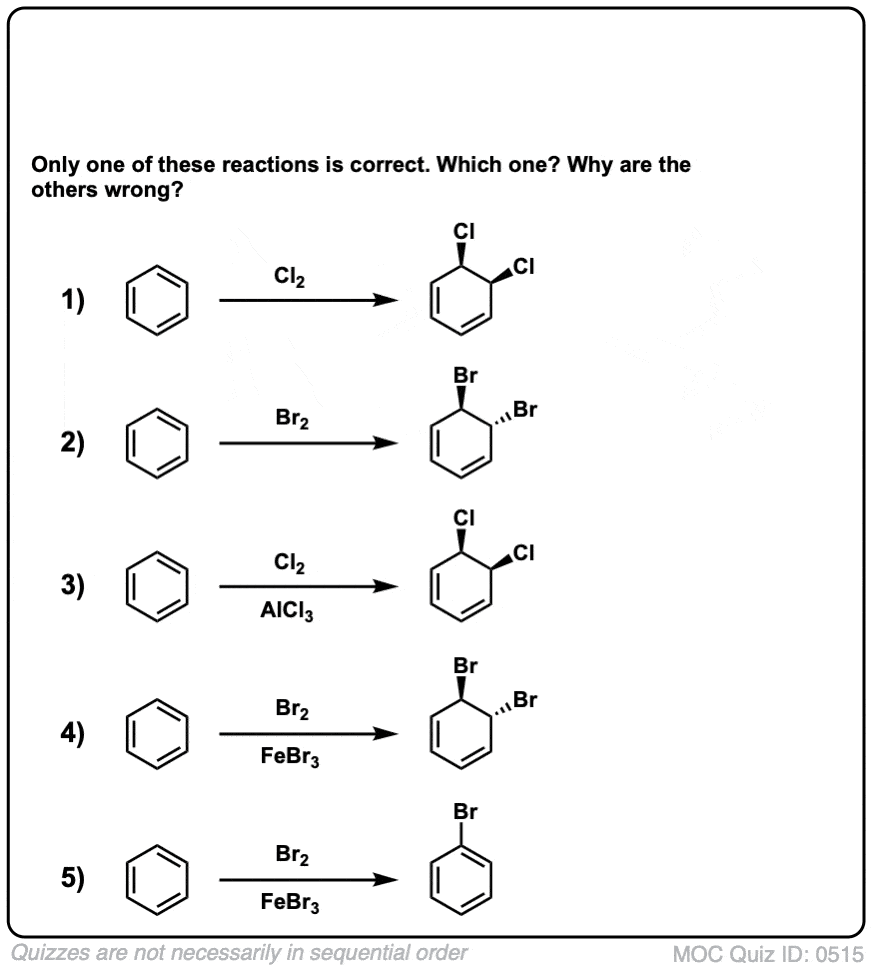 点击翻转
点击翻转
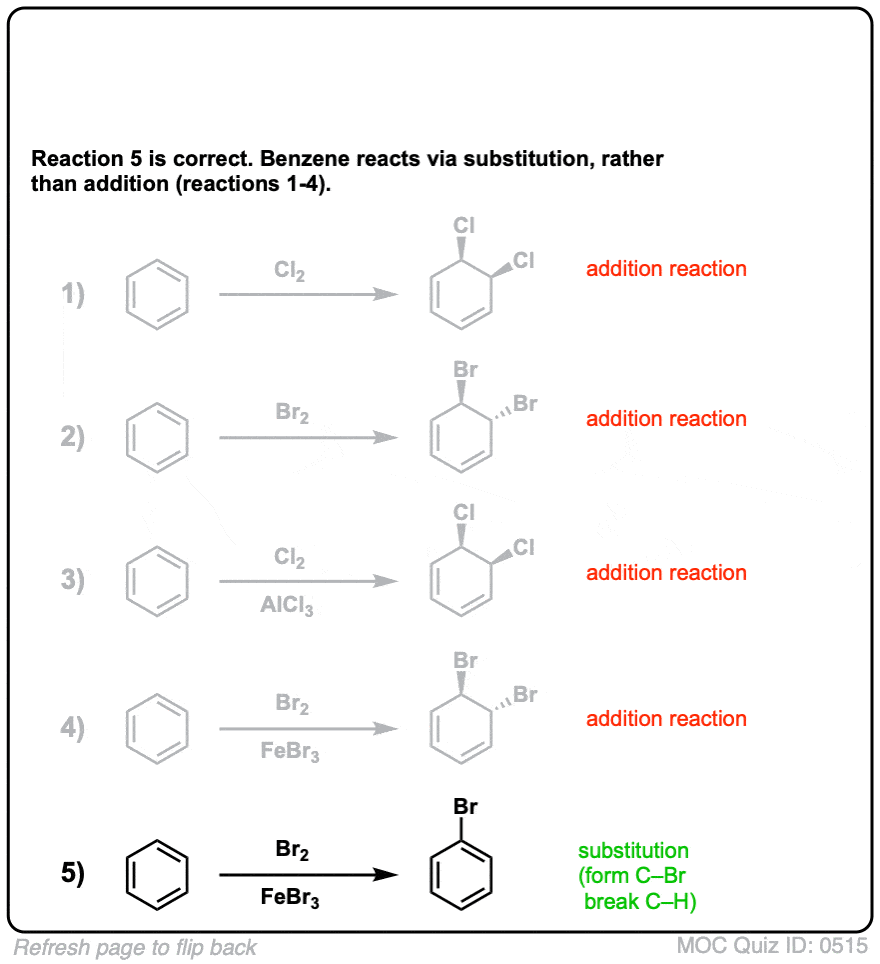
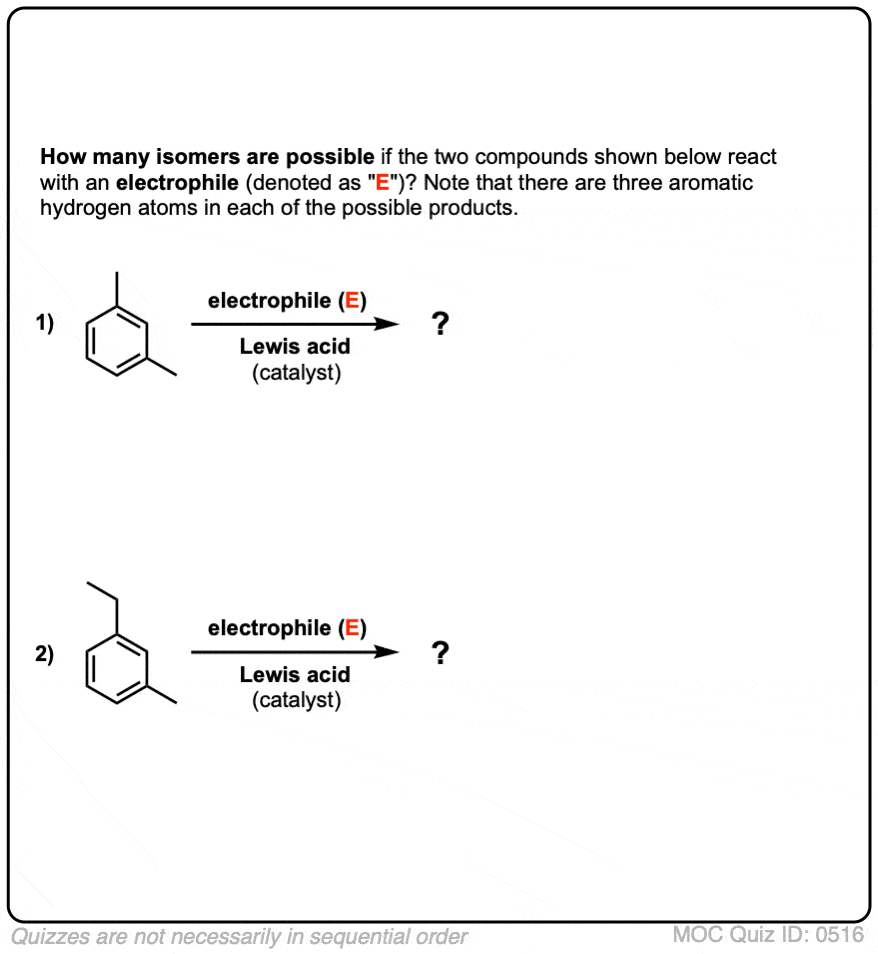 点击翻转
点击翻转
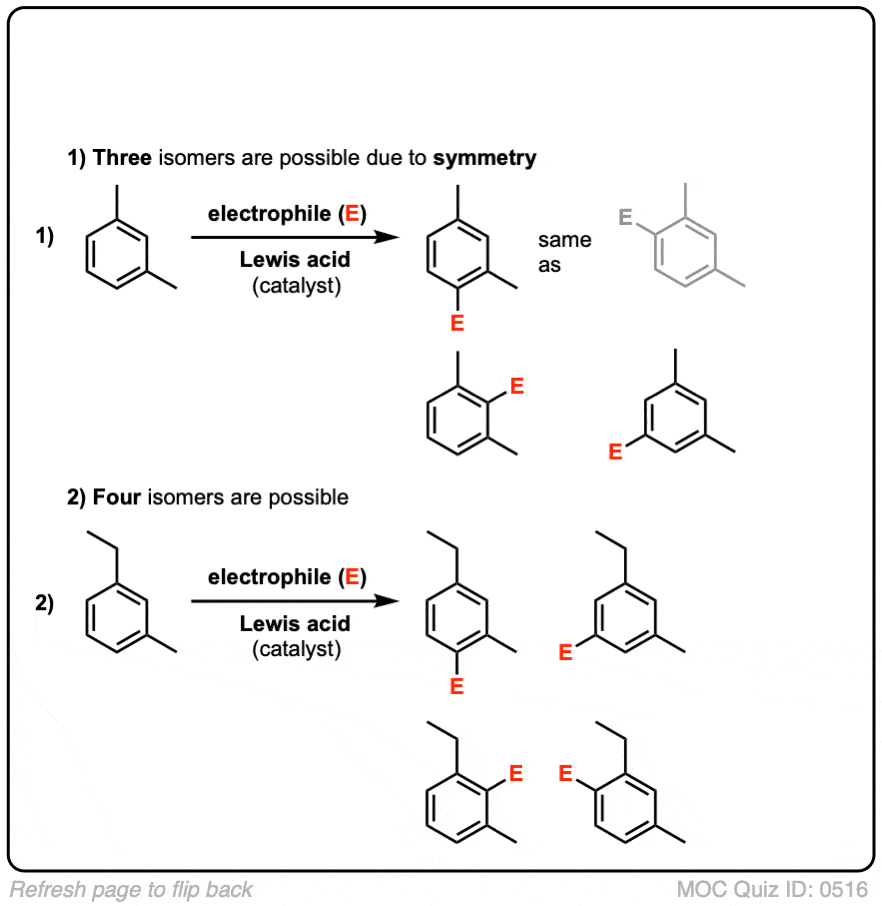
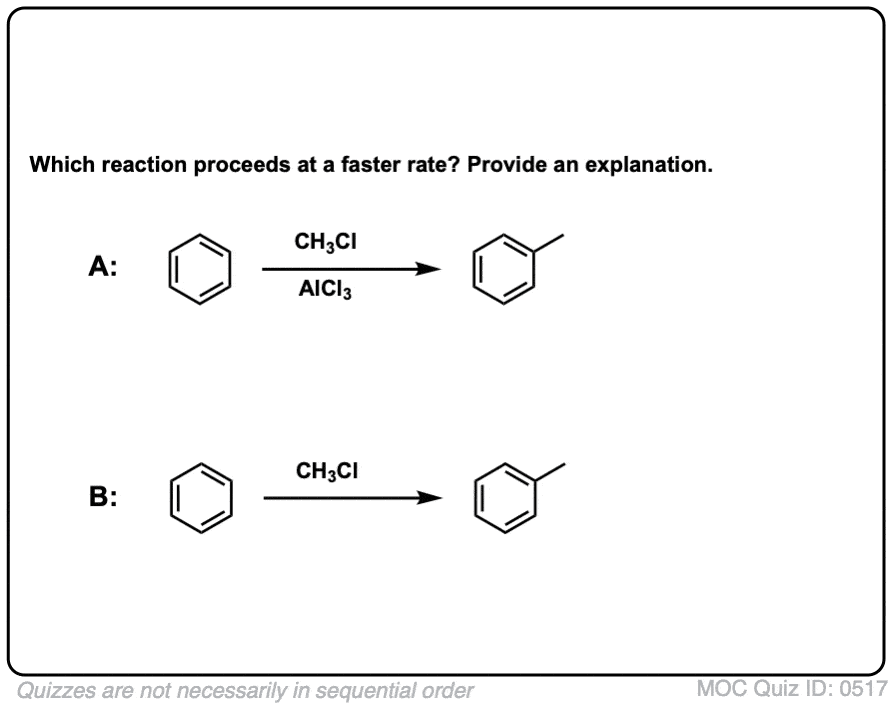 点击翻转
点击翻转
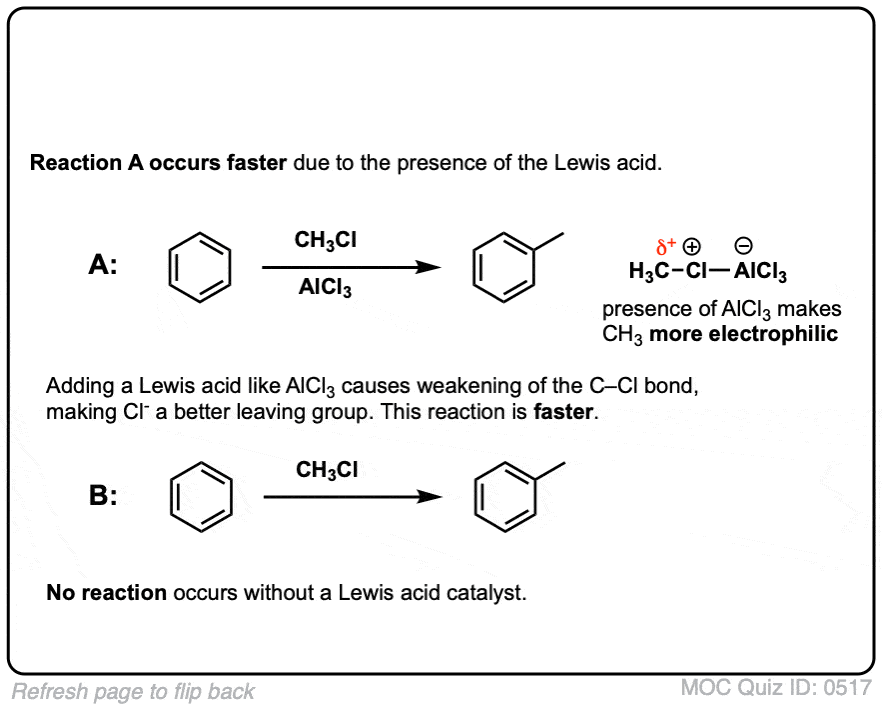
这是因为分子缺少一个对称面。
我真爱你解释! ! !谢谢你持续到…
你好,我不懂如何测试问题”有多少同分异构体形成“导致c (ch3) 3取代苯有四种同分异构体?
请还包括加成反应等多种芳香系统蒽,联苯等。这将是非常有用的
我有一个问题。目前我从事这个项目。它由双香豆素coumarine从肉桂。一步是添加哦小组第四个碳原子,所以我可以得到4-hydroxycoumarin。我不知道,我将非常感激如果有人回答了我自己的建议。请,真的很紧急。提前谢谢你
请提供订单的亲电反应在不同的芳香族化合物(苯并杂环)
那听上去是个好话题你研究!
好但不够。应该讨论双取代的化合物
覆盖在后面的帖子!
只是一个建议
请组织主题订单,以便读者可以通过串行明智,因为它对我们来说是非常困难的(学生)去寻找下一个话题,是浪费时间。
如果有提供,请接受我的道歉,我是新到这个网站。
但是教训是优秀. . ! ! ! !吗?的解释很好…。
谢谢你!
是的,在进步!
神奇的!
“既然Br2本身并不是一个足够强大的亲电试剂与苯反应在一个合理的利率…”——这通常是正确的,但快速反应是Br2浓度高(没有任何催化剂)[JCC 2016年,37岁,210 - 225;DOI: 10.1002 / jcc.23985]。
肯定的——它可能发生(特别是电子丰富的基质),但一般来说,你想要使用一个催化剂。