焊接、结构和共鸣
一个关键技能:如何计算形式电荷
最后更新:2023年5月22日|
如何计算形式电荷
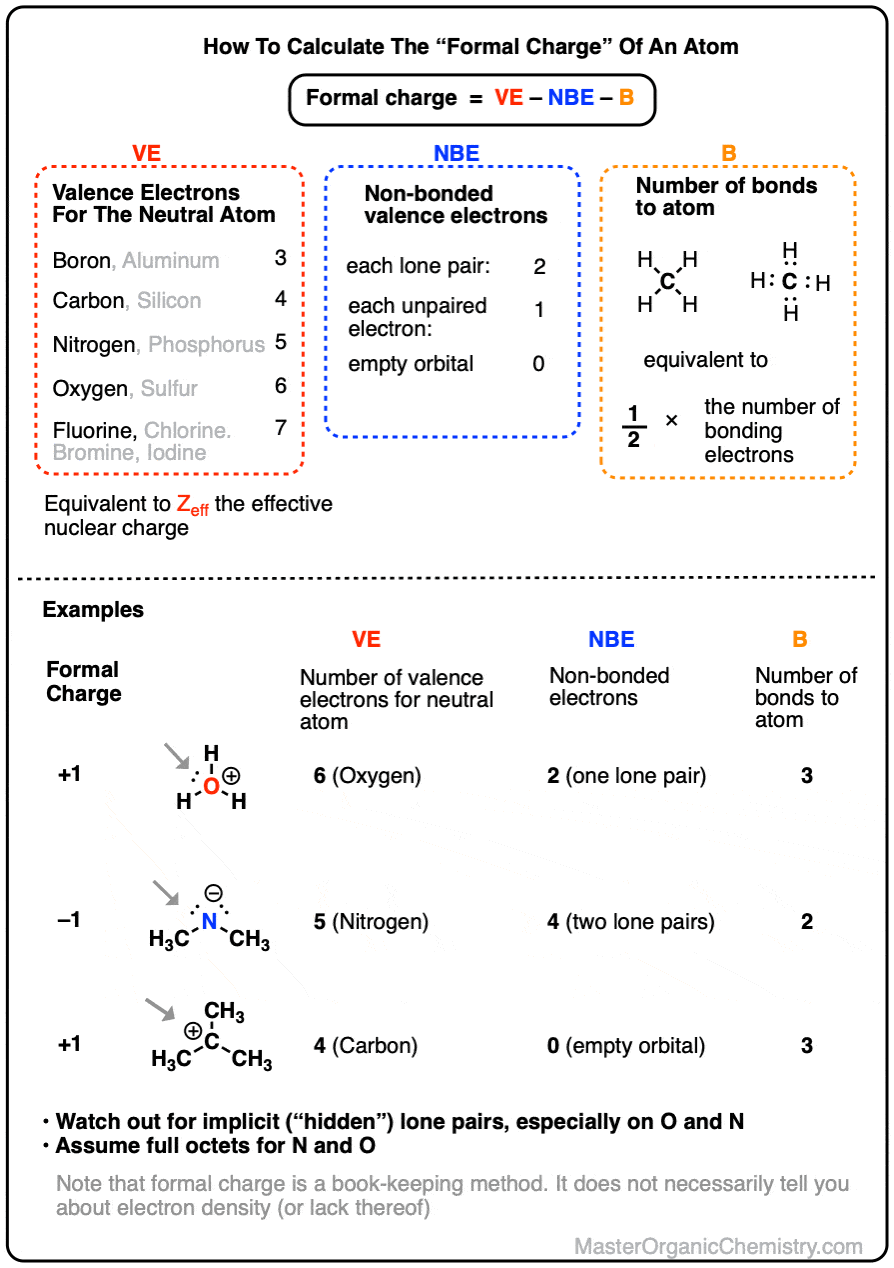
计算形式电荷一个原子,我们先:
- 评估的数量价电子(已经)的中性硼原子(如3、4为碳,5氮,等等)。(注意:这也相当于有效核电荷Zeff质子的数量,一个电子的价轨道“看到”由于内壳层电子筛选)。
- 数的数量非键价电子(NBE)在原子。每一个孤对计数2,每一个未配对电子计数1。
- 数的数量债券(B)原子,或者计算成键电子的数量和这个除以2。
的形式电荷足球俱乐部然后计算减去吗NBE和B从已经。
足球俱乐部=已经- (NBE+B)
相当于
FC =已经- - - - - -NBE- - - - - -B
计算很简单如果所有的信息是给你的。然而,为了简洁起见,有很多时候孤和碳氢键是没有明确画出。
所以技巧对你的一部分将被计算形式电荷在你需要的情况下考虑隐式的孤和碳氢键。
在下面的文章中,我们将处理这些情况。我们也会警告你的情况计算形式电荷原子的不一定是好线索反应性,这是非常重要的。
表的内容
1。形式电荷
形式电荷是一个簿记形式主义分配到一个特定的原子。
获取形式电荷一个原子,我们首先计算的数量价电子(注1)的中性原子,然后减去它的电子数量”拥有”(即在孤对电子,或独占轨道),一半它的电子股票(成键电子数的一半,相当于债券的数量)
最简单的方法写的公式形式电荷(FC)是:
足球俱乐部=已经- - - - - -NBE- - - - - -B
在哪里
- 已经对应于中性原子周围的电子的数量碳硼(3、4、5为氮、6氧,7为氟)
- NBE对应于非键电子在原子的数量(2孤对,独占轨道1,0为空轨道)
- B的数量是债券在原子(相当于半成键电子的数量)
它被称为“正式的“因为它假定所有的成键电子都共享同样。它不占电负性差异(即偶极子)。
因为这个原因形式电荷并不总是一个很好的指南,电子是在一个分子和反应可以是一个不可靠的指南。我们将会有更多的说下面。
2。板凳元素的简单的例子
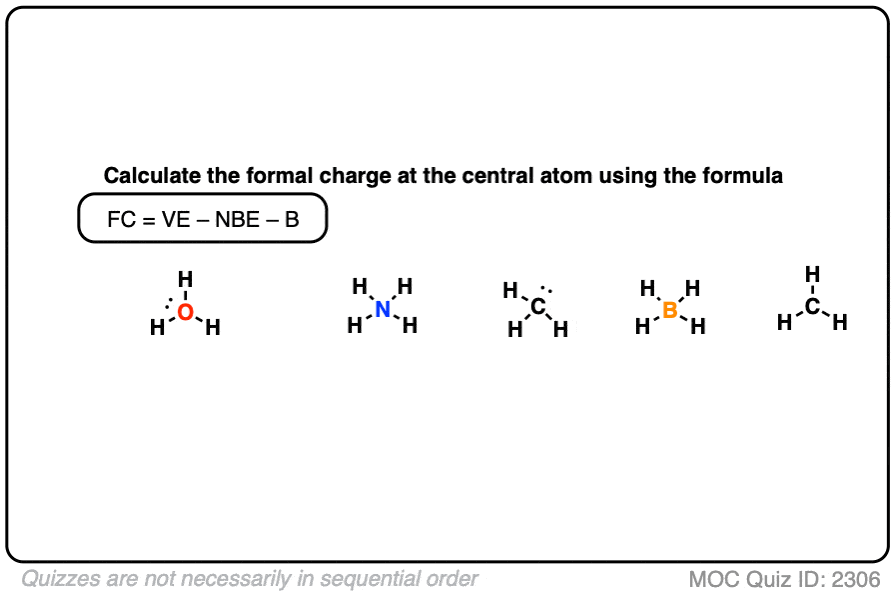
当所有的孤会被抽取出来,计算形式电荷相当简单。
让我们一起通过测验中的第一个例子如下。
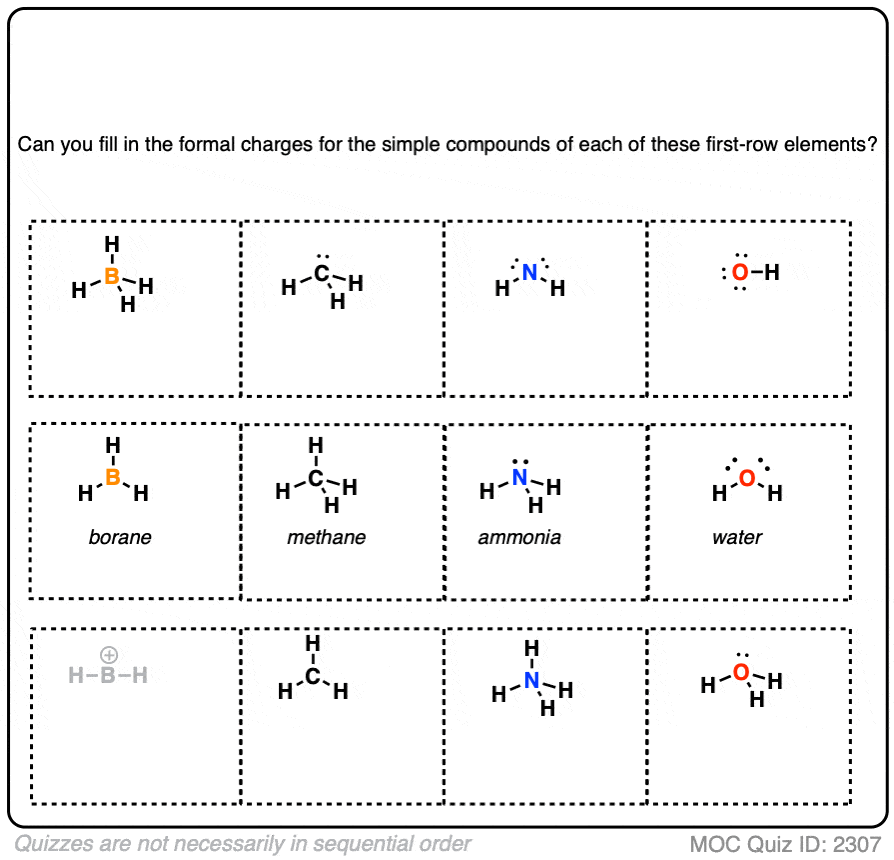
看看你能不能填写其余下面的例子。
 点击翻转
点击翻转
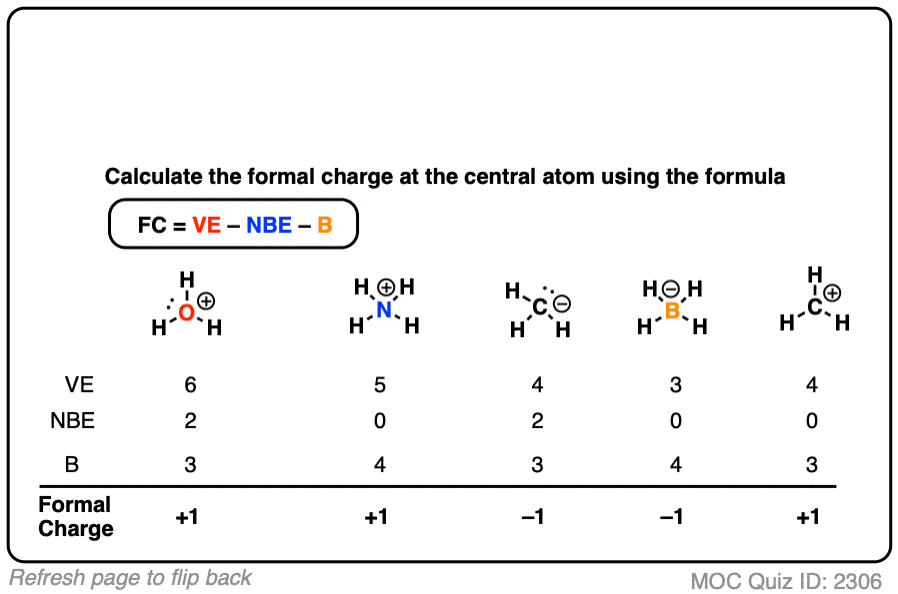
如果顺利,你可以试着填写正式指控的这个表中的示例。
 点击翻转
点击翻转
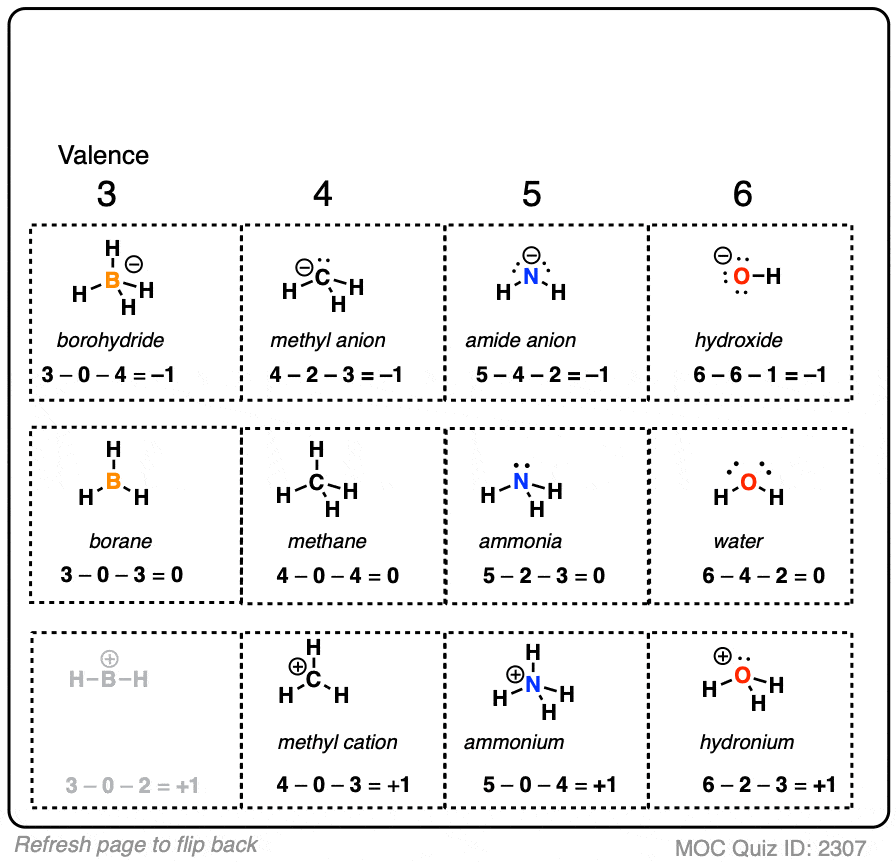
这将需要一些时间来适应形式电荷,但一段时间后假定你知道如何计算形式电荷,你可以识别结构,原子将会有一个形式电荷。
让我们处理一些稍微棘手案件。
3所示。当你没有给所有的形式电荷计算细节
当我们画一个棒的一个人,不要画在他们的手指,这并不意味着我们要画的人有一个糟糕的一天使用台锯。我们只是假设你可以填写的手指如果你真的需要,但你不只是为了节省时间。
化学线画简笔画。他们忽略了很多的细节,但仍假定你知道某些事情的存在。
- 与碳,我们经常忽略绘画氢。你还应该知道他们的存在,并添加尽可能多的氢需要给一个完整的八隅体(或六重奏,如果是碳正离子)。
- 如果有一个孤对碳或不成对电子,它总是吸引了。
 点击翻转
点击翻转
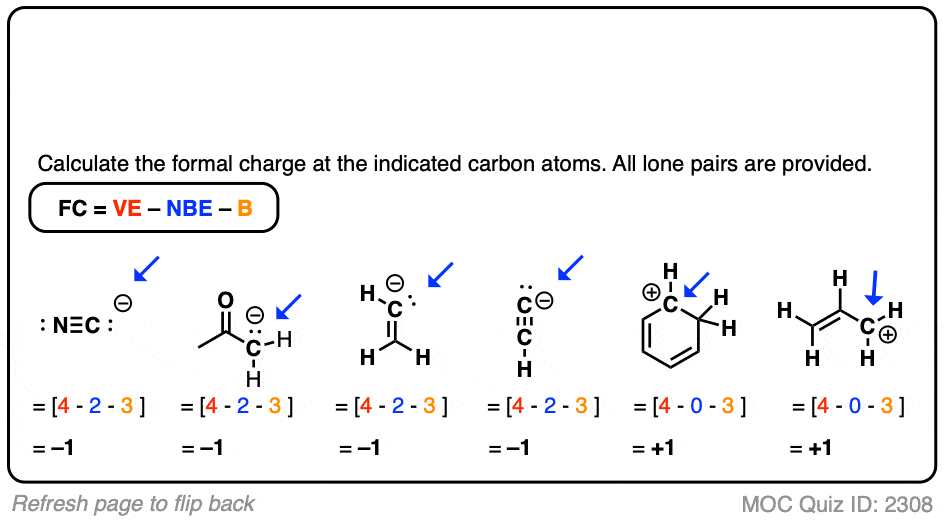
一个音符。如果我们画一个图,我们做画出手指,和花时间只画3,那么我们可以安全地假定人真的只有3个手指。所以在过去的两个例子,测验我们必须画在氢你为了知道它是碳正离子,否则你会认为它有一个完整的八隅体!
氧和氮(卤素)处理略有不同。
- 债券氢总是在绘制。
- 的孤经常省略。
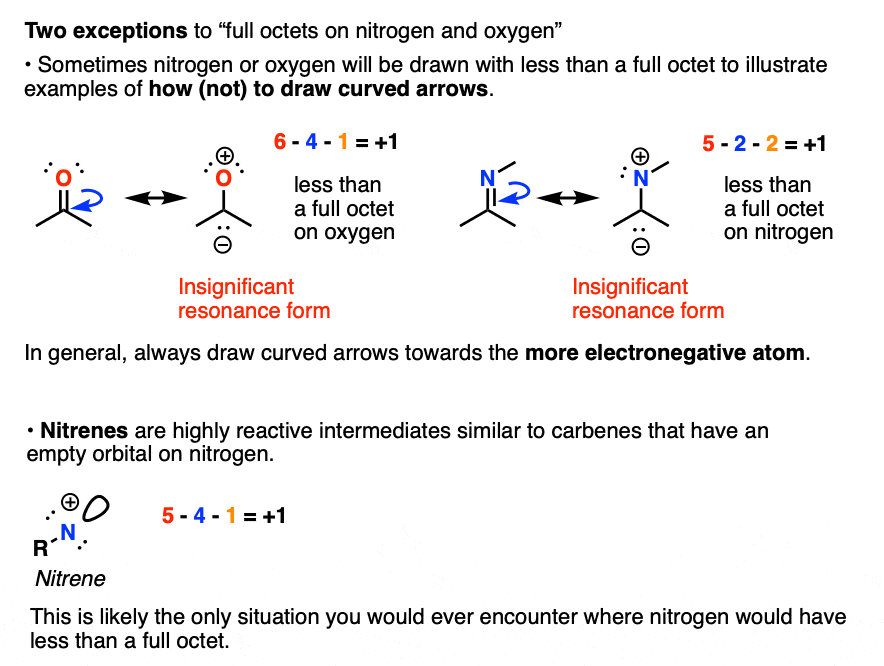
- 氮气和氧气将总是有完整的八位字节。总是这样。(注2- - - - - -好吧,两个例外]
所以即使孤不画,假设存在足以使一个完整的八隅体。从这些原子氢,当债券失踪,这意味着什么似乎是:实在是没有任何氢!
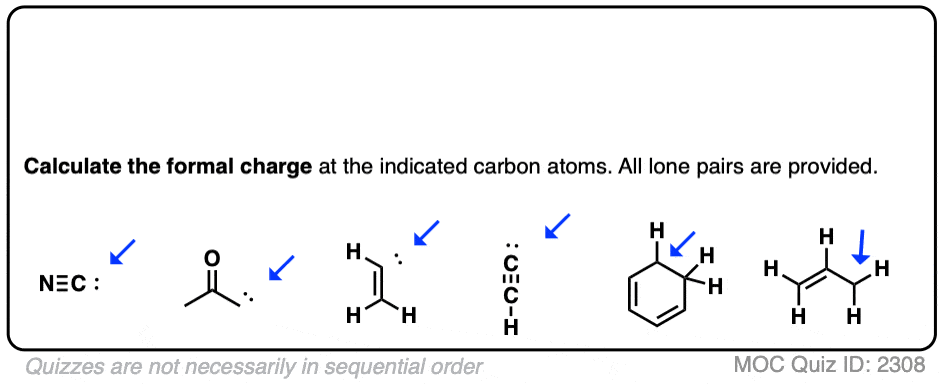
试试这些例子:
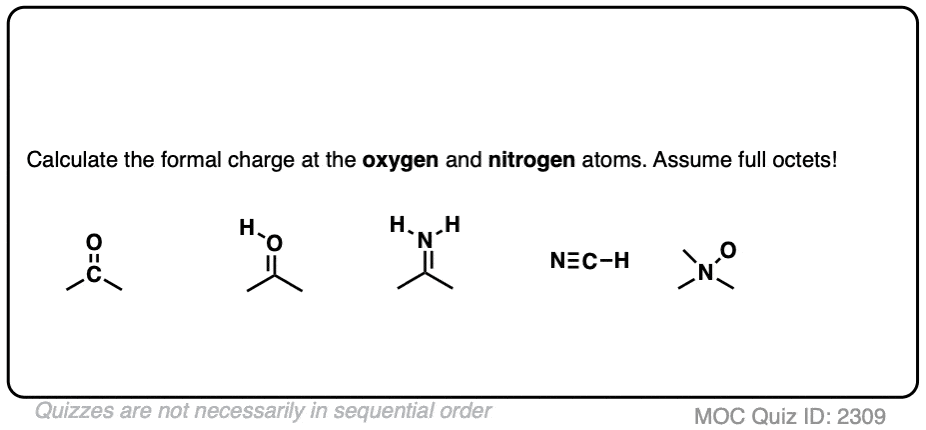 点击翻转
点击翻转
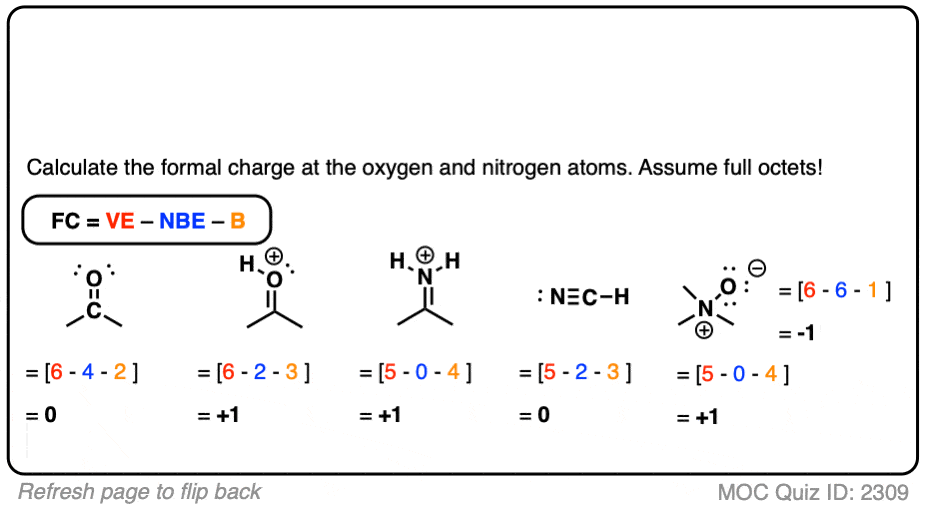
现在看看你能不能把这些例子!
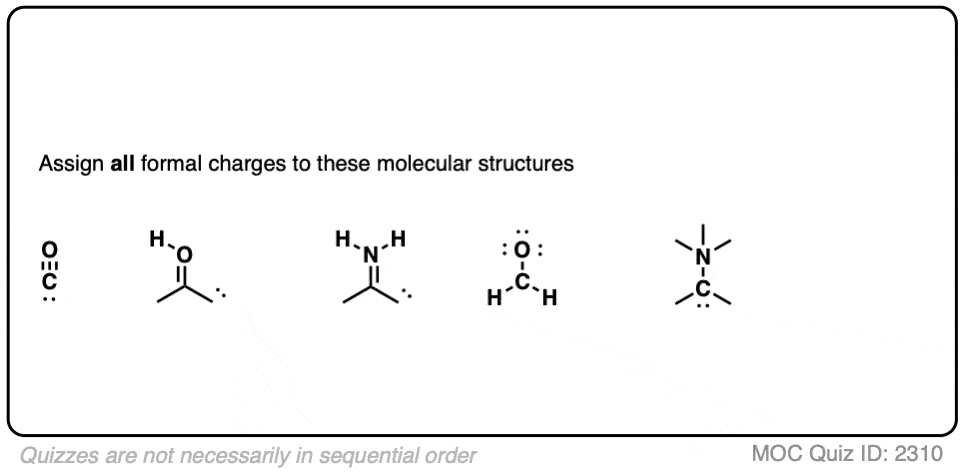 点击翻转
点击翻转
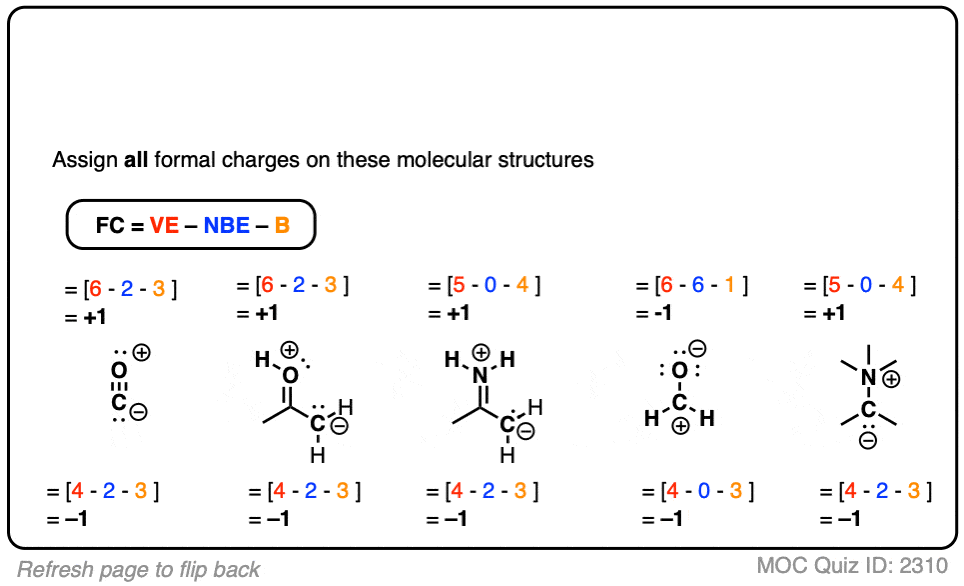
(注意,这些不稳定的分子,而是代表是共振形成期间,你会遇到各种点!)
4所示。一些经典的形式电荷的问题
我们可以用完全相同的形式电荷上面的公式,以及隐含的规则孤和氢,算出形式电荷在一些漂亮的异国情调的分子的原子。
下面是一些经典的形式电荷问题。
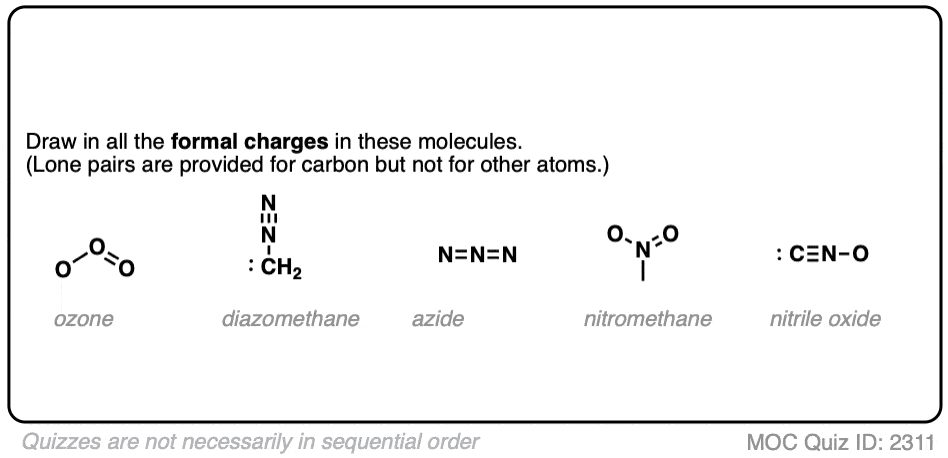 点击翻转
点击翻转
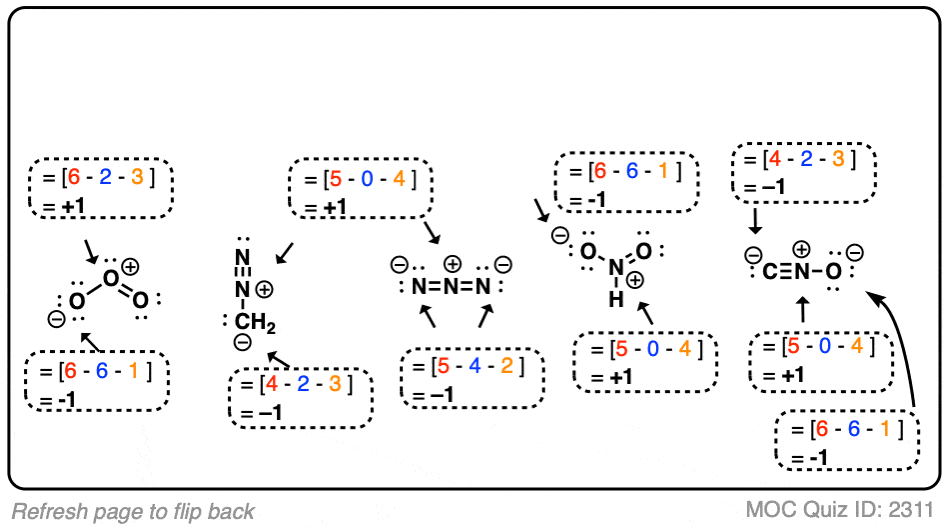
注意,尽管结构可能看起来很奇怪,的形式电荷公式是相同的。
的形式电荷公式甚至可以应用到一些相当奇异的活性中间体之后我们会见面在这个学期。
不要惊吓了。数的电子和债券,这将引导你正确的答案。
 点击翻转
点击翻转
5。正式的指控和弯曲的箭头
我们使用弯曲的箭头显示电子对运动的反应和共振结构。(看到帖子:弯曲的箭头的反应)
例如,这是一个曲线箭头显示氢氧根离子的反应HO(-)与一个质子(氢离子)。
箭头表示运动的两个电子氧形成新地债券。
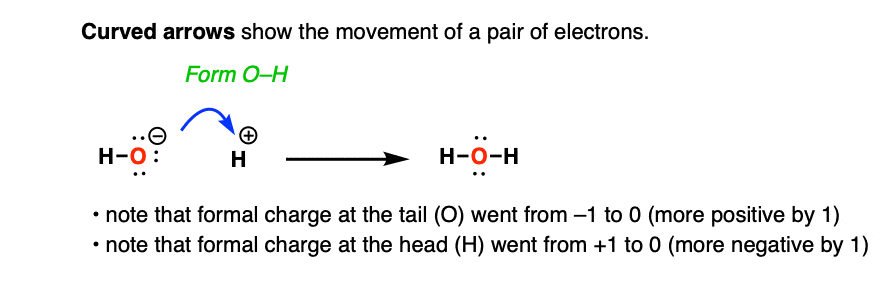
弯曲的箭头也用于跟踪变化形式电荷。请注意,形式电荷在最初的尾巴弯曲的箭头(氧气)更积极的(从1到0)和形式电荷在最后的尾巴(H +)更多的负面(从0 + 1)。
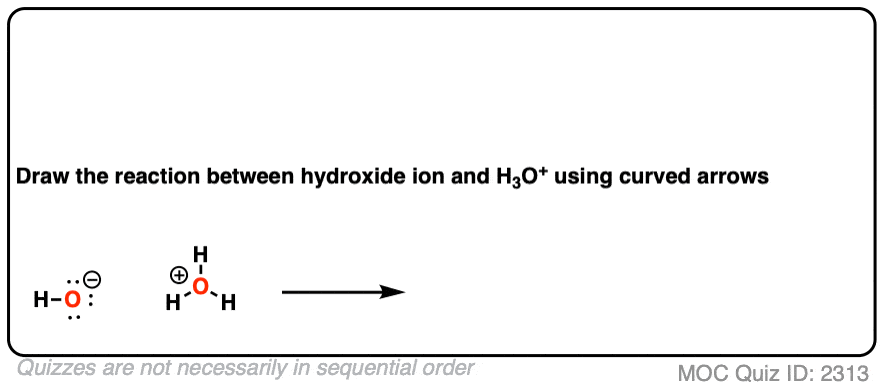
当酸添加到水,我们形成了水合氢离子,H3O+。
这是一个测试。看看你是否能画出曲线箭头从氢氧根离子H3O +。
 点击翻转
点击翻转
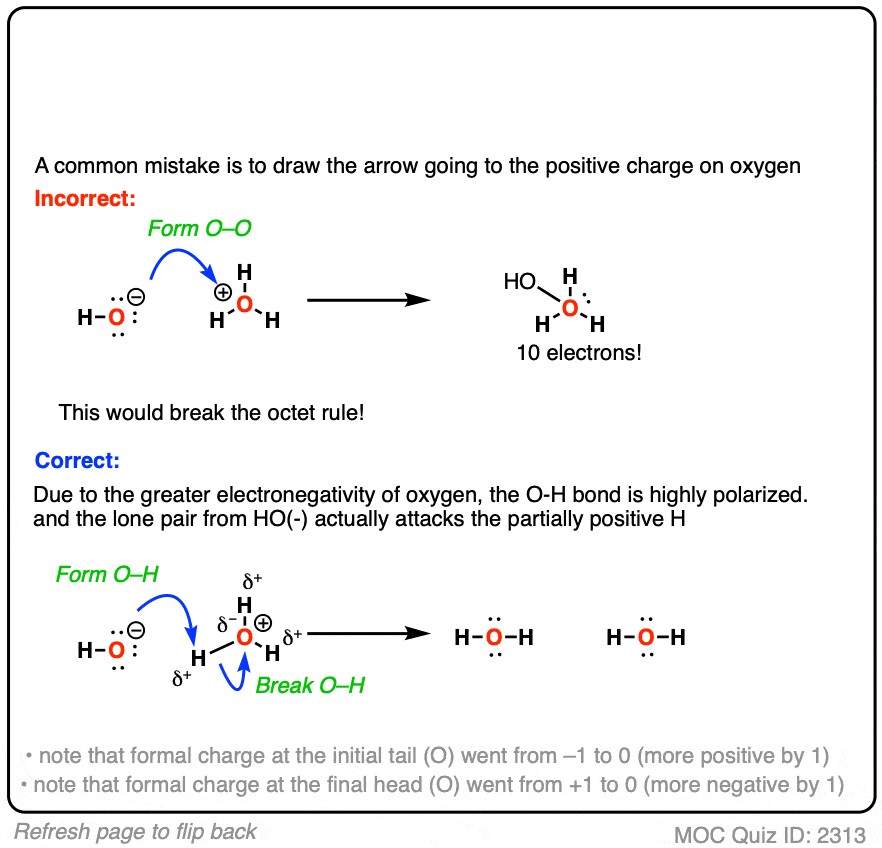
如果你成功做到了,恭喜你!
但我敢打赌,至少一小部分你去画出箭头带正电的氧气。
有什么问题吗?
在氧气没有空轨道,可以接受孤对。如果你遵循的逻辑曲线箭头,o - o键,将导致一个新的和10个电子氧,破坏八隅体规则。
坚持一分钟,你可能会说。”我认为氧气是带正电的吗?我f并不在氧反应,它在哪里应该作何反应?”
在氢!H3毕竟,O + Brønsted酸。对吧?
这是一个很好的说明为什么它被称为“正式的”,以及如何收费形式电荷不一样的静电电荷方。“部分费用”或“电子密度”)。
形式电荷最终是一个簿记形式主义,有点像把“赢”分配给一个5投手在棒球比赛。(注3]它不考虑电子的氧氢键不平等共享,大量的偶极子。
所以尽管我们画一个“正式的”在氧气,部分正电荷都在氢。尽管轴承一个积极正式的熊收取部分负静电电荷。
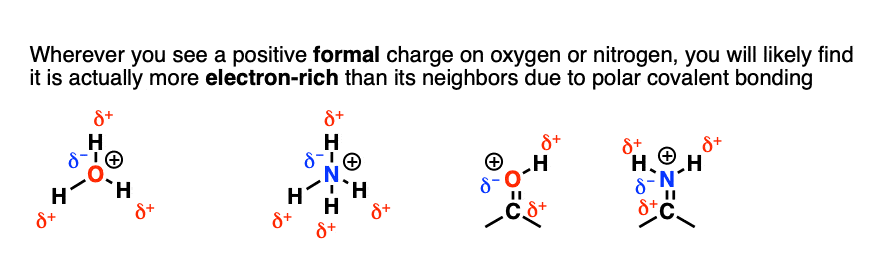
这就是为什么基地如HO在H(-)的反应,不是氧气。
再次重申:
- 正电荷在氧气和氮不代表一个空轨道。假定氧和氮有完整的八位字节!(注2]
- 相比之下,在碳正电荷做代表空轨道。
6。卤素
积极的正式指控卤素分为两大类。
我们经常会发现绘画halonium离子Cl +品牌+,+随着物种有六个价电子和空轨道(但从未F + -这是一个贪婪的野兽)
可以认为这些物种是轴承空轨道因为它们是大的和相对可极化的。他们可以把正电荷相对较大的体积。
这些物种可以从一个接受孤对电子路易斯碱,导致一个完整的八隅体。
Cl, Br,我还可以忍受积极结果连着的正式指控两个原子。
重要的是要认识到在这些情况下,卤素熊完整的八隅体而不是一个空轨道。他们会因此没有直接接受一对电子从刘易斯基地;通常情况下,原子相邻卤素接受电子。
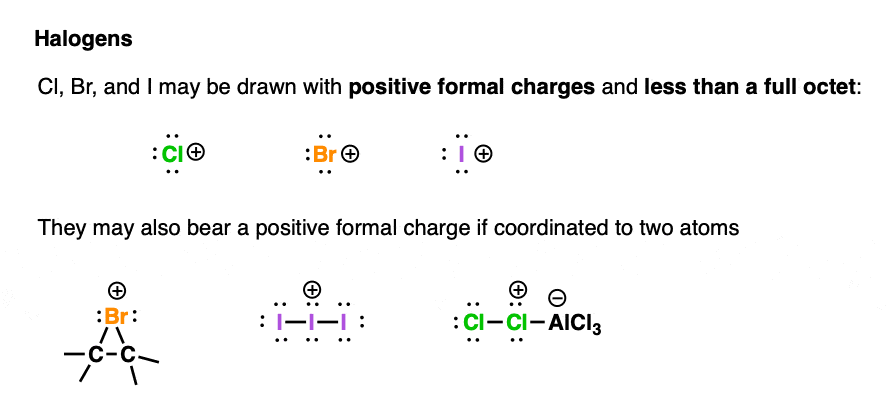
7所示。结论
如果你已走到了尽头,所有的测验,你应该准备好所有的例子形式电荷你看到在剩下的课程。
- 形式电荷可以使用公式计算足球俱乐部=已经- - - - - -NBE- - - - - -B
- 线图经常省略孤和碳氢键。对于这些情况在计算形式电荷保持警惕。
- 带正电的碳空轨道,但假设带正电的氮气和氧气有完整的八位字节。
- 的例子水合氢离子H3O +显示依赖的危险形式电荷了解反应。密切关注电负性的差异原子间并绘制出偶极子真正意义上的反应。
笔记
注1。使用“价电子”让你正确的答案。但是如果你仔细想想,它并没有多大意义。正电荷是从哪里来的?从带正电的质子在原子核中,当然!
所以这个方程的“价电子”更恰当的被认为是一个代理价质子——这是另一种说法“有效核电荷”;离原子核电荷感受到每一个价电子,除去了内心的贝壳。
注3。在棒球比赛中,每场比赛的结果在一个赢得或失去团队。在的日子老霍斯Radborn完成游戏是常态,这是分配的合理延伸赢得的个人投手。在当今时代,与多个救援投手,有规则确定哪些投手会因为这场胜利。很可能完全一个投手丘炮击,然而,在偶然的情况下,仍然是赢得称赞。看到帖子:也许他们应该称之为,“正式赢”?
同样,氧气个人信用为+ 1的指控水合氢离子H3O +,即使实际积极的氢原子之间的静电电荷分布。
注4。这张照片从先前的这篇文章成功了一些关系板凳的各种化合物的几何元素。
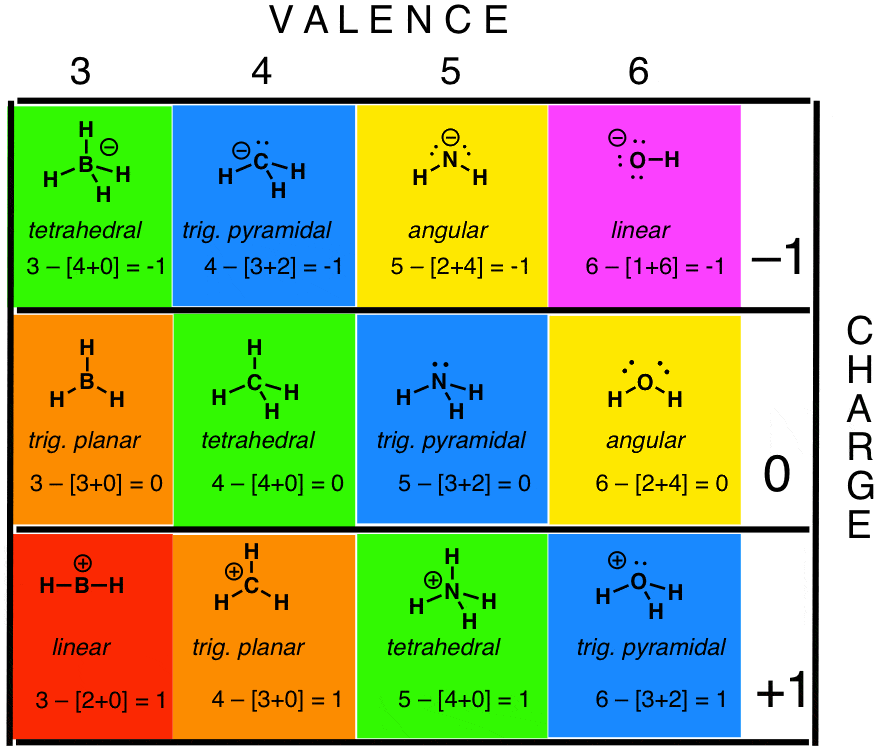
测试你自己!
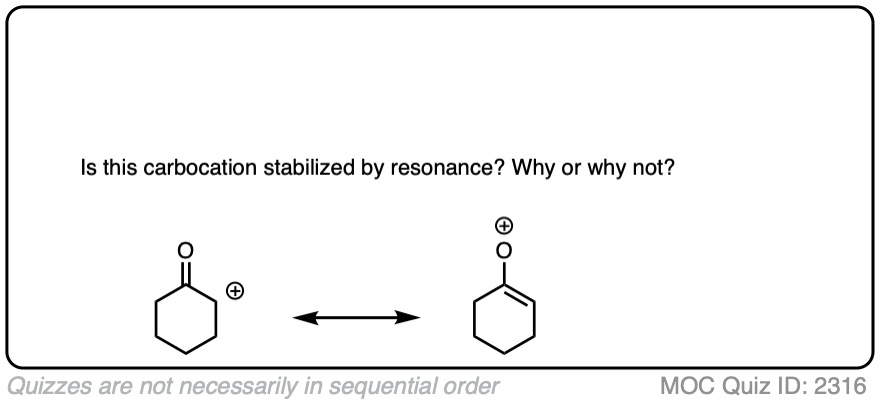 点击翻转
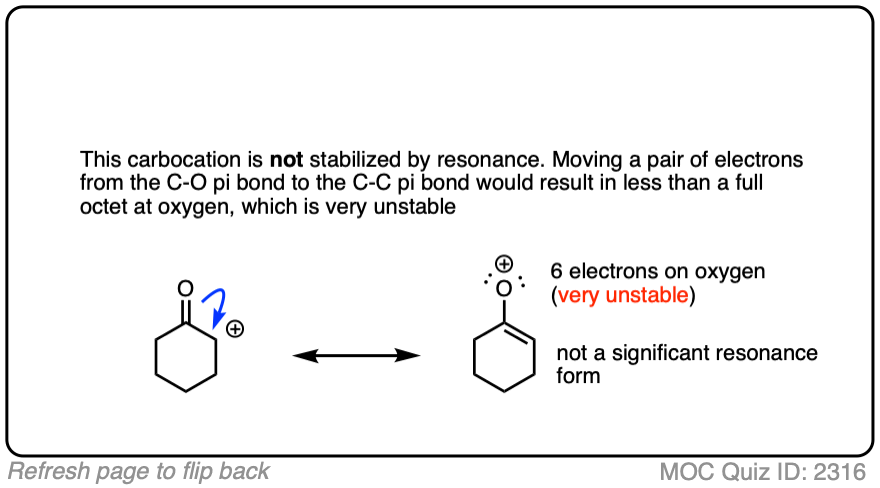
点击翻转
(高级)引用和进一步阅读
1。价、氧化值形式电荷:三个相关但完全不同的概念
杰拉德•帕金
《化学教育2006年83(5),791年
DOI:10.1021 / ed083p791
2。路易斯结构,形式电荷和氧化号码:更用户友好的方式
约翰·e·帕克和希拉·d·伍德盖特
《化学教育1991年68年(6),456年
DOI:10.1021 / ed068p456
你的解释和例子是清晰和易于理解。我感谢详细的一步一步的指示,这使得很容易跟随和理解的概念。谢谢你花时间来创建这个有用的资源
我认为对于测验ID: 2310年,碳的形式电荷在第四分子应该+ 1而不是1。
固定的。谢谢你的地方!
非常感谢先生。最后我明白了如何计算形式电荷
好简单的解释
伟大的教学,我可以知道你在哪里学习? ?
你好我非常困惑。你提供的两个公式计算FC是不一样的,不要当我试着他们产生相同的结果。
价电子的形式电荷=[#]-[电子孤+ 1/2的成键电子数)
和
形式电荷=[#原子的价电子]-[非键电子+债券)的数量。
他们不能产生相同的结果…
如果我有BH4的公式,并使用第一个公式提供了找到B的俱乐部,我将获得:
(3)- (0 + 2)= + 1
使用提供的第二个公式:
(3)- (0 + 4)= 1
这些公式不应该产生相同的结果吗?我很困惑,我不知道如果我错过了一些东西。
啊。我应该更清楚。的成键电子数BH4 = 8,因为每个键有两个电子,有4 b - h债券。这个数字等于4的一半。这应该给你同样的答案。
我要更新这个职位更明确。
这是我所见过的最好的公式,但是我有一个问题我想共享电子对的一边是假设是负但然后你是积极的,所以是finfding很难理解,因为幻灯片显示我们的讲师是减去不是补充道。我希望当你解释给我听。
这是一个非常伟大的解释!现在我有一个好概念如何找到公式。
而且我只是一个九年级的学生,所以我想说谢谢你。
你是最棒的。我得到了最高的马克我第一次测验,我知道通过我将在期中和期末得到最好的。我想要你们去youtube和遵循的步骤。非常感谢。
我记得学习,在氰离子、碳碳亲核,因为正式的负电荷,而不是氮,尽管氮电负性更强。所以我认为我不同的解释可能更准确,但我不确定如何妥善处理。我最好继续阅读。
氰离子,有两个孤对,一个碳,氮。孤对碳更亲核的,因为它是不那么严格了(氮原子的电负性比)。
在所有的例子表明,带负电荷(如BH4(-))没有一个孤对亲核性的复杂问题。
这真的帮了中性共价分子。然而,我难以应用这种技术分子0以外的总负责。(二氧化氯)——例如,Cl的形式电荷应该是1。然而,随着你的电荷方程应该是0。与传统的方程,确实是1。
我会很感激如果你尽早回答,我星期五有一个化学期中考试。我很困惑与正式的指控:)
谢谢你的学习指南。
这种方法是错误的
甲基,价eloctron是4,没有:债券是3,没有非保税电子是1
通过这个方程
F。C = 4 -(1 + 3) = 0,但这是作为+ 1
甲基的分析将是准确的。但是它失败甲基碳正离子。
这个例子指的是碳正离子。甲基,形式电荷确实是零。
这是如此有用的n最好的解释关于这个话题…
谢谢你的简单方法。
但是当我使用这个公式。因此
#价electrons_ #单身pair__ # 1/2。债券对
谢谢你的简单方法。
我有一个问题找到每个O原子的FC臭氧。你能帮我尽快?
中心原子的FC是+ 1,因为[6 - (2 + 3)]
FC在O原子配位键是:1因为[6 - (6 + 1)]。
FC在O原子双键:0,因为[6 - (4 + 2)]。
希望我解决你的问题!
今天非常感谢你我的考试,我不会通过没有这个信息
我真的失去了
甲基的例子
碳
#价电子= 4
#键= 3
非共享= 1 #
所以当我计算
价持续强劲表现的形式电荷=(#)+((1/2 #键)+(非共享的#))
形式电荷= 4 + [(1/2 * 3)+ 1]
= 1.5
请帮助我犯错误
应该是1/2(成键电子的#)+ #独享的。
这给了你4 - (3 - 1)
对甲基= 0。
应该为CH3(+),而不是甲基甲基。
我是铍,我生气了! ! ! ! ! !…………哈哈开玩笑的……。BTW, I found this article very useful.Thanks!!!!!!!!!!
这意味着什么,如果我们确定一个分子为零费用
吗?
它是中性的。
你说非保税电子在碳是2,但如何?
因为我认为这是只有1出4个价电子的碳,三是与氢只剩下1
如果电荷是1,必须有一个“额外的”电子碳——这就是为什么有一个孤对。如果只有一个电子,这将是中性的。
这个工作!我会带上你的类有机化学,如果你是一个教授。我现在把化学2。有机是下一个。
谢谢你这么多!
谢谢你非常多的简单的解释!难以置信的简单和节省很多时间! ! ! ! ! !
谢谢! ! !这是很棒的,我是一个初级化学这终于回答了我所有的问题关于形式电荷:)
很高兴这是有用的哈利!
如果正式指控现实毫无相似之处,他们的意义是什么?
我希望这个职位不被解释为“正式指控没有意义”。如果是我将不得不改变一些措辞。
我想传达的是形式电荷分配给原子不* *总是准确地描述原子的电子密度,和一个必须小心。
换句话说,形式电荷和电子密度是两个不同的东西,他们并不总是重叠的。
形式电荷是一个簿记的设备,我们数电子和充满电分配给一个或多个原子的分子或离子。
电子密度,另一方面,是一个测量电子的实际(或不)在一个物种,和这些指控可以部分或部分费用。
首先,电荷本身是非常真实的。HO - NH4 +离子,H3O +等等做一次充电。要记住的是,从电荷密度的角度来看,收费可能分布在多个原子。
例如,离子像H3O +。——* *熊的+ 1,
然而,如果一个电子在H3O +思考,一个意识到氧的电负性比氢,实际上是“把电子从每个氢。如果你看一个电子密度H3O +地图,你将看到正电荷分布三个氢,氧实际上有微小的负电荷。这里有一个不错的地图。
http://chemwiki.ucdavis.edu/Physical_Chemistry/Acids_and_Bases/Aqueous_Solutions/The_hydronium_Ion
当我们计算H3O +,形式电荷分配一个+ 1的氧气。这是保持书的原因。作为簿记设备,这将是一个皇家疼痛分数这样的指控。这就是为什么我们计算形式电荷和使用它。
有时它准确地描述电子密度。例如,在氢氧根离子,HO,负电荷是几乎所有的氧气。
如果你有一个公司的电负性,那么它就变得不那么令人困惑。
这有帮助吗?
有熊各种化合物结构的刻苦操练其中哪一个是更稳定的或更少的精力充沛有可能predicu形式电荷的计算?
嘿好解释。我有一个问题。为什么一般FC + / - 1 ?你能给我一个例子,当足球俱乐部不是+ / - 1 ?谢谢。
当然,试试氧气没有债券和一个完整的电子结构。
太棒了!我可以使用这个考试!谢谢!
不应该的形式电荷甲基1 ?我只是想知道,因为在你的例子+ 1和图1。
的问题. .它提到CH3没有孤. .这意味着价是4,但不会有任何电子(2)孤左. .因此这将是(4 -)- (0 + 3)= 1
是的。
CH3我认为俱乐部应该1 C碳价是4已经保税剩3氢原子一个电子是自由碳结合或与一个电子H因此,非保税电子孤对电子的数量是2。4 - (2 + 3)= 1。
在你的情况中如果我们0比c的化合价是不满意。
谢谢你的合作形式电荷
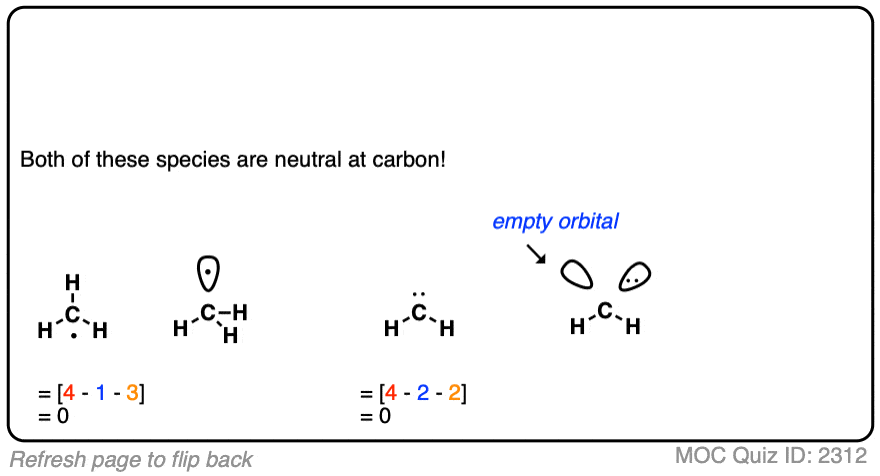
这个问题的答案在上面的帖子是“碳烯”——他们有两个取代基,一对电子,和一个空的p轨道,所以总共四个电子“本身”,这使得中性的。
谢谢你优秀的解释
很高兴你发现它有用的彼得!
很好的解释。我finally understood how to calculate the formal charge,was having some trouble with it.Thanks:)
很高兴你有帮助。
不错,简洁的解释
谢谢。
先生
表贴的你是非常优秀的。我的化学老师在印度前工程测试。如果u send me complete flow chart of chemistry i will great full for u