自由基反应
自由基反应的选择性:溴化与氯化
最后更新:2022年12月7日|
自由基溴化和氯化的选择性。一个详细的回答
在最后一篇博文激进分子我们看到这些数据,比较了丙烷与氯化溴化的丙烷。
对氯化反应的选择性二级碳氢键在主碳氢键的55倍/(45/3)= 3.6比1
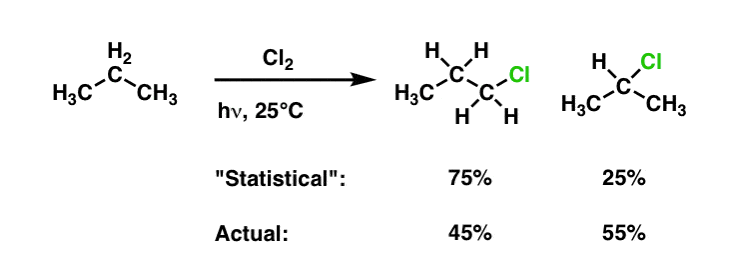
对溴化反应的选择性二级碳氢键在主碳氢键的因素97 /(3/3)= 97比1。
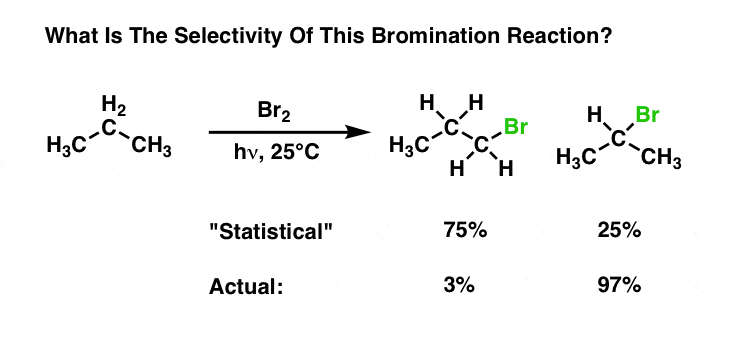
哇! ! !比氯化溴化更有选择性得可笑,还是什么? ?(同样,如果你想知道这是如何计算的,回到过去。)
今天我们要试着回答,“为什么溴氯的选择性比”吗?你可能会认为从4:1 97:1将包括一个巨大的能量上的差异。但是我们将会看到,这是比你预期的更加微妙。几个千卡每摩尔可以产生巨大的差异!
表的内容
- 碳氢键的Selectivity-Generating一步是破损的卤素自由基(传播步骤# 1)
- 背景:活化能和阿仑尼乌斯方程(是的,这是相关的)
- 热量增加了平均速度(能量)的分子
- 反应混合物加热,更大比例的分子将有足够的活化能(E一个反应)
- 选择性成正比的差异关键步骤的活化能
- 小的差异激活能量(~ 3千卡每摩尔)可以是选择性(97:1)之间存在较大的差异
- 为什么是激活的差异比氯化溴化能量更大吗?
- 氯化的过渡态类似反应物(一个“早期”过渡态)接近的能量。所以选择性很低。
- 溴化的过渡态类似产品(“末”过渡状态)相距很远的能量。所以选择性很高。
- 摘要:对自由基选择性氯化vs溴化
- 笔记
- (高级)引用和进一步阅读
1。碳氢键的Selectivity-Generating一步是破损的卤素自由基(传播步骤# 1)
,这篇文章希望回答的问题“为什么溴更多的“选择性”比氯仲碳吗?”。
这是一种长期的答案。这篇文章通过数据,使科学的论点。在下一篇文章我将提出一个简单的类比,简化了这个想法对很多学生。
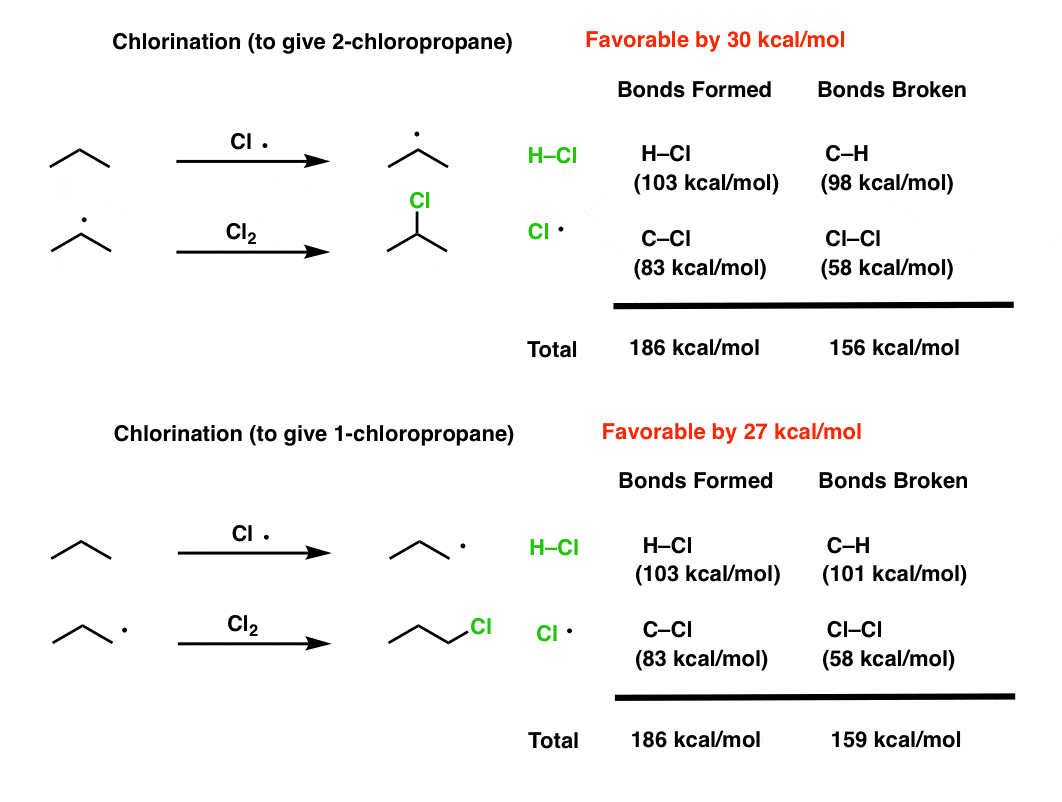
要注意的第一件事是形成不同的氯丙烷在发生链传播步骤(即启动后)。这里对我们来说我们只是将分析两个传播步骤和假定起始已经发生。换句话说,这一步:
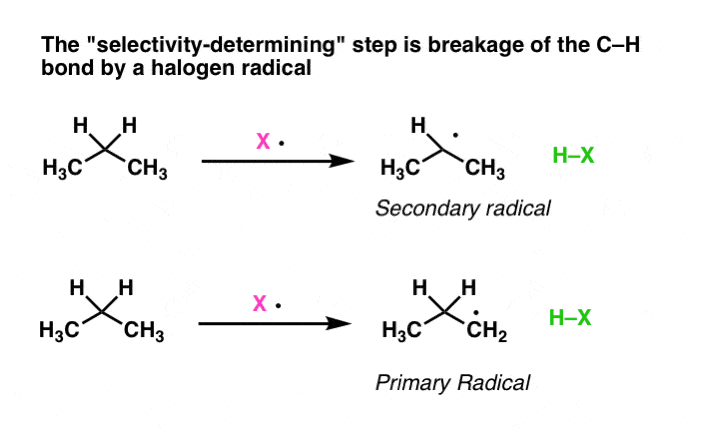
2。背景:活化能和阿仑尼乌斯方程(是的,这是相关的)
直接寻址选择的主题之前,让我们先开始谈论活化能。您可能还记得,为了使反应发生时,反应物必须接触到彼此有足够的能量来克服它们之间的斥力(电子云)。他们还必须碰撞以这样一种方式,允许电子转移(又名“轨道重叠”)
换句话说,汇率等于:
(分子具有足够能量的浓度)*(它们碰撞概率在“正确的方式”)
这是处理由阿仑尼乌斯方程:

在这里,“他们以正确的方式碰撞概率”由pre-exponential处理因素一个为每一个反应,是独一无二的。指数因子eea / RT是所谓的“分布函数”,这是我们如何计算%的分子在溶液中有足够的能量反应(迄今为止被称为“活化能”。)
3所示。热量增加了平均速度(能量)的分子
注意这样的事实,这是依赖于温度的。这是为什么呢?为分子加热的集合,这些分子的平均速度会增加。这是被称为一个相关函数玻耳兹曼分布这里,在三种不同温度下(= 1 = 2,和= 5)。y轴显示分子的#(“分布”)和x轴显示能源(谢谢维基百科)
热量增加分子的平均速度
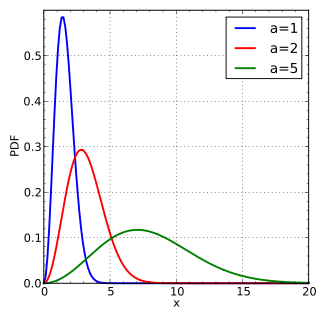
这显示了“分布”(又名“数量”)在特定能量的分子。中间的驼峰是“最可能的”能源,并像一个注意钟形曲线两端的尾巴。在最右边的规模是最精力充沛的分子。注意:当温度增加平均分子有更大的能量,同时右边的“尾巴”延伸。
4所示。反应混合物加热,更大比例的分子将有足够的活化能(E一个反应)
现在想象一下,我们有一个反应活化能E一个。在很冷的温度下,很少分子有足够的能量反应。但随着反应混合物加热,这些分子的比例增加。因此,反应的速率增加热量。这里有一个例子,它是如何工作的。注意,在这种情况下,反应不发生在300 k,但开始出现在一个合理的利率在330 k !
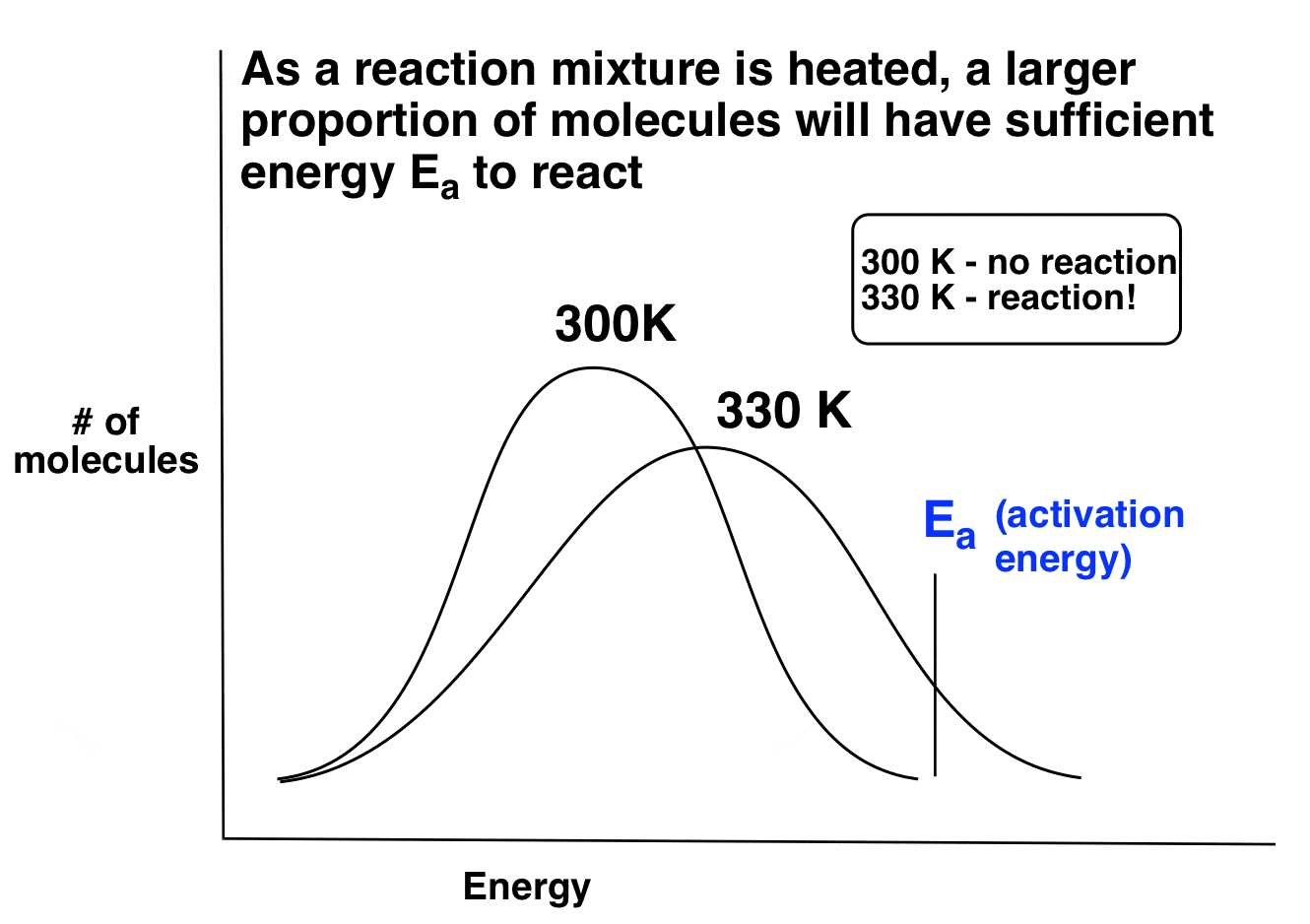
好的,这涵盖了改变反应温度。但是这和卤化的选择性?
5。选择性溴化和氯化正比于差异的关键步骤的活化能
在这里,我们保持反应温度恒定,但每个反应的活化能略有不同。
我们有四个反应总思考(两个不同的卤素和两个不同的碳氢键)。每个反应的活化能通过实验测量(Ref 2(在这里,我们讨论的是碳氢键的活化打破(即。传播不启动。这是他们的长相。
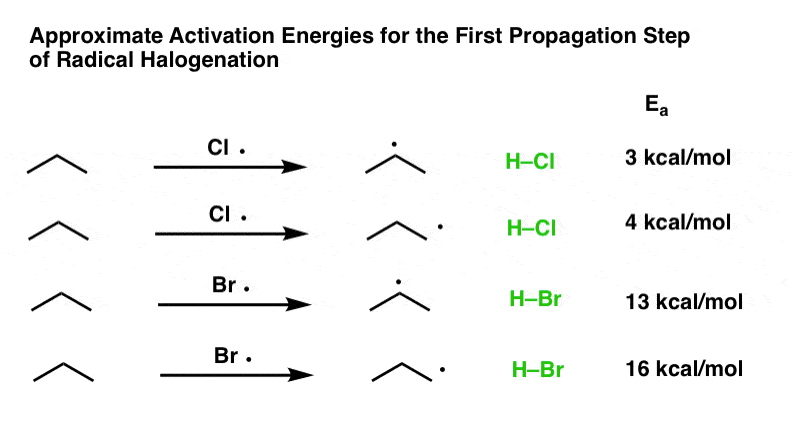
这实际上是所有我们需要的信息能够选择性的粗略估计。
在300 K的反应,我们可以使用气体常数计算RT(1.987大卡/ K摩尔),插入每个反应的活化能。除以两个方程,pre-exponential因素将大致抵消,我们可以获得选择性估计。
这里的底线是,由于阿仑尼乌斯方程的性质,更大的激活能量之间的区别,更大的选择性。可以戏剧性的效果,即使从1千卡每摩尔的区别(氯化)3千卡每摩尔(溴化主要与次要的)
6。小的差异激活能量(~ 3千卡每摩尔)可以是选择性(97:1)之间存在较大的差异
使用阿仑尼乌斯方程的数学,一个粗略的计算基于活化能的不同的选择性。
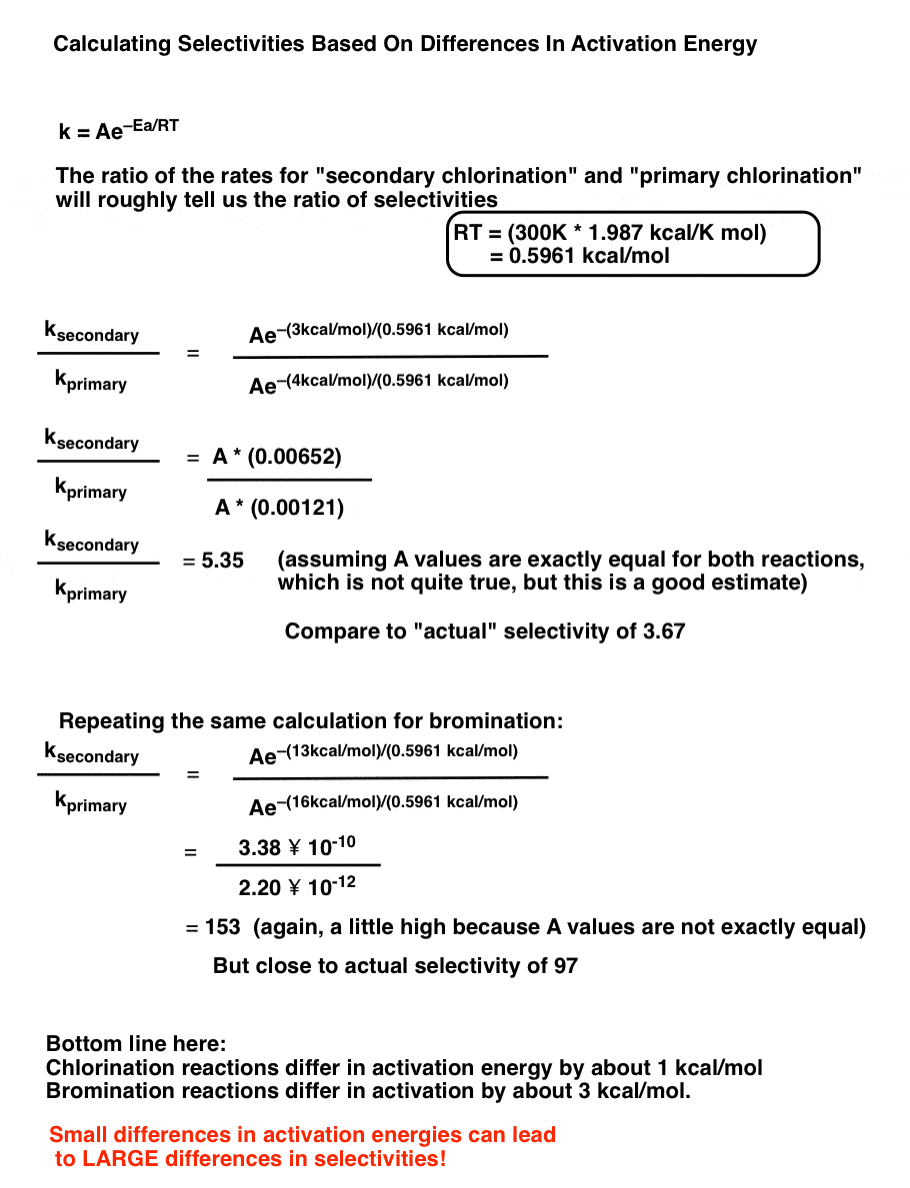
所有这一切都是美好的,它是基于实验数据的激活能量。但它只是打开了另一个问题。
为什么为溴化激活能量更大的区别(3千卡每摩尔)比氯化(1千卡每摩尔)。好问题!
7所示。为什么是激活的差异比氯化溴化能量更大吗?
理解这一点开始了解这两种不同的反应的能源配置文件(氯化、溴化)。
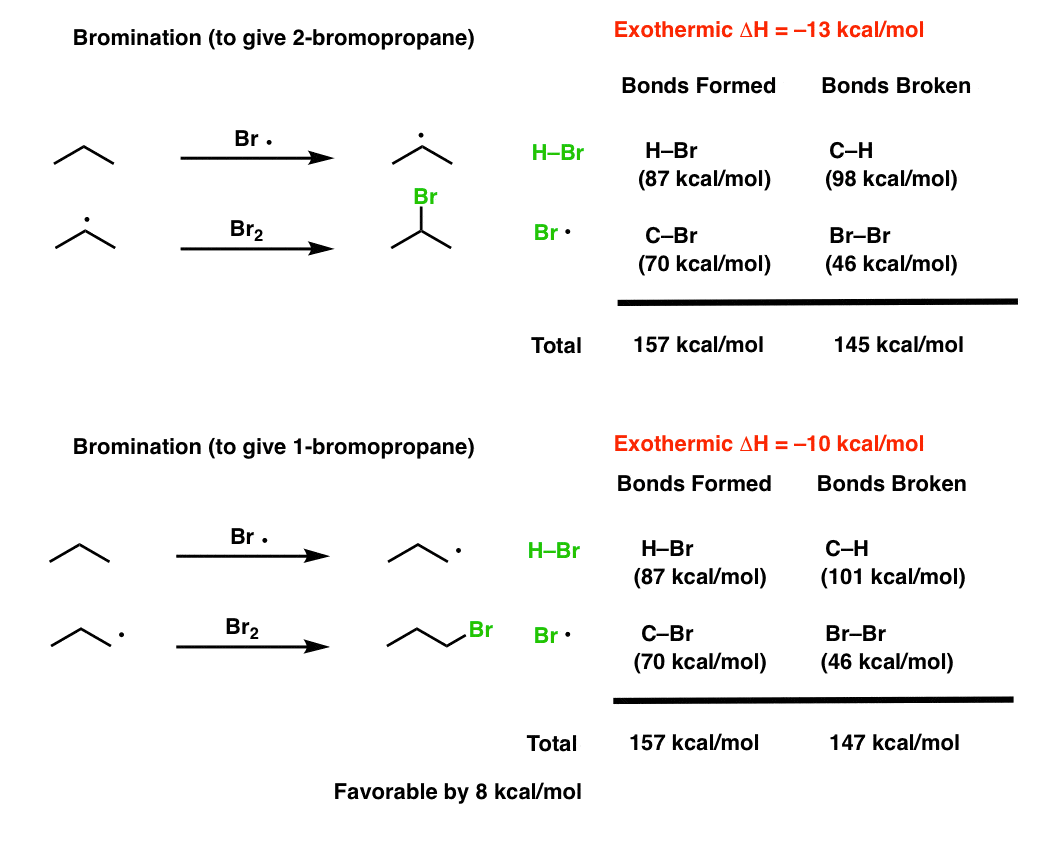
我们会做数学,但关键的区别是,在氯化,传播的关键一步放热在溴化,传播的关键一步吸热的。这是因为氯化形成强大的债券(103千卡每摩尔)氯和溴化形式更弱H-Br债券(87千卡每摩尔)。
这两个反应坐标大致是这样的:
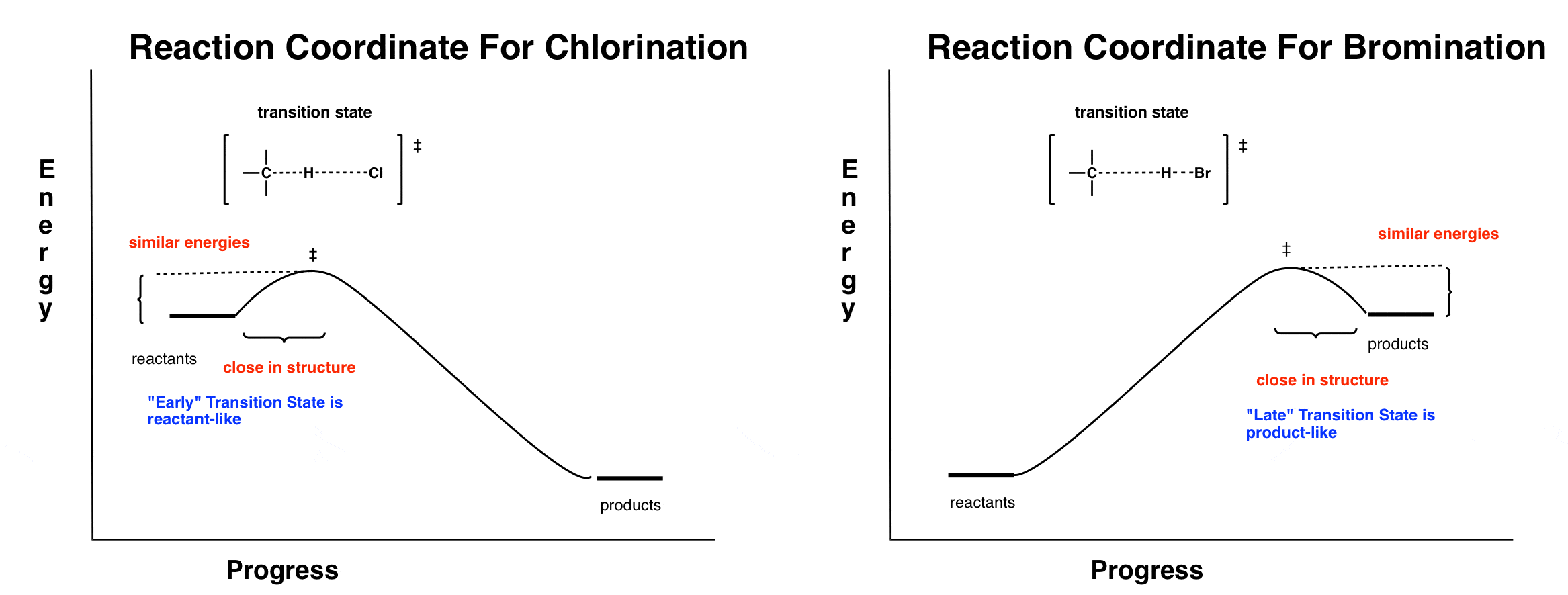
仔细观察每个反应过渡态的。
在氯化反应是放热的,过渡态类似反应物。根据哈蒙德的假设,我们可以说这个过渡状态是“早”。
在溴化反应是吸热的,过渡态类似产品。据哈蒙德的假设我们说这个过渡状态是“末”。
8。氯化的过渡态类似反应物(一个“早期”过渡态)接近的能量。所以选择性很低。
这意味着,对氯化,激活能量两个激进的通路之间的差异(即“二级”和“主要”)将最相似反应物(这是相同的能量)。这将是一个非常小两者之间不同的激活能量。
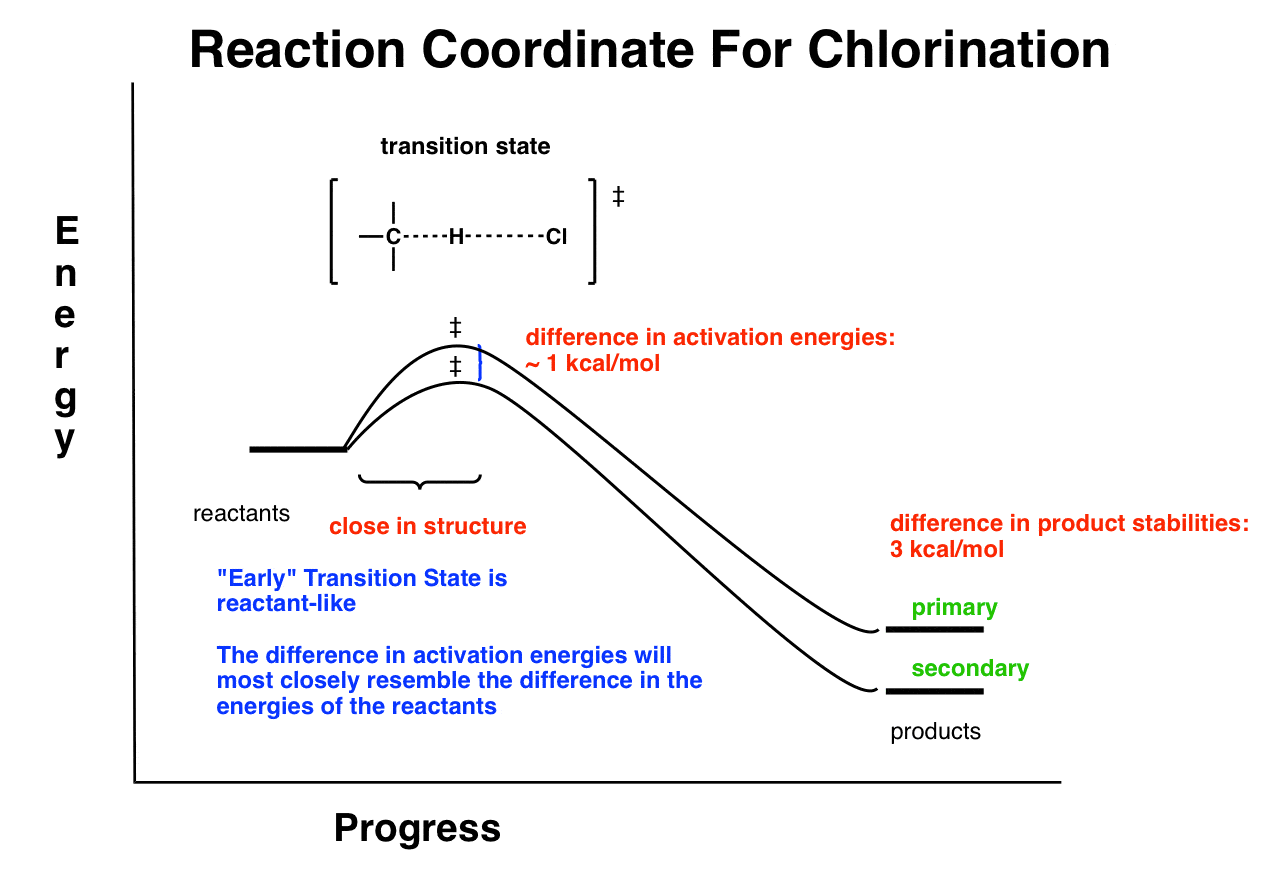
激活能量很小的差异(1千卡每摩尔),因为早期的过渡态。注意,即使有相当大的差异之间在能源产品(3千卡每摩尔)它不影响激活能量。
9。溴化的过渡态类似产品(“末”过渡状态)相距很远的能量。所以选择性很高。
我们可以做同样的分析为溴化。在这里,这是一个“迟到”过渡态,所以中小学之间的激活能量的差异将两者之间相似能量的差异。所以我们希望活化能的不同更像是产品的能量之间的区别。是这样!
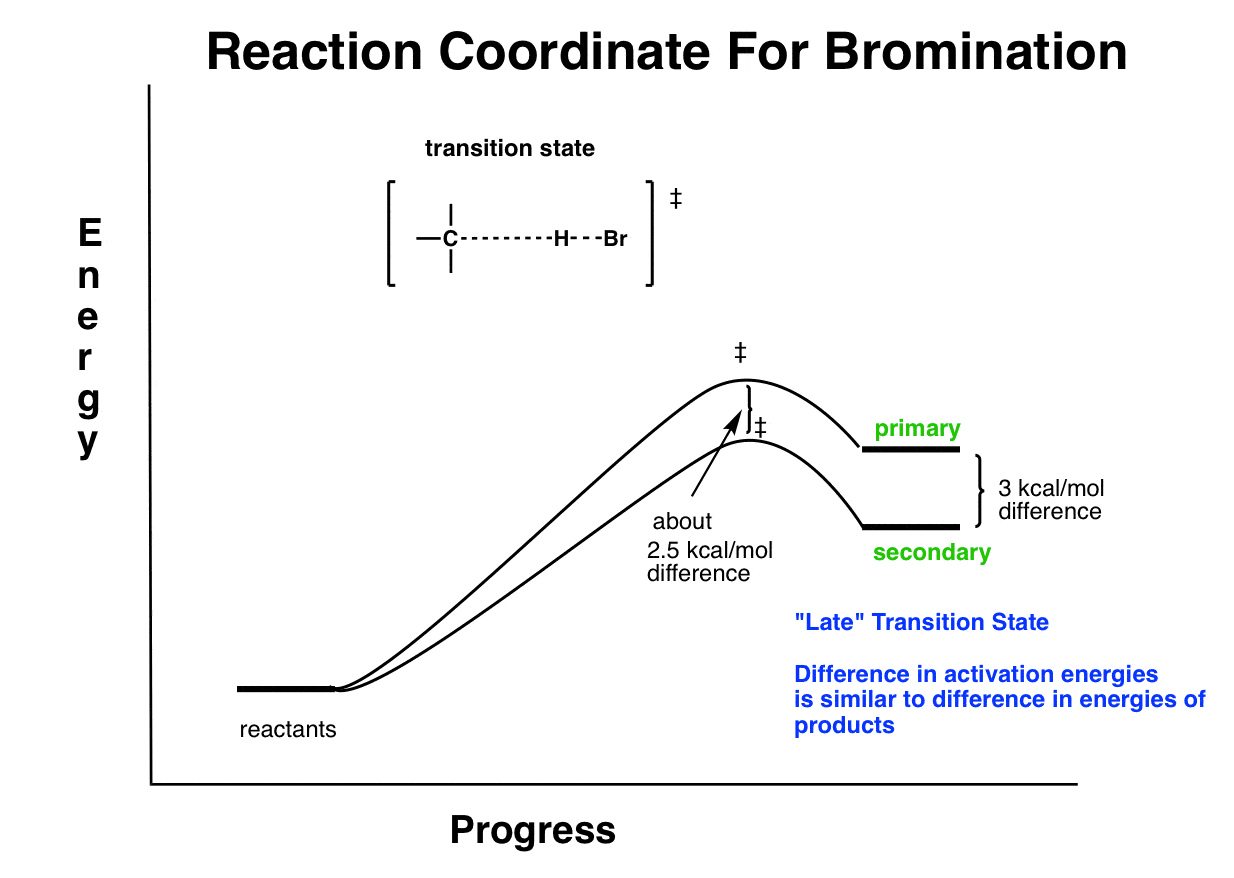
所以今天的帖子里的底线是几件事:
10。摘要:对自由基选择性氯化vs溴化
1)从一个激活能量差1千卡每摩尔大约3千卡每摩尔可能意味着不同反应选择性的3.5:1,反应的选择性97:1。哇! !
2)我们将反应与一个“早期”过渡状态和“末”过渡状态,看到“迟到”的反应过渡态是更有选择性。这是可以预料到的,当我们从相同的反应物和产品的能量有显著差异。
在下一篇文章我将使用一个简单的类比来指出的方式帮助学生理解这一点更直观的层面。
在下一篇文章:蒂凡尼的卤化
笔记
溴化:
(高级)引用和进一步阅读
- 自由基的相互作用与饱和脂肪族化合物
特德j . m .
问:启化学。Soc。1960年,14,336 - 356
DOI:10.1039 / QR9601400336
这篇评论,虽然过时,包含大量有用的信息,包括自由基脂族的活化能的推导溴化(13.3千卡每摩尔),和国家统计局的建议可以通过提供一个稳定的低浓度的溴化烷烃Br2。 - 竞争在气相氯化反应:氢和C1-C5饱和碳氢化合物
约翰·h·诺克斯和罗伯特·l·纳尔逊
法拉第Soc。1959年,55,937 - 946
DOI:10.1039 / TF9595500937
本文涉及自由基C1-C5氯化烷烃,和详细的动力学分析了氯化反应使用阿仑尼乌斯方程。实验确定激活能量都相当低,在0.02 - -4.1千卡每摩尔。 - 替换饱和碳氢键利用分子溴或三氯溴甲烷
格伦·a . Russell和查尔斯DeBoer
美国化学学会杂志》上1963年,85年(20),3136 - 3139
DOI:1021 / ja00903a019
本文研究苄基的通过自由基溴化机制。正如所料,反应速率增加而增加取代苄基的位置,但本文提供了实验证据。 - 指令在脂肪族替换。第十九。与N-Bromosuccinimide Photobromination
格伦a·拉塞尔和凯萨琳·m·德斯蒙德
美国化学学会杂志》上1963年,85年(20),3139 - 3141
DOI:1021 / ja00903a020
摘要立即遵循Ref。3的同样的问题江淮,并提供了证据表明,国家统计局也可以通过自由基溴化机制(即沃尔齐格勒反应)。 - 溶剂效应在自由基的反应和原子。八世。芳烷基的Photochlorination碳氢化合物
格伦·a·罗素Akihiko。伊藤,戴尔·g·亨得利
美国化学学会杂志》上1963年,85年(19),2976 - 2983
DOI:1021 / ja00902a022
重要的溶剂效应是观察的自由基photochlorination苄基的化合物。络合反应的溶剂可以显著减弱氯自由基,使其更多的选择性反应。 - 自由基的反应。42。氢对硝基苯激进的抽象
a·普赖尔k·史密斯,j . t . Echols和d·l·富勒
《有机化学》杂志上1972年,37(11),1753 - 1758
DOI:10.1021 / jo00976a019
除了溴和氯,其他自由基可以通过自由基反应生成和使用。有机自由基也可以使用,在这种情况下,苯和p -nitrophenyl自由基的分解可以生成各自的偶氮前体。的p -nitrophenyl激进的观察更比苯自由基在自由基取代反应选择性。 - 惯性和化学反应的驱动力
m·g·埃文斯和m·波拉尼
反式。法拉第Soc。1938年,34,11-24
DOI:10.1039 / TF9383400011
这是一个非常重要的论文,介绍什么是现在被称为Bell-Evans-Polanyi原则。这个观察到的差异两个反应之间的活化能同一家族的焓差成正比的反应,从而使比较相似的反应。有趣的是,当迈克尔·波拉尼(摘要),当选为英国皇家学会,他没有获得诺贝尔奖,但他的儿子,j·c·波拉尼在1986年获得诺贝尔化学奖为他在化学物理工作。 - 反应速率的相关性
乔治·s·哈蒙德
美国化学学会杂志》上1955年,77年(2),334 - 338
DOI:1021 / ja01607a027
哈蒙德的假设通常教化学本科生,是一种常见的心理工具也被有经验的科学家。放能反应系统将早期的过渡状态类似于起始材料,而吸能反应会有后期的过渡状态类似的产品。
回复斯蒂芬,
我想知道同样的事情…我猜这就是詹姆斯指的是之前指出的,“键的强度和激进的稳定”,他写道:
”这篇文章的总趋势是有效的,因为我们讨论债券H,但注意当比较氢…以外的任何其他类型的债券。使用不牵强附会的债券的债券的优点(12)的氢是一种合理的方法识别趋势激进的稳定性,在这篇文章中讨论。然而,12的本身不可靠的绝对激进的情况下稳定性债券可能削弱了应变,对孤电子之间的排斥力,或其他因素。例如过氧化氢的12是51千卡每摩尔,这并不意味着HO•激进是稳定的,而是o - o键不稳定之间的斥力,孤。”
现在当我看着12表在韦德的有机化学我找到的唯一病例三级12明显低于主要12碳氢键或碳碳键断裂。几乎没有12区别叔和初级卤化物(氟、C-Cl C-Br,我)或切断债券。
因为打破cx卤键仍然产生C *激进(和卤化物现在),C *激进本身必须更稳定的如果是三级,而不是主要的。对我来说,这表明12唯一能相等(三级和初级cx卤化物)如果第三cx卤化物债券比小学更稳定cx卤键。但是为什么会这样呢?
我猜(只是猜测):甲基-团体电子捐赠和卤电子撤回,所以也许稳定cx卤键的叔碳原子(卤化物像电子!),使卤化更讨厌离开作为激进(只需要单个电子的键)…但我不是chem-major…所以这是好如果詹姆斯重…
所以你说詹姆斯什么? ! ?
谢谢!
monohalogenation碘比溴反应?
碘是没有活性的自由基卤化烷烃。设定h键的强度太弱。
勒罗伊韦德哈蒙德假设——评论文章中说
“过渡态总是最高能量的能量图。
其结构类似于反应物或产品,哪个的
更高的能源。在吸热反应,产品有更高的能源,
过渡态是一类的产品。在一个放热反应,反应物的能量,和过渡态是reactant-like。因此,哈蒙德假设帮助我们理解为什么放热过程倾向于选择性比类似的吸热过程。”
明显的最后一行是如何理解ofChlorination vs选择性溴化的哈蒙德假设?
伟大的报价,与这篇文章有关。这是一个问题吗?
嘿,伙计们!这里介绍你有很棒的材料。你介意提供文献数据的来源吗?
3月,高等有机化学,5日患儿是我的标准参考。
你好,
只是指出R = 1.987大卡/ K摩尔(不是公斤)写在“计算基于选择性差异活化能”形象和上面的段落。
同时,你能解释一下“[…]在氯化,传播的关键一步是放热和溴化,传播的关键一步是吸热的。”
是什么使传播的第一步的“关键”一步?为什么不看看你的净能量差在底部的图片吗?
传播的第一步是关键的一步,因为它会导致形成一个激进的烷烃——这是缓慢的一步(碳氢键的断裂)。第二步是快速的,因为相当弱键被打破(Cl-Cl)。
谢谢你的修正卡尔vs千卡。固定!
很好地解释了主题!只有一件事我不明白(尽管这不是重要的特定选择的步骤):
为什么卤素和碳之间的键的形成积极中小学碳相同吗?(83千卡每摩尔的Cl, 70千卡每摩尔的Br ?)我认为还有一个微小的区别吗?不幸的是我找不到任何热力学数据。
我将感激你的简短的回答。
呵呵我的我的我的! ! ! !向你致敬……我说不出话来……它也详细和清晰的理解。
哇,非常详细的解释。我真的很感激你的网站。
伟大的工作!
认真我爱阅读的概念解释这么好!
很好的方式解释物理有机化学的概念
从物理有机化学的角度来看这是可怕的。怎么你不是一些学校教授。你真的知道你的化学。我希望你是我的学校的教授。这是一个伟大的帐面价值的!