羧酸衍生物
Addition-Elimination机制与中性的亲核试剂(包括酸催化)
最后更新:2023年5月22日|
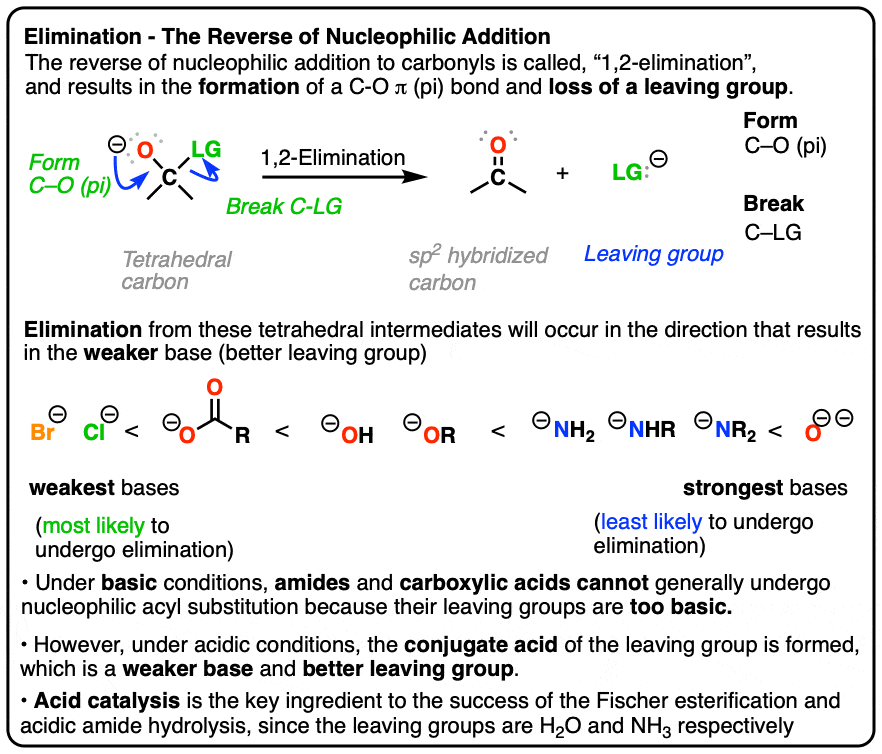
- 的反向亲核加成的C = O债券(给一个四面体中间)消除的离去基团从四面体中间重新C = O键。
- 这叫做,“1、2-elimination”或有时只是“消除”,是一个关键机制羰基官能团。
- 令人困惑的是,取消的烷基卤化物也称为1,2-eliminations。看到E2机制或E1cB或者是E1反应想了解更多关于这些。)
- 取消一般青睐当驱逐离去基团结果形成的较弱的基础
- 酸催化非常有助于促进亲核酰取代羧酸酰胺,自消除结果更好的离开组H2O和NH3(而不是啊2 -和NH (-)2在基本条件下)
表的内容
1。羰基的第二重要的机制
消除(2-elimination)是一个非常重要的反应机理羰基(C = O)集团存在于官能团如醛、酮、羧酸和羧酸衍生品。
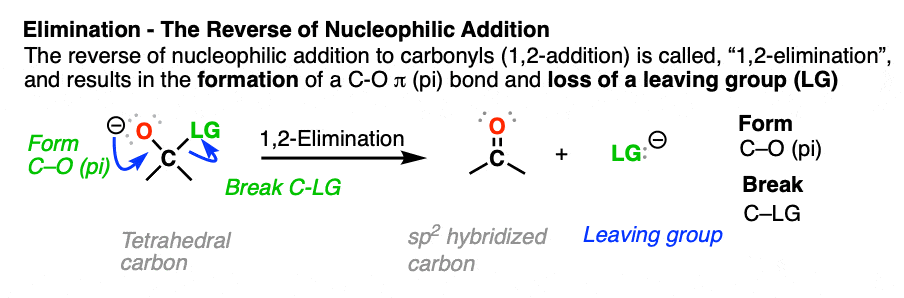
这是第二个最重要的反应金属羰基合物后,除了。事实上,它正好相反这亲核加成反应。(看到帖子:亲核加成)
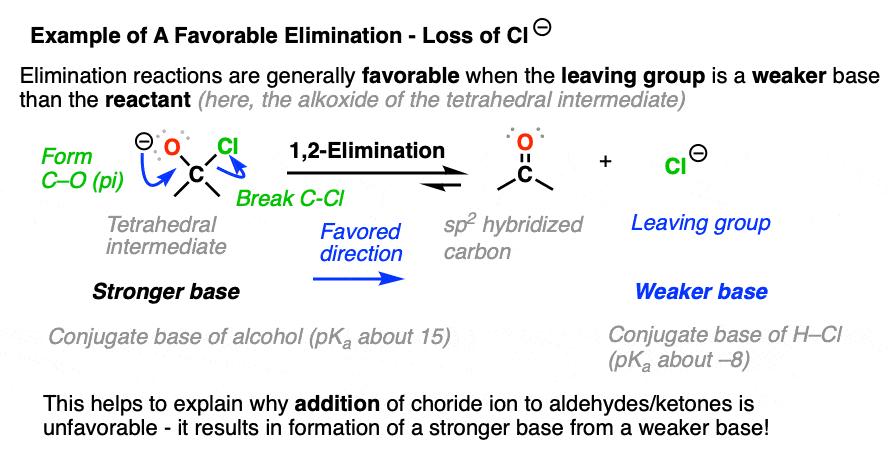
消除反应往往是有利的离去基团是一个较弱的基础比亲核试剂。(见:是什么让一个好的离去基团)
这就是为什么卤化物离子不成功执行醛和酮亲核加成。的反应是艰苦的碱度。由于Cl(-)是一个较弱的基础比O (-),消除更有利除了。(看到帖子:如何使用pKa表吗)
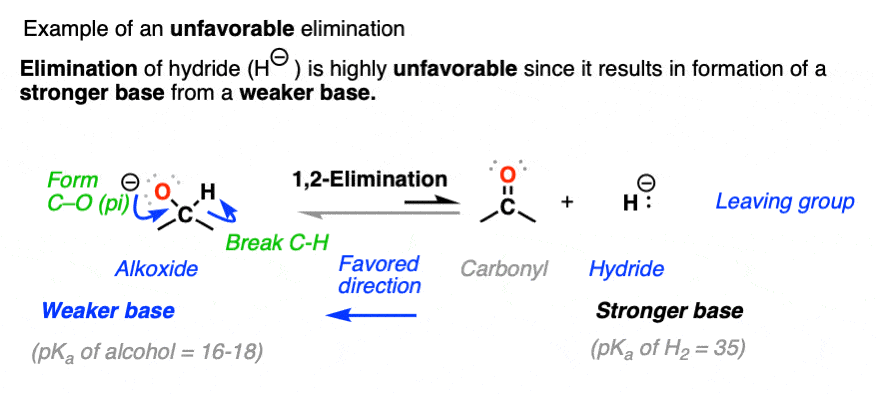
消除是不利的当它在一个结果强大的基础形成从较弱的基础。这就是为什么减少醛和酮的氢化物减少代理就像NaBH4是不可逆转的看到的:硼氢化钠)。
氢化物醛和酮的还原反应的正向反应的结果强大的基础(氢化,共轭碱H2,pK一个大约35)被转换为较弱的基础(醇盐,共轭碱的酒精,pK一个16日至18日)。
相反的反应(消除)大约是20 pK一个单位多不好的从酸碱的角度来看(看到帖子:如何使用pKa表吗)
一般来说,一个好的经验法则是,如果亲核试剂/基地和离去基团由超过8 pK一个单位,反应可以被认为是不可逆转的。(看到的:一个方便的经验法则对酸碱反应)
(然而,有一些反应的例子,H(-)可以作为离去基团在协调过程中,明白了注1)
酸碱平庸的原则(“更强的酸+强基地给弱酸性较弱的碱)总是一次又一次的出现!
2。消除在羧酸衍生物
除了醛和酮,加法和消除也发生在的反应羧酸衍生品如酸卤化物、酸酐,酯类和酰胺。
当发生亲核加成羧酸导数,它形成一个四面体中间两个潜在的离开组织。(但不是O -注2]
- 第一个潜在的离去基团是原始的亲核试剂;消除四面体中间的这只会给我们回到我们的原始材料(毕竟,离开团体只是亲核试剂作用相反)。
- 另一个潜在的离去基团是X的羧酸衍生品(如酸性氯化物(-)Cl, (-) OCOR酐,(-)或酯类(-)NR2(-NHR) - (NH2)酰胺)
当亲核试剂是一个强大的基础比离去基团X (-)羧酸导数,然后我们会换掉的X集团羧酸导数。这是亲核酰取代。(看到帖子:亲核酰置换用阴离子亲核试剂)
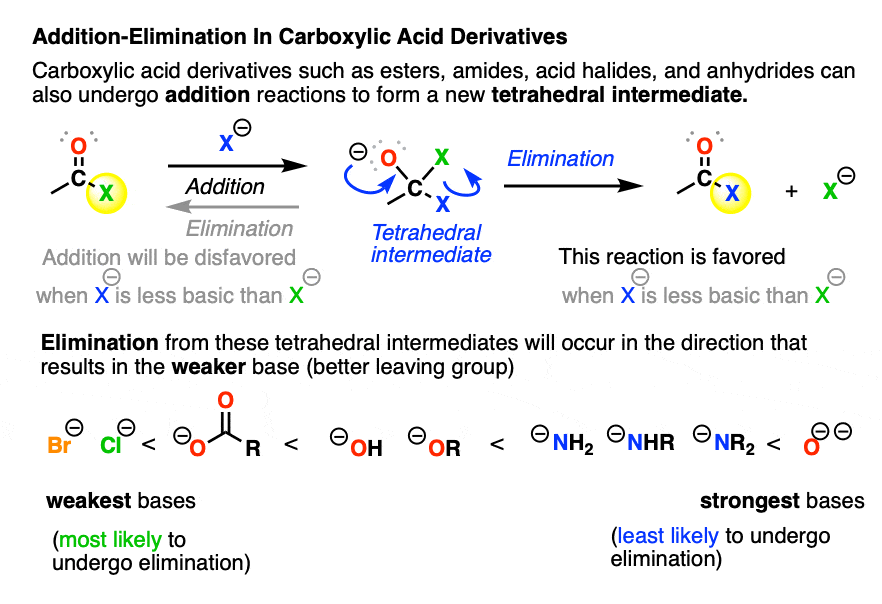
与带负电的亲核试剂亲核酰取代很容易执行酸卤化物和酸酐,更加难以执行酯类,本质上不可能的实现与酰胺,因为这需要非常基本的损失离去基团NH2(-),共轭碱一个胺(pK一个35-38)
 点击翻转
点击翻转
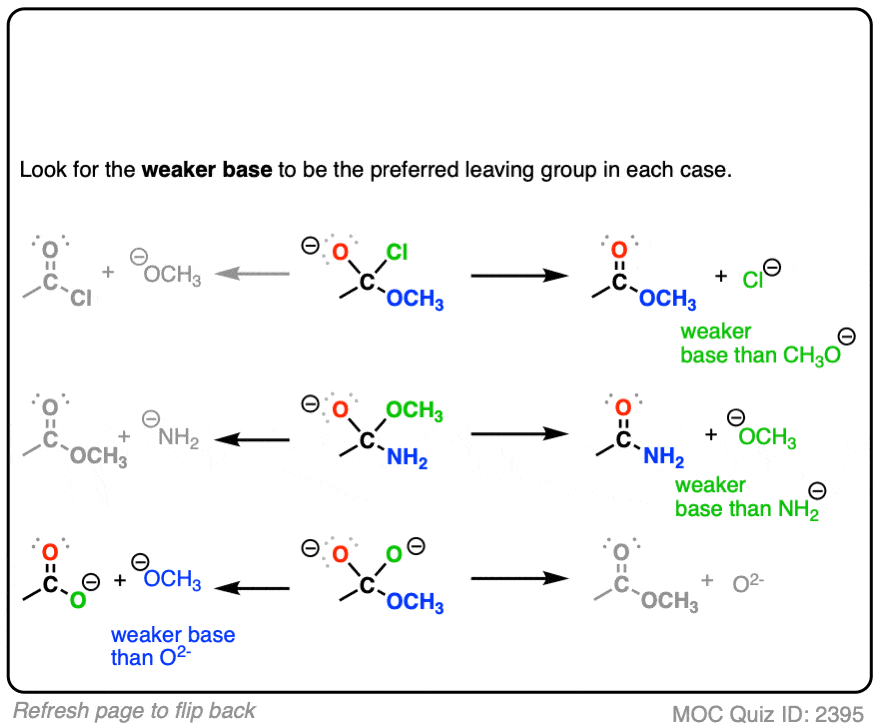
羧酸在基本条件下一般不接受addition-elimination因为他们将deprotonated强碱给羧化物,由此产生离去基团必须的强碱O (2 -)(在这篇文章中更详细地讨论:酯交换)
3所示。中性的亲核试剂呢?
这是不绝对需要使用基本然而,亲核试剂的亲核芳香取代。
中性亲核试剂完全有能力执行一些亲核酰替换。
一个著名案例是酸卤化物和酐,非常敏感的存在水。
这两种官能团可以水解与水给羧酸。
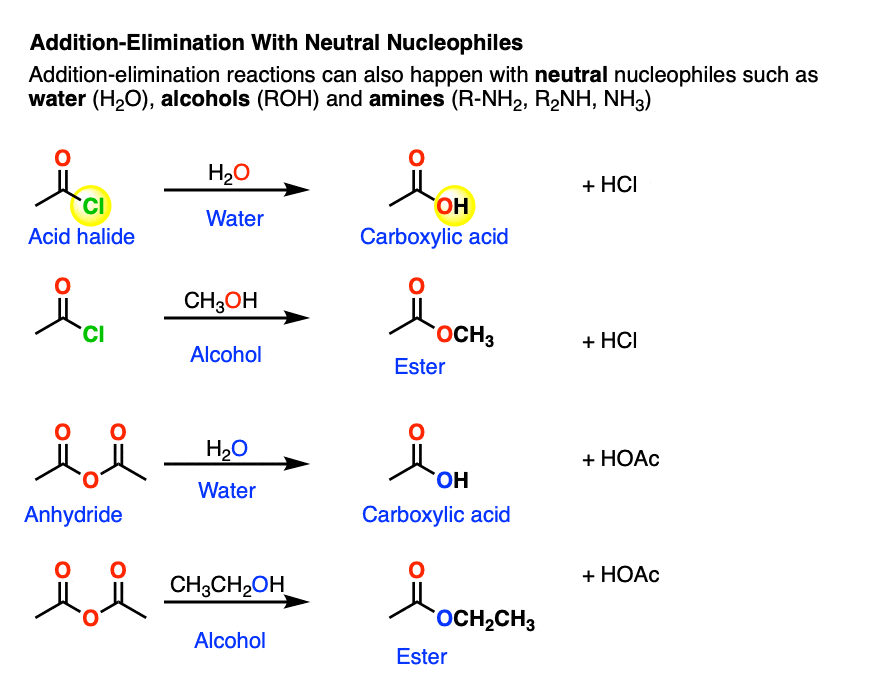
加法和质子转移后,关键的一步消除的卤离子,导致形成的羧酸。这仍然遵循的原则酸碱平庸,因为Cl(-)比H较弱的基地2O (共轭碱H3O +, pK一个0)。同样,水是羧酸至少可比的基础力量。
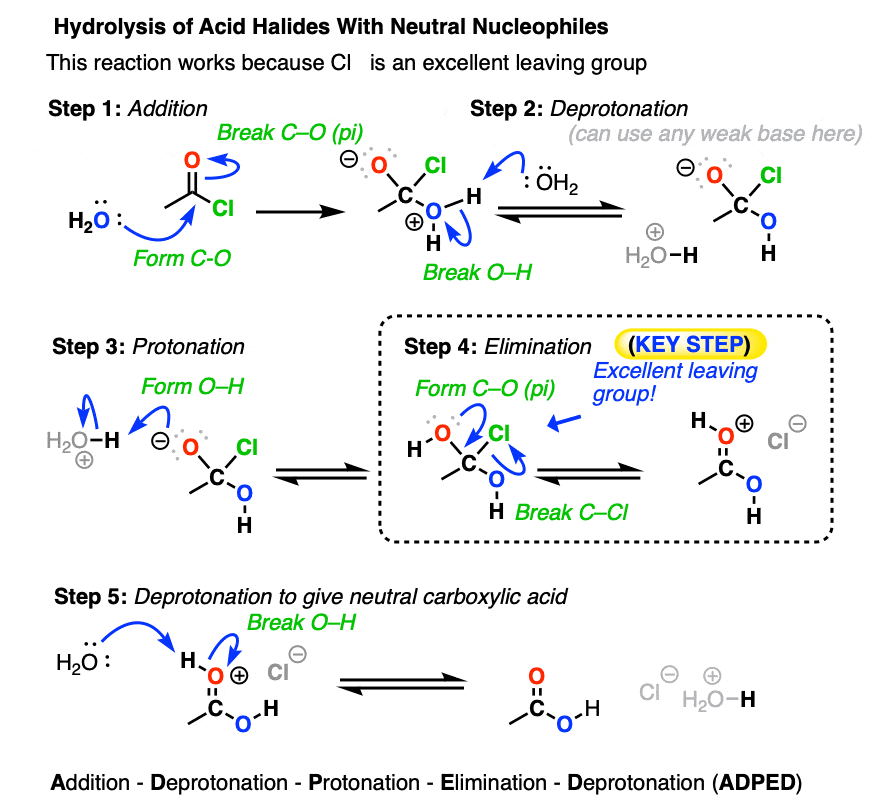
这些反应也工作得很好胺。酸卤化物和之间的反应胺是一些最好的方法使酰胺;这个反应有时被称为Schotten-Baumann反应(见合成酰胺酸卤化物)。
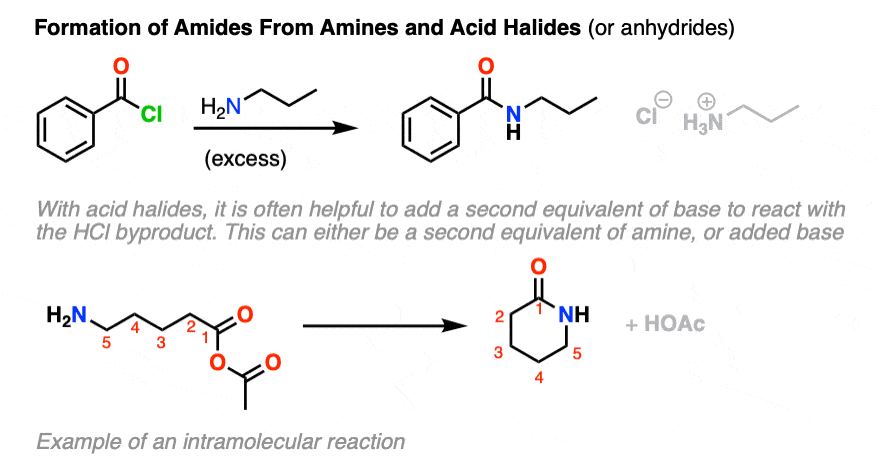
一般来说,至少有两个版的胺使用,因为一个相当于生成盐酸。(如果只有一个相当于胺被使用,反应不会继续完成自胺亲核试剂会使质子化给(non-nucleophilic) RNH3(+)。)
看到一个从卤化物酸酰胺的形成机制,徘徊在这里或点击这个链接。
4所示。酸性条件,消除共轭酸(更好的离去基团)
中性的亲核试剂与羧酸有其局限性,然而。水可以取代弱基本卤化物和羧酸盐,但不能取代更强大的基地RO(-)或R2N (-)。(胺,如果加热可能会取代酯类,但它需要大量的热量——看到的酰胺的合成)。
除了酸卤化物和酐,大多数其他羧酸惰性在中性条件下。
然而,当一个酸催化剂补充说,这是一个完全不同的故事。它打开了一套完全不同的反应,否则不会发生。
我们之前见过的一个例子的合成缩醛树脂(看到帖子:缩醛和半缩醛),消除一个等效的卢武铉半缩醛要求酸催化剂。(在缺乏酸,不排除发生!)。
这也是如此羧酸衍生品。
回想一下,酰胺的原因和羧酸不起化学反应的基本和中性条件下是因为北半球2(-)和O(-)是如此强大的基地,因此可怜的离开团体。
只是想象一下,我们可以运行这些反应酸性条件。
他们将不再是NH离开团体2(- - - - - -)和O (2 -);他们可能是质子化了的堂兄弟NH3和H2啊,这是较弱的基地因此多更好的离开团体。
突然,羧酸和置换反应酯类成为一个合理的反应!
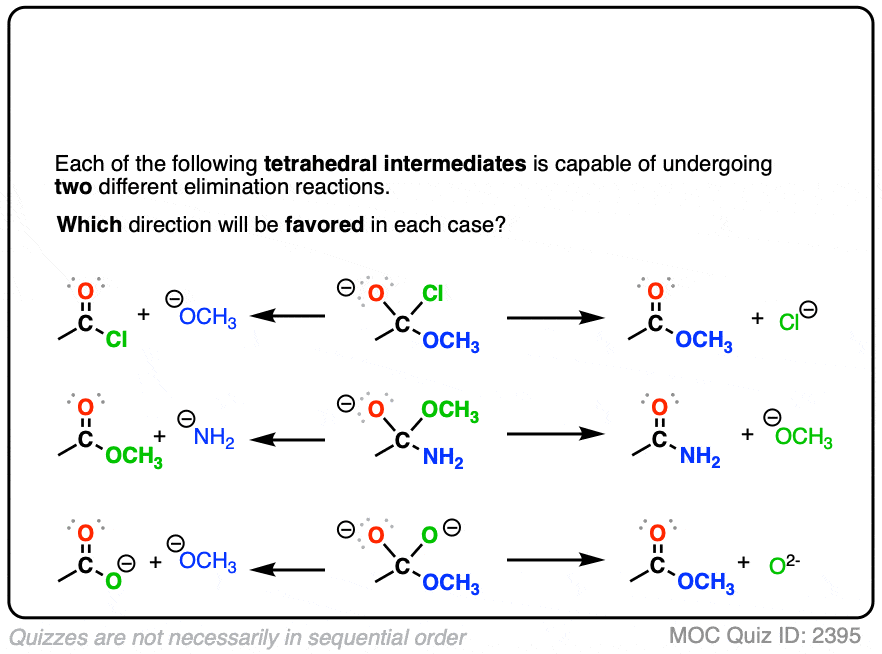
这两个反应比较离开组织
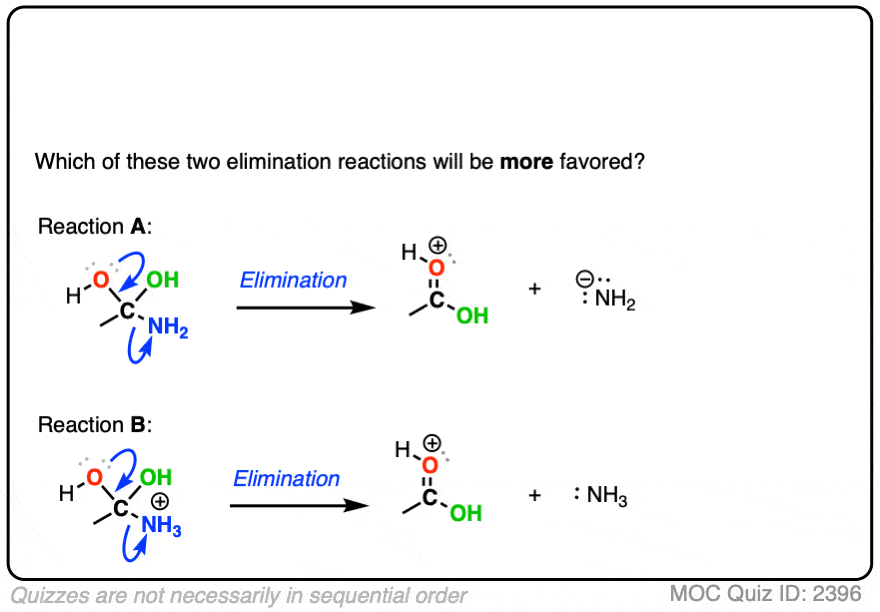 点击翻转
点击翻转
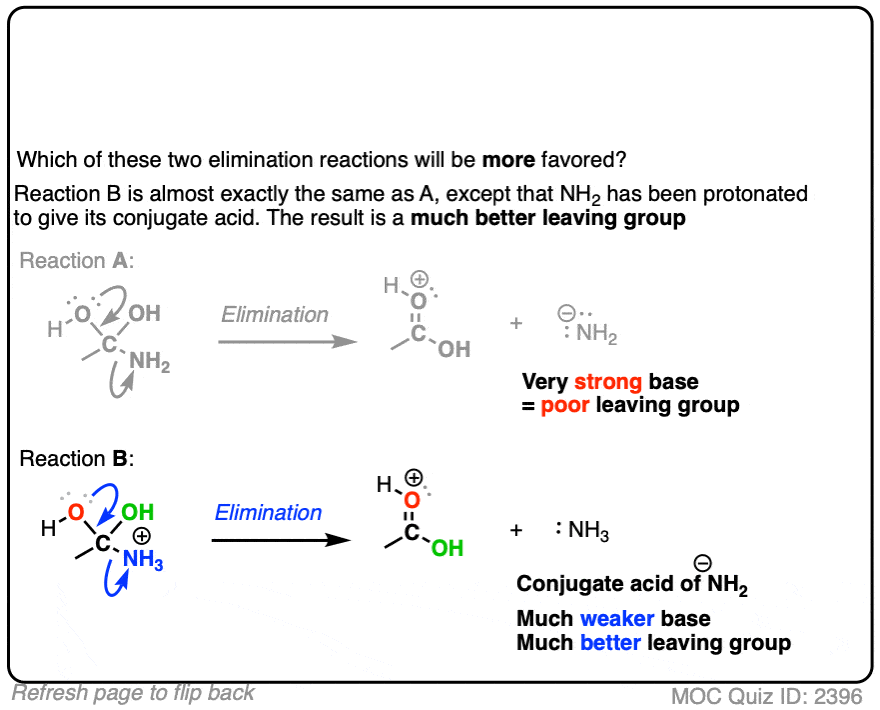
这两个反应或离开组织
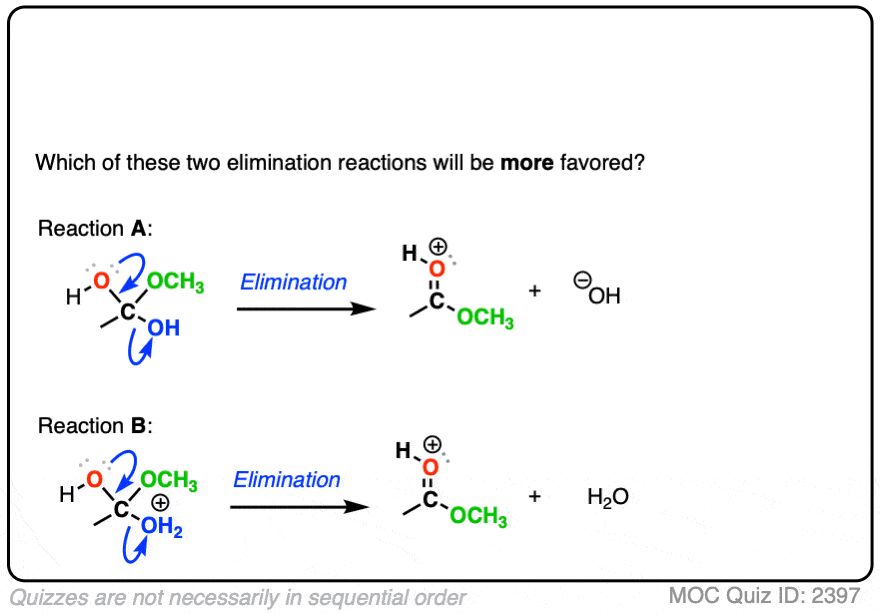 点击翻转
点击翻转
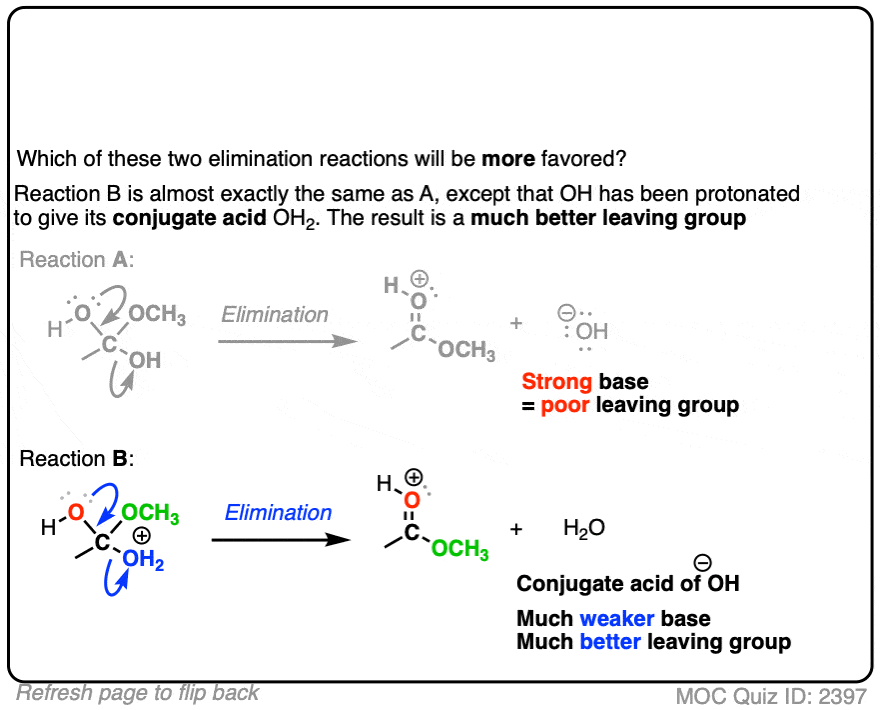
在每种情况下,质子化了的物种是更好的离去基团,因为它是较弱的基础。
T他共轭酸是一个更好的离去基团酸催化,这是一个重要的原因有助于消除反应。
5。在亲核酰酸催化替换的例子
这里有两个例子使用酸作为催化剂的亲核酰取代反应,以及酸协助损失离去基团。
一个羧酸能被转换成一个酯在酸性条件下。这是菲舍尔酯化(看到帖子:费歇尔酯化)。
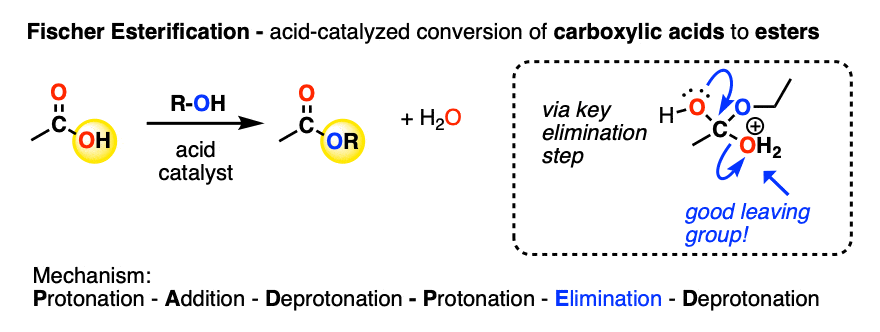
在关键的步骤中,一个分子的H2O是消除四面体中间,导致质子化了的酯。
类似地,可以转换为一个酰胺羧酸在酸性条件下。这叫做酸酰胺水解(看到帖子:酰胺水解)
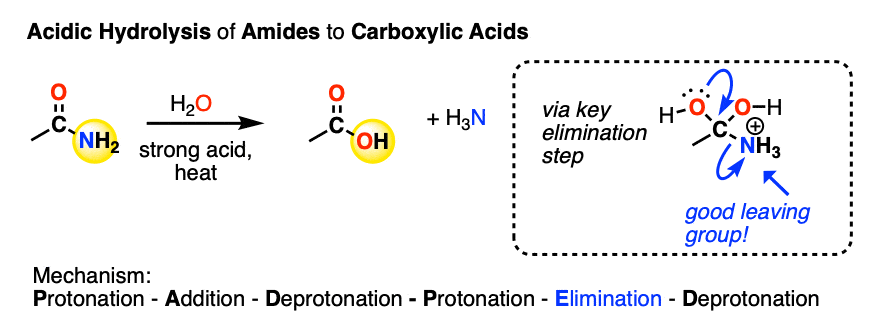
同样,关键的一步是弱碱NH的消除3四面体中间。没有酸,没有替换发生。
为消除酸催化的一个限制是,我们限制使用的亲核试剂,并不是不可逆转的摧毁了强酸。
这意味着像NH强碱性的亲核试剂2(-)(-),RO(-),氢化物和格里纳不兼容的酸性条件,因为酸碱反应通常远远超过任何反应碳。(看到帖子:酸碱反应快),
6。总结——结论
- 如果亲核加成是最重要的反应机理金属羰基合物,那么它的相反-消除排名是第二重要的机制。
- 这是一个关键机制在亲核酰取代反应,除了它在形成中的作用缩醛树脂和亚胺,我们看到以前一章醛和酮。
- 消除的好感度是决定的碱度的离去基团。好离开组织薄弱的基地。
- 贫穷离开组可以变成好离开组通过添加酸,因为共轭酸任何物种都是较弱的基础,因此一个更好的离去基团。
- 添加酸是必不可少的在羧酸的亲核取代反应和酰胺等费舍尔酯化和酸酰胺水解。
笔记
注1。一个例子,氢化做离开一个elimination-type过程Canizarro醛的反应。的关键一步是转移氢化从(deprotonated)醛半缩醛第二个相当于相同醛,导致一个醇盐和一个羧酸(快速进行酸碱反应)。
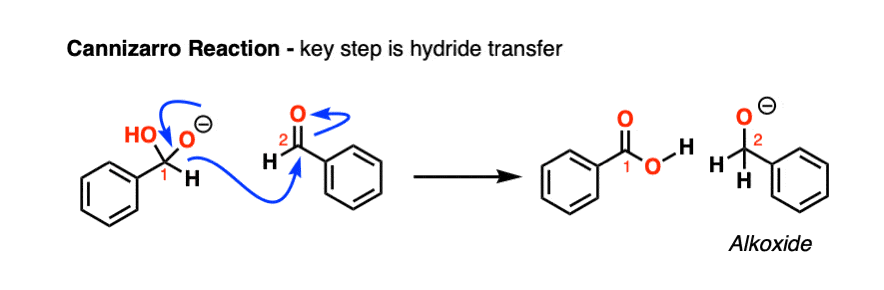
然而,这个反应需要极其基本条件和热(以及要求非enolizable醛)
测试你自己!
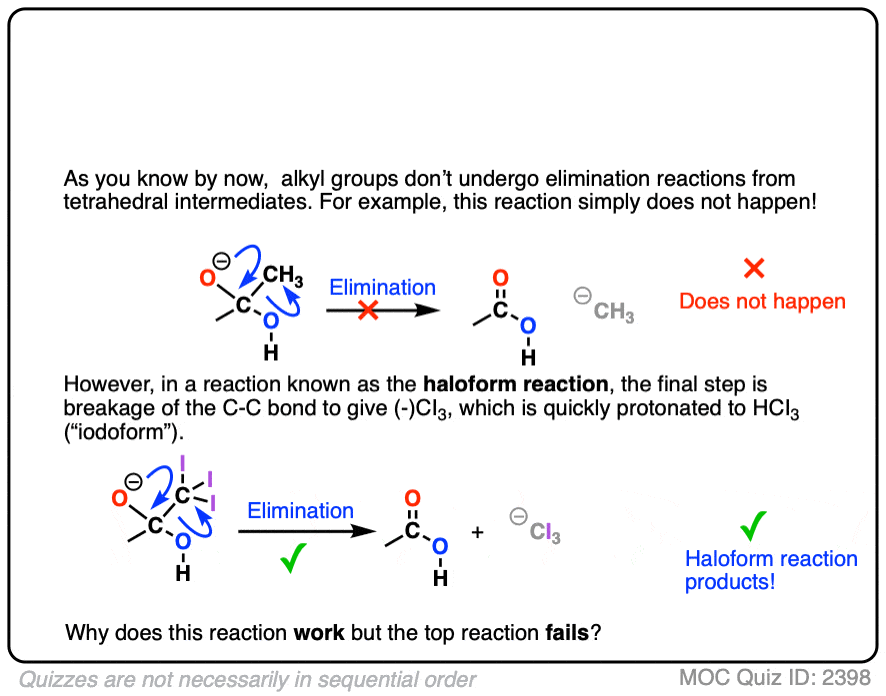 点击翻转
点击翻转
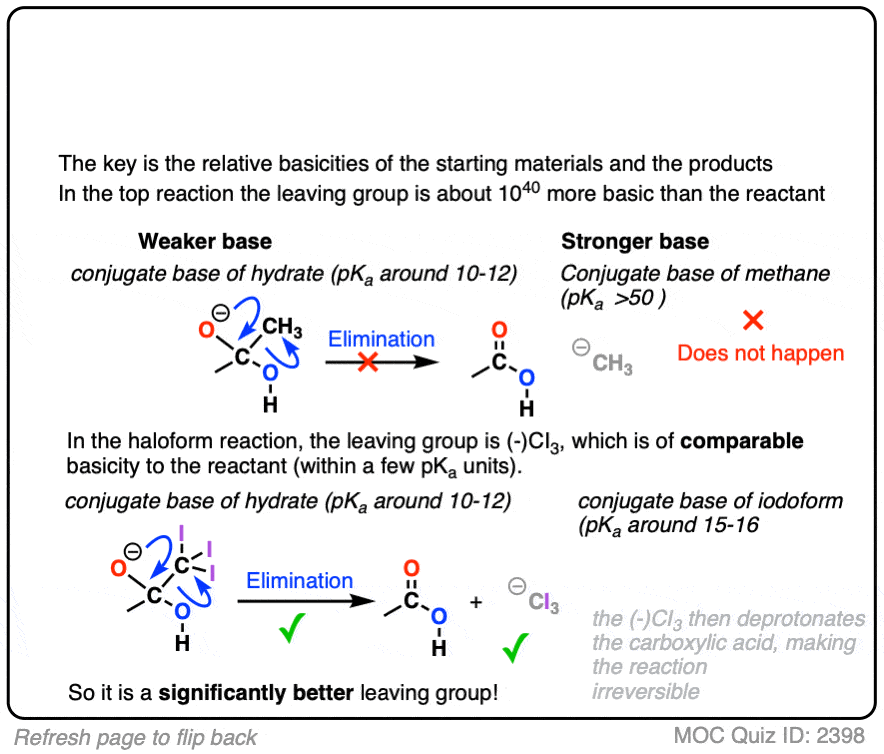
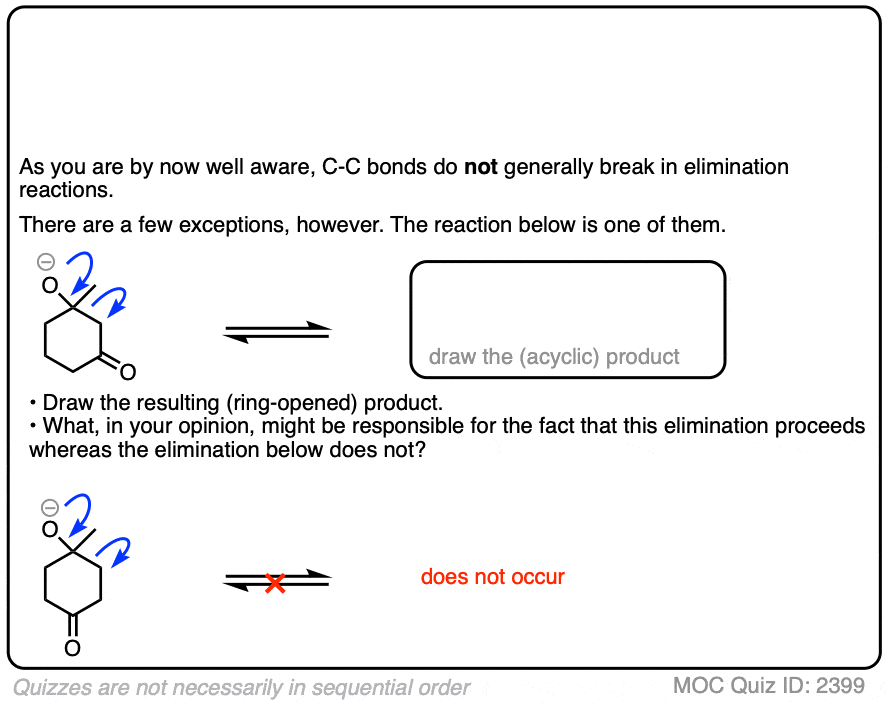 点击翻转
点击翻转
(高级)引用和进一步阅读
- 年代N2机制醇解、氨解和水解乙酰氯
t·威廉·本特利,加雷斯·卢埃林和j·安东尼去
《有机化学》杂志上1996年61年(22),7927 - 7932
DOI:10.1021 / jo9609844
尽管addition-elimination反应被认为在大多数情况下,有亲核酰取代的情况下结果来自直接攻击羰基碳与亲核试剂,尤其是在强极性溶剂离去基团很容易电离。 - 计算研究的亲核取代羰基碳:年代N2机制和四面体中间在有机合成
约瑟夫·m·福克斯,奥尔加·Dmitrenko联安辽,罗伯特·d·巴赫
《有机化学》杂志上2004年69年(21),7317 - 7328
DOI:10.1021 / jo049494z - 估计氢化物离子稳定冷凝系统:能源的生成和溶解在水和极性有机溶剂
- 苯甲酰哌啶
奇迹,c . s .;懒,w。
Org。Synth。1929年,9、16
DOI:10.15227 / orgsyn.009.0016
这个过程从有机合成,独立的测试和可再生的有机合成实验室程序,是一个典型的Schotten-Baumann酰胺合成。原Schotten-Baumann论文: - Ueber氧化des Piperidins死去
Schotten C。
的误码率。1884年,17(2),2544 - 2547
DOI:10.1002 / cber.188401702178 - Ueber一张einfache方法der Darstellung冯Benzoesaureathern
鲍曼,E。
的误码率。1886年,19(2),3218 - 3222
DOI:10.1002 / cber.188601902348
当主要脂族胺与酯反应,例如,丁烯二胺与碳酸二甲酯,反应速率非常缓慢,但当水是补充说,它变得非常快。如何解释这种现象?
碳酸二甲酯不是一种酯,碳酸盐,这是一个不同的官能团。
的一个关键的反应胺与碳酸盐是安装保护团体,如中银集团和通常做在基本条件下(即不仅仅是水,但水的存在基础如碳酸钠)。代表程序可以找到这个页面:
https://www.organic-chemistry.org/protectivegroups/amino/boc-amino.htm
将卤仿反应涉及亲核攻击的哦,紧随其后的是位移CBr3组织还算数吗?
是的,很好的例子。Cl3C(-)阴离子通过[1,2]叶子消除反应。
“…(卤化物,AcO (-),…”
AcO(-)是什么意思?
谢谢!
算法(-)意味着乙酰:CH3C (O) O -醋酸的共轭碱