二烯烃和MO理论
在一昼夜的HOMO和LUMO桤木的反应
最后更新:2023年2月7日|
一昼夜的桤木的HOMO和LUMO反应
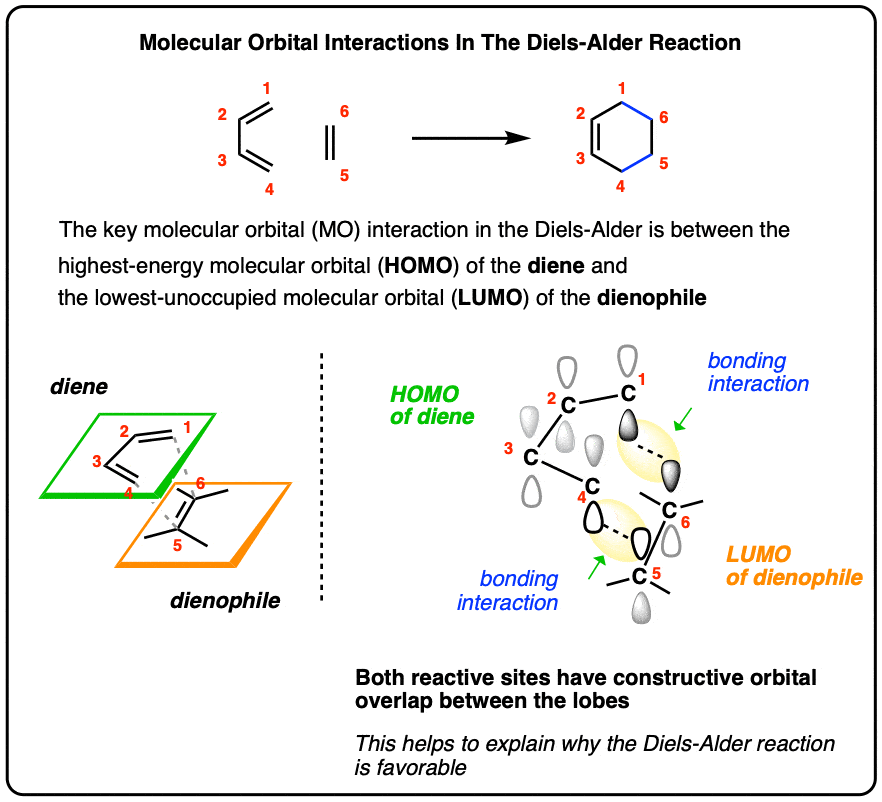
- Diels-Alder反应是a协调一致的反应二烯(4π电子)和亲二烯体(2π电子)形成一个新的六元环
- 新的碳碳σ键的形成重叠π分子轨道的C1和C4的二烯和C1和C2的亲二烯体。
- 为了让新债券形式,必须有有建设性的这些轨道重叠——也就是说,他们必须有相同的阶段。
- 通过分析二烯的分子轨道和Diels-Alder亲二烯体反应,它变得明显,建设性的重叠是可能的最高占据分子轨道(HOMO)之间二烯的最低未占据分子轨道(LUMO)亲二烯体。
- 这种类型的反应在两个重叠是不可能的烯烃。
表的内容
- 快速回顾Diels-Alder反应
- 键的形成需要一个分子的HOMO重叠(亲核试剂)与另一个分子的LUMO(亲电试剂)
- 协同反应:当两个债券形式同时,多个轨道必须重叠
- 分子轨道之间的[2 + 2]环加成反应中乙烯和乙烯显示为什么在“热”条件下的反应是不利的
- 分子轨道的Diels-Alder反应:互动的二烯HOMO亲二烯体LUMO优惠在Bond-Forming网站
- 在“光化学”情况下,[2 + 2]其实蛮好用的
- 总结——轨道对称性的关键作用在Pi-Systems协调一致的反应
- 笔记
1。快速回顾Diels-Alder反应
今天我们要进入Diels-Alder反应的机制从分子轨道的角度来看。使用我们先前的文章如何建立分子轨道,我们将展示如何Diels-Alder建设性的结果轨道重叠的最高占据分子轨道(HOMO)二烯的最低未占据分子轨道(LUMO)亲二烯体。
但是,首先,让我们回顾我们Diels-Alder为止:
- Diels-Alder反应二烯与亲二烯体结合形成一个新的六元环(参见:介绍Diels-Alder反应]
- 三个债券形式(两个σ键和一个π键)和三个债券打破(3π键)
- 产品的立体化学可以从分析可靠地预测二烯和亲二烯体的立体化学看到的:Diels-Alder反应的立体化学]
- 在某些情况下,非对映体的混合物(挂式- - -endo -得到了)。一般来说,endo——是青睐的精彩。(参见这篇文章挂式和endo]
我们还没有真正覆盖为什么Diels-Alder实际工作。毕竟,我们已经看到很多例子的东西不工作;两个烯烃,例如,不要把加热时形成四元环二烯和的亲二烯体结合形成六元环。也不做两双烯结合加热时容易给8人环。
为什么Diels-Alder那么容易,许多看似相关的反应如此之难呢?
这个问题的答案在于的安排π分子轨道在这个反应的两个组件。
在1960年的一个理论轨道对称性了,理解不了这些反应,提供了一套非常有用的预测规则的伍德沃—霍夫曼定律。
我们会刮伤表面的轨道对称性规则,使用它们来展示为什么二烯烃的反应烯烃(Diels-Alder)加热时容易发生,但的反应烯烃与烯烃(也称为[2 + 2]环加)没有。
2。键的形成需要一个分子的HOMO重叠(亲核试剂)与另一个分子的LUMO(亲电试剂)
我们看到涉及大多数反应亲核试剂(一个电子对捐赠)的反应亲电试剂(一个电子对受体)形成一个新的键。
为了使债券形式,填满轨道上的亲核试剂包含电子对的接触(重叠)空轨道上的亲电试剂可以接受电子对。

- 上的一对电子亲核试剂几乎总是来自于高能占据分子轨道(HOMO)亲核试剂。为什么?因为这些是最紧密的电子。
- 上的轨道亲电试剂接受电子的一对几乎总是最低未占据分子轨道(LUMO),因为这将导致最低过渡状态(和最快的反应)。
在大多数的反应(如SN2)只有一个键是在一个给定的中心形成一次:
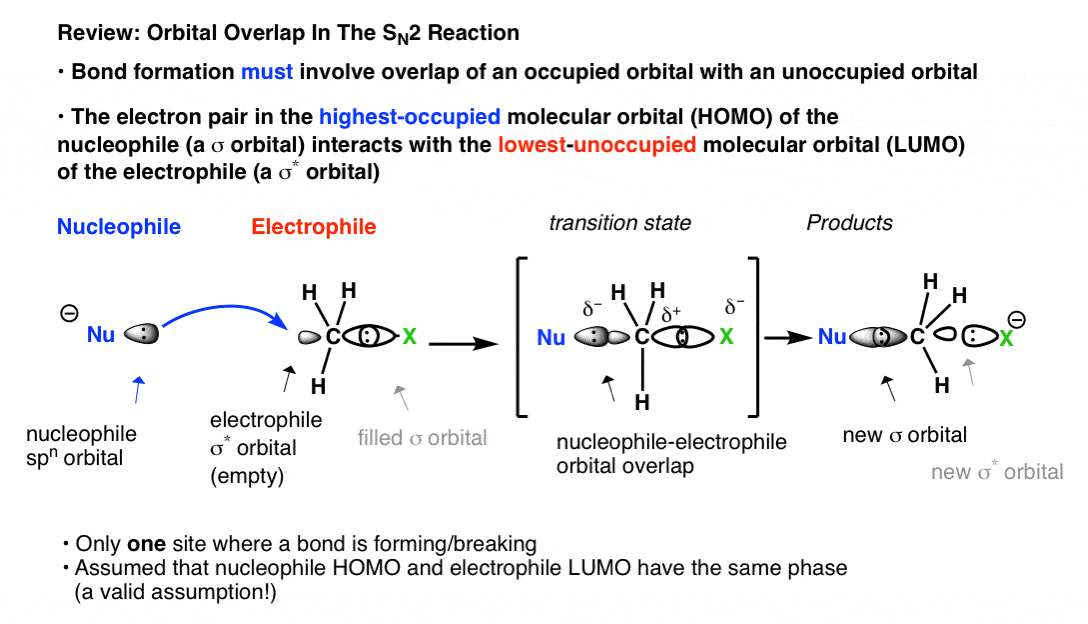
一个小音符。在这个年代N2我们假设HOMO和LUMO有相同的阶段。这是非常有效的只要我们只处理一个债券形成。
3所示。协同反应:当两个债券形式同时,多个轨道必须重叠
事情变得更复杂的反应时,两个或两个以上的债券是在同一时间形成的。这就是所谓的协调一致的反应(而不是“逐步”)。
把两个的组合烯烃给一个环丁烷环。(这是通常被称为一个[2 + 2]环加成作用。)
由于我们有两个债券形成同时,两个要考虑轨道的相互作用。
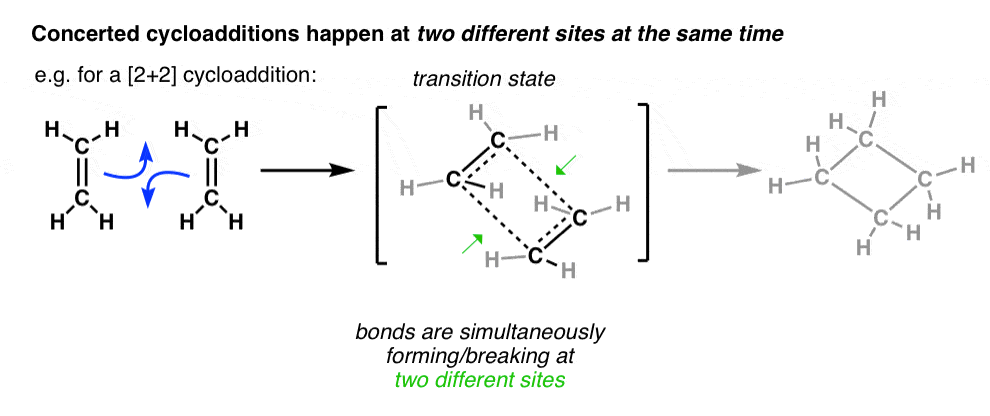
乙烯和乙烯。:-)
更具体地说,亲核试剂是一个乙烯分子的HOMO、亲电试剂是另一个的LUMO乙烯。
一个乙烯分子的HOMO必须结合另一个乙烯分子的LUMO。(我们不能把两个占据轨道,自然有一个严格的电子入住率限制/轨道。因为我们不能没有电子成键,结合两个lumo傻了)
4所示。分子轨道之间的[2 + 2]环加成反应中乙烯和乙烯显示为什么在“热”条件下的反应是不利的
让我们看看乙烯的π分子轨道。HOMO节点为零,LUMO只有一个节点。(我们学习了如何建立乙烯分子轨道,在这篇文章中]。
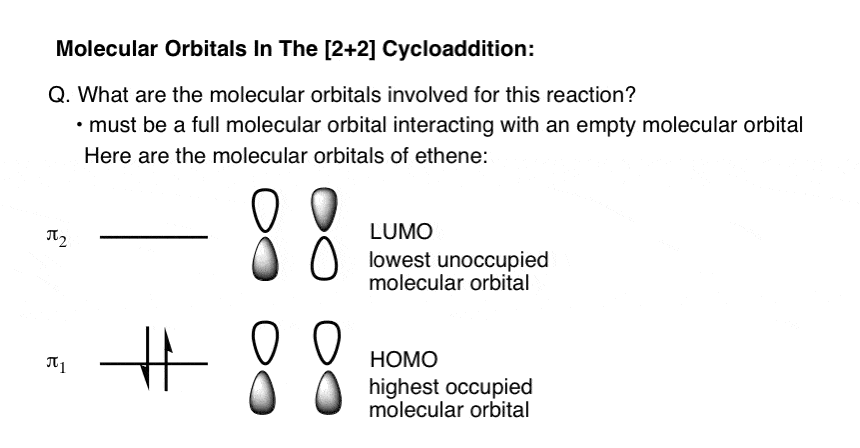
为了使反应发生在协调一致的方式,我们必须有建设性的重叠每个叶的债券之间正在形成。(如果对面的阶段,是轨道之间的相消干涉,因此零电子密度之间的原子)
现在让我们把两个乙烯分子在一起:
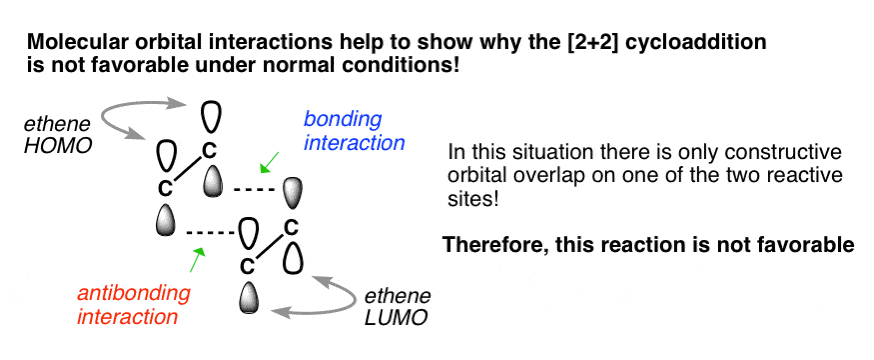
注意,只有一个相互作用的叶的叶像阶段互动(键)。反相交互的其他交互叶,不会造成债券。(注1]
这有助于我们理解为什么[2 + 2]环加通常不出现在“热”的条件下(即加热)。轨道不重叠!(注2]
[2 + 2]环加做然而,发生光化学的条件下。更多详情。
5。分子轨道的Diels-Alder反应:互动的二烯HOMO亲二烯体LUMO优惠在Bond-Forming网站
现在让我们执行同样的分析Diels-Alder反应。
因为我们已经看到乙烯的分子轨道,让我们看看丁二烯。(相关帖子:丁二烯的π分子轨道]。
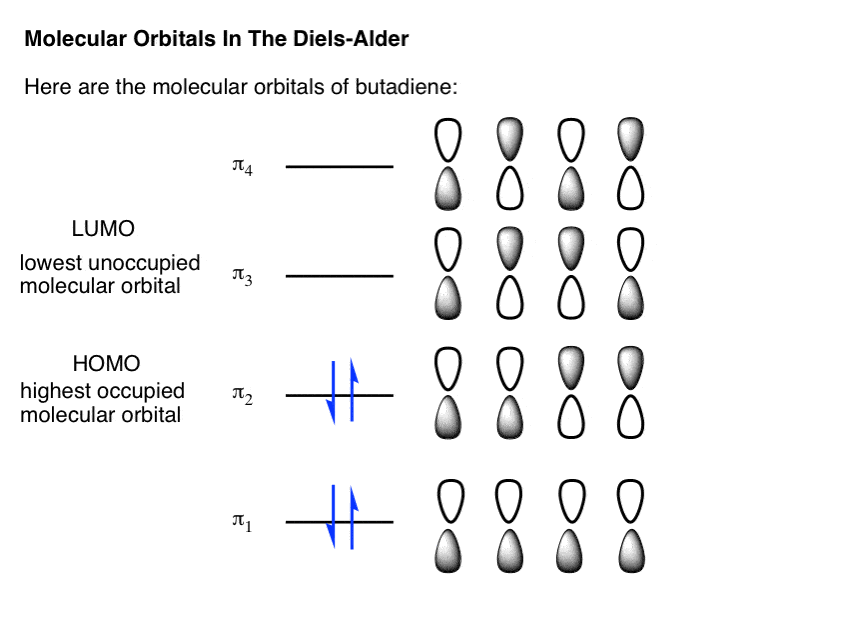
现在,让我们看看会发生什么当我们试图排队丁二烯的HOMO和LUMO乙烯。
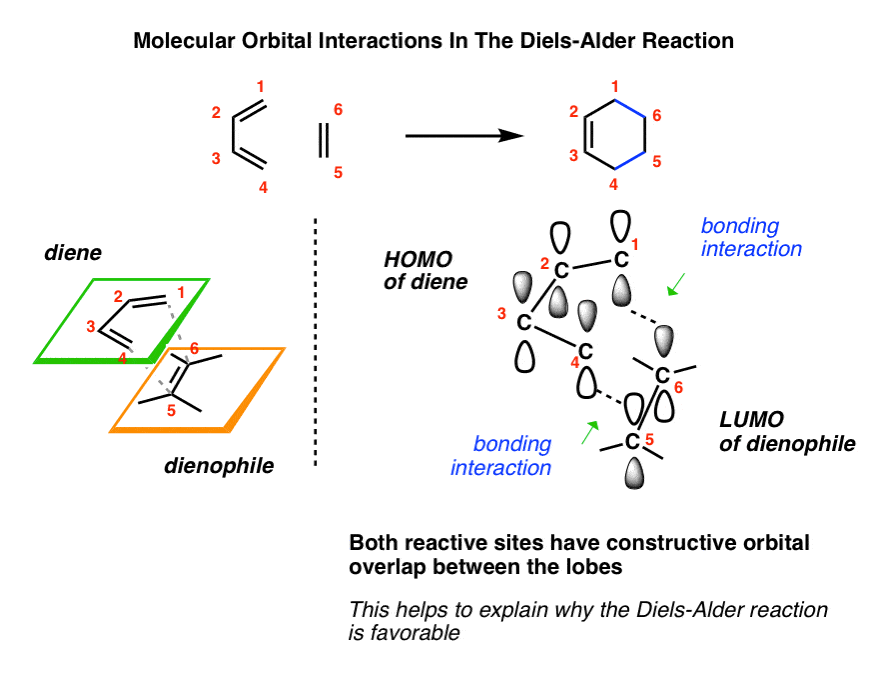
(为什么不反过来,LUMO丁二烯和乙烯的人类吗?看到注3]
这里我们有二烯(绿色飞机)接近亲二烯体平面(橙色),作为一个直升机停机坪可能方法。之间的新债券形式C1- c6和C4- c5。注意,每一对的叶交互的阶段匹配,因此有建设性的轨道重叠。
(还要注意,虽然二烯被描述为在“顶级”在这里,这如果是在底部也同样有效徘徊在一个弹出的形象或点击这个链接。对称性是在这两种情况下——就像两个乐高积木,尽管每个脸上的“叶”的阶段是相反的)
这有助于我们理解为什么Diels-Alder反应——工作轨道相互作用是有利的。
我们将停止Diels-Alder,但注意4继续讨论(书呆子只)。
6。在“光化学”情况下,[2 + 2]其实蛮好用的
上面我说的[2 + 2]环加成反应不工作在“正常”情况下,我的意思是“加热”。(有机化学家通常使用术语“热”条件)
然而,有人观察到,如果一个暴露紫外线(UV)光的反应,这种反应可以进行得很好。(这被称为,“光化学条件”)。
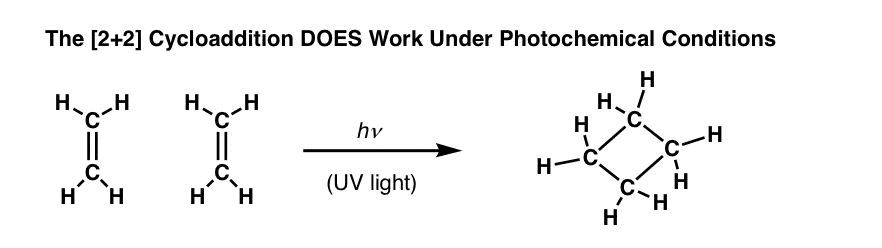
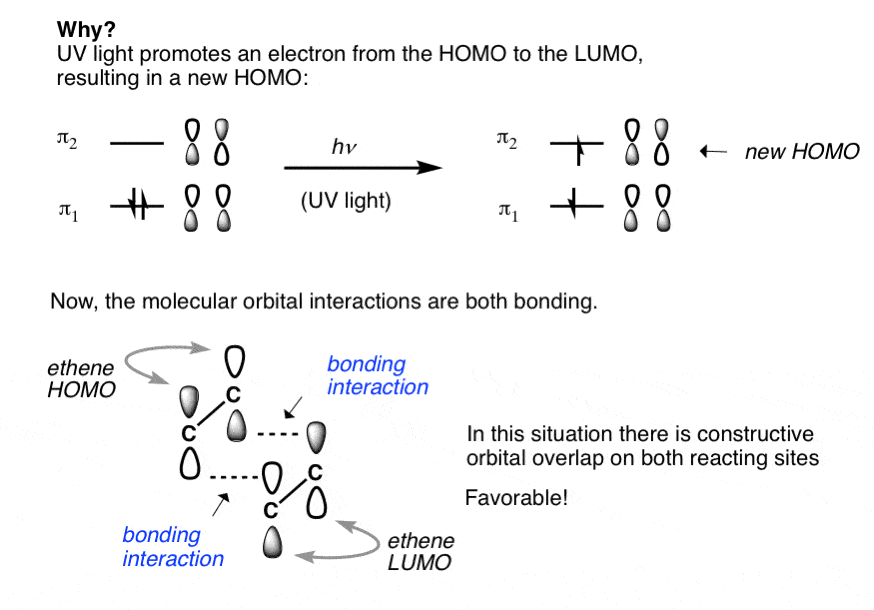
为什么?
紫外线能促进电子从人类LUMO,导致“新”人类。(有时称为HOMO-prime或SOMO(“单独占据分子轨道”))。(这是一个以前的文章在紫外光谱]。
现在有两个成键叶之间的相互作用。和反应确实有效!
没有人会想惹完美,但至少值得简要指出,促进Diels-Alder反应是通过加热,不通过光化学手段。试图运行一个“光化学条件”下Diels-Alder将会见了相同的失败[2 + 2]环加成反应在热条件下,轨道对称性,出于同样的原因,因为是错误的。
7所示。总结——轨道对称性的关键作用在Pi-Systems协调一致的反应
在“热条件”(加热,没有紫外线)[2 + 2]是“禁止”和Diels-Alder是“允许”。(注意4]
形势逆转的紫外线,可以晋升为一个电子给新人类以不同的轨道对称性。
在光化条件下,两个之间的[2 + 2]环加成作用烯烃是Diels-Alder“允许”和“禁止”。
我们可以这一切归结为一个简单的表:

随着我们继续探讨这个话题,我们将再次讨论这个表进行更新,因为有一个全家轨道对称性的反应起着至关重要的作用。
笔记
注1。我们的假设一个乙烯分子方法一个乙烯分子以相同的方式我们汇集两块乐高。面对一个组件底部连接的顶面。
每一对叶参与成键的分子的相同的脸上。这样的安排被称为同侧的。这是类似于”syn”。
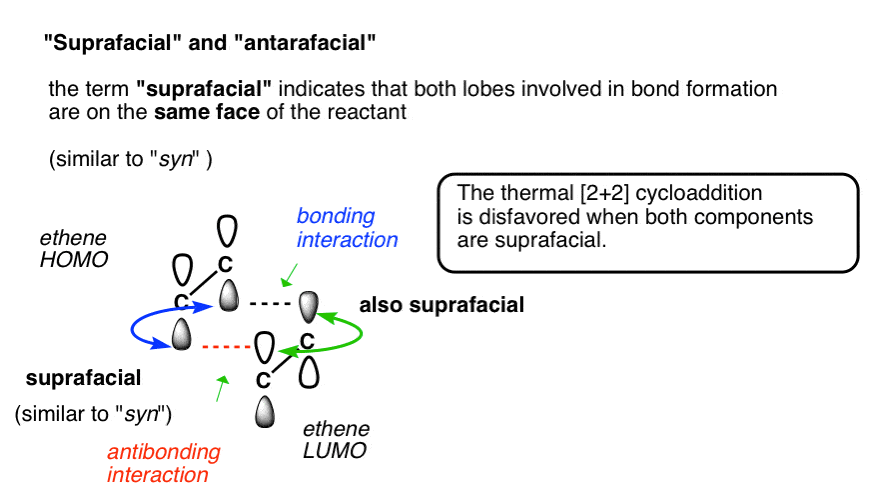
另一种可能性。如果,相反的“阴影”叶乙烯人类结合的“白色”叶LUMO,而是“阴影”叶在一起了其他的脸LUMO。因为叶都有相同的阶段,这将是一个结合互动!
有名字的情况叶相反脸上的反应物参与反应:它被称为,“antarafacial”(类似于“反”)。
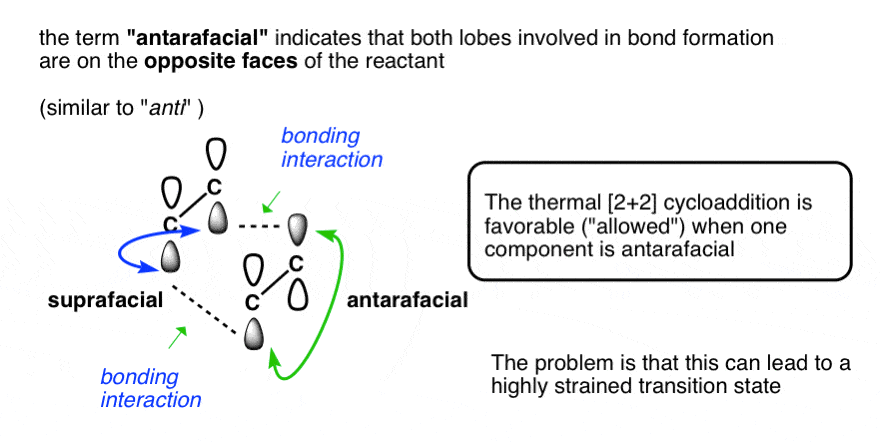
你可能会问为什么这不会发生在[2 + 2]环加成反应烯烃。然而如果你构建一个模型,你很快就会发现答案是它不是那么该死的简单!过渡态的[2 + 2]之间的两个烯烃与单个antarafacial组件是高度紧张。
[有例子的[2 + 2]环加热条件下工作,如涉及烯酮,有一个antarafacial组件。这不是今天的主题。]
注2。这种分析意味着是成功的,在这些类型的反应,分子轨道的对称性守恒,换句话说,我们可以把轨道上的叶的相对相位常数时间尺度的过渡状态。这就是为什么这些规则是题为“轨道对称守恒”。
注3。之间的相互作用的亲二烯体HOMO和LUMO二烯一样良好的从“轨道对称性的角度来看。然而,反应速率最快将在HOMO和LUMO的能量的情况下两人靠的很近。大多数Diels-Alder反应你会看到将富二烯烃(高能HOMO) electron-poor亲二烯体(低能LUMO)。
之间也有有利Diels-Alder反应electron-poor二烯烃(低能LUMO)与负电子的亲二烯体(高能HOMO)。这些被称为逆electron-demand Diels-Alder反应。
注意4——继续交替模式添加额外的π键;(4 + 4)是“热禁止”和(6 + 4)是“热”。(6 + 6)再次“热禁止”,等等。环加成作用的最大数量的π电子的我知道是一个[14 + 2]环加成作用。这是热允许仅仅是因为一个反应的组件(heptafulvalene)反应antarafacial时尚。
当我准备考试的时候,我往往会绕道从我需要学习什么,而是我挖的东西不足够的意义对我来说,直到他们做。我在学习pericyclic反应和HOMO和LUMO概念有点模糊,尽管能够预测正确的答案。本文然后我登陆。不能更感谢这个概念的深入了解,非常感谢先生。
嗨Dimitris——我很高兴你找到这篇文章有用!最好的祝福与你的研究!詹姆斯
你好詹姆斯,感谢这美好的,不会有更多的组织和点如果本文未读。谢谢,谢谢。更多的权力。
我更不可能谢谢。这是一个美妙的文章和帮助我非常理解pericyclic反应。
太好了,很高兴你Vaibhav发现它有用。
你好,詹姆斯,你的帖子已经帮助我很多在我本科研究有机化学!我有几个问题:如果我们要使用Woodward-Hoffman规则,我们如何应用它的4 + 4环加成作用?我努力识别(4 + 4的2丁二烯分子)一个是同侧的或anarafacial如果我画一丁二烯homo和丁二烯lumo !
在你结束陈词,14 + 2的例子很好用于我的幻灯片和大量的文本,他们是怎么知道它是antarafacial ?我看到一个图弗莱明的书,和许多其他资源就显示空连接antarafacially p轨道。