自由基反应
总之:自由基
最后更新:2022年12月7日|
总结主题的自由基反应
我们学会了在本系列中自由基呢?很多事情。我们已经看到,他们是中性的物种装价电子层往往是高活性烷烃和双键。我们已经看到,他们是稳定的电子给体和移位。我们已经证明机制要经过三个不同的阶段(起始、传播、终止),虽然反应往往是选择性的形成更稳定的自由基,自由基溴远比氯自由基卤化烷烃的选择性。最后我们也探讨烯丙基的(和苄基的)卤化和看到的例子烯丙基的重排。
表的内容
- 自由基是什么?
- 均裂和“Single-Barbed”弯曲的箭头
- 影响自由基稳定性的因素
- 因素破坏自由基
- 一个方便的快捷方式确定激进的稳定
- 自由基反应如何工作?开始,传播、终止
- 自由基卤化导致同分异构体的混合物——但有选择性
- 溴化比氯化选择性
- 烯丙基溴化、烯丙基溴化和烯丙基的重排
- 激进分子烯烃的自由基加成
- 笔记
1。自由基是什么?
自由基化学物种,包含一个单独占据轨道。他们是中性和高活性。
最常见的一种类型的自由基反应自由基取代。这是甲烷和Cl之间的反应的一个例子2:
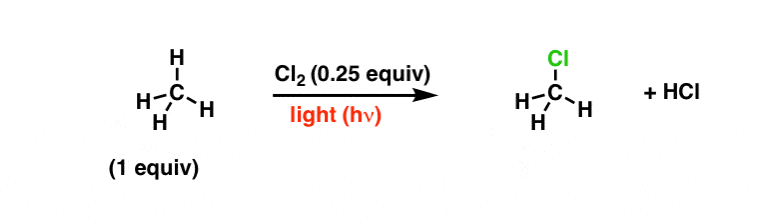
2。均裂和“Single-Barbed”弯曲的箭头
不像我们之前看过的许多反应,自由基反应不涉及电子的捐赠或验收孤对和他们不离子。相反,通过自由基反应均裂——也就是说,债券打破这样相同数量的电子分布到每个原子。修改曲线箭头形式主义:我们画与单个barb弯曲的箭头,显示了一个电子的运动:
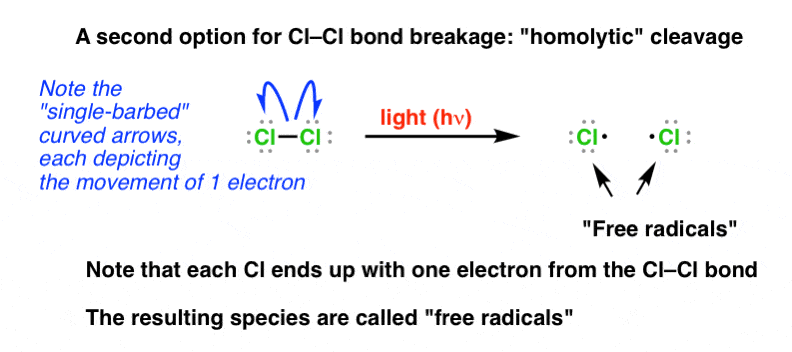
3所示。影响自由基稳定性的因素
像碳正离子自由基缺电子物种。(有助于知道:自由基的稳定性因素的影响是相同的影响碳正离子的稳定性。他们可以通过捐款来稳定的电子密度的邻居;出于这个原因,彻底稳定增加的顺序甲基< <二次<三级。(激进分子也稳定了相邻原子的孤氧和氮等)。(参见:3因素稳定自由基]
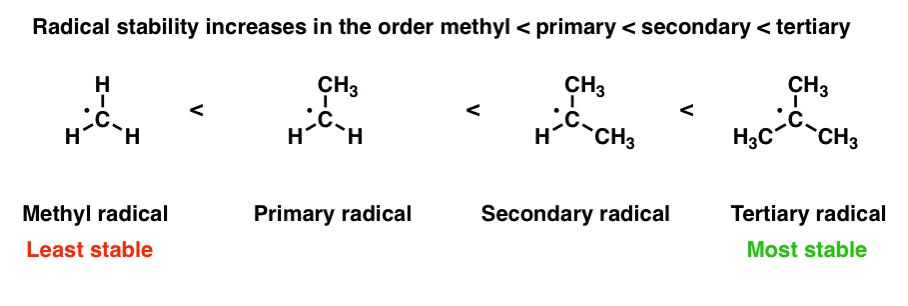
第二个重要因素稳定自由基是“移位”——也就是说,如果激进可以分散到两个或两个以上碳原子。一个更熟悉的说法是自由基是由共振稳定。
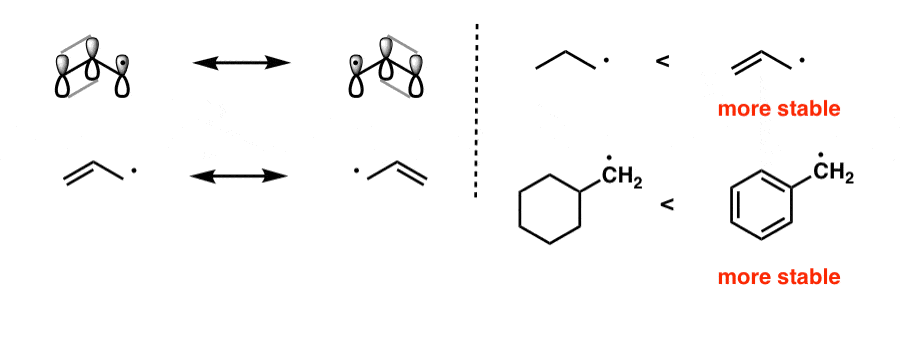
4所示。因素破坏自由基
作为缺电子物种,它也有助于记住的一些因素破坏自由基。有几个要记住的重要趋势(参见:哪些因素破坏自由基吗?]
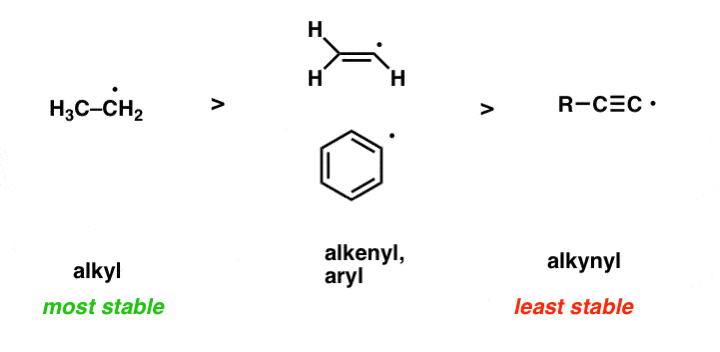
- 自由基稳定性下降%的提到的轨道(即增加。随着半空轨道变得接近原子核。因此,原子从自由基的稳定性降低烷基来烯基来炔基。

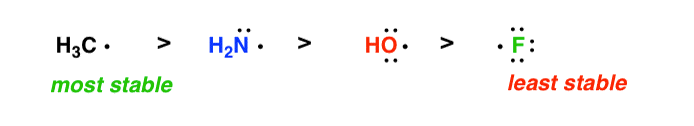
- 在一行的元素周期表,减少自由基稳定性随着电负性的增加

- 自由基稳定下降增加一列的元素周期表,F•< Cl•< Br•<我•由于缺电子轨道是分散到更大的体积。
- 自由基毗邻一个吸电子集团不太稳定,因为实际上,电子密度被远离已经不足一个电子的物种。(注意,然而,这只适用于电子撤回团体不能捐献一对电子,像CF3或CN。)
5。一个方便的快捷方式确定激进的稳定
键离解能量(12)测量所需的能量均裂债券乳沟,通过代理我们可以解释碳氢键的优势作为一个很好的衡量碳自由基的稳定性。通过检查的趋势X h键的强度(其中X是各种原子)我们可以辨别激进的稳定的趋势。(参见:债券的优点和激进的稳定]
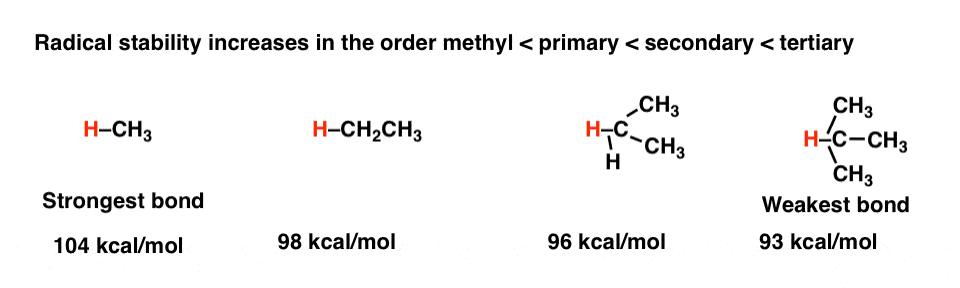
这也反映在的优势”烯丙基的“碳氢键,这是弱于正常由于共轭自由基产生上的事实。例如,碳氢键强度的甲基丙烷大约98千卡每摩尔,而甲基1-propene 85千卡每摩尔。为因素的完整列表,请参阅原文。
6。自由基反应如何工作?开始,传播、终止
“当然火”一个学生发现自己识别自由基反应是寻找“热”的存在(Δ)或“轻”[hν]。什么光或热与自由基反应?它可以促进任何自由基反应的重要的第一步:初始化。这是弱键均裂碎片的形成两个新的自由基。(参见:自由基反应,为什么需要“热”或“光”?]
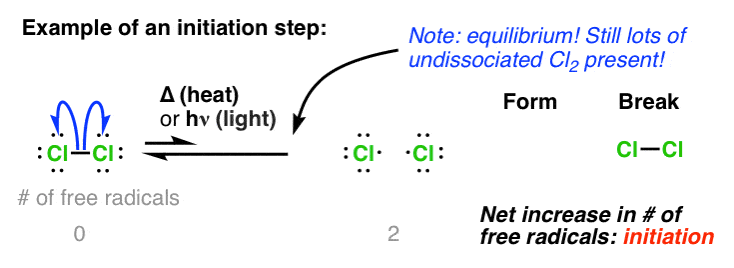
需要注意的是,“起始”不是一个反应,去完成。在任何给定的时刻,只有一个小浓度的原料转化为自由基。然而,由于反应是一个连锁反应,这通常是足够了。
第二步在自由基过程中至少有一个(但通常是两个)“传播”步骤。的自由基卤化烷烃,第一传播步骤除氢卤素激进,给一个新的碳激进。注意,自由基的数量保持不变(一个等式的两边)。
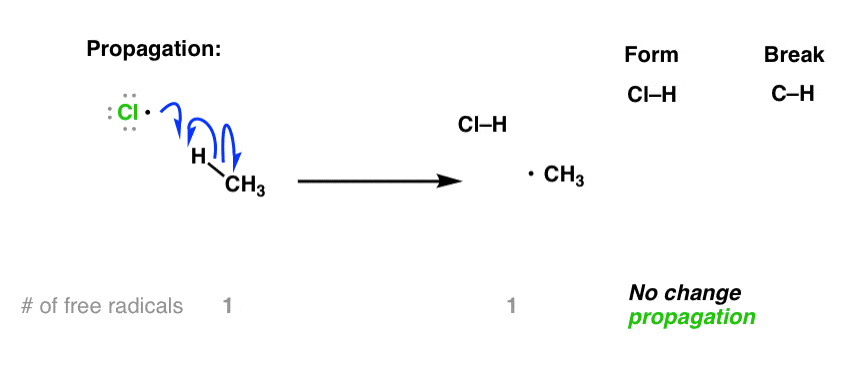
这是紧随其后的是第二个传播步骤。虽然可能会吸引很多新学生形成CH3通过结合CH cl3•氯激进,这不是接下来会发生什么(技术上是一个“终止”一步,见下文]。接下来会发生什么反应烷基激进的分子Cl开始2,形成一个新的C-Cl债券和Cl•激进继续连锁反应。再次,注意:这里没有净增长自由基的数量:
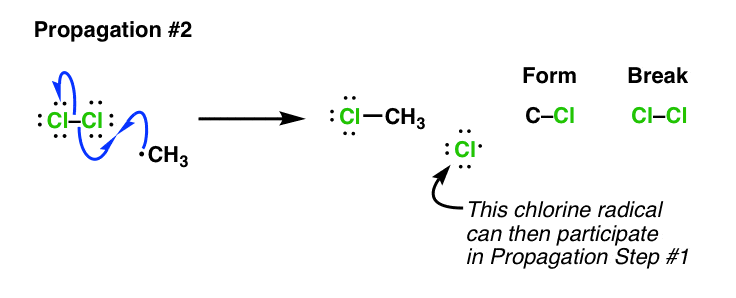
在任何给定的点在溶液中自由基的浓度很低。然而,在大部分的Cl2消费,自由基浓度会增加,直到radical-radical结合反应的速度是重要的。这就是所谓的“终止”因为它导致净自由基的破坏。有许多潜在的方法这可能发生——这是一个例子:
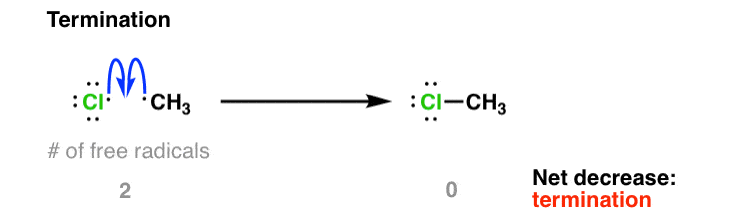
底线是,通过计算自由基创建或销毁的数量可以确定每一步一步开始,传播,或终止。
(参见:开始,传播、终止]
7所示。自由基卤化导致同分异构体的混合物,但有一些选择性
甲烷和乙烷是简单的例子。更换任何一个甲烷的4个氢氯会导致同样的产品。然而,当我们处理更复杂的烷烃,丙烷,丁烷,或2,3-dimethyl己烷,我们必须警惕各种化合物形成的可能性。这是一个重要的技能能够识别所有可能的化合物,这可能导致,说,等烷烃的mono-chlorination 2-methylpentane [5]。这些类型的问题最好接近系统:开始取代氢氯分子的一侧,并逐渐到另一边工作,它可以帮助双止没有重复试图命名(IUPAC)。(参见:同分异构体的自由基反应]
也就是说,同分异构体不会形成数量相等。有两个因素需要考虑。首先是这一事实并不是所有的碳氢键的强度相等;正如我们上面提到的,叔碳氢键比二级碳氢键更容易打破,比主碳氢键更容易打破。所以会有一个固有的这些债券之间的反应性差异仅仅通过它需要更少的事实活化能打破一个较弱的键。第二个因素是统计数据。以丙烷为例,主要有六个碳氢键和两个次要碳氢键。根据统计数据,我们希望mono-chlorination丙烷收率的比例3:1 1-chloropropane 2-chloropropane。
有趣的是,实际2-chloropropane比1-chloropropane 45:55 !
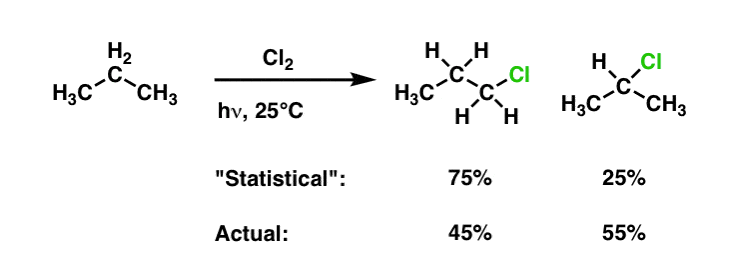
可以使用此信息来量化的反应性每种类型的氢分子。使用的方法这篇文章第二个碳氢键,我们可以确定是3.66倍比主在这些条件下碳氢键反应。(参见:自由基反应的选择性]
8。溴化比氯化选择性
有趣的是,溴代烷烃的选择性甚至超过三级和二级的氯化碳氢键。例如丙烷的溴化在25°C,二级碳氢键的反应是有选择性的主要因素碳氢键的97比1。
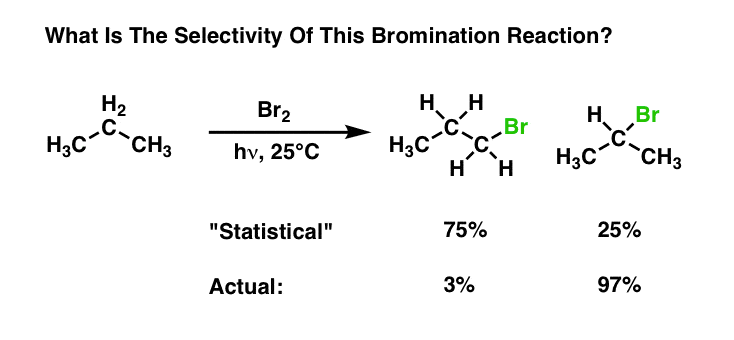
为何如此巨大的差异?最严格的方式看它是应用哈蒙德的假设:氯化是放热,溴化是吸热的;因此,氯化将“reactant-like”过渡态和溴化”产品,如“过渡态。在这种情况下能量之间的差异产品大于能量之间的差异反应物;由于选择性是由能量过渡状态之间的差异,因此,比氯化溴化会更有选择性。如果这听起来复杂,完整的贴在这里。另外,一个简单的类比我使用它来解释这个概念在这里。(参见:自由基反应,氯和溴的选择性]
9。烯丙基溴化、烯丙基溴化和烯丙基的重排
弱碳氢键(比如叔碳氢键)是很容易卤化。烯丙基的和苄基的碳氢键特别弱(约86千卡每摩尔)这使得他们优秀的溴化反应的底物。溴(Br分子2)可以用于苄基的溴化,但试图使用该试剂烯烃比如说,丙烯,将导致二溴化形成的。
解决这个问题的办法是使用有用的来源bromonium离子,N-bromo琥珀酰亚胺(国家统计局),它作为稀释Br的来源2。这允许更换烯丙基的与Br碳氢键。这个过程被称为“烯丙基溴化”。
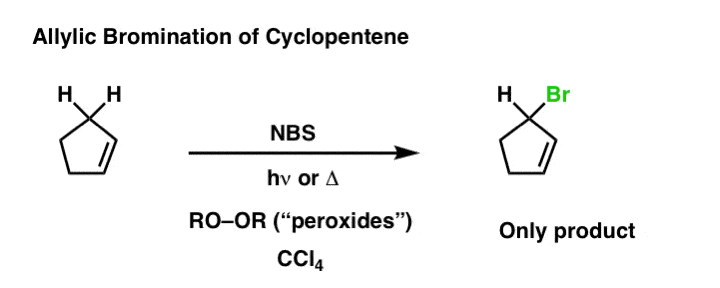
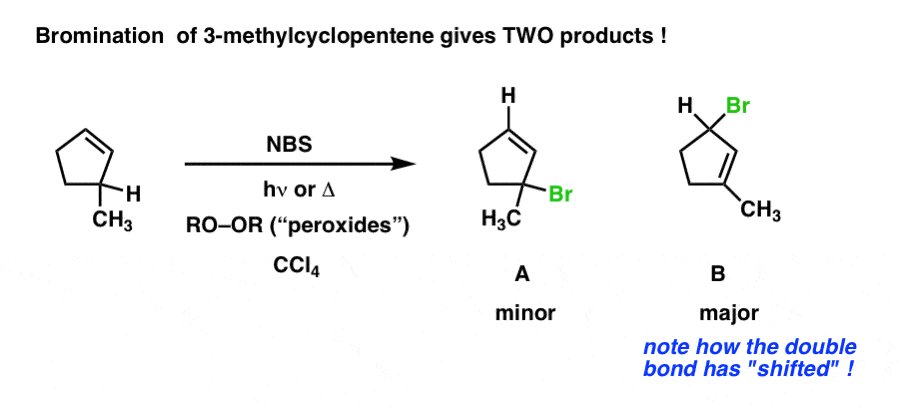
有趣的是,改变基质一点点可能导致一些令人吃惊的结果。下面的例子不同于上面的示例中,只有一个甲基。然而,这可能导致两个潜在的产品——“正常”的产物烯丙基溴化(A)和相关产品,烯丙基溴化与烯丙基的重排(B)。一个因素可以决定最终产品的形成是确定的烯烃代替。
10。激进分子烯烃的自由基加成
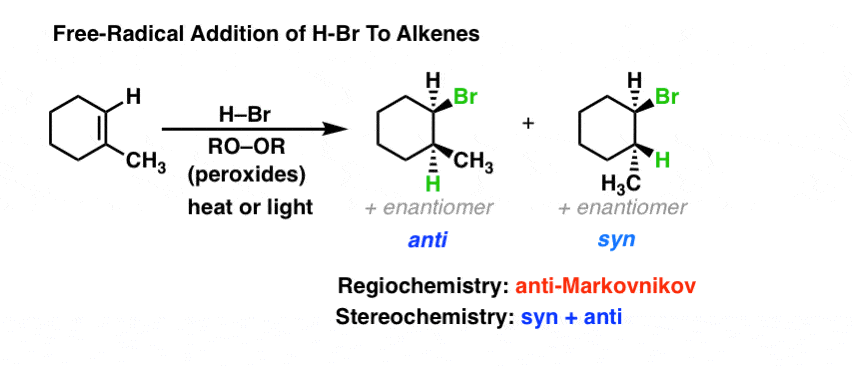
最后,重要的是要注意,H-Br可以添加烯烃以一个完全不同的方式取决于是否存在“过氧化物”。在缺乏过氧化物,H-Br补充说通过一个“正常”的亲电加成(贴在这里——而不是激进的相关)。然而,如果添加过氧化物混合物加热,它会导致均裂过氧化氢,形成新的自由基(启动)。过氧化氢可以删除从H-Br形成Br•激进,然后Br•可以添加烯烃。值得注意的是,Br•增加了烯烃在这样一种方式,我们最终得到最稳定的激进的中间,然后删除从H-Br氢,再生溴激进。最终的结果是“anti-Markovnikov“添加H-Br跨一个双键,相反的观察是什么在缺乏过氧化物。(在这篇文章中完整的机制]
它为自由基反应(现在)。
在接下来的系列,我们将开始我们的很多组织1反应在一起…,最后深入研究——我最喜欢的主题之一合成。
笔记
注1。与增加H-Br有关烯烃,是一个有趣的过程被称为“自由基聚合”。
如果某些烯烃被加热的激进initator(比方说“过氧化物”作为一个典型的例子),过氧化自由基可以增加吗烯烃,形成一个新的自由基最取代位置…和由此产生的自由基可以添加到另一个地方烯烃…。生成另一个自由基…。增加了另一个烯烃!——等等。
这个过程可以重复几千次终止前发生。日常生活的一些最常见的塑料可以这种方式,如聚乙烯、聚丙烯、聚苯乙烯。
在5点“有趣的是,实际2-chloropropane比1-chloropropane 45:55 !”
应该1-chloropropane 2-chloropropane,根据另一篇关于选择性。
由于这篇文章系列中,我不认为我现在就忘记自由基机理。
固定,非常感谢
你好詹姆斯,我想知道为什么自由基溴或氯不会引起聚合喜欢过氧化物吗?
没什么可说自己*不*,具体地说,尽管与烯烃、溴和氯自由基的前兆也倾向于作为亲电试剂添加到双键(如形成bromonium和chloronium离子)为聚合不会好。过氧化物不倾向于拥有这些阳离子通道。
点3下,因素破坏你提到的自由基自由基电子撤回旁边组不稳定对吧?你也提到比氰化物CN不能捐出一个电子。你能解释下为什么不能呢?我不看到它捐赠通过其孤对电子在胺或氢氧化物但不能通过共轭π电子的,例如,苯吗?
(p。字体非常满意)
为什么激进分子支持的碳氢键C-Cl最近债券形成吗?假设你有另一个解决方案,只有你有亚兰化合物,激进分子如hydroxel自由基能够打破C-Cl债券或不呢?如果是这样,C-halogen C-Cl hydroxel激进的攻击,更敏感C-Br还是我? ?
碳氢键的反应将有利于打破C-Cl债券,因为债券(103千卡每摩尔)产生的氯比结果O-Cl债券(65千卡每摩尔)。O-Cl债券相当薄弱由于孤对之间的排斥力。一个激进的驱动力打破C-Cl不够强大。
亲爱的先生,1度,2度免费药物意味着什么?
1°主要是免费的径向轴承激进连着另一个碳。2°是一个次要自由基的碳轴承激进与另外两个碳原子。
亲爱的Ashenhurst先生,
我不理解为什么激进分子是中性的。为什么他们不积极?
是不对的,他们想要填满他们的轨道?
你能解释一下我,好吗?
谢谢你的帮助。
你忠实的,
玛丽·B。
值得回忆的是,原子碳,C,有四个价电子,四个空地方八隅体,是中性的。
氟原子,F•,有七个电子,一个电子从满八隅体,也是中性的。
仅仅因为一个物种是反应和电子亲和能高并不意味着它必须起诉。
为证据,去甲基形式电荷公式,H3C•。如果碳有4电子本身,它是中性的。这里有一个电子本身(激进)和50%的份额在碳氢键的六个成键电子,(3)共有4。如果它失去电子成为甲基阳离子,CH3 (+)。如果它获得一个电子成为甲基阴离子,CH3 (-)。
所以,更重要的是在产品形成——中级激进的稳定或稳定(烯烃置换)?
我不知道如何回答你的问题。如果你问,“什么决定什么产品将形成”,答案就在比较各种竞争激活能量速率决定步骤。