醇、环氧化合物和醚
环氧开环与基础
最后更新:2022年11月9日|
环氧化合物开环与基本的亲核试剂
- 环氧化合物环醚有相当大的环应变(约13千卡每摩尔)
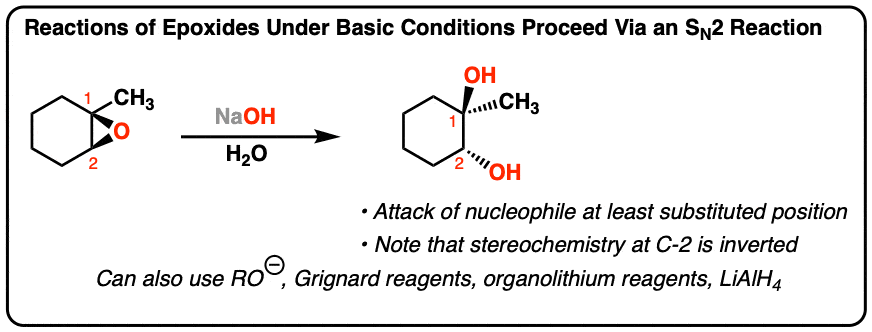
- 环氧化合物与亲核试剂在基本条件下进行反应至少替换的环氧
- 如果一个手性中心碳,其立体化学将会倒。
- 的亲核试剂,将添加到环氧化合物包括氢氧根离子(HO)醇盐、格氏试剂,organolithium试剂,LiAlH4(等)
- 一个简单的方法来记住这是认为基本条件下环氧打开程序就像一个年代N2的反应。
表的内容:
1。开环氧化合物与基础:它是如何工作的
在最后发表我们讨论了环氧化合物在酸性条件下的反应,看到他们如何与烯烃机制的“三人环”家庭。我们离开了指出环氧化物的反应(如上所示)与氢氧化钠在H2O给不同的产品相比,通过H3O +。因此,必须通过不同的机制。
我们的问题是,这个反应是如何工作的呢?
指出一个事实,即亲核试剂(HO)攻击环氧至少替换位置(C2)和立体化学的反演结果在这个位置,我们最好的证据是一致的反应通过熟悉年代N2机制其次是质子的转移弱酸性溶剂(H2O)醇盐(RO)提供一个中立的酒精。
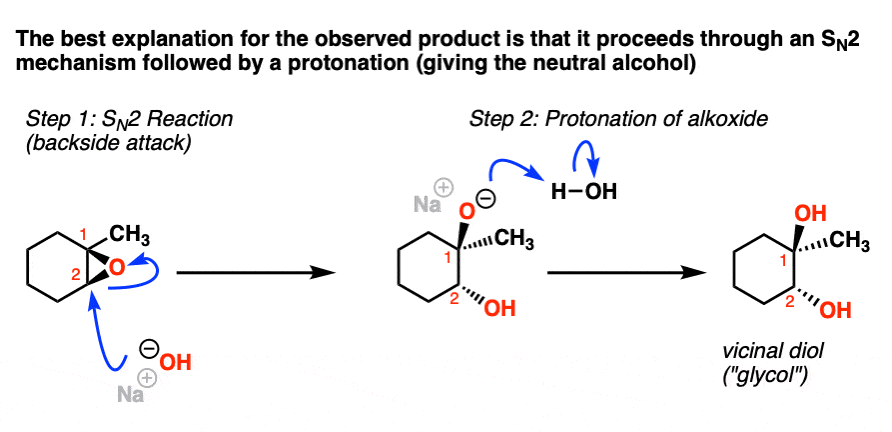
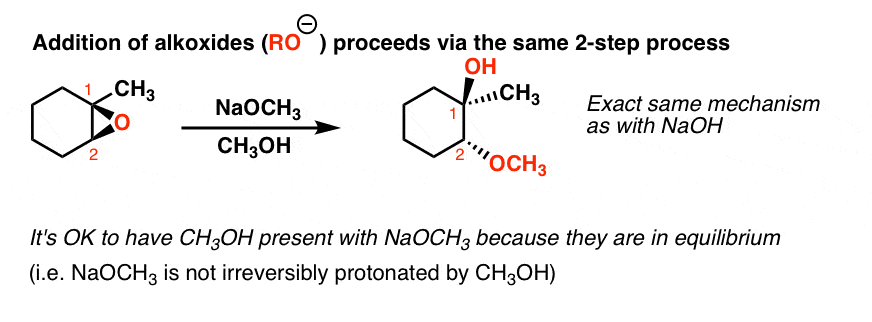
同理,如果环氧化合物醇盐处理(RO)在酒精溶剂,它们会导致基本相同的反应。这里有一个例子NaOCH3。注意,质子必须来自CH3哦,在这里。
2。溶剂的作用
现在,在最后一篇文章的最后,我们提到酸和一些强大的亲核试剂是不相容的,因为他们将被不可逆转的质子化作用[典型的例子:格氏试剂和水]。我们应该担心氢氧化钠在H2O或NaOCH3在CH3哦?不!这些都是基础的例子处于平衡状态与他们的共轭酸。
很好有氢氧化钠在同一反应容器与H2由于反应是可逆的。
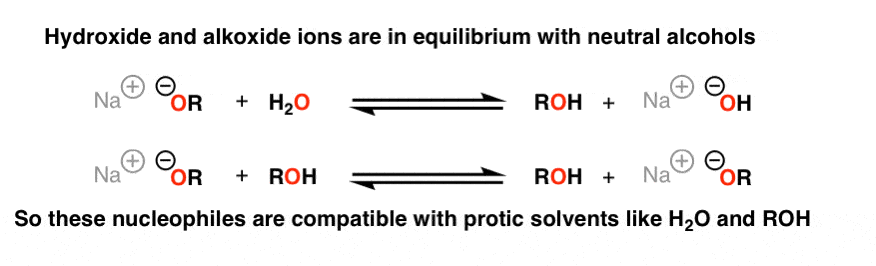
然而,如果我们搬到更强碱性的亲核试剂,如格氏试剂(RMgX) organolithium试剂(R-Li)或氢化物(H)应该是有关的,因为每一个物种的共轭酸(pK一个约50的烷烃,大约38 H2比卢武铉(pK)则要弱的多酸一个16日至18日)。
(一个好的经验法则“可逆性”的酸碱反应是pK一个差8或更少——看到一个方便的经验法则对酸碱反应]。
这意味着,如果这些卢武铉强碱接触,一个不可逆转的酸碱反应就会发生。我们因此获得一个醇盐(RO)在强度不足deprotonate烷烃或H2。
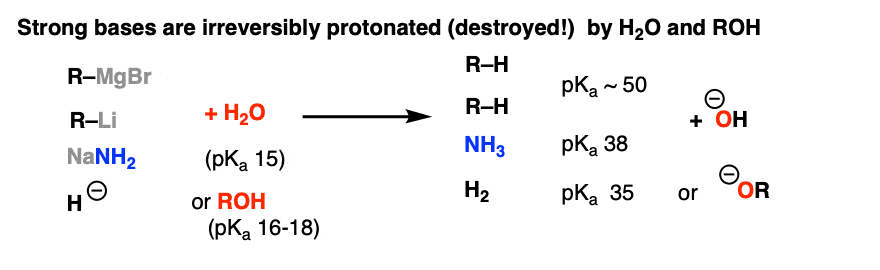
再见亲核试剂!
3所示。理解不同的淬火步骤:1)添加这个2)然后,添加这个!
在实践中这意味着什么,我们只是把质子化作用的步骤到最后,在一个过程有时被称为一个“淬火”。注意下面的每一个反应步骤1)和第2步)。
第一步是亲核试剂的添加。反应后就完成了,我们添加的质子来源(步骤2)淬火。请注意,有许多试剂通常写给这个过程——H2O H3O +、H +,在北半球4Cl,“酸检查”。他们都意味着同样的事情!
这里有一些例子与强碱性反应的环氧化合物的亲核试剂。格氏试剂、organolithium试剂和氢化(例如LiAlH4,H -)的来源。
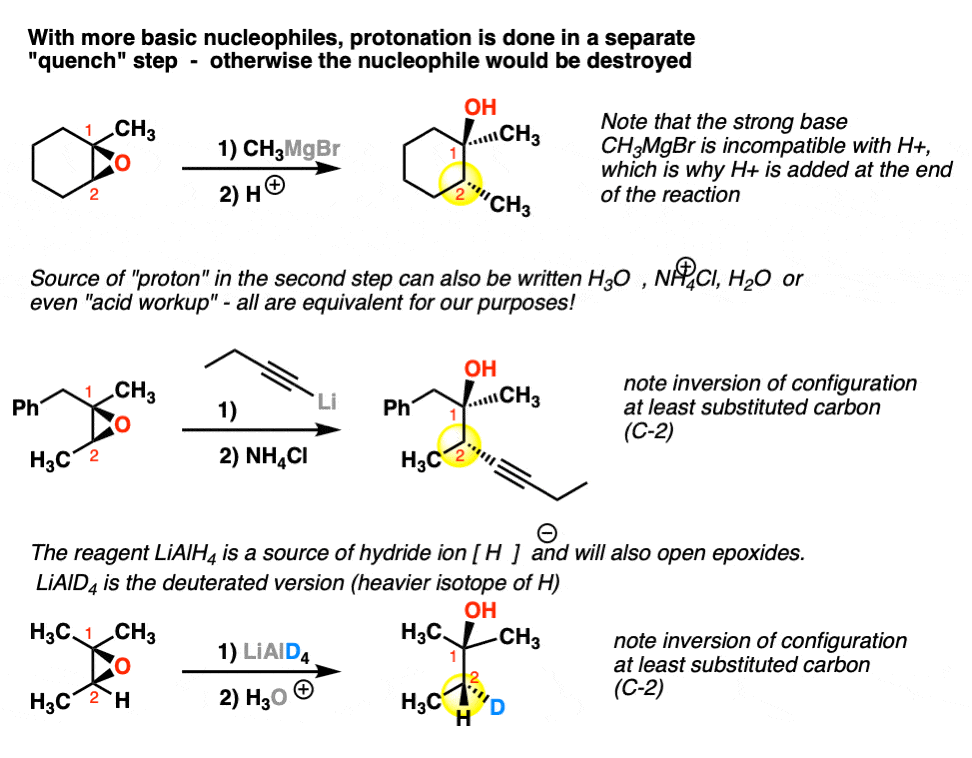
还有什么?(是的,还有其他的亲核试剂与环氧化合物反应,但它们很少见到在这个水平。但是我有补充道注1在底部]。
4所示。什么不工作:可怜的亲核试剂
就像任何年代N2反应,这个途径去工作,我们真的必须处理一个像样的亲核试剂。可怜的亲核试剂,尤其是中性物种像H2O,卢武铉,RCOOH是远远不够的。
为了使环氧化合物反应我们需要使用强酸性条件(适合弱的亲核试剂)或基本条件(HO - RO - RMgBr扶轮领导学院(RLi), LiAlH4)。

这就是探索环氧化合物和醚。但是我们还有很多谈论关于醇——当然我们没有完成年代的例子N1和年代N2反应。这是下一个。
在下一篇文章- - - - - -卤代烃与醇
笔记
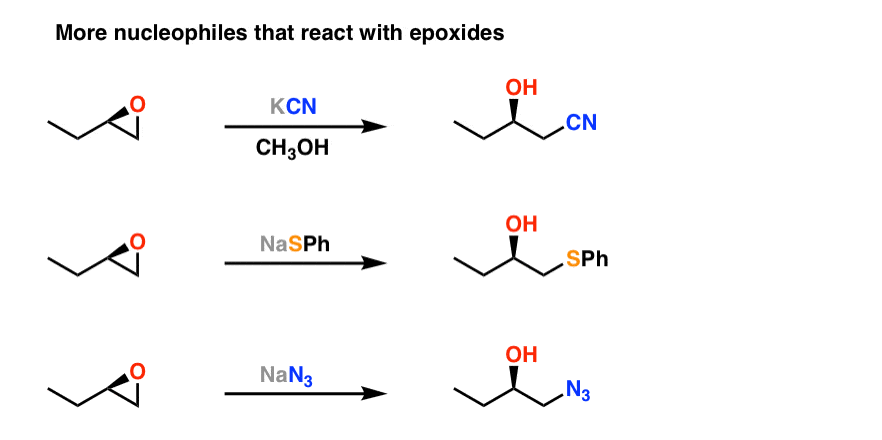
注1。一些其他的亲核试剂与环氧化合物反应,但很少出现在介绍有机化学。注意,第二个和第三个例子不显示来源的质子(氢离子),增加了氧气,但它可以添加在“淬火”一步。
(高级)引用和进一步阅读
- ——速度钠衍生品组合的酚类化合物与烯氧化物
大卫西曼博伊德和欧内斯特·罗伯特并线
j .化学。Soc。,Trans.,1914年,105年,2117 - 2139
DOI:10.1039 / CT9140502117
这篇论文以及随之而来的是早期的例子的环氧化合物开环醇盐。 - ——速度钠衍生品组合的酚类化合物与烯氧化物。第二部分
大卫西曼博伊德和多丽丝小姐Feltham托马斯
j .化学。Soc。,Trans.,1919年,115年,1239 - 1243
DOI:10.1039 / CT9191501239 - 环己烯亚胺
伊恩·d·g·沃森,尼古拉斯Afagh和安德烈·k·yudi
Org。Synth。2010年,87年,161年
DOI:10.15227 / orgsyn.087.0161
这个过程的第一反应有机合成与叠氮化钠氧化环己烯的开环。yudi教授显示,这个反应是一个有用的- h氮杂环丙烷的合成前体,环氧化合物的氮模拟。 - Dimethylmagnesium的反应和Diethylmagnesium环氧环己烷
保罗·d·巴特利特和男子气概的浆果美国化学学会杂志》上 1934年 56(12),2683 - 2685DOI:10.1021 / ja01327a045这是一个早期的例子与格氏试剂的环氧化合物开环。
- 立体化学的环氧开环烯丙基格氏试剂
休•Felkin乔治Roussi
四面体。1965年,6(46),4153 - 4159
DOI:10.1016 / s0040 - 4039 (01) 99581 - 4
这是一个更高级的(也许不那么相关),试图解决烯丙基Gringard试剂是否经过一个年代N2的反应。这可能是容易与同位素标记和解决13C NMR。 - 酸,base-catalyzed或位阻环氧开环反应
赫伯特·迈尔,Rainer Koschinsky、德将和Englbert Bauml
《有机化学》杂志上1987年,52(7),1342 - 1344
DOI:1021 / jo00383a033
一篇优秀的论文描述了不同的产品获得当打开一个阻碍在酸性和碱性条件下环氧化物。娃教授(LMU、德国)而著称,他非常严格的在物理有机化学工作,在那里他有发达的亲电性和亲核性量化尺度标准。
与铝环氧化合物开环醚是什么?
铝醚催化这个反应如何?
通过铝醚,你能说的具体些吗?你有一个具体的例子你的打算,还是指一个或多个例子的职位。
嗨,将会发生什么如果环氧反应与NaBH4 EtOH的存在,将NaBH4作为亲核试剂,然后EtOH接触吗?谢谢
一般NaBH4不是一个足够强的亲核试剂与环氧化合物反应。你需要一个更强烈的抗衡离子协调氧气。LiAlH4将工作。
NaBr在基本条件下工作吗?
通常不会。即使它会释放环应变,你会从一个非常弱碱(Br)到一个更强大的基地(O)如果溴离子打开了环氧化物。此外,即使那样,相反的反应就会很容易发生——回想一下,环氧化合物是由关闭deprotonated halohydrins !
//m.deriinvest.com/2015/01/26/epoxides-the-outlier-of-the-ether-family/
你真的需要一种酸的存在在halohydrin阶段停止反应。
当使用强碱的存在一个环氧等提供的示例中可以让E2反应发生而不是Sn2 ?不能一个醇盐deprotonate碳环氧毗邻,开始氧气和形成π键电子?
这确实可以发生!然而你,往往需要一个非常庞大的酰胺基的发生。霍奇森的工作很重要,在这方面,看这里:https://onlinelibrary.wiley.com/doi/10.1002/0471264180.or029.03
谢谢你这个漂亮的网站真的是生命的救星
如果对你有用,太棒了!
佳作先生。我想问LiAlH4在三氯化铝的存在,它能打破环氧?(我们没有最后一步布仑斯惕使质子化来源!)
和三氯化铝LiAlH4甚至是兼容的吗?我从没见过这两个试剂一起使用。
你好,很好地解释道。我有一个查询如果我想附加一个半胱氨酸glycidyloxypropyltriemthoxysilane使用氢氧化钠为溶剂?会工作吗?
base-promoted开口的环氧化合物与其他的亲核试剂我推荐你读迈尔斯的讲义。http://hwpi.harvard.edu/files/myers/files/25-transformations_of_23-epoxy_alcohols.pdf
你好詹姆斯,谢谢你!我想知道你能否帮我解决这个问题:我是一个新手在合成化学和我试图摆脱我的一些半缩醛环氧产品。我试着在酸溶液水解。结果环氧水解。你会建议任何可能帮助吗?
半缩醛本身应该消失,除非你有一个电负性很高的组毗邻羰基或如果你是形成一个环状半缩醛。这不是回答你的问题,但水解环氧的缩醛的存在是可能不会工作。您可能需要重新配置你的合成方案,也许保护酒精,这样它不会在第一时间形成半缩醛。
你怎么打开一个环氧与氢氧化钠反式是两个手性中心,?
我不确定如何回答你的问题没有图。如果你正在寻找选择性开放两个环氧化合物,与氢氧化钠,将很难实现,除非有明显的空间或电子偏好倾向于攻击与另一个。
如何反应的环氧化合物1,2环氧环己烷与PCl5说? ?如何接近他们,请一定要告诉. .
这不是真正的打开的环氧基。那里,你试图协调环氧亲电磷氧,形成瞬态离子对释放氯离子和打开环氧化物。超出了我们的范围的处理。
你好,
我有一个产品从oxido-reductase酶,我怀疑有环氧基团,而不是另一种类型的氧化。我做过核磁共振和质谱符合环氧假说,但是我真的很想用另一种方法来确认。这个网页已经有帮助。我想做的是甲醇分解反应。我的计划是在干燥的甲醇溶解使冻干后的化合物。然后准备1 N H2SO4溶液在干燥的甲醇,并添加足以导致最终的0.2 N H2SO4浓度。该标签的环氧甲基组。根据下面的纸应该是1 h后在室温下完成的。
然后我可以用气相色谱-质谱,分析结果和/或核磁共振。
我不是一个核心有机化学家,我想知道如果我忽略的东西。
你好,
我是一个机械工程师,我的化学知识很差,抱歉提前,如果我的问题是愚蠢的。我进行实验并附上一些聚合物链胺组与环氧基团的表面不需要做任何特殊的配置,只是在磷酸钾缓冲(PH值7.4)。现在想象一下,在一个点,我想禁用环氧团体和停止我的聚合物链之间的任何反应,表面(也许通过关闭环氧环? ?)而我的聚合物链仍然存在。我的问题是如果这是可能的,如何?
谢谢
谢谢
詹姆斯,我怀疑是环氧乙烷环怎么开放的a音的唱名和三氯化铝(亲电试剂)。
错误的”溶剂的作用“第一个例子…第一个方程应该氢氧化钠,而不是NaOR。
这可能是一个愚蠢的问题。从我的理解,对于一个环氧,取代碳将承担更多的正电荷。为什么不亲核试剂进攻更多取代碳呢?它与位阻的东西吗?
嗨——不是一个愚蠢的问题。你是对的,代替碳越多将承担更多的正电荷。然而,当我们有一个相对强亲核试剂(如RO、HO、格氏试剂,或LiAlH4)什么是更重要的是位阻。
把它像SN2反应,至少取代碳反应最快。
当涉及到一个较弱的亲核试剂(例如水),我们需要添加一个酸催化剂。在这种情况下,反应主要发生在碳最能稳定正电荷。在这方面它有点像SN1反应,尽管它仍然发生反转的配置。
希望这可以帮助!詹姆斯
亲核试剂是RO -或哦?
在这种情况下吗?它可以是,根据条件。
优秀的帖子!
我有一个疑问。如果我试图添加一个叔醇不对称环氧化物。因为他们是最弱酸性醇,他们会遵循一个基本机制(sn2) ?结果将取决于所使用的溶剂或中等?他们甚至在第一时间反应吗?如果他们做了,他们会更愿意接受切断债券乳沟从而形成稳定的碳正离子?我很困惑,这将是一个很大的帮助如果我能得到这个了…
谢谢
这篇文章涵盖了环氧化合物与基地。添加一个中性叔醇不属于这一类。你需要形成的共轭碱叔醇——比如说,例如,t-butoxide钠。钠t-butoxide至少可以作为亲核试剂进攻环氧的取代位置和打开它,就像其他醇盐。
碳正离子不相关讨论,因为他们不会在这些基本条件下形成。