有机反应的底漆
3因素,稳定的碳正离子
最后更新:2023年6月16日|
碳正离子:属性、形成和稳定
- 碳正离子是缺电子物种和一个空的p轨道
- 缺乏一个完整的八隅体和轴承一个正电荷,他们相当高能(即不稳定)瞬态物种和经常遇到的中间体在许多化学反应。
- 三个主要因素增加碳正离子的稳定性:
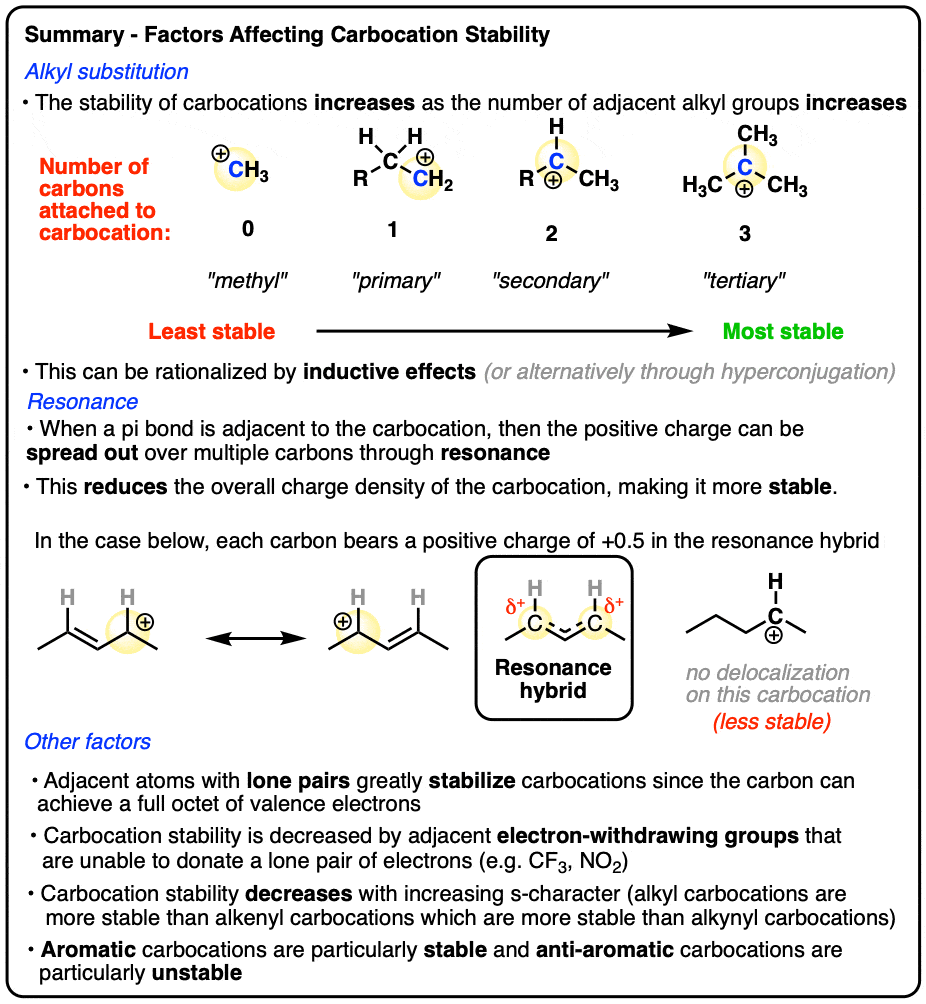
- 增加的数量相邻碳原子:甲基(最不稳定的碳正离子)< <二次<三级(最稳定的碳正离子)
- 相邻π键,使碳正离子p轨道的共轭pi-system系统(“移位共振”)
- 相邻原子与孤可以提供完整的碳八隅体。
- 相邻电子撤回组无法捐赠孤对(例如CF3,没有2)大大减少碳正离子的稳定性。
- 此外,碳正离子减少在稳定的秩序烷基(最稳定)>烯基>炔基(不稳定)
- 一些额外的碳正离子稳定性影响因素,包括芳香性/ antiaromaticity、平面化(桥头堡不稳定的碳正离子)和特殊案件小戒指。
表的内容
- 什么是碳正离子?
- 形成碳正离子
- 稳定的碳正离子的因素——替换
- 稳定的碳正离子的因素——共振
- 应用碳正离子稳定性理解的反应
- 稳定的相邻
- 更重要的——共振或替换吗?
- 归纳影响
- 一些特殊情况
- 总结
- 笔记
- 测试你自己!
- (高级)引用和进一步阅读
1。什么是碳正离子?
一个带正电的碳原子轴承三个共价键和空轨道称为碳正离子(或者更正式,“carbenium”离子,尽管对于我们的目的,我们将使用“碳正离子”(注1])
除了负责+ 1中央碳,绝大多数的结构和性能注2碳正离子的相似的中立硼化合物。

碳正离子和中性硼化合物一般都有
- 一个sp2杂化中心原子
- 6个价电子,
- 一个空的p轨道,
- 三角形的平面几何
- 和键角为120°。
(我们怎么知道呢?x射线晶体学注3]
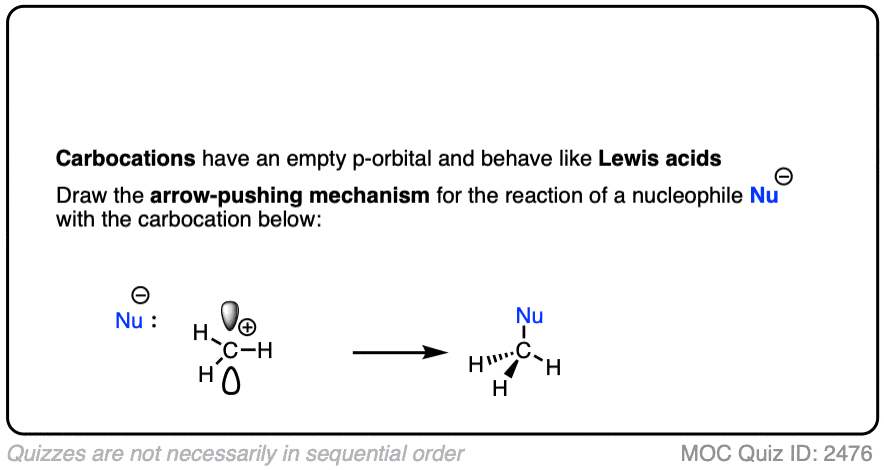
像硼化合物,碳正离子,路易斯酸,容易缺电子结合刘易斯基地,导致一个四面体,sp3杂化原子与一个完整的电子结构。
看看你能不能画的曲线箭头下面的反应。
 点击翻转
点击翻转
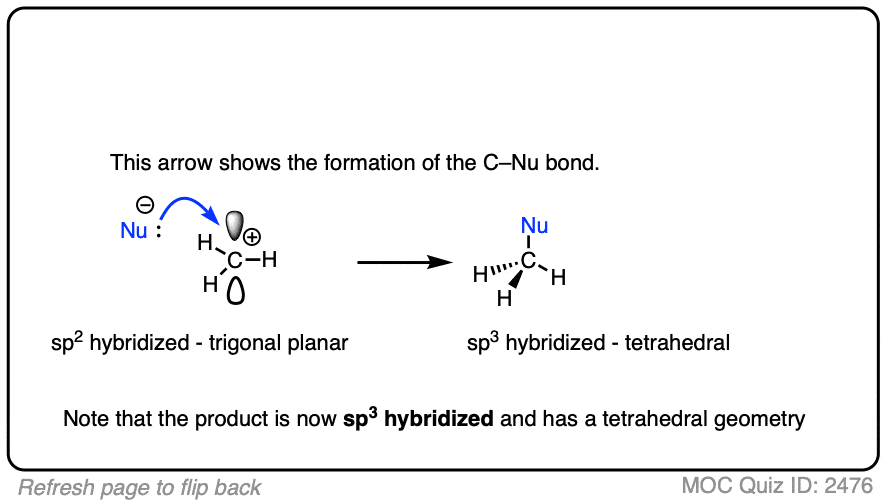
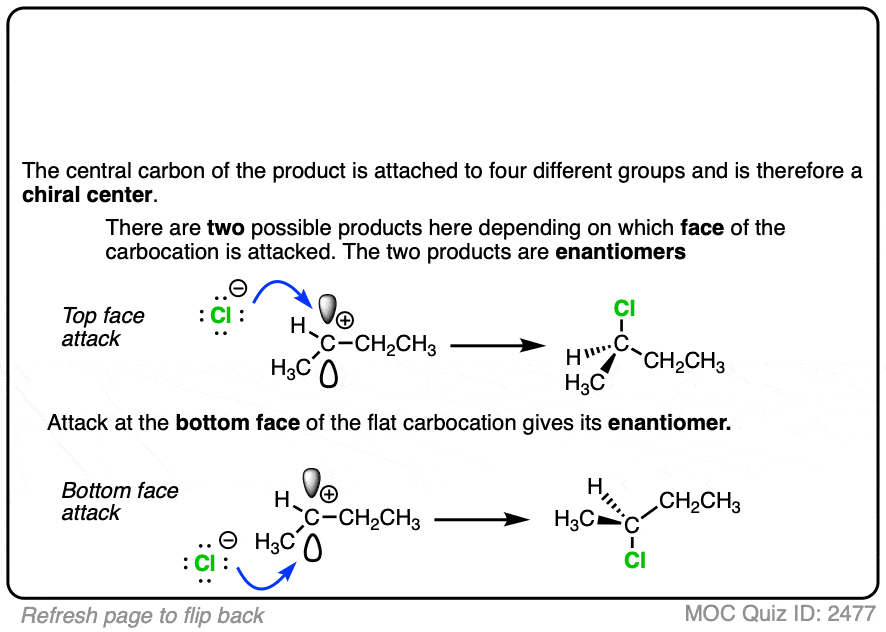
由于他们的三角平面几何,碳正离子可以进行攻击的空的p轨道。
保持警惕的情况下,这可能导致一对立体异构体。
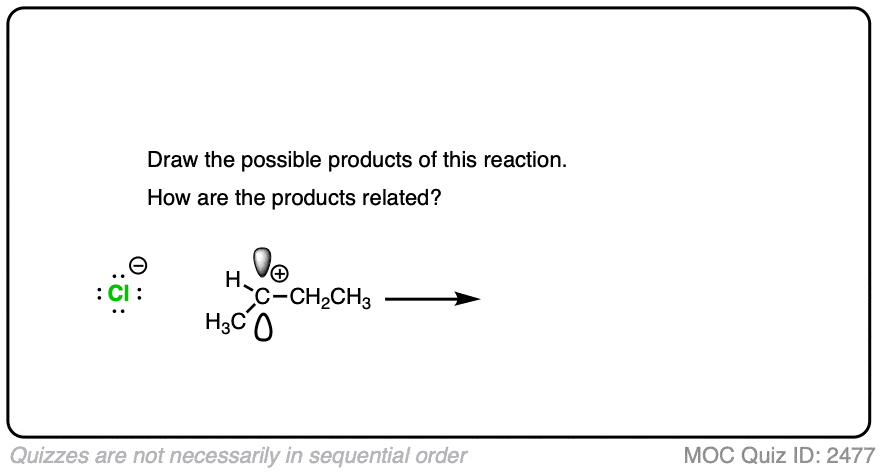 点击翻转
点击翻转
2。形成碳正离子
碳正离子是重要的中间体在许多反应。(一个中间,而不是一个过渡态,是一种潜在可孤立的物种在反应和反应坐标图中占据了一个势能最低。转型国家部分债券,寿命极短,不能孤立的)。
缺乏一个完整的八隅体的电子在碳和轴承一个正电荷,在能源和更不稳定的碳正离子高于中性碳化合物。
一些知名反应涉及碳正离子中间体是添加氢卤化物(例如哈佛商业评论,盐酸,你好)烯烃和单分子的替换N1)和消除(E1)的反应烷基卤化物。
在这个年代N1 /E1反应,第一步是失去好离去基团(一般来说,一个非常弱的基础——见“是什么让一个好的离去基团”)碳正离子。这通常发生在一个高度H等极性溶剂2O或乙酸可以帮助稳定碳正离子中间体。
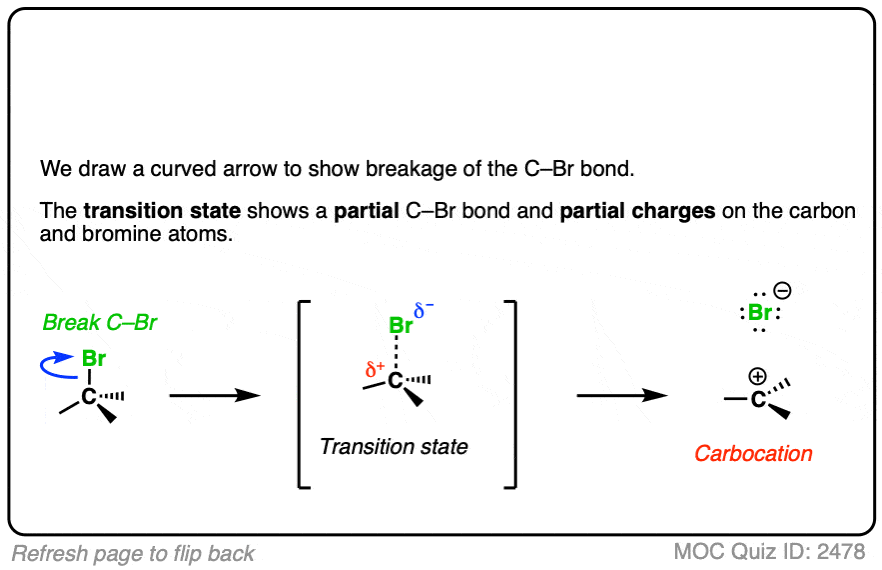
看看你是否能画出曲线箭头从这个三级碳正离子的形成烷基卤化物和过渡态:
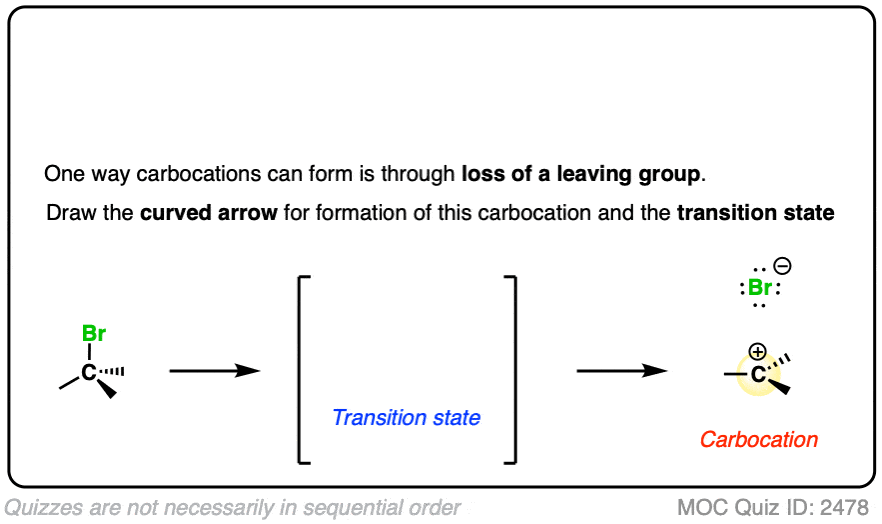 点击翻转
点击翻转
在添加hydrohalic酸烯烃,第一步是攻击的H +对碳碳π键电子的碳正离子中间体。
看看你是否能画出曲线箭头推动机制和反应的过渡态:
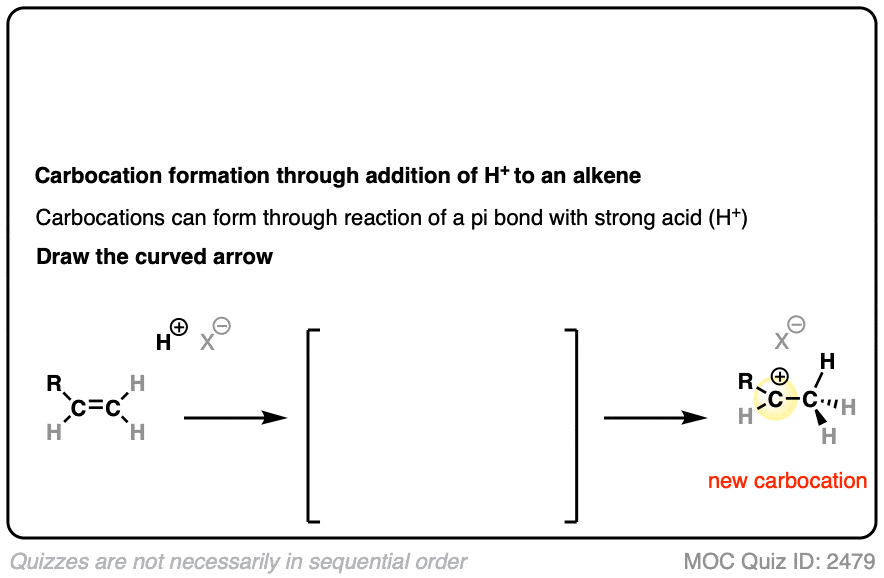 点击翻转
点击翻转
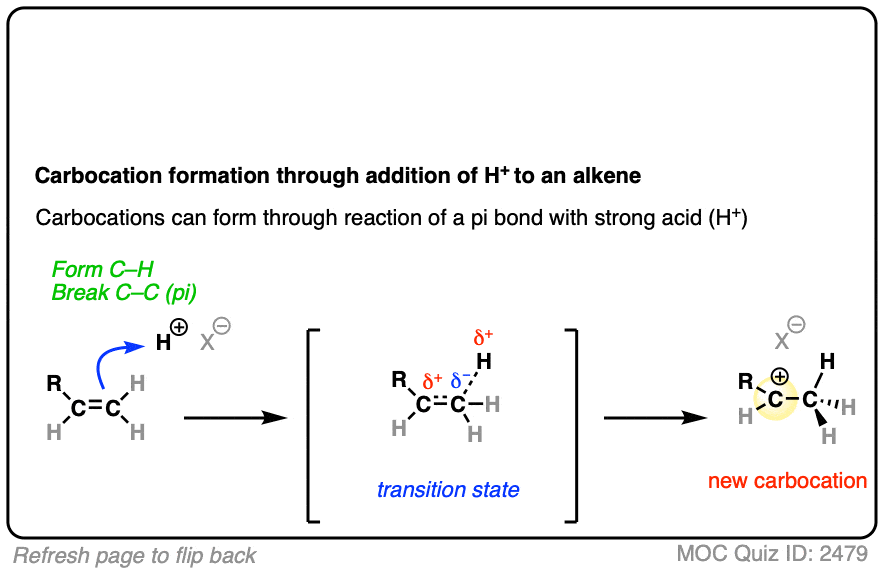
在这两种反应,我们从一个相对低能起始物料,途中经过一个高能过渡态的碳正离子中间体。
在第二步中,然后碳正离子的反应路易斯碱在解决方案给产品碳四面体和sp3杂化。
草图的反应坐标这两个反应看起来有点像这样:
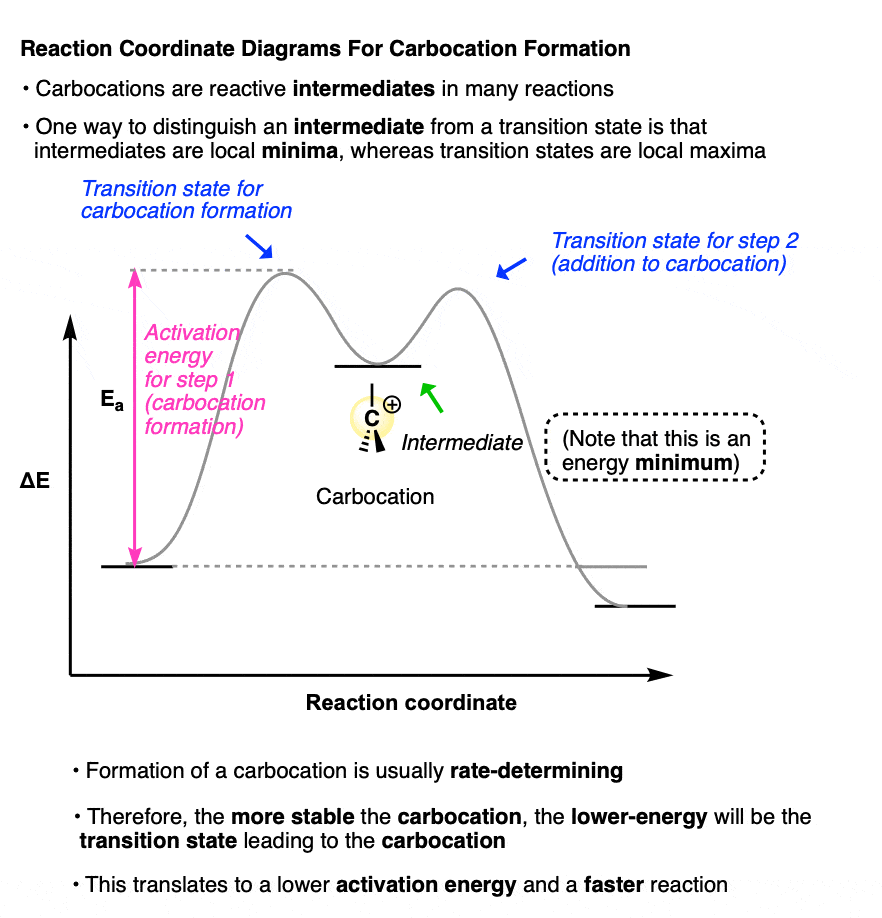
(注意,碳正离子中间占据了一个当地的最低在这个反应坐标图;当地两个过渡状态maxima)。
为什么把这个了?
因为速率决定步骤为每个这些反应形成的碳正离子中间。
的更稳定的碳正离子中间低能源的过渡状态,导致碳正离子,转化为低活化能和一个更快的反应。
因此,如果我们理解管理的因素稳定的碳正离子,那么它也将帮助我们理解为什么某些反应发生迅速而别人不!
3所示。稳定的碳正离子的因素——替换
实验测量了稳定(注意4碳正离子的显示了以下趋势:
甲基(不稳定)< <二次<三级(最稳定)
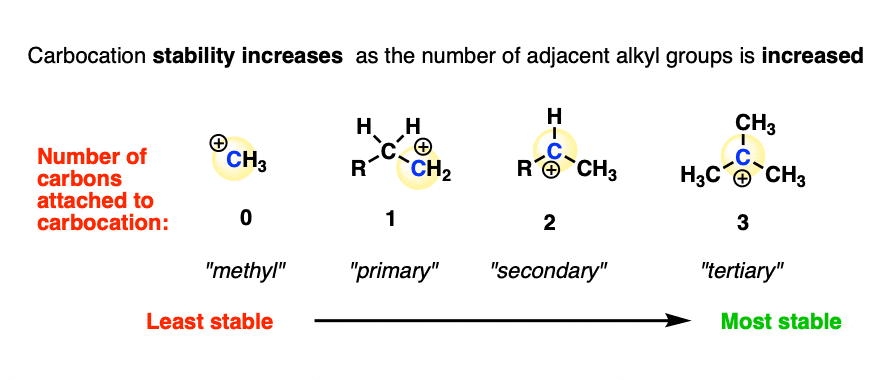
换句话说,碳正离子稳定性增加碳氢键取代碳碳键。
为什么?
electron-poor,碳正离子稳定通过捐赠从邻近的电子密度电子的原子。
正如我经常告诉我的学生,“当你贫穷,它有助于有丰富的邻居”。
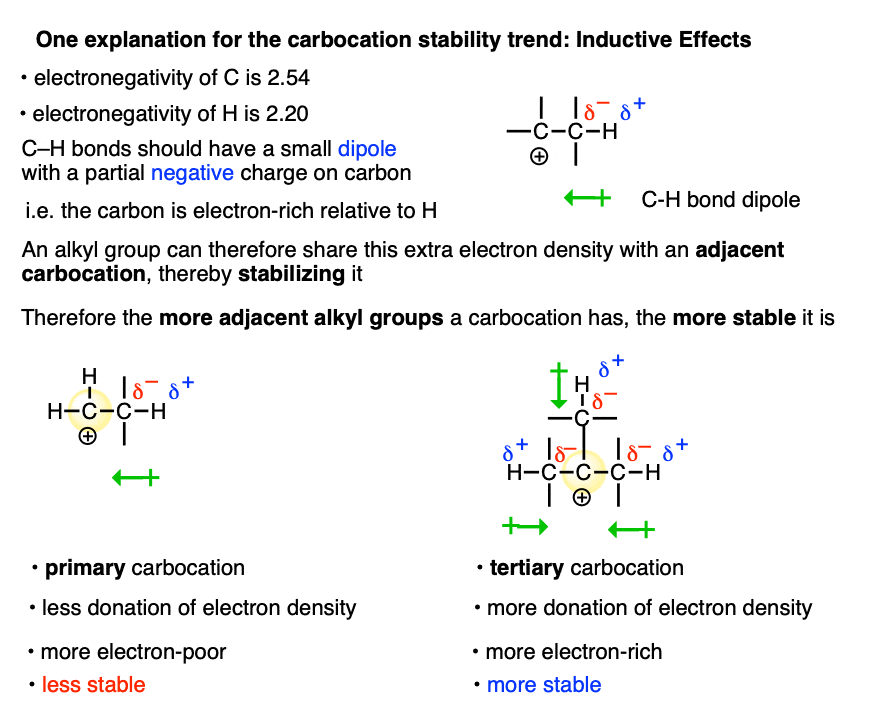
合理化这一趋势的一个方法是通过应用电感的影响。
碳比氢电负性(2.54)(2.20)。所以碳氢键熊小偶极子即碳部分负面和氢部分是积极的。
电子密度从多个碳氢键偶极子可以添加。所以的碳烷基集团将有一个小的部分负电荷可以捐赠给邻碳正离子,减少electron-poor。
这不是可能的碳正离子时是直接连接到H。
一个更令人满意的(一些!)解释来自超共轭现象。
想象中的两个电子排队碳氢键(或碳碳)σ键的空的p轨道碳正离子。然后想象一种“共振”,这些电子共享与p轨道形成π键(H +)。
由于电子密度被捐赠给一个空轨道,这应该是稳定空的p轨道(即碳正离子)。
我们没有空间在本文中进入所有超共轭现象的影响在本文中,但它确实使一些实验证明所证实的实验。(注3——adamantyl碳正离子的结构是非常有益的]
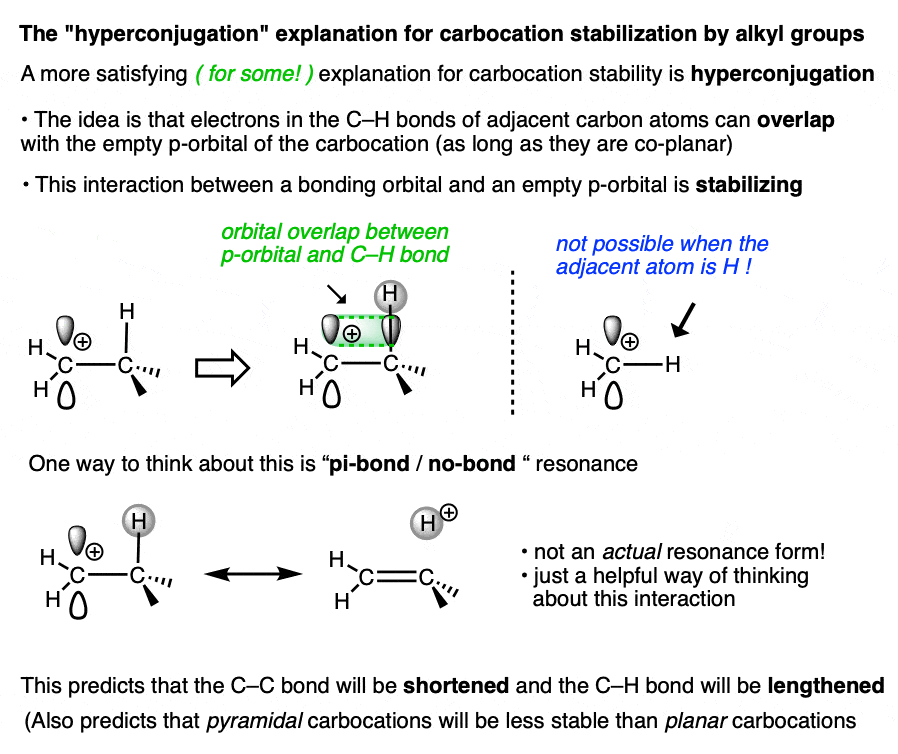
不管你喜欢什么合理化,观察到的趋势是相同的。的更多的代替的碳正离子,更大的它的稳定。
4所示。稳定的碳正离子的因素——共振
有机化学中是一个良好的工作原则集中充电通常是更多的不稳定(高能)比稀释负责(低)注5]
一个地方我们以前见过的概念极化率,一个大阴离子喜欢碘(-)比小的更稳定的离子像F(-)由于负电荷分散到更大的体积。(这是负责更大的酸度的因素设定h和氢氟键也越大离去基团我的能力(-)]
另一个因素导致这种“扩散”的指控是“共振”。
等碳正离子n丙基阳离子(CH3CH2CH2+),正电荷局部单一碳。
但如果一个π键相邻碳正离子,我们可以画两个共振形成正电荷的颈- 1上或颈- 3。
共振混合,正电荷之间共享这两个碳原子,每有一个电荷密度+ 0.5而不是+ 1。(这是是什么意思“共振移位”——电荷被涂抹在多个碳)
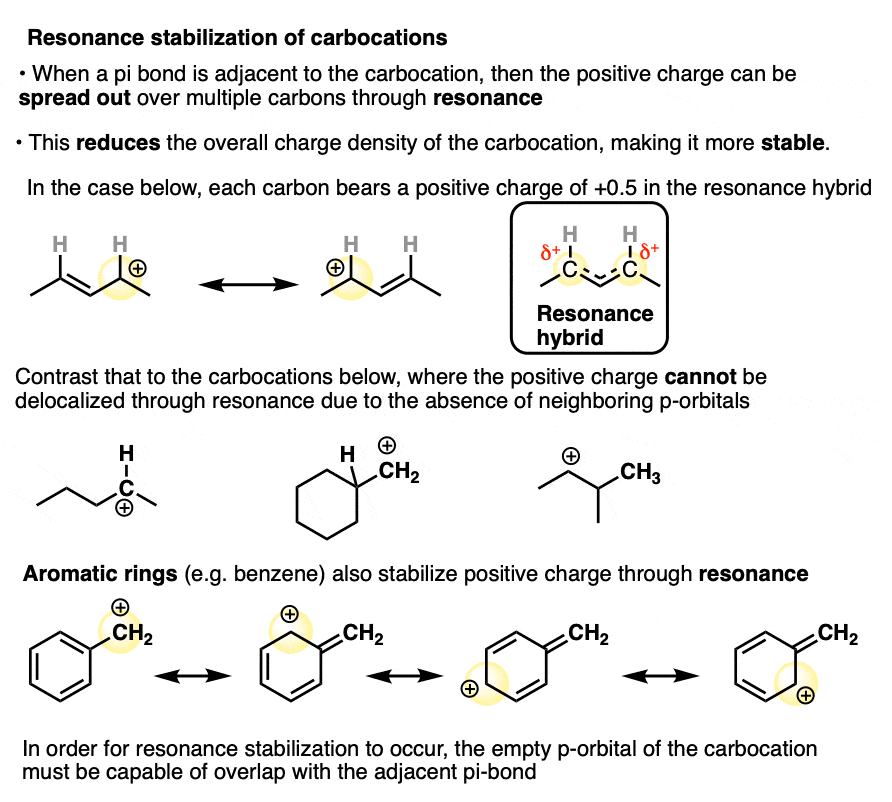
更加稳定的碳正离子(被称为烯丙基阳离子)相对于父丙阳离子被众多测量证实。(注意4]
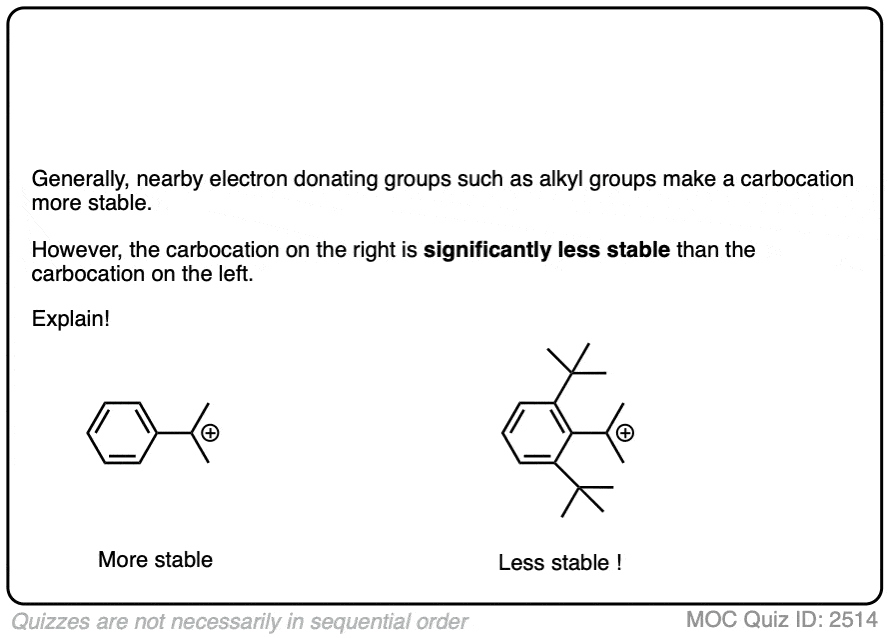
时也会出现类似效果等一个芳环碳正离子是邻苯。碳正离子的稳定性,被称为苄碳正离子远比“正常”的主要碳正离子。(事实上,苄叔丁基阳离子碳正离子是基本稳定的,注意4)
碳正离子的稳定性往往会增加潜在的共振形成的数量增加。
例如,“三苯甲基”阳离子,Ph3C(+)非常稳定,它形成一种结晶盐,可以放入一个瓶和无限期地存储在一个架子上。
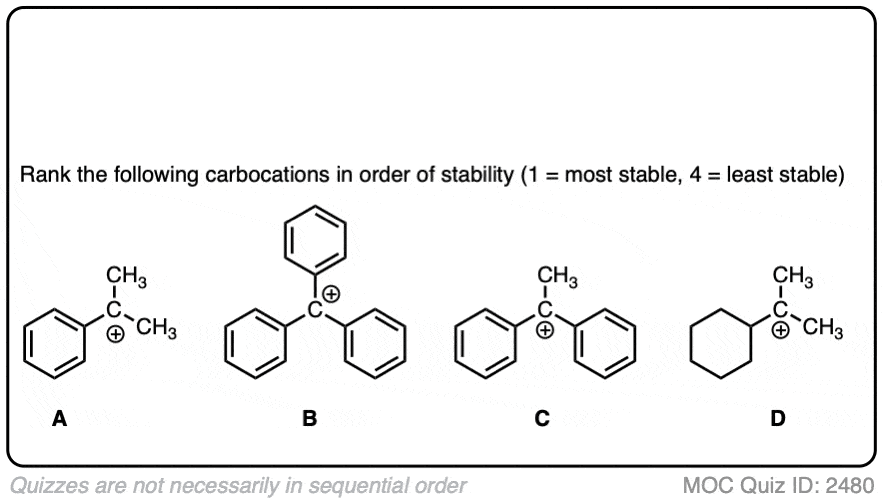 点击翻转
点击翻转
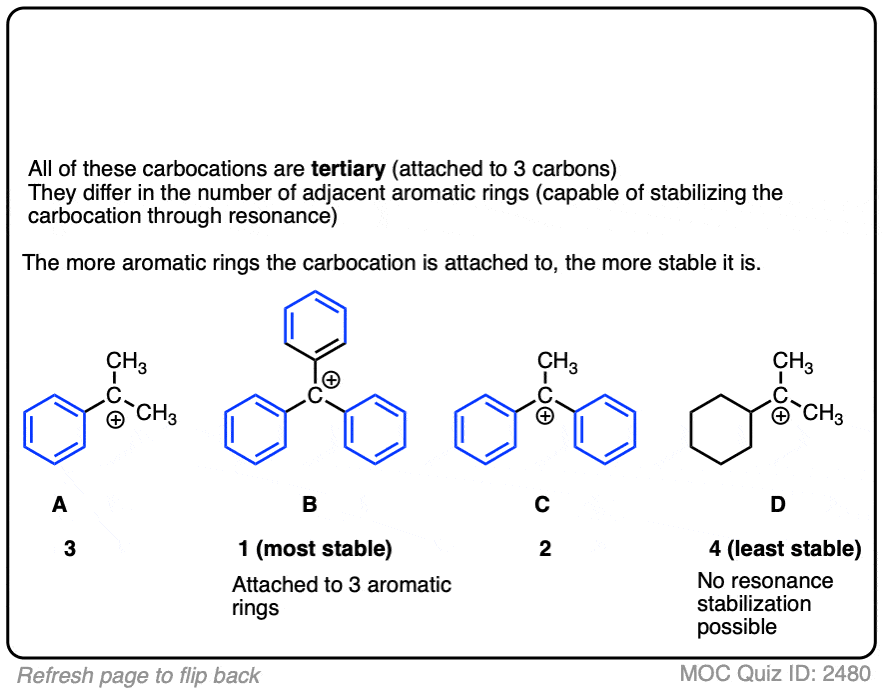
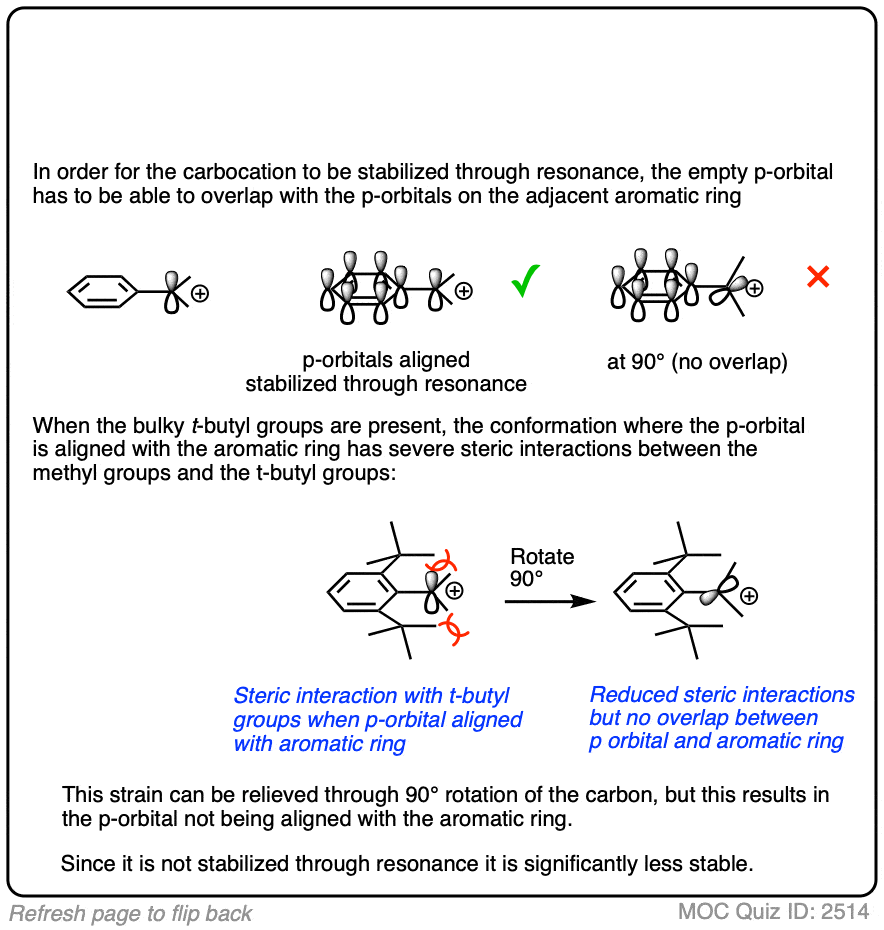
一个字的警告。为了稳定的碳正离子共振,碳正离子的p轨道必须可以重叠的p轨道相邻的π键。(见文章-结合和共振)
没有重叠意味着没有移位,这意味着不添加稳定。
测试你对这个概念的理解通过回答下面的小测验。
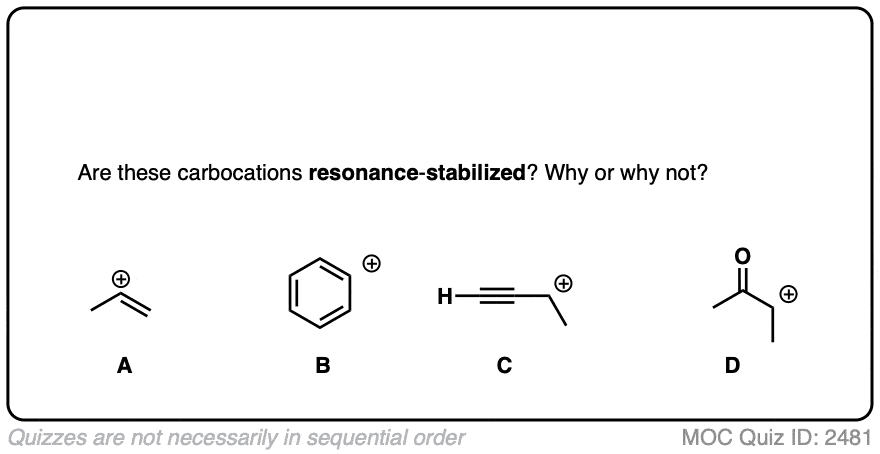 点击翻转
点击翻转
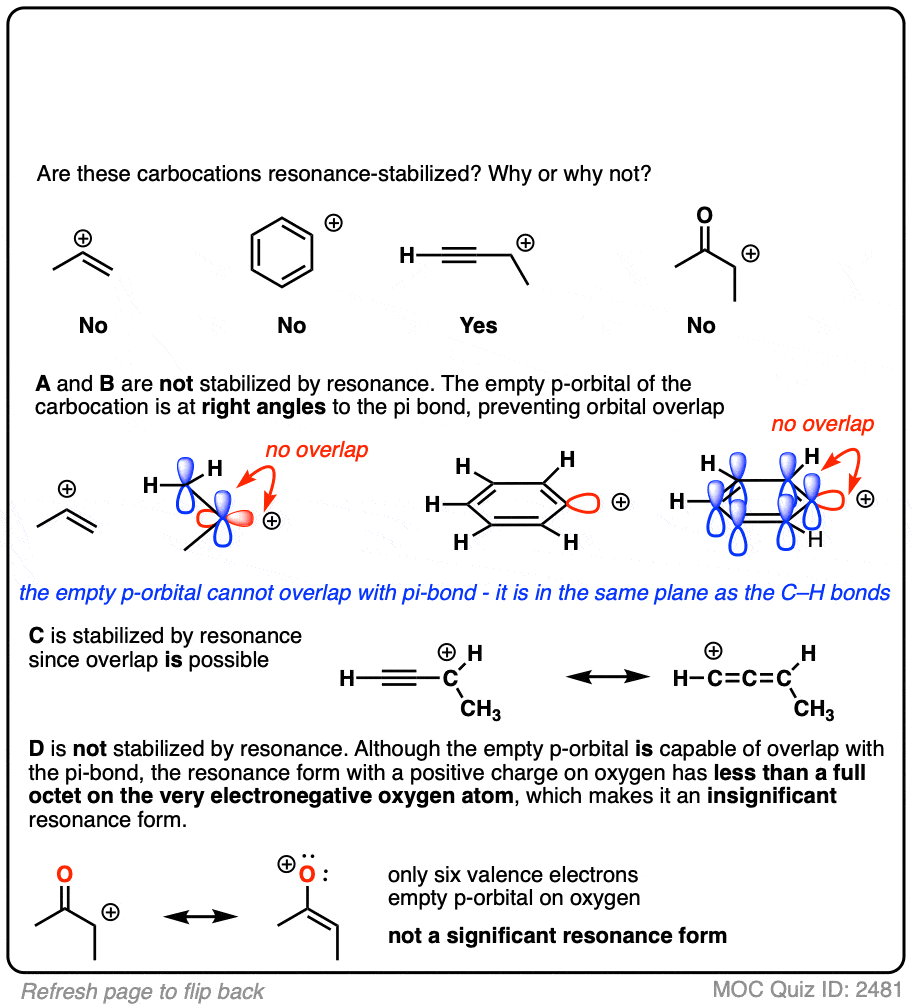
一个常见的错误是认为直接附加到一个π键共振稳定的碳正离子。这不是如此!π键必须相邻碳正离子。
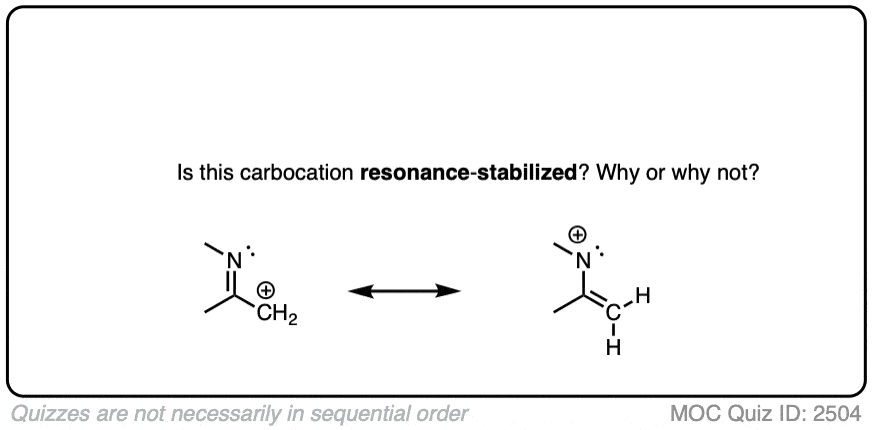
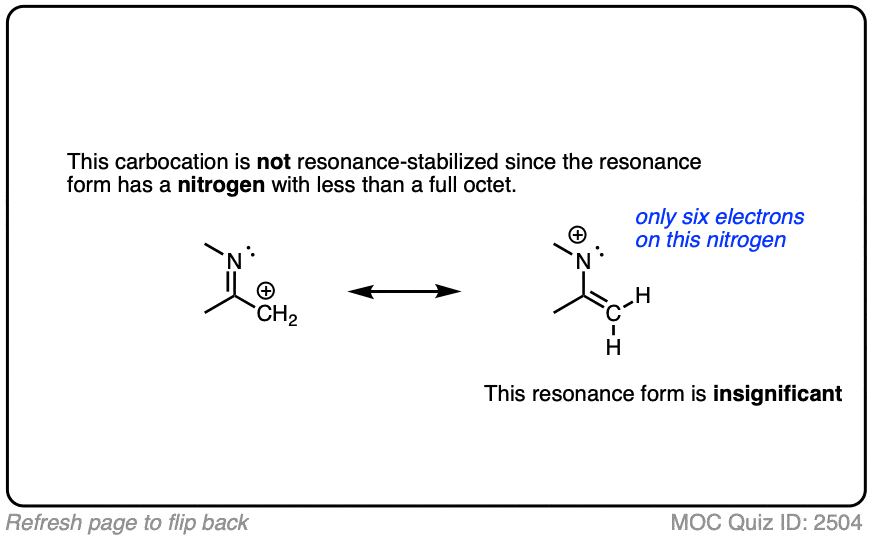
另一个潜在的反直觉的情况是当碳正离子毗邻一个C = O(或C = N)债券。有人可能会天真地认为稳定的碳正离子的共振。
然而,如果你画出共振形成的时候,你会发现在形成碳碳π键和打破切断π键,最后形成一个缺电子的氧物种只有6个价电子。这“共振”是高能,基本上没有贡献共振杂化。
(高电负性原子像O在稳定优秀的负电荷,但他们是可怕的在稳定空轨道)
5。碳正离子反应的稳定的重要性
让我们回到碳正离子的作用在几个重要的有机反应中间体。
反应的速率决定步骤如下质子化作用与H +π键的碳正离子中间体。
你认为这两种反应的更快呢?
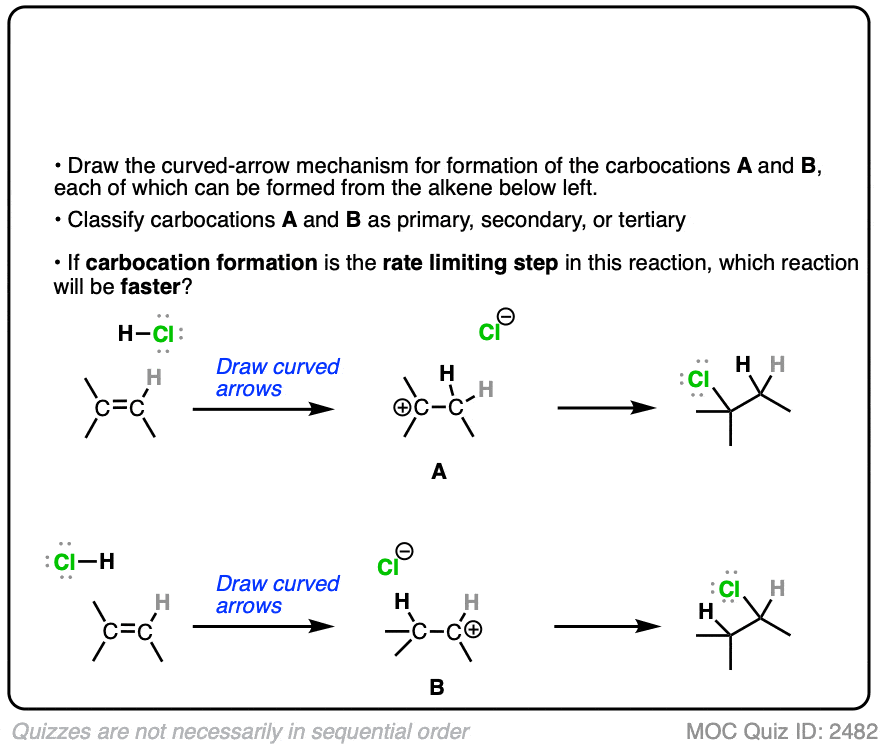 点击翻转
点击翻转
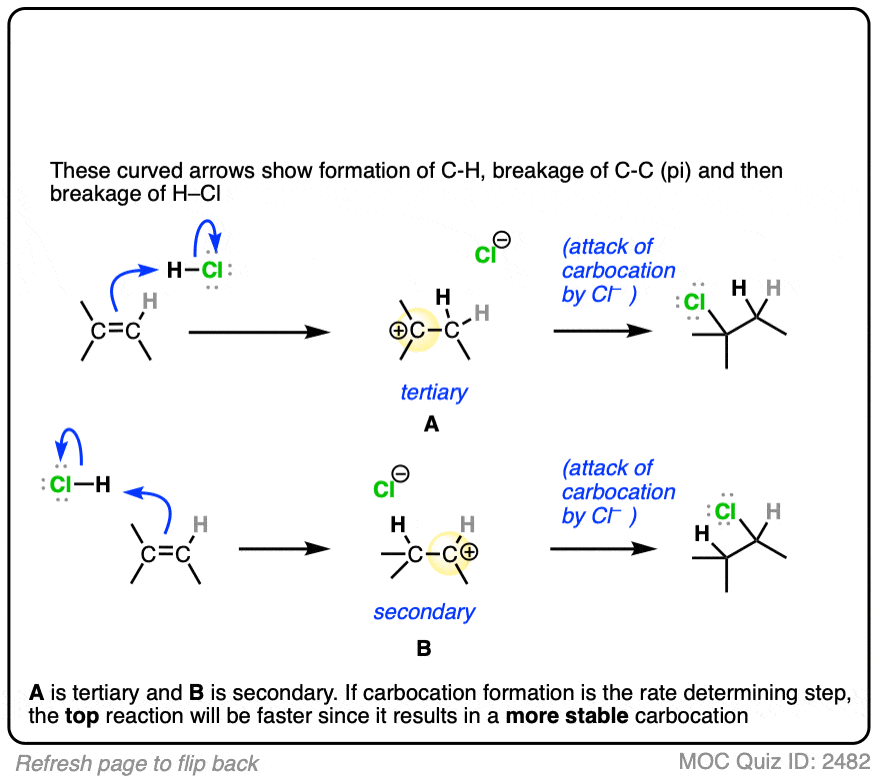
如果你回答正确,恭喜你!你显示你理解背后的原因马氏规则的像!(见文章-马氏规则的像]
让我们看看另一个。
反应的速率决定步骤下面是失去离去基团形成碳正离子。
这两种反应收益更快呢?
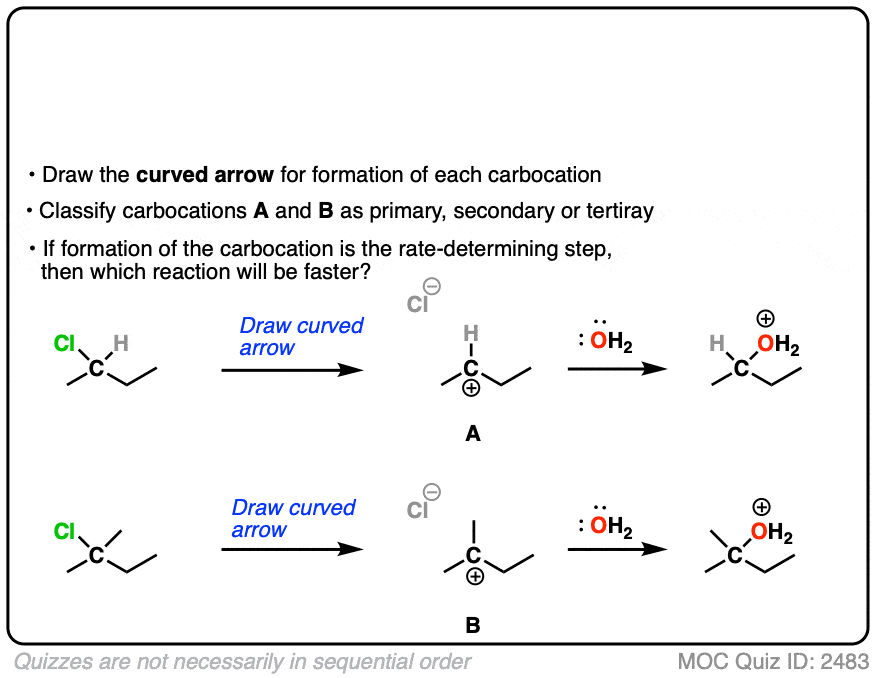 点击翻转
点击翻转
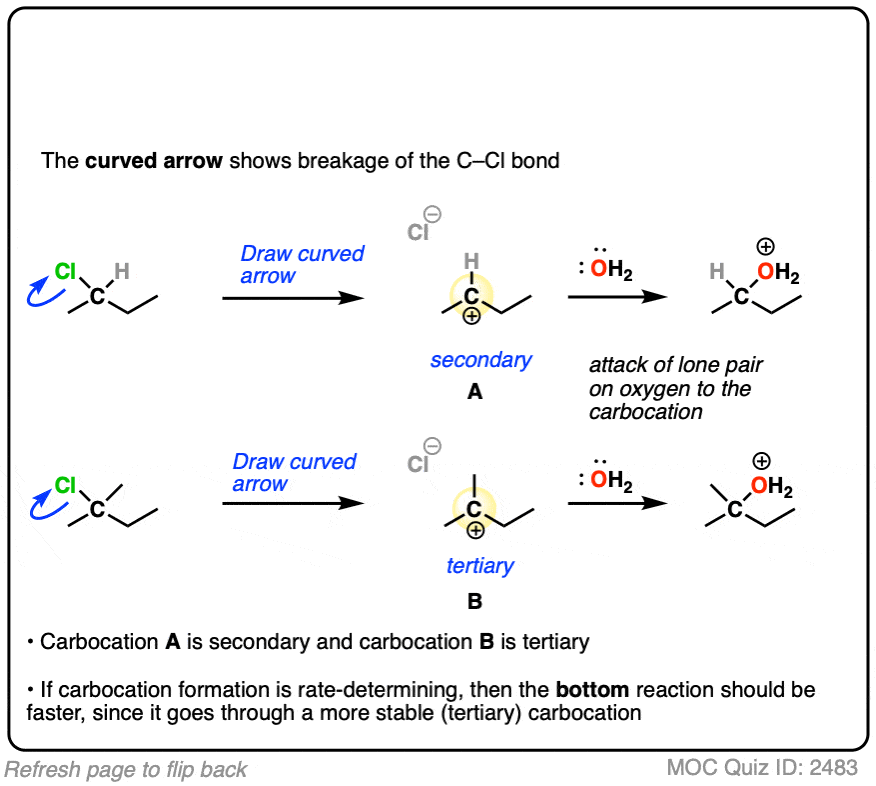
如果你回答正确,你刚才表现出的理解的关键因素之一,去决定是否将通过年代进行反应N1,年代N2,E1或E2。(见文章:SN1 SN2 / E1 / E2 -底物)
6。稳定的碳正离子的因素——邻孤
的另外一个因素是稳定的碳正离子,我们还没有涉及到。
如果形成碳正离子相邻一个原子轴承一个孤对(即路易斯碱),那么原子可以捐出其对碳正离子的电子,在这个过程中形成一个新的π键。
这就是所谓的“pi-donation”(见文章-π捐赠)
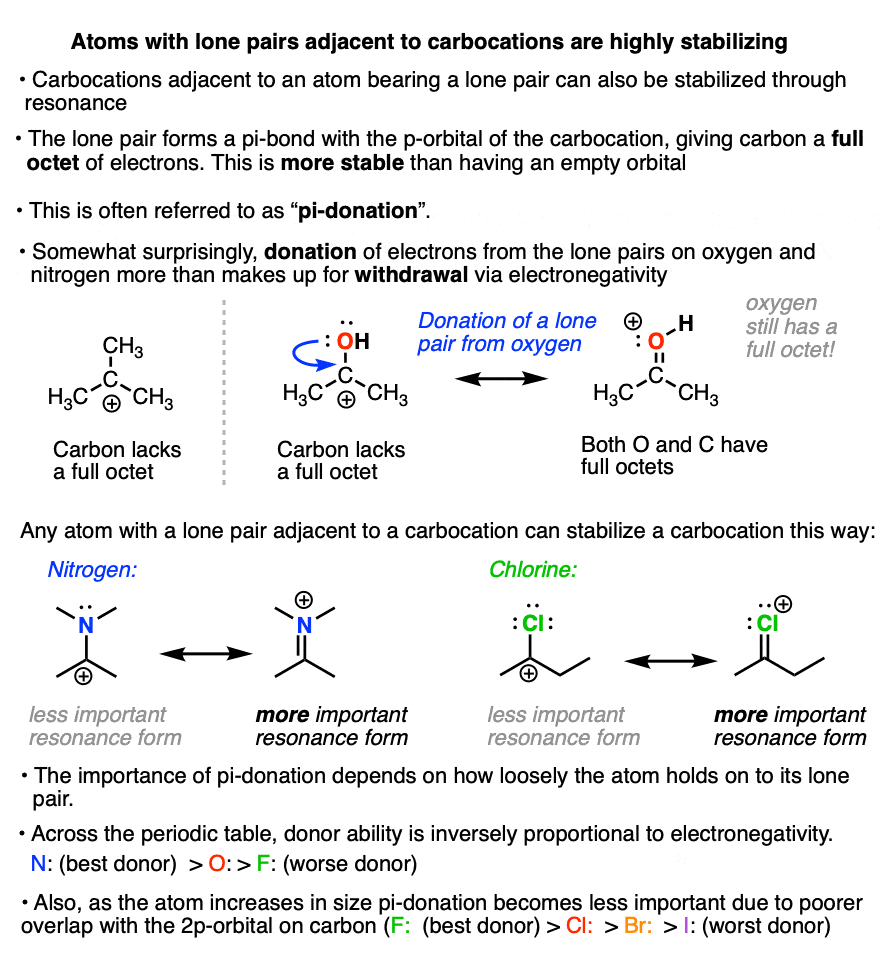
似乎有点反直觉的,高电负性很高的原子氧或氮可以稳定的碳正离子。
但pi-donation的净结果是所有原子都有一个完整的八隅体,这是高度稳定。(注意,即使氧和氮将承担正式的+ 1,他们仍有完整的八隅体的电子!见文章-如何计算形式电荷)
在多大程度上原子的孤对稳定一个相邻的碳正离子正比于其碱度。更基本的原子,pi-donor越好。
在一行的元素周期表,捐出一对电子的能力是电负性成反比。因此,所有其他因素不变的情况下,一个孤对氮将更稳定的孤对氧气,这是比一个孤对氟更稳定。
会下来元素周期表,原子的能力捐赠一对电子与原子的价层轨道的重叠与空碳2 p轨道。
一般来说,随着轨道大小的增加,轨道重叠(和pi-donation能力)减少。
因此氟pi-donor碳比氯,pi-donor比溴,比碘(在碘价层轨道是5 p和5 s轨道,不匹配的小2 p轨道的碳)。
这是一篇关于碳正离子的稳定性,我想保持专注,但是这个部分的内容是非常重要的,并将一次又一次地出现在有机化学。一个应用程序稍后您将看到-亲电芳香取代。
7所示。哪个因素更重要——替换或共振?
我们有两个因素影响碳正离子的稳定性:替换(一级、二级、三级)和共振。
那么哪个更重要呢?
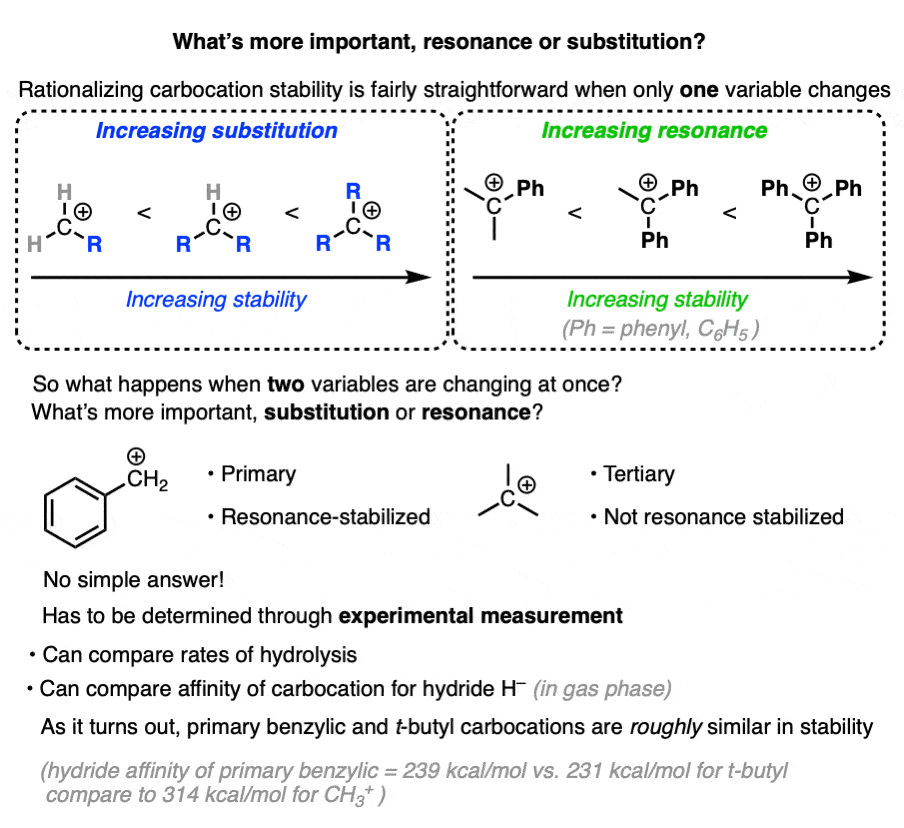
“他们这两个这个问题重要”是我non-answer。
实际的回答这个问题的方法是观察实验结果。
测量碳正离子稳定性的一种方法是采取一系列相关的烷基卤化物和测量率极性质子溶剂条件下的水解SN1可能会。
(这种方法的优点是,它更接近实际的反应条件。一个缺点是,它只适用于碳正离子下能够形成年代N1条件。)
另一种方法是所谓的测量氢化物亲和力——通过碳正离子的反应释放的能量相当于氢化物离子(H- - - - - -)。(尽管这可以应用到更大范围的碳正离子,只适用于气相)。
主苄基的碳正离子的氢化物亲和力是239千卡每摩尔与231千卡每摩尔t丁基碳正离子,所以这是非常类似的能源。
桌子下面的一些值。看到注意4。
8。一些因素破坏碳正离子
自电子基组有助于稳定的碳正离子,合理预计,吸电子集团将会破坏碳正离子。
,正如我们上面提到的,原子的电负性与孤独的对像O, N,和F直接附加到一个碳正离子会帮助稳定通过pi-donation碳正离子。
我不会考虑这些“吸电子集团”的目的。
我将包括“吸电子集团”
- 碳原子上吸电子集团(例如CF3CCl,3)
- 电负性原子没有孤(例如NR3(+))
- 包含一个π键的原子电负性更强原子(如C = O, CN,没有2,所以2R,等等)。
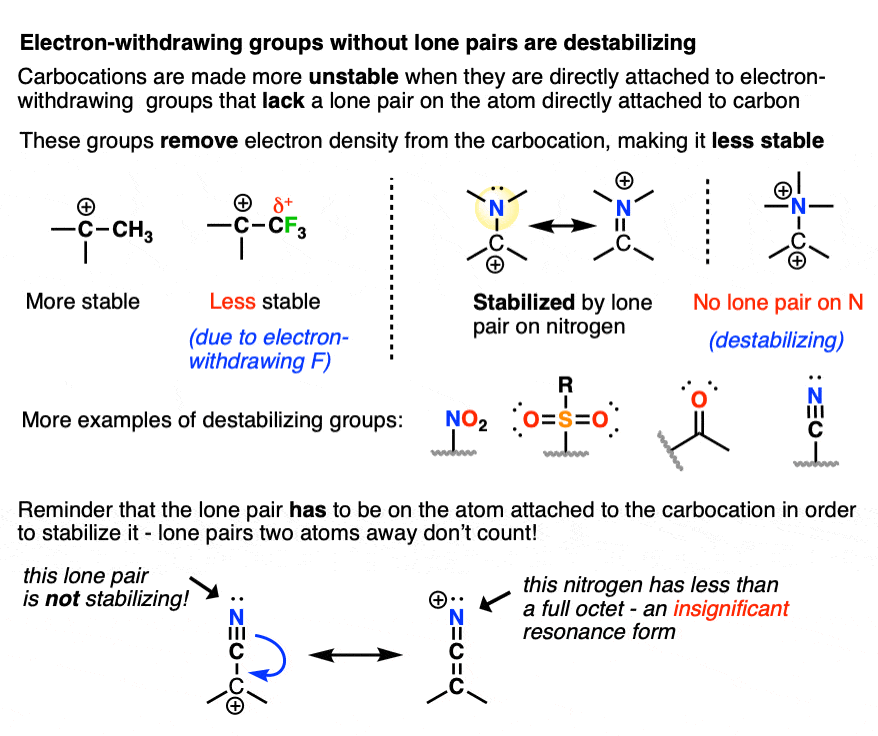
另一个因素,造成碳正离子是提到的碳原子的数量。
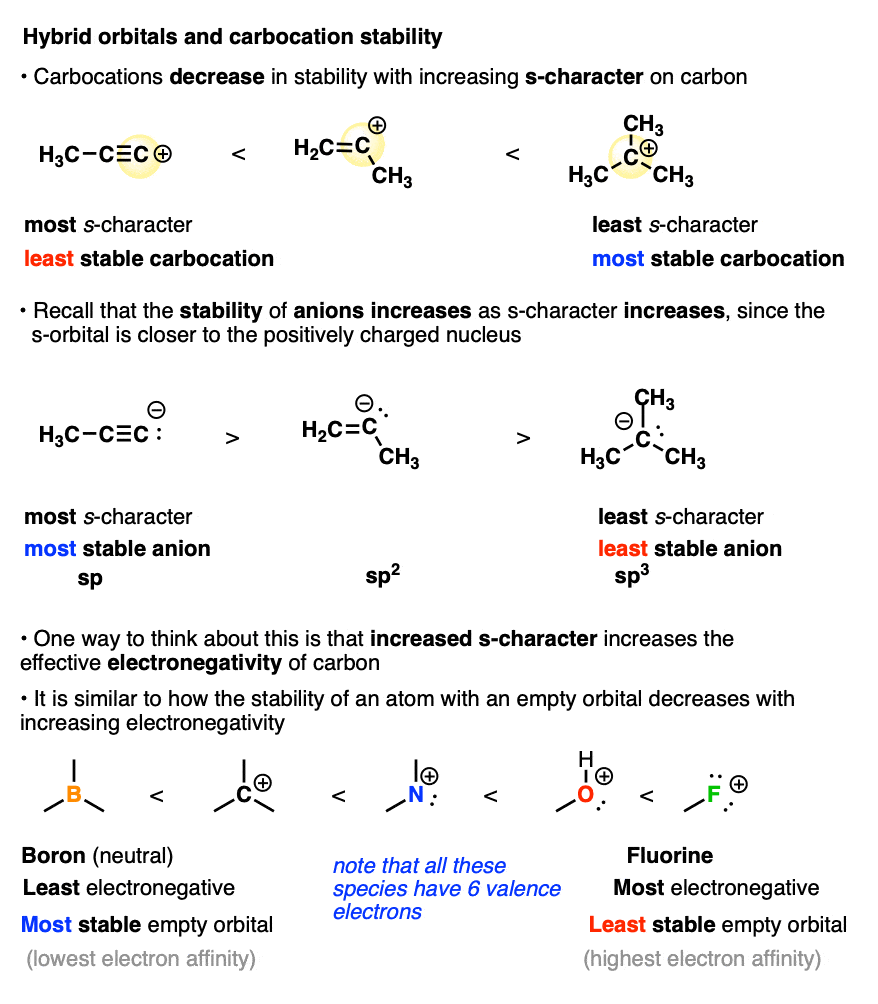
您可能还记得,炔烃碳氢键尤其酸性因为他们的sp轨道提到50%,由于s轨道是带正电的原子核,这有助于稳定的负电荷共轭碱(碳水化合物阴离子)。
嗯,当涉及到碳水化合物的稳定阳离子,这一切都被扔进反向。
提到碳正离子的越多,越接近空轨道是带正电的原子核。这使碳核的影响有一个更有效的电负性。删除一条电子形成碳正离子随着提到的增加变得越来越困难。(这可以量化通过测量氢化物亲和力或电子亲和能)
桥头堡碳正离子也特别不稳定是因为他们不能达到理想的三角形平面几何,(注6)碳正离子在小环(如环丙基阳离子和环丁基阳离子)。(请注意7]
9。一些特殊情况
为了完整性我们应该提到的最后一个因素,更多的是当日的主题,但有一个非常大的对某些碳正离子的稳定性的影响。
一些分子特别稳定的财产被称为芳香性。(见文章-芳香性规则)
一个相关的现象称为antiaromaticity负责不同寻常不稳定某些化合物。(见文章-Antiaromatic化合物和Antiaromaticity)
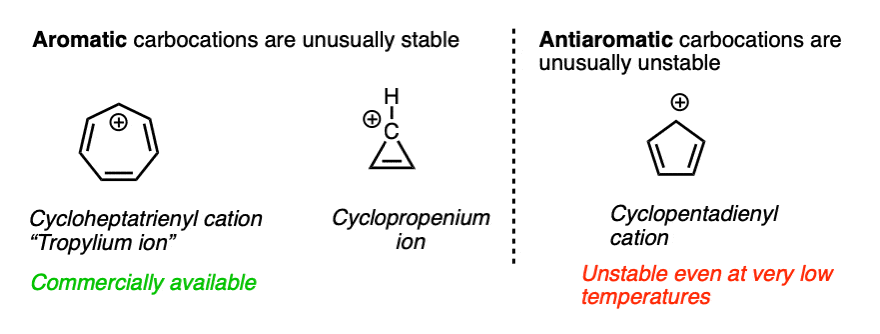
heptatrienyl(卓鎓)阳离子,C7H7+是芳香由于其不寻常的稳定,形成一个稳定的盐,可以放进一个瓶子和销售商业。cyclopropenium离子C3H3+还芳香和异常稳定。
另一方面,环戊二烯基阳离子,显然应该共轭系统,实际上是anti-aromatic小心控制的条件下,只有一个短暂的存在在非常低的温度。
10。总结
带正电的碳正离子,six-electron碳原子和一个空的p轨道。他们在许多反应是重要的中间体,高活性向刘易斯基地。
稳定的碳正离子的三个关键因素:
- 首先,他们是由相邻的稳定烷基组,可以捐赠缺电子碳原子的电子密度。
- 其次,他们可以通过共轭π键,稳定正电荷可以通过共振离域。
- 第三,稳定的碳正离子原子的孤对能力形成一个π键。
缺电子,碳正离子稳定的强吸电子取代基不能提供电子对(例如CF3C = O)。他们也不稳定,如果他们无法达到理想的三角形平面几何,它可以发生在桥头堡碳正离子。出于类似的原因,碳正离子的高度紧张的戒指环丙烷和环丁烷等往往是很不稳定的。
笔记
注1。在大多数情况下,“碳正离子”是指碳三键和一个空轨道,在绝大多数情况下,使用这个术语。年长的文献中有很多不一致是否这些都是“阳碳”或“carbenium”离子。隔离的CH5(+)物种极强的酸溶液的研究小组乔治Olah南加州大学领导IUPAC定义术语“碳正离子”作为三价碳和“阳碳离子”作为five-coordinate碳。(裁判]。
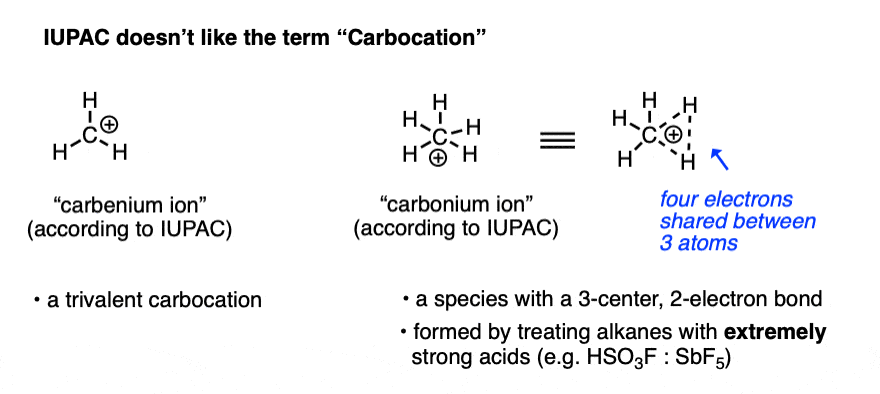
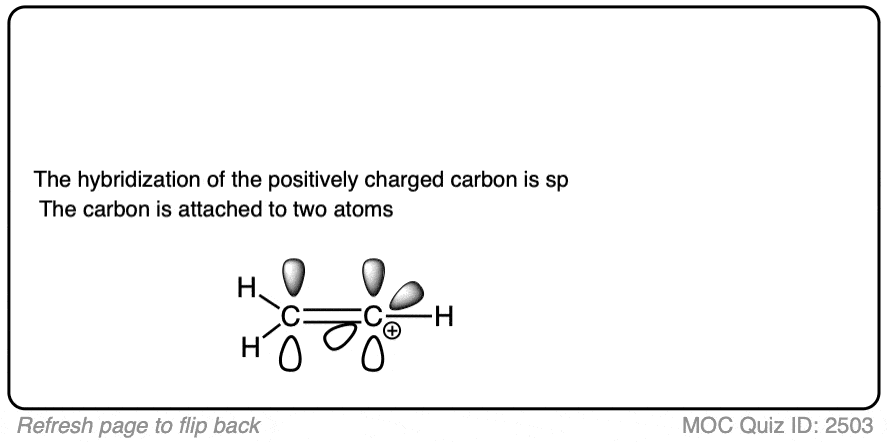
注2。两个著名的例外乙烯基碳正离子和acylium离子。
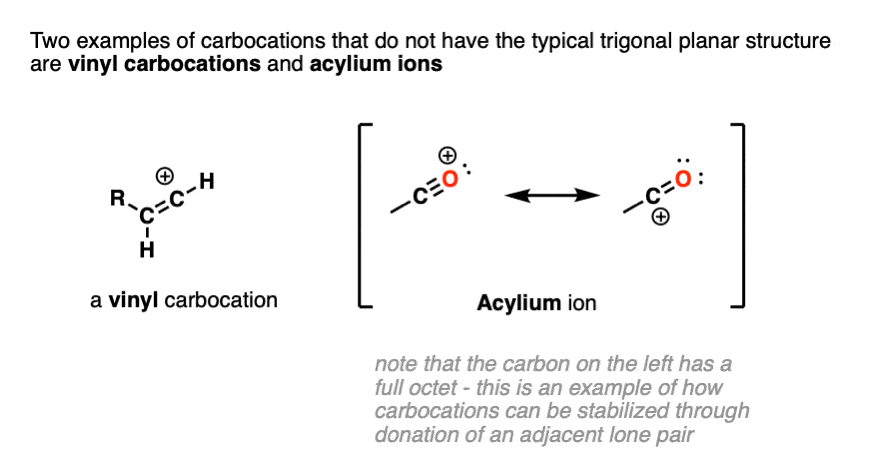
请注意,乙烯基碳正离子有线性几何和中央碳sp-hybridized。
acylium离子是一个很好的例子,一个稳定的碳正离子通过捐赠的孤对相邻。(acylium离子的例子,请参阅- - - - - -弗里德工艺品烷基化和酰化)。
例如,的结构t丁阳离子显示了一个三角形的平面结构(债券角度120°)碳碳键的长度为1.44埃(裁判]大概是介于典型碳碳单键(1.50)和碳碳双键(1.40)
adamantyl阳离子的结构是特别有趣的。在金刚烷,所有碳碳键大约相同的长度(1.53)。然而,在adamantyl碳正离子,直接连着碳正离子变得大大短(1.43),而碳碳键能与碳正离子的p轨道重叠明显长(1.608)。
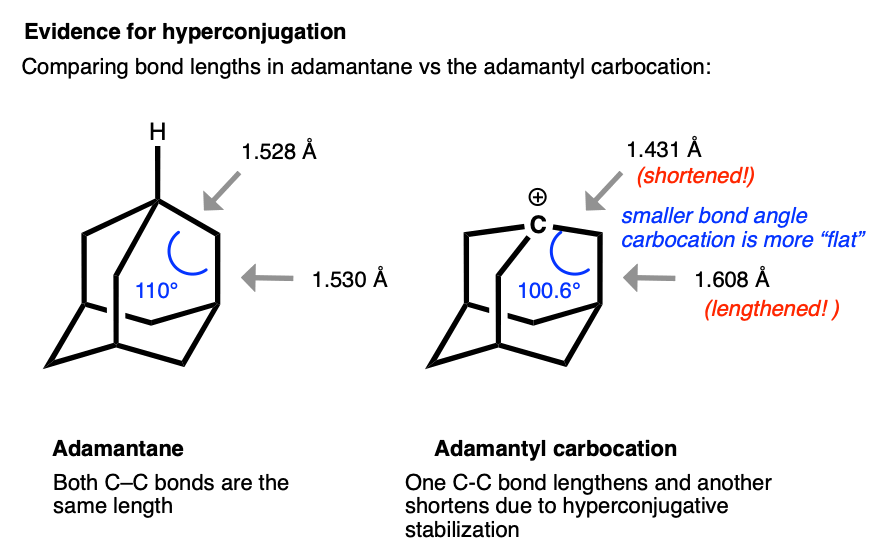
这正是我们预测使用超共轭碳正离子稳定性模型,其中一个碳碳键收益部分双键性格和另一个键是削弱。
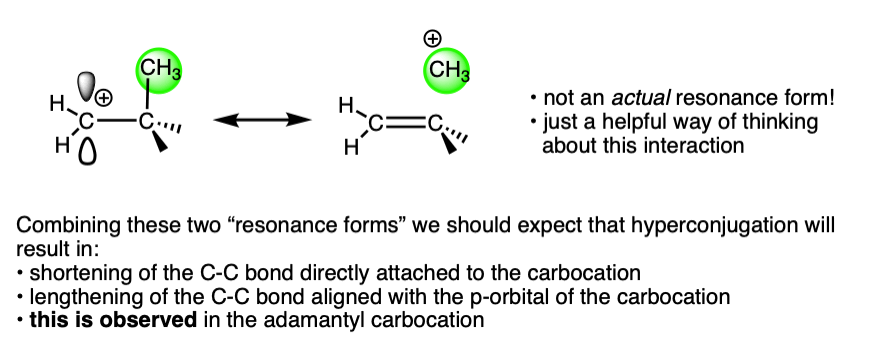
为更多的细节,我强烈推荐讲座30从教授大卫·埃文斯的先进的哈佛大学有机化学206链接在这里。
注4。量化碳正离子的稳定性的一个方法是通过测量他们的氢化物相似,也就是说,释放的能量在氢化反应碳正离子的离子。大量碳正离子的氢化物亲和力测量气相(他们寿命更长)。
下面提供了一个选择:
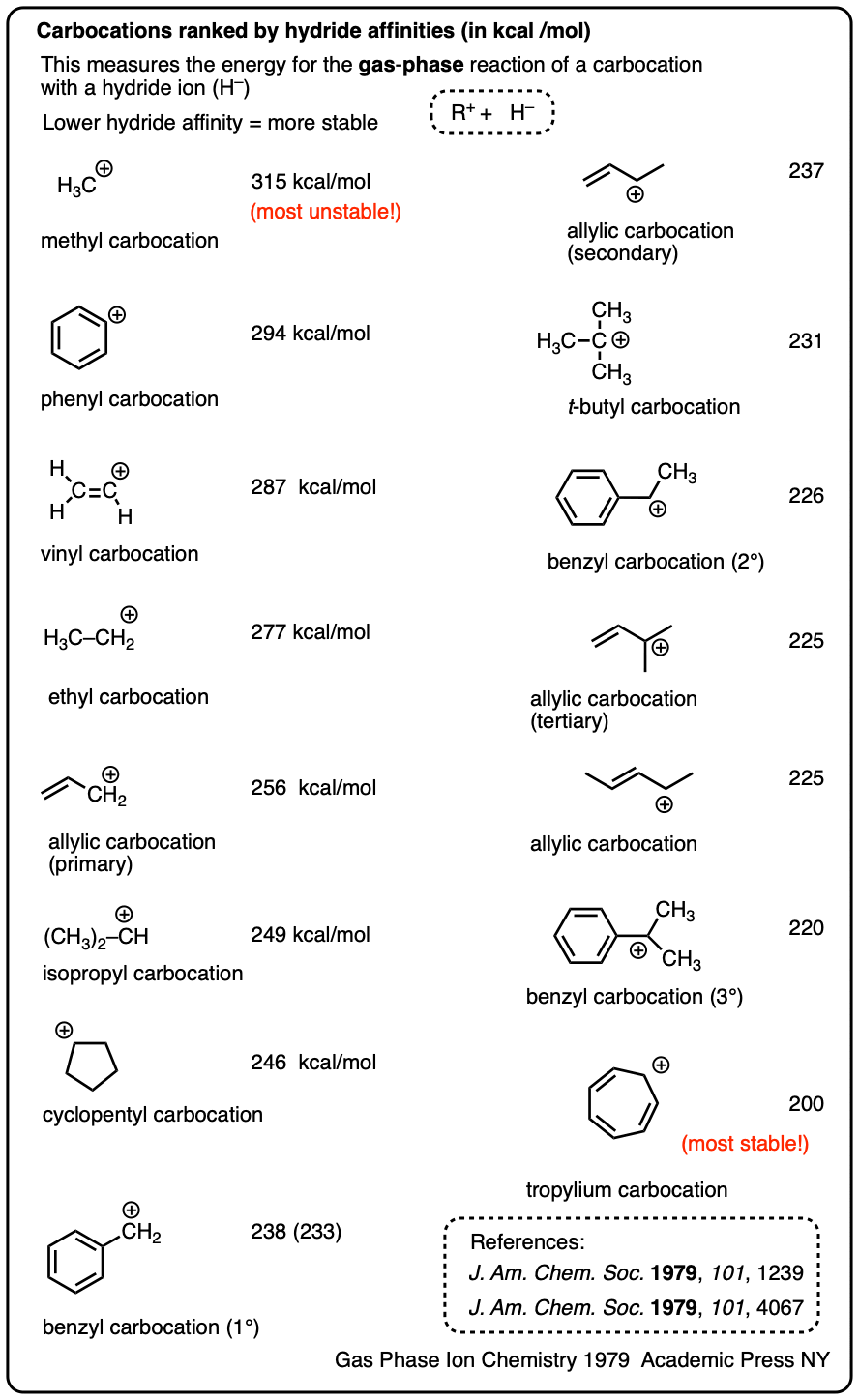
液相氢化亲和力也被测量的一些更稳定的碳正离子(括号中的气态氢化物关联性)
- Ph值3C(+): 96千卡每摩尔
- Ph值2CH(+): 105千卡每摩尔
- PhCH2(+):118千卡每摩尔(238千卡每摩尔)
- 卓鎓离子:83千卡每摩尔(200千卡每摩尔)
注5。形成碳正离子容易等溶剂介电常数高的水或羧酸(如乙酸、甲酸)。
注6一类三级碳正离子特别不稳定的碳正离子是限制在一个桥头堡。环应变阻止这些碳正离子采用三角形平面几何。
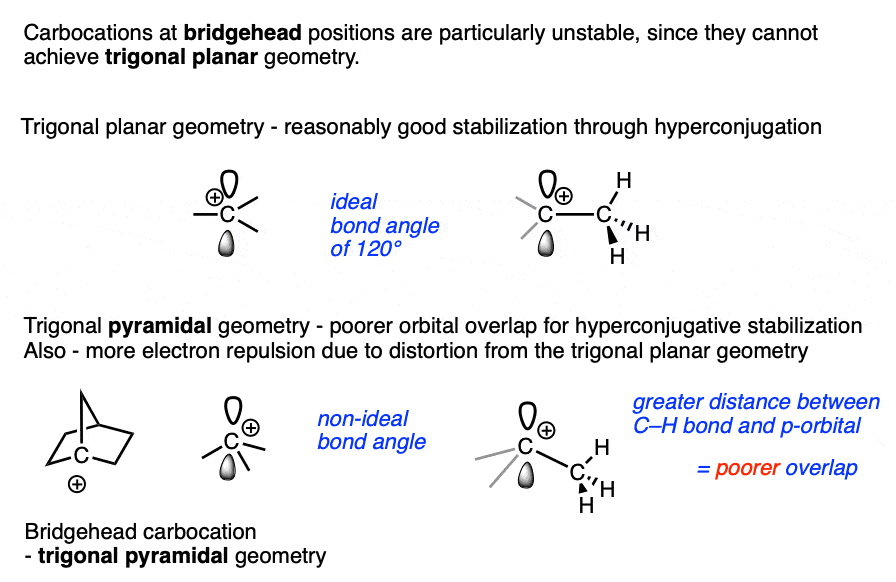
请注意7。碳正离子的小戒指,如环丙基环丁基碳正离子也非常不稳定。
注8。衡量碳正离子稳定性的另一种方法是通过测量的水解率在一个亲核的溶剂。然而,当这个图表埃文斯显示,这两个措施并不总是关联好了…

测试你自己!
 点击翻转
点击翻转
 点击翻转
点击翻转
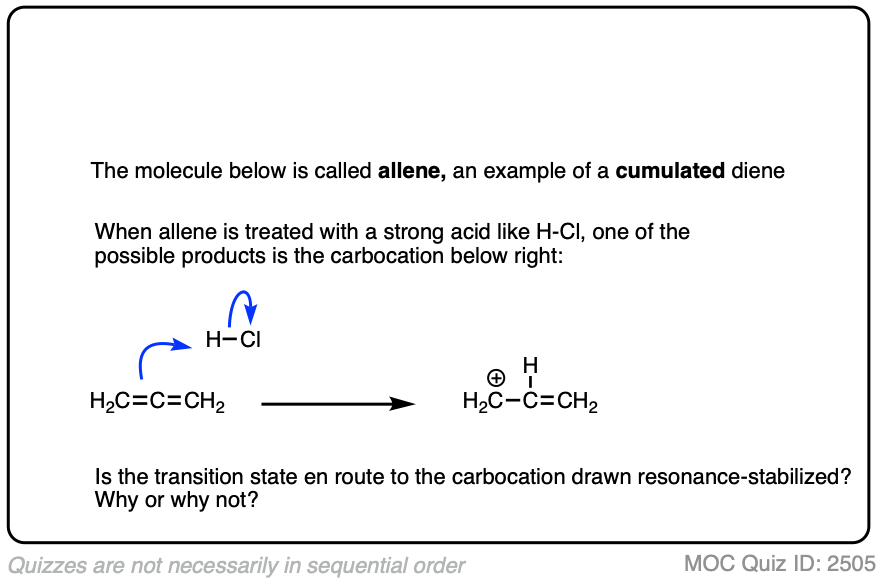 点击翻转
点击翻转
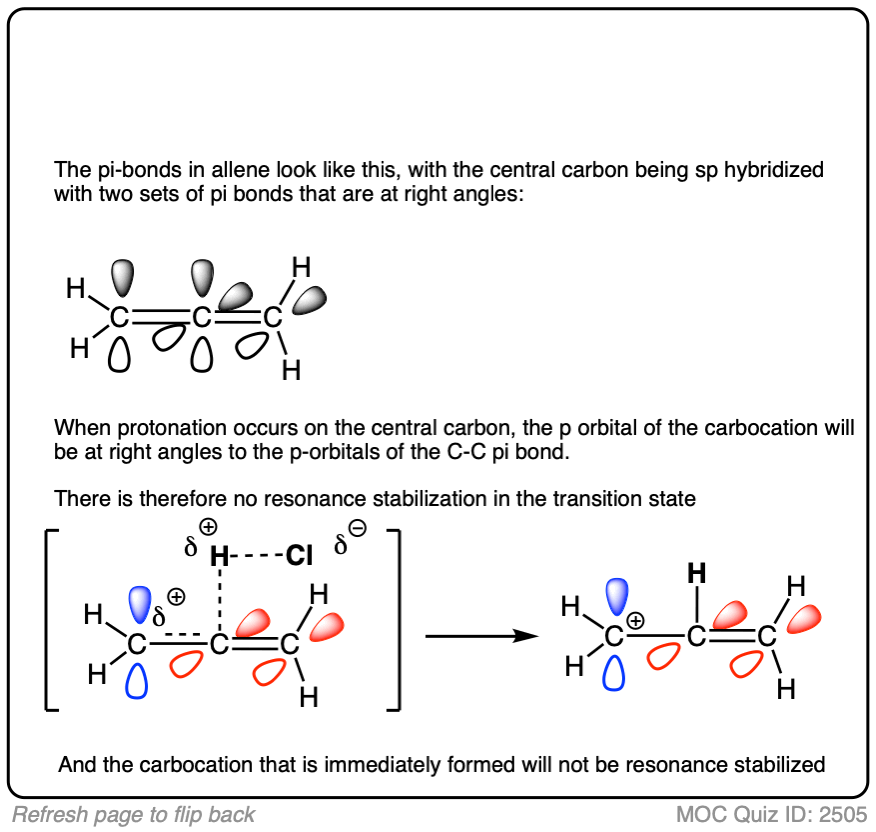
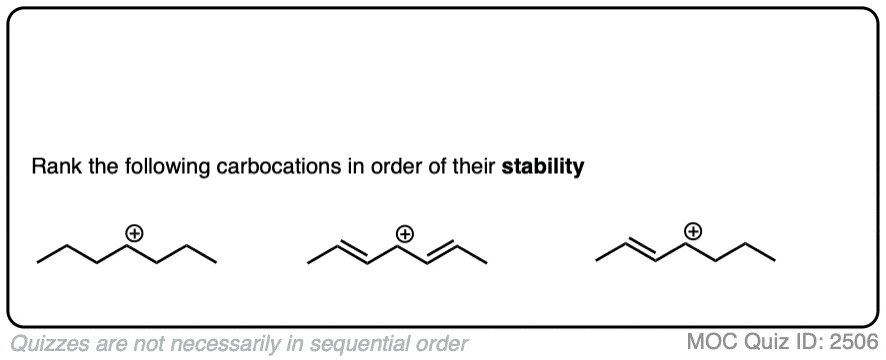 点击翻转
点击翻转
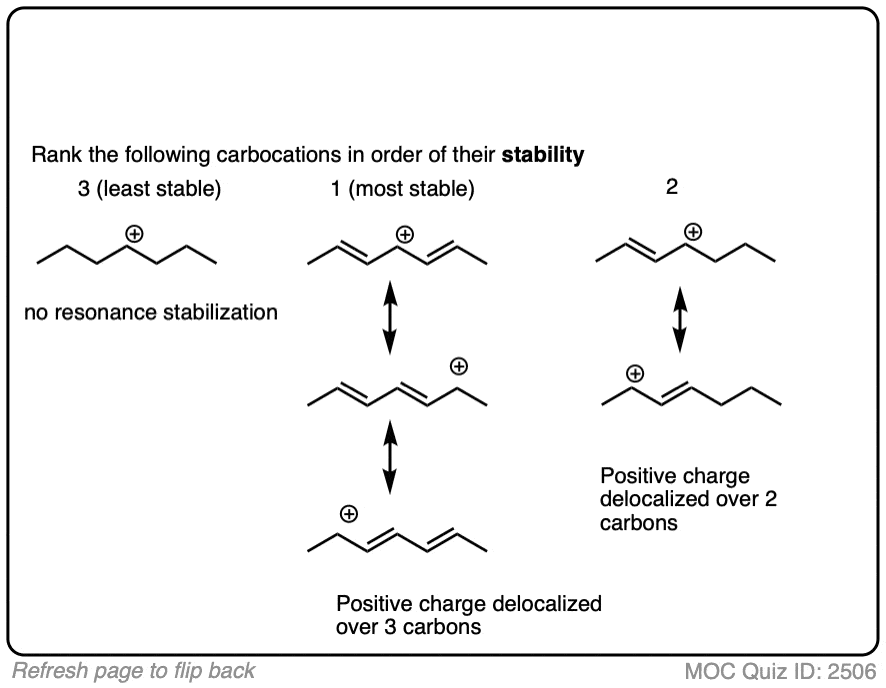
 点击翻转
点击翻转
(高级)引用和进一步阅读
引用
- 100年的碳正离子化学及其意义1
乔治·a·Olah《有机化学》杂志上 2001年 66年(18),5943 - 5957
DOI:10.1021 / jo010438x
从乔治Olah教授历史的角度来看,他在1994年获得了诺贝尔化学奖为“对碳正离子化学的贡献”。 - 碳正离子的稳定性的解决方案。14。一个扩展的热化学常见的酸性过多的碳正离子稳定性的规模
爱德华·m·阿奈特和托马斯·c·Hofelich
美国化学学会杂志》上1983年,105年(9),2889 - 2895
DOI:10.1021 / ja00347a060
本文的39个碳正离子的稳定性提供了一个表,衡量calorimetrically通过生成热(电离辐射超强酸从相应的甲醇)。 - x射线晶体结构桥接或超共轭的碳正离子稳定
托马斯Laube
的化学研究1995年28(10)399 - 405
DOI:10.1021 / ar00058a001
非常有趣的评论从Laube教授比较和对比各种碳正离子的结构,包括adamantyl非常明确的证据超共轭碳正离子。碳碳键缩短从1.528到1.431。碳碳lengthenend从1.530到1.608。100度角vs 110度角 - 阳碳离子。即一个酸性函数(C0)源自Arylcarbonium离子平衡
c . Deno j。j Jaruzelski),艾伦Schriesheim
美国化学学会杂志》上1955年,77年(11),3044 - 3051
DOI:10.1021 / ja01616a036
碳正离子的稳定性也可以表示在pKR +本文中定义。本文研究了碳正离子都相对稳定arylcarbonium离子。 - 氢化物carbenium离子的亲和力乙腈和二甲亚砜解决方案
联合国开发l . Handoo Jinpei Cheng和弗农·d·帕克
美国化学学会杂志》上1993年,115年(7),2655 - 2660
DOI:10.1021 / ja00060a014
氢化碳正离子稳定性也可以表达的亲和力(R++ H- - - - - -- > RH)。本文研究了碳正离子也相当稳定arylcarbonium离子,因为这些是电化学测量DMSO溶液或乙腈。 - 光电子能谱的甲基,乙基,异丙基和叔丁基激进分子。对自由基的热化学和结构及其相应的阳碳离子
答:Houle和j·l·波
美国化学学会杂志》上1979年,101年(15),4067 - 4074
DOI:10.1021 / ja00509a010
摘要表三世为基本的生成热烷基阳离子(甲基、乙基、异丙基和叔丁基),但在气相。同意的数字直觉从液相试验;稳定增加从甲基乙基- > - >异丙基- >叔丁基。 - 定量的准备和重排的焓仲丁基阳离子
w·Bittner e·m·阿奈特和m·桑德斯
美国化学学会杂志》上1976年,98年(12),3734 - 3735
DOI:10.1021 / ja00428a072
介绍了一种新颖的量热法测量热异构化的证券交易委员会丁的阳离子叔丁阳离子在酸性过多的解决方案。使用这个,所获得的价值是14.5±0.5千卡每摩尔。 - 的稳定性烷基碳正离子
托马斯·汉森,帕斯卡染色体,f . Matthias Bickelhaupt和特雷弗·a·哈姆林
化学。Commun。2022年,58,12050 - 12053
DOI:10.1039 / D2CC04034D
对碳正离子稳定性理论研究的趋势。摘要:“我们定量地建立了一个通常被忽视的推动力碳正离子的稳定性,即父母的基质被取代基的引入显著不稳定,经常在溶液中发挥主导作用。这源于取代基之间的斥力和cx债券。” - Wagner-Meerwein重排的故事
柳德米拉Birladeanu《化学教育 2000年 77年(7),858年
DOI:10.1021 / ed077p858
一篇文章的历史兴趣的发展了解Wagner-Meerwein碳正离子重排。
你好詹姆斯,谢谢你的清晰的解释。
一个问题关于碳正离子。我们说的更稳定的碳正离子与亲核试剂反应更快。我们在这里连接的热力学稳定性动力学?
嗨Chenglin,我假设你是指图像在第五节。
整个* *这些反应动力学将由碳正离子的形成,即病原反应步骤。通常更稳定的碳正离子,将低活化能的形成(“末”过渡态)和整体反应速率越快。
它不应该被解释为意味着有一个碳正离子的稳定性和速度之间的关系的第二* *(即快速碳正离子的亲核试剂)的步骤。
Cyclopropenyl阳离子被芳香可以存储在瓶。但有没有可能储存环丙基甲基阳离子更稳定。
更稳定的碳正离子是哪家
环丙基甲基阳离子或cyclopropenyl阳离子
环丙基甲基。Cyclopropenyl迅速将烯丙基阳离子。
谢谢你的文章非常hepful爵士和他们帮助我理解archj-enemy O-chem更好
谢谢你! ! ! !
从气相裂解键能,叔丁基碳正离子是关于7千卡每摩尔更稳定(232千卡每摩尔)比苄基碳正离子(238千卡每摩尔),但取代基效应可以大大改变这些数字。来源:先进的有机化学3月5日。表5.2 224页。
你好先生!
我就一个问题。
哪一个是更稳定
Benzyllic阳离子或CH2(+)环丙烷? ?
这是一个非常好的问题和数据有所矛盾。Cyclopropylmethyl阳离子比苄通常被认为是更稳定。我正在找一个更好的参考不仅仅是222年3月5日患儿p。但是引用其中是很好,但是有点模糊,评论。水解率表明cyclopropylmethyl阳离子更稳定。
然而回答这个问题的另一种方法是看13 c NMR确定碳正离子的化学位移。化学位移越消极,越不稳定。2-cyclopropyl碳正离子化学位移为-86.8 ppm, 2-phenylpropyl阳离子的化学位移为-61.1,表明苯基更好地稳定。看到https://pubs.acs.org/doi/10.1021/ja00731a026
主要卤代烷能够接受SN1反应由邻近的氧原子是否稳定?或将碳正离子反应还是太不稳定?
取决于你指的“周边”。如果是直接连接到相同的碳(如H3C-O-CH2Cl)那么氧很容易形成一个π键和C和Cl -容易会流离失所。例如看到benzyloxymethyl氯。(这些东西往往是不稳定的)
如果邻近你的意思是一个C = O附近碳碳轴承碳正离子,那么这将是不稳定的。
不管我在哪里上网…我永远结束。你的教学方式是惊人的…致敬
我希望这持续!
有可能不相邻的原子的孤对稳定的碳正离子?有一个问题在第八版,布朗的有机化学问为什么CH2CHCOOH (https://image.ibb.co/cdThRJ/structure_1.png)+盐酸CH2ClCH2COOH形式而不是CH3CHClCOOH这将会由于通常更大的二次碳正离子的稳定性。我在想如果你可以在周围的碳链卷曲本身(https://image.ibb.co/d6eBLd/structure_is_this_what_s_happening.png)所以羟基氧上的孤对可以帮助稳定主要碳正离子吗?
对不起,一个额外的碳溜进了这些分子模型。正确的起始物料的结构是(https://image.ibb.co/nOFkfd/structure_1.png)和我提出的正确结构稳定的碳正离子是(https://image.ibb.co/cxTSty/structure_is_this_what_s_happening.png)。
我想这也可能是一个共振结构的贡献(https://image.ibb.co/hj8Vfd/structure_contributing_resonance_structure.png)。
会发生什么是分子内的亲核攻击给某种环。“Anchimeric援助”。
非常感谢你,先生!你比喻在钱和电子使得这个概念更加容易!更多的权力给你!
有答案“应用概念”问题吗?
亲爱的詹姆斯:
我没有问题- nh2 -哦,因为我们在东亚峰会,建立电子捐赠。但是我不明白为什么卤化物应该稳定碳正离子。据说在所有教科书之间的mistmatch 3 p 2 p原子轨道导致减少共振移位,并赢得卤化物的诱导效应,使其吸电子。所以删除电子密度和创建一个更大的正电荷的中间芳香的反应。但是我们这里有相同的卤化物和碳正离子(它不是戒指除外)但其现在捐赠有什么区别?谢谢!
如果你有一个中等碳正离子,一点点的共振稳定和叔碳正离子(没有共振稳定),哪个更稳定?(我的教科书说二级共振…)
你好,你能告诉我哪个更稳定的碳正离子…(CH3) 3 c或(C2H5) 3 c ?
如果不增加碳原子的烷基…+ I效果将减少或增加?
也许tri-ethyl视线稳定增加。相应的卤代烃的电离率会告诉你。
我在想如果有一个底部应用问题的答案检查自己? ? ?
俺们的例子在哪里?
(CH3) 2 c +羧基,能产生共鸣呢?…我的意思是有πσ和+ ve电荷共轭系统…。但是我在做一个问题,这不是答案。
所以为什么不能请回答引起共鸣
共振的形式会得到不到一个完整的八隅体氧气,这是极其不稳定的。这不是一个重要的共振。
没有共振稳定。如果你打破C = O键形成C = C键你将留下一个氧气只有6电子- >高度不稳定。
我没有找到任何的文章负碳离子的不稳定
稳定负电荷的一些因素:
//m.deriinvest.com/2012/02/27/7-factors-that-stabilize-negative-charge-in-organic-chemistry/
这就跟你问声好!
我在想,这将是更稳定的然后tertiatry碳正离子和碳正离子通过共振稳定?(如在# 2 ?)
谢谢你!好文章!
嘿,詹姆斯…。
为什么一个中间带正电的氧气比碳正离子不稳定
有两种类型的中间体与带正电的氧气。氧气的中间有一个完整的八隅体就可以了(一般来说更稳定的碳正离子)。中间体氧气不足一个完整的八隅体非常不稳定的,因为一个电负性很高的原子(氧)与非整八隅体将有巨大的势能(因此不稳定)拉电子对原子核。
我所说的带正电的氧气与6电子电子。它更负电性元素将会有更大的电子亲和能把电子对原子核。非常不稳定的情况。
你好,詹姆斯,
我想选择你的大脑一点。我一直拿我的头往墙上撞,我似乎并不算出来。
假设你有两个仲胺。在第一个,一个取代基炔丙基(prop-2-yn)组和第二个是甲基。二胺,一个取代基是一个(indol-2-yl)甲基(通过亚甲基胺是保税集团的位置2吲哚),第二个是甲基。现在,在这两种情况下二次碳正离子形成胺氮。哪一个应该更稳定?
在这两种情况下氮稳定正电荷通过孤电子捐赠,但炔基,indolyl一半吗?我想他们应该都有stabylizing影响通过移位但稳定带电种类更多的哪一个?归纳影响呢?在这种情况下他们应该玩一些有意义的角色?我很困惑…
你好,詹姆斯,
谢谢你的解释。我不是一个有机化学家和我有一个问题关于稳定的碳正离子。你认为这是可能的稳定的碳正离子通过把它旁边的某事能稳定吗?溶剂化作用的影响,或一些带负电荷的物种吗?喜欢静电稳定吗?
在所有这三个例子中,碳正离子通过分子内的稳定效果,分子间稳定呢?
谢谢。
碳正离子在酸性过多的相对稳定的解决方案。这就是乔治Olah研究它们,这帮助他赢得了诺贝尔奖。http://www.nobelprize.org/nobel_prizes/chemistry/laureates/1994/olah-lecture.html
谢谢。
有机化学最退出和美丽的主题一直是一个像我一样的极客和所有这些文章启发我去更深入的话题。bdapp平台
阿门,兄弟
你好,为什么是一个比一个叔碳二烯丙基的碳正离子更稳定吗?谢谢你!
嗨,莫尼卡
有几个因素并不总是容易判断,只是看着他们——我们需要做实验。例如我们知道,碳正离子增加稳定从小学,中学到三级。
我们也知道,如果他们共振稳定碳正离子增加稳定。
然而,更重要的因素是什么?替换模式或共振?
没有办法算出来只要看它。我们必须做实验(我们做!)(通过测量电离率”)
这些实验告诉我们,二烯丙基的碳正离子稍微容易形成比普通(非共振稳定)三级碳正离子。
这是为什么呢?好问题(这就是它可以复杂)。可能有更多的电子密度的事实被捐赠的相邻的p轨道比附近(超共轭)碳氢键叔碳正离子。
这些因素可以在微妙的平衡。如果我可以做一个类比,这有点像运动队。更重要的在足球,进攻或者防御过得好吗?嗯,它们都是重要的。我们怎么知道的相对重要性?玩很多游戏,试图弄明白通过查看数据。幸好化学一摩尔的材料给我们机会玩6 x 10 ^ 23“游戏”所以我们可以算出来相当可靠。
希望这可以帮助!詹姆斯
你好,
我在想如果你能把这些示例问题的答案吗?我在做,但是我没有办法检查如果它是正确的。
感谢,
助教阮
嗨,第一个碳正离子在每种情况下更稳定。这3个因素适用于我们了解到稳定的碳正离子。
三级比二级碳正离子更稳定
烯丙基的碳正离子(共振稳定)比非共振稳定稳定的碳正离子
碳正离子相邻原子与孤(氧气)更稳定的碳正离子与孤不相邻的原子。
希望这有助于
詹姆斯
你好…我有一个问题我们能说resonanse因素更有效因素除了当芳香性濒危呢?
你能请告诉我叔的稳定秩序,苄和烯丙基自由基吗?
试着看叔的力量,苄酯和烯丙基碳氢键。因为碳氢键强度测量均裂,然后你将得到稳定的自由基。较弱的碳氢键更稳定的激进。
这就跟你问声好!谢谢你的帮助:)
我有一个问题。将一个仲碳被认为比主更稳定的碳正离子保税卤素?这是在练习测试,我有点困惑o_O
很难说没有看到确切的例子,但我的猜测是,后者情况会更稳定,由于卤素可以捐献一个孤对,每个原子分子可以有一个完整的八隅体。这是一个更加稳定的情况比自由碳正离子,那里是一个空轨道。
首先,谢谢你解释这个。
但你能告诉我,通常效果数量更多,归纳或超共轭现象?
例如,如果你有乙基碳正离子和如果你有2甲基丙烷碳正离子(主要碳正离子)将更稳定?
这是更强大的稳定的超共轭,但它是更容易解释的角度归纳影响。如果你是一个主修化学程序我会花时间去学习超共轭和应用研究。这是一个非常强大的概念。
你能解释为什么1、3、5 hept-triene碳水化合物阳离子(+ sp3碳)比三苯基稳定碳水化合物阳离子? ?
芳香性。看到的://m.deriinvest.com/2017/02/23/rules-for-aromaticity/
这是这么多的帮助!有机化学是一种痛苦,有更多的解释其他orgo科目吗?bdapp平台
光谱学、我真的需要帮助,可以使用这样的好网站
谢谢。
很难找到阳离子稳定的简要解释。谢谢!绝对书签网站。
谢谢。我现在学习有机化学下周考试,这是有利于我的研究
我只有一个小问题。数量更多,共振稳定或者其主要或次要碳?由于这个事实,更稳定,+ CH2-CH = CH2或CH3CH(+)甲基吗?谢谢你提前xD
好问题。你引用的例子中,共振数量更多。
非常感谢,这救了我的命。很感激。
其实我的主要问题是关于pinnacol pinnacolone重排。
H +攻击哦,收益更稳定的碳正离子
所以应该攻击啊?
哦哦
我我
CH3-C-C——C2H5
我我
甲基C2H5
哦服务器忽略空间的复合混乱起来。
它是
(CH3) 2 c (OH) - - - - - - c (OH) (C2H5) 2
ch3ch2ch2 +和ch3ch2 +哪个更稳定的碳正离子
都是主要的但
前有一个笨重的烷基,因此更多的诱导效应
,后者有更多没有α氢,因此没有hyperconjugative结构. .
原因都是冲突……! ! ! ! !
我们预计第一个直觉但是我们怎么能忘记这一事实hyperconjugaion更占主导地位的诱导效应呢?
两者都是主要的碳正离子;他们将有非常相似的稳定性。氢化丙基碳正离子可以重新排列通过转移给第二个碳正离子。
所以结论是,丙基碳正离子是更稳定的…。
bcz可以重新排列
不——一旦它重新安排,我们讨论的是一个完全不同的碳正离子。
“弯曲或伞债券”呢?你不觉得弯曲债券参与碳正离子的稳定性?
你能添加碳正离子的转变使这个完整的。
rearrangments系列中讨论。
哦,这完全是了不起的人。你告诉每一个思想答我们在学习了!现在和我的每一个疑问了! ! n ! n ! n !
兄弟,你这狗屎容易。你真的太棒了!
本文重新帮我很多! !高兴你发布:D
好文章!
伟大的文章。
好的解释可以eaisly理解通过阅读这篇文章
很高兴你有帮助。
你能解释一下吗,如果我有一个苄基碳正离子和叔丁基碳正离子
这将是更稳定吗
1日稳定由于苄共振
和2 9可能hyperconjugative结构
请回答
亲爱的Jeetesh !你应该知道共振比超共轭,发音稳定阳离子相比,超共轭。
是的伊克巴尔,共振主要支配……bt这里已经发现,叔丁基更稳定……
库,你有一个参考吗?
莫里森博伊德说。(http://www.chemicalforums.com/index.php?topic=33527.0)
作为一个评论者说,小替换可以提示的平衡方式的变化。
我没有一个实验参考,但在“有机化学电子流”保罗飞毛腿声称在65页他“碳正离子稳定性排名”图表,“三级阳离子”是比“苄阳离子”更稳定(苄基所主,即两个H)。
我想象一个三级苄阳离子,sp2碳轴承烷基苯基和两个团体,当然应该比叔更稳定的阳离子轴承三个烷基组(均有两个超共轭现象,然而芳香π捐赠者比第三超共轭)。
二苄基正离子与三烷基阳离子会更模糊。
亲爱的所有,碳正离子稳定性可以推断气态氢化物亲和力的。请参见高级有机化学:凯莉和桑德博格的第五版,一部分表3.10。,303页。氢化物越低亲和力、更稳定的碳正离子。(239千卡每摩尔为叔丁基苄基的阳离子VS 237千卡每摩尔阳离子)
我理解丰富的解释。这是令人满意的。谢谢你!
这是由于苯组不在一个平面共振发生,R组应该躺在同一个平面上。这种扭曲形状的化合物发生由于立体皇权苯组的化合物
其异常情况下,叔丁基碳正离子更稳定……
苄carbocatian更稳定,因为电荷离域…
非常简单的方法来理解化学
关于有机化学的信息
以简单的方式解释科学是一门艺术。你做了它!
谢谢!
好教程。