焊接、结构和共鸣
四个分子间作用力以及它们是如何影响沸点
最后更新:2022年12月14日|
熔点和沸点等属性是多强的测量单个原子或分子之间的吸引力的力量。(我们称之为国际米兰分子的力量,力量之间的分子,而不是内部分子部队,部队在一个分子。)
所有来自这个一般原则:债券变得更加分化,原子上的费用变得更大,从而导致更大的分子间吸引力,导致更高的沸点。
主要有四类分子之间的相互作用和它们都是“相反电荷吸引”的不同表现形式
四个关键分子间作用力的如下:
离子键>氢键>范德瓦耳斯偶极-偶极相互作用>范德瓦耳斯色散力。
让我们看看他们分别,从最弱。
表的内容
1。离子的力量
离子部队带电原子或分子之间的相互作用(“离子”)。
带正电荷的离子,如钠(+)(+),和Ca(2 +),称为阳离子。
带负电荷的离子(例如Cl (-), Br(-),(-)被称为阴离子(我总是有了直通记住“N”的“负离子”代表“负面”)。
电荷相反的离子之间的引力是由库仑定律,描述力的增加费用和减少这些离子之间的距离增加。
高度极化分子离子(带电)的本质是反映在他们的高熔点(氯化钠的熔点为801°C)以及他们的高水溶度(碱金属盐,无论如何;金属,形成多个指控要留残留在你的浴缸里)
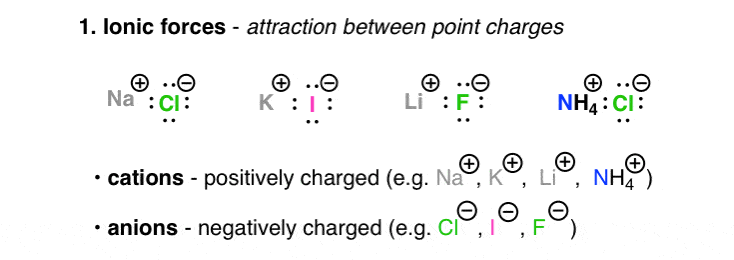
2。氢键
氢键发生在分子包含高度电负性元素F, O, N或直接绑定到氢。
自从2.2 H的电负性(比较为Na 0.9和0.8 K)这些债券是不像纯离子极化债券和拥有一些共价的性格。
然而,债券仍将氢极化和拥有偶极子。
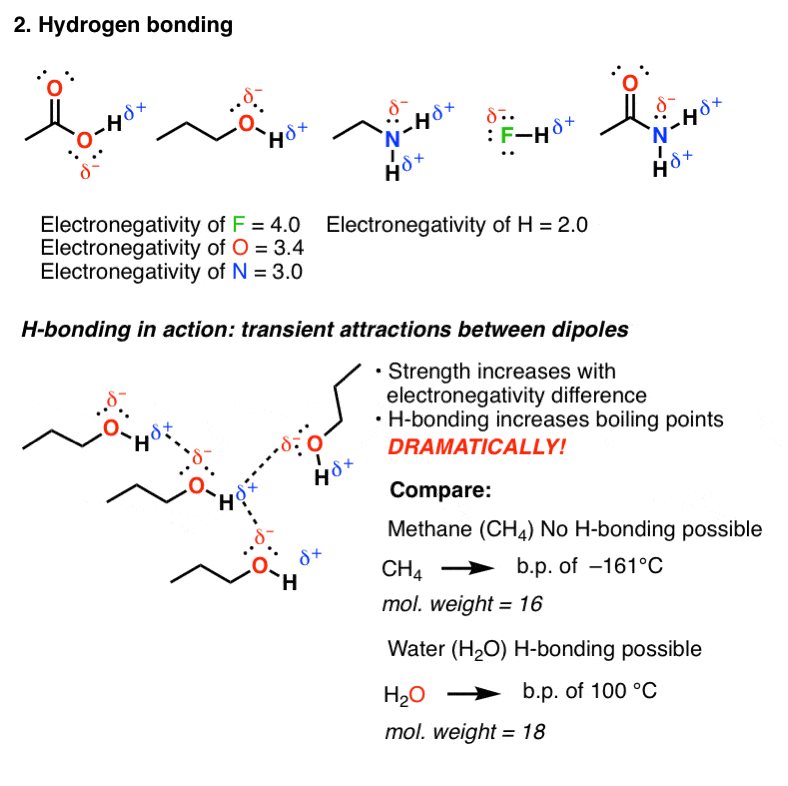
一个分子的偶极子可以与另一个分子的偶极子,导致一个有吸引力的互动,我们称之为氢成键。
由于分子运动的快速解决方案,这些债券是瞬态(短暂),但有明显的优势从债券(9焦每摩尔(2千卡每摩尔)(NH)约30焦每摩尔(7千卡)和高频高。
如您所料,键的强度增加的电负性组绑定到氢是增加。
所以从某种意义上说,何鸿燊,NH“粘性”——包含这些官能团的分子会高沸点基于他们的分子量比你所期望的。
3所示。范德瓦耳斯偶极-偶极相互作用
其他组旁边的氢可以参与与强烈的电负性原子极性共价键。例如,每一个分子包含一个偶极子:
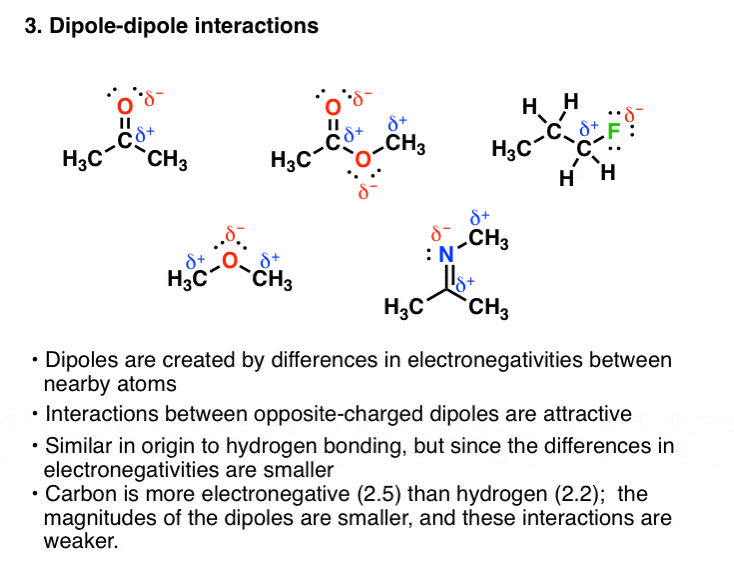
这些偶极相互作用的有吸引力的时尚,这也会增加沸点。
但是由于碳电负性差异(电负性= 2.5)和电负性很高的原子(如氧或氮)小的电负性比氢(= 2.2),极地交互强大。
所以平均这些力量往往较弱的比氢键。
4所示。范德瓦耳斯色散力(“伦敦力”)
所有被称为色散力的弱的分子间作用力伦敦部队。
这些代表之间的吸引力瞬时偶极子在一个分子。
考虑一个原子氩。它是一种惰性气体,对吧?但是如果你酷-186°C,你可以凝结成液氩。它形成了一个液体这意味着的东西是维系在一起。“东西”是色散力。
考虑电子价电子层。平均,他们均匀分散。但在任何给定时刻,可能有一侧有多少电子之间的不匹配,另一方面,有多少可以导致瞬时负责不同。

这有点像篮球。在平均每名球员都是一对一的,球员的均匀分布。
但在任何给定时刻,您可能有一个防守的球员的分布情况是“波浪起伏的”(这也意味着有人打开)。在价电子层,这种“块度”创造了偶极子,这些偶极子负责分子间吸引力。
的极化率我们用这个词来描述如何消除原子形成这些瞬时偶极子。
极化率随原子的大小。这就是为什么氩的沸点(-186°C)更高的比氦的沸点(-272°C)。同样的类比,碘的沸点,(我184°C)的沸点远高于氟(f, -188°C)。
碳氢化合物和其他非极性分子缺乏强有力的偶极子,这些色散力是真的只有分子间的引力。
由于偶极子弱和瞬态,他们依靠分子间联系——这意味着力量增加表面积。
这样的小分子甲烷已经非常弱的分子间作用力,和有一个低沸点。
然而,随着分子量的增加,沸点也上升。
这是因为这些力量的表面可以增加了。因此,维ispersion部队分子量增高而增强。个人,每个交互不值得,但如果集体,这些力量可能会非常重要。壁虎蜥蜴如何走在墙上吗?看它的脚。

(碳氢化合物的确定趋势可能有点棘手根据具体结构,对称的沸点和熔点中也扮演了重要的角色。前面我们谈到这一点。(见文章分支和熔点)
5。底线
- 沸点是分子间力的测量。
- 增加极化的分子间作用力增加债券。
- 分子间作用力的力量(沸点),因此影响离子>氢键>偶极偶极子>色散
- 沸点随分子量,和表面积。
笔记
提醒——不要忘记自由沸点学习指南(包含所有在这篇文章中讨论的要点)
ion-dipole交互呢?这些也存在对吧?会在你的离子>氢键>取向>分散层次?
气氛也影响沸点吗?例子,如果我代替的气氛与二氧化碳或霓虹灯室,会改变沸点吗?
取决于大气压力。沸腾时汽压力等于大气压力。如果大气的压力仍然是大气压力(760托/ 1条/ 101.25 kPa)那么沸点应该保持不变。
气体比空气重,然而,它需要更少的摩尔的气体达到压力。例如如果你有一个两室,一个氩和一个与空气,每个都有相同的摩尔量的气体,然后在氩气的压力室会更高,因此bp的液态氩室会更高因为一摩尔氩重量超过一摩尔的空气。这说得通吗?
你能评论的定向或非定向性质以下交互:
1。取向
2。Dipole-Induced偶极子
3所示。Ion-Dipole &
4所示。离子感应偶极子
你的文章有很大帮助!谢谢你!
下列物质中,如何从弱的分子间作用力,最强的吸引力。庚烷、己酰戊酸和丙ethanoate。
庚烷弱。戊酸最强。己酰…你是说己醇吗?
为什么CH3OH NH4沸点较低?他们都有氢键和nh4更小。
计算氢键的数量。更多的氢键意味着更强的IM的力量
因为科学
因为甲醇有“哦”功能组,可以参与氢键。铵也可以参与氢键。碳和氮之间的质量也影响沸点。是的,甲醇总比铵质量更高,但事实上,你正在处理一个酒精与离子影响mp。
CH3OH比NH4较大的摩尔质量。摩尔质量越大(在某些情况下),imf的越强。
我猜是因为沸点取决于分子间作用力(货币基金组织)。国际货币基金组织(IMF)决定从三件事:色散力、Dipole-to-Dipole部队和氢键力。是的,CH3OH更多电子(大)所以它有色散力。是的,CH3OH Dipole-to-Dipole更多力量,因为它是极地NH4不是。然而,我认为氢键力是它改变的地方。氢键部队携带的价值在国际货币基金组织总比色散和偶极子的力量更重要。CH3OH只能有氢键的氢原子共价结合的氧。就是这样。但是,氢键可以形成四个氢原子。
极化率是我们用这个词来形容容易原子如何形成这些瞬时偶极子。极化率随原子的大小。这就是为什么氩(-186°C)的沸点远高于氦的沸点(-272°C)。同样的类比,碘的沸点,(我184°C)的沸点远高于氟(f, -188°C)。
NH4,我以为你的意思NH4 +。包含NH4 +离子债券的化合物,沸点,因此应该高于化合物没有离子键,像CH3OH。
为什么N2沸点低于公司尽管他们等电子的吗?
最好的方法记住阳离子和阴离子的区别,每个人都将永远记住是:阳离子总是PAWWWSSITIVE: D myy创化学教授告诉我,它永远停留。
为我即将到来的实验报告很有帮助。只是想点一些东西,本文不同于我在学校被教导:
1。氢的极性为2.1
2。债券与0.4或更少的电负性不是极地。
我不知道哪一个是正确的,但这似乎并不重要。
保持好工作。
只是有点清晰:
1)“电负性”是一个测量的原子强烈希望留住其价电子。至少有5种不同版本的这个值,每一种稍微不同的方式计算,尽管大多数化学家把李纳斯鲍林的电负性,当他提出了第一种方法的计算。顺便说一下,他的方法只有措施电负性差异(见下文),所以氢的电负性是设定在2.20,和其他原子的电负性是相对的价值。
2)“极性”是一个术语,反映出不同的两个成键原子的电负性。
),极性总是相对于两个原子之间的电负性差异,这与任何一个原子。
b)债券与电负性差异大于0(也就是说,没有两个相同的原子之间的任何债券,这被认为是一个纯粹的共价键)技术是一个极性键,但公约应大于0.5的差异被认为是实际极地。
c)一旦差异大于某个阈值(不同的化学家已经确定截止为1.7,1.8,2.0,2.2,我知道),电子组成债券已经完全或几乎完全被更多的原子的电负性。这导致一个原子有一个完整的负电荷(阴离子)和一个原子有一个完整的正电荷(阳离子)。他们不再是共享的电子,但两个电荷相反的离子的静电吸引,称为离子键,相当强劲;频繁的结合能比典型的共价键(非极性或极性)。
d)事实是,即使有着最高的两个原子电负性(F)和最低(Fr),电负性的差异还导致债券只有约92%的离子特性。也就是说,几乎每一个键,我们称之为“离子”实际上仍然有一点共价(即。、共享电子)字符。
我希望这对您有所帮助。我不知道多久以前你发布你的问题。
马克
谢谢你这么长时间和雄辩的回应,马克。
如果液体具有高极性表面张力增加行为呢?
还告诉我醇、酯类、醚类、芳香族碳氢化合物沸点之间有任何关系,分散、表面张力或润湿性(这是专门为液体油墨)
谢谢你这一页!
解释是惊人的! ! ! !
保持好!
我总是记得Pawsitive阳离子。谢谢你的沸点的帮助
谢谢你谢谢你谢谢你!
爱篮球的类比,)
为什么HCl diplole偶极相互作用,而不是氢键?
像高频。
盐酸* *氢键,它不是特别强。
所有与氢分子的氢键,但它就是这样一个非常弱的程度,它并不重要。
然而,当氢键与元素电负性非常强(主要是F, O, N)它们紧紧地抓住和氢键发生在他们是极其重要的。
为什么氦的沸点低于氢的沸点吗?
因为氦气包含两个电子都在1 s轨道非常接近原子核。氦实际上是一个非常小的原子更小比氢自电子近了…也不想得到或失去任何因此将尽其所能保持其电子。当我们学会了更小的原子沸点较低。
H必须连着,F, O, N为了展览氢键。