羧酸衍生物
酰胺水解
最后更新:2022年12月29日|
酰胺水解-羧酸酰胺转化
在这篇文章里,我们讨论的例子和酰胺的酸性水解机理,以及一些例子的酰胺水解异常“容易”。我们还简要讨论了在基本条件下酰胺水解。
表的内容
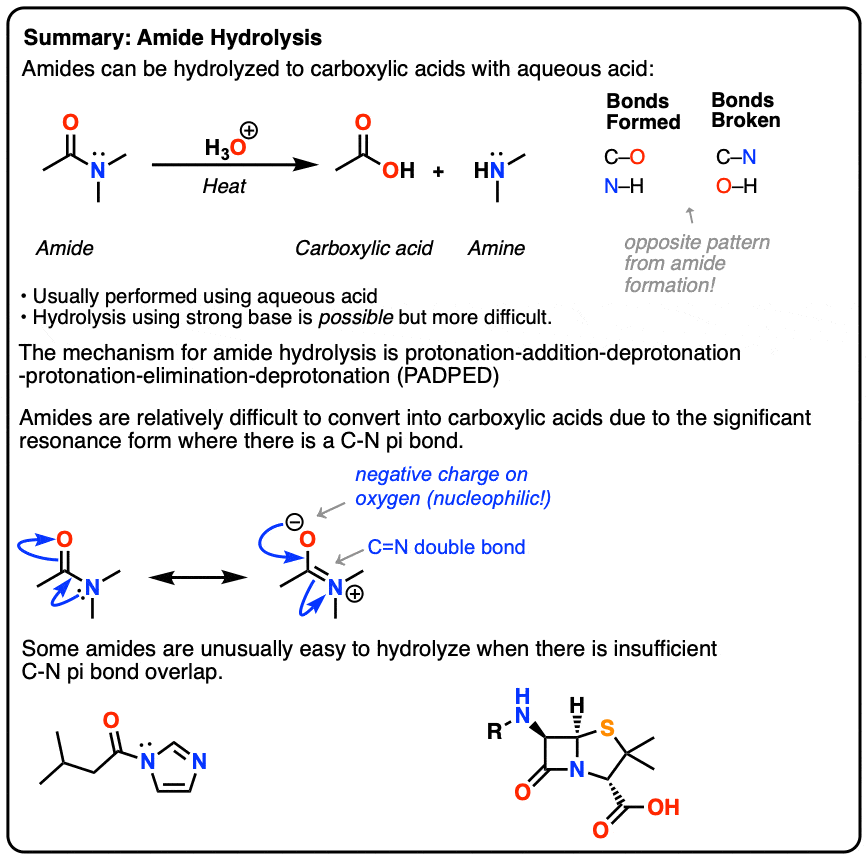
1。酰胺的水解
酰胺是羧酸衍生品的-哦羧酸已经取代了nh吗2、-NHR或nr2一个胺。因为之间的反应羧酸和一个胺给一个酰胺也释放水,这是一个“缩合反应”。(我们讨论的命名法和合成酰胺在这里]。
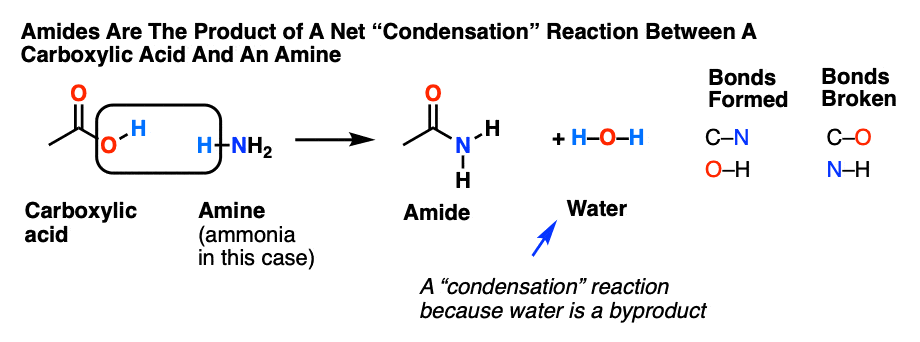
当两个氨基酸形成一个酰胺,我们称之为物种肽,除非你一直生活在一块岩石上,你会知道,蛋白质是由氨基酸通过肽(酰胺)债券有关。酰胺官能团不容易打破,也是一件好事,因为地球上的生命是如此依赖他们。
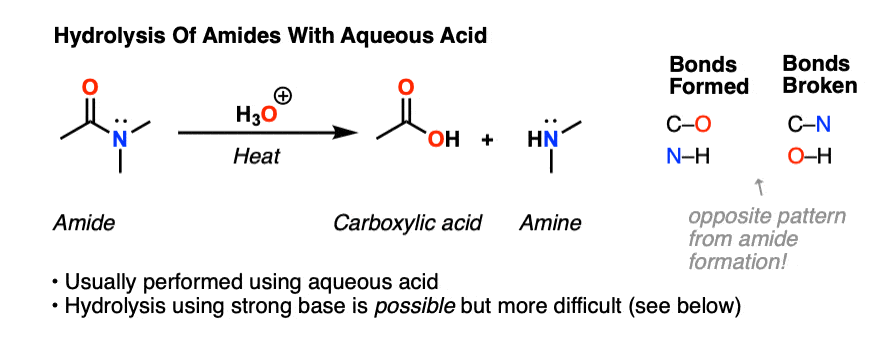
缩合反应是相对的水解的反应。酰胺的水解是通常不是一个容易的事。典型的酰胺水解条件涉及长时间加热水的酰胺酸。
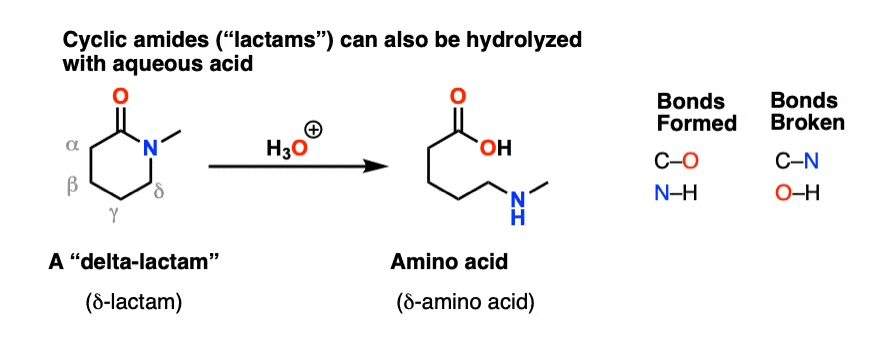
环酰胺被称为,“内酰胺”。就像解开皮带的结果在一个简单的皮革,循环的水解内酰胺结果在一个线性氨基酸。(下面的例子是一个“δ”以来氨基酸胺是一个取代基第四碳从羰基——不是混淆与生命的“氨基酸”,“阿尔法”氨基酸)。
2。为什么是酰胺的水解酸卤化物和酯相比如此困难?两个原因
所以使酰胺很难打破相比,酸性氯化物或甚至是一个酯。
是一个关键因素氮上的孤对捐赠能力。记得,孤氮(胺)少比孤紧紧举行(更多的电负性)氧气,因此更容易获得对捐赠(即更基本的)。共振形成的氮碳双键因此比相应的共振形式更重要酯类。(这个主题可能熟悉:这正是为什么北半球2是一个“激活”比哦在芳环取代基。
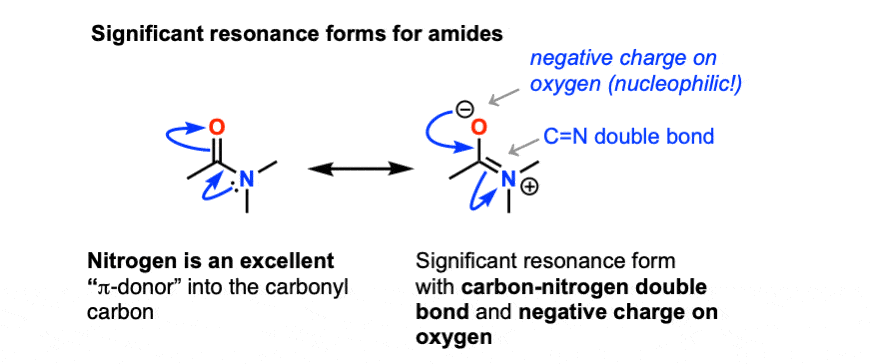
这有几个有趣的后果。首先,最基本的网站一个酰胺不氮上的孤对,而是氧气。
质子化作用发生在氧气先!
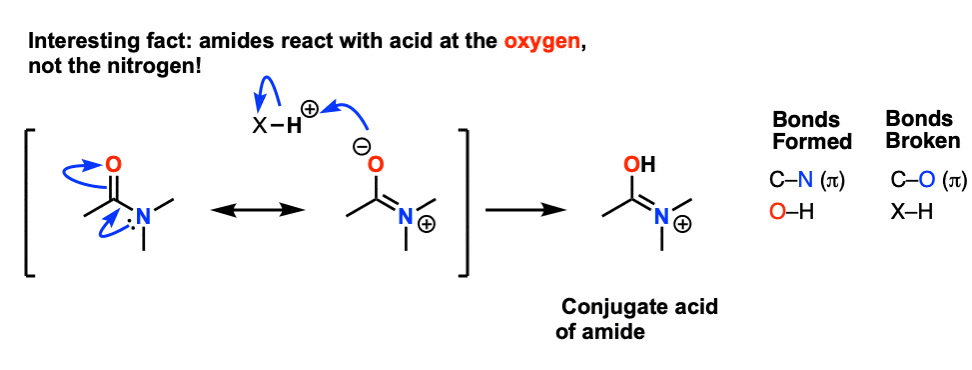
第二个有趣的结果是,由于右手共振形成的重要性,有碳氮键的重要“双键”字符。在以前的文章结合和共振我们提到,这表现为一个旋转的碳氮键的障碍对15 - 20千卡每摩尔)
3所示。使用水酸酰胺的水解:机制
所有这些都是说,执行一个酰胺的水解不是那样容易裂开一个酸卤化物。也不是简单的机制。
所以反应是如何工作的呢?
正如我们所指出的,第一步是可逆的质子化作用对氧气给酰胺共轭酸。
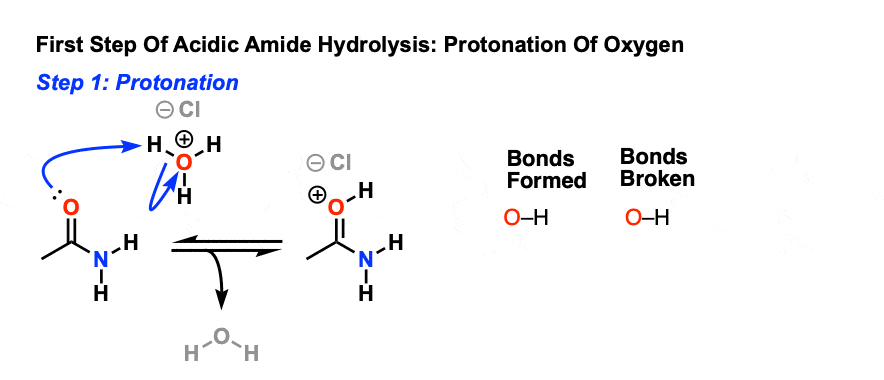
质子化作用的羰基氧气使羰基一个更好的碳亲电试剂,因为切断π键减弱和共振形成碳正离子碳变得更加重要。
下一步是添加亲核试剂(水、溶剂或co-solvent)形成一个新的切断债券和打破切断π键。
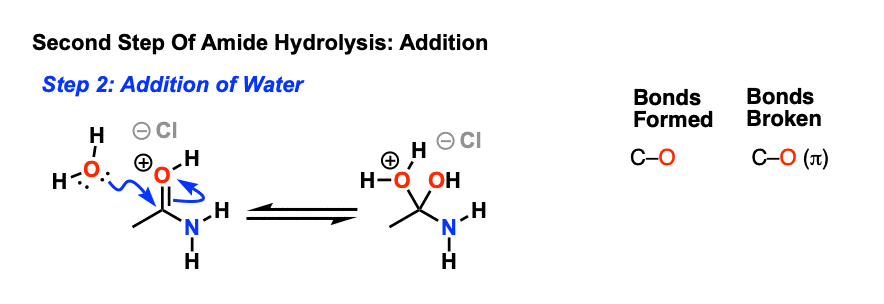
这将导致一个新物种与一个正电荷的氧气。在下一步中,质子是穿梭在氮原子通过去质子化的氧和氮的质子化作用。(去质子化——质子化作用,或者只是“质子转移”]
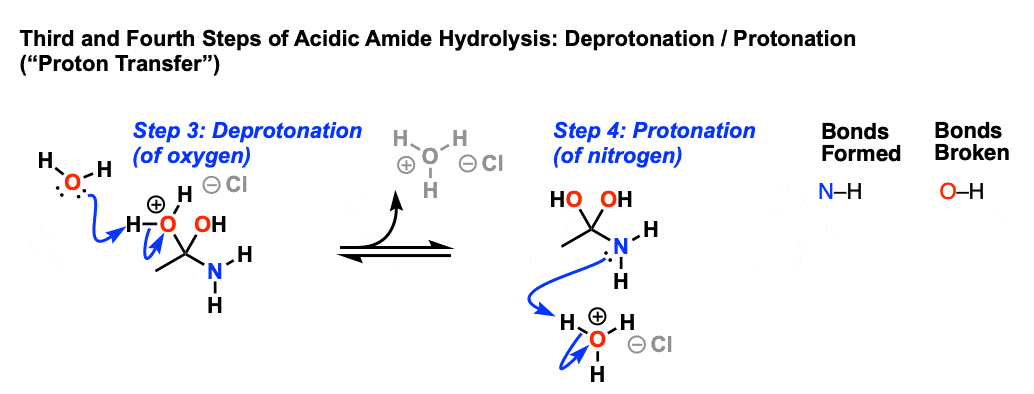
结果现在是一个带正电的氮物种更好离去基团,因为离去基团将曼公司2(弱碱)而不是NR (-)2(一个很强的基础)。因此在下一步消除发生时,形成一个新的切断π键和碳氮。
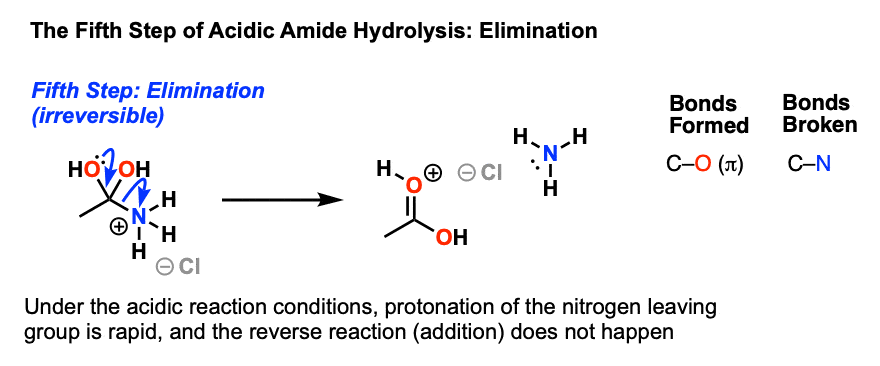
这导致一个带正电羧酸导数,然后deprotonated给中性羧酸,完成酰胺的水解。
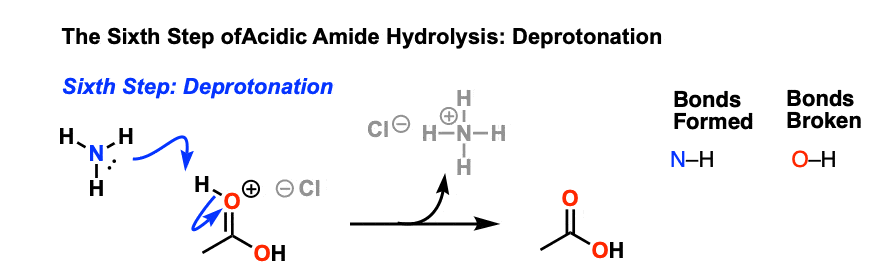
这六步机制(质子化作用,另外,去质子化,质子化作用,消除,去质子化)看起来很眼熟。在费舍尔的确切顺序步骤酯化和其他各种机制,PADPED的缩略词。(看到做音乐与机制]
的所有步骤的过程达到平衡,直到消去反应发生。一旦打破,碳氮键以来极不可能胺存在的共轭酸和不作为亲核试剂。
平均酰胺,这就是所有有酰胺水解。显然主要酰胺,离去基团将NH3,第二个酰胺RNH2。
4所示。基本的酰胺水解呢?
这是酸性水解。基本的水解呢?
这是可以做到的,但它通常是不容易的。如果坚持蛮力,这是有可能的。酰胺的水解基地需要长时间加热。
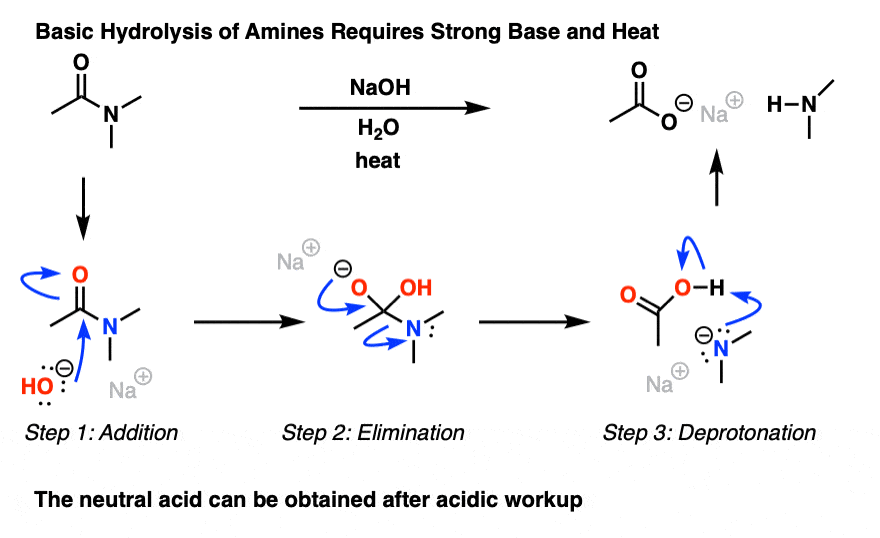
是为了整个问题取代反应(无论是年代发生N2 -酰基取代)需要一个体面的离去基团。因为它是这样一种强碱,deprotonated胺(令人困惑的是也称其为“酰胺”,有时“金属酰胺基”)是非常体面的反面离去基团。所以即使强碱氢氧化钾和大量的热量,裂开一个酰胺是很困难的。(注1]
5。摘要:水解氨基化合物与酸或碱羧酸
酸酰胺的水解是一个“肉和土豆”的化学反应是必不可少的认识和理解。彻底理解的关键机制之一是分解反应的六个步骤(PADPED)和比较它反应分享这个核心机械的途径(如费舍尔酯化、水解酯类等等)。
确保你可以画出产品循环酰胺的水解(内酰胺自循环的反应分子(和他们的反向,分子内反应)考试常见的饲料。
这个反应在之后的斯特合成氨基酸,始于亚胺氰根离子的增加,水解的紧随其后腈给羧酸。
感谢公斤援助数据在这篇文章中!
笔记
注1。一些研究表明,断裂的碳氮键才会发生第二个哦组是deprotonated。
补充:3酰胺异常容易破坏
酰胺,非常容易破坏(1)- Acylimidazole
当我们说,酰胺往往很难打通。然而值得关注的一些例外,有助于说明这里的要点。
一个特别容易打破是酰基咪唑酰胺。还有一个碳氮键,还有氮上的孤对。
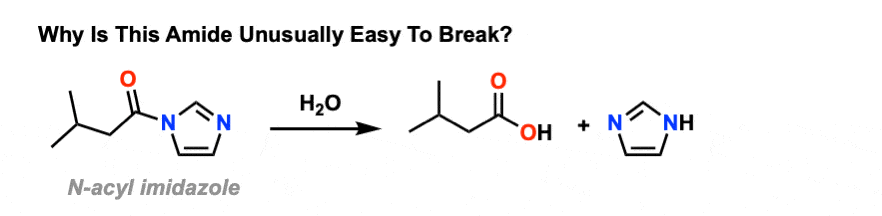
那么为什么这么容易破坏呢?
考虑到共振形式。你注意到在左边的共振形成咪唑与共振形成的对吧?
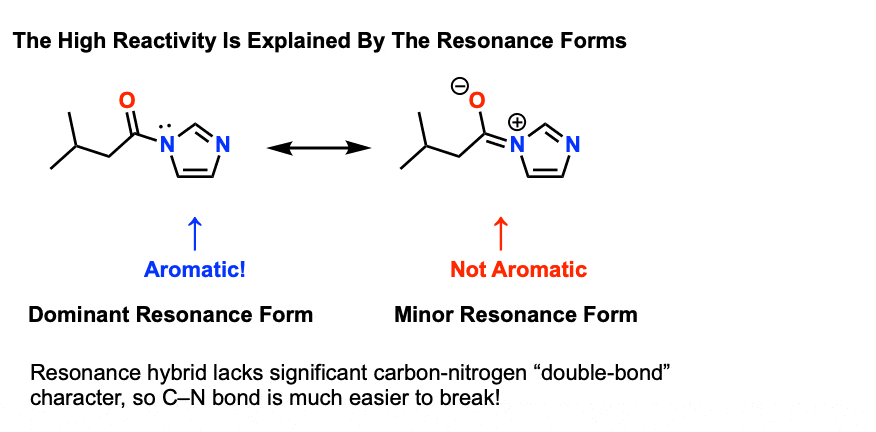
在共振形式(左),咪唑芳香。在右边的共振形式,有部分碳氮双键的性格,芳香性。
这不是N-acylimidazole独有。N-acylindole N-acylpyrrole也是如此,其他物种的孤对“忙”是一个芳环。
酰胺,非常容易破坏(2)- Beta-Lactams
中描述的魔法戒指,麻省理工学院的化学家约翰·希恩和他的研究小组有一个可怕的时间合成青霉素。问题是就会形成4-membered酰胺环(一个“测试版内酰胺”)使用常规条件那该死的系统就会崩溃。最终席汉氏集团发展DCC(后来EDC)是一个非常温和的方法形成酰胺联系,问题已经解决了。
β-内酰胺异常容易破坏有两个原因。首先,最明显的,是共振的形式有一个碳氮双键4-membered戒指,和一个四元环双键(如环丁烯)系统增添了更多的压力。这最小化谐振的重要性因素C = N双键。第二个,更微妙的原因是sp3杂化碳环结(毗邻氮)传授氮略有皱纹,所以轨道重叠是更加困难比在线性酰胺。
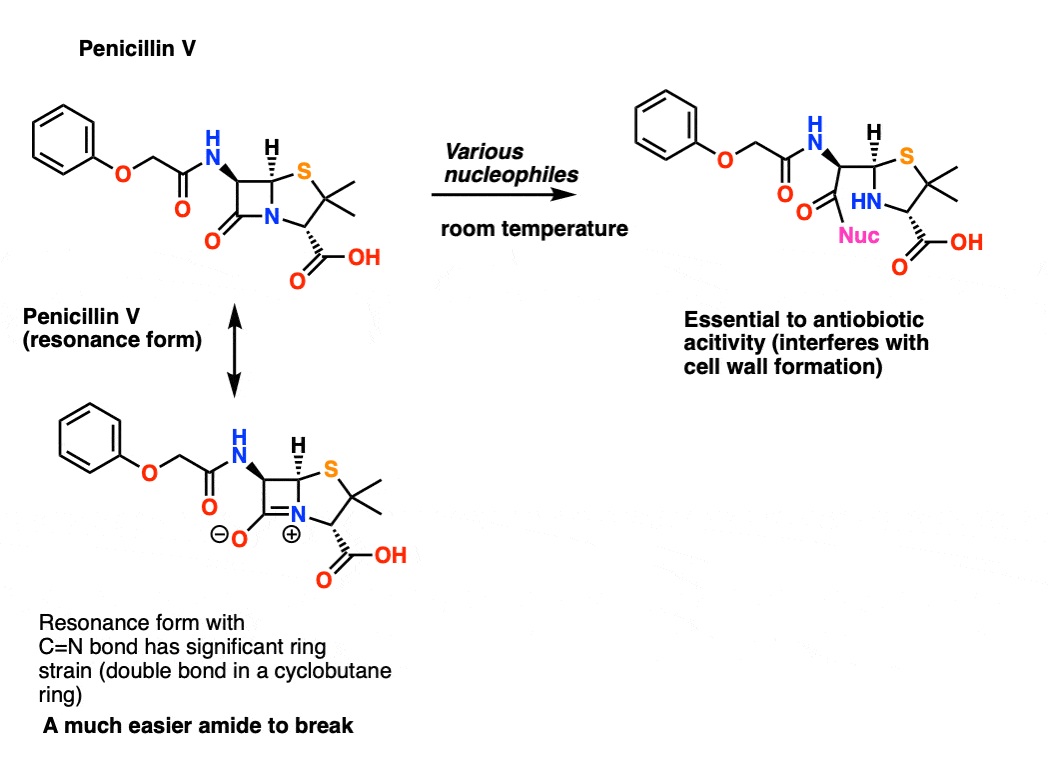
因为轨道重叠不好,碳氮键缺乏部分双键特性,并且很容易打破。
酰胺,非常容易破坏(3)- Quinuclidine酰胺
一个相关的例子是酰胺quinuclidinone“桥头堡”。虽然乍一看可能不会看起来很奇怪,当你构建一个模型你看到氮孤对指出在一个奇怪的角度防止重叠相邻羰基。右边的晶体结构(从本研究教授Brian Stoltz加州理工学院)使轨道重叠的缺乏更明显。
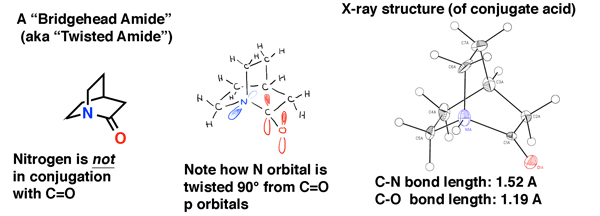
还记得Bredt法则关于桥头堡烯烃不稳定?也是如此的酰胺氮桥头堡。为了“部分双键性格”在共振形成,必须有轨道重叠,Bredt的工作显示,合理的轨道重叠极其微弱的小环的大小。
- α-AMINODIETHYLACETIC酸
Steiger罗伯特·E。
Org。Synth。1942年,22, 13
DOI:10.15227 / orgsyn.022.0013
对酸酰胺水解的一个例子,这个过程在有机合成是相当典型的。浓盐酸的主要酰胺是回流2.5小时获得的羧酸。 - 酰胺水解的催化效率。两步机制
理查德•l . Schowen和拉里·h·Jayaraman创作
美国化学学会杂志》上1966年88年(14),3373 - 3375
DOI:10.1021 / ja00966a034
机械的基本的酰胺水解的研究支持两步addition-elimination机制。 - 合成和结构分析的2-quinuclidonium tetrafluoroborate
Kousuke塔和Brian m . Stoltz
自然441年,页面731 - 734 (2006年)
DOI:10.1038 / nature04842
合成和结构极其不稳定的“扭曲”酰胺Stoltz和塔,与晶体结构完整。
谢谢你詹姆斯先生!很有帮助!
你好,詹姆斯,
我不懂最后注意意味着什么。你能解释一下吗