醇、环氧化合物和醚
威廉姆森醚合成:规划
最后更新:2023年7月8日|
计划一个威廉姆森醚合成:避免陷阱
- 威廉姆森的醚通过一个年代综合收益N2机制
- 当规划的合成醚威廉姆森,记住N2适合初级和甲基的反应烷基为三级卤化物和失败烷基卤化物。
- 此外,年代N2反应根本不工作烯基或芳基卤化物。
- 这意味着,在某些情况下肯定有“正确”和“错误”的方式来计划使用威廉姆森醚的合成。
表的内容
1。威廉姆森醚合成:逆向思考
在最后发表我们介绍了威廉姆森醚合成,我们所知道的最简单的方法之一进行醚。如果你一直在战壕里的时间足够长,你也会发现其实没有什么新-威廉姆森只是“重塑”反应我们之前看到的,年代N2之间的反应醇盐(RO)和一个烷基卤化物(r×)。(看到帖子:的年代N2机制)
(注:1850年威廉姆森报道反应时他不知道一个年代N2——科学家们甚至不知道电子是什么,对于这个问题——这再次表明有机化学的科学发展首先通过大量的实证观察,和理论的发展。]
我们经常会在需要的位置计划的合成醚利用威廉姆森(这是一个非常受欢迎的考试的问题]。今天我们要应用我们所知道的关于这个反应想向后。这将是很好的训练过程中多次之后,你会被要求计划日益复杂分子的合成。
这就是我们今天要讲的:
- 威廉姆森的审查机制醚合成
- 显示两个容易计划威廉姆森的例子
- 显示两个更加困难计划威廉姆森的例子,以及如何避免最常见的错误
2。威廉姆森醚合成的机制
正如我们上面所说的,威廉姆森只是一个年代N2之间的反应醇盐和一个烷基卤化物。这是机制。
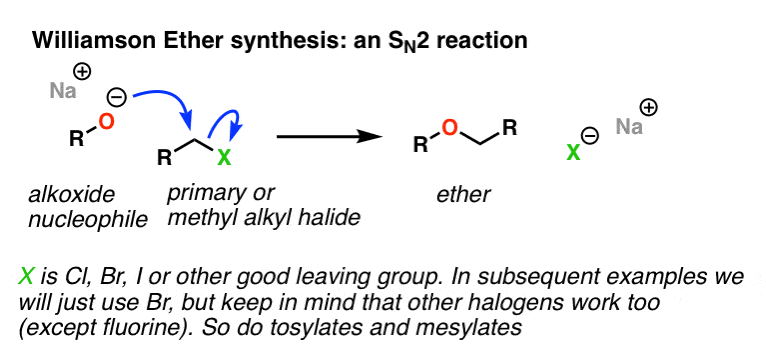
这里是一个很好的“X”离去基团,如氯、溴,OTs或网络营销峰会。我喜欢展示具体的例子,而不是“X”,所以在下面的图片中,我将使用Br,但请记住,他们工作很好如果您使用任何其他离开组织我刚才提到的在前面的句子。只是不使用F。
最重要的几点是什么年代回忆呢N2反应?
- 这是一个非常简单的反应:一个键形式在碳和债券休息时间在同一碳。
- 因为它通过一个背后攻击的亲核试剂在烷基卤,“大障碍”(h / t史蒂文)是“位阻”。减少的速度烷基甲基卤化物从初级到中级三级
- 年代N2反应不进行在所有三级烷基卤化物。他们也不使用烯基或炔基卤化物(如卤素在哪里可以直接附着在碳碳双键或三键)。
记住这些因素,威廉姆森醚合成涉及三级烷基卤化物或烯基卤会失败。
3所示。规划威廉姆森:两个简单的例子
我们来看第一个例子(乙醚向后)和工作。我们怎样才能使这个分子通过一个年代N2反应?
我们需要一个亲核试剂(醇盐)和一个亲电试剂(烷基卤)结合取代反应形成乙醚。让我们“打破”的一个切断债券乙醚和策略离去基团(Br在这个例子)。
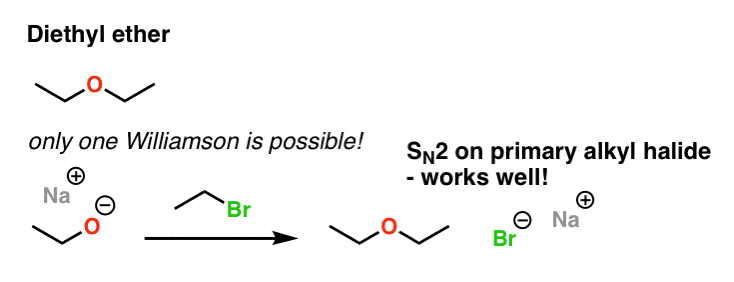
请注意,这是对称的。无论你选择什么切断键形成过程的年代N2的反应,你应该得到相同的起始原料。
在这个例子中我们有一个年代N2之间乙醇盐离子和一个乙卤。这是唯一可能的方式使用威廉姆森这个分子。这是一个完美的年代N2反应,因为亲电试剂是一个主烷基卤化物。
我们的下一个例子是甲乙醚(“methoxyethane”)。注意,与乙醚,这是不一个对称的分子。
因此我们可以有两个可能的切断债券形式的年代N2反应产生的醚。
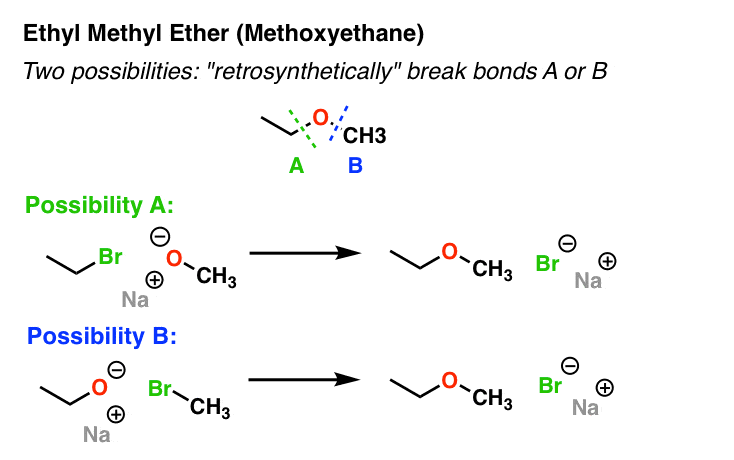
我们叫他们(绿色)和B(蓝色)。想象起始原料将是必要的N2形式的债券,然后想想起始原料将是必要的N2形成债券b,我们称之为“retrosynthetically”(reverse-synthesizing,如果你愿意)打破这些债券。
- 甲醇可能导致我们之间的反应(CH3O- - - - - -)和一个主烷基卤素(溴乙烷在这个例子)。
- B可能导致我们之间的反应乙醇盐(CH3CH2O- - - - - -)和甲基卤化物(甲基溴这里)。
这两个年代N2反应应该很好地工作。所以没有“错误”的方法,使这个分子通过威廉姆森在这里。
4所示。规划一个威廉姆森可以去哪里错了吗
在前面的例子是没有“错误”的方式计划通过威廉森合成醚的合成。它并不总是那么简单。
让我们看看乙基叔丁基醚为例。与甲乙醚有两种可能的方法,“断开”我们所需产品为起始原料。让我们称之为路径和路径B。
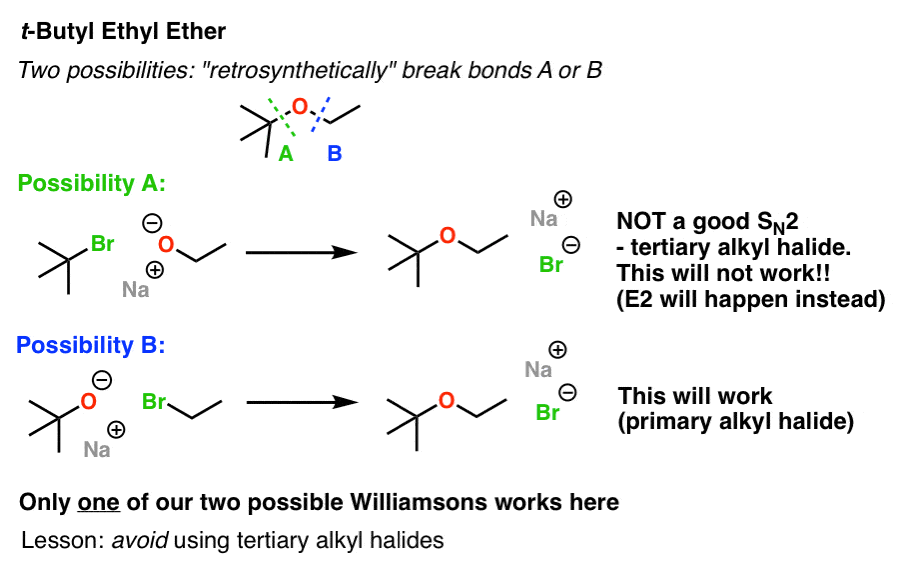
- 涉及到的可能性N2乙氧基金属(CH3CH2O- - - - - -)和叔丁基溴化。
- B可能涉及到N2 t-butoxide之间[(CH3)3有限公司- - - - - -)和溴乙烷。
你注意到错了吗?其中一个年代N2反应不会工作。
这绝对是一个“正确的方法”和“错误的方式”来构建使用威廉姆森这个分子。如果你计划一个年代N2,涉及一个三级烷基卤,你做错了。
和之前一样,让我们把它分成两个可能性。
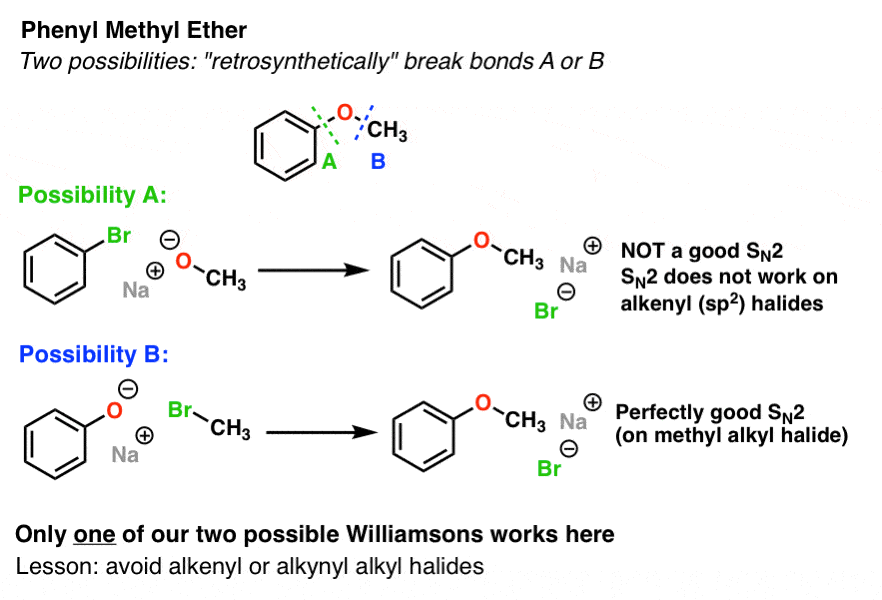
- 涉及到的可能性N2甲氧基(CH3O- - - - - -),苯基卤化物。
- B可能涉及到N2的酚盐(越南河粉- - - - - -)与甲基卤化物。
这年代N2是要更好的工作吗?
如果你说可能性B,你是对的。再一次,可能不行,因为我们会努力执行N2在一个sp2杂化碳。这些不是有效的。的年代N2是一个反应,只有有效的sp3杂化碳原子。
5。摘要:避免规划N2叔或芳基卤化物的反应
这里的底线是,你应该计划的合成醚以同样的方式使用威廉姆森你计划任何年代N2。
打破你的选择醚的方式允许您使用,理想情况下,一个甲基或主烷基卤化物。避免任何需要采用三级或合成烯基卤化物。
我们并没有真正涉及二次烷基卤化物。他们是边缘型威廉姆森和不清楚的选择。
这引出了一个问题。如果我们要合成一个醚像这样的吗?

显然,威廉姆森。那么我们该怎么做呢?
答案,我们会看到在接下来的帖子,将涉及更多的似曾相识Org 1。
想想一会儿。氧气与叔碳原子。
你能想到一个反应吗更喜欢叔碳原子作为起始物料(主要)?
下次回答。
在下一篇文章:醚的合成(2)——回到未来!
在叔丁基乙醚的合成,我认为B的产品可能是不正确的。对吧?
有一个错误,现在已经修好了。谢谢你!
你好,
K2CO3如何作为一个基地,这个反应?
它在某些方面有益的吗?
谢谢
K2CO3 deprotonate酒精导致醇盐,这是比自由更亲核的酒精和将执行的SN2反应更快。
合成叔丁基乙醚,你有错误的产品
是的,谢谢你。固定的。
感谢你让这容易理解!你太棒了。
很高兴你找到网站有用Mellisa !
在最后一个例子中,B,可能性为什么负电荷氧烷基卤化物攻击?我认为亲核攻击应通过碳(碳负电荷通过共振)。
为了支持这一点,我可以提供两个原因虽然基本上相同。
1。(C)是一个更好的亲核试剂(O)
2。(C)比(O)和软基地的网站也是一个软酸性网站的攻击。
如果我错了,请纠正我。
谢谢。
不。你需要回去复习亲核取代。我们不应对负碳离子。碳在CH3-Br是亲电。
我认为你的叔丁基乙醚可能性B错产品了。不应该是一个乙基叔丁基醚代替甲基乙醚吗?
这幅画里没有第三合成错误?有一个坏产品! ?
是的,固定。谢谢!
我有点困惑之间的SN2 t-butoxide和溴乙烷。我认为t-butoxide是一个庞大的基地,这将导致E2反应。为什么它为SN2工作吗?
嗨——t-butoxide和卤代烃,SN2可以工作(尽管你可能有一些E2副产品,特别是如果你加热)。这是二级烷基卤化物,得到更多的消除。
是甲基或苯基一个更大的障碍?例如2-ch-ch2-O-ch2-Ph (ch3)
你比较苯,异丙基,而不是甲基。如果你通过为位阻的值作为一个代理,然后异丙基(一个值2.15)不如苯sterically笨重(值3.0)。https://en.wikipedia.org/wiki/A_value
“…烯基、炔基卤化物”:也许你应该包括芳基卤化物,使用术语“芳基”在谈到苯甲醚。同时,快速校对这篇文章可能是有用的。
但否则伟大的工作,像往常一样