焊接、结构和共鸣
如何确定杂交:捷径
最后更新:2022年12月28日|
一个确定的快捷方式杂交一个原子的分子
这是一个如何的快捷方式确定杂交一个原子的分子将工作在至少95%的情况下,你看到Org 1。
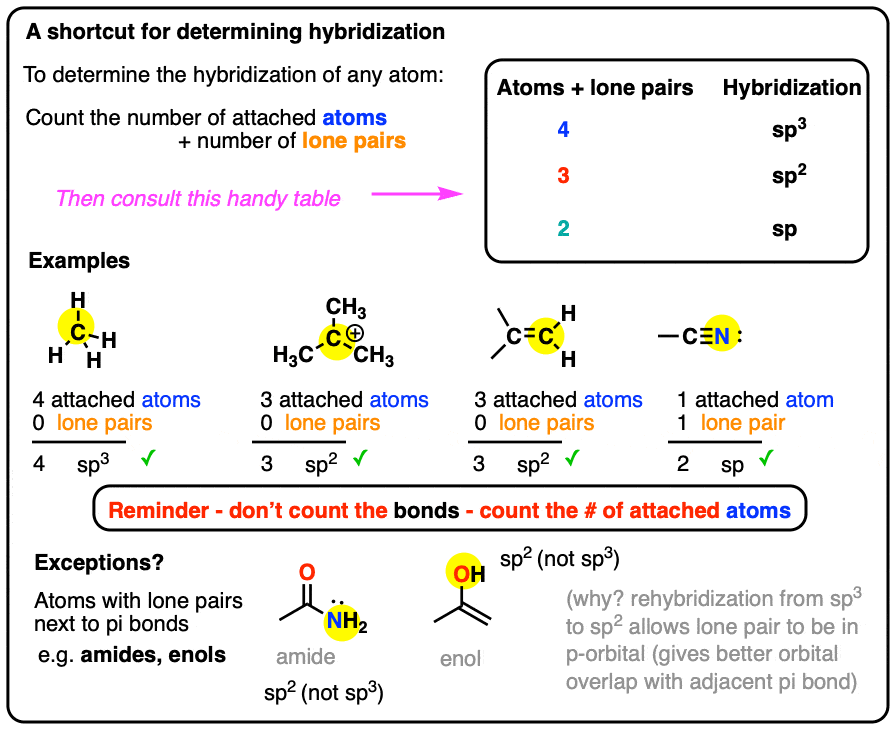
对于一个给定的atom:
- 数的数量原子连接到它(原子-不是债券!)
- 数的数量孤连接到它。
- 添加这两个数字加起来。
- 如果它是4,你的原子sp3。
- 如果它是3,你的原子sp2。
- 如果它是2,你的原子sp。
(如果是1,可能是氢!)
主要的例外是原子的孤相邻π键,我们将在下面详细讨论。
表的内容
- 一些简单的例子杂交工作的捷径
- 如何确定一个原子的杂化:两个练习吗
- 有什么异常吗?
- 除了# 1:孤毗邻π键
- 孤对p轨道(与杂化轨道)与相邻π系统有更好的轨道重叠
- 异常# 2。几何约束
- “几何确定杂交,而不是反过来”
- 笔记
1。一些简单的例子杂交工作的捷径
sp3杂交附加:笔原子+孤=4
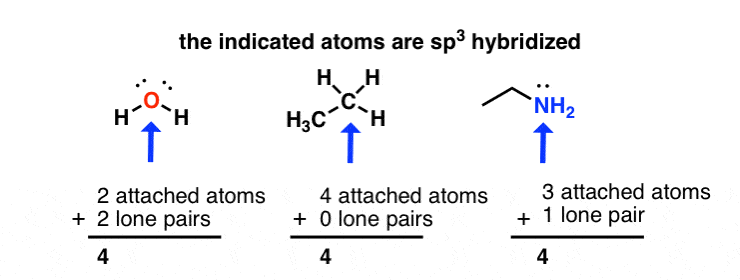
sp2杂交附加:笔原子+孤=3
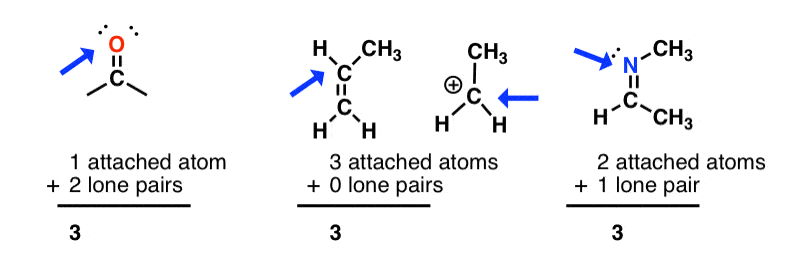
sp杂化附加:笔原子+孤=2
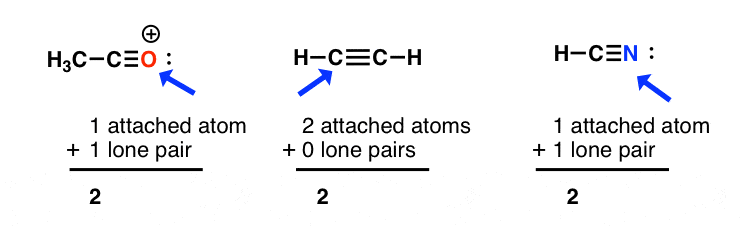
可以开始变得稍微棘手的是在处理直线图呢含隐式(“隐藏”)的氢和孤。
化学家省时快捷方式就像其他人一样,和学习来快速解释行图一样的基础有机化学学习字母表是书面英语。
记住:
- 仅仅因为孤不画在氧、氮、氟不意味着他们不存在。
- 假设一个完整的八隅体C、N、O和F以下一个例外:碳表明只有一个正电荷六个电子围绕它。(氮和氧气轴承的形式电荷+ 1还有完整的八位字节)。
(高级:注1介绍了如何确定杂交原子在自由基等一些奇怪的情况下,碳烯和氮烯)
2。如何确定一个原子的杂化:两个练习吗
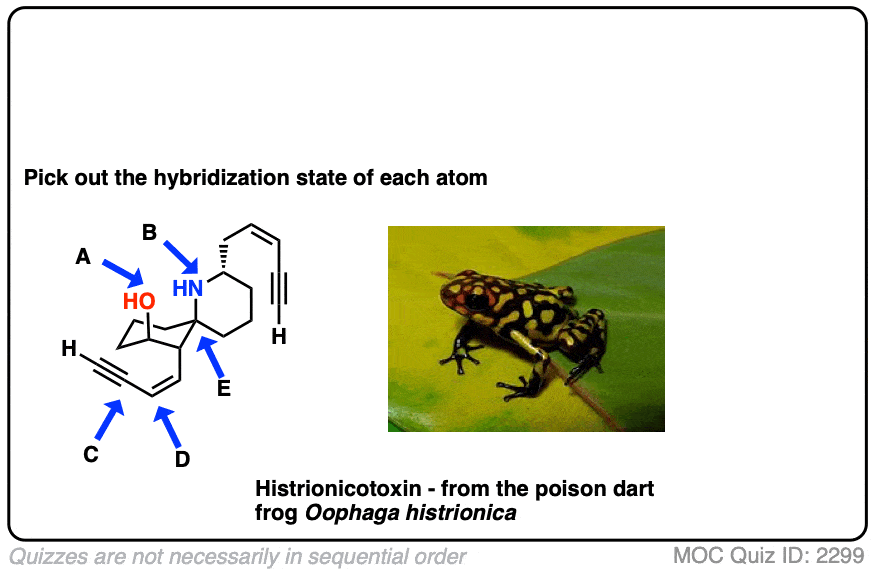
这是一个锻炼。试着挑选杂交这个高度有毒分子由原子的青蛙在时髦的睡衣,下面正确的。
(别担心如果分子看起来有点疯狂:只关注单个原子箭头指向(A, B, C, D, E)。A和B。如果你还没有掌握线路图(和“隐藏”氢)也许得到一些更多的练习,以后回到这里。)
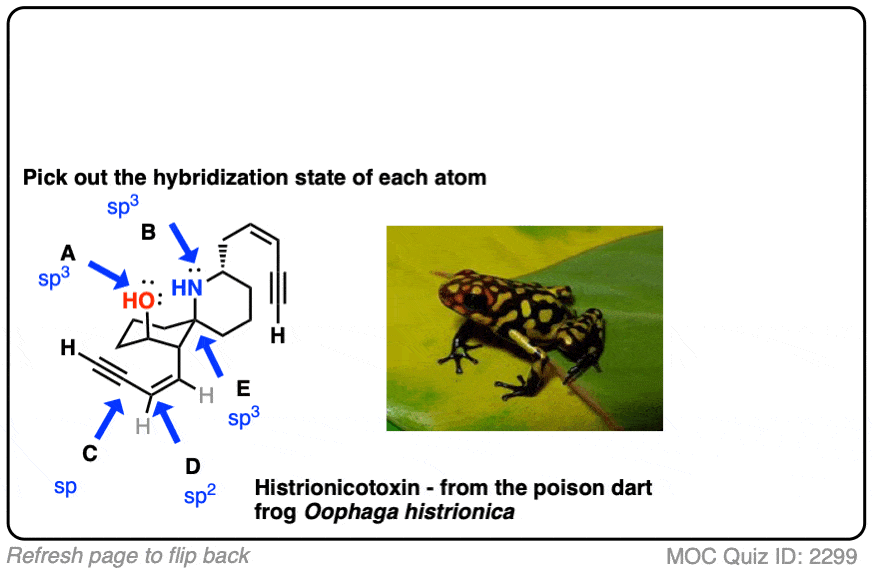
 点击翻转
点击翻转
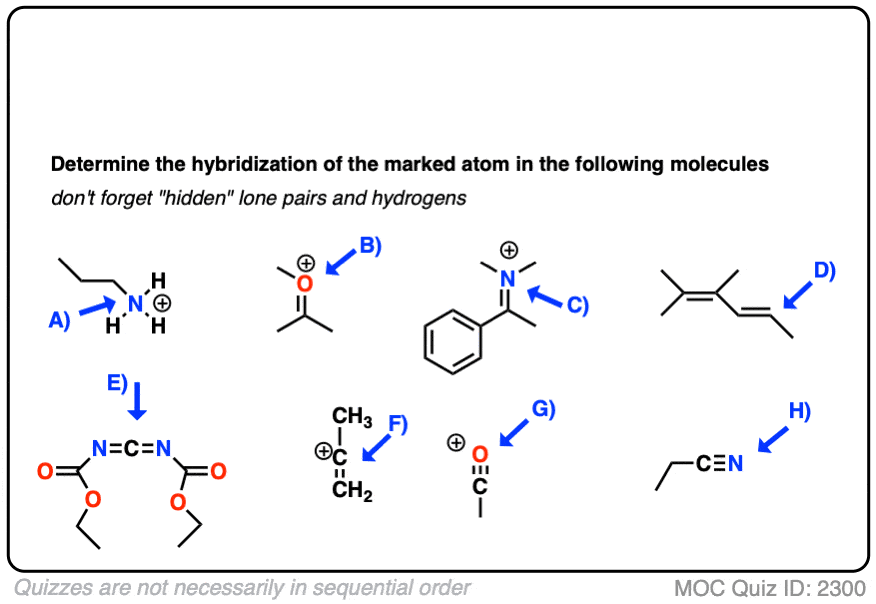
这里有一些更多的例子。
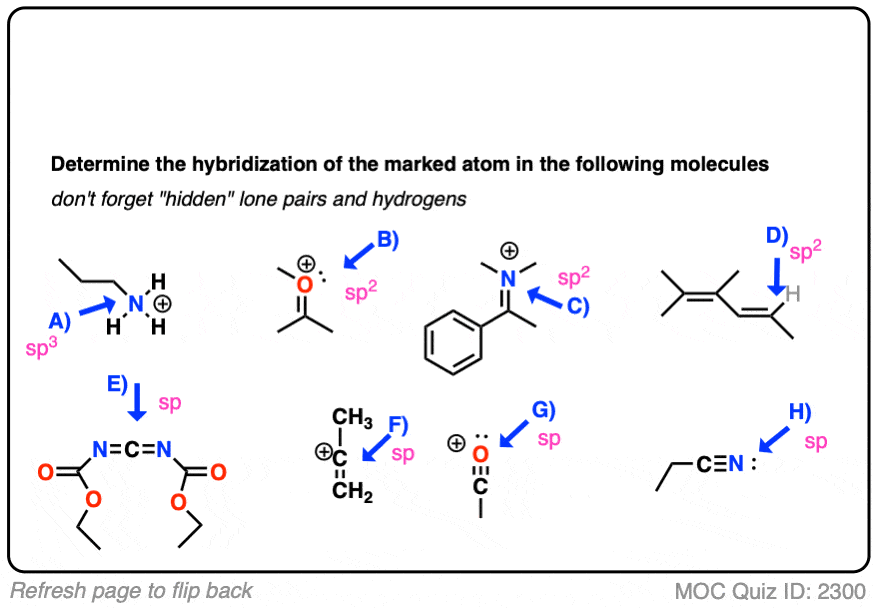
 点击翻转
点击翻转
3所示。有什么异常吗?
确定。虽然与许多事情一样,解释快捷大约需要2分钟,而解释异常需要大约10倍的时间。
有益的是,这些异常分为两大类。应该注意的是,当你解释了为什么这些例子是例外,它可能已经远远超出杂交。
底线:这些可能不会被发现在你的第一个期中考试。
4所示。除了# 1:孤毗邻π键
主要的例外是原子的孤毗邻π键。
快速快捷方式:孤毗邻π键(pi-systems)往往是在的unhybridizedp轨道,而不是在杂化spn轨道。
这是最常见的氮和氧气。
在以下情况下,氮气或氧气,我们可能期望sp3杂化实际上是sp2杂化(三角形平面)。
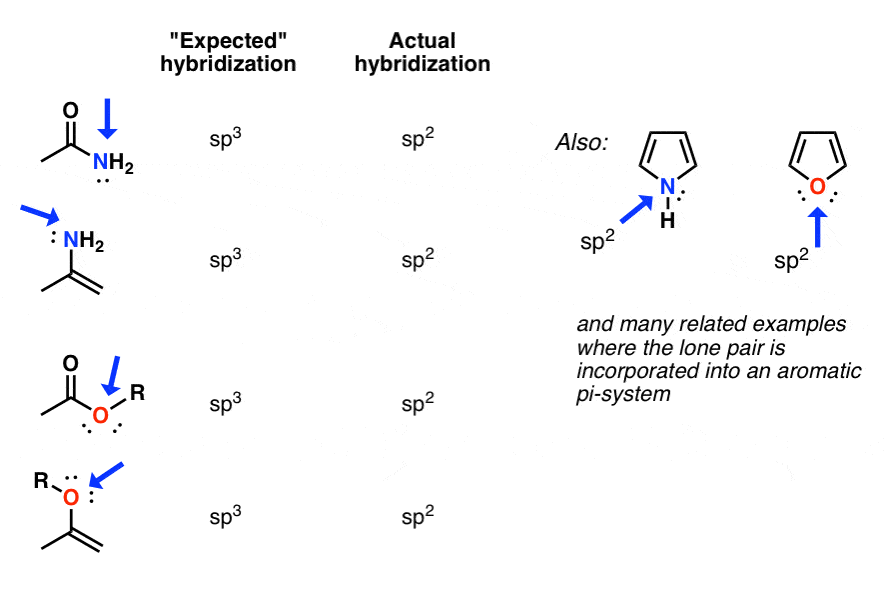
为什么?快速的答案是,能量的降低结合p轨道的相邻的π键超过补偿能量的增加,由于更大的电子对sp的排斥2与sp3
这篇文章(参见:“结合和共振”)
长答案是什么?
5。孤对p轨道(与杂化轨道)与相邻π系统有更好的轨道重叠
让我们回想为什么原子杂化首先:电子对排斥的最小化。
对于一个主要胺如甲胺,采用四面体(sp3由氮和三角形平面(sp)几何2)几何是价值约5千卡每摩尔(约20焦每摩尔)。
可能听起来不是很多,但对于两个物种处于平衡状态,5千卡每摩尔的差异在能源代表的比率4400:1]。(我们怎么知道呢?看到这个(高级)注2在氮反演)
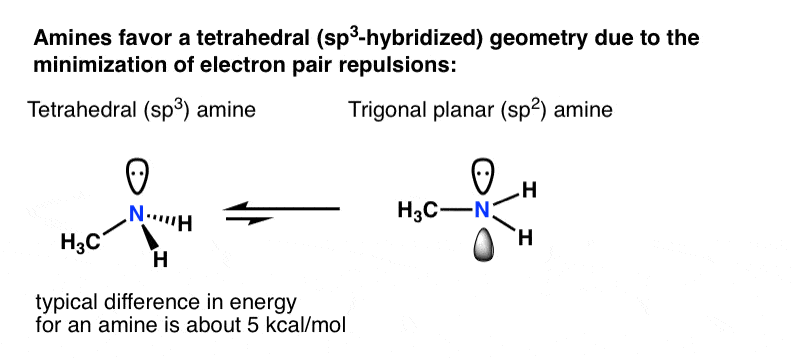
如果有一些补偿效应,孤对unhybridized p轨道实际上是比如果是更稳定在一个杂化轨道?
原来是这样,在许多情况下孤对毗邻π键!是最常见的和重要的例子酰胺,这构成了氨基酸之间的联系。氮酰胺平面(sp2),而不是三角形金字塔(sp3),如x射线晶体学证明。
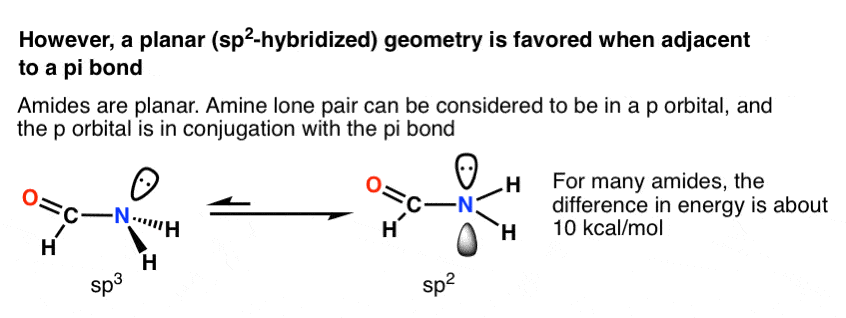
能量的差异变化很大,但一个典型的值是10千卡每摩尔偏袒三角形平面几何。(我们知道这个,因为许多酰胺旋转的可衡量的障碍我们还谈到一个话题结合和共振邮报》)
为什么三角形平面几何青睐呢?更好的轨道重叠p轨道的π键与sp(杂化)3轨道。
下面的图试图展示如何改变杂交从sp3对sp2将p轨道接近临近的p轨道的π键,允许更好的轨道重叠。更好的轨道重叠允许强pi-bonding孤对氮和之间羰基p轨道,这将导致一个总体降低的能量。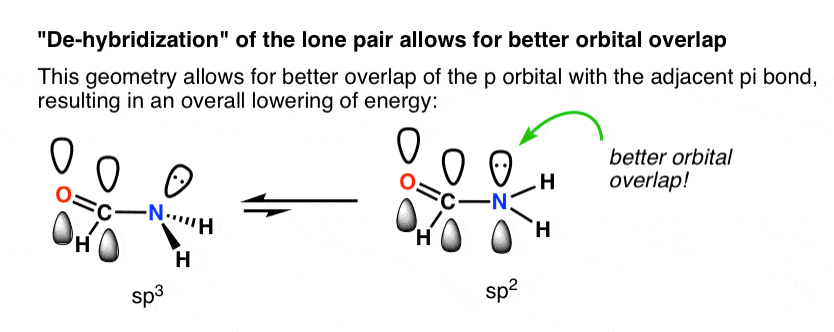
你可以认为这是导致一个更强大的“部分”碳氮键。这种交互的两个重要的后果限制旋转酸酰胺,以及事实与酰胺反应的氧气,而不是氮孤对(!)
中的氧气酯类和烯醇也还sp2杂化,氮烯胺和无数的其他例子。
你可能会看到在Org 2中,一些最引人注目的情况下是那些“de-hybridized”孤对参与芳香系统。这里的能量补偿的改变杂交从sp3对sp2可以非常大,在某些情况下超过20千卡每摩尔。
出于这个原因,最基本的吡咯氮孤对,但在碳(c - 2) (!)。
6。异常# 2。几何约束
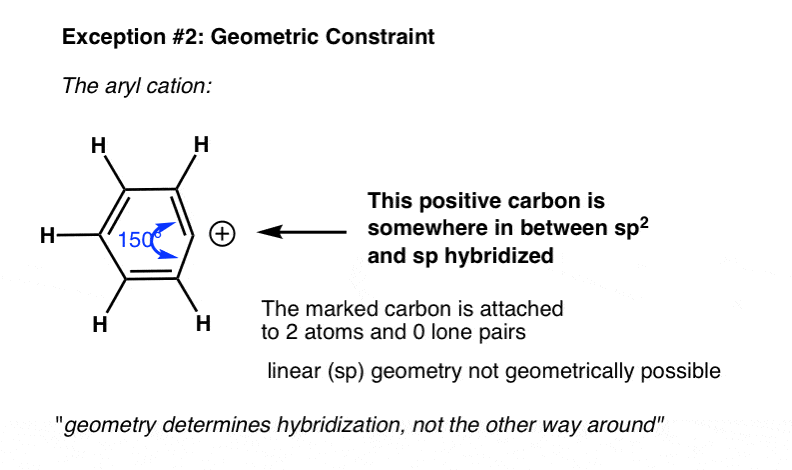
另一个例子的实际杂交不同于我们可能期望从快捷方式与几何约束的情况下。比如在苯基在下面的阳离子,表示2连接两个碳原子和零孤。
是什么杂交吗?
从我们的快捷方式,我们可能期望杂交是sp。
实际上,原子周围的几何形状更接近于sp2。这是因为角应变采用线性几何(sp)会导致太多角应变是一个稳定的分子。
7所示。“几何确定杂交,而不是反过来”
引用传递给我马特似乎是适当的:
“几何形状决定杂交,而不是反过来”
嗯,这可能是比你想知道如何确定杂交原子组成。
足以说,本网站的任何帖子标题中包含快捷方式确定fire-bet有超过1000单词和> 10位数。
由于房产中介公司的马特•皮尔斯有机化学解决方案这篇文章重要贡献。问马特调度在线辅导会议在这里。
笔记
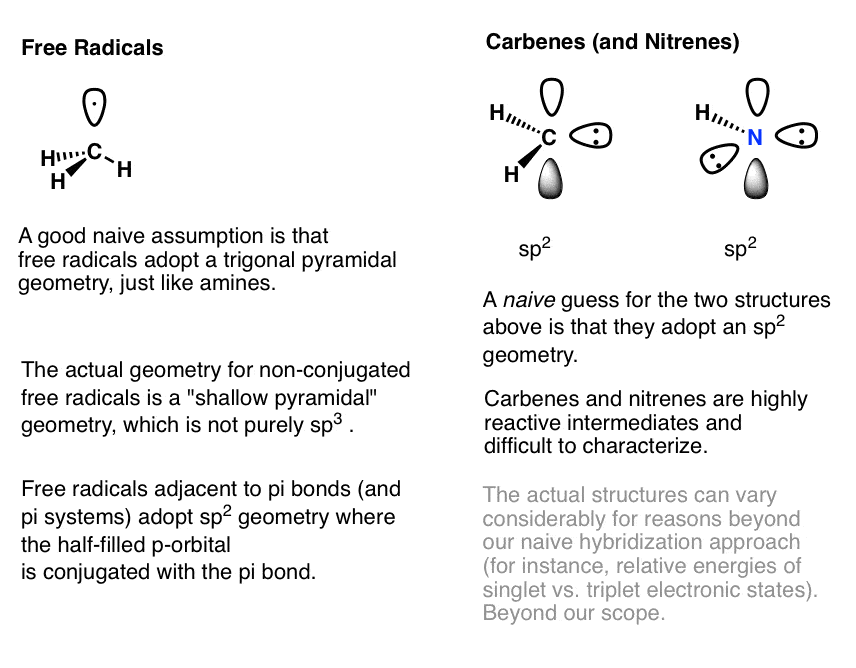
有时你可能会被要求确定杂交的自由基和碳烯(或氮烯)
虽然你可能遇到这些,我们还有一看。
- 自由基的存在浅锥体几何,而不是纯粹的sp2或sp3。
- 然而,如果他们相邻π体系(如碳碳双键或三键),那么肤浅的金字塔re-hybridize给它一个sp2几何,它允许共振移位的自由基。
- 碳烯和氮烯会给我们sp2几何形状的杂交快捷方式。然而他们的实际结构可以取决于电子对是否存在于一个轨道(a单线态碳烯)或分为两个singly-filled轨道(a三联体碳烯)。这是真的超出了介绍有机化学的范围。
块元素如硫和磷高呢?
第三行元素,如磷、硫可以超过一个八电子结构,通过加入混合d轨道。这是在无机化学领域的所以我不想讨论它。这里的一个例子杂交的科幻小说4从在其他地方。(sp3d轨道)。
注2:5千卡每摩尔图,在这里看到的。1971年[四面体,37,3437]。(Kurt Mislow把)。
一个胺连接到三个不同的取代基(R1R2和R3)应该手性,因为它总共有4种不同的取代基(包括孤对)。不过,所有的光学纯早期的尝试做准备胺遇到失败。后来发现胺接受反演在室温下,就像一把伞被大风迫使由内向外。
在反演的过渡态氮是三角形的平面。一个可以计算sp之间的能量差3和sp2几何图形通过测量激活这个过程(见的障碍裁判)。
注3:一个有趣的反例Coelenterazine。
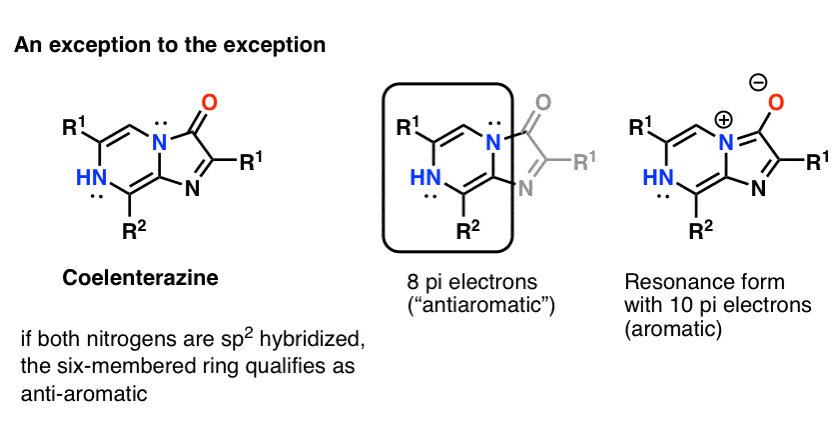
一个不会期望两个氮原子sp2杂化,因为这将导致循环,平坦,与8π电子共轭体系:换句话说,antiaromatic。我找不到一个晶体结构的核心分子确认(但会欢迎任何附加信息!)
(注)-添加之后如果你画的共振形成氮孤对形式的π键羰基碳,然后环系统有10个电子,因此会“芳香”。
- 障碍锥体dibenzylmethylamine反演的氮
迈克尔·j·s·杜瓦和w·布莱恩·詹宁斯
美国化学学会杂志》上1971年93年(2),401 - 403
DOI:10.1021 / ja00731a016 锥体反演障碍:基态几何的重要性
约瑟夫·斯塔克豪斯,雷蒙德·D。Baechler,库尔特·Mislow
四面体的信问题37卷12日,1971年,3437 - 3440页
DOI:doi.org/10.1016/s0040 - 4039 (01) 97199 - 0
谢谢你的好的文章,像往常一样。
我认为有一个错误在第一部分点5和图片;几何图形是三角形金字塔而不是四面体。
很有帮助谢谢先生
谢谢youuuuu ! ! !你真的帮了我的实验室报告讨论有机化学是明天到期。你可以有一个讨论的影响π系统?我期待着它!
我可以问为戊烷的碳杂化和π体系的影响。
戊烷,C5H12 ?四面体碳,sp3杂化
我不知道说什么真的有助于我能够理解,非常感谢你
嗨,詹姆斯!首先,非常感谢你的解释的杂交!在这里我有一个问题。它说如果原子的孤对π键,rehydridization会发生所以我们不能使用上面的指令。所以我们如何能确定一个原子与孤对π键。谢谢你!
嗨,最熟悉的例子就是哦的孤群羧酸,R-CO2H。以来哦氧气sp2杂化原子的孤对毗邻一个π键(即C = Oπ键)。
另一个例子是一个酯,R-CO2CH3。在这种情况下氧上的孤对轴承CH3(例如O-CH3)是sp2杂化,因为它毗邻一个C = O键。
酰胺、电阻-电容(O) - nh2 sp2杂化氮,由于氮上的孤对毗邻一个C = O键。
带负电的碳烯丙基阴离子是sp2杂化。
更多的例子,但这些都是少数。
这是一个伟大的评论!多年来我没有做氮杂化,需要快速复习。谢谢! ! !
由于卡拉
如何确定杂交的N原子3号在咪唑环图吗?:https://upload.wikimedia.org/wikipedia/commons/thumb/b/b8/Imidazole_2D_numbered.svg/110px-Imidazole_2D_numbered.svg.png
因为几何,你期望它sp2杂交,但是还有一个相邻的π键系统(C4和C5),所以你会希望它是sp杂交(孤对占据了p轨道,可以接受与C = Cπ轨道共振)。
教学是如此美妙的艺术。很清楚,一步一步的解释。向您表达我最衷心的感谢。我祝贺进一步继续您的服务。
我想知道将杂化碳正离子ethynylium离子或乙炔基碳正离子。
你好詹姆斯,谢谢你的简洁直白的解释这些异常。我今年秋季教学orgo课程,准备向学生解释这个感觉更好。
很高兴听到它,CK,很高兴你有帮助。
这就跟你问声好!首先,我想说,我发现你的帖子非常有用,当然大多数有机化学我学到的技巧。阅读这篇文章和研究主题我想到了偶氮苯和氢化偶氮苯的结构,我希望他们spbdapp平台2和sp3,分别,但由于他们有苯环上连接到每个氮,这些杂交过程会有效吗?
你好,谢谢你这么多的深入解释。我想问如果例外# 1(孤毗邻π键)适用于N原子HCN吗?这是一个例子包括在第一节sp,但我想澄清因为我发现的资源冲突。呵呵,非常感谢,先生!我希望你是好和安全。
HCN的N原子是sp杂化。一个sp轨道是氮σ键,和其他有孤对氮。在任何条件下氮上的孤对参与共振,因为这会导致氮物种周围6个电子(不到一个八位字节),这是非常不稳定!
如果原子连接到它的数量和孤对为什么添加超过四个,总共你称这种类型的杂交
我会小心应用杂交概念的债券在第三行,如硫,超过八隅体。
节省时间的概念
非常感谢这个信息。我到处都找遍了,但没有任何这些异常的杂交。
很高兴你有帮助!
很有帮助!谢谢:))
很高兴你有帮助!
谢谢你清楚的解释为什么旁边的N和O原子π键或系统宁愿sp2杂化。给了我作为一名非有机化学教师更深层次的认识。
你是欢迎Willetta。谢谢你停下来。
再次感谢!我终于获得了一些设施在这多亏你深刻理解加上你非常清晰的写作。
约翰很高兴听到它。谢谢你!
你,先生,是一个巨大的帮助和信贷的职业教育。谢谢你,谢谢你!
的1 H - nmr coelenterazine (DOI: 10.1021 / ct300356j)显示两个信号在9.13(年代,1 H),和6.44 (b, 1 H),这表明该系统是共轭羰基使得平面和芳香在考虑整个双环系统。你可以观察到类似deshielding效应,甘菊蓝的质子7-membered戒指。
现在我看一遍,你是绝对正确的。谢谢维克多。
“第三行元素,如磷、硫可以超过一个八电子结构,结合d轨道的混合。”
这是不正确的,被证明是错的年前。看到http://pubs.acs.org/doi/abs/10.1021/ja00273a006和引用引用。更准确和更直观的继续遵循的八隅体规则硫,磷,和其他重型主族元素。SF4,例如可以表示成四个大盘共振结构的形式[SF3] + [F] -,给整个0.75每个S-F键的键序。这种方式,每个原子的八隅体规则在每一个共振结构。当然,你总是可以用分子轨道理论结合symmetry-adapted原子轨道的线性组合,然后你不需要处理“扩大八位字节”hypercoordinate分子。
是的,没有。
本质上没有什么错误的短语本身“hypervalent”原子一样使用在某种程度上更高的轨道。它是更重要的轨道参与整体焊接方案。不,没有人,至少有一些杂化的概念的理解,将坚持说,硫在SF4 sp3d杂交将严格意味着我们有100%的参与1 s, 3 p,和1 d轨道成键结构。
同样的参数我们可以带在讨论,说,cyclopropanone。羰基碳的杂化是什么?sp2吗?sp2 +吗?sp2——吗?是介于两者之间吗?的杂交di-central铼复合物与第四纪债券?或谜语我,例如,周期性的确切碘在每个表单的杂交酸;)
当我们承认我们使用的理论的局限性,他们彼此在一个很好的协议,)虽然使用莫是最好的路要走,它不是一般的化学或有机化学教学水平,也就是学生面临考试。