烯烃的反应
烯烃Hydrohalogenation机制以及它如何解释马氏规则的像
最后更新:2022年11月17日|
机制Hydrohalogenation烯烃——理解为什么马氏规则的作品
我们组装所有的事实知道烯烃与酸的反应像HCl迄今为止。然后,我们提出一种机制。
表的内容
- 烯烃与酸的反应(Hydrohalogenation)遵循马氏规则
- Hydrohalogenation反应提供了一个Syn和反产品的混合物
- Hydrohalogenation反应可以进行重组,如氢化和烷基转移
- 提出的机制与所有这些事实一致
- 这种机制如何解释这个反应的区域选择性和立体选择性?
- 再形成的马氏规则。“在烯烃的氢卤化物的反应,反应将继续通过最稳定的碳正离子”。
- 笔记
1。烯烃与酸的反应(Hydrohalogenation)遵循马氏规则
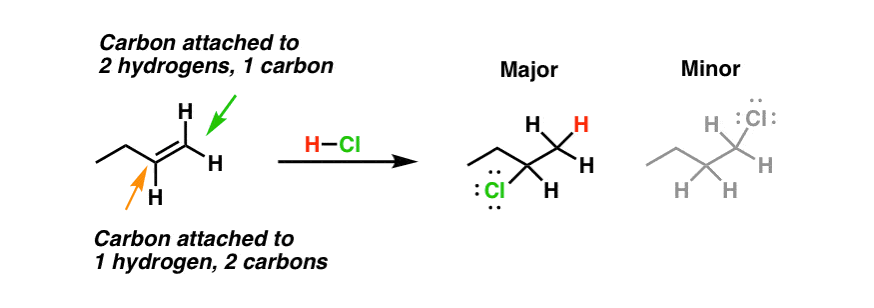
- Regiochemistry:我们看到在过去的帖子,烯烃与酸的反应像HCl跟进马氏规则:这是氢的主要产品形成增加了碳包含大部分的氢。
2。Hydrohalogenation反应提供了一个Syn和反产品的混合物
- 立体化学:正如我们看到的立体化学帖子,这个反应提供了一个“syn”和“反”产品的混合物(当反应物使之成为可能)。
3所示。重组如氢化物和烷基转移Hydrohalogenation都可能发生
- 重组。最后简要介绍了另一个问题。在某些情况下,烯烃的反应与盐酸等酸可以导致重组如氢化物转移或烷基转移。
所以这个反应是如何工作的呢?我们提出的任何机制必须符合所有这些事实。
4所示。提出的机制与所有这些事实一致
此外,我们需要考虑这个反应而言,我们已经知道些什么电子流。电子从高电子密度的区域(“电子丰富”,或“亲核”地区)地区的低电子密度(“电子差”或“亲电”区域)。还记得电子极化的分子喜欢H-Br吗?氢的电负性较小,因此更多的电子差。溴电子的电负性更强,因此更丰富。在烯烃,我们将考虑在相关电子π键,形成一种“π电子云的上方和下方的平面烯烃。
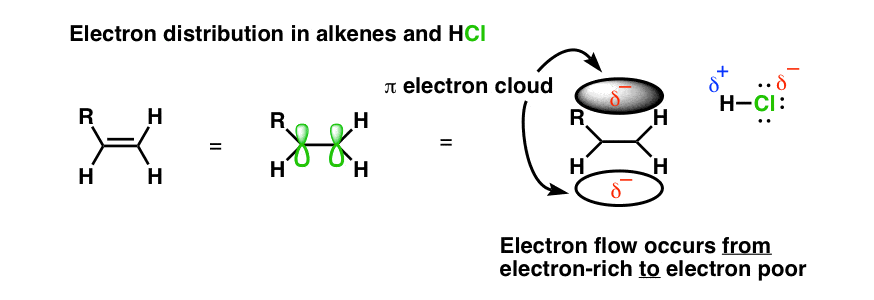
这是我们最好的假设在这个反应是如何工作的。
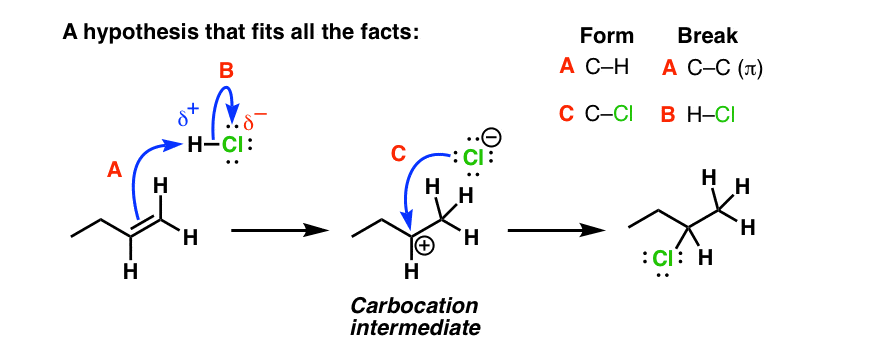
在这个反应,电子从富碳碳流π键电子可怜的氢。(步骤1,箭头)导致破损的氯键(箭头B)。(回想一下,这也不是一个坏的事态Cl -因为它是弱碱,因此一个好的离去基团)。这形成一个中间碳正离子,然后受到氯离子(步骤3,箭头C)导致卤代烷的形成。
5。这种机制如何解释Hydrohalogenation反应的区域选择性和立体选择性?
为什么这个假设符合数据?
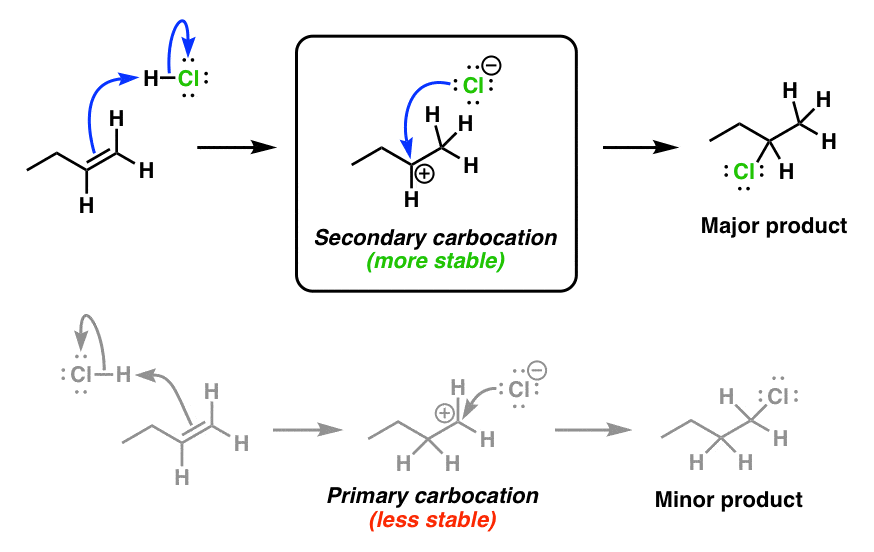
- 区域选择性。我们看到在过去的帖子,烯烃与酸的反应像HCl遵循马氏规则:这是氢的主要产品形成增加了碳包含大部分的氢。这和碳正离子模式是一致的,因为碳正离子稳定性随氢碳原子所取代。
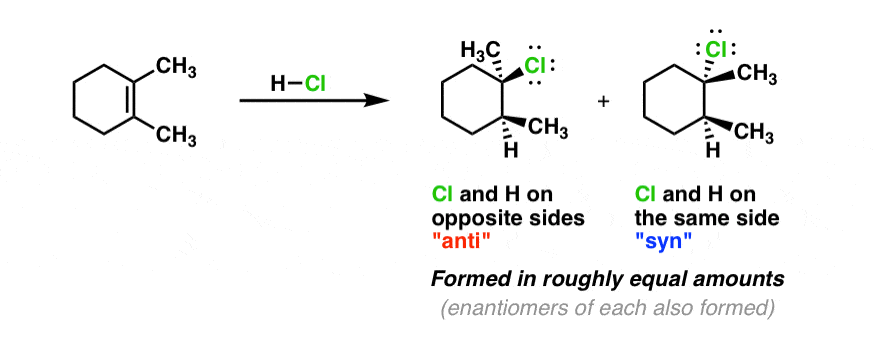
- 立体化学。观察syn和反产品也符合碳正离子中间体。第二步的反应是亲核试剂的进攻(Cl -在这种情况下)的空的p轨道自由碳正离子。因为这可以从两个方向发生(“顶级”或“底”的面孔的碳正离子)我们应该期待syn和反产品的混合物。这就是我们所看到的:
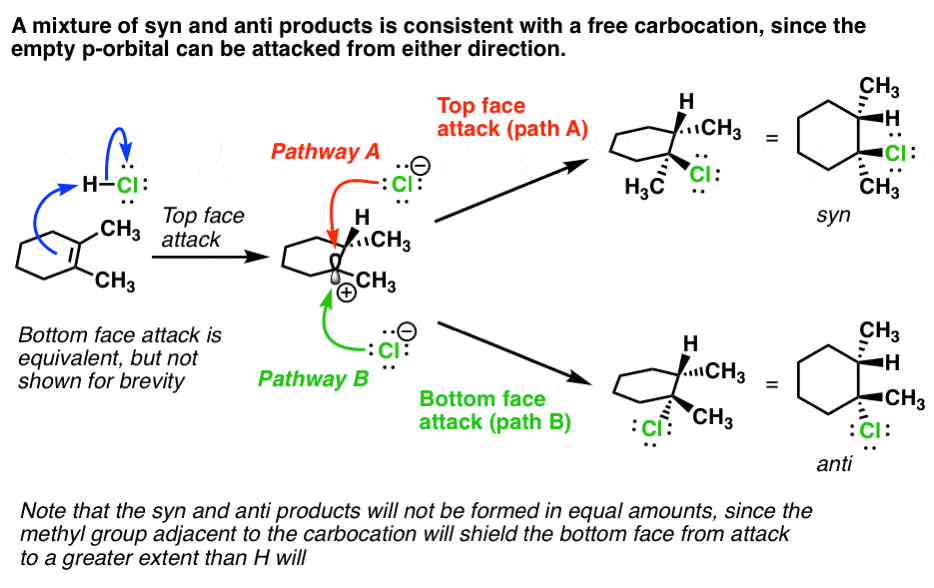
注意,在上面的反应,碳正离子的两副面孔不精确相等。底部的脸是屏蔽的甲基邻碳正离子,它占据了更多的空间比相应的氢在顶面。因此我们应该期待(实际上观察)更多的syn产品相对于反产品。然而,这两个产品还观察到。
6。再形成的马氏规则。“在烯烃的氢卤化物的反应,反应将继续通过最稳定的碳正离子”。
记住这些事实,提出新的假设,我们现在可以提出挖出根据马氏规则。在其前身——马氏规则这是听起来很随意(H增加了碳与氢?为什么?)。在这个描述中,我们可以准确地说为什么这些反应进行。
与氢卤化物烯烃的反应,通过最稳定的碳正离子反应进行。
我们会看到这不仅适用于烯烃的反应与氢卤化物也与其他酸的亲核试剂(比如水和醇)。
最后一个音符。如果你看上图,第一次我们使用箭头推形式显示电子从一个π键流向形成新的sigma键。换句话说,它是作为亲核试剂!这个箭头可能看起来有点奇怪。在下一篇文章我们将更详细地探讨这个。
在下一篇文章:弯曲的箭头和加成反应
你的网站很棒!我总是把它推荐给任何化学的学生,以及克莱因和Freelanceteach。我的问题是:
无论是新的取代基添加氢时(例如,halohydrin形成),如何确定这两个需要更多的取代碳分子被认为是“马氏”吗?总是一个作为亲核试剂的机制(或有某种优先基于原子序数或电负性)?
谢谢老板,我很感激。关于你的问题,这是作为亲核试剂的物种。就是这样。
有* *一个例外,如果你想要斤斤计较,硼氢化反应。叫做“anti-Markovnikov”,它给“anti-Marknovnikov”烯烃水合作用的产物,即使它并不通过碳正离子。
嗨,詹姆斯。
你的文章很好。我非常感动和启发。谢谢。
优。
我很高兴你发现它有用,尤。
非常感谢尤其是sterochemistry部分大多数书籍和其他材料从未接触,我们有一个问题在我们的测试中,我获得了与sterospecificity混淆的反应。谢谢你使它晶莹剔透。我爱你的文章他们化学那么简单。期待你的下一个话题。
非常感谢
Aditya
是的,立体化学分为几个关键模式,一旦你学习模式,这是相当简单的。
在你的照片首先讨论可能的“假说”机制的反应,你有一个错误在你的债券列表。债券形成步骤C应该C-Cl不是八氯,是吗?
如果你看看这个从氧化还原的角度来看,你认为烯烃正在减少盐酸?如果是这样的话,你会说盐酸氧化吗?第二部分是令人困惑。
一个碳原子的烯烃是形成碳氢键(因此减少)。一个碳原子的烯烃形成C-Cl(因此氧化)。*网*基础上,烯烃不减少或氧化,即使各个碳原子。
至于HCl,让我们看看。氢气从连着Cl是连着C H)的氧化态(没有变化。氯从连着H是连着C (Cl)的氧化态的变化。
烯烃反应Br2或技术将氧化氯。
一个碳被氧化(C-Cl债券交易一个碳碳键)和其他碳正在减少(交易一个碳氢键的碳碳键)。净,它不是一个氧化。
期待你的下一篇关于氢化和/或烷基转移。我第一次看到他们的课本,我很困惑。