消除反应
比较E1 vs SN1反应
最后更新:2022年12月2日|
- 醇不发生消除反应,直到哦转化为更好的离去基团
- 添加酸醇会导致更好的离去基团的
- 当竞争淘汰和替换:E1 vs SN1
- 为了让E1支配vsN1反应的醇使用H2所以4、TsOH或H3阿宝4(热)
- (高级)引用和进一步阅读
1。醇不发生消除反应,直到哦转化为更好的离去基团
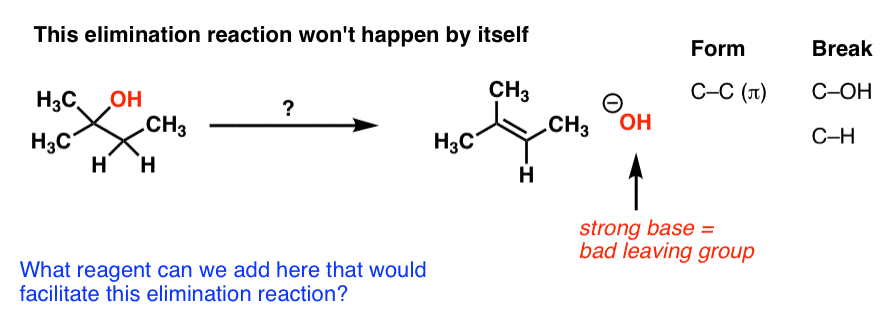
债券所形成和破碎的吗?我们形成碳碳(π),碳氢键,我们打破哦。这是一个消去反应。
注意到一个问题吗?我们需要(-)离去基团。如果你还记得,强大的基地(就像HO(-))是可怕的——这使得离开团体E1途径不太可能。(见文章:是什么让一个好的离去基团)
如果我们试图使用强碱,也许试图推动一个E2反应?嗯,这将是更糟的是,我们可能deprotonate哦碳氢键之前,你可以想象,我们必须有O (2 -)作为离去基团在这里。不是很好!
这意味着反应,写,不太可能发生。
2。添加酸醇会导致更好的离去基团
然而,有一些非常简单的,我们可以做这个反应工作。我们需要一个更好的离去基团(一个较弱的基础)。我们如何做呢?
添加酸!
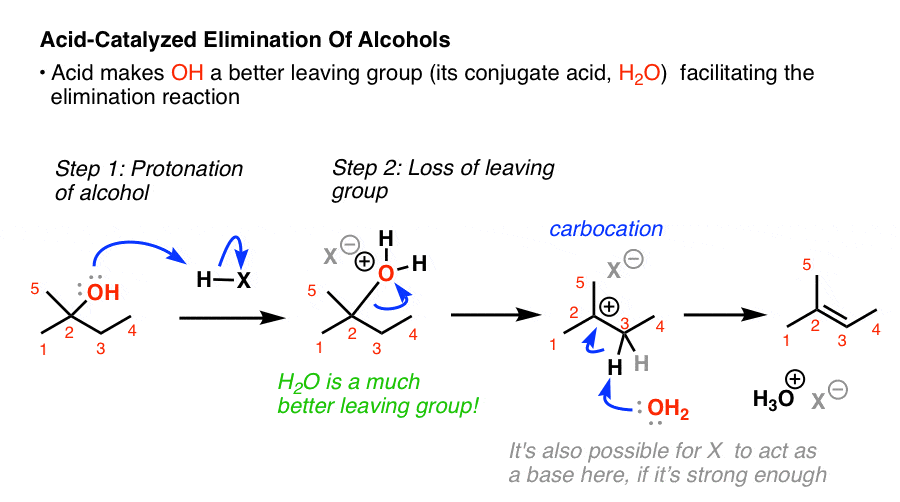
如果我们添加一个强酸,哦变成H2O+,更好的离去基团的共轭酸。现在,水可以离开,形成碳正离子;然后一个基地可以打破碳氢键,形成的烯烃。
请注意,这是现在一个经典E1的反应。率是依赖碳正离子的稳定性。这是三级,所以应该继续以相当高的速度。
一个问题出现了。将作为基础是什么?目前,一个碳氢键相邻碳正离子有极高的酸度(至少低于2,如果你遵循pK一个)。这意味着任何弱碱(水,或共轭碱酸)足以deprotonate碳。有可能不止一个物种可以作为基础。我展示了水把质子,但它不是不合理的共轭碱脱酸的质子在大多数情况下。
3所示。当竞争淘汰和替换:E1 vs SN1
现在有一个关于有机化学的东西,经常给学生造成不必要的麻烦。的第一次在我们的讨论,我们处理情况竞争反应。
让我们后退。的E1通过碳正离子反应,正确吗?好吧,如果你还记得,SN1反应。
我们已经看到的例子碳正离子是由一个在哪里酒精通过添加强酸如盐酸,哈佛商业评论,或嗨,我们结束了烷基卤化物。
为什么?卤化物离子(Cl - Br -,我)是体面的亲核试剂在反应条件下。
所以我们如何能堆栈的甲板赞成E1过程?
通常的选择是H2所以4。HSO汽车贸易公司的4(-)离子是一个相对贫穷亲核试剂由于负电荷的氧气被分布在整个分子(共振)。另外两个酸要达此目的,你可能会看到p-toluenesulfonic酸(p-TsOH),本质上是一个表哥的H2所以4和磷酸(H3阿宝4)。
还有,别忘了,消除反应的热量(见文章:消除反应的热量)
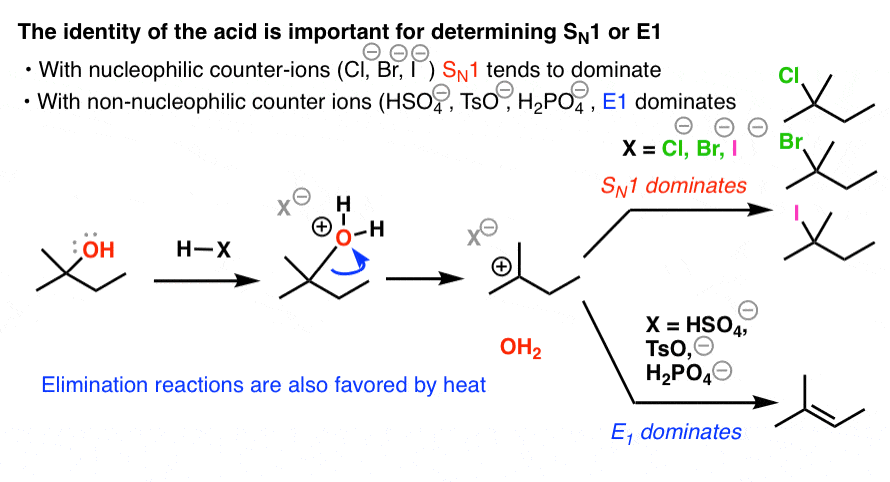
4所示。为了让E1支配vsN1反应的醇使用H2所以4、TsOH或H3阿宝4(热)
总之,如果你想E1来支配SN1:选择一个酸弱亲核反离子(H2所以4、TsOH或H3阿宝4),和热。
如果你想SN1来支配E1,选择一个酸盐酸,哈佛商业评论,或者嗨。
我们几乎完成了讨论消除反应。在下一篇文章,我们将讨论重组。
笔记
(高级)引用和进一步阅读
自E1和SN通过共同的碳正离子中间体1反应同时进行,这些途径可以互相竞争在很多反应条件。
- 在消除离子对
m . Cocivera和Winstein
美国化学学会杂志》上1963年,85年(11),1702 - 1703
DOI:10.1021 / ja00894a046
扫罗教授Winstein(加州大学洛杉矶分校)是一个非常有影响力的早期物理有机化学家20th世纪,现在介绍几个概念有机的基础机制,如anchimeric援助,离子对,内部回报,和许多其他人。摘要Winstein表明教授E1反应有很强的溶剂依赖——溶剂的介电常数(或极性)减少,大量的烯烃也得到降低,因为不能形成碳正离子容易。在无水乙醇、叔丁基氯和溴化给收益率为44%和36%烯烃而在冰醋酸,分别73%和69%烯烃,分别。 - 消除反应的机制。习的一部分。动力学烯烃叔的消除。丁和叔。- - - - - -一个myl bromides in acidic and alkaline alcoholic media
m·l·达·e·d·休斯和c·k·英格尔德
j .化学。Soc。1948年,2065 - 2072
DOI:10.1039 / JR9480002065
的E1综合反应不是很有用烯烃合成,因为消除的比率大大低于在替换产品E2的反应。例如,溶剂分解干燥乙醇收益率只有19%的叔丁基溴化异丁烯,而93%的收益率烯烃获得与乙醇2 m。 - 化学空间压力的影响。二世。结构的影响烯烃形成三级脂肪族氯化物的水解
赫伯特·c·布朗和罗斯林Silber弗莱彻
美国化学学会杂志》上1950年,72年(3),1223 - 1226
DOI:1021 / ja01159a043
本文由诺贝尔奖得主h·c·布朗教授提供了一个完美的研究基质的结构如何影响E1- sN1竞争。一系列的t- - - - - -烷基氯化物的比例烯烃获得在增加80%的乙醇作为溶剂分解烷基组织变得更加高度支化。 - 消除反应的机制。八世。温度影响利率和product-proportions uni - bi-molecular替换和消除反应烷基卤化物和hydroxylic锍盐溶剂
k·a·库珀·e·d·休斯,c·k·英格尔德,b . j . MacNulty
j .化学。Soc。1948年,2049 - 2054
DOI:10.1039 / JR9480002049
英格尔德教授表示:“[. .]对于任何给定的同时有两个分子的过程,消除了在每个调查的情况下,一个阿伦尼乌斯的能量激活位于陪同替换高于1 - 2千卡/ g.-mol。消除因此一直较大的温度系数,所以温度的上升会增加的比例烯烃形成”。温度的增加产生适度的比例增加烯烃在E1- sN1反应。 - 消除反应的机制。第七部分。溶剂的影响率和product-proportions uni - bi-molecular替换和消除反应烷基卤化物和hydroxylic锍盐溶剂
k·a·库珀·m·l·达·e·d·休斯,c·k·英格尔德b和l . j . MacNulty伍尔夫
j .化学。Soc。1948年,2043 - 2049
DOI:10.1039 / JR9480002043
另一个温和的产量增加烯烃在E1- sN1反应被发现从含水乙醇到无水乙醇。 - 消除反应的机制。第二部分。单分子的烯烃形成从sec.-octyl卤化物溶液酒精。新标准的机制
爱德华·d·休斯,克里斯托弗·k·英格尔德和乌列g·夏皮罗
j .化学。Soc。1937年,1277 - 1280
DOI:10.1039 / JR9370001277
本文演示了如何E1和SN1当使用辅助底物竞争反应。2 -溴和2-chlorooctane给的14%左右烯烃当在60%乙醇溶液加热到100°C。
作为一个学生,化学专业教育计划,对我来说很难理解它的E1和SN1反应的不同。谢谢你eexplanation。
在酒精中二级卤化物喜欢SN1机制?
我有一个问题,当你提到的文本,有利于消除热霍夫曼甚至所以总是有效的产品
叔碳正离子或共振稳定的碳正离子反应主要见于SN1…请回答快…
SN1的速率决定步骤是什么?哪些因素影响这第一步吗?
碳正离子可以给一个质子在消除反应基础。E1只是SN1的替代。我说的对吗?
谢谢你!
我不同意,强酸的共轭碱是一个主管基地最后去质子化。它的逻辑,使反应获得一定量的对称(尤其是如果你强调硫酸催化),但恕我直言就是HSO4——太弱的基地是一个称职的基地去质子化。相同的Cl -或TsO或任何其他强酸的共轭基地。班里,就是HSO4——作为一个基地是明显错误的。
(如果真是…+催化,统计水存在于更大的数量)
H2SO4我得到的pKa 3左右,所以我不认为这是不合理的,把它作为一个基地。但我明白你的意思,尤其是关于最后一部分!
就是HSO4 -共轭碱。
因为硫酸是一种强酸,就是HSO4——它的共轭碱是弱碱。