炔的反应
炔反应模式- Hydrohalogenation碳正离子通路
最后更新:2022年11月14日|
炔烃Hydrohalogenation——增加HX炔烃- HCl,哈佛商业评论,你好
在前面的三个职位炔烃我们介绍了一些新的反应的炔烃(相对于烯烃):
- 去质子化(以及随后的替换)(看到帖子:炔烃的两个最重要的反应)
- 部分减少烯烃(看到帖子:部分减少炔烃)
- 醛和酮的形成通过净“水分”。(见文章:硼氢化反应和炔烃Oxymercuration)
与所有关注的方式炔烃化学可以不同烯烃化学,是有用的提醒的方式是相似的。
在本帖里,我们将回到一个关键反应机理模式我们观察到烯烃:所谓的”,碳正离子的途径”,其中包括HX和H3O +和探索反应的多少烯烃我们熟悉也可以使用炔烃。
表的内容
- 添加氢卤化物(HCl,哈佛商业评论,嗨)炔烃——一次
- 添加第二个相当于HX的乙烯基卤化物给偕的二卤化物
- 添加氢卤化物炔烃的机制
- 比较烯烃和炔烃的“碳正离子通路”。
- 摘要:添加氢卤化物炔烃
- 笔记(+三分子的机制!)
- (高级)引用和进一步阅读
1。添加氢卤化物炔烃(一次)- Hydrohalogenation
这个类别中的三个主要的例子是hydrohalic酸的反应(氯、H-Br和设定h)炔烃。如果你还记得,当添加到烯烃这些试剂:
自炔烃只是不同于烯烃之外的第二个π键,我们所期望的,这些反应也会工作炔烃——和他们做!
如果我们把一个炔烃用一个相当于八氯(注意,我们就使用氯在所有的这些例子中,但哈佛商业评论和嗨工作在完全相同的方式)我们最终形成烯基氯。
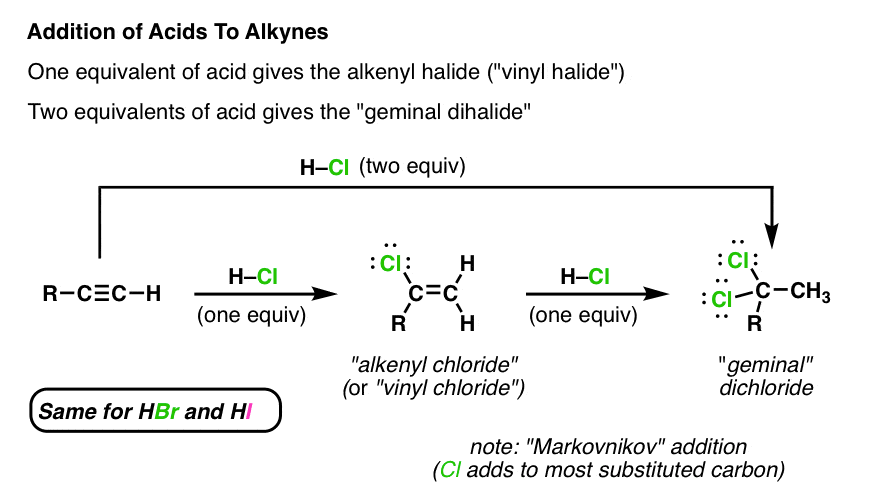
如果我们只使用一个相当于HX,我们可以得到反应停止烯基卤化物阶段。
2。添加第二个相当于HX炔
您可能想知道如果有可能这个π键的反应第二个当量八氯。答案是肯定的。【注——它是可能只是“停止”反应在这个阶段如果我们用一个等效,因为产品(烯基活性对盐酸氯)小于起始炔烃]。
事实上,如果我们添加第二个相当于八氯,它增加了碳碳π键的两侧,给我们的产品在两个氯原子在同一碳。顺便说一下,我们称之为一个”偕的“二氯化(认为拉丁语——“双子座”=双胞胎)。
我们也可以得到这个产品如果我们只是添加两个氯的等价物开始炔烃。
3所示。添加氢卤化物Hydrohalogenation炔烃的机制
这个反应会如何工作的呢?非常相似的方式如何氯补充道烯烃。
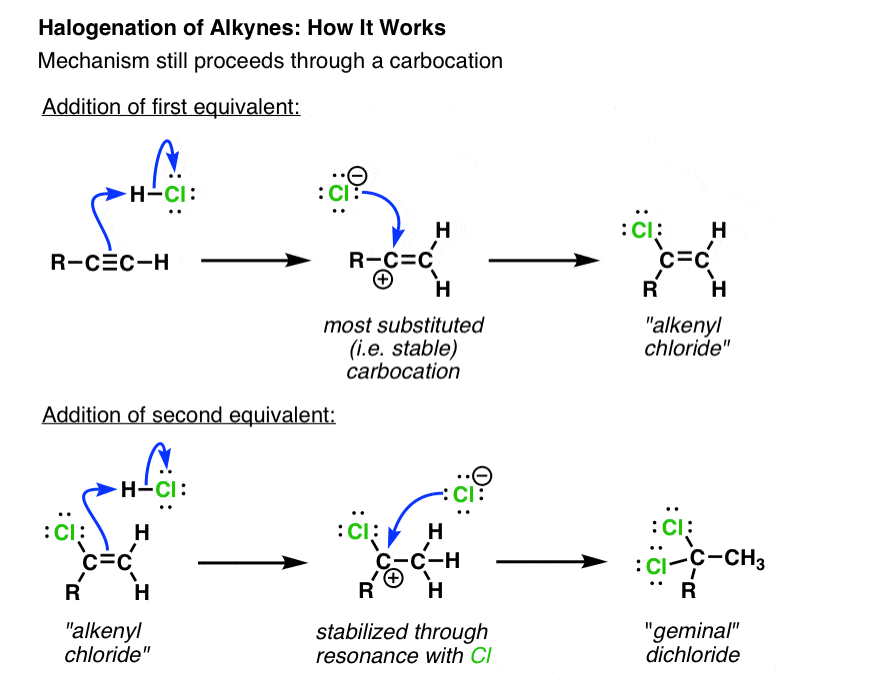
第一步是质子化作用炔烃与氯等方式给最稳定的碳正离子中间体。
由于碳正离子是稳定在更大程度上由电子释放烷基取代基比氢、新碳正离子的最后形式炔烃轴承的碳取代基。
在下一步中,碳正离子受到氯离子给的烯基氯。
第二种相当于八氯呢?考虑到这一事实偕的二氯化是这里的产品,最合理的机制形成的仅仅是一个重复的步骤从第一反应(如图所示)。
但是值得指出的是一个有趣的特性。请注意,碳正离子在这种情况下,熊氯取代基。由于碳正离子电子差,和氯是一个电负性元素,有趣的是指出电子释放的能力烷基组和氯的捐赠的孤对碳正离子)“胜出”的吸电子字符氯。
(如果你继续当日的有机化学和求职的芳香环的反应,你会发现Cl和其他卤化物离子作为pi-donors向邻碳正离子。看到帖子:为什么卤素邻对位导演才会安静下来吗?]
正如上面提到的,的反应炔烃哈佛商业评论和嗨(以及高频,以防你好奇)遵循相同的途径。
(请注意:有相当多的证据表明,这个反应事实上收益不是通过碳正离子中间体,但通过“三分子的反应将两种H-X和等价物炔烃。这是覆盖在课程和教科书不一致。我强烈建议你仔细检查你的教科书来验证它是如何教的课程。看到注1]。
4所示。比较烯烃和炔烃的“碳正离子通路”
它可能将回到这篇文章文章的价值烯烃和碳正离子的途径,并指出化学之间的异同烯烃和炔烃。希望这个表将被证明是有用的:

5。摘要:添加氢卤化物炔烃(Hydrohalogenation)
与烯烃通过碳正离子反应,遵循这一途径进行中间,提供“马氏“作为主要的产品。
关键的区别在这个通路的水合作用烯烃醇,而水化的炔烃给了羰基衍生品酮后(即酮/醛)烯醇互变现象的中间烯醇。
在下一篇文章中,我们将探索“三人圈”的途径炔烃。
在下一篇文章:炔烃三人环通路
笔记
注1。hydrohalogenation的“三分子的途径炔烃
独到的乙烯基碳正离子除了炔烃似乎属于桶”机制过于简单化的入门的听众”,与希望教科书在未来达成共识。
巴德学院的希尔顿维斯教授写道:
我做了很多工作,当然,我相信我自己的结果。我最初否认了乙烯基阳离子中间体(做任何研究之前)是在1993年JChemEd, 873页…你可能看看梅特兰琼斯的教科书或凯莉和桑德博格。其实我现在是信念乙烯基在添加阳离子极其罕见炔烃。在跑车的论文“叔丁基的重排乙烯基阳离子”相应的溶剂分解triflate triflate酯通过添加三氟甲烷磺酸t-butylacetylene。这没有发生重排。如果triflic酸(pKa= -10)不会使质子化炔烃,什么都不会。共轭炔烃(如苯乙炔)可以形成共轭乙烯基只在强酸阳离子但。酸溶液甚至没有关闭。(哈佛商业评论H3O + = -1.7, = 9, HCl = 7)。我不会感到惊讶如果最强的酸添加通过短暂的离子对,但这是罕见的。大多数教科书说,烯烃和炔烃同样的反应机制:对学生更容易,只要你看起来不太近。顺便说一下,三分子的机制不涉及一个质子和一个卤化物离子攻击炔烃在同一时间;太不可思议了。首先是一个可逆π酸和之间的复杂炔烃紧随其后的卤化物附加反periplanar更积极的碳。
感谢维斯教授写作。j .化学的链接。患儿的文章在这里。
(高级)引用和进一步阅读
- 极性的增加烯烃和乙炔。诉双分子、三分子的乙炔氢氯化反应的机制
罗伯特·c·费伊和Do-Jae李
美国化学学会杂志》上1968年,90年(8),2124 - 2131
DOI:1021 / ja01010a034
氯化氢增加了芳基乙炔在醋酸给a-chlorostyrenes和相应的混合物乙烯基醋酸。 - 在醋酸反应乙炔和氯化氢。结构在AdR2和Ad3粉反应速率的影响
罗伯特·c·费伊,迈克尔·t·佩恩和Do-Jae李
《有机化学》杂志上1974年,39(8),1124 - 1130
DOI:1021 / jo00922a024
机制取决于个人的偏好结构炔烃和总体反应条件。 - 溶剂分解的乙烯基triflates。的影响烷基取代基,溶剂,加入亲核试剂
理查德·h·萨默维尔卡罗尔·a . Senkler和保罗v . r . Schleyer
美国化学学会杂志》上1974年,96年(4),1100 - 1110
DOI:1021 / ja00811a026 - 立体化学的乙烯基阳离子和vinylic替换
h·萨默维尔和保罗v . r . Schleyer
美国化学学会杂志》上1974年,96年(4),1110 - 1120
DOI:10.1021 / ja00811a027
炔烃加热后与三氟乙酸反应给另外的产品。的混合物syn和反除了产品,和类似的反应与trifluoromethanesulfonic (triflic)酸。这些反应可能还继续通过乙烯基阳离子中间体。 - 理论研究碳正离子。C的结构和稳定性3H5+C4H9+(2-butyl阳离子),C5H5+C6H7+(使质子化苯)和C7H11+(2-norbornyl阳离子)
汉斯约阿希姆克勒和汉斯Lischka
美国化学学会杂志》上1979年,101年(13),3479 - 3486
DOI:1021 / ja00507a009
一种机制,提出了反应的初始质子化作用炔烃通过桥接的中间体。本文表明,这种氢键结构不是积极可行的。各种莫计算位置上方的桥接离子30 - 45千卡每摩尔乙烯基阳离子的能量。 - 丙二烯的催化水合动力学和丙炔
保罗·克莱默和托马斯·t·Tidwell
《有机化学》杂志上1981年,46(13),2683 - 2686
DOI:1021 / jo00326a016
溶剂同位素效应表明速率决定质子化作用。 - 取代基对乙炔的酸水合作用的影响
安妮特·d·艾伦,伊冯蒋介石,a . j .责任和托马斯·t·Tidwell
《有机化学》杂志上1982年,47(5),775 - 779
DOI:1021 / jo00344a006
炔烃反应性随取代基的电子基。的反应性炔烃取代基的影响更敏感比的情况吗烯烃。 - 2-Butyne和氢氯共晶:固态Cl-H几何••p氢键碳碳三键
迪特里希Mootz Axel Deeg
美国化学学会杂志》上1992年,114年(14),5887 - 5888
DOI:10.1021 / ja00040a077
短的长度江淮交流掩盖了这个实验工作的困难!本文描述了一种x射线结构添加复杂的盐酸和炔烃盐酸,垂直于p碳碳键。 - 的亲电之外炔烃
希尔顿·m·韦斯
《化学教育1993年,70年(11),873年
DOI:1021 / ed070p873
本文认为,乙烯基阳离子太不稳定,因此不能在亲电增加中间体炔烃。这不是完全正确的,乙烯基阳离子曾被观察到在酸性过多的媒体在合适的条件下。 - 溴化辅助添加溴化氢炔烃和艾伦
希尔顿·m·维斯和金姆Touchette
j .化学。Soc。帕金反式21998年:1523
DOI:10.1039 / A703569A
与组织4-octyne CH的反应2Cl2包含0.1 - -1.0米溴离子主要通过收益反加法。溴离子的存在极大地加速组织单独的反应与反应,表明Br的参与- - - - - -的速率决定步骤。
我有。Apriciation这一边。很多
hydrohalogenation过程最好的催化剂是什么? ?
使用化学计量反应(非催化)酸。
可以重排在Hydrohalgenation炔烃发生在烯烃。
我有问题。什么发生如果分子含有双键和三键?都将与哈佛商业评论的反应吗?以及如果只使用1摩尔的哈佛商业评论?我真的很困惑,因为我认为其中一个可能的反应,因为只有一个哈佛商业评论分子反应的反应物分子。
烯烃会比炔烃反应向哈佛商业评论。一个分子烯烃和炔烃的反应与哈佛商业评论烯烃。使质子化烯烃时,生成的碳正离子sp2杂化(33% s轨道)。质子化了的炔时生成的碳正离子sp杂化(50% s轨道)。提到出现在碳正离子越多,越难形式(不稳定)自空轨道将接近原子核。
3甲基丁炔的反应时多余的哈佛商业评论我们得到2,2 dibromo 3甲基丁烷?
为什么我们不得到2,3 dibromo 3甲基丁烷甚至烯丙基的碳正离子是更稳定的那么vinylic碳正离子形成中间吗?
这是一个很好的问题。如果你看的轨道会发生,为了一个1,2-hydride转变,碳氢键必须与空sp2杂化轨道。发生后,剩下一个空的p轨道不符合的p-oribtals双键,所以实际上不是共振稳定!
这是类似于丙二烯的质子化作用会发生什么在中央碳。你最终的碳正离子* *像烯丙基的但过渡态没有空的p轨道与π键,实际上这不是一个非定域化的碳正离子的烯丙基碳正离子。
詹姆斯是碳正离子重排发生当第一个碳正离子即乙烯形成碳正离子
为什么视频不玩
什么视频?你能说的具体些吗?
的证据三分子的过程,避免了不利的乙烯基阳离子和立体选择性将占?
是的。值得报道。谢谢你带。
你好,当ethynilcyclohexane反应与一个相当于哈佛商业评论有阳离子rearrangment所以Br“触摸”环联合国最终产品?
谢谢!
炔烃的反应时是什么反应2存在ROOR哈佛商业评论吗
好的文章!值得注意的是,质子化作用后产生的乙烯基阳离子HCl是线性的(吸引),不弯曲。线性阳离子的LUMO能量高于假想的LUMO弯曲阳离子。我得到了这个从前…:-)
詹姆斯,你知道一个实验使用DCl显示偏好(或缺乏)syn或反对增加D和Cl炔吗?
指出,谢谢!
再保险:DCl,我假设都将获得的混合物。看不到直接引用今年3月,虽然有一个脚注引用机械讨论HX除了炔烃的跑车,p . J等人在“乙烯阳离子”学术出版社纽约1979 p。24。3我的版本不是最新的。
“溴化辅助添加溴化氢炔烃和艾伦”杂志《化学学会帕金II, 1998, 1523。
哈佛商业评论增加了终端炔烃几乎只在某些情况下反。与酸性更强的解决方案,混合起来,部分原因在于烯烃异构化的产品。
谢谢你!