SN1 SN2 / E1、E2的决定
决定SN1 SN2 / E1和E2(2) -亲核试剂/基地
最后更新:2023年5月24日|
- 本文假设您了解的机制N1 / SN2 /E1和E2反应。进行审核,看这里年代N1][年代N2][E1][E2]
- 年代N1 / SN2 /E1/E2反应就会发生烷基卤化物(看到确定替换和消除反应发生]
- 确定是否烷基卤是初级,二级、三级(或甲基)有助于缩小的可能性(看到SN1 SN2 / E1 / E2 -底物]
- 主烷基卤化物往往经历年代N2反应。三级烷基卤化物从来没有去的年代N2。
- 单独确定衬底通常不足以缩小可用的可能性,因此下一步是检查亲核试剂/基地。这是本文的目的!
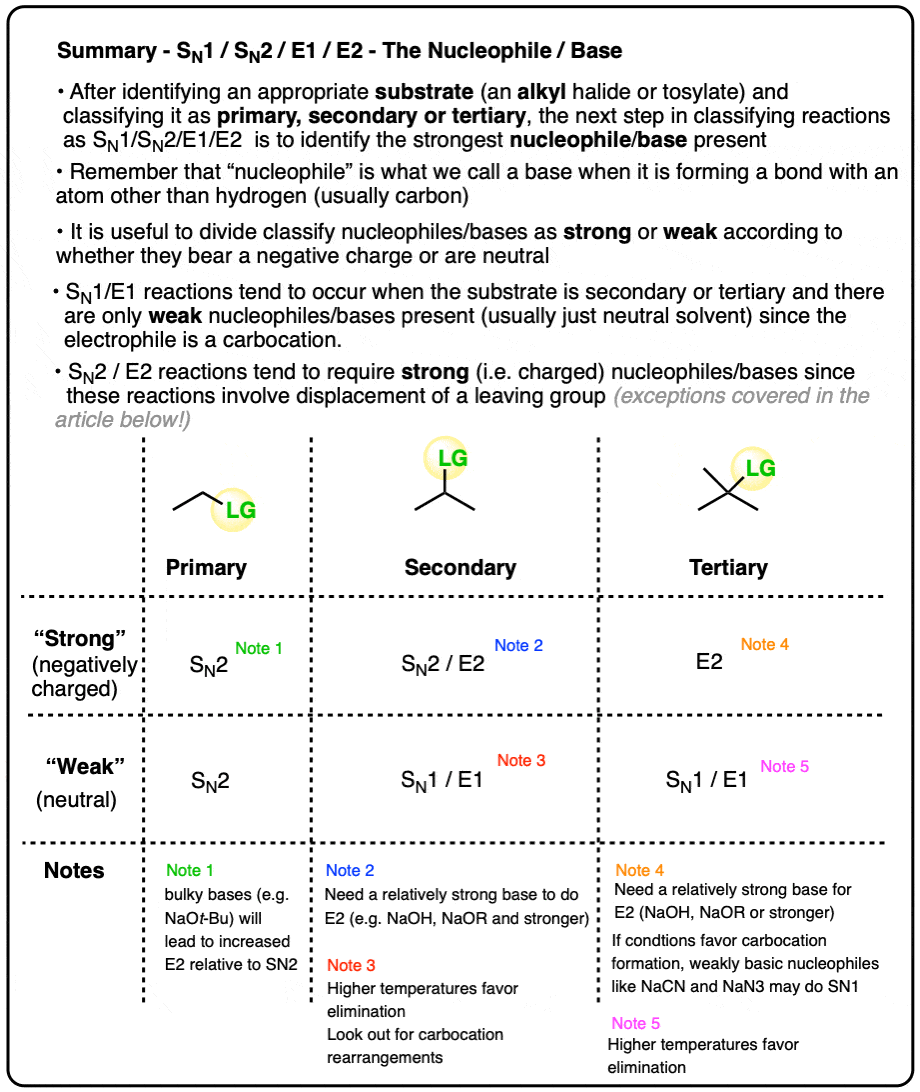
- 就我们的目的而言,“强大的“亲核试剂/基地消极的指控和“软弱”亲核试剂/基地中性
- 一个好的经验法则是期望年代N2/E2以“强大的”(即带负电荷)的亲核试剂/基地和期望年代N1 /E1与中性亲核试剂/基地
- 所以本文的重点年代的区别N1 /E1从年代N2 /E2,尽管本文还将讨论某些方面的区别N2E2基于碱度。
- 许多测试和下面的例子,包括异常。
表的内容
1。确定亲核试剂/基地
在先前的文章中能够识别基板作为初级,二级或三级。(看到的文章- - - - - -确定替换和消除反应发生,和年代N1 / SN2 / E1和E2 -衬底]
这是有助于能够迅速排除某些反应。
- 例如,如果一个衬底主通常,你可以排除N1或E1因为他们通过碳正离子反应中级和初级碳正离子是不稳定的。除了少数例外(庞大的基地)主要基质通常会经历N2。
- 如果一个衬底三级,你可以排除N2从背后攻击将会由于位阻阻碍太慢亲核试剂C-LGσ*轨道的方法
一旦你这样做了分析,你仍然可能会有几个可能性。你怎么能进一步缩小下来?
在演绎过程中下一步是检查亲核试剂或基地。(记住,一个“亲核试剂”就是我们所说的一个基地当它攻击以外的一个原子氢,碳等。)
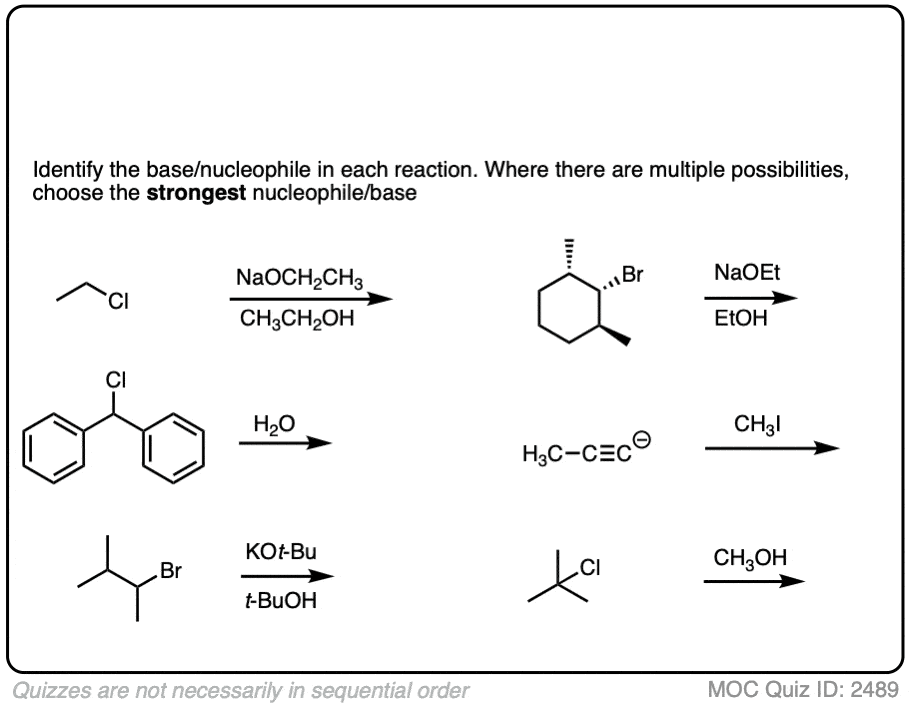
看看你能不能识别亲核试剂在下面这些反应或基地。当有多个潜在的亲核试剂/基地,选择最强的一个。(更多详情)。
 点击翻转
点击翻转
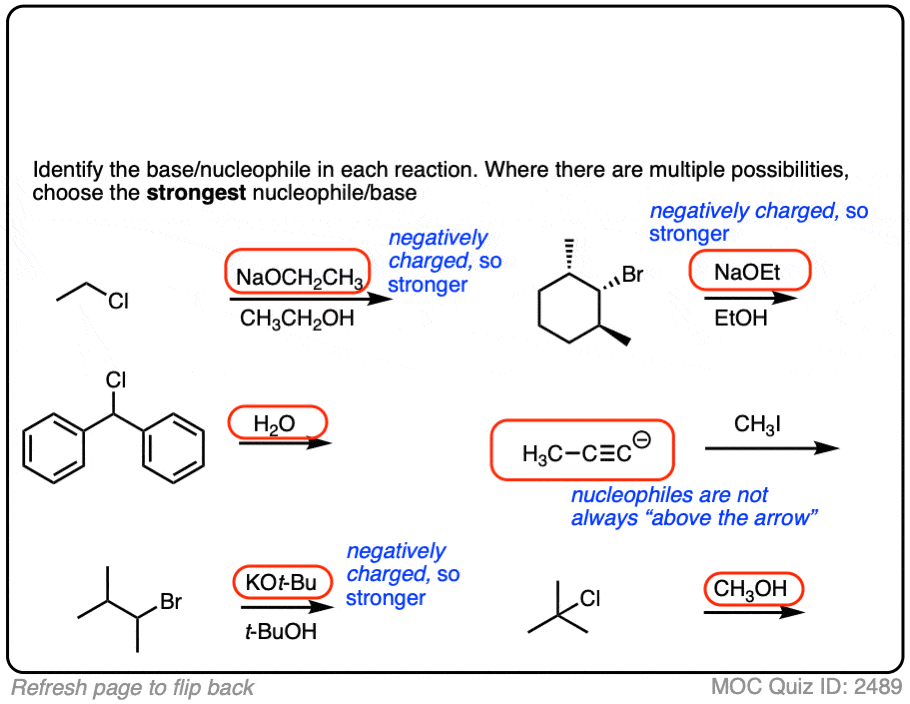
底物的反应最快与最强的亲核试剂/基地。
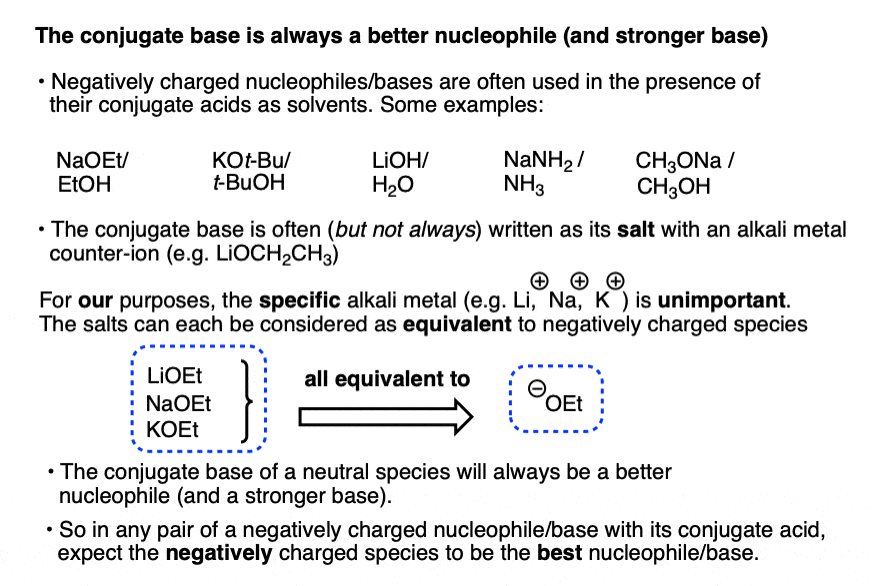
的共轭碱总是更好的亲核试剂(见文章-是什么让一个好亲核试剂?),共轭碱一直是一个强大的基础(见文章-如何用pK吗一个表]。
所以如果你看到NaOCH2CH3在CH的存在3CH2哦,或tBuO(-)的存在t -BuOH,带负电荷的物种将会是活跃的。
另一个提示:不要假设的常见陷阱亲核试剂总是会上市顶部的箭头。有时它实际上是亲核试剂这是反应物和绘制底物结束了箭!
最好试着理解发生了什么比试图记住简单的(和常常是错误的!像“)规则亲核试剂永远是第一件事上面箭头”。
好的。让我们看看另一个稍微复杂的问题。
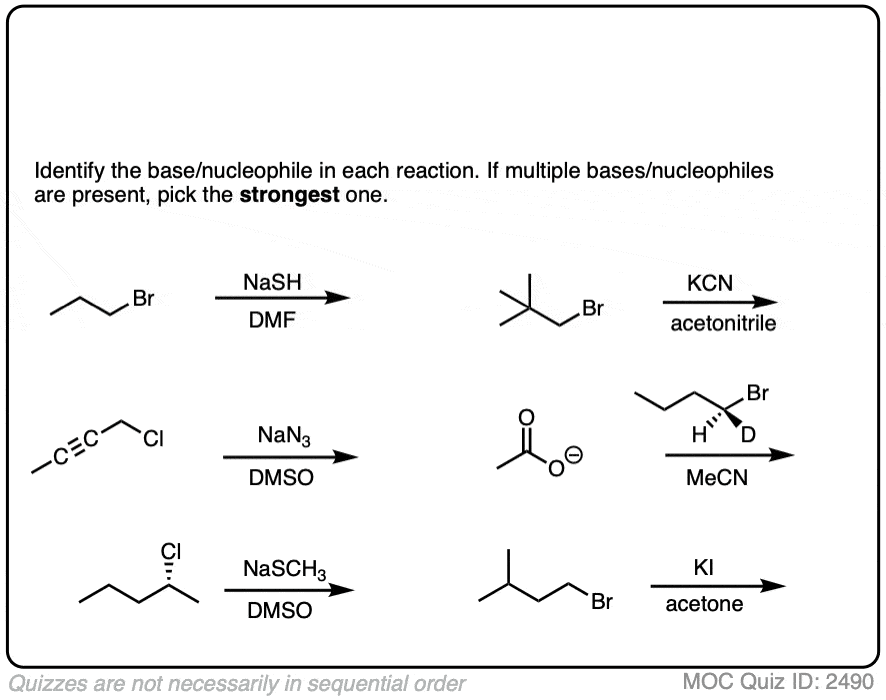 点击翻转
点击翻转
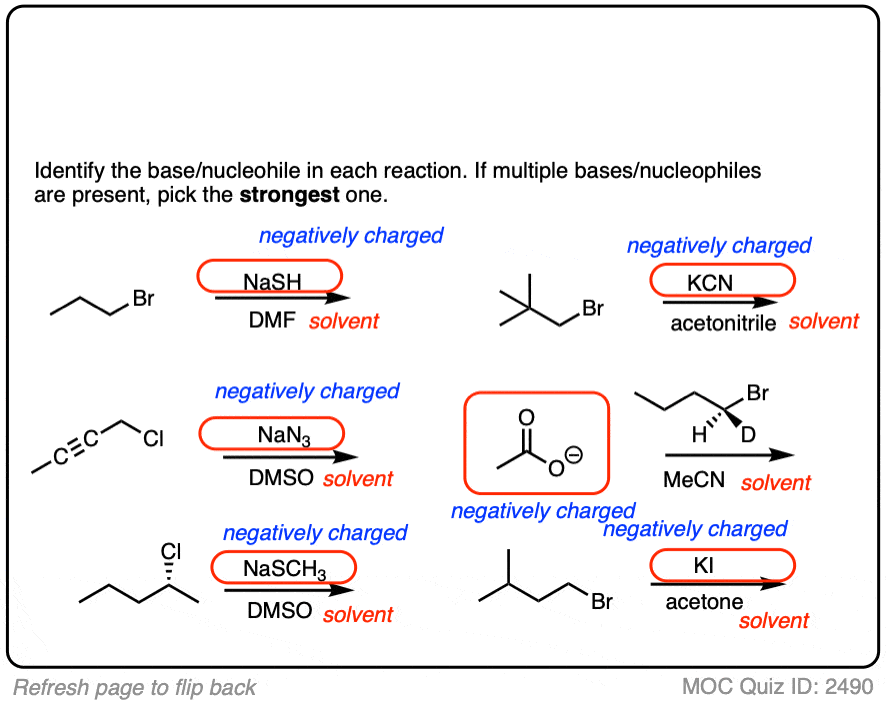
另一点,经常旅行的学生是没有区分潜在的亲核试剂和各种非质子溶剂发现使用,但不参与,这些反应。
极性非质子溶剂时候总是选择替换(通常SN2)是理想的,因为它们是极地足以溶解的亲核试剂,但不能形成氢键。结果是,亲核试剂在极性非质子溶剂相对“自由”并与亲电试剂反应更快,相对于利率极性质子溶剂。(见文章-极性质子?极性非质子?关于溶剂]
下面是一些常见的溶剂要注意的替换和消除反应。请注意,他们可以在几种不同的方式描述!(乙腈例如,可以写成CH3CN,MeCN或者只是“乙腈”。)
在各种各样的极地底部质子溶剂,例如水、醇、羧酸和氨。这些溶剂是能够参与替换/消除反应。
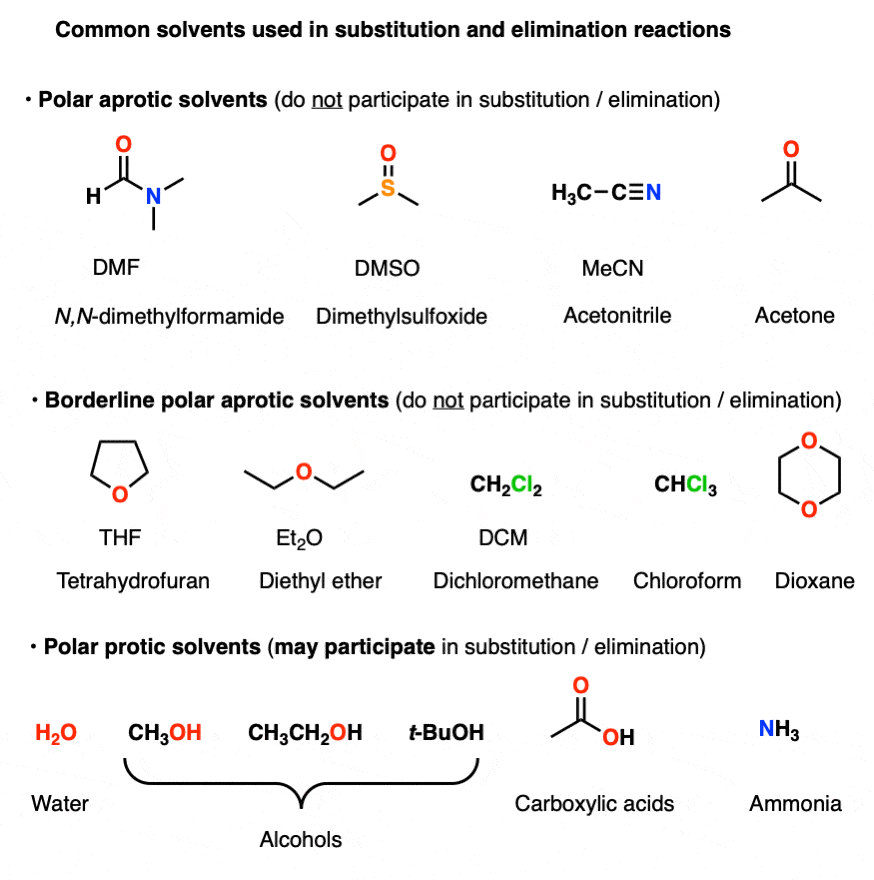
注意,溶剂的选择(vs极性非质子极性质子)可以对反应倾向是否有强烈的影响E2或年代N2。我们将讨论这后续的一篇文章。(见文章-决定年代N1 / SN2 / E1 / E2 -溶剂]
另一组更有挑战性的情况下:
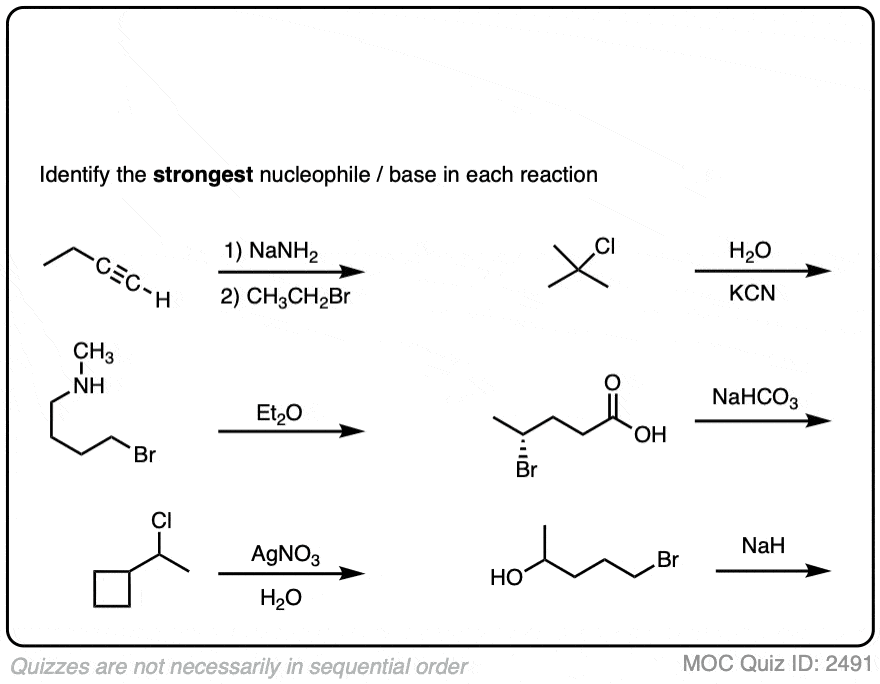 点击翻转
点击翻转
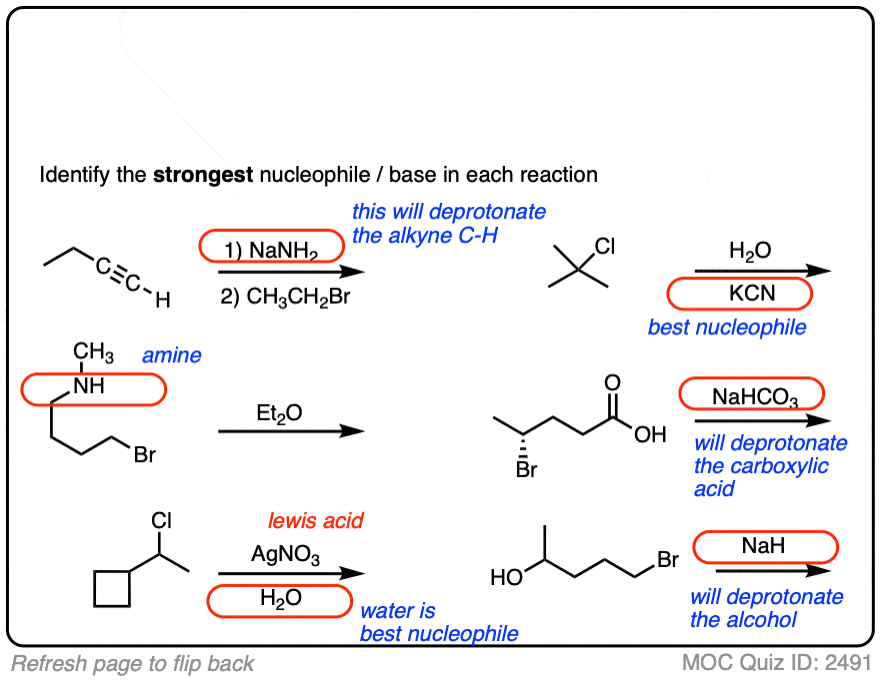
总结本节:
- 没有硬性规定的亲核试剂高于或低于反应出现箭头
- 寻找带负电荷的物种是“最好”的亲核试剂/基地
- 知道如何识别潜在的溶剂——他们不会参与替换或消除,但他们可以影响的比例替代和消除产品
- 有时,亲核试剂/基地存在基质本身!这些都是“分子内反应的例子(更多的下面]
2。“强”与“弱”的亲核试剂/基地
现在,我们已经有一些实践确定的可能亲核试剂,我要建议有点粗糙但很有用的分类,将有助于区分N1 /E1反应的年代N2 /E2反应。
我们叫带负电的亲核试剂”强”并调用中立的亲核试剂弱”。(请注意2]
年代的速率决定步骤N1 /E1反应是形成碳正离子,通常只可能与二、三级基质高极性、电离溶剂如水、醇、羧酸及其混合物。碳正离子有一个空的p轨道,将很容易把甚至与刘易斯基础薄弱等水和醇碳以来产生的产品将有一个完整的八隅体。
年代的速率决定步骤N2 /E2要求亲核试剂/基取代离去基团从一个已经有一个完整的碳八隅体。通常这些反应时效果最好亲核试剂比/基地是一个强大的基地离去基团。
由于醇、水和羧酸是相对贫穷的基地,许多年代N2 /E2反应与他们的亲核试剂/基地从酸碱的角度来看是不好的。(见文章:是什么让一个好的离去基团][注3]
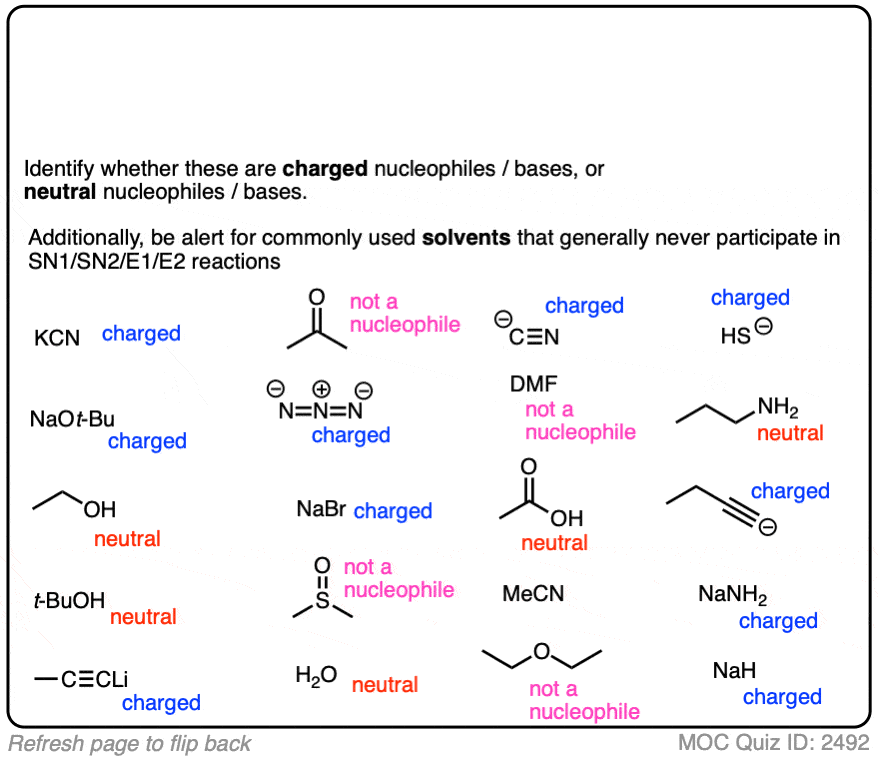
记住这一点,下面的亲核试剂归为“强烈”或“软弱”(有些地雷埋在这个问题!)
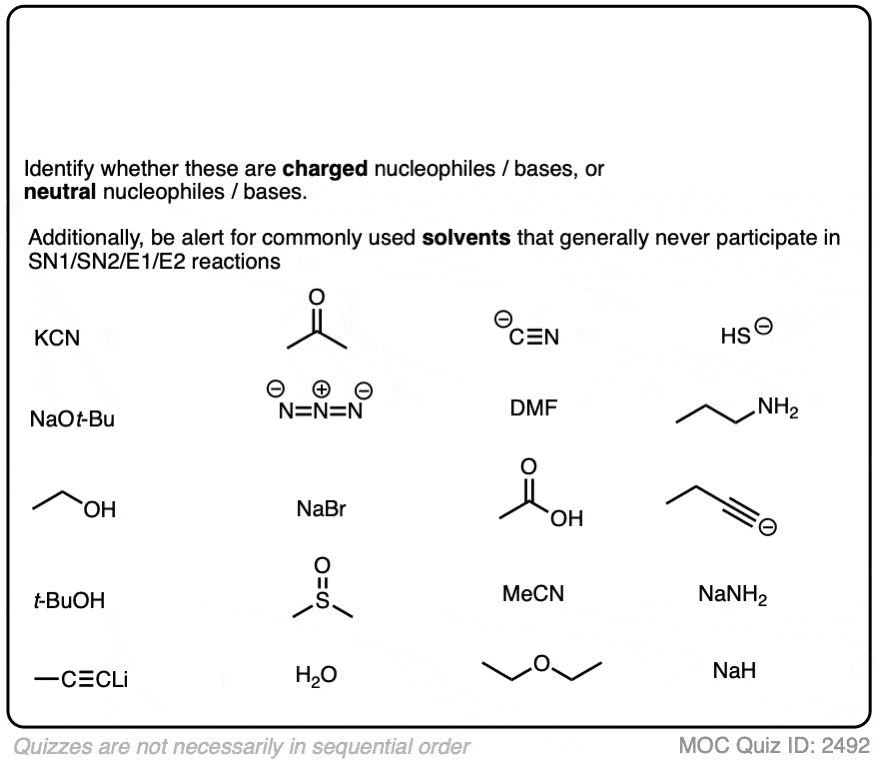 点击翻转
点击翻转
3所示。六大情况下,基于基质+亲核试剂
你已经学会了如何确定基质为主,二级、三级。
确定了最佳的亲核试剂,和分类强弱,我们现在准备开始应用一些反应。看看你做的事:
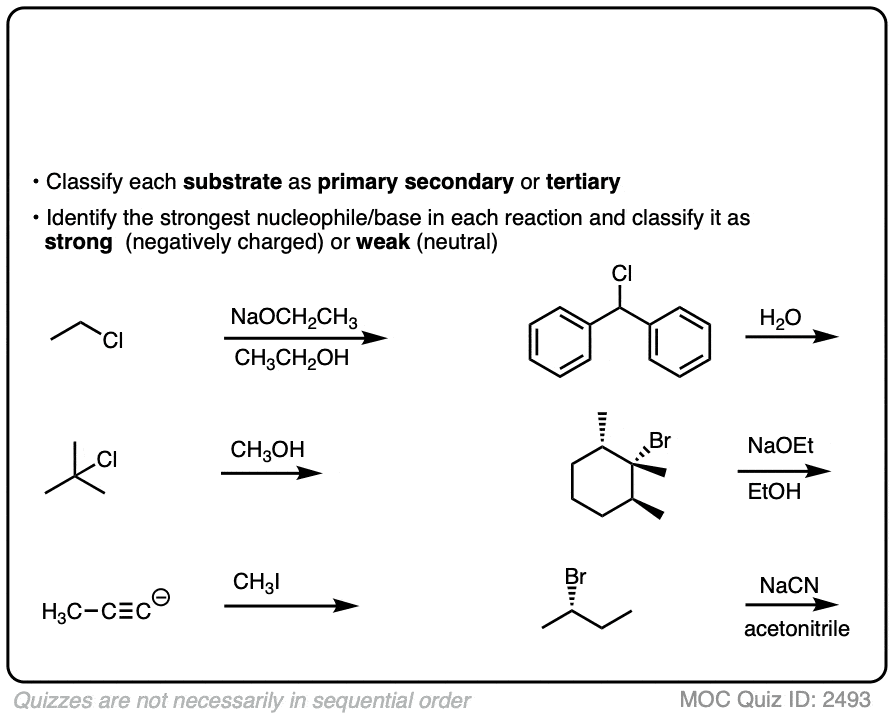 点击翻转
点击翻转
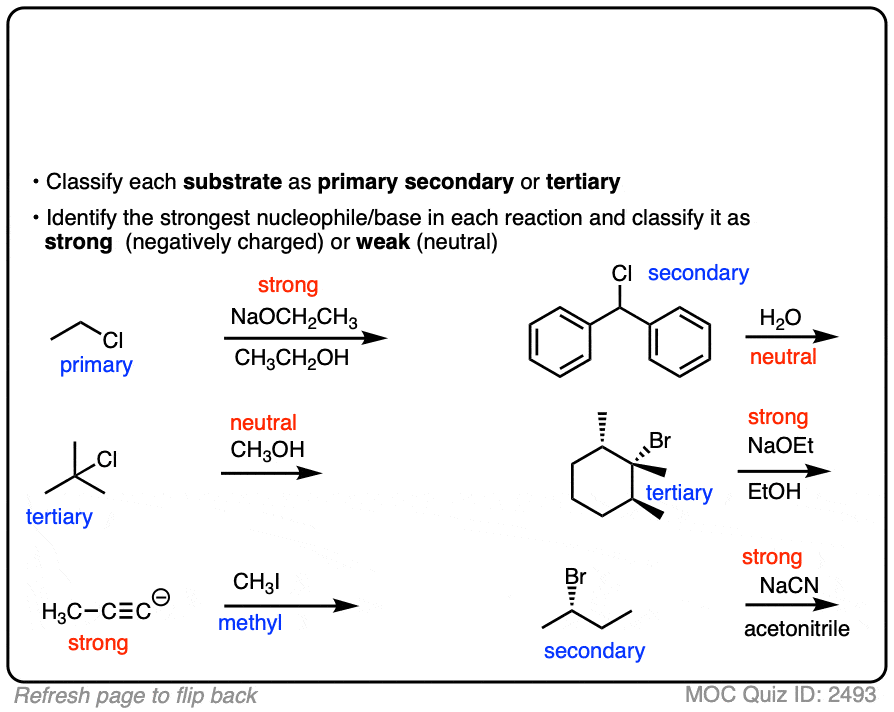
因为只有六大情况下(不包括甲基)可能有助于制定一个网格是这样的:
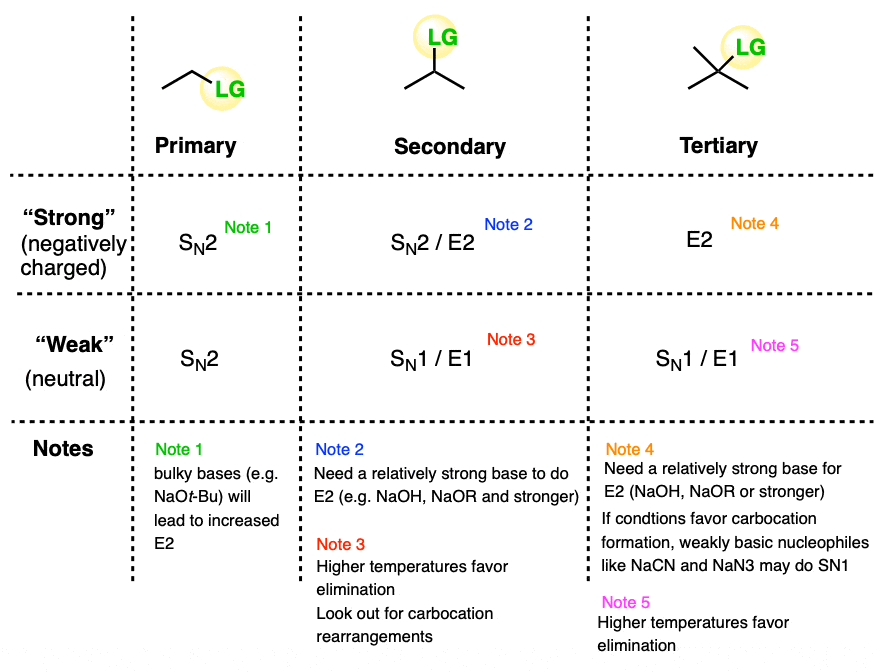
六个一般情况:
这里有一些更多的练习:
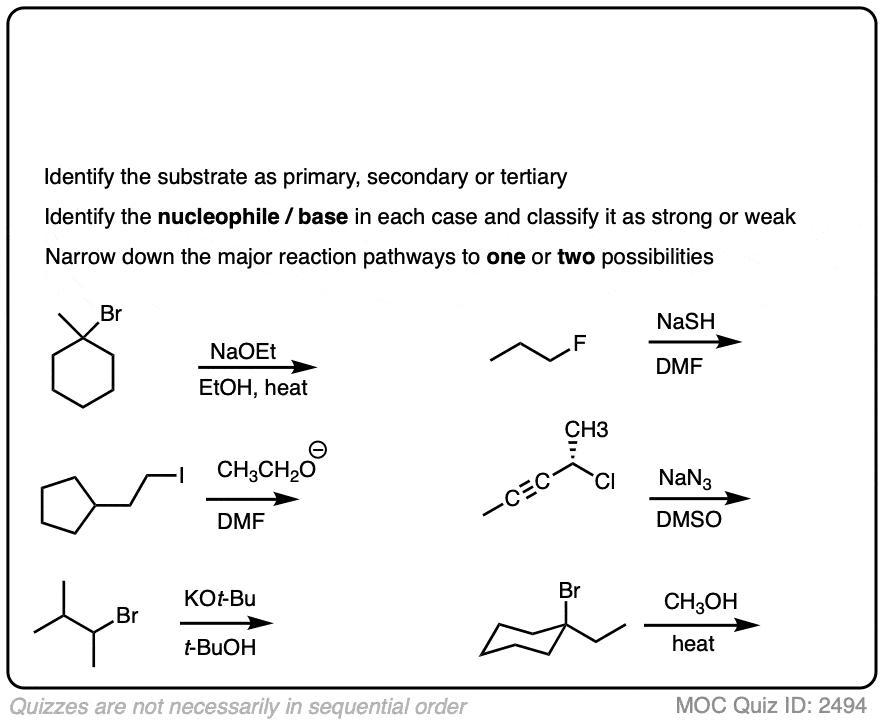 点击翻转
点击翻转
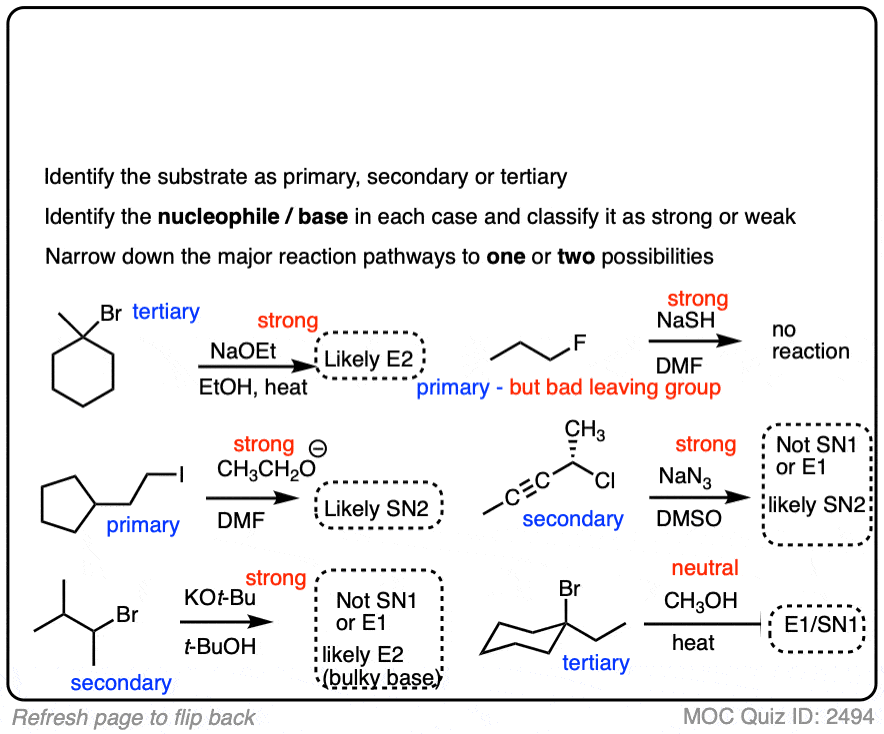
你可能会觉得它很讨厌,毕竟这项工作分析衬底和亲核试剂我们仍然有多个的情况下我们仍然不能确定的主要途径。
有益的是,分析碱度一些强大的亲核试剂/基地将帮助我们做一些更清晰的区分。
4所示。二烷基卤化物:基础力量的重要性
的E2反应通常需要一个强大的基础。带负电荷的物种软弱基地如卤化物、羧酸盐,氰化物,叠氮化或硫醇盐(RS(-))通常不会执行E2反应。(注5]
强大的基地,例如氢氧根离子HO(-),醇盐RO(-),和物种比他们更基本的(例如乙炔化物、酰胺基、氢化物)完全执行的能力E2然而,反应。
所以相当好的分界线”E2能够“基地是pK一个12的共轭酸。基本比硫醇盐,换句话说。
这个图表可能会有所帮助。注意,这是特定的二次烷基卤化物。
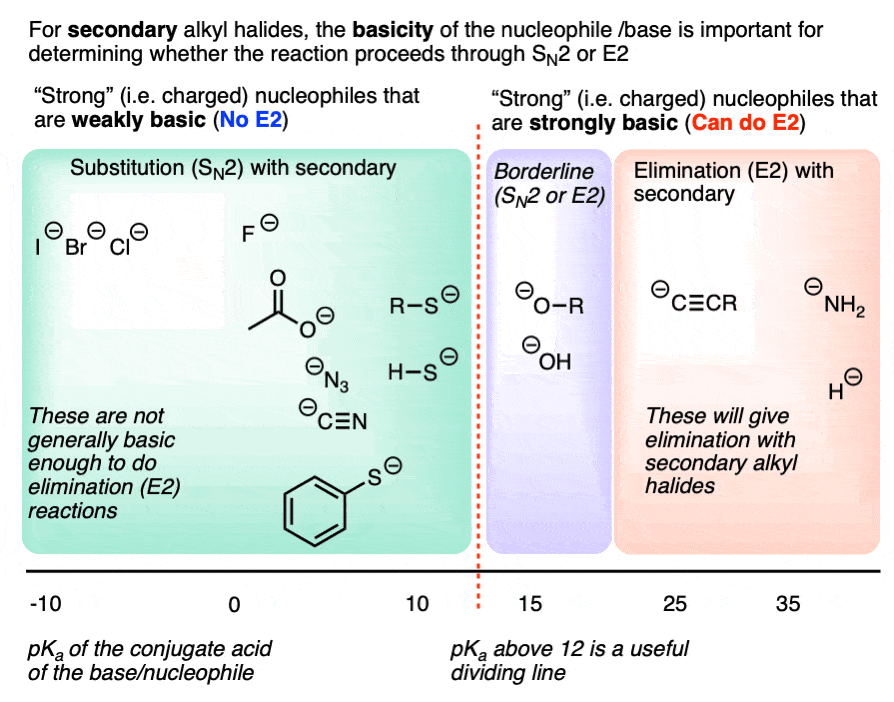
为二级烷基卤化物与弱基本的亲核试剂,期望N2硫醇盐,所做的一切和一切比醇盐基本消除。(例如NH酰胺基地2(-),R2N(-),不,和乙炔化物主要会给E2产品。(乙炔化物与主没事的亲核试剂烷基卤化物,但将执行E2在二次反应烷基卤化物)。
根据条件,氢氧根和二级醇盐本身可以有较多的选择烷基卤化物,我们将讨论更多的细节在后面的一篇文章。(见文章-决定SN1 /秒N2 / E1 / E2 -溶剂]
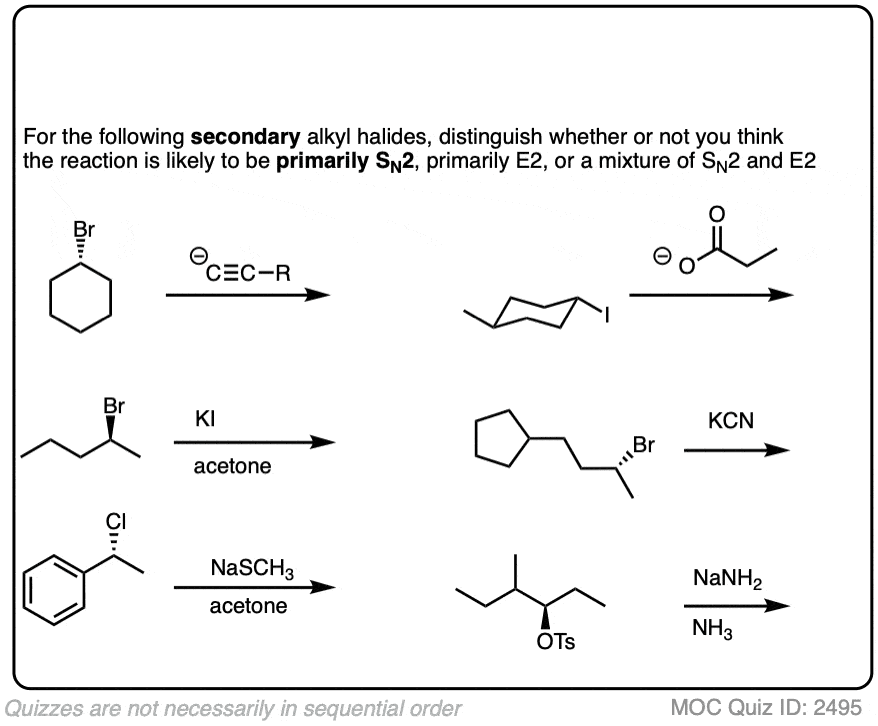 点击翻转
点击翻转
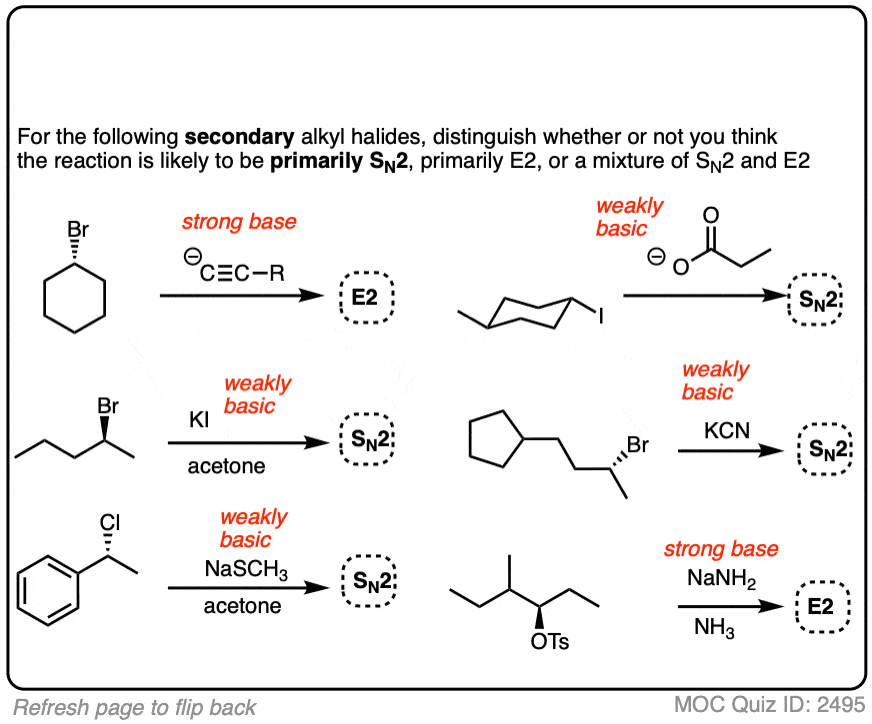
的E2反应叔烷基卤化物也需要一个合理的强碱如氢氧根、醇盐或物种比这更基本。(一个例外——如三乙胺或中性氮基地DBU还将执行E2反应)
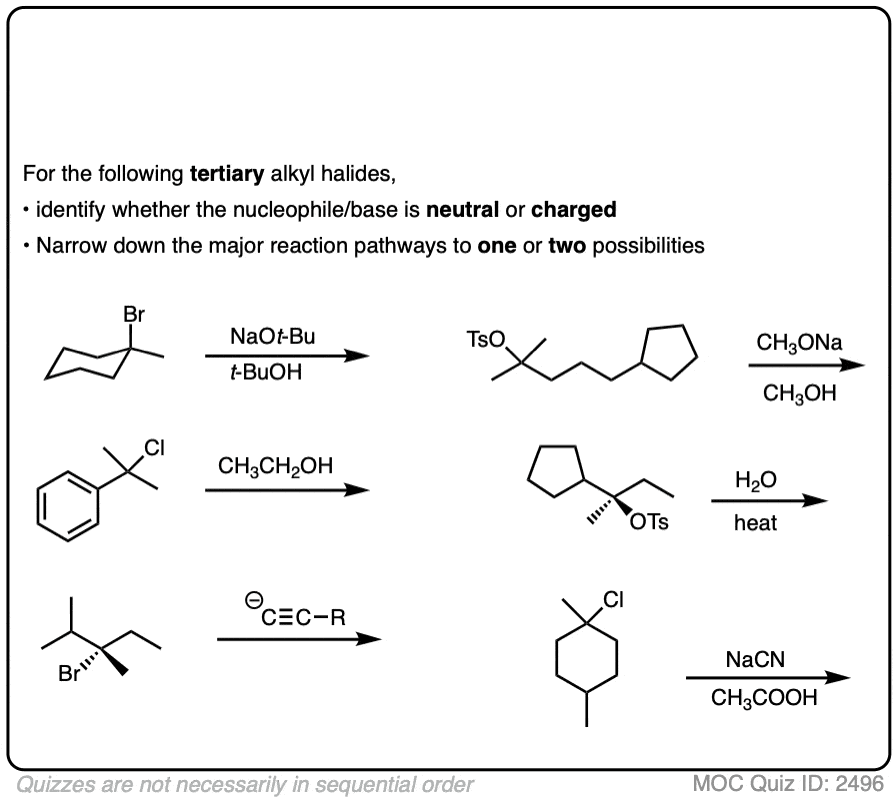 点击翻转
点击翻转
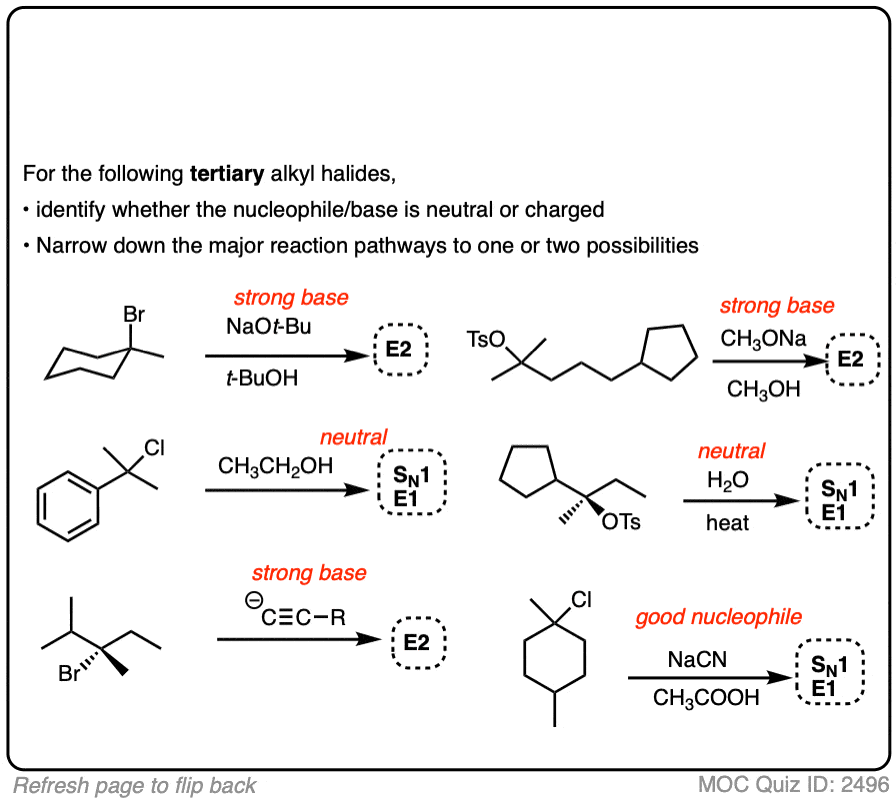
年代N1反应有时是观察当“强劲”,弱等基本的亲核试剂(-)CN或N3(-)与一个叔在溶液中烷基卤的情况下,形成碳正离子。这些物种是如此优秀的亲核试剂,他们可以竞争溶剂。(裁判]
5。更多关于“SN1 vs E1”和“年代N2对E2”案件
在这一点上我们已经展示了如何识别烷基卤化物为主,二级或三级,那么如何识别“强烈”或“软弱”的亲核试剂,然后如何进一步缩小带负电的亲核试剂,以确定哪些更有可能执行N2或E2。
这两个问题,综合作业的年代N1 / SN2 /E1/E2是:
- 年代的区别N1E1(简短的回答是,有利于消除热量,在后续的文章中,看到的更多决定年代N1 / SN2 / E1 / E2 -温度)。
- 年代的区别N2E2为二次烷基卤化物与强大的亲核试剂/基地“边缘”地区(氢氧化和醇盐)。(我的回答很简单,除了“问问你的老师,因为许多不同意”——是极性非质子溶剂替换,但更多的决定SN1 /秒N2 / E1 / E2 -溶剂)。
我们将在后续处理这些文章。
除此之外,还有其他的欠缺和例外的领带?是的!
让我们结束处理酸碱反应、分子内的例子,和最后一个单词从你的底物。
6。提醒先做酸碱反应
在我们急于覆盖基本的强和弱的亲核试剂,上图,我们只考虑亲核试剂要么做替换或消除/基地。
有第三种可能(第四,如果算上“不反应”)。
的亲核试剂也可以执行一个/基地酸碱反应在衬底上。
这是最有可能当酸性基质如醇、硫醇、终端乙炔和羧酸处理强大的基地。
往往是酸碱反应快相对于替换和消除反应(见文章-酸碱反应快]。所以是有意义的应用第一个。
由此产生的共轭碱是,正如我们上面所讨论的,上级亲核试剂相对于其/基地共轭酸。
这些反应显示的例子去质子化步骤替换步骤紧随其后。看看你是否能画出产品。
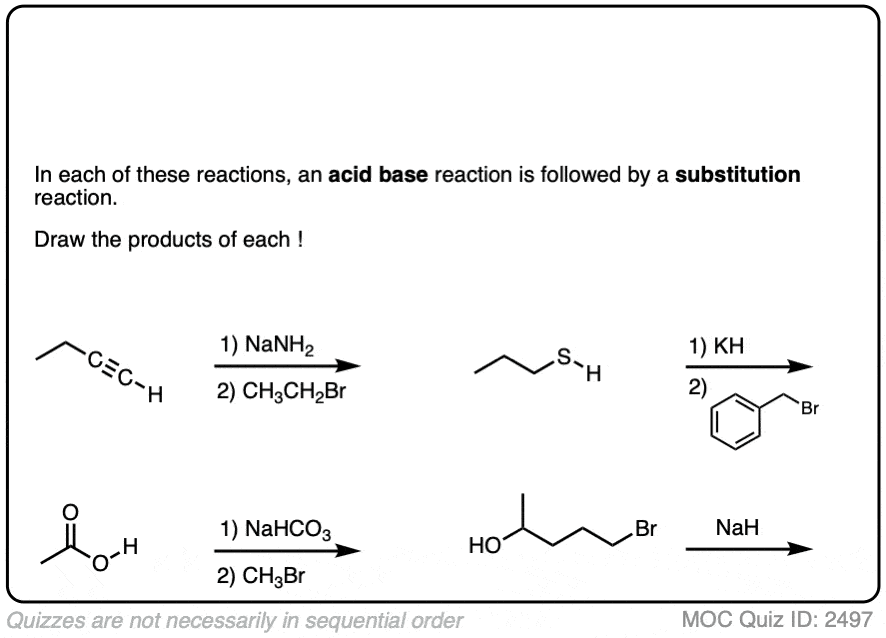 点击翻转
点击翻转
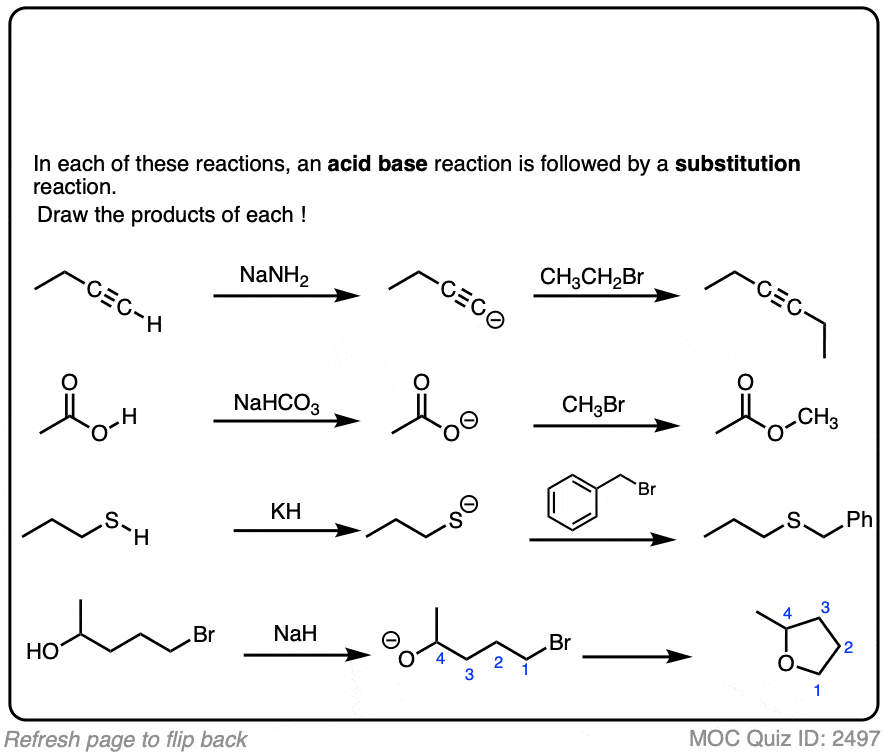
”的必然结果共轭碱是一个更好的亲核试剂“是”共轭酸是一个更好的离去基团”。
添加酸(包括路易斯酸)将帮助穷人离开团体变成更好地离开组织。
这是最常见的醇,添加H +转换穷人-哦离去基团到(更好的)离去基团H2O。
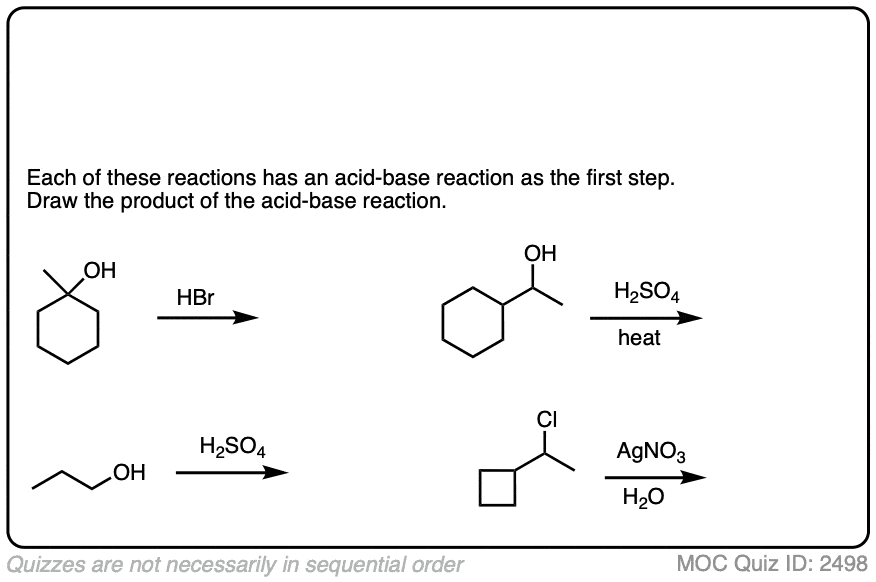 点击翻转
点击翻转
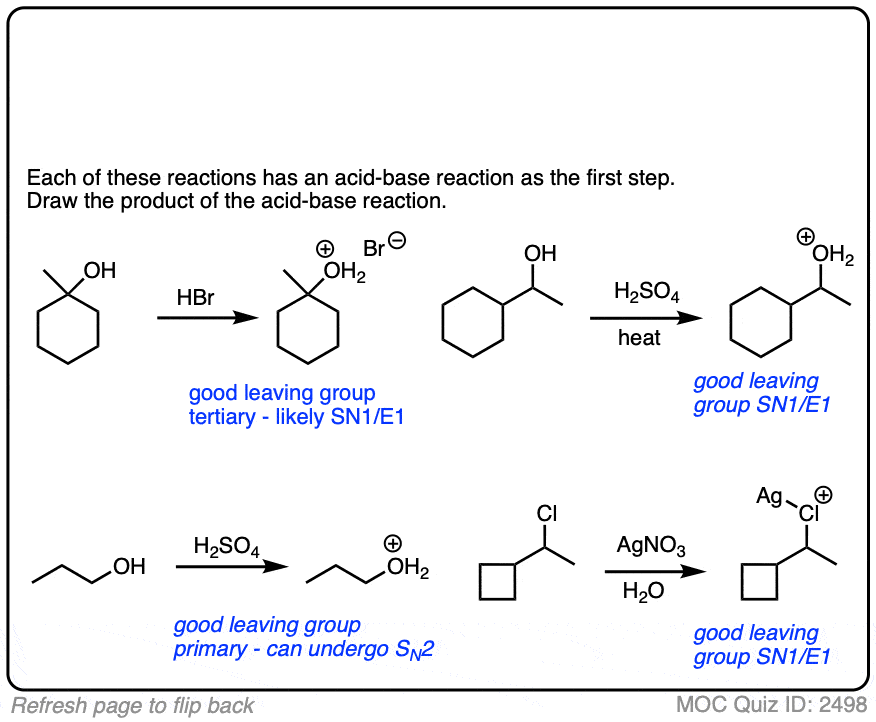
卤化物可以制成更好离开团体通过添加银盐,这不可逆转地沉淀的卤化物的解决方案。
7所示。分子内反应
它总是值得看分子内的变体的每一个新的反应你学习,因为他们是一个常年的最爱exam-writers无处不在。
在一个分子内的年代N2反应,亲核试剂和底物在同一分子。他们的组合将导致一个新的戒指。
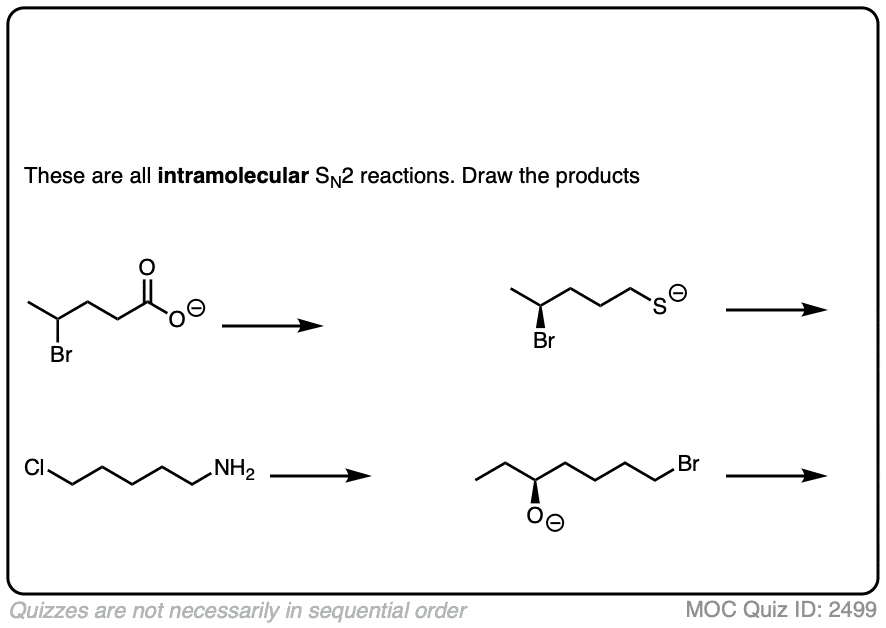 点击翻转
点击翻转
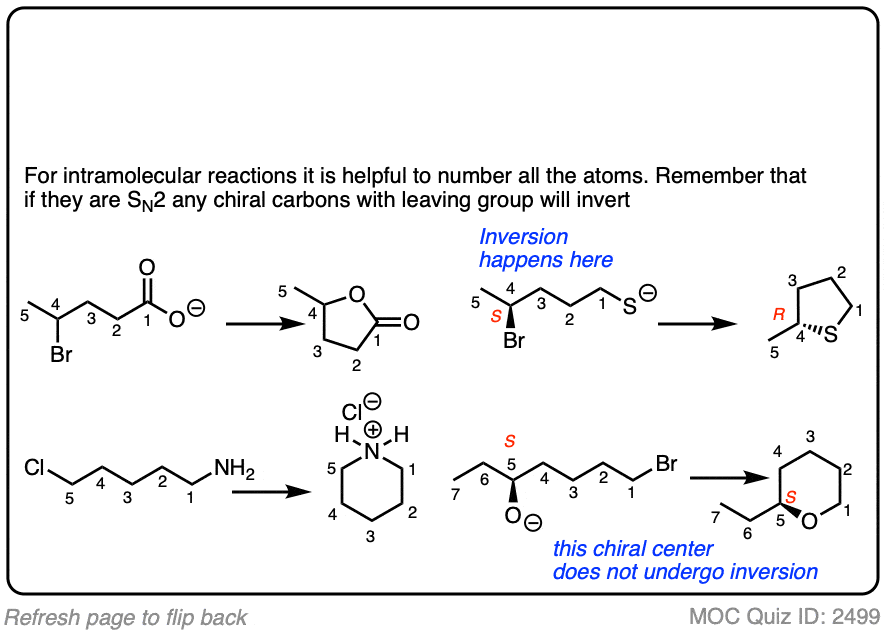
你永远不可能有足够的实践与分子内反应。
8。底物总是有最终决定权
我知道这是很多东西要学。基质的亲核试剂,反应。这是很多原因的一个学生发现有机化学困难。
经验法则、清单和流程图非常有助于理解你要求的所有信息的过程。
你可能不会喜欢,还有最后一件事,但是还有最后一件事。
最后分析过程仍将需要适当的bond-forming /破坏模式适用于你的底物才能画出正确的产品。
有时…即使你已经贯穿所有的清单…你的基质可能仍有(或缺乏)的一个重要功能,结果在一个特定的反应是行不通的。
这里有一些例子。
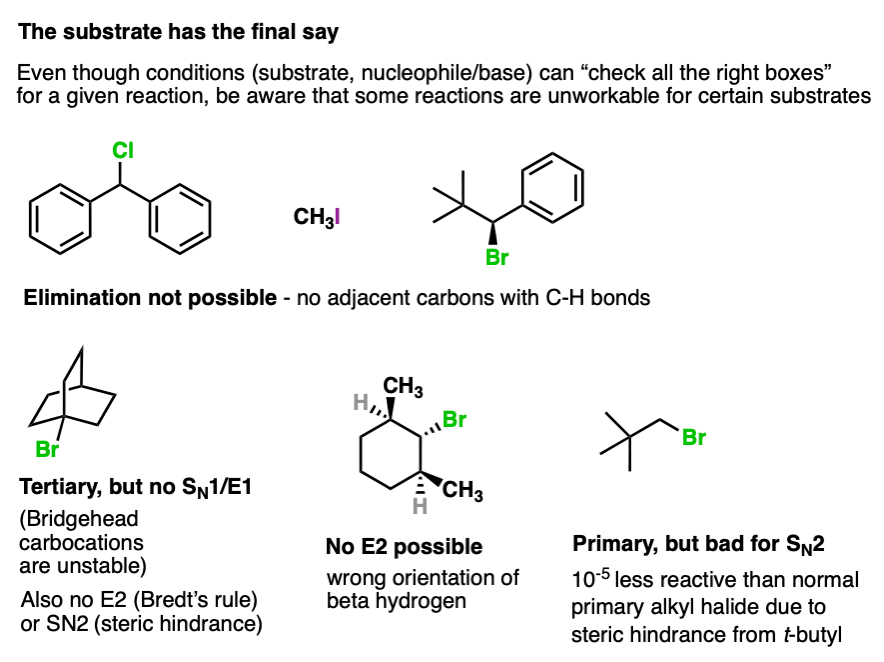
所以使用流程图和经验法则,但不要太“锁定”下面的流程图,你忘了看看分子本身和决定是否这个反应是偶数可能的。
你的底物总是拥有否决权。
9。总结
在试图决定的过程中如果一个反应是SN1 / SN2 /E1/E2,有五个步骤。这篇文章是第三个五。
我们之前所覆盖步骤1(寻找烷基卤化物(链接])和步骤2(确定烷基卤是初级,二级或三级(链接])。步骤4(溶剂链接])和步骤5(温度(链接])。
在本文中,我们第一次看到各种反应和寻找最强的亲核试剂/基地在每种情况下。(一个亲核试剂是我们的名字为基本当它与其他原子形成的债券比氢吗)。
- 然后我们做了一个经验法则在定义的亲核试剂/基地轴承一个负电荷作为“强大”,和中立的亲核试剂/基地作为“软弱”。
- 这给了我们六个关键案例分析(一级、二级、三级强/弱)。
- 主烷基卤化物倾向于接受N无论是否2反应亲核试剂强或弱。
- E2反应通常需要相当强大的基地(如氢氧化醇盐或更强)。
- 为二级烷基卤化物、强亲核试剂/基地倾向于执行N2 /E2反应,亲核试剂/基础薄弱往往执行N1 /E1反应。
- 与二次基质,带负电的亲核试剂比氢氧化倾向于较弱的基地N2只,和带负电荷的亲核试剂比氢氧化物/醇盐倾向于更强的基地E2独家。
- 氢氧化/醇盐离子与二次烷基卤化物边缘区域,可以去N2或E2。(更多关于下一个)
- 为三级烷基倾向于执行卤化物,强大的基地E2反应,亲核试剂/基础薄弱给SN1 /E1产品。
- 酸/碱添加到衬底时,首先进行酸碱反应。
- 通过各种方法适用的经验法则/流程图,但仍为基质,S保持警惕N1 / SN2 /E1/E2反应可能不工作由于存在与否的某些结构特性(如缺乏一个β碳碳氢键E2不可能的)。
笔记
注1。上的孤对乙腈(和其他腈)将与碳正离子反应在一个反应称为里特反应但这超出了我们的范围覆盖。(链接]
注2。最大的挑剔我有关于这个“强大”和“弱”称号是中性的胺三乙胺等都能很好地执行E2反应。
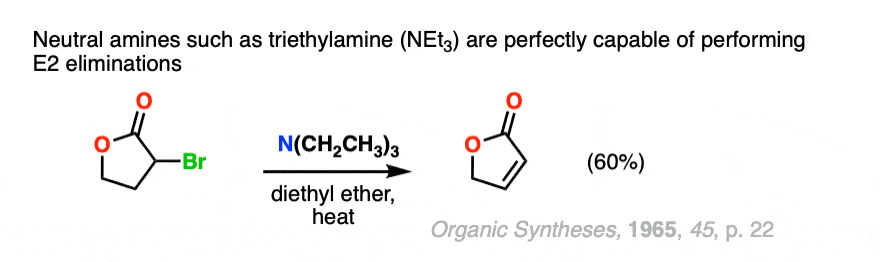
等含氮碱基DBU和DBN将执行消除反应。
其次,中性PPh3完全有能力执行的年代吗N2在一些次要的烷基卤化物。
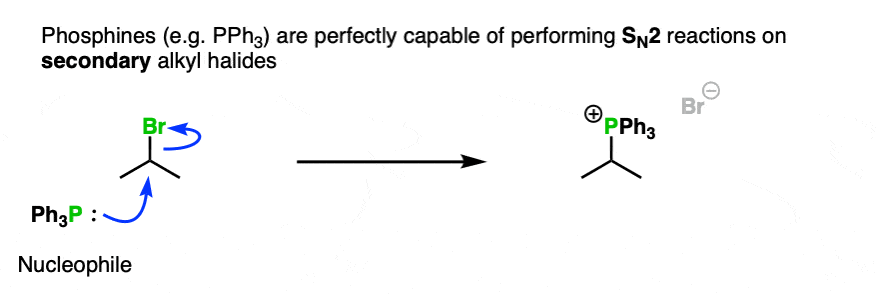
注3。你不会太错了如果你认为的置换反应是一类奇特的酸碱反应,往往是成功与底物反应更强的基地时的结果(一个较弱的基地离去基团)。
一个关键的区别是,替换和消除反应往往不可逆,酸碱反应是可逆的。
注4。“强大”的一个例子亲核试剂/基地三级反应烷基卤可以找到在这个例子中叠氮化的离子形成碳正离子的Ph值“拦截”3三地在水里。
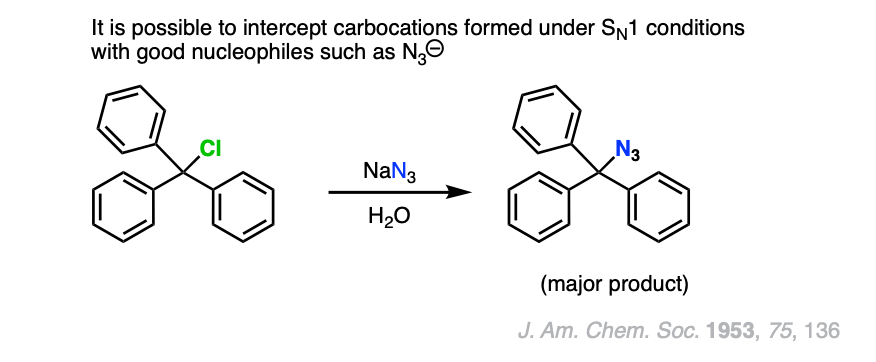
测试你自己!
(测试)
(高级)引用和进一步阅读
(文学)
如果我们有2-bromo-2-methylpropane爵士和反应HCC-CH3丙炔NaNH2的存在。所以se将E2还是SN2产品作为主要产品?
终端炔先deprotonate乙炔化物。之后,乙炔化物将deprotonate 2-bromo-2methylpropane给烯烃(E2)。
主要卤代烷+ aq。KOH,产品是由SN2决定或E2 ?老师告诉它跟着SN2但根据快速和肮脏的方法将E2(水是极性质子溶剂)。先生请告诉答案。我很困惑?
主要卤代烃一般给SN2。唯一的例外是新戊二卤化物,非常位阻。
根据我的教科书,为什么当二级烷基卤化物甲苯磺酸盐与醇盐反应在DMSO,心态占据主导地位形成烯烃醚(85%)?极性非质子溶剂应该支持Sn2 / E2和甲苯磺酸盐是一个很好的离去基团。不支持的亲核试剂,而不是消除呢?谢谢你!
课本确实比大多数教材更好地描述现实。在现实中SN2很次要的卤代烃/甲苯磺酸盐。我可以问你正在使用什么教材吗?
谢谢你! ! !
我的另一个问题是当你说,“这是一个很好的经验法则:如果该基地的共轭酸/亲核试剂小于12”你指pKa = 12吗?
真的,这是一个更quantitiative说氢氧根和醇盐(pKa的共轭酸14以上)会取消,但硫醇盐(pKa的共轭酸- 11)将做替换。
先生,
如果我使用乙醇钠在乙醇,2-chlorobutane什么样的途径应该反应遵循…E2还是SN2 ?
我认为它应该SN2基础很小,是一个带电的物种所以它可以作为亲核试剂。
也…
它改变如果我使用乙醇钠在不同溶剂对这个反应?
这是一个威廉姆森醚反应。
使用乙醇,这很好。
乙醇钠是亲核试剂吗?我们如何来知道吗?
它有一个孤对。任何带有孤对,可以捐赠(即路易斯碱)是一个潜在的亲核试剂。乙醇盐攻击H时,我们说这是作为“基地”(具体地说,这个实例的布仑斯惕基地),将导致取消。当乙醇盐攻击其他原子比H(如碳)我们说它是作为“亲核试剂”,这将导致替换。
NaBr是一个可以接受的替代氯化钠?
在什么情况下?
从所有的实践我已经很多个月了,我想“快速n脏”规则决定SN1 SN2 / E1和E2是(> 95%)适用,但是否会执行替换或消除更多的是一种直觉。如果你做足够的练习,你会主要猜它正确,纯粹由于经验。
为什么酒精KOH作为基础而水KOH作为亲核试剂E2和SN2反应?
它完全取决于衬底。反应物是什么?
使用CH3I & NANH2是什么
我得到了一枚戒指6
哦在一份元位置和CH3在另一个元CH2OH
NaNH2是基础。CH3I的卤代烷与醇盐反应。
“这是一个很好的经验法则:如果基础/亲核试剂的共轭酸小于12,E2反应将是极其不可能的。”
我没有得到这个的意义。请解释一下。
这是一个更精确的说法,软弱基地不会促进E2的反应。
在芳香胺的情况下,苯胺、联苯胺等,是如何叔胺的存在(三乙胺)诱发亲核性?(在非质子极性溶剂)
苯胺的pKa大约是30。三乙胺deprotonate它不够强大的基地。
嘿,你能告诉我这水氢氧化钠会选择机制
这实际上取决于衬底。
你好,詹姆斯,
不错的工作。只是一个简单的问题:在你的例子“SN2和E2例外:中性的亲核试剂反应”不应该三乙胺的形式取代烯烃越少。在这里你最取代烯烃。正常的规则将“主要产品w /笨重的基础:少取代烯烃的形成(位阻)”,我觉得NEt3很笨重。你能解释一下吗?我很难理解这个。
你提出一个有效的点。这可能会导致两个产品,但是我不确定的比率。我不认为NEt3太笨重,它将完全防止形成的多取代烯烃。
嗨! !
我有一个化学问题,因此最初的反应是1-bromopentane与氢氧化钠进行的SN2反应,然而实验修改可以做什么为了形式(E2产品)1 -戊烯。我已经说阻碍基地可以像中国天文学会(CH3) 3但是我需要一个实验修改之后,热量能行吗?只是通过添加头1-bromopentane将有利于E2反应而不是的SN2反应?
是的,就是这样嘛。
我明白了。
利率因素在起作用在这里吗?SN2 / E2通常比SN1 / E1(一阶二阶>)?
你能解释背后的推理规则# 3吗?(一个带电的亲核试剂或基本排除了E1 / SN1)
为什么不带电带电亲电试剂亲核试剂进攻?
通常,E1和SN1与溶剂发生亲核试剂或很弱中性的亲核试剂。因此当一个带电的物种是补充说,它往往是促进SN2或E2。
记住这些是粗略的指导方针。有大量的异常——例如胺或膦类化合物的亲核试剂,或者当一个盐KI添加到叔卤代烷叔丁基氯等。更多关于这个话题比其他测试。bdapp平台
如果我们的亲核试剂(CH3) 3 cona, E2,对吧?
和二次反应?SN1吗?
是的,应该E2。二、三级卤代烃。
你写的…
“SN2和E2通路的反应是“共同”——也就是说,亲核试剂/基础形式债券C-LG键坏了。由于重大bond-breaking发生在过渡态,这一步是高于的能量势垒的E1或SN1”
但是,C-LG债券保本的情况下SN1 / E1反应…所以上面的线怎么解释什么吗?
你可以这样认为:碳烷基卤化物SN1 sp3杂交之前。因此,四面体几何。但在形成碳正离子、碳sp2杂交,平面几何,因此,更大的稳定性。
啊…是的。我明白这是令人困惑的。我指的是* *的第二步的E1和SN1反应,* *后的碳正离子形成了。我编辑的文本,以反映。谢谢你!
P (Ph) 3是弱碱由于孤对Phospohorous与三苯基团体参与共振,因此可用的孤对减少捐赠。这将降低其能力作为基础(路易斯碱的概念)。首先这是正确的吗?
由于P (Ph) 3是一种弱碱它有利于Sn2 / E2即使bulky.Right ?
但不是弱酸强碱的共轭碱吗?HCN is a weak acid and hence its conjugate base CN- must be a strong base.
但它已经表明CN -是一种弱碱,因此不会支持E2在Sn2 !
我有一个问题。
如果亲核试剂/基础虽小,但是是一种强碱…E2 predomimate正确吗?随着质子的absraction变得容易些?
CN -强亲核试剂,但弱碱。它将支持替换消除。
CN -是弱碱? ? ! !这怎么可能?
简单的问题关于符号…当一个反应是用一种化合物在顶部的箭头,一个在底部,是那些被理解为亲核试剂(reagant)和溶剂。他们总是写在这个订单吗?我意识到这可能是一个非常基本的问题,这是年前创化学。
谢谢!
一般来说,是的。是的,他们通常总是用这种方式写的。很多时候,你也会看到反应条件(如温度和rxn时间)写在箭头。
如果我们说2-chloro-3-methylbutane然后用弱亲核试剂的反应/基地如乙醇,但我们把它在极性非质子溶剂如丙酮,这将意味着我们可以任何反应,SN2, SN1, E1和E2反应,因为极性质子溶剂中支持SN2和E2反应,因为我们有弱碱/亲核试剂应该支持SN1 / E1反应?或者有什么失踪,我起初以为因为我们有弱碱,在乙醇和非笨重中等极性非质子溶剂中烷基卤化物会经历的SN2反应,但后来我意识到乙醇基地不带电,我应该假定它被指控通过分离乙R组和哦,(哦)- ?
乙醇本身基本不太可能足以促进E2反应;我希望与乙醇的SN2反应为亲核试剂和丙酮为溶剂。
如果你有一个产品开始Cl-CH3-CH3-CH3-CH3-OH和哦——在DMF溶剂的亲核试剂吗?我知道它不工作,但是为什么呢?
啊哈…好吧,有一个反应除了替换,可以发生在Cl-CH2-CH2-CH2-CH2-OH(相比,它的快速替换)。发生后,然而,有一个取代反应,尽管也许不是你预期
詹姆斯你是怎么决定的哦——将deprotonate Cl-R-OH吗?
确实有Cl使分子的酸性比说长度相同的酒精(这反过来使得它更容易交换质子氢氧化)?
如果没有分子的长度显著降低Cl的有效性作为一个电子撤回组?
一般酸碱反应速度远远超过替换/消除由于规则我们称之为“最小的规则运动”这意味着质子转移等原子O不涉及杂交变化或任何其他重要的分子重组,而子和琳反应碳。
“酸碱反应快”。
为什么你决定,这酸碱平衡:
哦——+ CL-R-OH这里+ CL-R-O -
喜欢的产品吗?
*箭因为某种原因被删除(CL-R-OH平衡和这里)
我认为最好的紧急的快捷方式,如果衬底叔你可以排除SN2如果主忘记SN1,它让你更接近正确的答案,也许部分信贷
评论为什么没有看到? ?
请告诉我的E2反应CH3CH2CH {S (CH3) 2} CH2CH3试剂的存在,根据霍夫曼规则吗?
首先画出分子。你的离去基团是S (CH3) 2和硫上应该有一个正电荷。你会形成一个新的π键失去这离去基团和一个碳氢键附近碳碳硫。尝试画出那些潜在的产品。
Dilek,当我们谈论醋酸的电离后形成CH3COO, H,导热CH3COO -共轭基地和一个好的亲核试剂bcoz髯负,可以捐赠电子更有效。
是什么意思“共轭碱总是强亲核试剂?”
(这意味着哦)-共轭碱比水更强的亲核试剂(酸)。每当我们我们得到一个带负电荷的物种形成共轭基地。带负电荷的物种是一个更好的亲核试剂我们可以叫共轭碱强亲核试剂
是的,阿卡什。
“这是一个很好的经验法则:如果基础/亲核试剂的共轭酸小于12,E2反应会非常不可能的。”
少于12什么?我在这里困惑!这个建议听起来很方便,但我不知道为什么图12应该支持!
我不知道如果你已经算出来了,但我仍然只是想快速反应…这个数字“12”在你提到的情况的数值是pKa给定的化合物。基本上,它告诉你通过数值测量程度的化合物的酸度或碱度你看着。詹姆斯说,“如果基地/亲核试剂的共轭酸小于12,“那么基地可能是太酸,不够基本为E2作为消除剂反应途径发生的反应物和试剂。
你应该能够找到好的参考表pKa值计算和有机化合物等已经上市,在线或一个主要化学教科书(特别是o-chem教科书),如果你需要查找的值!希望这可以帮助!
对不起,但我们没有在考试中PKA值。为什么没有人明白这一点。这就是为什么我们要求如何图——我们并没有考虑到PKA值。这是最难的部分,亲核试剂和基地可以滚蛋
你应该诚实所有熟悉的pKa的常见官能团,以及常见的酸。如果你打算超越有机I和II,你一定会被要求记住这些。他们会出现在你的每一次考试,你需要知道他们能够及时解决问题。毕竟,由于时间的关系,很多人表现不佳,尤其是那些不记住重要的信息如pKa价值观和作为一个结果,查阅教科书。如果你现在开始,我保证他们会有用的,你不会忘记他们。
嘿。伟大的网站的时候,我现在可以更好地理解和享受有机化学。
一个问题。How can triphenyl phosphine be a good nucleophile ?? It has three phenyl rings then it should be sterically hindered.
首先PPh3三角金字塔形几何,所以孤对指向相反的方向从苯组。其次,c p债券相当长,降低了位阻。PPh3是个好足够的亲核试剂的SN2反应主要和次要烷基卤化物。
因此,在我的化学作业我有以下方程:
CH3CH2CH3CH3OCH3 + N3 - - - > ?
的溶剂丙酮。
这是SN1 SN2, E1, E2反应吗?我认为这可能是一个消除2反应但我困惑,因为在这种情况下我们不删除岩盐和N3 -不是我为基本上市/亲核试剂在我的笔记。
你看到一个好的离去基团…………?总是第一个问题要问
下面,你写道,“相比之下,庞大的基地下面(tert-butoxide离子)是一种强碱,但一个贫穷的亲核试剂由于其大位阻,所以E2反应比SN2更有可能。”
我认为你打错图片了
不过谢谢你这个非常有用的网站!
CH3OH比水更酸。甲基的+ I效果降低的极性
地键。是什么让CH3OH酸性更强。?
第3部分在Q2,硫酸一个中立的亲核试剂是为什么呢?似乎它会捐赠H +,然后成为带电。就是HSO4——这是惰性气体作为基础(因为它的共轭碱强酸),但由于负电荷可以体面的亲核试剂。
氧气的负电荷就是HSO4——非常共振稳定和不作为主管亲核试剂在绝大多数的情况下,所以很容易把它当作non-nucleophile。
然后从氢磺酸盐的形成到哪里来的照片吗?
如果你使用硫酸酸和酒精,就是HSO4——平衡离子。通常它不与底物反应。
关于NR3,是亲核&比得上哦——由于电负性较低的原因和诱导效应?
异常列PPh3经历SN2但P是稳定3 Ph值,因此将经历Sn1对吧?或者在P e -密度高,因为它不是电负性(不像F)即使共振稳定吗?
CH3OH比水酸性以及任何酒精卢武铉在平衡RO -和H +,所以不会RO -作为一个好亲核试剂进攻?我知道这是一个奇怪的问题但仍然我们如何解释这只会卢武铉攻击总是和RO -。请尽快回复
平衡的自电离酒精卢武铉RO -和H + 10的16次方冷宫。
但当我们带反应和看弱碱和弱酸,总是有一个盐的形成。我的观点是如果它开始反应平衡转变,整个反应!
你好,如果你有一个强亲核试剂和强碱哦——你叔卤代烷反应。不Sn1和E2途径既可能吗?然后选择是否Sn1如何工作呢?假设没有溶剂。谢谢!
E2发生哦,是一个很好的亲核试剂即不稳定所以无论进入的手将它而且Sn1因此需要穿透空间障碍提供E2优先。E2并不需要一个极性非质子溶剂(我们就这样说)
为什么E1没有发生呢
如果主要卤代烃,他们会与温和的SN2反应基地,像-哦,- cn或CH3O -。
谢谢的份额。
我昨天在考试中一个棘手的问题。想知道如果methylchloride与水反应会SN1或SN2。教授把它将SN1,但不会methylhalide SN2迫使它吗?我认为这个问题可以做或没有反应。你的意见是什么?我显然错了,因为我选择SN2自那些只有两个选择。
泰米,我同意,这不是一个公平的问题。
甲基卤化物不会使用SN1反应不可能因为一个甲基碳正离子形成。它也不会使用SN2因为水是极性质子反应。
和你的教授谈谈吧!
你错了,因为你选择了对氯甲烷SN2 ? ? ? ?是谁教你SN1发生在甲基阳离子不知道他们在做什么。
它必须是SN2。甲基cabocation极其不稳定。如果它是一个叔碳正离子,它会通过诱导效应稳定。SN1需要一个稳定的阳离子进行。SN2另一方面不需要,和它直接攻击电子缺乏碳原子形成一个中间。唯一推出sn2位阻,完全没有在一个小小的像甲基碳正离子。是的,它的Sn2。至少你知道比谁教给你:D