二烯烃和MO理论
结合有机化学共振
最后更新:2023年1月17日|
结合有机化学:定义,例子,探索,和后果
这是第一个在一系列的文章涵盖接合,π体系,分子轨道理论,双烯、1,2 - 1,4 -添加,一昼夜的桤木的反应和其他pericyclic反应。我们将开始通过回顾基础知识!
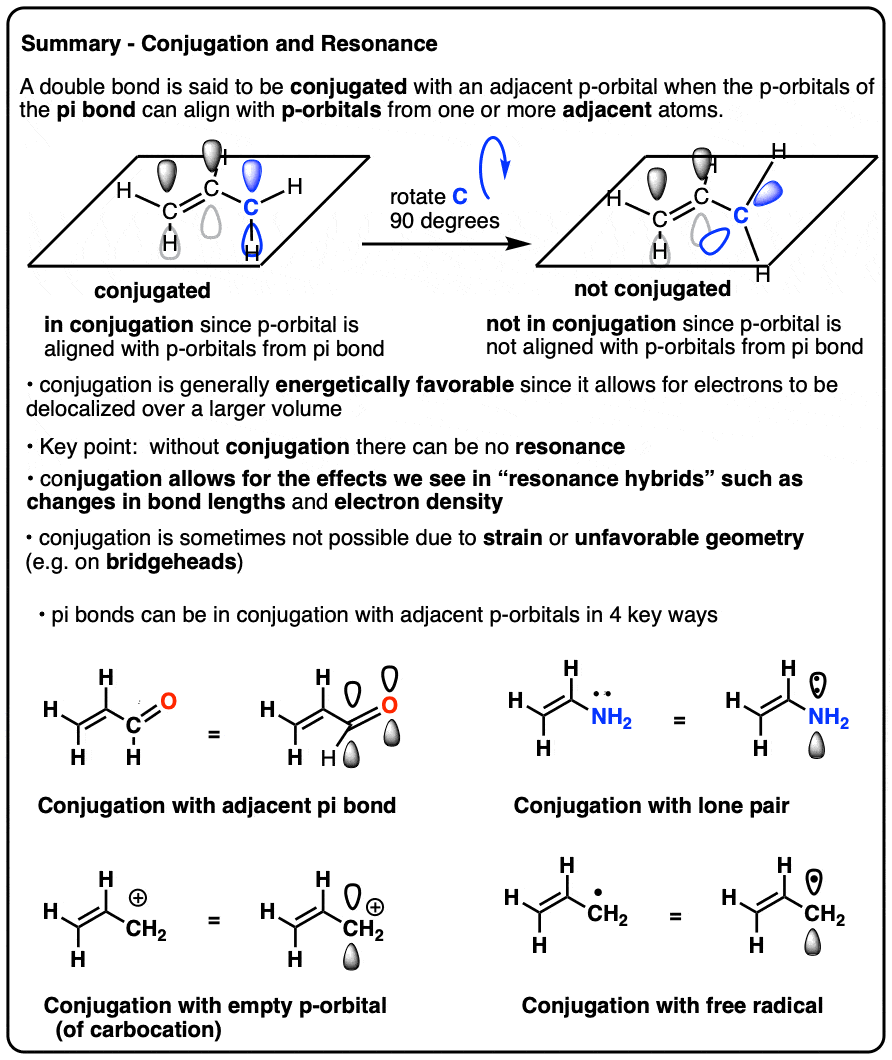
- π键(π-bonds)是由两个相邻p轨道的重叠
- 如果一个p轨道存在一个原子相邻π键,那么它也可以与π键的p轨道重叠,提供它是对齐的同一架飞机
- 这种重叠被称为动词的词形变化我们允许de-localization电子电话共振。
- 原子可以包含一个p轨道包括碳正离子、原子轴承孤,参与一个相邻的原子π键和原子轴承自由基
- 结合相邻的原子π键将影响其债券的长度和电子分布
- 结合是不可能的桥头堡许多二环原子分子,因为桥头堡的p轨道不能正常与p轨道重叠相邻原子。
表的内容
- 回顾π键和π键:“旁边”轨道重叠相邻的p轨道
- 为π成键轨道重叠的重要性
- 除了π键:“接合”的3 p轨道
- 结合之间的区别和共振
- 结合的后果(1):债券的长度
- 当共振形式并不相同,共振杂化将是一个最重要的“加权”混合共振形式
- 结合(2)的后果:“部分”双键
- 接合的后果(3):共轭体系的反应通常是揭示了其“次佳”共振的形式
- 轨道重叠(所有p轨道在同一个平面上)需要结合(共振)
- 桥头堡酰胺不共轭,比“普通”酰胺更容易破碎
- 更多的接合的后果:颜色和环加
- 接下来:分子轨道理论
- 笔记
1。回顾π键和π键:“旁边”轨道重叠相邻的p轨道
的第一件事你了解烯烃是,旋转的碳碳π(π)债券不发生。例如,在正常的温度和压力。反式2-butene(左)所示是从来没有观察到自发地皈依独联体2-butene(右)。他们分离化合物,熔点和沸点不同。你可以买他们每个人分开奥尔德里奇。这不会是可能的如果有自由旋转的双键。
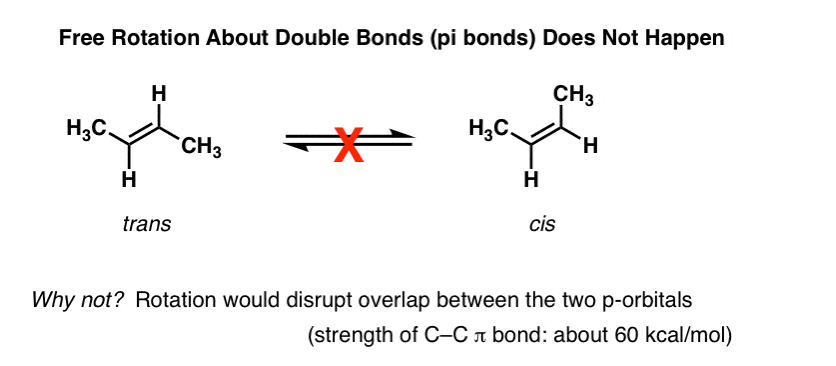
深入了解这一点,我们看到,这是由于一种现象叫做“π键”——一个重叠的两个相邻p轨道的旁边,每个都包含一个电子,结果在一个p轨道的择优取向“排队”相邻,像士兵一样。由于dumbbell-like p轨道的几何重叠时,不可能两个p轨道在90°,占“旋转障碍”。
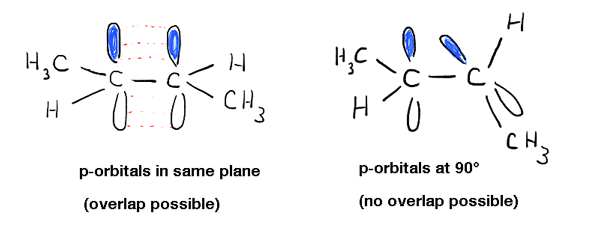
(阴影(蓝色)和无遮蔽的(白色)叶的每个p轨道代表一个属性叫做“相”,这是p轨道的属性——我建议重新考虑这个话题如果这让你感到不适,因为我们将使用它在未来的文章很多。如波,叶之间有建设性干涉的“喜欢”阶段,和叶之间的相消干涉的“与”阶段)
这有旋转障碍以外的其他物理后果:它的影响分子几何。由于Pi-bonding p轨道独有现象,这意味着每一个π键原子参与将少一个p轨道供”杂交剩余”s轨道和p轨道(s)]原子(见文章:杂化轨道)。这导致了熟悉的“三角平面”(sp2)为典型的几何烯烃碳和“线性”几何(sp)炔烃碳原子。
2。为π成键轨道重叠的重要性
一个生动的例子的重要性提出了轨道重叠的情况我们会天真地认为一个双键,“应该”形式但不。Bredt1924年观察到的,烯烃往往不会形成“桥头堡”头寸,如在左下角分子,观察到被称为“Bredt法则”。
为什么不呢?如果你把模型,您将看到双环戒指部队那些p轨道的几何定向成直角。没有p轨道之间的重叠。因此,它像一个有两个相邻的碳激进分子超过它真正的π键!
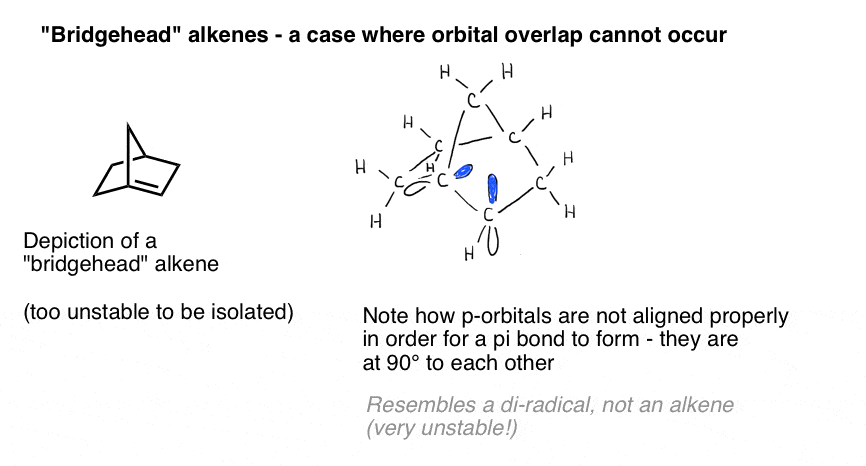
三维图纸放在一个平面上真的不公平对待的荣耀三维结构。这是一个模型和相应的视频。[把葡萄树,这是很棒的有机化学视频短片)
这些粉红色的东西应该是p轨道。看到他们彼此成直角?这意味着他们不重叠。
底线是,你需要p轨道重叠一个π键组成。在非循环系统,通常不是一个问题(见注1著名的例外)
3所示。除了π键:“接合”的3 p轨道
有机化学在第一学期我们学习这种重叠的p轨道并不一定局限于两个相邻p轨道。可以超越两个p轨道包括重叠三,四,五,甚至更多个p轨道连续原子,建造更大“pi-systems”(见证番茄红素,例如)。
我们也看到,“p轨道”是比较灵活的定义,和可以包括如例子
我们称之为“建立”的p轨道成规模更大的“π系统”,“结合”。下面,在中间的每一个分子烯烃(π键)是共轭相邻p轨道。
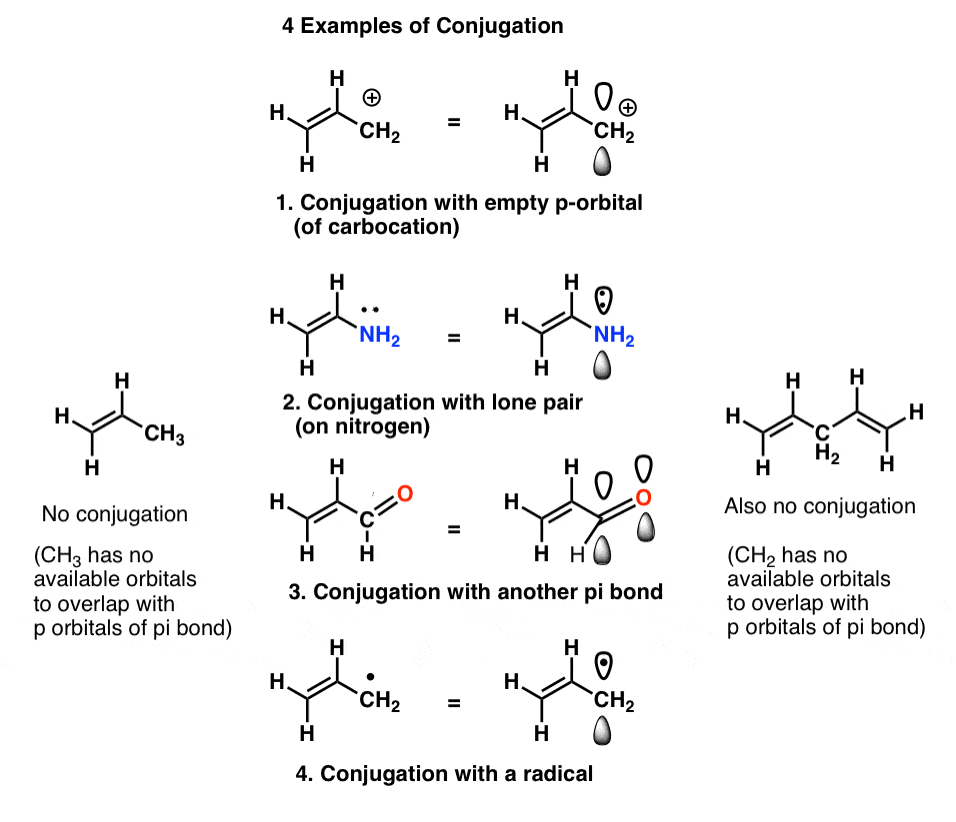
小心的“共轭杀手”是一个原子缺少孤只单键相连,如CH2在示例below-right (1, 4-pentadiene)。这两个π键不共轭。
(第二个例子的注意。我们通常认为的几何氮与三个单键三角金字塔形(如在北半球3)。但在一个相邻的π键的存在,有一个轻微的“re -杂交“从sp的氮3对sp2(三角形的平面),这样的孤对p轨道,不是一个sp3轨道。这是一种权衡:黯然失色的应变略有增加氮氢键是由由整体能源减少由于p轨道的重叠与π键。我们通常认为这是“共振能量”。)
这是一个有趣的技巧问题。下面的分子中双键(丙二烯)结合?为什么或为什么不呢?
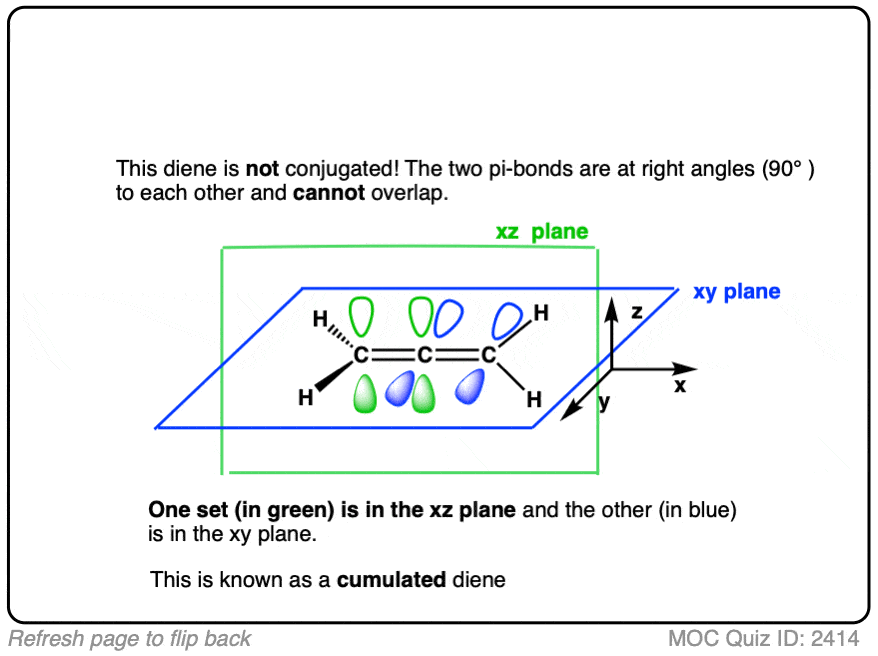
4所示。结合之间的区别和共振
你可能会问:这听起来像共振。有什么区别呢?
我们来看第二个区分动词的词形变化和共振。
- 动词的词形变化的时候就是我们所说的3或更多的p轨道连接在一起成一个更大的“π体系”。
- 这些共轭π系统包含电子,我们常常称之为“π电子”区别于电子在分子组成单一债券。
- 电子的不同安排在这个被称为“π体系”共振形式。
一个粗略的类比可以是这样的:
- 认为p轨道是有点像“房间”电子(最大占用:2)
- 加入一些房间在一起成一个更大的建筑是接合
- 不同的容许安排人(电子)大楼是共振形式。
结合的关键需求轨道重叠,我们将扩大。
现在,让我们回顾一些接合的后果。
5。结合的后果(1):债券的长度
就像我刚才说的,我们更多的上下文中用于接合”共振”,一个概念我们之前覆盖(因为这个系列是进入学期领土,值得表演自己)
例如,与醋酸盐离子(CH3有限公司2)- - - - - -和烯丙基阳离子(如下所示),我们发现有两种不同的方式安排π电子,我们称之为“共振形式”。
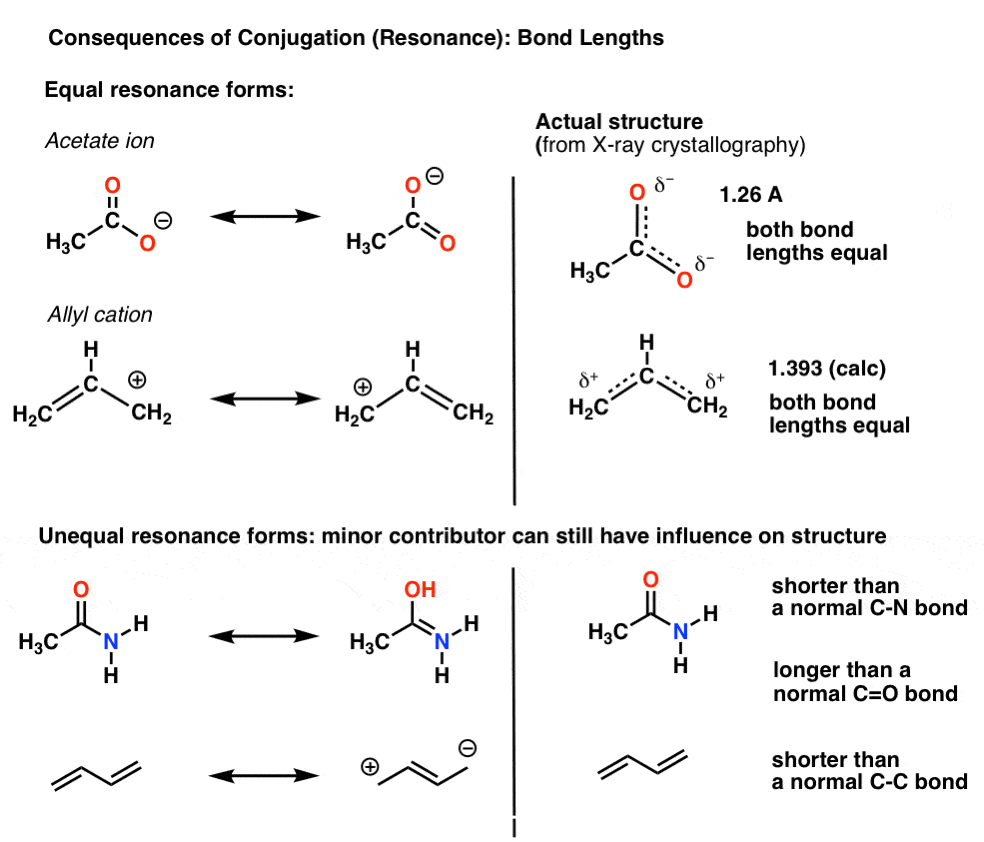
π电子的重要的一点要注意的是,这些都不是原子之间不停地来回切换;相反,“真实”的分子是一种混合结构的共振形式。
一个重要的共振的结果债券长度介于两种形式。
例如,切断键长在乙酸离子(1.26)我们期望之间切断π键(1.20)和碳氧单键(1.4)。
6。当共振形式并不相同,共振杂化将是一个最重要的“加权”混合共振形式
在醋酸盐离子和烯丙基阳离子的形式是两个重要的共鸣等效,所以都最终造成同样的混合。
更常见的情况是发现分子的下面有一个混合的不平等的共振形式。一些共振形式比其他人更重要。(回到决定如何评估共振的形式,去这一系列的文章吗。]。
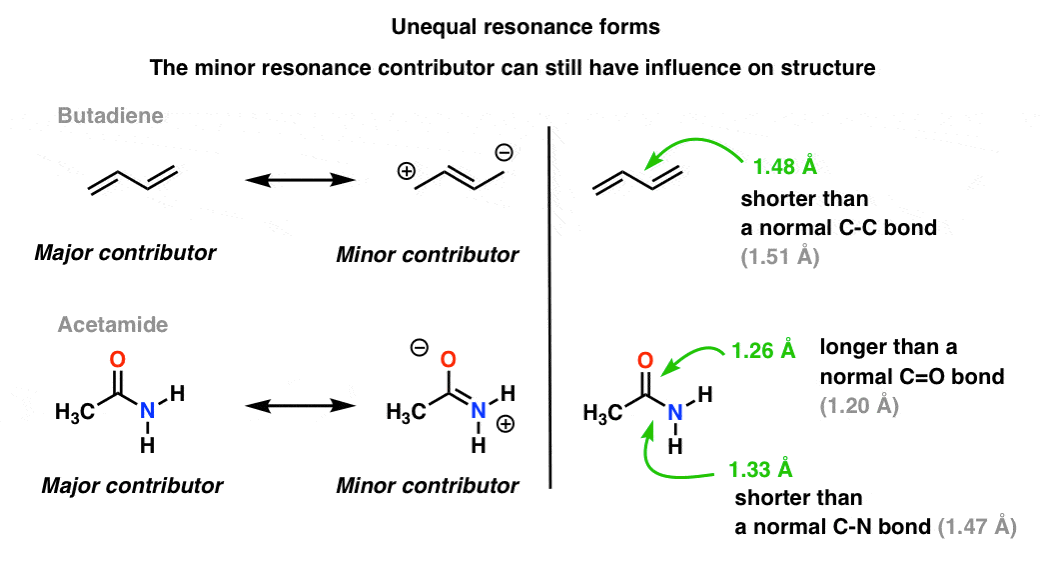
化学的视觉语言用它那锋利的单键和双键之间的区别并不准确描绘分子的电子密度,一个加权混合动力共振的形式。小共振贡献者影响分子中键的长度,使其比平常更短或更长时间。
在分子(丁二烯),中央碳碳键有点更短的比“正常”的碳碳单键双键(即它的字符)由于混合小共振的影响因素。(注意,键长不是介于单引号和双碳碳键,因为它是在烯丙基阳离子:这是因为两种共振形式不是同样重要(即不做出同等的贡献共振混合))
在底部的分子(乙酰胺)切断键有点长比“正常”的C = O键(即有单键字符)和碳氮键有点更短的比“正常”的碳氮键(即含有更多的双键字符)。这反映了“小因素”的影响(或“第二最好”的因素,如果你喜欢)中有一个碳氮π键和碳氧单键。
让我们使我们的第一个概念上的飞跃。
7所示。结合(2)的后果:“部分”双键
有一个有趣的结论“部分双键特性”碳氮键。它有一个“旋转障碍”就像我们期望从一个“双键”!碳氮键的旋转障碍酰胺大约是15 - 20千卡每摩尔肽债券(比较碳碳键约2 - 3千卡每摩尔)。
这意味着两个构象可以还互变,但在室温下相对缓慢。在下面的分子(N甲基乙酰胺)可以观察年代- - - - - -独联体构象异构体(绿色甲基碳氮键的同侧)和s -反式构象异构体(绿色甲基碳氮键的两边)分开。(注意4矫形器)这通常是不可能的,除非你把温度降至100 k左右!
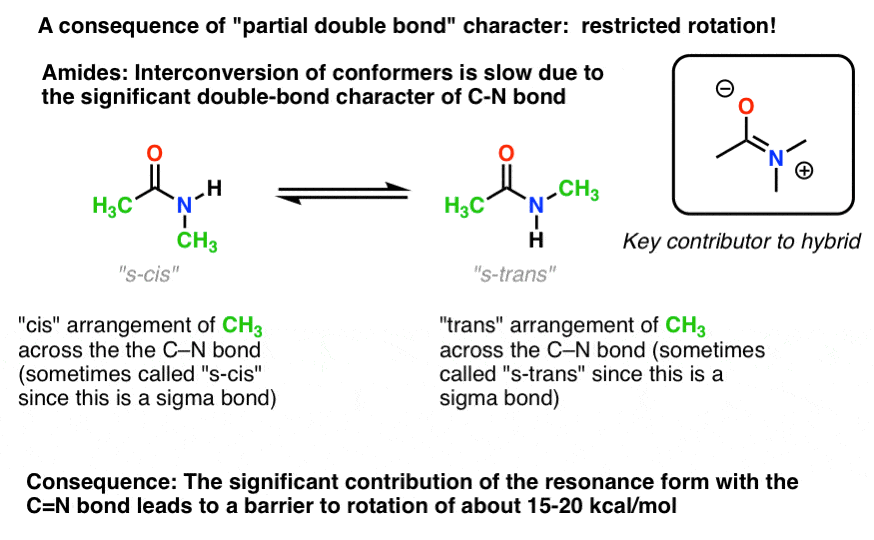
上图,这里的关键概念只是部分双键的性格。如果年代- - - - - -独联体和年代- - - - - -反式对你没有意义的思考之后,没关系。不重要的讨论。
8。接合的后果(3):共轭体系的反应通常是揭示了其“次佳”共振的形式
我们已经证明接合的作用(进而共振)债券的长度。
让我们仔细看看它的影响电子密度,最终影响反应性。
为了便于说明,让我们继续看烯烃。
的反应性烯烃可以通过附件修改显著不同的组。
看看“第二最好的”当我们附上一个共振形式pi-donor比如N (CH3)2到一个烯烃。这将导致增加负电荷(δ- - - - - -在终端的碳烯烃,结果是这样烯烃(我们称之为一个烯胺)是一个很好的亲核试剂。一个突出的例子,烯胺反应烷基卤化物(比如CH3我)和其他亲电试剂反应有时被称为一个类鹳烯胺反应后其发现者,吉尔伯特鹳。普通的烯烃如2-butene(下图)不工作在这个反应。
附件的pi-acceptor如C = O结果累积的正电荷(δ+)的终端碳烯烃,结果是这个物种(我们称之为α,β不饱和醛,迈克尔受体,或enone)是一个很好的亲电试剂。α,β不饱和金属羰基合物与亲核试剂(如CH反应3年代- - - - - -)和许多其他类型的我们叫的亲核试剂一般类型的反应共轭添加有时迈克尔反应。
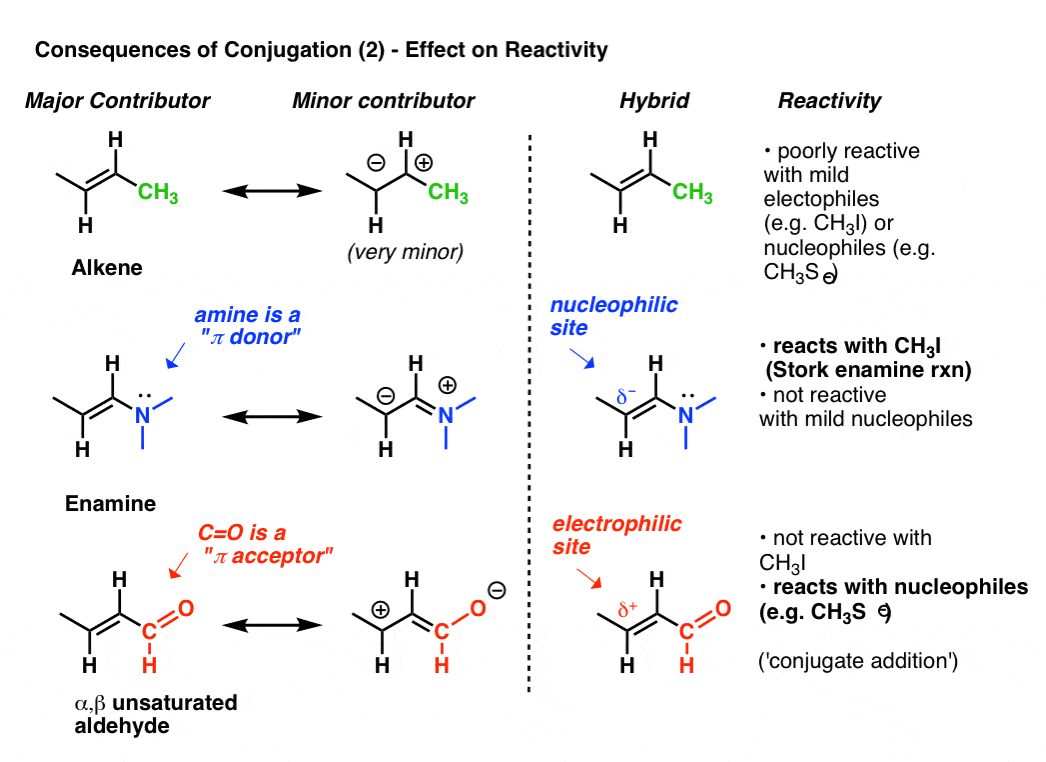
这仅仅是冰山的一角,词形变化如何影响反应活性,但今天就足够了。
9。轨道重叠(所有p轨道在同一个平面上)需要结合(共振)
到目前为止,我们已经看到:
- p轨道重叠形成π键是必要的
- 一些“单键”可以“π键字符”由于贡献从一个小共振形式(例如酰胺等)
这两个语句的逻辑后果:
- 为了结合存在,因此为了使共振发生时,所有的p轨道必须重叠。他们必须保持一致在同一个平面上。
还记得“烯丙基阳离子”“共振稳定”?为了获得这种“共振稳定的碳正离子,空的p轨道碳正离子必须与相邻的π键排列。
如果p轨道在一个90度角p轨道的π键,没有结合,因此没有共振稳定。
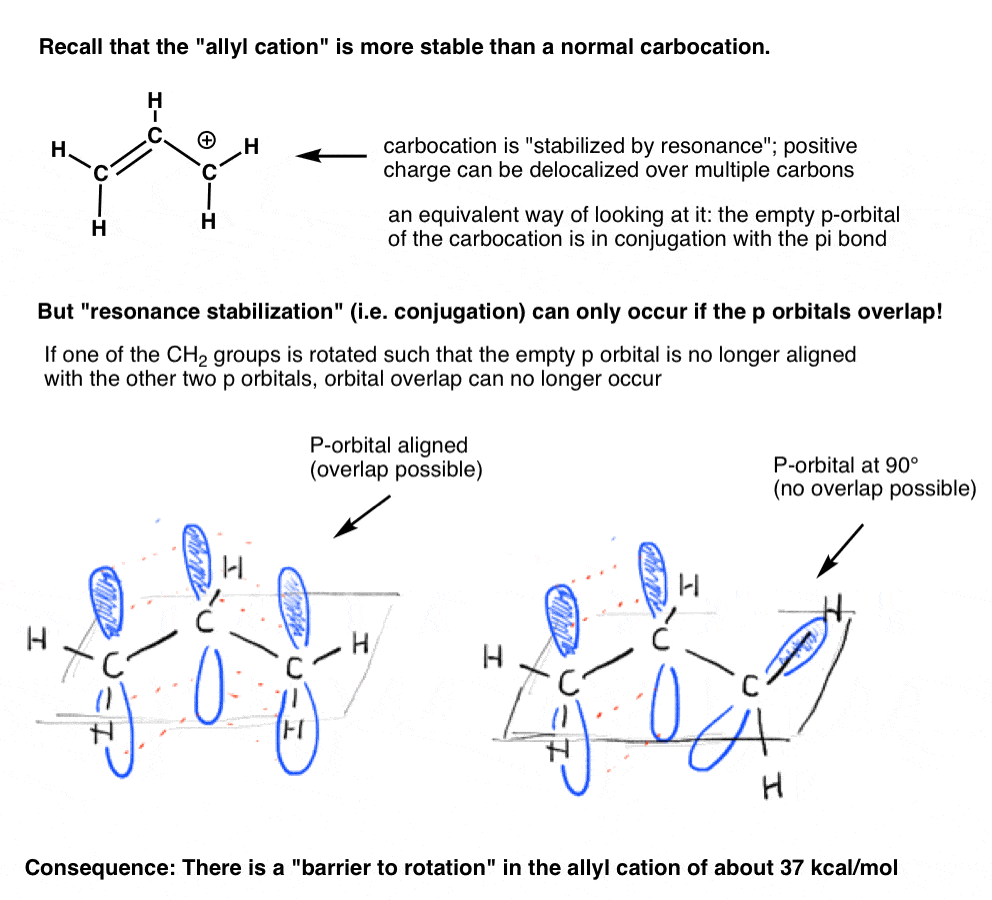
我们可以预测,有一个障碍烯丙基阳离子旋转,就像一个旋转的障碍烯烃。烯丙基阳离子的旋转的障碍37个千卡每摩尔——一半多一点的力量碳碳π键。
我们也看到,酰胺的碳氮键部分双键特性,障碍旋转约15 - 20千卡每摩尔。
同样,这只是“部分双键”字符可能含有孤对p轨道能够重叠的p轨道组成的C = Oπ键。
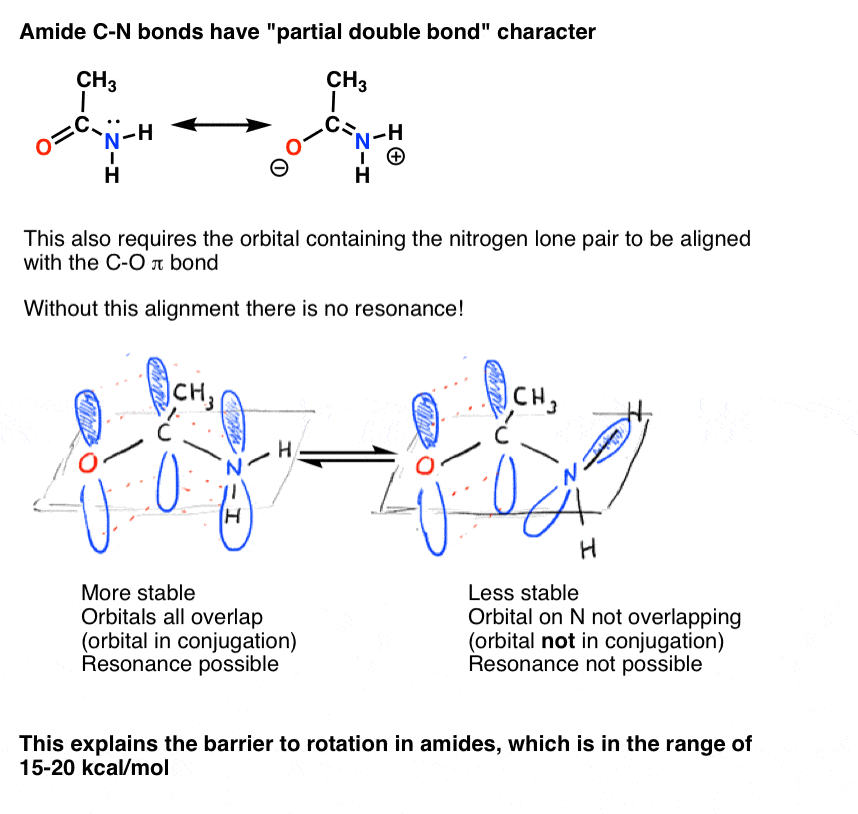
部分双键碳氮键的字符酰胺一直被认为是主要的原因为什么他们更耐破损,说,酯类(一个先进的治疗,明白了注2]。因为我们身体中的蛋白质是加入了肽(酰胺)的联系,这是一个不小的重要的事情!生命形式的基础上酯而不是酰胺的联系将会更加脆弱!
10。桥头堡酰胺不共轭,比“普通”酰胺更容易破碎
桥头堡酰胺给的例子发生在酰胺重叠时是不可能的。
正如我们看到的桥头堡烯烃在桥头堡酰胺氮孤对和轨道之间的重叠羰基碳是不可能由于扭曲。结果是,碳氮键没有部分双键的性格和很容易打破比“正常”的酰胺。
下面的桥头堡酰胺是“quinuclidone”,一个扭曲的酰胺,躲避合成了几十年。直到2006年,终于(就像它共轭酸通过实验室的一个聪明的路线)布莱恩Stoltz加州理工学院。
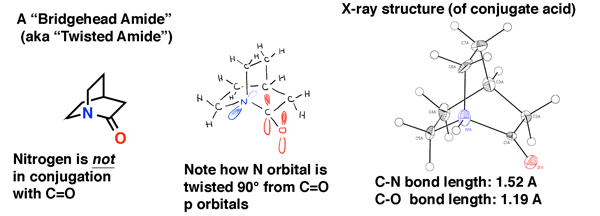
x射线晶体结构见证缺乏结合酰胺。碳氮键的长度是1.52(典型的单一碳氮键)和C = O键长是1.19,这是一个典型的键长醛或酮(1.20)。我们会因此认为不少比正常酰胺不稳定对亲核攻击,这是证实Stoltz实验室的研究。
11。更多的接合的后果:颜色和环加
到目前为止,这篇文章几乎是第一学期的回顾的概念。没有什么在上面的讨论中,无法合理解释我们已经学习了共轭和共振。
然而,这个简单的方法只能带我们到目前为止。
两个简单的例子,因为这篇文章已经足够长的时间。
第一:共轭和颜色
如果你看到这篇文章漂白剂是如何工作的,你知道我们延长共轭长度,我们改变分子吸收光的波长。一些色彩鲜艳的分子如胡萝卜素、番茄红素和叶绿素都有很长的共轭双键。
例如,番茄红素是负责红色的西红柿。如果我们删除双键,我们删除颜色。为什么?
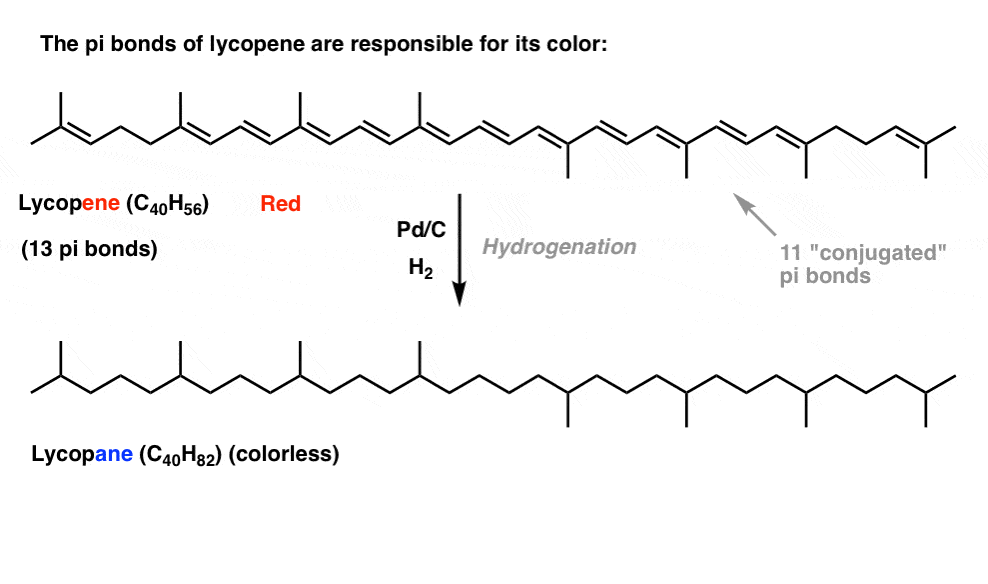
颜色和共轭之间的关系是什么?为什么双键的数目会有影响吗?共振未能阐明这个问题。bdapp平台
第二:二烯烃的反应,形成环
这里有一些奇怪的反应。
如果你善待丁二烯分子其(马来酸甲基)你获得新产品包含一个六元环。没有我们看到到目前为止准备我们这种类型的反应,叫做“环加成作用”。
有趣的是,如果你把相同的乙烯分子,什么也不会发生(除非你用紫外线治疗它。然后你会得到一个4-membered戒指,但我跑题了)。
为什么?
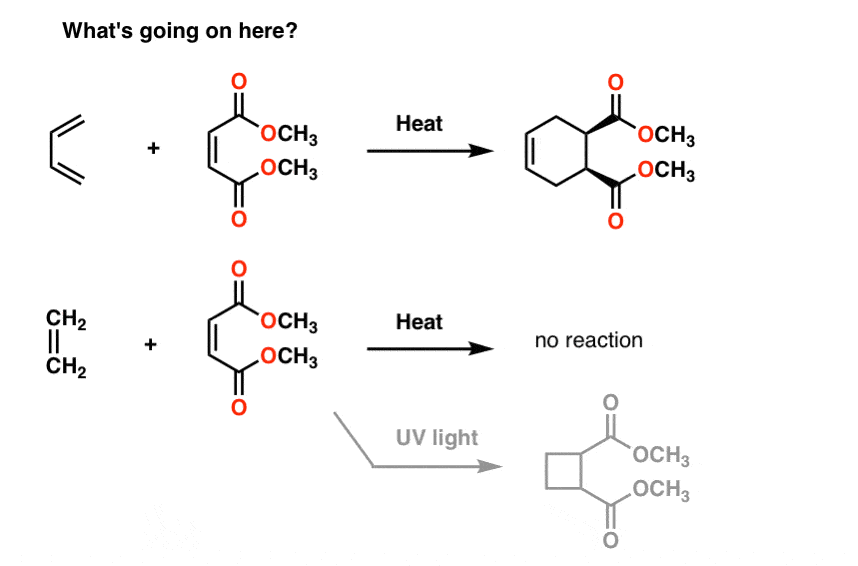
共振并不能帮助我们。
12。接下来:分子轨道理论
什么将帮助我们回答这些问题,以及许多其他的未来是一个概念分子轨道理论。
在接下来的本系列文章中,我们将更深入挖掘如何p轨道的重叠形式分子轨道,我们将检查这些轨道的能级。我们还将看到如何影响分子的反应活性,使我们对它们的化学行为进行预测。
我们会看到,分子轨道理论为我们提供了一个非常强大的概念,将帮助我们了解化学反应在更深层面上。
感谢汤姆Struble他所有的帮助这篇文章。
笔记
注1。a - 1, 2菌株的原因tetra-tert-butylethylene尚未合成。
注2。π键是不共轭。看组成两个π键的轨道。他们相互成直角,不能重叠。
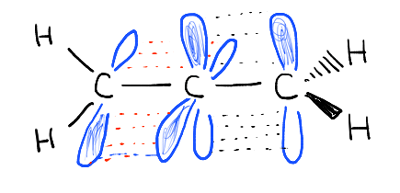
注3。最近的工作表明,共振是不像被认为重要的酰胺键限制。看到在这里(现代物理有机化学Anslyn和多尔蒂,23页))
注4。利用核磁共振、核磁共振光谱学。这些构象异构体是有时被称为“旋转异构体”或“旋转异构体”,他们可以使核磁共振光谱。峰值通常可以被加热合并样本调查。
这种鲜明的对比,不同的椅子形式的环己烷,通常仍然可以互换在室温和合并到一个高峰。但是如果你酷足够取代环己烷可以“冻结”分别不同的矫形器和观察。
这是很好的和有用的。(我跑过而寻找共轭和共振关系)
你把相关评论一个共同的主题非常好。我现在提示您看看其他的作品。
谢谢
将but-1-en-3-yne只有2轨道共轭因为它是平行的吗?,只有2分子轨道图?
是的。一个π键的炔共轭烯烃π键,但另一个不会。
同时,共轭体系的分子轨道图4 p轨道(两个π键)不会6 p轨道。
非常感谢您的有价值的工作。这是很明显的。
谢谢拉吉,我很高兴你发现它有用。
这是如此有用你解释一切很好,谢谢!
这个页面(Ashenhurst j . (2019)。结合和有机化学中共振)组织,全面,和非常非常清楚。很神奇的。谢谢你!
谢谢你阿提克斯,很高兴你有帮助——詹姆斯
u问关于丙二烯,它不会参与结合r p轨道垂直的和我们所知共轭之间发生异于寻常平行p轨道
谢谢你
这是正确的。
为什么不能酮的共轭而酯可以吗?
酮可以参与接合。例如,α,β不饱和酮共轭。