焊接、结构和共鸣
轨道杂化和债券的优势
最后更新:2022年12月13日|
如何轨道杂交影响债券的优点
理解杂化轨道的概念(见以前的帖子)让你在债券的优势发展趋势作出准确的预测。在本帖里,我们将给几个例子如何做到这一点。
表的内容
- 一个快速测试(键离解能)
- 关键原则轨道杂化和债券的优点:提到越大,债券越强
- 电子年代比电子轨道更接近原子核在相应的p轨道
- 摘要:在其他条件保持不变的情况下,提到越大,债券越强
- 奖金部分:答案,一些人可能会问的问题
- 均裂与异种溶解的债券乳沟
- 给你一个测试
- 最后一件事:这个概念也解释了为什么CH3比NH +更稳定3+
- 笔记
1。一个快速测试
让我们先从一个快速测试。
最强的碳氢键,下面吗?
(换句话说,碳氢键键裂解最高能量?)
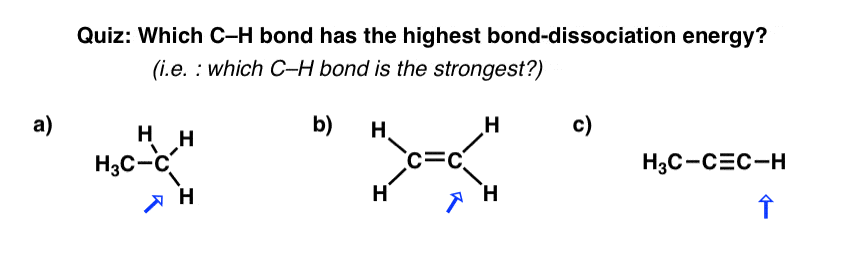
答案是C。
- ),碳sp3杂化键离解能是105千卡每摩尔
- 在b),碳sp2杂化键离解能是110千卡每摩尔
- 在c),碳是sp杂化键离解能是126千卡每摩尔
2。关键原则轨道杂化和债券的优点:提到越大,债券越强
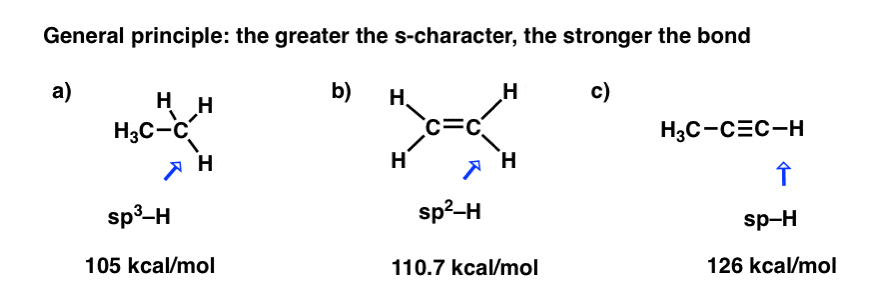
注意,上面的趋势对债券的优点,,是sp > sp2> sp3
换句话说,更多的提到碳,更强的债券。
让我们再试试这个。这三个碳碳键呢?
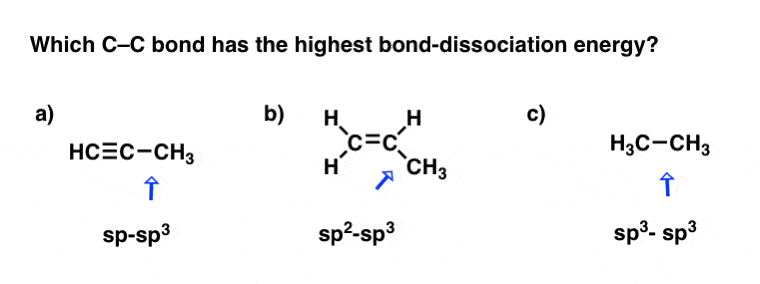
希望你排名B > C >。
其他所有条件都相同:一个sp-sp3债券比一个sp2- sp3键,反过来比一个sp吗3- sp3债券。
为什么?
3所示。电子年代比电子轨道更接近原子核在相应的p轨道
平均:电子年代轨道更接近原子核(因此感到更有效的正电荷)比电子在相应的p轨道。
电子在一个sp轨道(50%提到)将经历更大的吸引力比电子离核sp2(提到33%)或sp3(提到25%)轨道。
“键离解能”(12)上面所提到的,是一个测量所需的能量均裂劈理的债券(人类=相同;溶菌作用=打破)。(参见:键离解能量=均裂]
也就是说,它的措施所需的能量破损的债券,这样每个原子最终相同数量的电子,如以下反应:
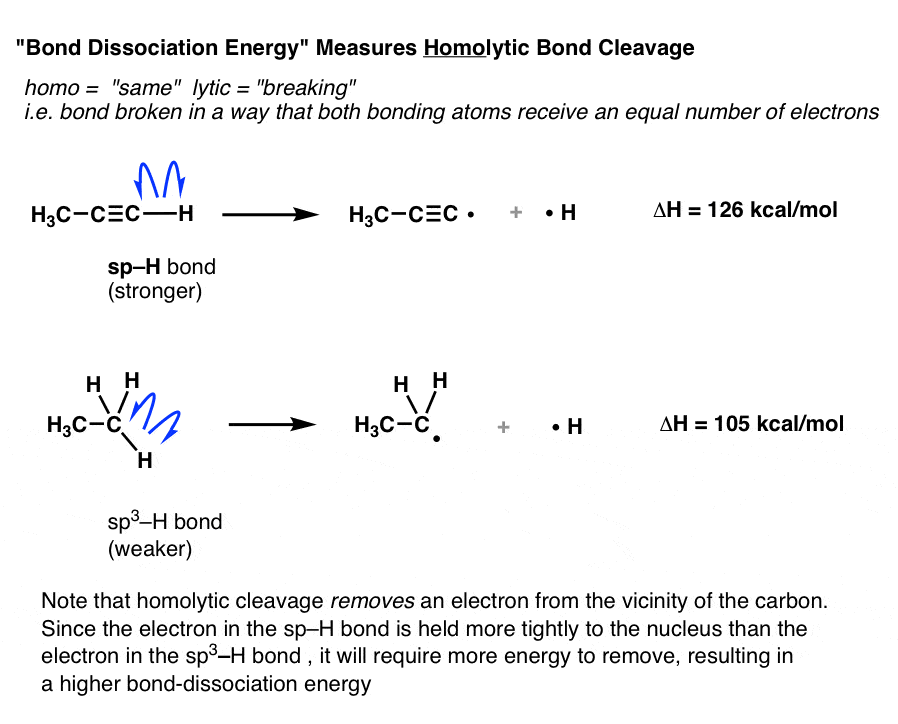
在均裂上面的反应,一个电子删除碳氢键分子轨道和放置在氢,水解。其他电子仍在碳。
sp-H键的键离解能高于sp3- h因为更多的部队(能源)移去一个电子所需要的更牢牢攥在手中,sp-H分子轨道,并将其氢原子。
因此电子在轨道和s轨道将接近原子核和感觉更强的静电力。
这有助于解释键能越高。
在分子识别类型的债券是一项关键的技能。(参见:碳碳σ键有六个品种,碳碳π键进来)。
对于大多数的目的,这目的的关键教训。
4所示。摘要:在其他条件保持不变的情况下,提到越大,债券越强
但是…如果你发现自己试图调和一个明显的矛盾,来自另一个课程的一部分,继续读下去。
5。奖金部分:答案,一些人可能会问的问题
炔烃(pK一个25比典型的烷烃(pK)更强的酸一个> 50)。
例如,炔烃很容易deprotonated NaNH等强大的基地吗2,而烷烃不:
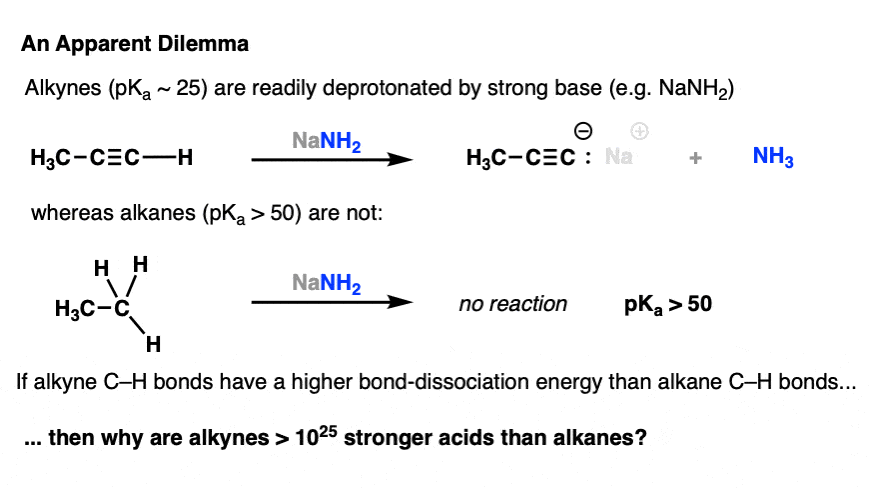
为什么?因为在一个碳氢键炔烃有更多的年代字符,由此产生的孤对碳举行更严格的细胞核呈现共轭碱更稳定的。
哦亲爱的。似乎有一群愤怒的暴民接近。
等等!你只是说,炔烃碳氢键是更强的比烷烃碳氢键,因为他们有更多的提到,现在你说他们更容易打破因为他们有更多的提到。
不应该让炔烃少酸性因为碳氢键有更多的提到吗?

把干草叉!这是一种非常合理的解释!
6。均裂与异种溶解的债券乳沟
混乱的根源是什么?
让我们跟随电子。
最终解决这个难题是识别的区别均裂劈理(这是什么键离解能的措施)异种溶解的劈理(这是发生在一个酸碱反应,H +)的损失。
让我们看看这两个过程。
在均裂碳氢键,一个电子是完全从附近的碳和氢。因为大提到的债券,它更难移去一个电子从一个从sp sp-hybridized碳比3杂化碳。正如我们上面所说的,这就是为什么需要能量炔烃碳氢键是高于烷烃碳氢键。
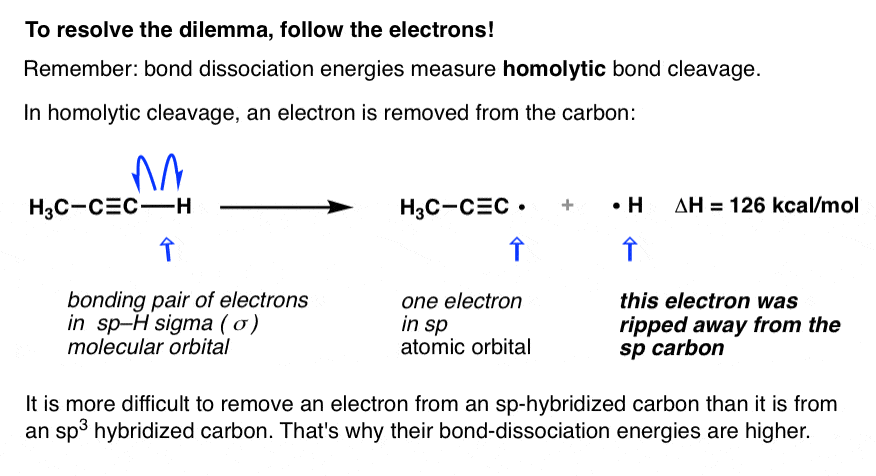 酸碱反应,碳氢键也休息,但它打破了这样一对电子保持在碳原子上。由于债券的方式导致了不均匀电子的分布,它被称为异种溶解的债券劈理(异性恋=不同,溶解=打破)。
酸碱反应,碳氢键也休息,但它打破了这样一对电子保持在碳原子上。由于债券的方式导致了不均匀电子的分布,它被称为异种溶解的债券劈理(异性恋=不同,溶解=打破)。
让我们再说一遍:酸碱反应,对电子保持碳,导致带负电荷的碳原子(“负碳离子”)。
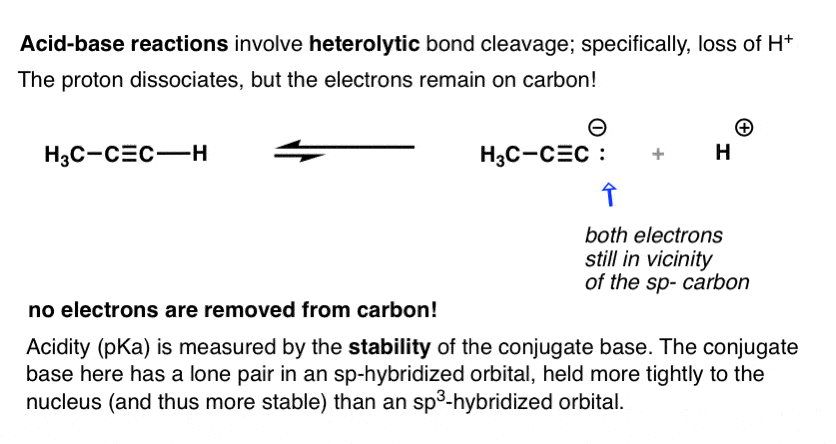
酸度,以pK一个是一个衡量一个酸及其之间的平衡共轭碱。越平衡支持共轭碱,pK越低一个和较强的酸。换句话说:
这使得任何因素共轭碱更稳定,增加酸度。
什么孤对会更稳定?
更紧密的孤对核—也就是说,sp-orbital。
希望这使它更清晰更强的碳氢键和更大的碳氢键酸度的两面的现象。
(你会发现它有助于认为sp轨道有效的电负性大于sp2轨道,从而有一个电负性大于sp3轨道。所以酸度越大的原因炔烃相对于烯烃不是真的那么不同酸度越大的氢氟键相对于H2o .]
7所示。给你一个测试
在嗡嗡作响的风险,有一个第三方的这种现象需要考虑。
均裂只能发生的一种方法。但也有两个碳氢键的方法画异种溶解的乳沟,你可能已经注意到,我只显示一个。
还有第二种(虽然不太可能)异种溶解的乳沟可以发生。碳氢键的一对电子迁移而不是氢,碳,导致氢化物阴离子和碳正离子。(再一次,不太可能,但容忍我这里)。
这是一个测试我对你。基于所有我们经历了到目前为止,这下面的两个产品(A或B)会更稳定?
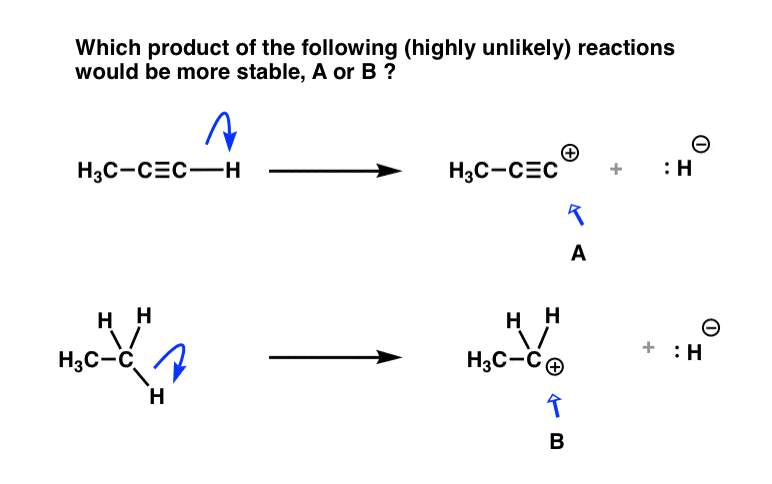
认为它通过。
- 形成,我们必须把一对电子从一个sp-hybridized碳。
- 形成B,我们必须把一对电子从一个sp3杂化碳。
更有利的是什么?
- 反应给需要删除两个电子从一个sp-hybridized碳。
- 反应给B需要把两个电子从一个sp3杂化碳。
反应给B应该容易得多,因为电子不太紧密了。事实上,sp3杂化碳正离子曾被观察到,甚至孤立。
相比之下,sp-hybridized碳正离子如一个极其不稳定的和从来没有直接观察到。(注1]
这个观察也符合上面所有的观察!
8。最后一件事:这个概念也解释了为什么CH3比NH +更稳定3+
正如上面我说的,它可以帮助认为sp-hybridized碳有效的电负性大于sp2杂化碳原子,从而有更大的电负性比sp3杂化碳原子。我们使用这个合理化的原因炔烃更强的酸比烷烃,类似于为什么氢氟键比H酸走强2O。
这也可以翻转了,就像在上面的碳正离子的例子。
原子的电负性越大,越不稳定缺电子的物种。
这有助于解释为什么,例如,H3C +(6个价电子)多比H更稳定3N +(也有六个价电子)反过来远比氧气或与六氟价电子更稳定;增加电负性具有相同的缺电子的稳定性影响物种增加提到。
笔记
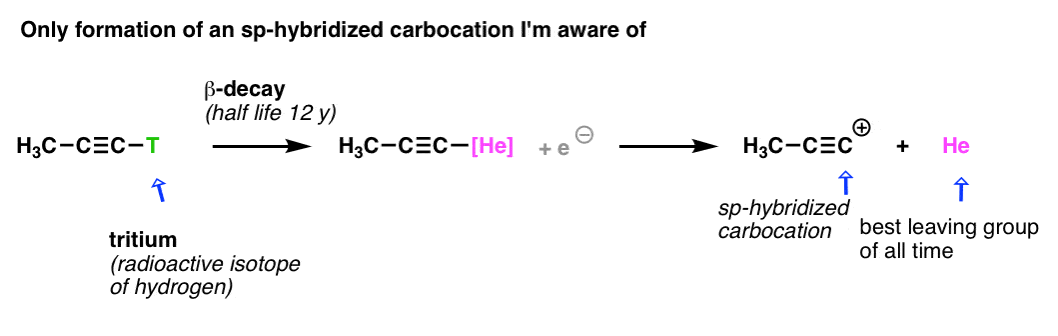
注1:这是一个值得关注的试图使sp-hybridized碳正离子。唯一的氦在有机化学中的应用,我见过。
杂交有限只碳?
不——氮、氧、硫、其他原子轨道杂化
第7部分你问哪个产品最稳定,但讨论处理的反应,每一点你是明智的。sp3轨道(B)的反应将有助于更有利的反应相比,sp轨道(a)的反应。我的问题是,也许我对这事太多心了很多经验与苯乙炔基结束描述和氟化环烯烃,不会电子丰富三键往往借电子在分子de-localize碳正离子使甲基乙炔产品更稳定。维克多说的好如何干扰三键会导致快速反应/聚合反应。我知道答案不会麻烦只有乙炔但在我头脑混乱的头脑甲基搅浑了结果。或者我把箭地像我在学校几十年前所做的一样。同时,这个网站是惊人的。
谢谢就好了
我可以用键离解能和键能源interachegeablly ?
是的,这是正确的。
σ键是最强的
A - s_重叠
B - s p重叠
C - p p重叠
吉姆,我试着发帖评论两次。我小心翼翼地复制和粘贴和阅读在这个盒子只是检查就可以了。但每次我的一些评论被删除后发送和读取可怕。啊!为什么? ! ?第三次幸运(可能没有)
吉姆,
首先,谢谢你的优秀文章(和数据)澄清很多点。
我的问题与你的文章的第二部分有关。麻烦我不理解,在一个电子对酸/碱反应喜欢坐在一个轨道有s轨道而不是一个p。
但是我想我的问题是当你说认为烷烃/炔酸碱性质类似于跨连续电负性,另一种可能是把一列,在更小、更原子的电负性更糟酸(盐酸高频< < <哈佛商业评论<嗨)。
所以不会碳氢键也有s轨道稳定债券更好?符合这个碳氢键长度从烷烃炔烃略有减少。
显然实验数据支持你的思维方式…但有化学直觉可以用来解释为什么一个应立即想到这是穿过一行而不是一个列?
我能想出的最好的是,这里的大小的变化是非常温和的你从烷烃炔烃更符合穿过一排,即从碳氟共价半径:84点至57点的差异只有50%,而一个列,碘氟大小从139 - 57点,144%的差异(壳数量变化)。
还有其他的直觉你可能会提供为什么电负性失败列大小参数吗?
对不起,长度……谢谢你的美妙的网站。
问候,
乔治
先生谢谢您上面的解释。
但不要我们比较键的强度基于轨道的重叠程度。我的书的话,债券的相对强度大于s p p重叠造成的重叠,由于更大的程度上p p轨道的重叠。
根据这个逻辑我们能说sp2-s重叠将大于sp-s重叠因此导致更高的碳氢键键能在烯烃相比,在炔烃(相信一个p轨道和更大的字符有更好的重叠)。
你能请明确这种混淆…
我用,”键离解能量“互换与“债券的优势”。比较键离解能导致这样的结论:粘结强度随p轨道性格减少。
你用什么书,比s p p轨道重叠更有利?如果你看碳系列(烷烃烯烃炔)进展是显而易见的。
注意,移植性和n n似乎π键强,但这是一个人工制品从孤对排斥的救济。
你好,只要提到,应该提到sp = 50%, sp提到和sp ^ 3 ^ 2 = 33.3% = 25%提到吗?你说sp最大s性格所以提到的其他杂交过程应该更低。
固定的错误。谢谢! ! ! !
很好的帖子,詹姆斯,很像往常一样。花了几年我的生活把EWG的(如F、硼烷和恶)在终端乙炔使它们更活泼。一半的时间,产品将聚合或做其他的事情我还没来得及snap-freeze liq.氮。
从一个方面说明,你错过了注2。所以,我不得不注意你的注2,事实上,注1。双关语,)
谢谢你——注1删除,因为我设法掩盖它的文本。