二烯烃和MO理论
Electrocyclic开环和闭包(2)——六个或八个π电子
最后更新:2022年10月27日|
Electrocyclic环打开和关闭(2)- 6(8)π电子系统。
在上一期,我们引入electrocyclic环打开和关闭,与共轭系统的两个π键(4π电子)。(看到帖子:Electrocyclic反应]。我们发现系统4π电子经历”顺旋热条件下“闭环(开放),和“对旋“闭环光化学条件下(开放)。(我们将在下面的文章中介绍这些术语]
如果我们向系统添加一个额外的π键,给我们6π电子?如何改变?
如果您想跳过正确的答案,这里有一个简短的摘要。
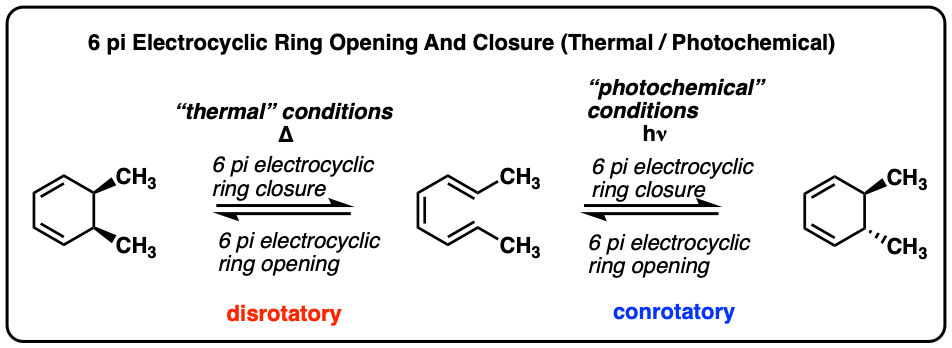
Electrocyclic ring-closing和6π的开环系统发生在完全相反的意义上的4π体系。
你可能会问,这是为什么呢?好问题!在下面的文章中,我们将通过这个主题从一开始。bdapp平台
表的内容
- 6π热Electrocyclic环打开和关闭
- 的“引擎盖下”的6-πElectrocyclic环关闭:确定最高占据分子轨道(人类)
- 对旋和顺旋环闭包:“轨道对称性”的重要性
- Electrocyclic环打开呢?
- Electrocyclic反应是立体定向
- Electrocyclic环关闭“光化学”条件下(开放)
- 摘要:6πElectrocyclic环打开和关闭
- (奖金)8π体系呢?
- 笔记
- 测试你自己!
- (高级)引用和进一步阅读
1。6π热Electrocyclic环打开和关闭
所以当我们说,“4π”,“6π”,甚至“nπ”系统,是什么意思?
我们指的是系统的4、6,甚至“n”原子轴承p轨道能够重叠(“共轭”),一组4,6,或“n”π分子轨道就形成了。(参见:结合和共振]。因为每个π键是由两个相邻的p轨道,一个分子与三个共轭π键的结果“π体系”包含6π分子轨道。
让我们从最简单的开始6π示例,可以接受electrocyclic环关闭:(Z) - hexatri-1 3 5-ene。当这三烯加热,形成一个新物种,看起来像这样:
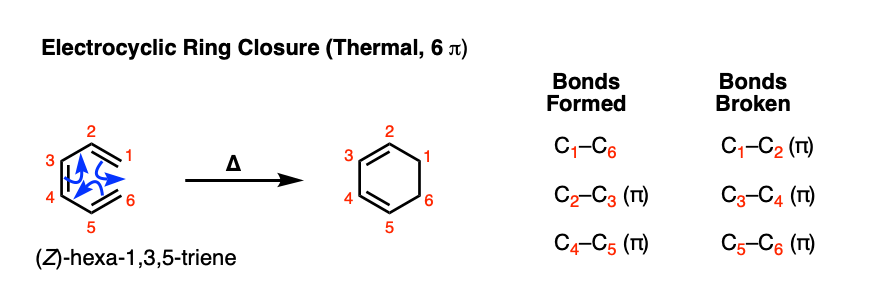
【注:这不会为E异构体工作。为什么不呢?(见注1)
注意形式和打破这里的债券。我们打破3碳碳π键形成两个碳碳π键和一个σ键。
的反向electrocyclic环是electrocyclic开环。加热1,3-cyclohexadiene将导致至少有一些(Z) -hexa-1 3 5-triene:
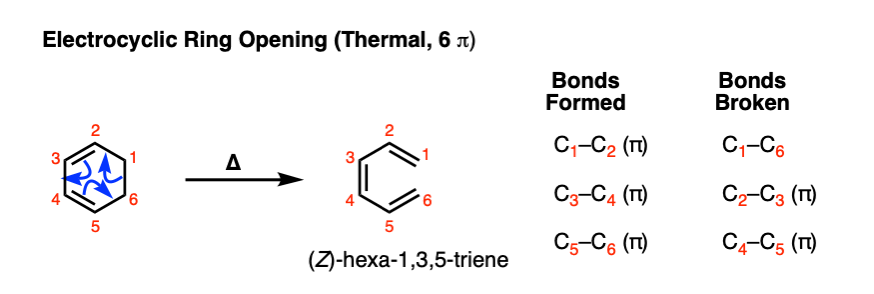
注意,债券形式和打破这是确切的相反比正向反应。
electrocyclic开环和闭环以一致的方式进行(没有中间)和通过一个共同的过渡状态。这些反应属于一个类的共同反应循环状态称为过渡pericyclic反应,包括Diels-Alder,应对和克莱森重组,和许多其他人。
因为反应是可逆的,通过相同的过渡状态,我们也可以把它作为一个平衡。
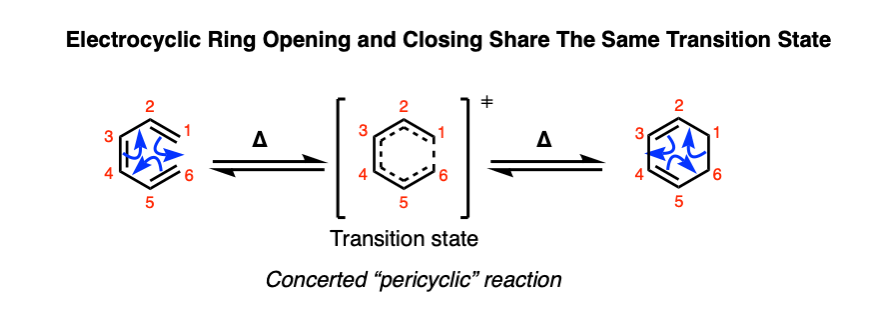
注2这里显示的平衡。
2。的“引擎盖下”的6-πElectrocyclic环关闭:确定最高占据分子轨道(人类)
如果你看看债券形成/债券破表,你会发现有一个净破坏一个π键和净形成一个sigma键。
是什么实际上当hexatriene被转换为1,3环己二烯?
嗯,新形成σ键重叠的两个p轨道的结束hexatrieneπ体系(碳1和6)旋转,从sp和这些碳原子的杂化的变化2对sp3。(我们会在第二个)。
π分子轨道参与这种转变将会是最的一个电子与原子核或者换句话说,这些的最高能量。
高能电子在这种情况下是什么?的电子高能分子轨道(人类)。
那么我们如何知道人类的样子吗?很高兴你发问。
我们介绍了如何建立π分子轨道在这个先前的帖子。(看到的:丁二烯的π分子轨道]
π分子轨道1、3、5 hexatriene看起来像这样:
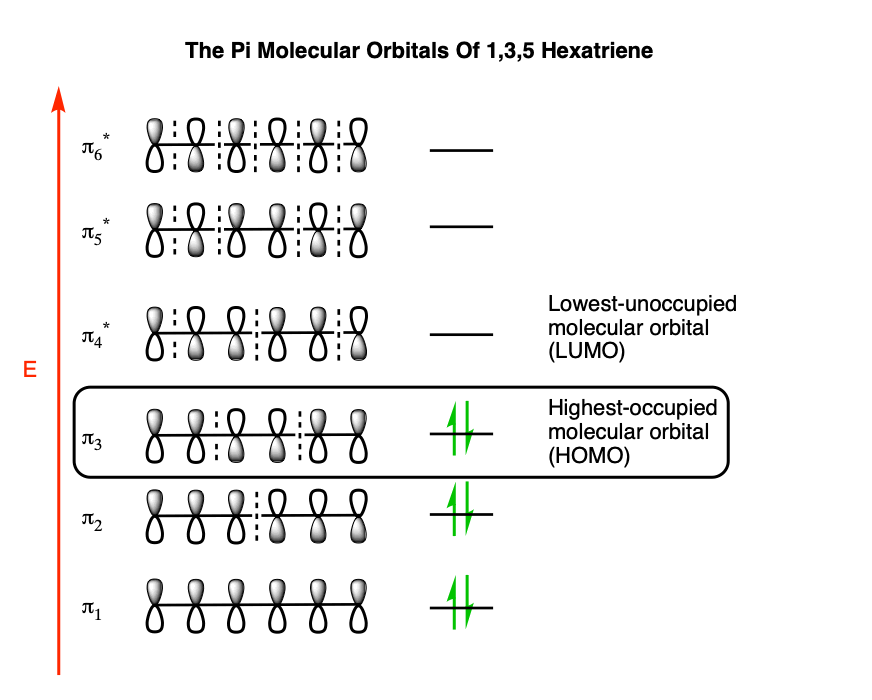
这是一个很多吸收!值得庆幸的是,出于我们的目的,我们不需要使用所有的分子轨道1、3、5 hexatriene在这个实例中。
我们真正关心的是高能电子(大部分与原子核);的电子最高占据分子轨道(人类)。在hexatrieneπ3,我们画出下图:
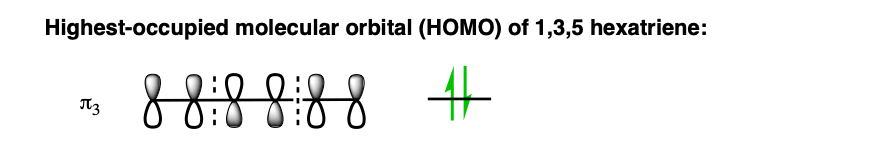
我们可以进一步简化。为了形成新的σ键,我们只会关心C1和C6的轨道,因为这些轨道参与形成新的sigma键。

现在我们可以在映射到1、3、5 hexatriene构象的反应就会发生。

现在怎么办呢?
3所示。对旋和顺旋环闭包:“轨道对称性”的重要性
为了让新σ键形式,C1和C6必须这样,旋转建设性的重叠轨道。他们必须有相同的阶段。
6π系统1,3,5 hexatriene,轨道上的每一个目的地(C1和C6)每个阶段的对齐相同方向(任意的“阴影”叶指向上,但是它会工作一样,如果他们都画阴影叶向下)。(如果你喜欢,你可以称之为“对称”取向;“轨道对称性”一词通常是指这些叶的相对取向。)
形成σ键可以实现如果一个碳旋转顺时针方向和其他逆时针方向的。这是被称为对旋债券形成的模式。
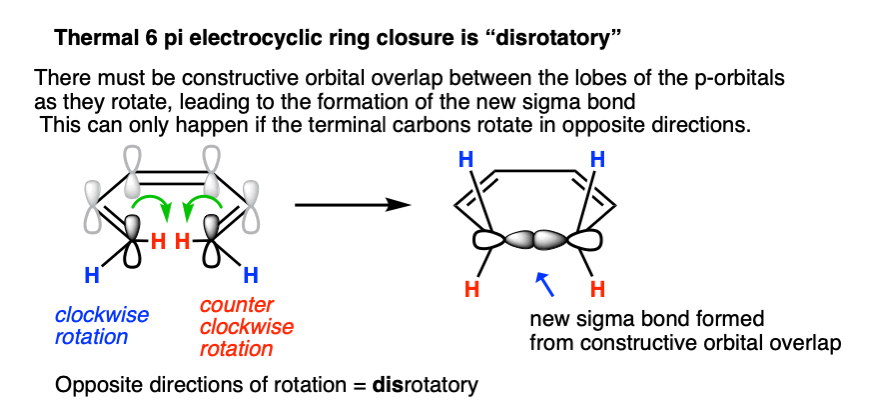
如果他们在同一方向转动呢?由于叶是相反的阶段,这导致具有破坏性的轨道重叠和不能形成一个σ键。这种债券的旋转模式,”顺旋”。
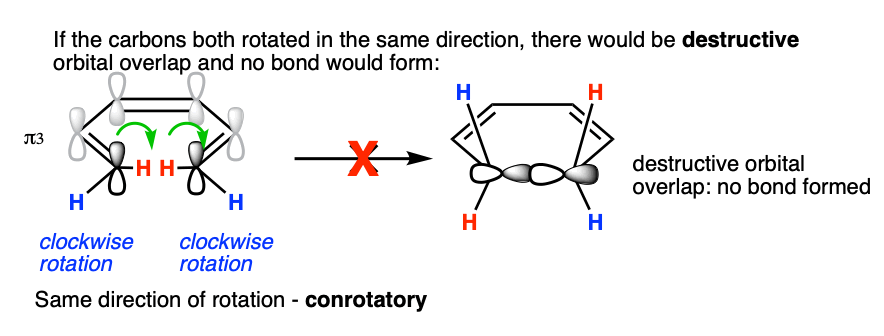
我们看到在前面的帖子,4π热环关闭和打开顺旋的方式发生。如果你看的安排在C1和C4的HOMO轨道1,三,你可以看到,他们有一个相反的安排与C1和C6的HOMO 1, 3, 5-hexatriene (“反对称”,如果你想使用一个更具体的词)。
所以,总而言之,增加两个p轨道π体系变化的模式热electrocyclic ring-closing反对旋转(4π)说旋转(6π)。
4所示。Electrocyclic环打开呢?
想象电影制作electrocyclic环关闭基于我们刚才看到的。
现在想象一下,在反向运行那部电影。
我刚刚所说的反向electrocyclic闭包——是electrocyclic开环。
Electrocyclic开环和Electrocyclic环关闭共享相同的过渡态,所以一切适用于electrocyclic环闭合前进方向的应用同样对electrocyclic开环(反方向)。
Electrocyclic 6π系统开环热条件下必须发生在这样一种方式,σ键断裂,再生的HOMO(π3)1、3、5 hexatriene。所以它必须对旋。
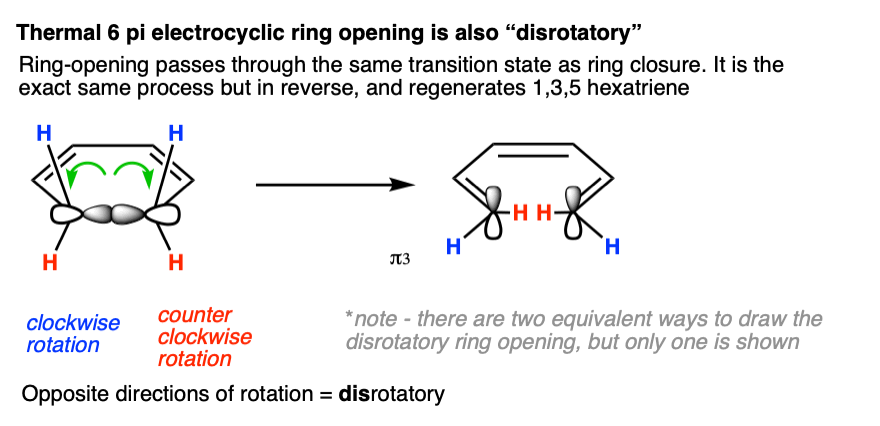
注意4在这个图的蓝色氢所示旋转“向外”。它会工作如果蓝色氢旋转“向内”吗?是的,因为这仍然是“对旋”。对于每个对旋和顺旋模式,通常有两种可能性(内/外)。在本文中,为了简单起见,我们只会显示一个。
5。Electrocyclic反应是立体定向
到目前为止,我们已经讨论了“顺旋”和“对旋”,但没有描述任何情况下立体化学将发挥作用。
我们现在准备看看会发生什么有取代基的结束碳6π系统1,3,5 hexatriene。
这里有两个例子从化学文献[在这里看到的]。试图证实自己,这些环闭包是真的对旋。
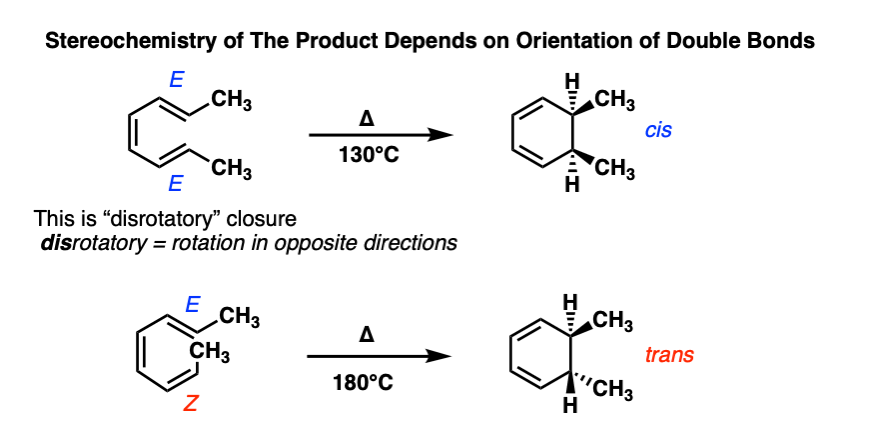
看到翻转对一个双键的几何E Z导致抛产品的几何?
Electrocyclic反应的另一个例子立体定向的反应。从IUPAC:反应称为立体定向如果起始原料的不同只有在它们的配置转换成立体异构的产品。这是真的,因为起始原料和产品都是立体异构体(非对映体)。
Electrocyclic开环也发生在对旋模式:
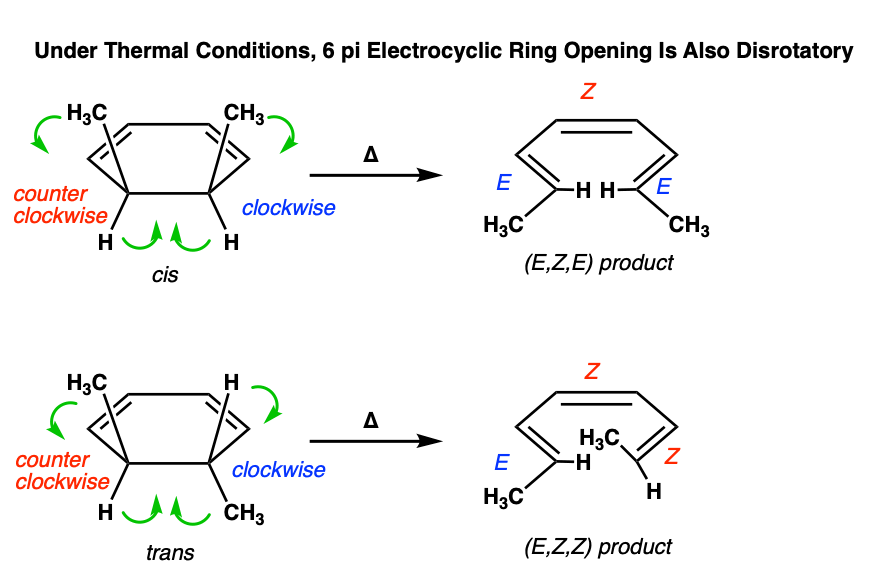
计算出旋转(对旋或顺旋)的模式可以花一些时间和实践。有助于想象看着面前的分子,和跟踪每一个取代基的路径从原料到产品。一些练习测验包括底部的职位,这样你就可以获得更多的经验与这些类型的问题。
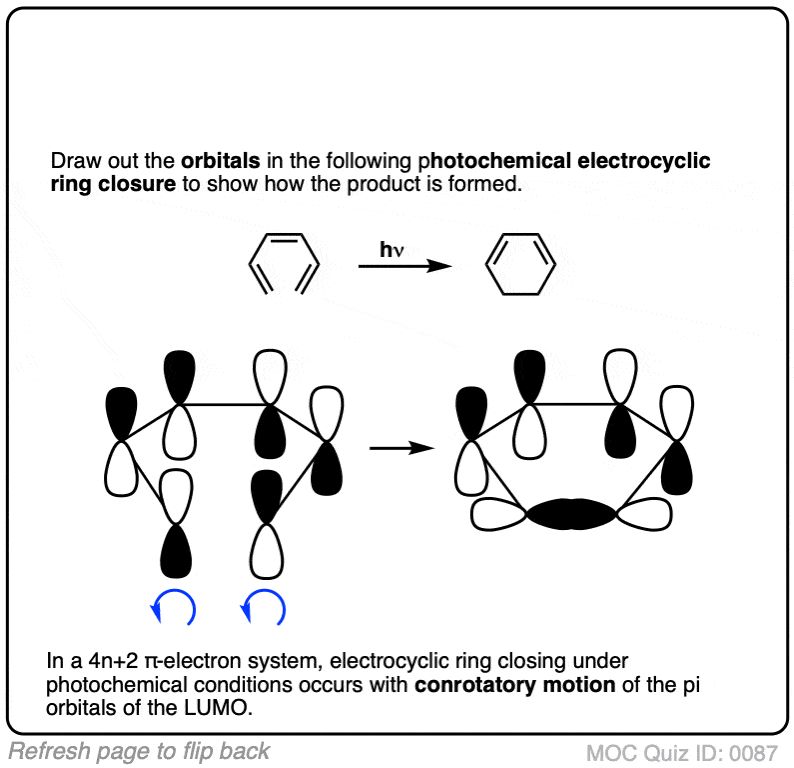
6。Electrocyclic环关闭“光化学”条件下(开放)
当我们看到4π体系,还可以诱导electrocyclic环打开和关闭通过紫外线的影响(hν)。
然而,旋转的方式不同的。6π体系,我们看到(上图),加热系统导致对旋环关闭。
下光化学条件下,环模式发生在关闭相反方向。
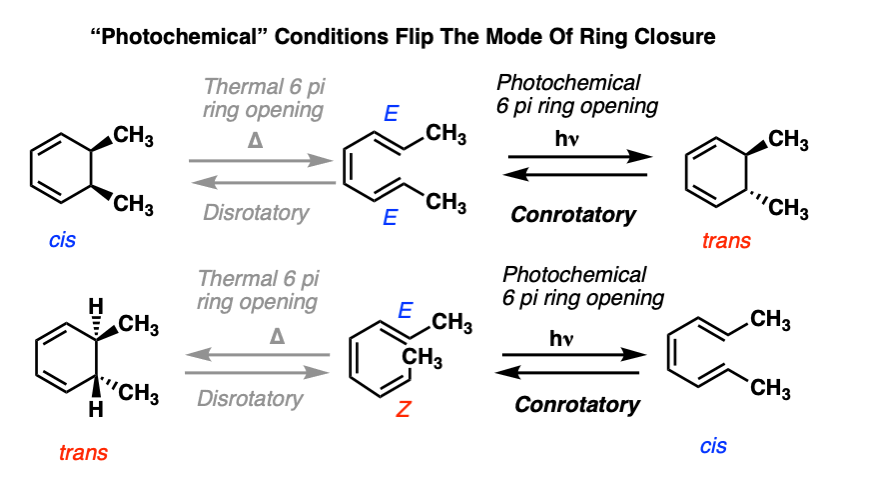
这些反应的例子反对旋转环关闭,每个碳末端旋转方向相同。
为什么紫外线影响这些反应?
回想一下,在我们的文章紫外可见光谱(参见:介绍了紫外可见光谱),我们看到紫外和可见的光可以促进π电子系统的最高占据分子轨道(HOMO)最低未占据分子轨道(LUMO)。
hexatriene实际上,这将是一个从pi3 (HOMO)过渡到pi4 (LUMO)有效地成为“新”人类。
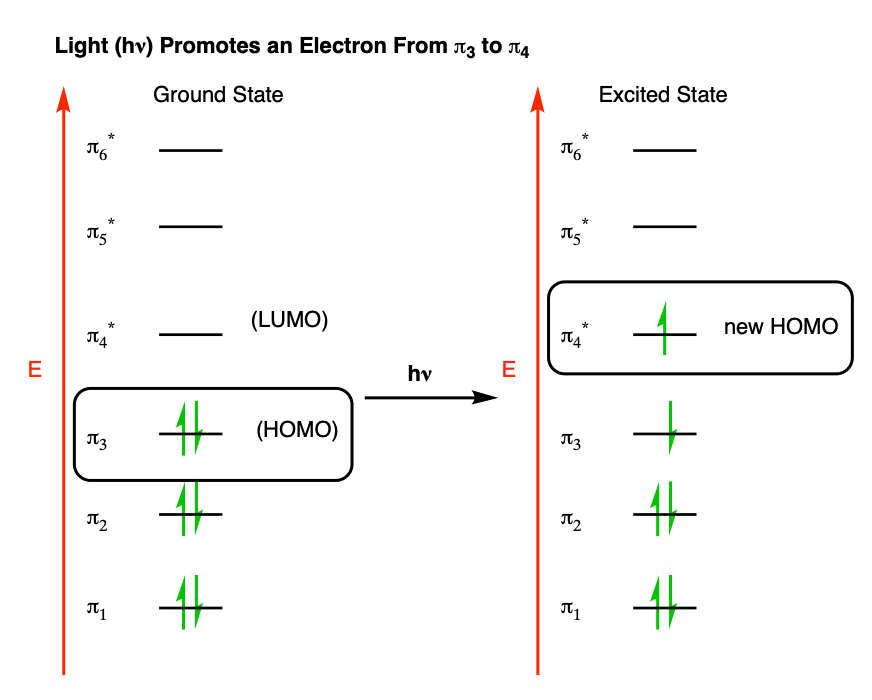
这意味着,如果我们看一个electrocyclic反应在这些条件下,我们需要做分析基于π4代替π3。
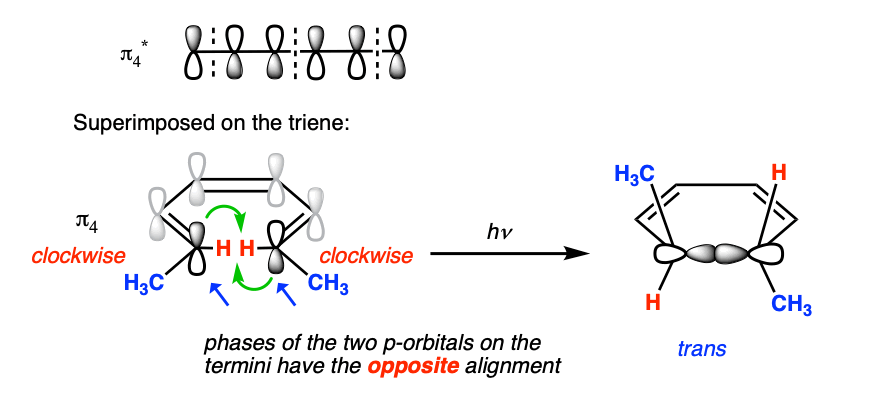
的轨道对称性π4是不同的。我们覆盖π4 1,3,5-hexatriene。然后我们回到了轨道上的目的地反对称的——就像在热4π的情况下。
因此我们应该期待(!)反对旋转环关闭。
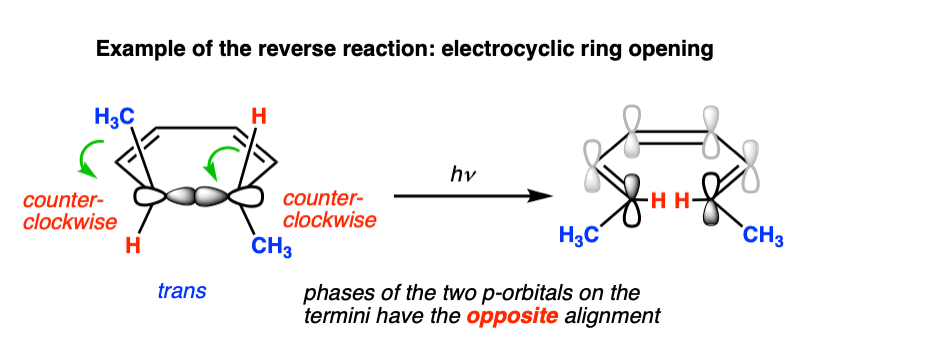
光化学electrocyclic开环6π系统中也观察到,和同样是顺旋。
你可能熟悉这方面的一个例子反应,即使你不知道。
在某种程度上,你的父母可能让你在外面玩你可以让你的维生素D”。
你的父母什么没有告诉你,你需要紫外线(290 - 330 nm)激活6π顺旋electrocyclic 7-dehydrochloresterol转换成前维生素D3开环:
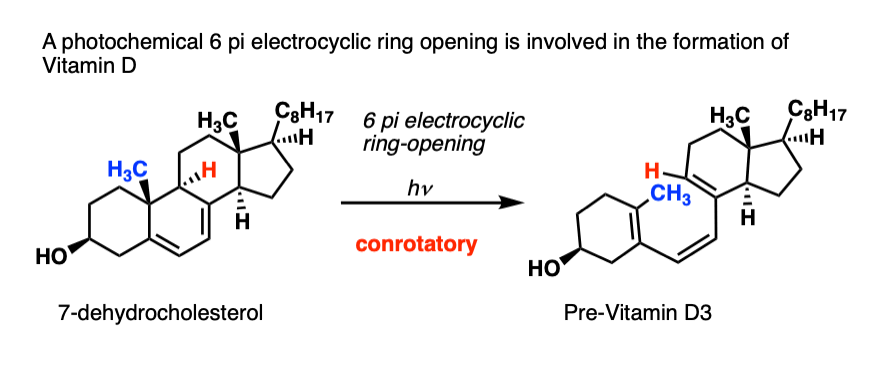
我将这个传递给你,所以你可以告诉你未来的孩子在外面玩时到底发生了什么。
(注3- - - - - -还有第二种pericyclic反应参与维生素D3的形成从“前维生素D3”,但今天我们不打算去那里。]
7所示。摘要:6πElectrocyclic环打开和关闭
这可能是足够的一篇文章。我们可以在一个表中总结的关键模式。

从化学206的教授大卫·埃文斯是一个有用的概念叫做“切换”算法。
自旋转“翻转”的模式从热光化条件,或添加2 p轨道的π体系,你只需要记住这些情况下,你可以获得所有的其他人通过使用“切换”算法。
8。[安可]8π体系呢?
好吧,让我们面对现实吧。你不能得到足够的轨道对称性的信息。你上瘾,想知道更多。
我明白了。
有更多的吗?地狱哦是的还有更多,但我们会给一个例子。
以来我们经历了4π(热、光化学)和6π(热、光化学)你可能有一个紧迫的问题:8π体系呢?
好消息。如果你知道“切换算法可以求出模式的热情况和光化学情况。
- 因为4π(热)顺旋6π(热)对旋一个开关(8π)将我们带回顺旋。
- 同样,4π(光化学)对旋6π(光化学)顺旋和一个开关(8π)我们回到移动对旋。
Electrocyclic反应也可以发生在序列。例如,这是一个8π热electrocyclic环关闭(顺旋),后跟一个6π热electrocyclic环关闭(对旋)。
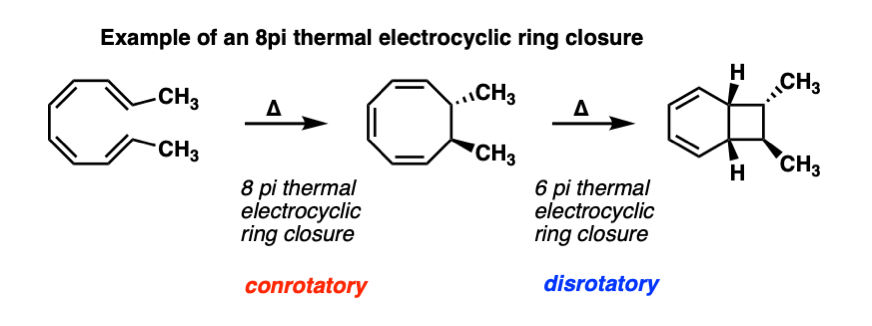
更有趣的是实际上这些反应发生在自然!一个最吸引人的自然产物的合成的合成endiandric酸的实验室k . c . Nicolaou它有一个丰富的盛宴electrocyclic对咀嚼的反应。看到引用。一个非常有益的经典篇章也总合成。
合成也覆盖在汉斯帝国的页面,在这里:Endiandric酸
笔记
注2。我画的平衡箭头为“平等”,但那不应该是为了暗示平衡常数是1。一般来说,关闭环应该喜欢在开环自碳碳σ键(约80千卡每摩尔)比碳碳π键(约60千卡每摩尔)。
注3。“前体形式D3”转化为维生素D3通过antarafacial 1 7氢转移,我们可能会在后面的帖子。这个网站很好地涵盖了话题。
注4。的空间里,我们并没有真正进入这一事实每个模式(“顺旋”和“对旋”)可以发生在两个方向,例如一个顺旋过程,碳原子都可以顺时针旋转或两者都可以逆时针旋转。这里只显示了两个选项之一。在前面的帖子里,我们花了更多的时间讨论这两个可能性。术语“torqueselectivity”是指一个分子的倾向偏爱的一个方向,或使用实际的定义:“倾向于向内或向外旋转的取代基在顺旋或对旋electrocyclic反应”。
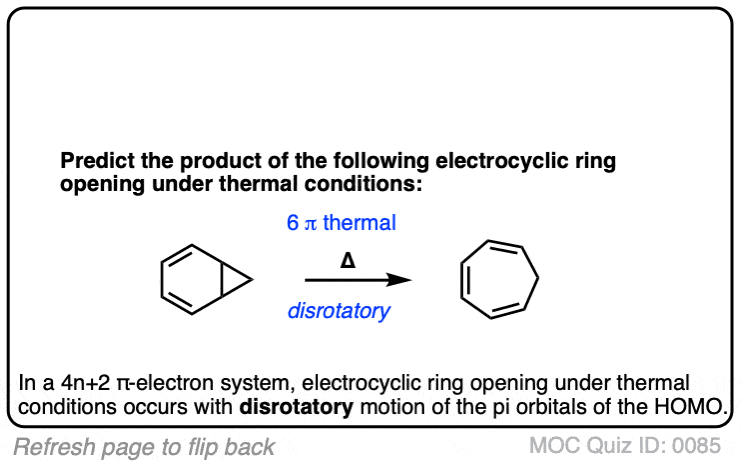
测试你自己!
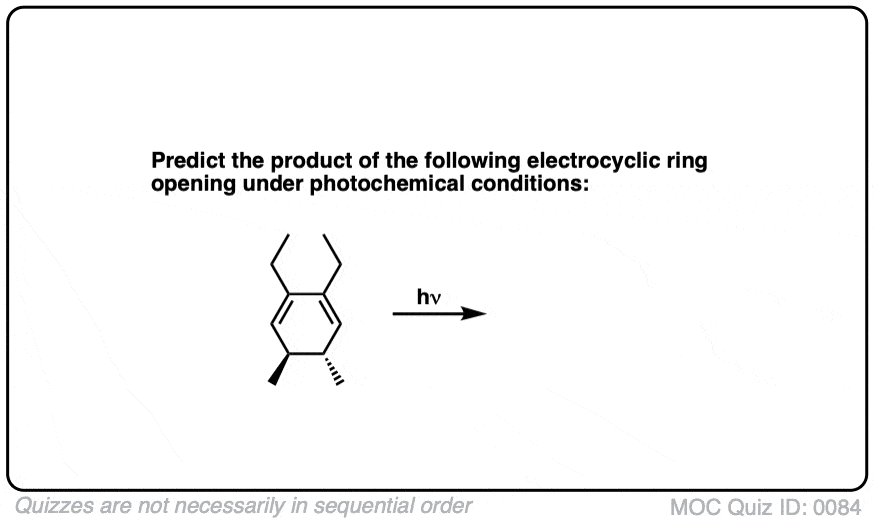 点击翻转
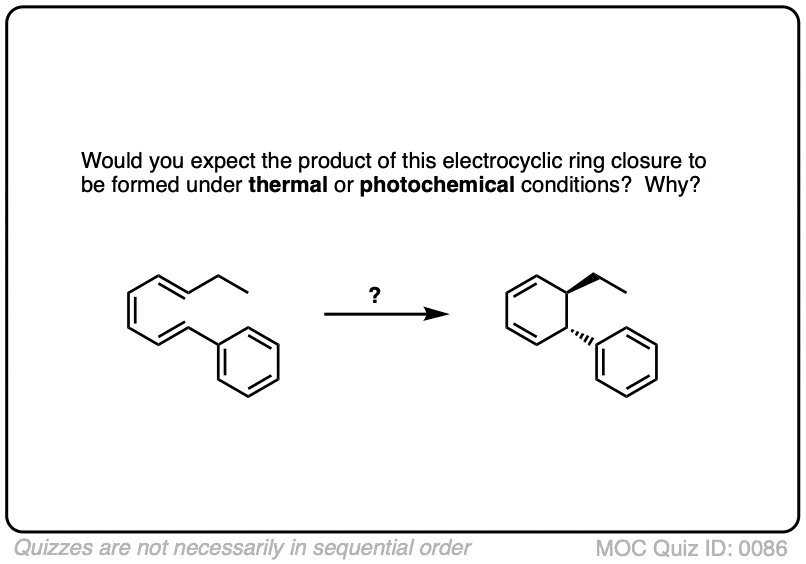
点击翻转
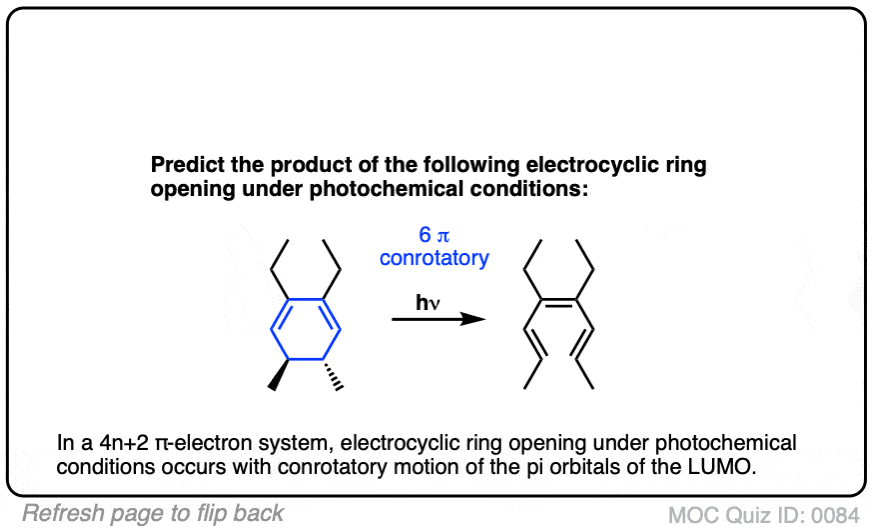
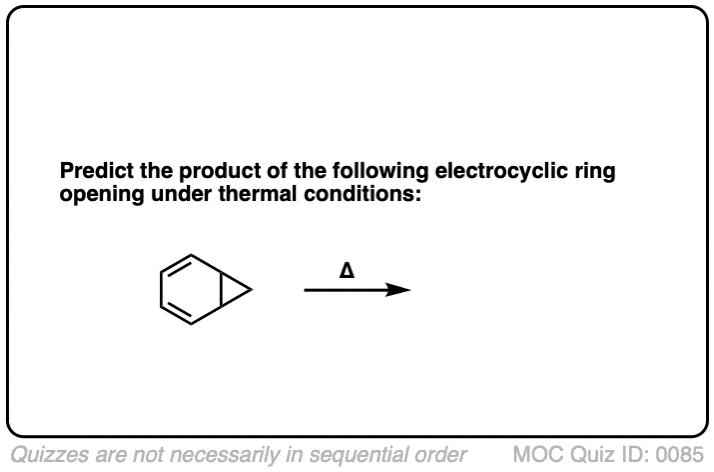 点击翻转
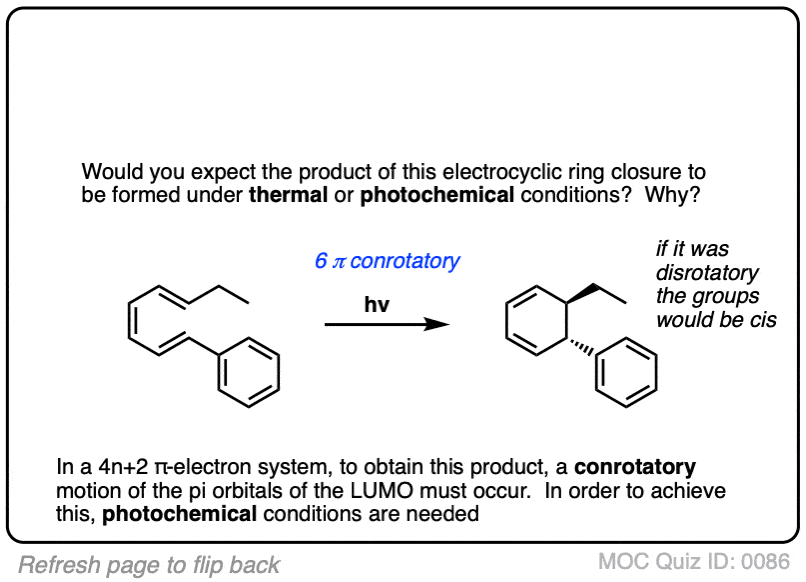
点击翻转
 点击翻转
点击翻转
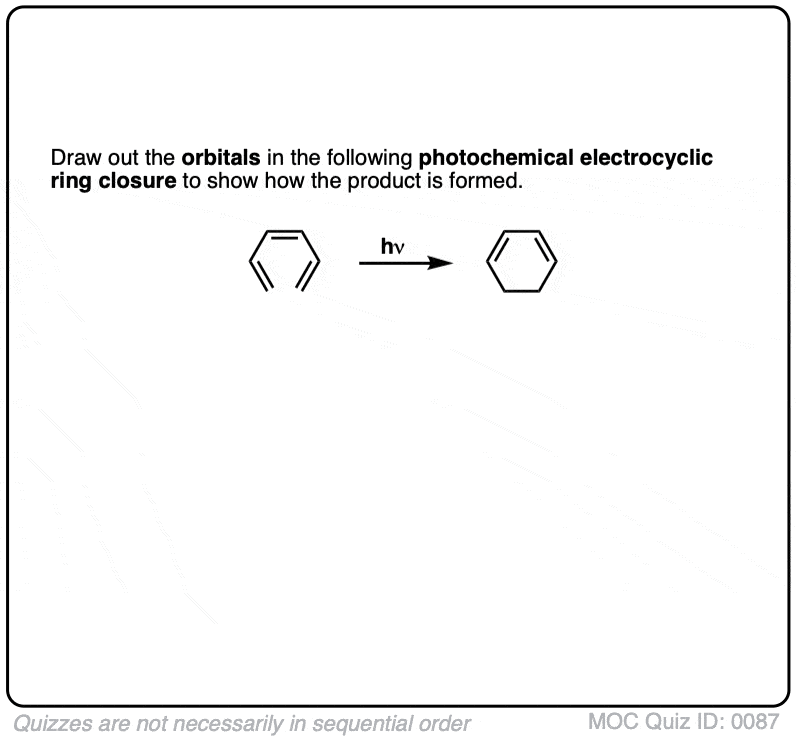 点击翻转
点击翻转
(高级)引用和进一步阅读
这些都是非常常见的一类反应,这些反应的立体化学的预测是成功的一大前沿分子轨道(FMO)理论,获得教授。罗尔德·霍夫曼和Kenichi福井1981年诺贝尔化学奖。r·b·伍德沃德教授无疑也分享了奖(同名“Woodward-Hoffmann”规则)的发展如果他不是当年早些时候去世了。
- 这苏珥是stereospezifitat der conrotatorischen cyclisierung decatetraens
亚历山大•Dahmen Rolf Huisgen
四面体。1969年,10(19),1465 - 1469
DOI:10.1016 / s0040 - 4039 (01) 87915 - 6 - 立体定向顺旋价键异构化octatetraenes cycloocta-1, 3, 5-trienes
罗尔夫Huisgen,亚历山大Dahmen,赫尔穆特•休伯
美国化学学会杂志》上1967年,89年(26),7130 - 7131
DOI:10.1021 / ja01002a060 - Electrocyclic反应1-substituted 1, 3, 5, 7-octatetraenes。一个从头开始的分子轨道torquoselectivity研究l electrocyclizations
伯特·e·托马斯j . d . Evanseck和k·n·胡克
美国化学学会杂志》上1993年,115年(10)4165 - 4169
DOI:10.1021 / ja00063a039 - 热价异构化:立体化学的2,4,6-octatriene, 6-dimethyl-1 3-cyclohexadiene环关闭
艾略特·n·马维尔,杰拉尔德Caple,布鲁斯
四面体。1965年,6(7),385 - 389
DOI:10.1016 / s0040 - 4039 (00) 89964 - 5 - 静脉beitrag苏珥stereochemie der valenzisomerisierung冯trienen麻省理工学院zentraler cis-doppelbindung祖茂堂cyclohexa dienen——1.3
沃格尔,w . Grimme大肠吃晚饭
春节。列托人。1965年,6(7),391 - 395
DOI:10.1016 / s0040 - 4039 (00) 89965 - 7 - 热动力学之间的互变现象cis cis-1 3, 5-octatriene,独联体,独联体,cis-2, 4, 6-octatriene,独联体,独联体,trans-2, 4, 6-octatriene
约翰·e·鲍德温和诉Prakash Reddy
《有机化学》杂志上1988年,53(6),1129 - 1132
DOI:10.1021 / jo00241a001 - 理论的stereoselection顺旋electrocyclic取代环丁烯的反应
尼尔森·g·Rondan和k·n·胡克
美国化学学会杂志》上1985年,107年(7),2099 - 2111
DOI:10.1021 / ja00293a046 - 顺旋electrocyclic异构化和对旋静止点的环丁烯顺丁
雅克Breulet和亨利·f·奇科夫
美国化学学会杂志》上1984年,106年(5),1221 - 1226
DOI:10.1021 / ja00317a009 - endiandric酸级联。Electrocyclizations有机合成。逐步,stereocontrolled总endiandric酸A和B的合成
k . c . Nicolaou: a . Petasis r . e . Zipkin和j . Uenishi
美国化学学会杂志》上1982年,104年(20),5555 - 5557
DOI:10.1021 / ja00384a077 - endiandric酸级联。Electrocyclizations有机合成。2。逐步,stereocontrolled总合成endiandric酸c g
k . c . Nicolaou: a . Petasis j . Uenishi和r . e . Zipkin
美国化学学会杂志》上1982年,104年(20),5557 - 5558
DOI:10.1021 / ja00384a078 - endiandric酸级联。Electrocyclizations有机合成。3所示。“仿生”的方法来endiandric酸g。的合成前体
k . c . Nicolaou r . e . Zipkin, n . a . Petasis
美国化学学会杂志》上1982年,104年(20),5558 - 5560
DOI:10.1021 / ja00384a079 - endiandric酸级联。Electrocyclizations有机合成。4所示。仿生方法endiandric酸g。总合成和热研究
k . c . Nicolaou: a . Petasis和r . e . Zipkin
美国化学学会杂志》上1982年,104年(20),5560 - 5562
DOI:10.1021 / ja00384a080
一系列的4背靠背的论文江淮endiandric酸合成的教授Nicolaou莱斯大学(现在)。研究生Petasis教授,是在所有4论文合著者,他现在是一个南加州大学教授(洛杉矶CA)。Petasis教授是为数不多的(或者只)人有反应(Petasis反应),试剂(Petasis试剂),和重排(Petasis-Ferrier重排)以他的名字命名。 - 生物合成和仿生Electrocyclizations
克里斯托弗·m·德里耶利米·Malerich和德克特劳纳
化学评论2005年,105年(12),4757 - 4778
DOI:10.1021 / cr0406110
这里简要介绍生物合成维生素D。脱氢胆甾醇的开环是一个6 p conroratory electrocyclization。反应将禁止允许热光化学地因为涉及不同的轨道电子一旦兴奋。 - 轨道对称性守恒
罗尔德·霍夫曼和罗伯特·b·伍德沃德
的化学研究1968年,1 (1),17-22
DOI:1021 / ar50001a003
这是一个极重要的论文。轨道对称性守恒允许一个预测electrocyclic反应的立体化学。本文是一个伟大的介绍主题的创造者和介绍有关条款(同侧的,antarafacial synrotatory,顺旋,等等)。霍夫曼教授在1981年获得了诺贝尔化学奖这项工作,并与伍德沃德教授无疑也共享这一年(这是伍德沃德的第二个诺贝尔)如果他没有过早地去世了。
评论
评论部分