SN1 SN2 / E1、E2的决定
确定替换和消除反应发生
最后更新:2023年5月22日|
确定碳替代和消除反应可以发生
- 需要一个替代和消除反应离去基团为了让它们发生。
- 找一个好离去基团在衬底进行替换或消去反应。
- 如果有没有好离去基团,那么不会替换或消去反应。就是这么简单。
- 是什么让一个好离去基团吗?评论(见文章:是什么让一个好的离去基团),但底线是寻找卤素和其他物种薄弱的基础。
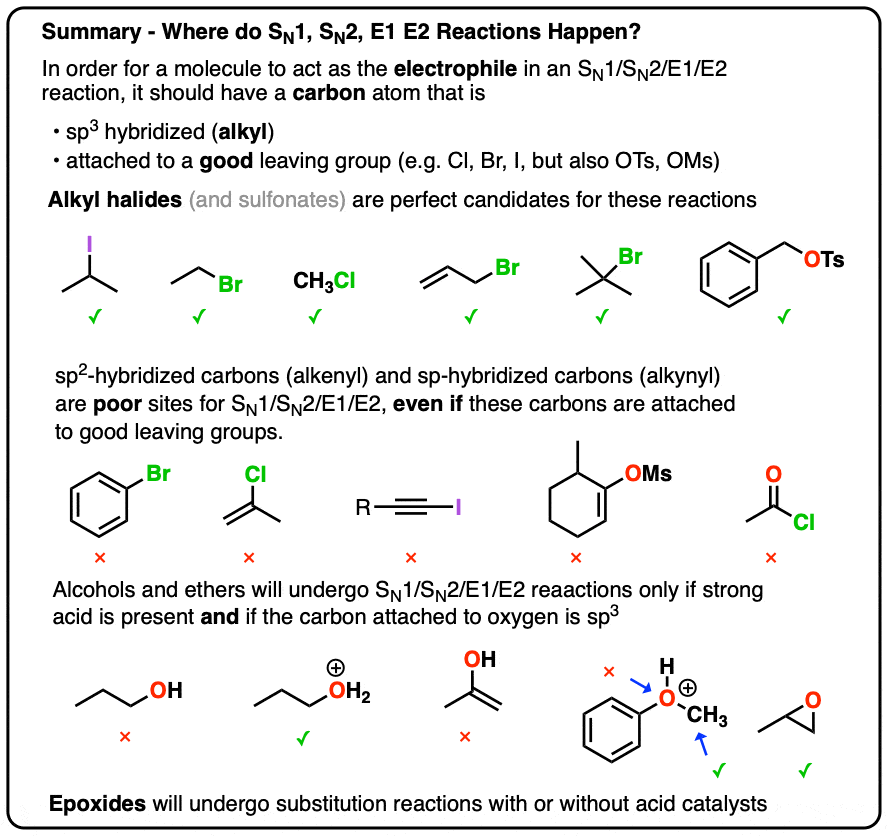
- 羟基(HO)贫穷离开团体,除非酸。
- 此外,SN1/SN2和E1/E2通常只发生在sp3杂化碳原子。
- sp2杂化碳等烯基、芳基炔基卤化物将不接受SN1/SN2/E1/E2
表的内容
1。寻找一个好的离去基团在衬底上
本文假定您熟悉的年代N1,年代N2,E1,E2反应。如果你需要回顾这些反应,请按照以下链接,然后回来。
在亲核替换的反应,底物或亲电试剂(一个电子对受体,例如一个烷基卤)进行攻击的亲核试剂(电子对捐赠)。一个新的碳-亲核试剂债券形式和碳-离去基团债券休息时间从底物。
在消除的反应,基地衬底上的碳氢键,和一个新的碳碳π键形式,打破碳-离去基团衬底的债券。
这两个反应要求失去一个离去基团从底物(即分子接受孤对的亲核试剂或被一个基地deprotonated)。
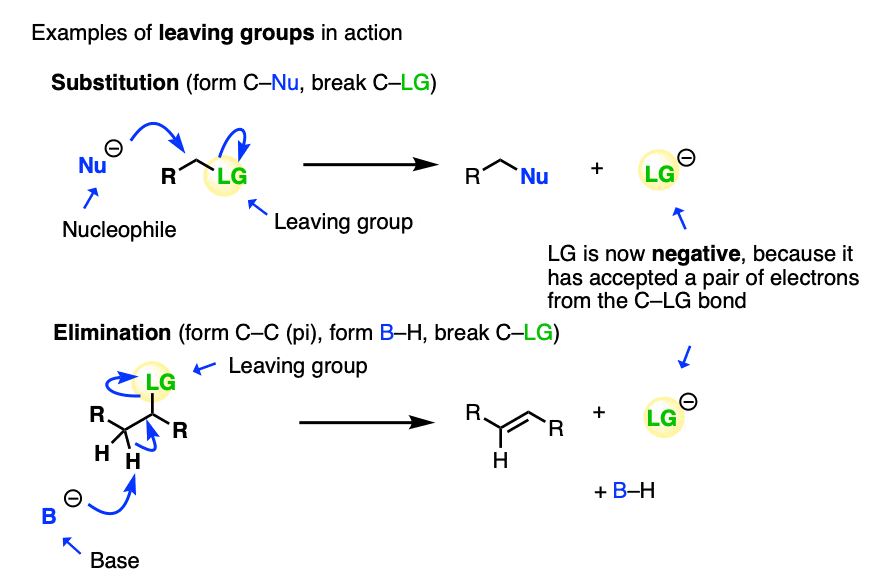
如果没有好离去基团衬底上…然后没有替换消去反应可能发生!就是这么简单。
常见的例子好是物种,可以离开团体薄弱的基础一旦他们接受孤对电子:
- 卤素(氯、溴、我,但不是F氟键很强)
- 磺酸盐(OTs或OMs)
- 酸基组(O c (O) R)
- 带正电的组包含氧[哦2(+),哦(R) (+)], [NR氮3(+)),甚至硫(SR2(+))
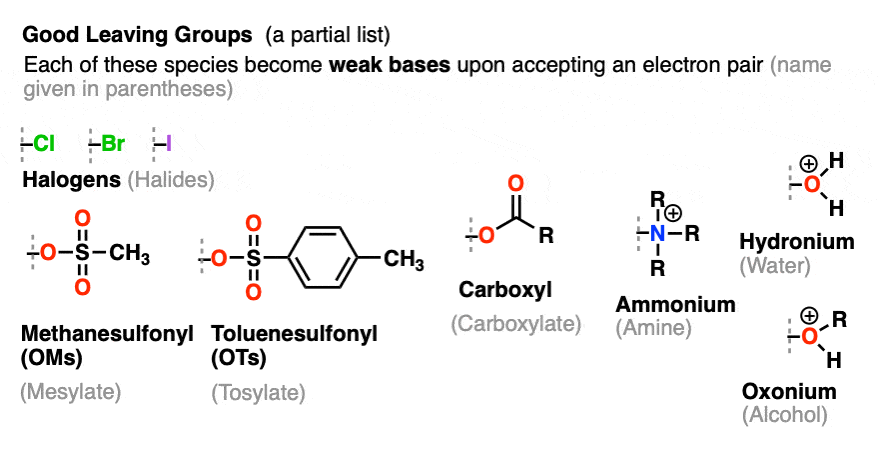
(有一个很好的相关性低的pK一个和离去基团的能力共轭碱。更多信息,见文章:是什么让一个好的离去基团?)
的例子可怜的离开人群包括强大的基地,例如氢氧化(HO)- - - - - -)、烷醇酰胺(NH)2- - - - - -)氢化(H- - - - - -)和负碳离子(R- - - - - -)。氟离子(F- - - - - -)也往往是一个穷人离去基团在替换和消除反应,因为它极其形式强大的债券碳。(注1含氰基的集团(CN)是弱碱但不倾向于充当离去基团在替换或消除反应。(注2]
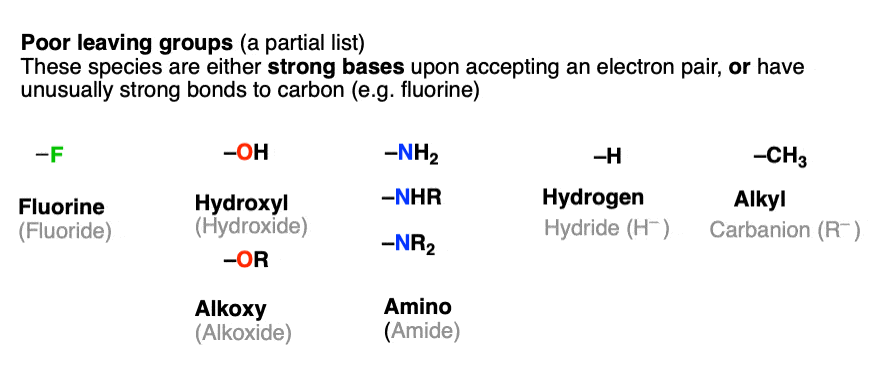
第一个订单的业务在决定任何这些反应的产物确定衬底上的网站(s),那里是一个很好的离去基团。
换句话说,寻找群体薄弱的基础当他们接受孤对电子。
并不是所有的分子都能够替换或消除!
例如,碳氢化合物不作为基板在年代N1 / SN2或消除反应,因为离开团体必须H(-)或极强的基地烷基阴离子(例如CH3(-))。
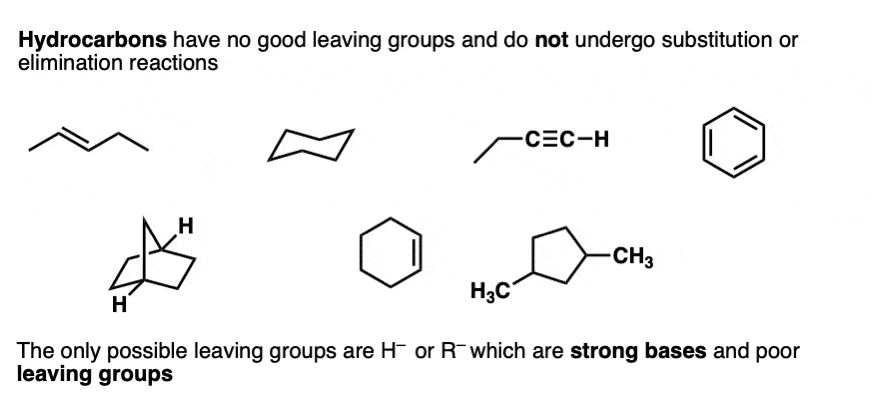
一些碳氢化合物可以作为的亲核试剂在替换和消除反应,但这是不同的衬底。(见文章:乙炔化物炔烃和使用置换反应)
这些练习让你识别网站的挑战一个分子,替换或消除可能发生。
如果你确定离去基团,那么你是识别至少一个的债券,这将打破。你走过了一半的旅程!
 点击翻转
点击翻转
这是另一个例子。
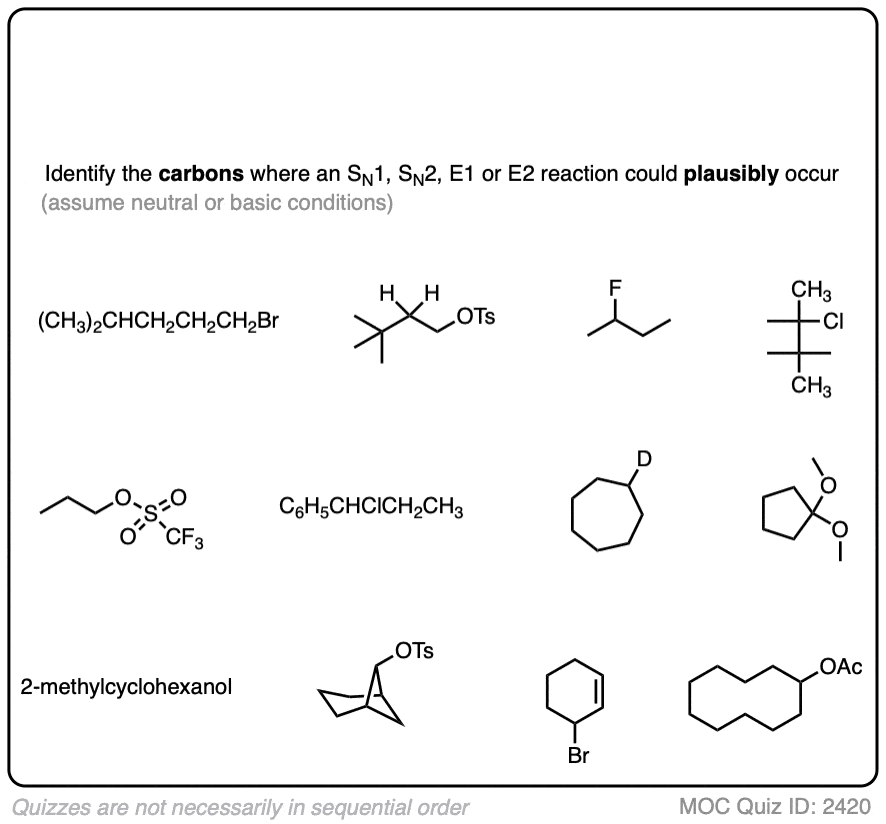 点击翻转
点击翻转
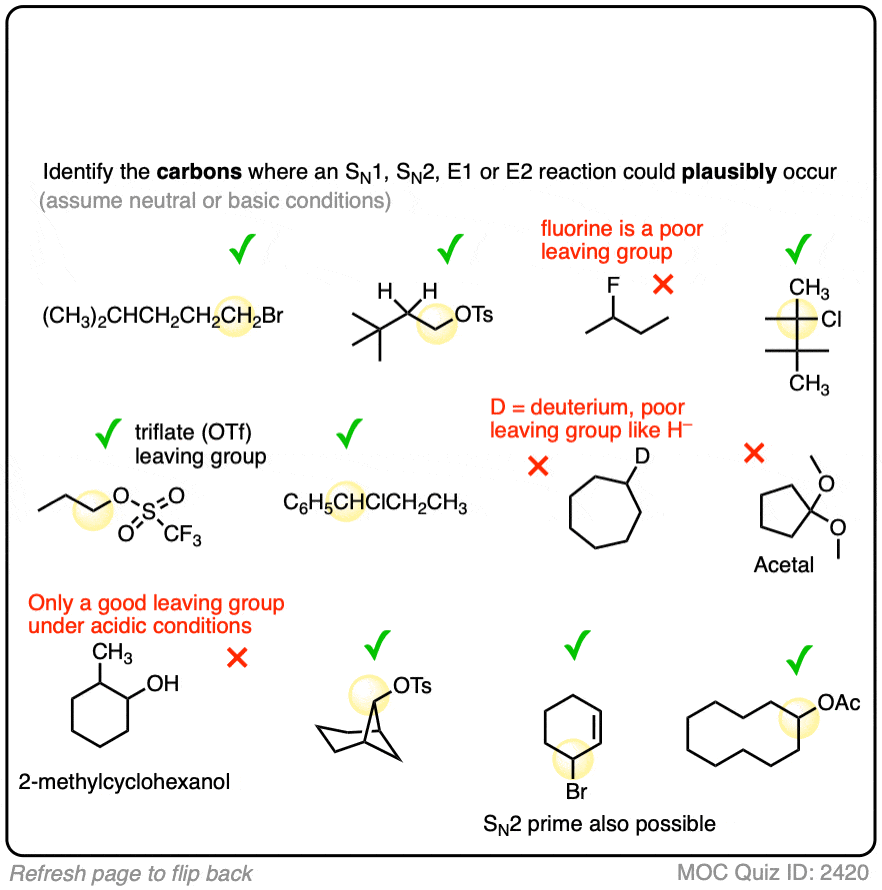
这些测验应该希望推到家,你想寻找卤素,磺酸盐或其他物种薄弱的基础一旦他们离开衬底。
一些群体,贫困离开团体可以制成更好的通过添加离开组织酸。更多关于这在下面。
2。好的离去基团应该附在一个sp3杂化碳
替换和消除反应的过渡态通常涉及的形成部分积极在碳轴承离去基团。
形成碳正离子是最稳定的损失离去基团在一个sp3杂化碳。删除一个离去基团从一个sp2或sp-hybridized碳是非常困难的,因为提到越大意味着电子接近原子核。(见文章:碳正离子的稳定性][注3]
所以确定亲核取代或另一个关键消去反应将会是检查碳附着在好离去基团。
- 如果离去基团连着一个sp吗3杂化碳,那么这是一个好候选人的反应。
- 如果它是连接到一个sp2或sp杂化碳,那么它就是不太可能进行亲核取代或消除。
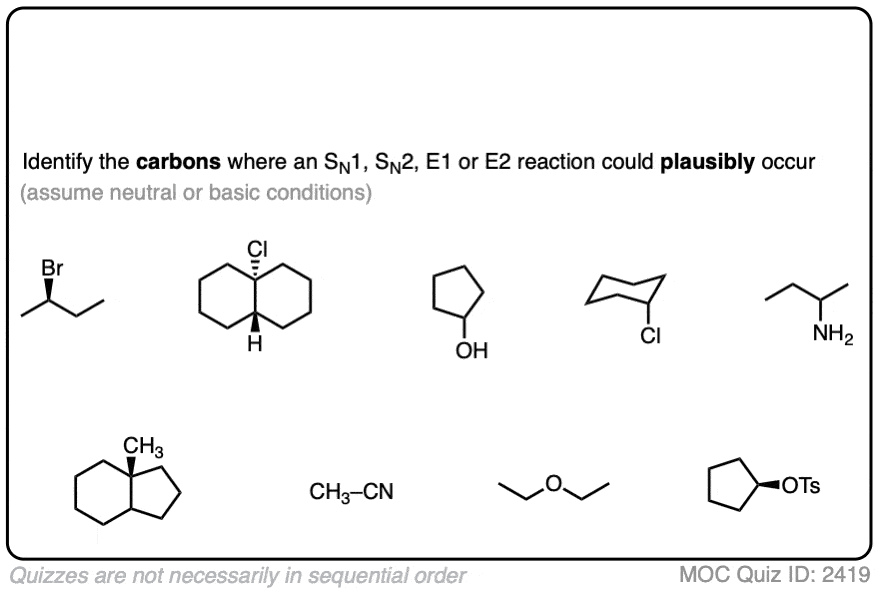
在此练习中,识别能力的碳原子进行替换或消除。
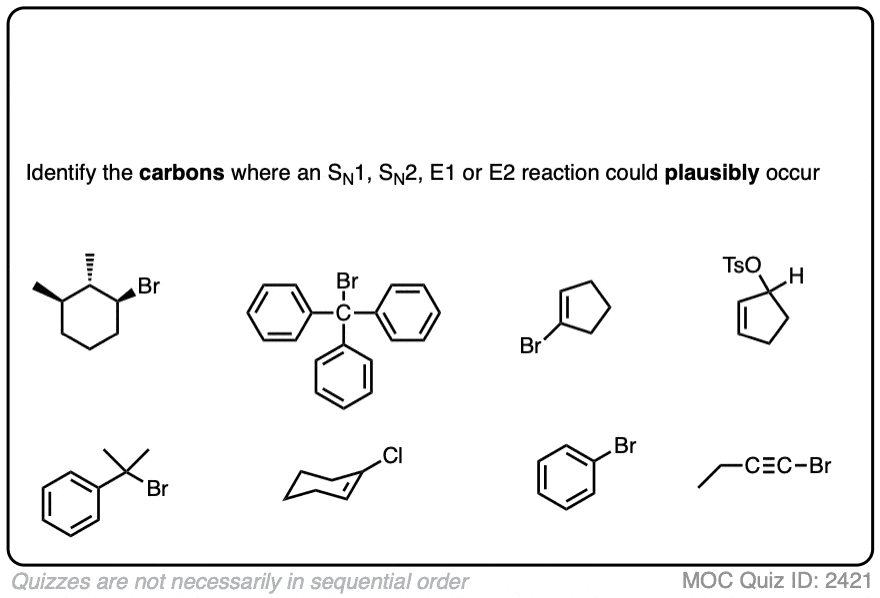 点击翻转
点击翻转
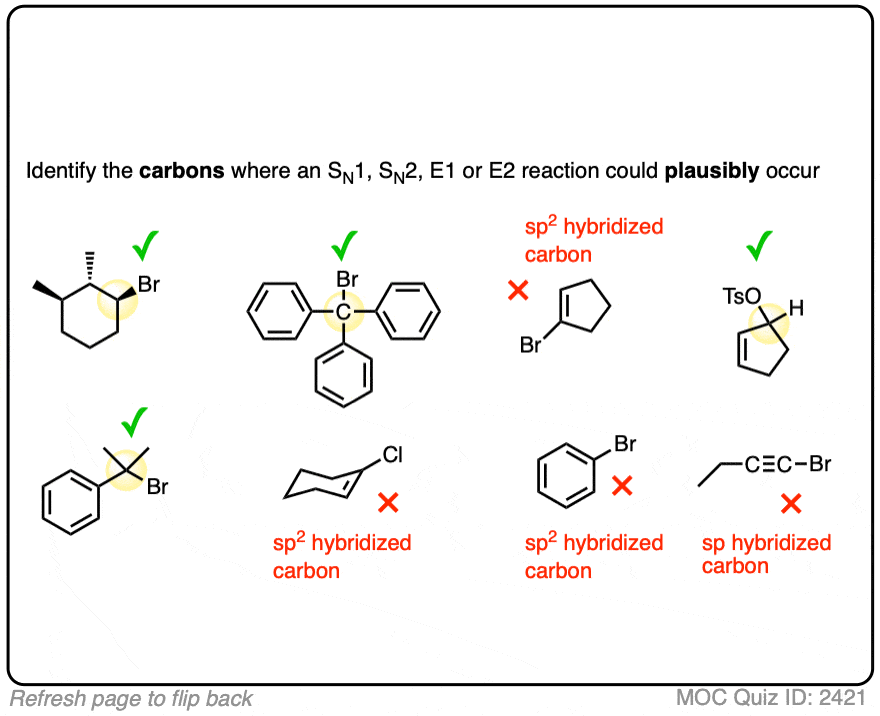
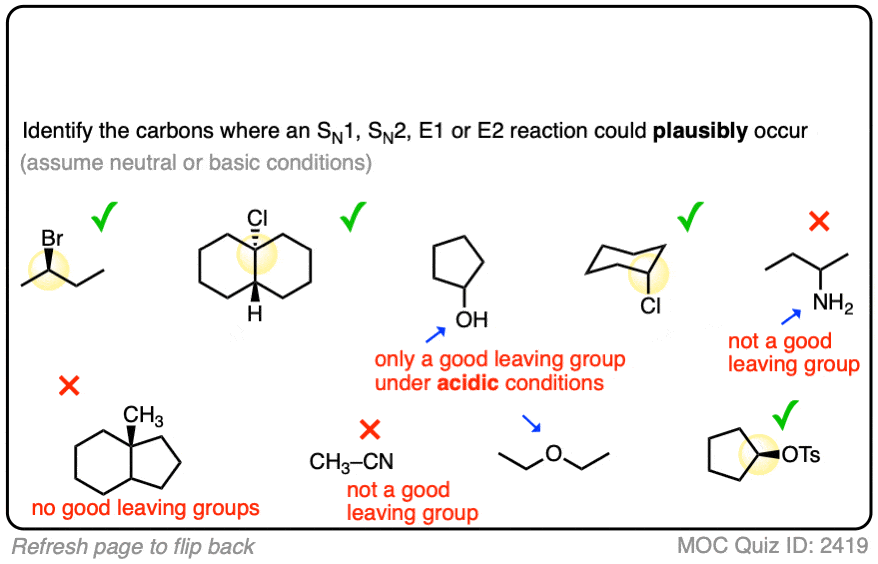
这是另一个例子。
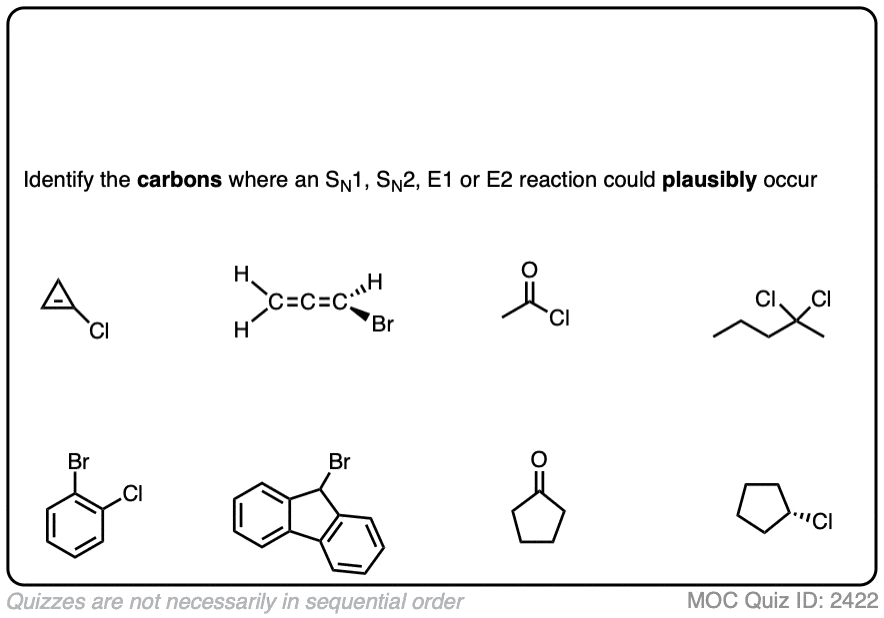 点击翻转
点击翻转
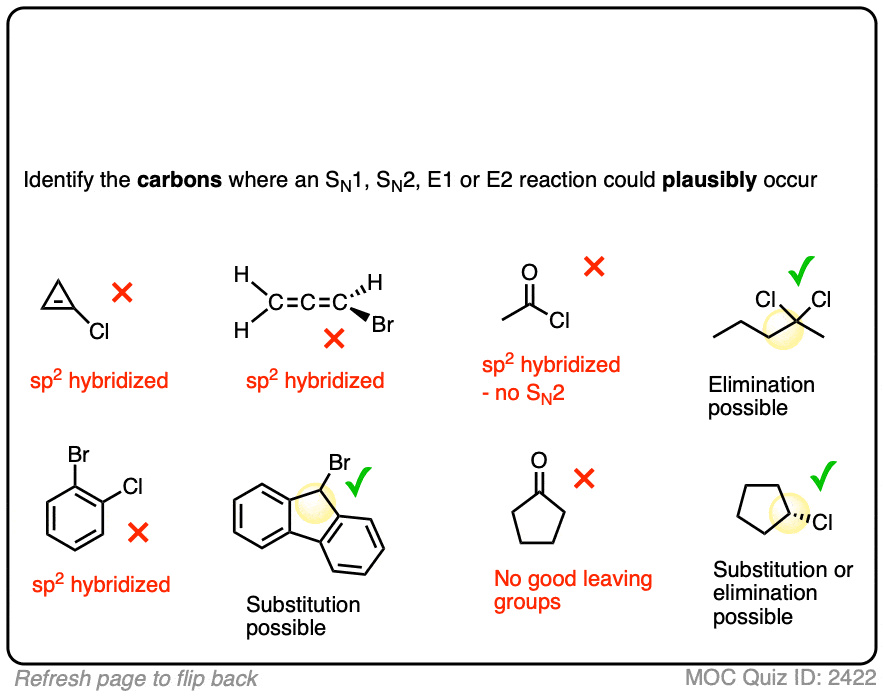
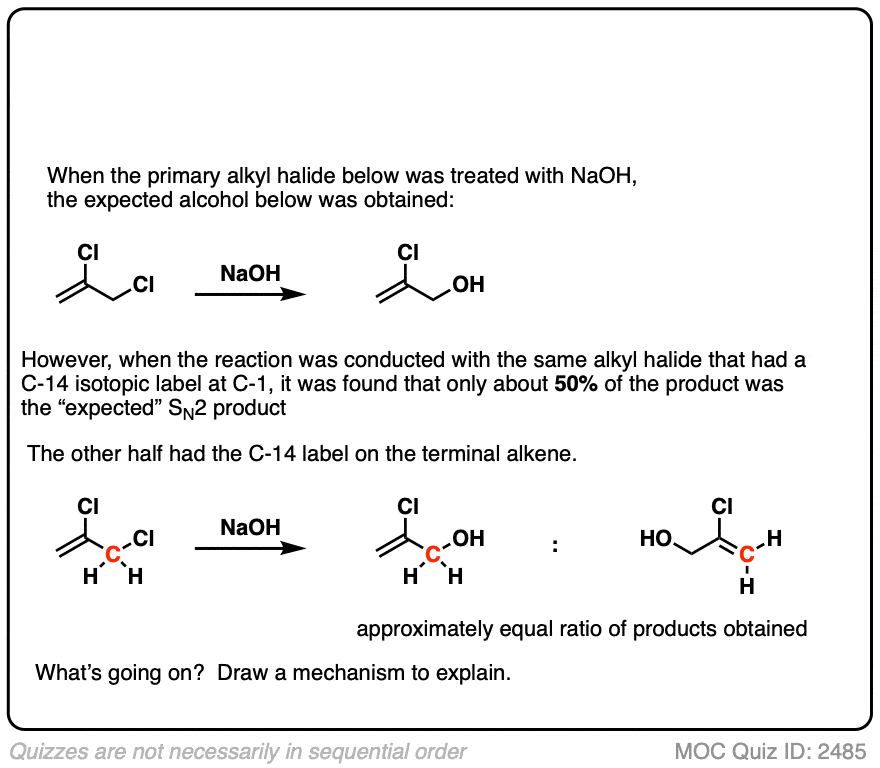
重要的是要知道少数例外。(注意4)消除给炔烃发生在sp2杂化碳使用NaNH极强的基地2。(见文章:通过消除炔烃的反应]。另一个例外,在先进的课程,是一个反应相关N2的年代N2 (N2′)C-LG C-Nu和破损的形成是伴随着碳碳转移的π键。(注5]
3所示。确定碳与离去基团为主,二级或三级
一旦一个可信的网站替换或消除已经发现,下一步是能够分类,碳主,二次或三级。
为什么这个很重要?因为它将极大地帮助决定是否通过收益的反应SN1,SN2,E1或E2途径。
我有更多要说在随后的文章(见文章:SN1 SN2 / E1 / E2 -底物)
 点击翻转
点击翻转
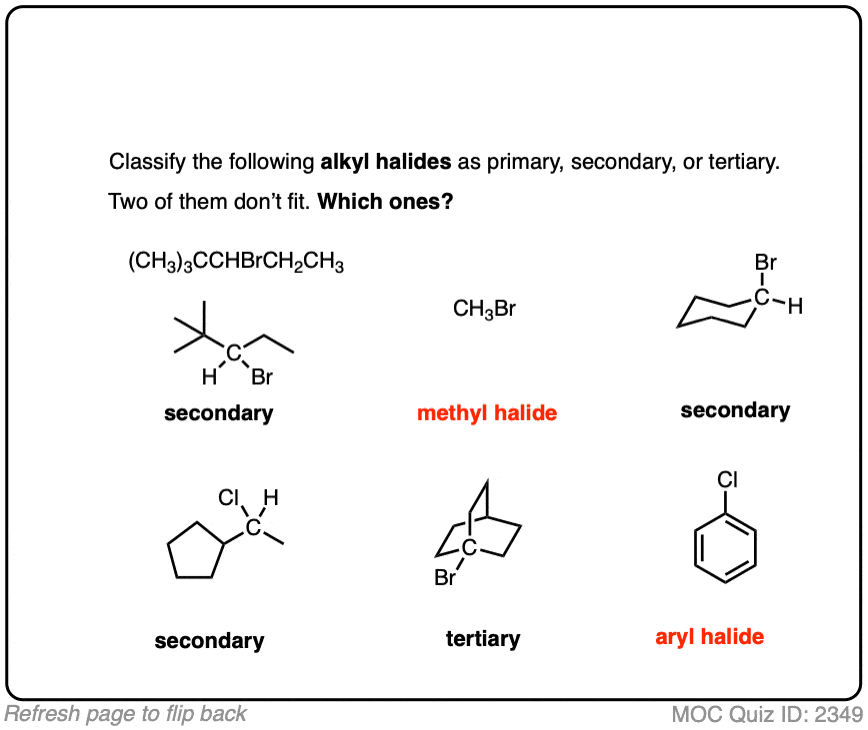
这是另一个测试:
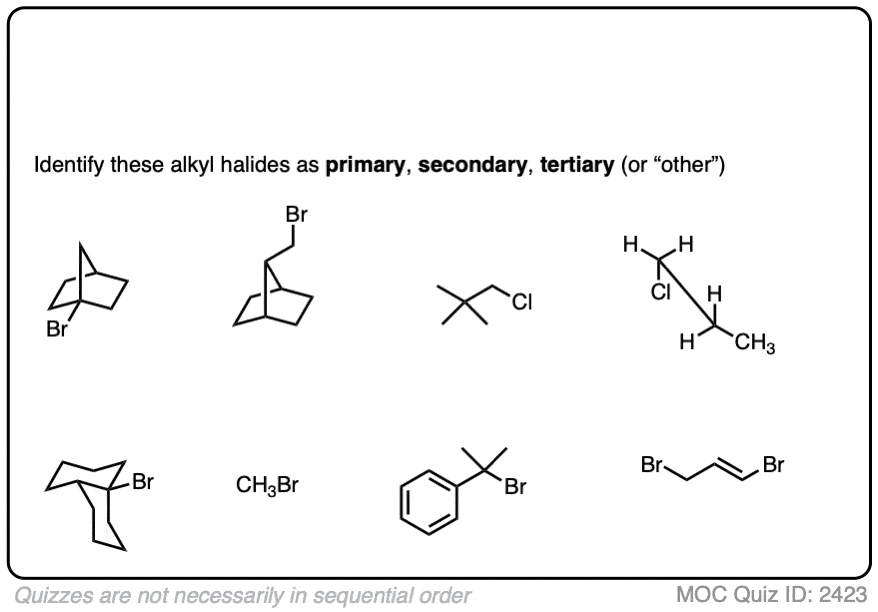 点击翻转
点击翻转
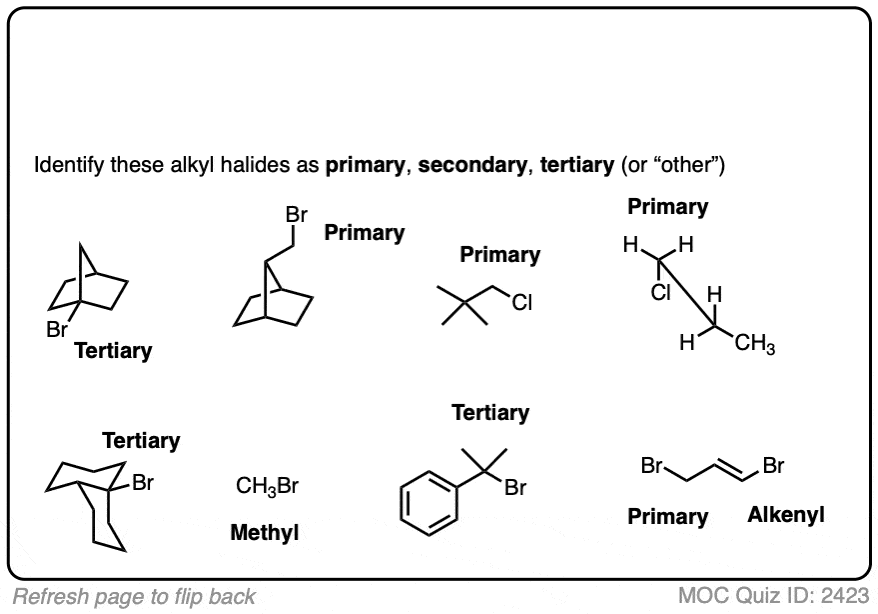
4所示。醇类和醚类可以参与替换和消除反应是否存在酸
如果你做到这一步,没有覆盖醇或环氧化合物,那么你可能是准备继续下一篇文章。
如果你是覆盖替换和消除反应的醇类和醚类,然而,你需要知道另一个重要的转折。
羟基(OH)贫穷离开组织替代和消除反应。除非强酸存在,在这种情况下,他们可以给他们的共轭酸质子化了的。(见文章:更好的离去基团的共轭酸)
你怎么知道的酒精或醚可能是质子化了的吗?寻找强酸如盐酸、哈佛商业评论,嗨,H2所以4或TsOH。
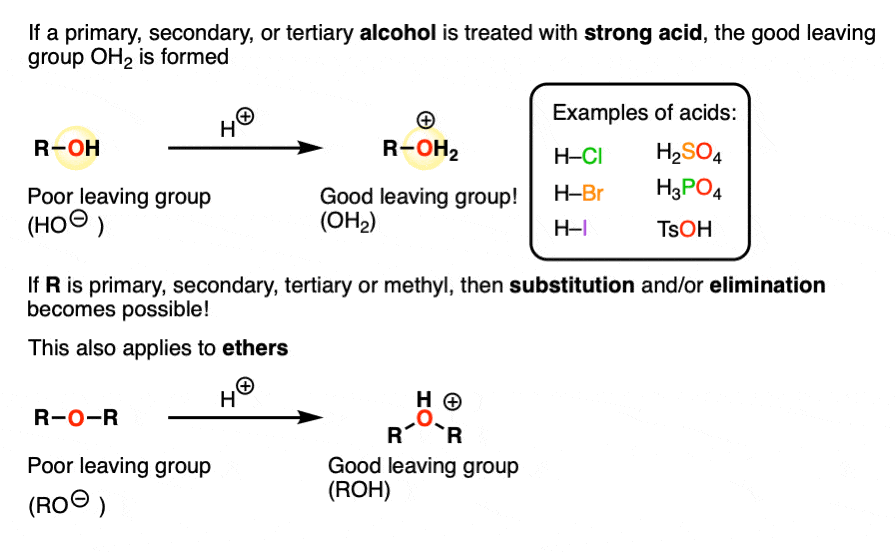
替换的限制和消除反应只发生在sp3杂化碳年代直到适用然而,。
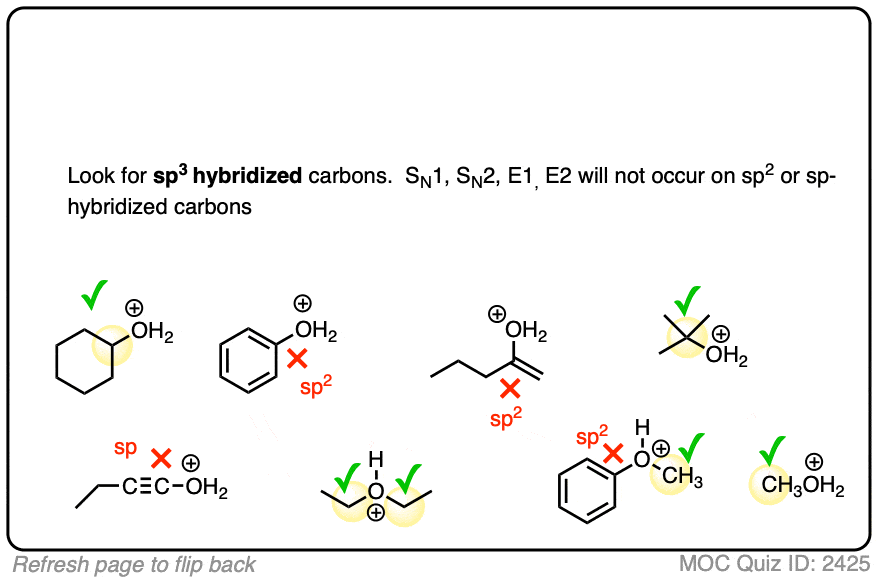
看看你是否能确定碳在每种情况下可以进行替换或消除反应。
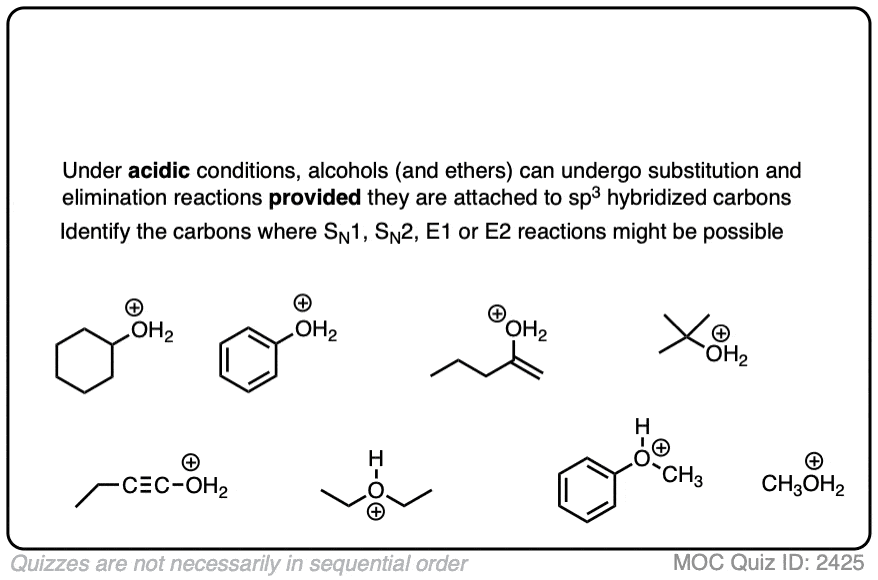 点击翻转
点击翻转
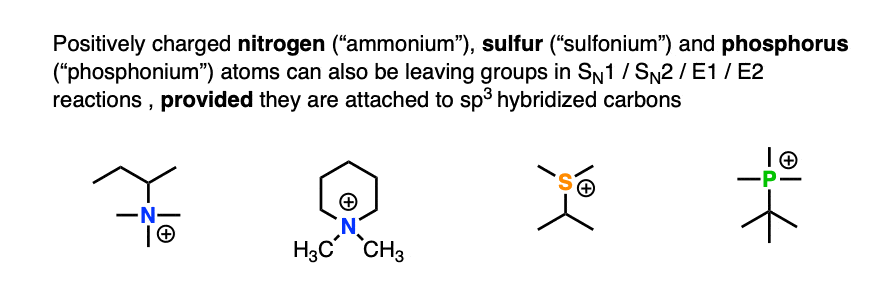
边注,甚至带正电荷硫、氮和磷也可以好离开组织。的离去基团在这种情况下是中性的胺(NR3硫化物(SR)2)或膦类化合物(公关3)。
5。情况下两个离开组
在一些情况下,您将看到多个好离开组存在的情况下,和你的挑战将是找到一个网站在分子替换或消除最有可能发生。
正如我们之前看到的,找一个好的离去基团附加到一个sp3杂化碳。
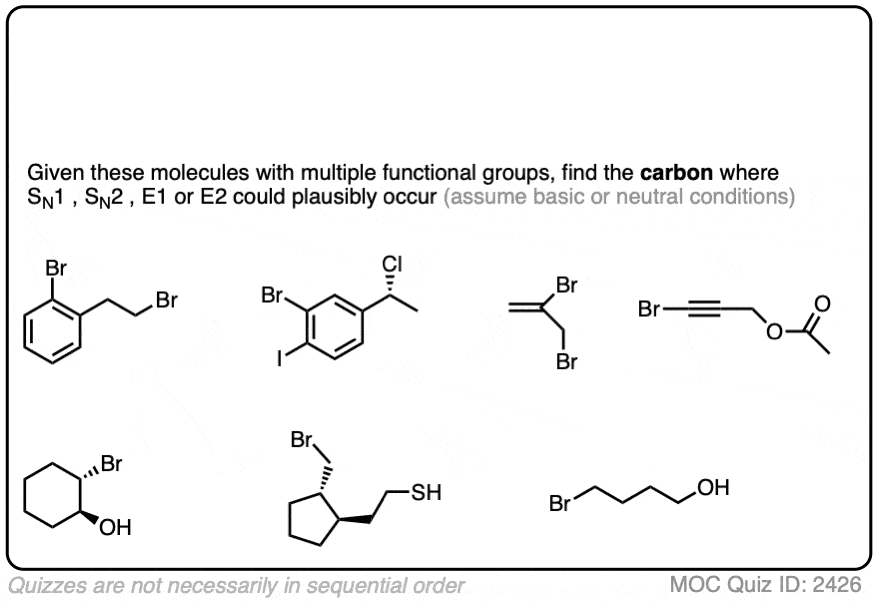 点击翻转
点击翻转
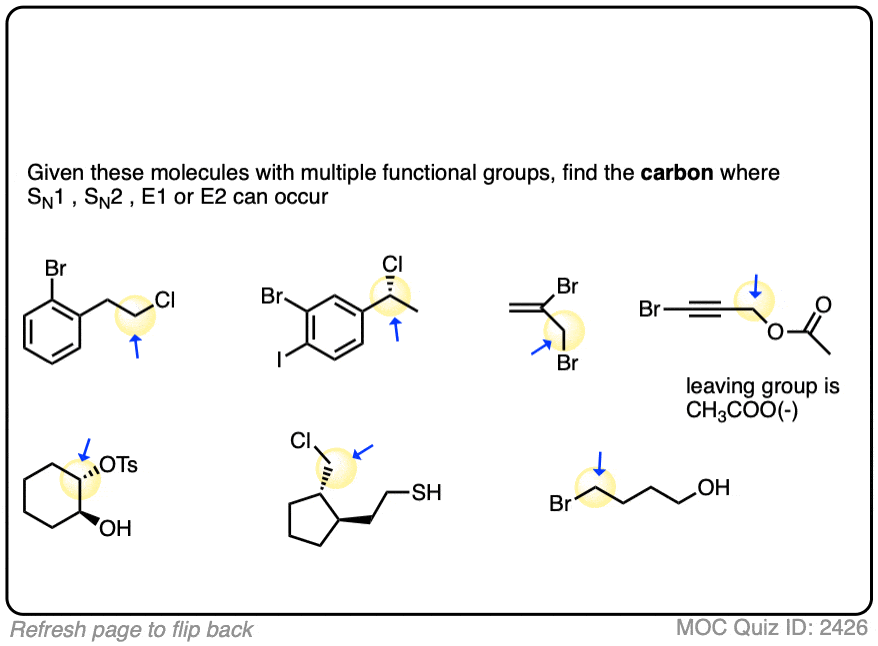
你可能会看到其他组像哦,NH2或SH除了好离去基团。这些都是有可能的亲核试剂通过一个能与底物发生反应分子内的取代反应。(见文章:分子内的SN2反应)
6。环氧化合物
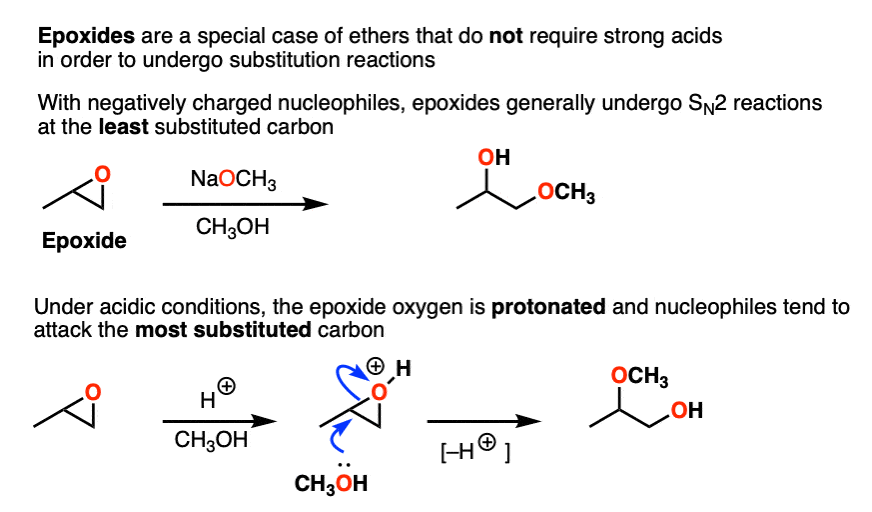
环氧化合物醚的一种特殊情况,将进行替换没有添加酸反应。这是由于相当大的环三元环的压力(见文章:环氧开环与基础)。
7所示。总结
总之,确定年代的过程N1 / SN2 /E1/E2反应的发生是这样的。
下一步是确定碳轴承离去基团作为主,二次,或三级。这将有助于缩小的反应是否会参与一个年代N1,年代N2,E1或E2的反应。在下一篇文章。
在下一篇文章:决定SN1 SN2 / E1 / E2 -底物
笔记
注1-氟键离解能的CH3F是大约109千卡每摩尔,甚至比碳氢键离解能(104千卡每摩尔)。
注2——尽管是弱碱(pK一个9.2)HCN的氰根离子并不作为好离去基团在年代N2氟离子反应类似的原因;C-CN债券实在是太庞大了。(一个估计是反应不宜约15千卡每摩尔,这使得位移CN(-)不太可能)
事实上,乙腈,俗称乙腈,是一种常用的极性非质子溶剂的年代N2反应。
注3——为什么SN1/SN2/E1/E2反应只发生在烷基卤化物而不是烯基或炔基卤化物吗?
这是看它的一种方式。
记得s轨道是接近原子核,这就是为什么乙炔化物离子更稳定烷基阴离子吗?你能想到的烯基和alkynl碳原子有一个伟大的有效的电负性比烷基碳,这使得他们“抓住”电子更紧密,使其更难的电子对离开。
另一个相关的解释与碳的相对能力稳定正电荷当提到的数量增加。
的E1和SN1通过碳正离子的反应,而SN2反应需要一个过渡态中碳部分正起诉。
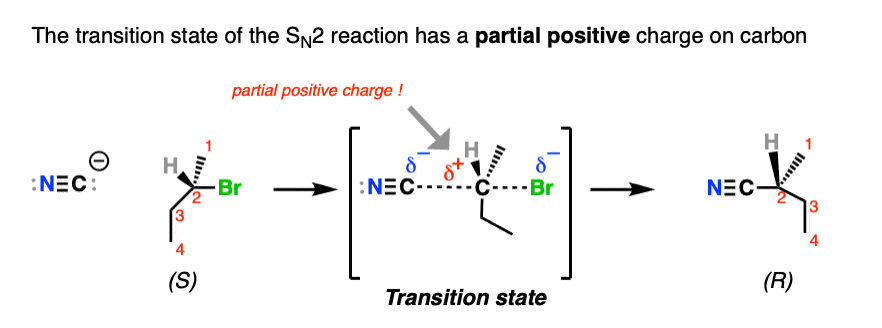
每个这些反应需要一个过渡态,中央碳部分正电荷。
如果你回想一下,稳定孤对电子的能力增加随着提到增加(sp3< sp2< sp)然后把趋势相反的方向;碳的能力稳定一个正电荷减少随着提到增加,随着空轨道接近带正电的原子核。
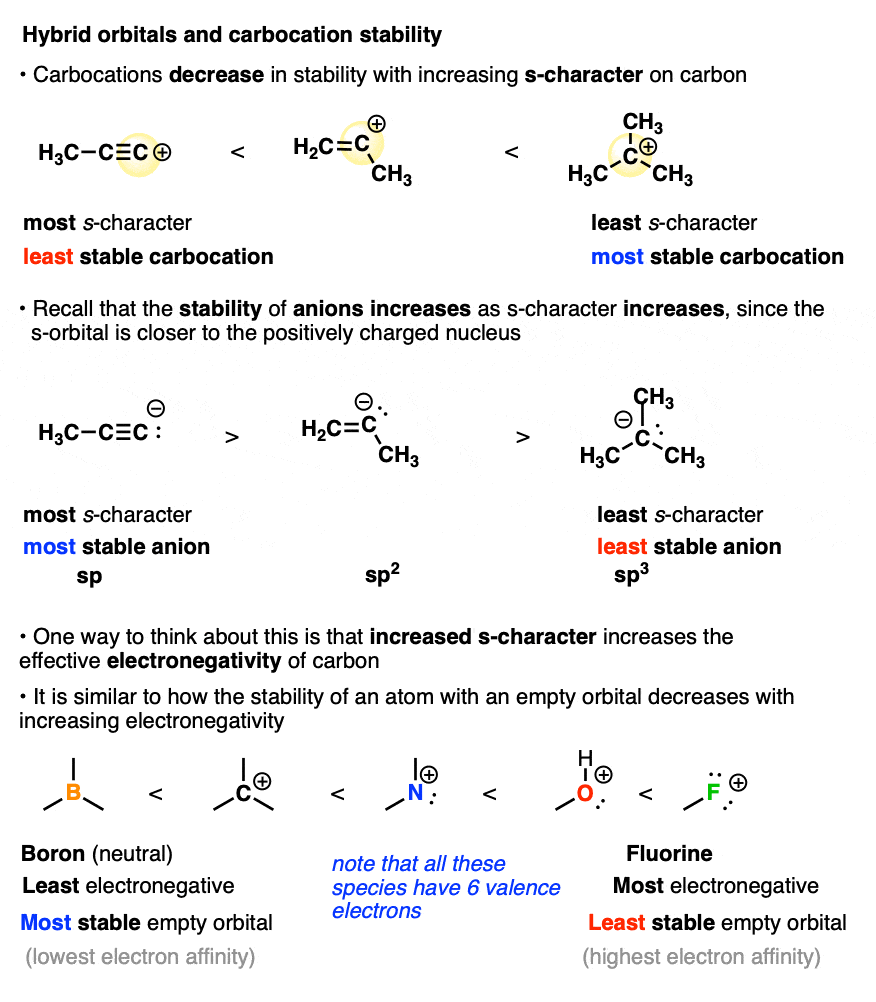
更多碳正离子的稳定性,看到这篇文章碳正离子的稳定性。
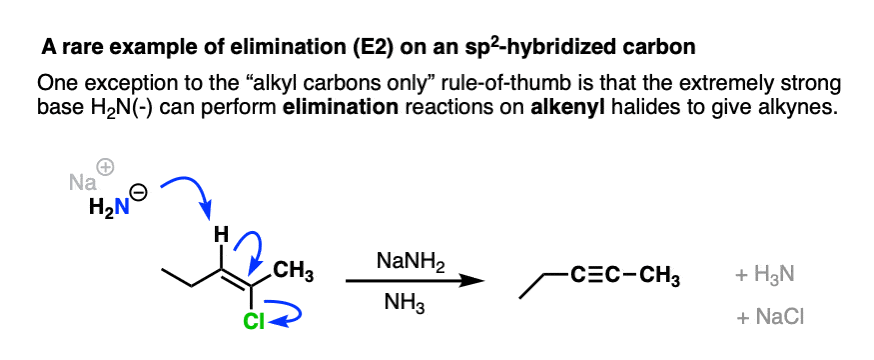
注意4——“没有年代例外N1 / SN2 /E1/E2在sp2杂化碳”的形成炔烃从烯基通过使用极其强碱NaNH卤化物2。见文章-通过消除炔烃的合成烯基卤化物
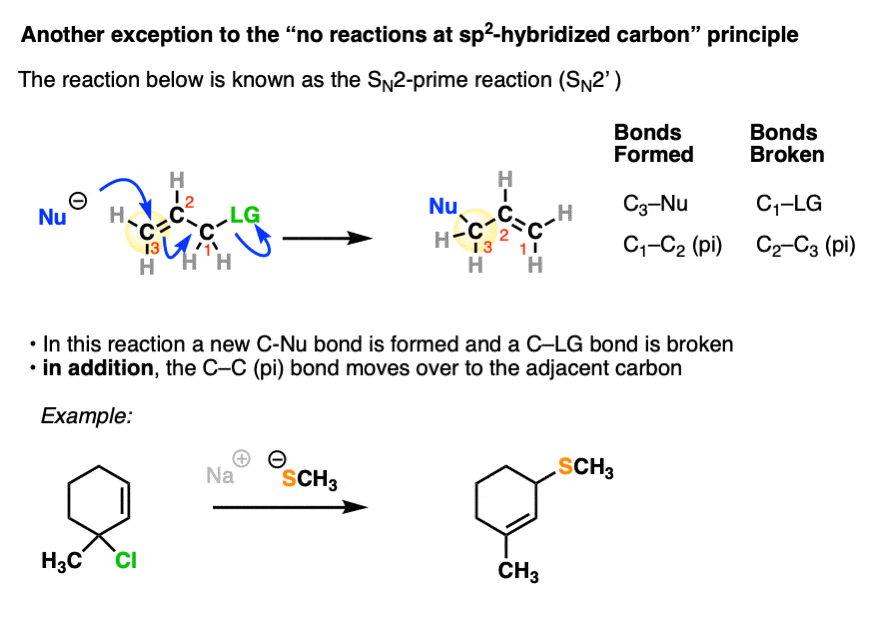
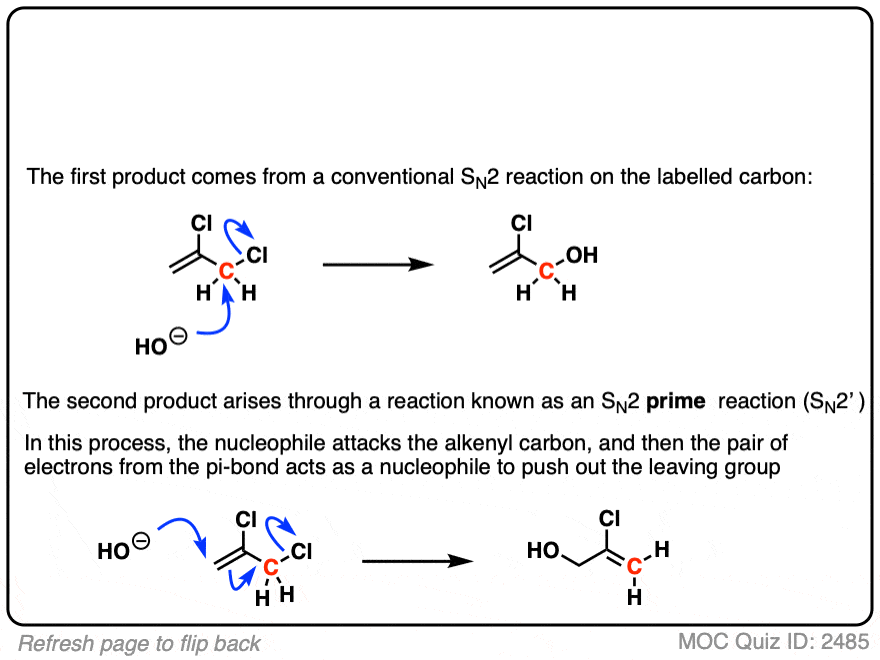
注5。“没有年代的另一个例外N1 / SN2 /E1/E2在sp2杂化碳”是发现在反应称为年代N2 (N2′)的反应。这是类似于年代N2,它是协调和双分子的,但略有不同,攻击并不直接发生在sp2杂化烷基卤化物。
这不是一个反应,出现太多的在介绍有机,但一个好的考试问题。
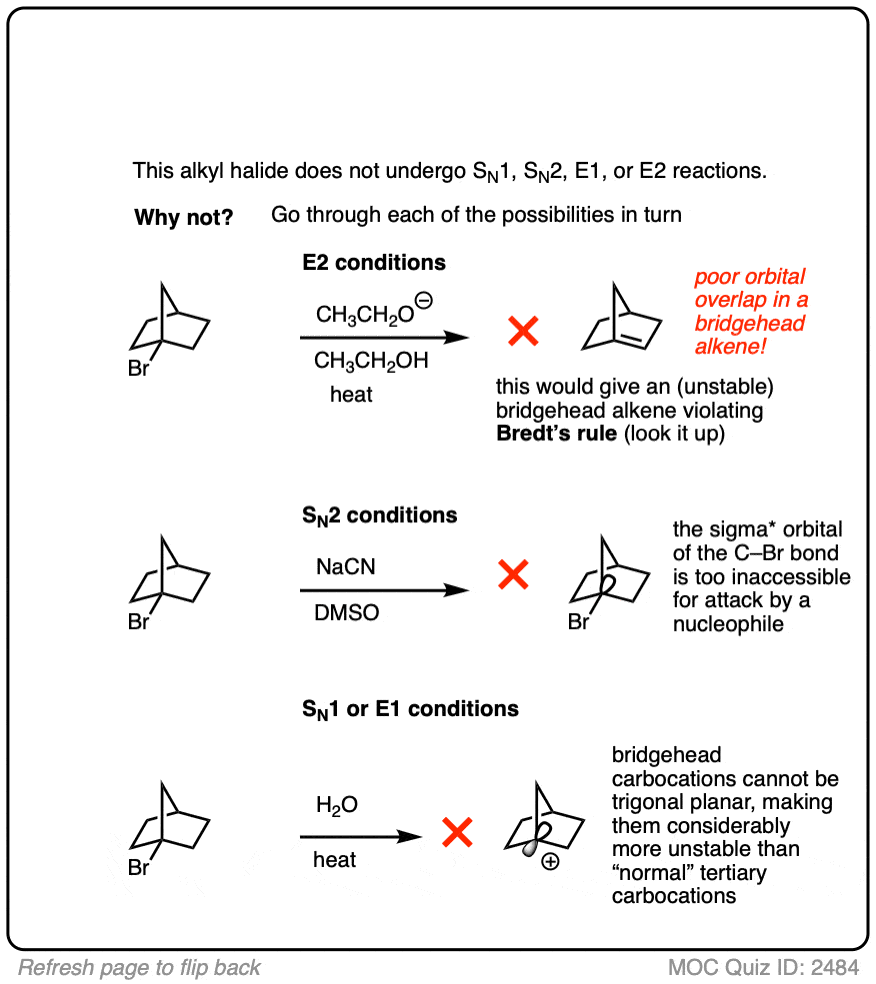
测试你自己!
 点击翻转
点击翻转
 点击翻转
点击翻转
(高级)引用和进一步阅读
Streitweiser溶剂离解作用的位移反应,31日页:
(根据计算)甲基溴离子与氢氧根离子的反应是放热的,16个千卡每摩尔。相当于增加了活化能逆反应的对应于一个10倍-12年率;即速度太缓慢。自的反应烷基卤化物与乙醇盐、酚盐、醋酸、氢硫化物氰化物硫代硫酸盐和亚硫酸盐离子都是由10 - 20千卡放热,相反的反应会慢的因素107到10-14年,因此将无法观察到除了最特殊的条件下。”
- 离子反应的机制。热离子置换反应
r . a . Ogg
反式。法拉第Soc。,1935年,31日,1385 - 1392
DOI:10.1039 / TF9353101385
测量的一些简单的亲核取代反应的反应热烷基卤化物与各种亲核试剂。
评论
评论部分