构象和环烷
计算在环烷环应变
最后更新:2022年12月13日|
在环烷环应变(1)-环应变计算
这篇文章是关于如何计算环应变。如果你想要更多的具体细节在环丙烷环应变和环丁烷,我建议继续下一篇文章。
在上一期,我们了解了碳可以形成环的一个结果——我们可以形成立体异构体(cis /反式)。这篇文章试图解释成环的另一个非常有趣的结果:环应变。
这一切都始于:事实证明你可以学到很多关于分子通过燃烧。当然,在控制和量化方法。:-)
表的内容
- 烷烃的燃烧热
- 燃烧热链长度的函数
- 燃烧热很长链每CH 157千卡每摩尔2
- 环烷通式(CH2)n
- 任何偏离平均值为157千卡每摩尔CH2代表环应变
- 什么因素可能会导致环应变?
- 笔记
- (高级)引用和进一步阅读
1。烷烃的燃烧热
摩尔燃烧热,你可能还记得从创化学、燃烧释放的能量在一摩尔的物质。这是一个焓值(ΔH)——通常以焦每摩尔或千卡每摩尔。在这里我们要用千卡每摩尔(看到帖子:为什么有机化学家使用千卡吗),但将焦每摩尔,乘以4.184,得到同样的事情。
让我们从一些简单的开始。想象我们有一系列的直链烷烃。乙烷、丙烷、丁烷、一直到十二烷(12)。
我们增加碳的数量,增加燃烧时释放出的能量将会增加。我喜欢用无限楼梯的类比:每一步我们走高,我们增加我们和地板之间的距离,因此增加释放的能量如果我们从楼梯下到地面:-)。

2。燃烧热链长度的函数
我们问一个简单的问题:如何燃烧热改变当我们添加额外的碳?
你认为我们会希望看到一个间距相等的能量我们先后添加碳(通过类比与等距的楼梯步骤)?或者间隔逐渐改变?重要的是,我们可以使用这些信息来做出预测吗?
让我们燃烧不同直链烃类和测量多少能量(千卡每摩尔)发布的每个分子。
我们可以计算平均能量释放每个碳——这给了我们每一步之间的“距离”。这将帮助我们预测下一步释放的能量。
(在这里,运用你的想象力,因为我们可变长度的燃烧碳氢化合物和测量每个案件)的燃烧热。
现在让我们看一下数据。当我们这样做时,我们看到了千卡每摩尔/碳开始高:213年甲烷(没有显示),186(乙烷)然后开始达到限制稍微低于160千卡每摩尔。这就像一个楼梯,开始大的步骤,但高度逐渐降低,直到他们都成为一个统一的高度。
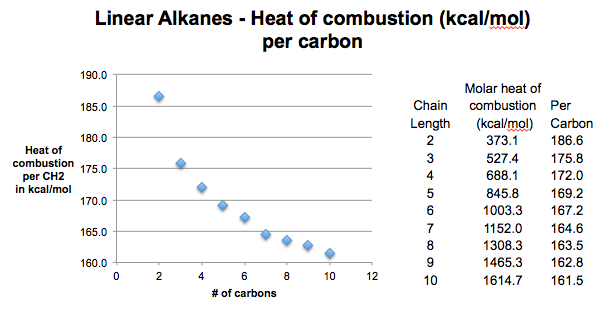
3所示。燃烧的热量很长直链烷烃是每CH 157千卡每摩尔2
的曲线,顺便说一下吗?很微妙的问题。答案很长,所以它是注1。
- 短版:CH直链烷烃的公式3(CH2)nCH3,热量从燃烧释放结束(CH3)高于来自燃烧室内CH2组。
- 链变长,# CH2> > # CH3的相对贡献2 CH3集团整体ΔH将减少。因此,在无限的极限nΔH的价值燃烧将CH方法2(约157千卡每摩尔)。
4所示。环烷通式(CH2)n
这与环烷什么?环烷由只有CH的2组。没有“结束”的担心。如果我们重复同样的燃烧实验,从环丙烷,并增加CH2每一次,我们可能只期望看到的燃烧热,只有ΔH CH2(157千卡每摩尔)。
换句话说,我们会天真地希望看到一个楼梯统一的阶梯高度,所有的。
科学通常开始通过这些天真的观念自然应该如何工作,然后做实验,发现现实是相反的(因此更有趣比)我们的预期。这是一个典型的例子!
5。任何偏离值每CH 157千卡每摩尔2告诉我们关于环的压力
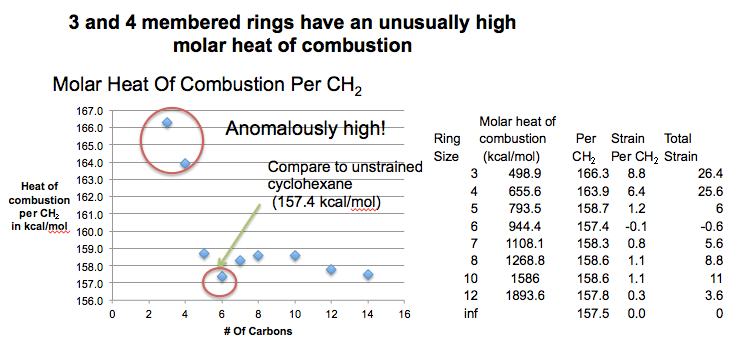
这就是当我们燃烧。看那个“平均阶梯高度”(又名ΔH燃烧/ CH2)。
比我们预计的C = 3(环丙烷,166.3千卡每摩尔)和C = 4(环丁烷,163.9千卡每摩尔),达到最低C = 6(环己烷157.4千卡每摩尔)然后推动起来,直到触及另一个最低C = 12(环十二烷)。
(虽然不包括在图,那里的阶梯高度不变,约为157.4千卡/摩尔)。
如果我们把157.4千卡/摩尔作为基线,环丙烷版本8.8千卡/摩尔/碳“额外的”,总共26.4千卡每摩尔。环丁烷6.4版本“额外”千卡每摩尔/碳,总共25.6千卡每摩尔。
这意味着这些分子实际上是“额外”能量更多的比我们预期的不稳定(比我们想象的“更高的阶梯”,所以有更远的落地)。我们称之为“额外”不稳定。”压力”。
注意,我们会得到类似的结果,如果我们的生成热,而不是燃烧加热相比,但燃烧更生动的:-)
6。什么因素可能会导致环应变?
像任何好的实验,这引发了很多新的问题。
- 首先,这可以是一个来源的什么“应变”?为什么环丙烷和环丁烷比我们天真地期望更不稳定吗?
- 第二,为什么不牵强附会的环己烷超过环戊烷?例如,五角大楼的内角(108°)更接近理想的键角是一个四面体(109°)比六边形(120°)。给什么?
- 第三,增加了应变之间C = 6(环己烷)和C = 14 ?为什么从环己烷压力上升,然后再回来吗?
在下一篇文章我们将处理环丙烷环丁烷,然后未来的职位将在未来的两个问题。
笔记
注1:超过O2,所有C转化为有限公司2和所有H转化为H2O。
燃烧甲烷(CH4)给我们1枚有限公司2和2枚的H2o .乙烷给我们2枚有限公司2和3枚的H2o .丙烷给我们3枚有限公司2和4枚H2o .在单位碳的基础上,我们增加碳的#,有限公司2/小时2阿比方法1。的ΔH燃烧根据单位碳甲烷是最高的,因为更多的H2O形成,因此比例更多的能量释放。回到顶部
(高级)引用和进一步阅读
- Ueber Polyacetylenverbindungen
阿道夫·贝耶尔
的误码率。1885年,18(2),2269 - 2281
DOI:10.1002 / cber.18850180296
传奇的原始纸环应变药剂师阿道夫·冯·贝耶尔。尽管本文标题是在一个完全不同的话题,讨论了环应变在论文的结尾。 - 评价应变的碳氢化合物。金刚烷及其起源的应变
保罗·冯·R·Schleyer、詹姆斯·厄尔·威廉姆斯和布兰查德k·R。
美国化学学会杂志》上1970年,92年(8),2377 - 2386
DOI:1021 / ja00711a030
早期论文p v . r . Schleyer教授在他搬到德国在1970年代。金刚烷是一种宠物的话题,作为他最高被引论文一份单页的沟通江淮简单的合成金刚烷。表七世在本文中有大量的应变能量的各种碳氢化合物,包括环丙烷和环丁烷(分别为28.13和26.90千卡每摩尔)。 - 分子力学的关键评估
爱德华·m·恩氏和保罗·约瑟夫·d·Andose v . r . Schleyer
美国化学学会杂志》上1973年,95年(24),8005 - 8025
DOI:1021 / ja00805a012
表二世在这篇文章中包含一个大表的生成焓变和应变能量,在实验和理论上计算决定。 - 焓和异构化动力学quadricyclane降。应变能的quadricyclane
David s . Kabakoff Jean c . g . Buenzli Jean f . m . Oth威利斯b·哈蒙德和杰罗姆·a·Berson
美国化学学会杂志》上1975年,97年(6),1510 - 1512
DOI:1021 / ja00839a039
本文经过详细的热化学quadricyclane异构化的研究,并确定应变能在96±1千卡每摩尔。 - 紧张的有机分子的调查
乔尔·f·Liebman和阿瑟·格林伯格
化学评论1976年,76年(3),311 - 365
DOI:1021 / cr60301a002 - 有机化学中应变的概念
肯尼斯·b·Wiberg
Angew。化学。Int。。1986年,25(4),312 - 322
DOI:10.1002 / anie.198603121
环应变也可以称为“角应变”,结果失真的键角,增加能量的分子。本文还讨论了propellanes,一个有趣的一类小分子紧张。虽然(1.1.1)propellane可以被孤立,(2.2.1)尚未获得作为一个纯物质。这是由于中央的力量键均裂,它提供了一种路径分解。这种能量是强烈的影响区别在反应物之间的应变能和由此产生的双游离基。(1.1.1)propellane,区别是65千卡每摩尔,在(2.2.1)propellane 5千卡每摩尔。 - 烃特性的理论分析。1。债券、结构、电荷浓度,风头
肯尼斯·b·Wiberg理查德·f·w·巴德和克莱门特·d·h·刘
美国化学学会杂志》上1987年,109年(4),985 - 1001
DOI:1021 / ja00238a004
杂交的变化与电负性的变化。越大年代字符的特定碳轨道,它的电负性越大。因此,碳原子的紧张对氢环的电负性大于正常。 - 紧张的化合物的反应:基态扰动率提高的主要原因吗?
阿里尔鞍,哈罗德Basch Shmaryahu Hoz
美国化学学会杂志》上1996年,118年(2),416 - 420
DOI:1021 / ja951408c
环的压力可能会导致债券的性质定性变化(杂交),和这些变化可以增加反应性。 - 立方烷的热化学合成:50年后立方烷及其衍生物的高层次的理论研究
菲利浦- Agapito鲁伊·c·桑托斯,鲁伊·m·博尔赫斯多斯桑托斯和何塞·a·Martinho摄影记者
《物理化学》杂志上2015年,119年(12),2998 - 3007
DOI:10.1021 / jp511756v
立方烷的热化学性质的重新评估使用的计算方法。作者在这里重新评估立方烷的应变能,是667焦每摩尔(159千卡每摩尔),这是非常接近之前已经确定(154千卡每摩尔)。
为什么环己烷-应变?
环己烷应变为零,不是消极的压力。
我试着计算角应变环丙烷和得不到26.4。
这是24.75而不是26.4
3 * 8.8
精彩的文章…。vry容易理解…! ! !