醇、环氧化合物和醚
卤代烃与醇
最后更新:2022年11月7日|
使烷基从醇卤化物
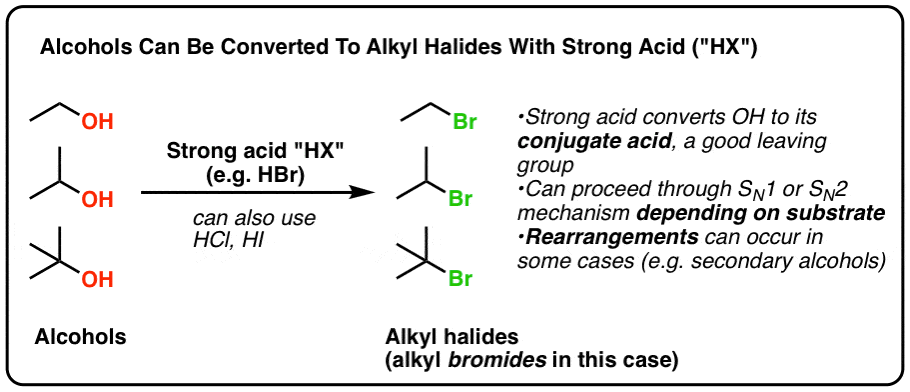
在今日的帖子里,我们表明,治疗与HCl醇,哈佛商业评论,或者嗨(所有属于统称“HX”,其中X是一个卤)导致的形成烷基卤化物。
- 主要醇往往通过一个年代N2机制
- 叔醇往往通过一个年代N1机制
- 当心重组在二级碳正离子反应可能形成
表的内容
- 添加酸对酒精产生一个好的离去基团(水)
- 从甲基烷基卤化物,主要通过SN2醇反应
- 从三级醇烷基卤化物所得的年代N1通道
- 一个好的经验法则为二级醇HX:假设N1
- 重组在卤代烃与醇的形成
- 重排示例# 1:氢化物转移
- 重排例2:烷基转移
- 重排示例# 3:烷基转移的一种特殊情况——环扩张和萎缩的分水岭
- 什么不工作?
- 摘要:从醇烷基卤化物
- (高级)引用和进一步阅读
1。将酸加入酒精导致一个好的离去基团
我们已经说过很多次在这个系列的文章醇是可怜的基质N1和年代N2反应。这是因为氢氧离子(HO)是一个穷人离去基团,因此不可能1)离开自己的协议,只留下一个碳正离子(SN1通路)或2)传入流离失所亲核试剂(这将是一个年代N2反应)。
但是我们也看到,治疗酒精与酸会导致一个有趣的“个性调整”:酒精(R-OH)转换为它共轭酸(R-OH2+)现在拥有一个像样的离去基团(我们所知道的弱碱水,H2O)。看到帖子:如何使醇反应)
我们看到,在以前的文章,这允许(对称)醚醇的形成,通过N2通路(主要醇)或一个年代N1通路(三级醇)。
我们可能会问:这可以扩展到形式以外的其他官能团醚?
绝对的。用盐酸处理醇,哈佛商业评论,或者嗨(所有属于统称“HX”,其中X是一个卤)导致的形成烷基卤化物。
这发生在一个两步的过程:
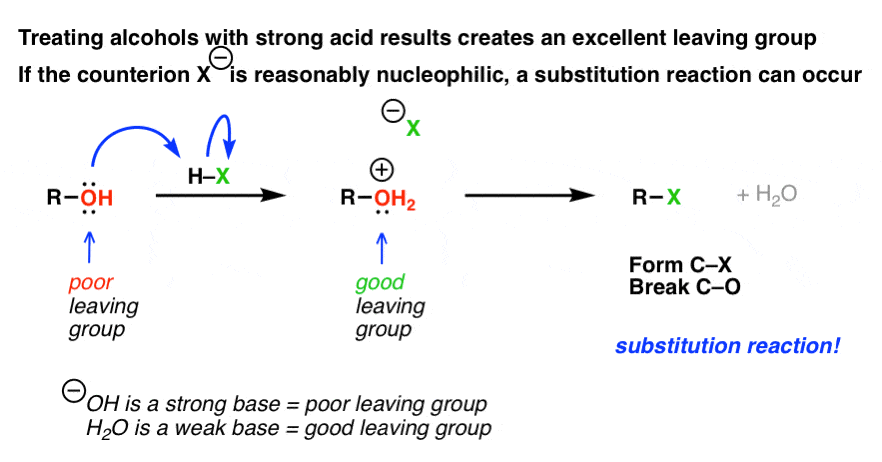
注意,第二步(替换)模糊的在上面的图。这是因为,正如我们所看到的,替代途径取决于基质的类型。
2。从甲基烷基卤化物,主要通过年代醇N2反应
知道敏感的年代N2反应是位阻,我们应该期待的甲基酒精主要的醇,SN2通道占主导地位。和它!(看到帖子:的年代N2机制)
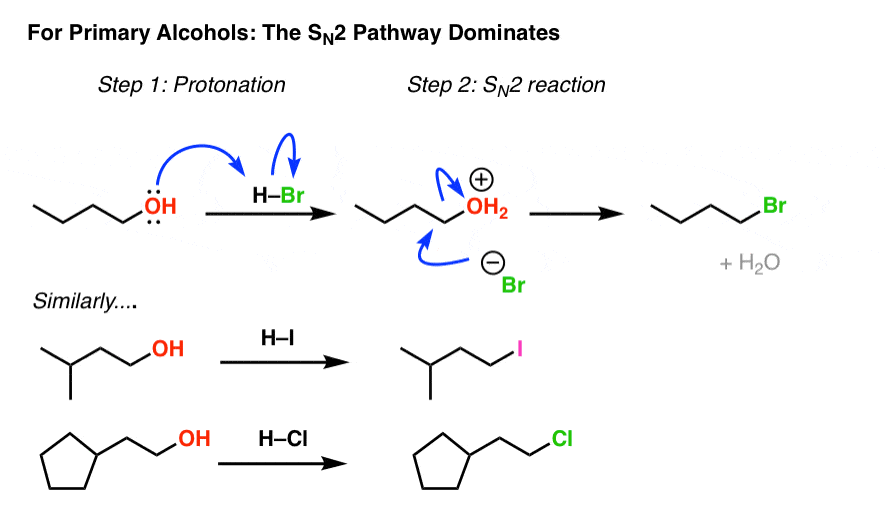
注意在每一种情况下我们首先使质子化酒精,创造一个良好的离去基团然后流离失所共轭碱的酸。(看到帖子:是什么让一个好的离去基团吗?)
烷基氯化物、溴化物和碘化每一个可以让这种方式。
3所示。从三级醇烷基卤化物所得的年代N1通道
同样,理解的趋势碳正离子的稳定性我们应该期待,叔醇转化烷基通过一个年代卤化物收益N1通路。和它。(看到帖子:的年代N1机制)
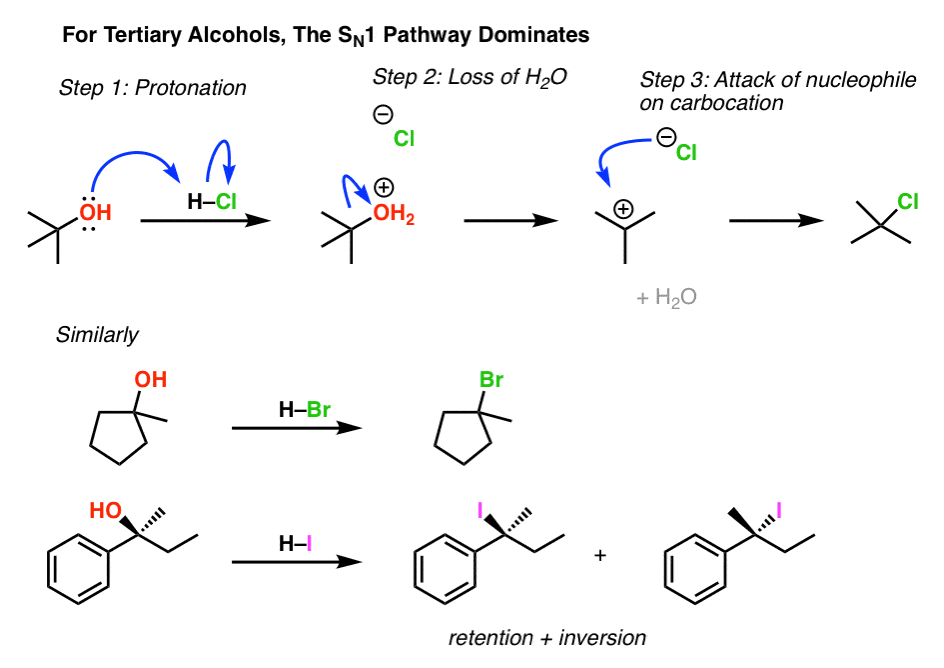
注意开头的最后一个例子,一个手性原料会导致反演和保留的混合物(通常被称为”,外消旋化”),因为它经过(平)中间碳正离子。
4所示。一个好的经验法则为二级醇HX:假设N1
甲基,小学,叔醇都表示很简单的情况下。
“所以二级醇呢?“你可能会问。哦,是的。这正是事情变得有趣的,,因此,考试的东西的问题。
在实验室里、治疗的二级醇HX导致产品从年代的混合物N1和年代N2通道。为实用目的通常不是一个有用的过程,特别是如果你关心保护立体化学。
然而,你的入门教科书和课程笔记不是“实验室”。课程的目的是向你介绍有机化学中的重要概念。并从教师的角度来看,所以发生二级醇二次的转换烷基卤化物的HX提起这个话题,是一个很好的机会bdapp平台碳正离子重排。这属于范围的年代N1通路。
所以一个好的经验法则是假设——为了你的课程——二级醇处理HX将通过一个年代N1机制。
5。重组在卤代烃与醇的形成
我们重组(氢化和覆盖烷基转移之前的年代N1反应。但是值得再次接触。
基本前提是这样的。不稳定的碳正离子,electron-poor物种。其稳定性一般随附碳的数量,这有助于电子密度捐款。因此,碳正离子的稳定性增加的方向甲基< <二次<三级。我们也看到,碳正离子被共振稳定。
正如我们看到的之前的系列文章——咨询这个如果你需要更多的牵手!——碳正离子可以接受1 2碳氢键和碳碳键的变化,导致新碳正离子。
这样的重组是最可能发生如果他们能导致一个更稳定的碳正离子。例如,二级到三级碳正离子重排,是a青睐(积极“下坡”)的过程,而从一个二级三级碳正离子重排(积极“上山”)不太可能。
随时通过碳正离子中间体反应所得,我们需要注意是否相邻碳,可以生成更稳定的碳正离子通过碳氢键的转变或碳碳键。
有三个情况下尤其要注意。
6。重排示例# 1:一个氢化的转变
寻找一个二次酒精邻叔碳。注意这个常见的例子,质子化作用导致损失的水,其次是氢化物转移和捕获碳正离子的卤化物离子。
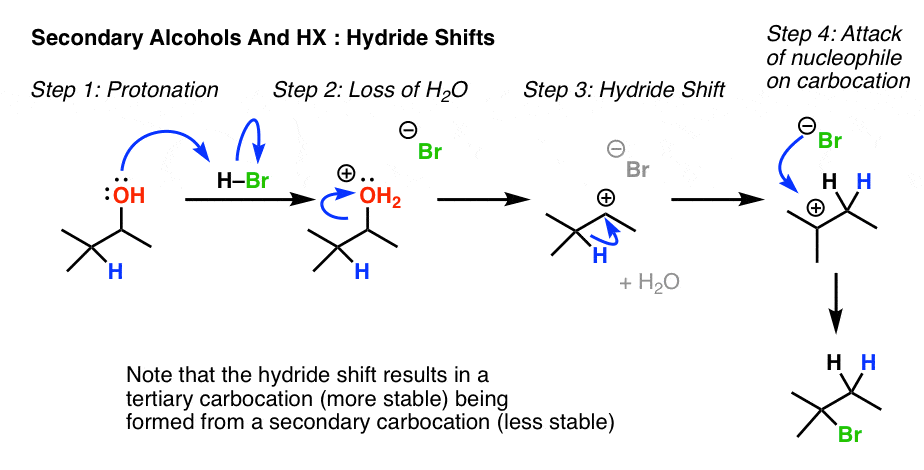
有利的重排的另一个例子是当一个仲碳是邻”烯丙基的或苄基的氢。重排导致仲碳稳定的共振。
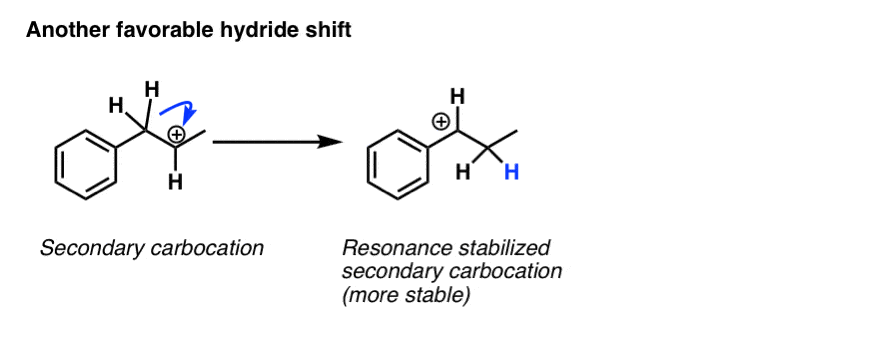
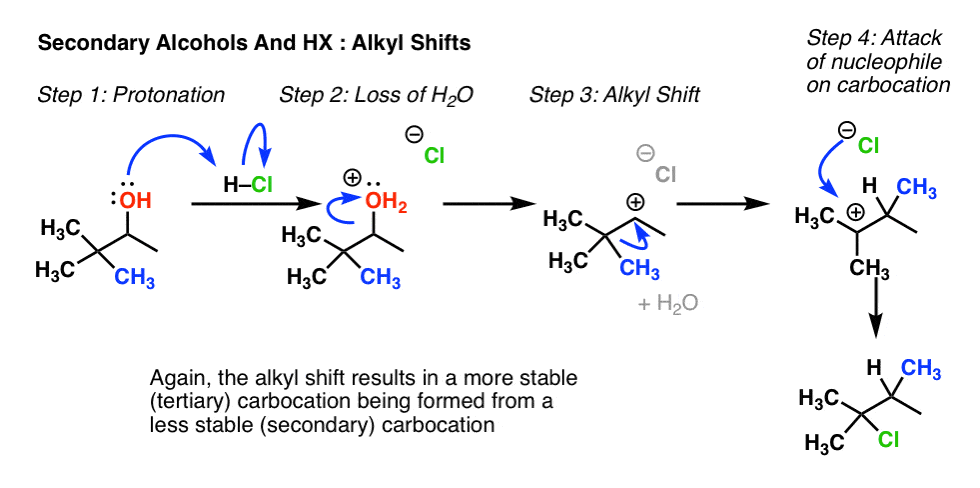
7所示。重排例2:烷基转移
寻找一个二次酒精邻近一个季碳(即碳连着4个碳)。注意,这就是上面的相同的氢化过程的转变中,除了CH3是迁移,而不是H。
8。重排示例# 3:烷基转移的一种特殊情况——环扩张和收缩
寻找一个二次酒精毗邻紧张环(环丁烷在经典案例)。一旦二次生成碳正离子,紧张的债券环迁移,导致扩张环。这是特别有利的情况下环丁烷环戊烷由于环丁烷是高度紧张(约26千卡每摩尔)而环戊烷环应变最小。
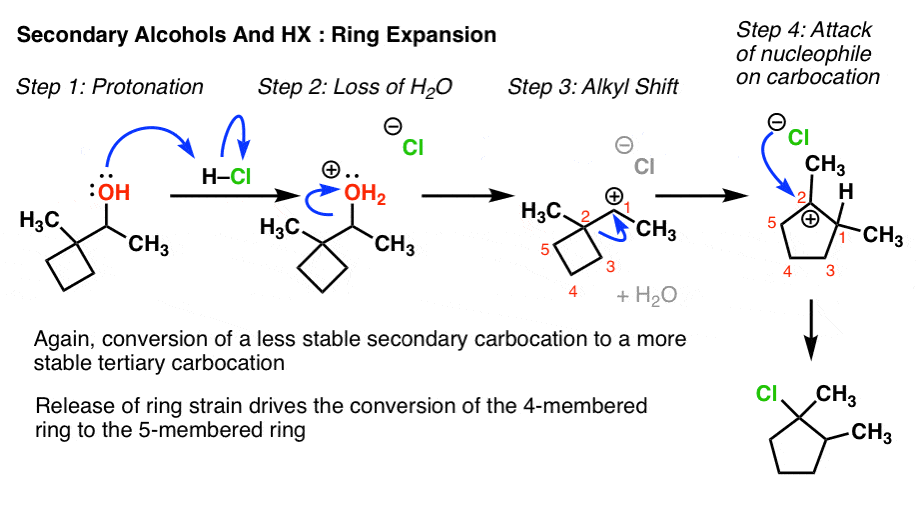
这种类型的烷基通常给学生很难转变,这当然是一个最喜欢的教师考试的问题。虽然曲线箭头画比前面两种情况一样,没有什么不同我认为映射的主要困难是产品从起始物料。在这方面我建议两件事:
- 碳原子数(IUPAC不一定,只是号码跟踪)。例如在步骤3中箭头(在这里烷基)向我们展示了打破C2-C3和形成C1-C3转变。应用弯曲的箭头意味着C1的规则将中性和C2将成为碳正离子。这是正在发生的一切。没有其他债券形成或打破在这一步。它需要练习能得到这个权利。
- 首先画丑陋的版本。然后画让它看起来不错。
环收缩也是有可能的,尽管不那么有利的紧张的戒指。应用相同的原则。
9。卤代烃与醇类:什么不工作?
它总是有助于知道行不通的形成烷基从醇卤化物。
首先,因为我们这里处理置换反应,一些熟悉的规则适用。只有烷基醇(醇在sp3杂化碳原子)将接受N1,SN2反应。的年代N1和年代N2通道涉及的正电荷积累碳,和sp2和sp杂化碳正离子是极其不稳定的。这年代未遂N1的苯酚为例,将失败:
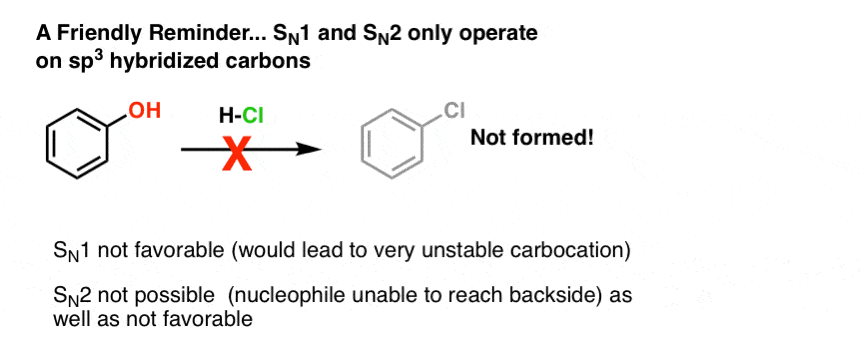
您可能还想知道我们可以用试剂如HCN,霍阿克,风琴3将醇转化为腈,酯类分别,和叠氮化。一般来说,没有。问题是,这些是相当弱酸(pK一个4及以上)这只会给一个低浓度的质子化了的酒精。由于反应速率与浓度成正比,形成这些产品将是缓慢的。(与叠氮化,也有潜在的并发症与不同类型的重排,但作为一个curtiusy我们不会处理施密特现在:-)]
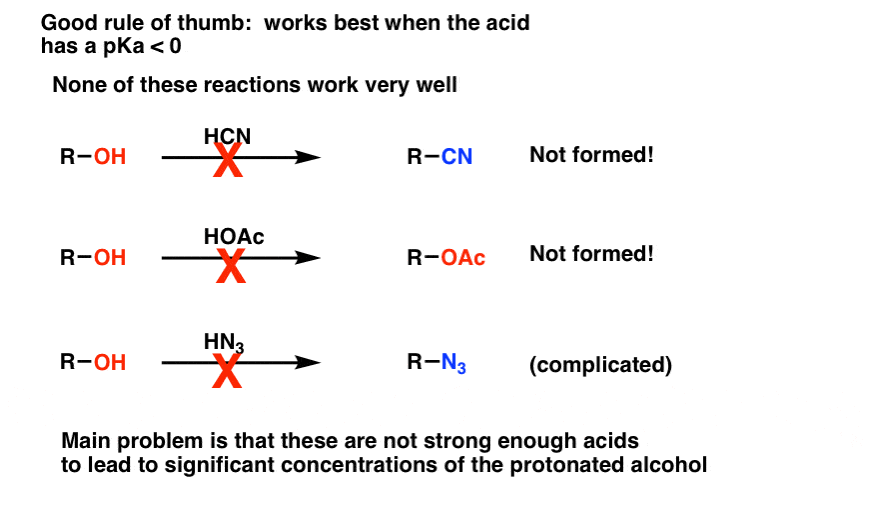
就我们的目的而言,醇类转换成其他替代产品使用强酸仅限于HCl,哈佛商业评论,嗨,和H + /卢武铉的特殊情况给出了对称醚。一个好的经验法则是,共轭酸的亲核试剂应该有一个pK一个0或更少的反应发生。
10。摘要:卤代烃与醇
所以可以转化为醇烷基卤化物。你可能会问,“我们为什么要在意吗?”。答案是,当我们说,转换一个酒精(这很差离去基团)到一个烷基卤化物(有很大的离去基团)现在允许我们做各种官能团互变现象没有以前。的年代N2是一个非常有用和强大的反应,例如。一次伯醇已经转换成主烷基卤,我们可以把它与所有种类的亲核试剂,使大量的官能团。
但是好它是能够做到这一点,虽然,它远非理想。我们必须使用强酸,这常常会导致并发症,如果我们有acid-sensitive官能团分子。此外,所有那些讨厌的重组二级碳是一个麻烦。他们可以用我们的立体化学和螺丝导致不受欢迎的产品。你可能会问,“没有办法让周围?”。
是的!我们将讨论一个很好的方式在这种困境下一篇文章!
在下一篇文章- - - - - -甲苯磺酸盐和甲磺酸
笔记
(高级)引用和进一步阅读
烷基氯化物醇:
- 氯化丁基
詹姆斯·f·诺里斯和阿兰·w·奥姆斯特德
有机合成,科尔。卷1,p。144 (1941); Vol. 8, p.50 (1928).
DOI:10.15227 / orgsyn.008.0050
的一个例子N1转换tert-butanol与HCl叔丁基氯。这是来自有机合成,独立的来源可靠,测试了有机化学实验过程。烷基从醇碘化: - 不饱和醇与碘化钾反应多磷酸的存在
理查德·琼斯和j·b·帕蒂森
j .化学。Soc。1969年,1046年
DOI:10.1039 / J39690001046
本文运用KI +磷酸生成嗨原位碘化,将醇。 - 1,6-DIIODOHEXANE
赫尔曼·斯通和哈罗德Shechter
Synth。1951年,31日31岁的
DOI:10.15227 / orgsyn.031.0031
一个过程的有机合成,独立的来源可靠,测试了有机合成实验程序,转换为醇与KI +碘化PPA(多磷酸)。 - 合成方法和反应。63年。吡啶保利(氟化氢(30%)吡啶-70%氟化氢):一个方便的有机氟化试剂反应
约翰·t·韦尔奇乔治•a . Olah Yashwant . d . Vankar Mosatomo Nojima,什特克雷克斯,朱迪斯·a·Olah
《有机化学》杂志上1979年,44(22),3872 - 3881
DOI:1021 / jo01336a027
吡啶保利(氟化氢),也称为PPHF或“Olah试剂”可以用来作为转换的布仑斯惕酸醇碘化,随着KI或奈。 - 一个简单、高效和醇转化为一般方法烷基由CeCl碘化37小时2O /奈系统乙腈
米蕾迪托恩里科Marcantoni,伊丽莎白·Torregiani朱塞佩莎娃,玛丽亚克里斯蒂娜·贝鲁奇,玛塞拉黄宗泽,和莱蒂齐亚Sambri
《有机化学》杂志上2000年,65年(9),2830 - 2833
DOI:10.1021 / jo991894c
路易斯酸可用于这个反应而不是布仑斯惕酸,允许温和的反应条件。 - 直接醇转化为相应的碘化
Reni约瑟夫,Pradeep s Pallan a . Sudalai Ravindranathan
四面体。1995年36(4),609 - 612
DOI:10.1016 / 0040 - 4039 (94)02315 - 3
元素碘(我2)也可以用于直接碘化醇转化为。可以转化为醇烷基与PBr陈词滥调3: - 方便不稳定的合成光学活性的次要的烷基陈词滥调的手性醇
罗伯特·o·哈钦斯Divakar。Masilamani和辛西娅·a·Maryanoff
《有机化学》杂志上1976年,41(6),1071 - 1073
DOI:1021 / jo00868a034 - 合成光学活性的烷基卤化物
哈里·r·哈德逊
合成1969年,112 - 119
DOI:1055 / s - 1969 - 34195
PBr的主要工具3是它允许转换的手性醇陈词滥调反演的配置没有重排上面的两篇论文演示。他们也说明反应的机制,通过中间烷基亚磷酸盐。 - TETRAHYDROFURFURYL溴化
l·h·史密斯
Org。Synth。1943年,23,88年
DOI:10.15227 / orgsyn.023.0088
这个过程从有机合成,独立的来源可靠,测试了有机化学实验过程,展示了PBr3与醚兼容。
先生,我可以问为什么干氢卤化物作为反对HX的水溶液吗?
水与氢卤化物反应会给H3O + X -。产品可能会喝酒,不是卤。
先生,我有一个小困惑。当我们使用卢卡斯试剂即优化选取的氧醇锌中心坐标,将它转换成一个好的离去基团。但是使用优化选取+盐酸的主要醇促进Sn1吗?因为我看到很多问题,他们已经要求写产品当伯醇对卢卡斯试剂,但他们都有显示1,2变化也不能发生除非Sn1紧随其后。但显然像你说的,我发现在许多其他来源Sn2显然应该发生。
你能想到的氢化作用有点像亲核试剂的SN2反应氢化物转移发生的同时破损切断键。这可能是最好的办法。
我混淆了卢卡斯的反应试剂与伯醇一个分支在β碳收益(比如ch3ch2ch (ch3) ch2oh)。它遵循Sn1 Sn2吗
嗨。卢卡斯试剂合成的甲基氯fr。甲醇+盐酸+优化选取盐酸…做多余的水导致的形成氯化二甲基锌或别的东西,?答案是两个复杂的对我的大脑豌豆,哈哈
它不会是二甲基锌,由于甲基二甲基锌是相似的碱度的格氏试剂(并将被水很容易)。锌与氧形成强烈的联系,然而…
为什么这个resaction认为是亲核取代,而不是一个亲电取代吗?
取代反应,债券优惠和形式在相同的碳。反应物中含有碳称为“基质”。
在亲核取代,衬底与亲核试剂反应(如酒精)和一个新的切断债券形式和cx (carbon-halide)债券了。
还有一个叫亲电取代反应。在亲电取代,基质(如苯)和一个亲电试剂反应(例如Br +)导致形成C-Br债券和碳氢键的断裂。仍然替换,但由于衬底与亲电试剂反应,它被称为“亲电取代”。
还有这样一个东西作为自由基替换。
你好,
反应会如何改变如果我们有2-bromo-1-propanol和哈佛商业评论的反应吗?而不是仅仅丙醇吗?
不是最好的例子,因为我不确定这是一个非常稳定的化合物(它很容易就关闭形式一个环氧)但最终酒精仍将溴取代,得到1,2-dibromopropane。
2)-烷基shif,
是CH2失踪? ? ? ?
是的固定。谢谢!
感谢你投入大量的努力,将对我们的杰作。有机化学笔记一直帮助我,让超级有趣。
谢谢Sheetal。很高兴你找到有用的。
不好意思,图节(例2)有一个错误
是的,固定。谢谢你指出这一点。
我想问为什么我们用亲核取代卤代烷的形成而不是亲电吗?
优点是,替换是可以预见的。你知道carbon-nucleophile债券将形成碳轴承离去基团。相比之下,当执行亲电子除了在烯烃,区域选择性可能是一个问题。主要产品将取决于马氏的规则,甚至然后选择性可以坏(4:1)。anti-Markovnikov如果你想要什么产品?或者如果你有一个烯烃两端同样代替吗?这些问题不出现替换。
当观察的反应与HCl butan-2-ol生成2-chlorobutane和水,我们可以期望看到什么呢?还是不会有过激的反应?真的当叔醇与盐酸反应,这种物质变得更加浑浊的原发性醇,这种物质是浑浊的无色/低于二级或三级反应?或只属于卢卡斯试剂吗?
无水氯化烷基的优化选取用于制备从酒精和浓缩的。盐酸。为什么?
这是一个很好的路易斯酸,坐标和协助氧作为离去基团。
浓缩的。你好不是首选的制备烷基卤化物的酒精。为什么?
它* *在纸上工作,但是在实验室里,集中嗨(48%)是没有人的想法一个有趣的试剂。还有许多其他的方法。使用它们。
你好,我相信你有一个错误在烷基转移的照片。从第二到最后一步,最后你失去一个甲基,取而代之的是hi-lighted蓝色。
是的,固定。谢谢!
有必要使用优化选取盐酸的反应和醇制备卤代烃或我们可以简单的醇与盐酸反应制备烷基卤化物吗?为什么?
你在谈论卢卡斯测试。转换一个酒精烷基卤化物优化选取没有严格的要求,尽管这并加快反应。
我想我发现了一个错字。在例2),最后的结构应该有一个蓝色的甲基,而不是一个蓝色的H。
谢谢你伟大的一页!
是的。固定的。谢谢!
可以做环扩张环丁烷环己烷吗?有一个甲基转变是优于环扩张,例如当戒指变得非常大吗?
不可能直接从环丁烷环己烷,自从碳正离子会毗邻4元环和它总是包括1、2的转变。
当环应变不是问题(碳正离子在5、6、7元环)然后你可以有混合物的烷基转移和环扩张/收缩产品。
从酒精,使烷基卤化物HX使用。HX干燥和由NaX与硫酸反应或与H3PO4嗨的。为什么不使用NaX烷基卤化物直接将酒精吗?
因为哦——是一个可怕的离去基团相比,它的共轭酸(水)。
PKa HCl的价值小于H3O +。所以,Cl -比水仍是一个较弱的基础。你提到的老文章Sn2不能取代一个更强大的基础,一个较弱的基地。如何通过Sn2主要醇然后与盐酸反应吗? ?
好问题。
“弱基础不能取代一个更强大的基地”,作为一个经验法则,当pKa的差异大约是8或更高。当不同的是,会有一些平衡两个酸,然而小。
事实证明,氯离子实际上是优于水的亲核试剂,与卤代烃反应速度更快的速度。实际上,将水作为取代反应的副产物,这可能会导致一些小的可逆性。这可以通过添加一个相当于HCl过剩,将会使质子化水给H30 +(这当然是一个更穷的亲核试剂)。
嗨,詹姆斯!下一篇文章出来是什么时候?
我在想如何让anti-Markovnikov卤化物anti-Markovnikov酒精。谢谢你的帮助!
这正是一个情况下你想执行的亲核取代酒精与卤代烷的形成通过HX的烯烃。
好文章!你使用哪个软件进行分子结构呢?
ChemDraw。大多数教育机构有一个网站许可证