消除反应
E1的反应
最后更新:2023年2月7日|
的E1反应,三个关键的证据和机制
最后一次在这介绍消除反应,我们讨论过两种类型的消除反应。在这篇文章中,我们将挖一点更深的一种消去反应基于实验告诉我们,想出了一个假说,它是如何工作的。
表的内容
- 我们如何解释发生了什么在这个消去反应(我们将称之为“E1”)
- 第一个线索的机制“E1消除”:速度只取决于基质的浓度(不是基地)
- 第二个线索关于E1消除反应的机制为三级基质——速度是最快的
- 第三个线索关于E1消除反应的机制:竞争的年代N1反应
- 把它在一起:E1机制通过损失离去基团,然后去质子化
- 笔记
- (高级)引用和进一步阅读
1。我们如何解释发生了什么在这个消去反应(我们将称之为“E1”)
这是反应。首先,看看债券形成和破碎。这是一个经典的消去反应-我们形成新的碳碳(π)键,打破碳氢键和C -离去基团(Br)债券。
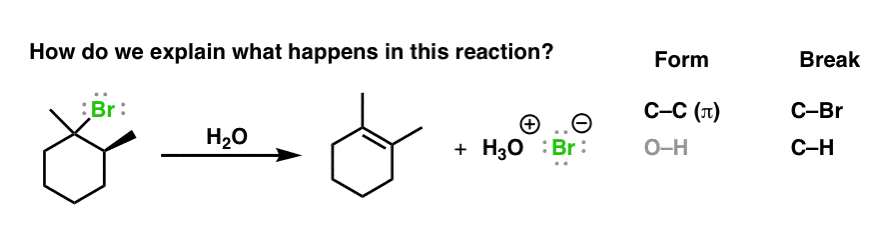
但是现在我们想要知道的不仅仅是“发生了什么”。我们想知道如何它会发生。bond-forming和债券打破的顺序是什么?以了解它是如何发生,我们需要看看数据告诉我们。
因为化学是一门实验科学;我们看一下证据,然后向后工作。
2。第一个线索的机制“E1消除”:速度只取决于基质的浓度(不是基地)
让我们看看第一个反应的重要线索。我们可以测量反应率相当容易。当我们改变底物的浓度,反应速率相应增加。换句话说,有一个“阶”依赖率底物的浓度。
然而,如果我们改变碱的浓度(H2O)反应的速度不会改变。
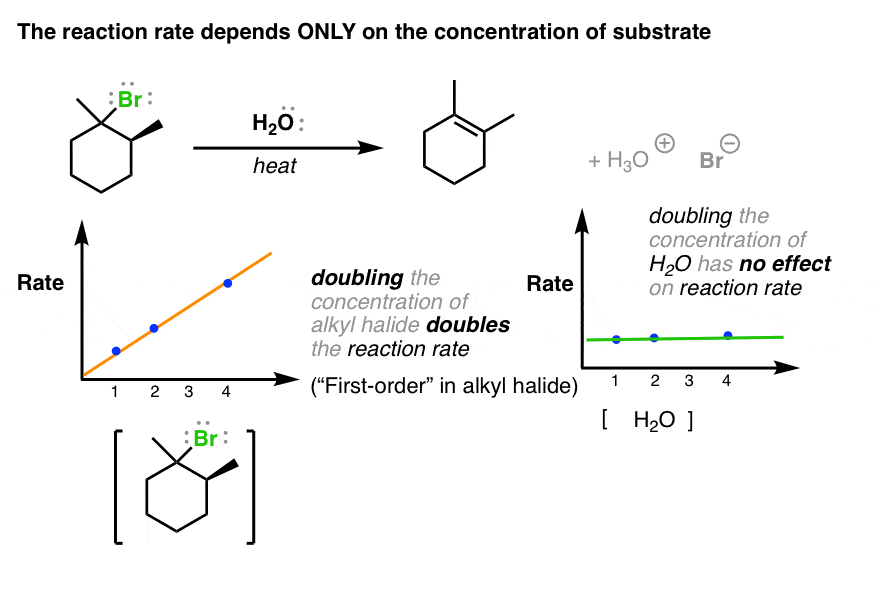
从这里我们可以推断出什么信息?这个反应的速率决定步骤因此(不管是什么)不涉及到基础。无论它是什么机制的,我们画将必须考虑到这一事实。
的反应是一阶在底物(烷基卤),零阶在基地(即双倍浓度不率的两倍)。
3所示。第二个线索的机制E1 -消除反应三级基质的速度是最快的
另一个有趣的证据我们可以获得这个反应是通过改变类型衬底,测量结果的速率常数。如果我们把简单的烷基卤化物左边(下图),碳与Br也连着3个碳(这被称为三级烷基卤),速度是快于中间烷基卤化物(二次烷基卤),这本身就是比一个快主烷基卤化物(附加到只有一个碳除了Br)。(看到帖子:一级,二级,三级)
因此,利率收益的顺序三级(最快)>二级> >主(慢)
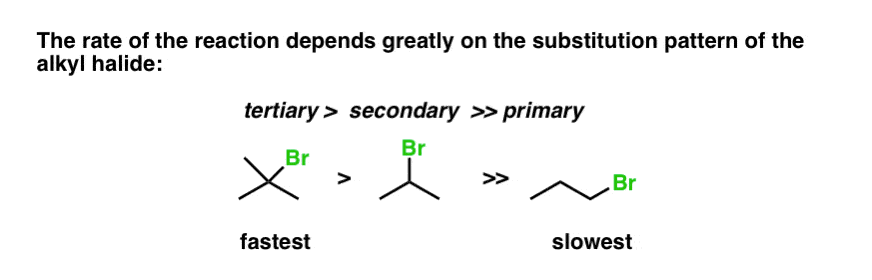
任何机制我们画这个反应同样要占这个事实。可能是怎么回事,三级基质比主吗?
4所示。第三个线索关于E1消除反应的机制:竞争的年代N1反应
最后一个有趣的线索对这个反应的机制问题往往得到的副产品。例如,当烷基卤化物下面是受到这些反应条件,我bdapp平台们做获得预期的淘汰产品。
然而,我们也会替换反应在产品组合。记住——替换C -反应涉及破损(离去基团)和C -形成(亲核试剂)。
是什么东西让这种特殊开始烷基卤化物特别有趣的是,碳与Br是一个异构中心。如果我们从单一对映体的起始物料,我们注意,形成的替代产品是一个立体异构体的混合物。注意,两种反演和保留的立体化学异构中心发生。
我们之前看过这个模式——这是一个年代N1反应!(见文章:SN1反应)
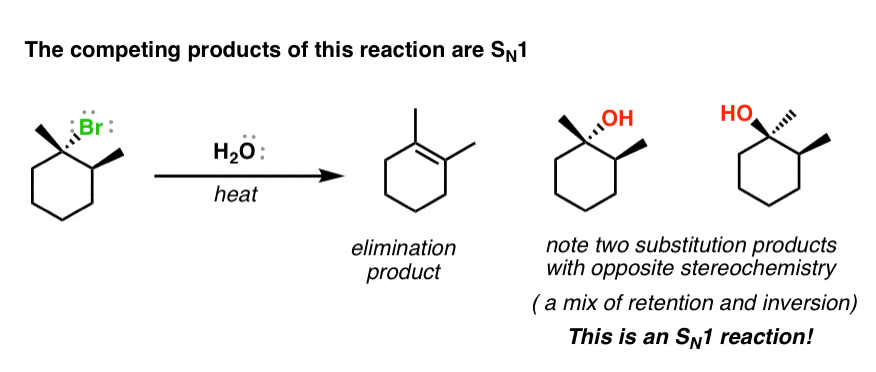
最后一个部分是一个非常重要的线索。如果一个年代N1反应是发生在反应混合物,回顾机制的年代N1可以帮助我们思考什么样的机制可能是在这种情况下给我们消除产品。
5。把它在一起:E1机制通过损失离去基团,然后去质子化
考虑到所有这些线索,解释所发生的最好的方法是什么?这样的:
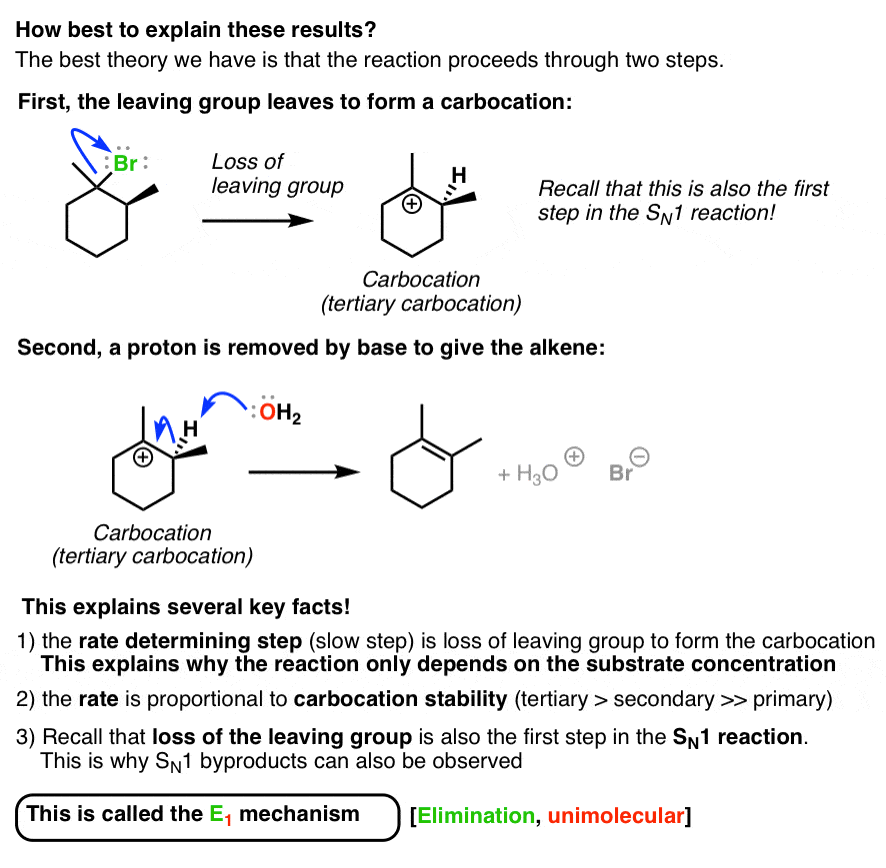
提出的反应是发生在两个步骤:首先,离去基团叶子,形成碳正离子。第二,基本消除了一个质子,形成了烯烃。这很好地符合上述三个线索。(还要注意,代替烯烃形成,之后扎伊采夫规则]。
类似于年代N1机制,这被称为E1机制(单分子的消除)。
所以在其他类型的发生了什么消去反应吗?下一篇文章的主题!
笔记
(高级)引用和进一步阅读
- 消除反应的机制桑德斯和Cockerill,1973年,p . 210。
这本书说,“有三个主要因素,有利E1机制:提供一个相对稳定的碳正离子的衬底,电离溶剂,缺乏强有力的基地或亲核试剂”。 - 二、三级的水解烷基卤化物
爱德华·d·休斯
美国化学学会杂志》上1935年,57(4),708 - 709
DOI:10.1021 / ja01307a033
早期的论文,可能第一篇论文特性术语“E1”。本文还指出,E1反应竞争的年代N1反应数基质。 - 单分子的消除和电导的意义,外消旋化和卤素取代有机卤化物的解决方案。
休斯,E。,INGOLD, C. & SCOTT, A.
自然1936年,138年,120 - 121
DOI:1038/138120b0
本文介绍了导电性实验三级和二级基质2HCl的支持E1机制。 - 在消除离子对
Cocivera和美国Winstein
美国化学学会杂志》上1963年,85年(11),1702 - 1703
DOI:10.1021 / ja00894a046
在不同高度极性和溶剂(比如水醇)碳正离子相对“自由”的数量烯烃产品的性质无关离去基团。摘要教授Winstein表明,在极性溶剂少,碳正离子是更少的“免费”和紧形成离子对。因此消除/替换比率可以强烈依赖的碱度离去基团。这里的关键发现是更基本的离开团体(Cl - Br)导致更多E1产品比基本离开组(I - S (CH3) 2)。此外,的比例E1产品在极性溶剂中高于分离溶剂。 - 消除反应的机制。部分x动力学烯烃消除从异丙基、sec.-butyl 2-n-amyl, 3-n-amyl陈词滥调在酸性和碱性酒精媒体
m·l·达·e·d·休斯和c·k·英格尔德
j .化学。Soc。1948年,2058 - 2065
DOI:10.1039 / JR9480002058
表III摘要显示辅助底物通常是可怜的基质E1反应,收益率从4.7%到17.4%不等。 - 消除反应的机制。八世。温度影响利率和product-proportions uni - bi-molecular替换和消除反应烷基卤化物和hydroxylic锍盐溶剂
k·a·库珀·e·d·休斯,c·k·英格尔德,b . j . MacNulty
j .化学。Soc。1948年,2049 - 2054
DOI:10.1039 / JR9480002049
如何消除温度效应/替换比率,英格尔德:“[. .]对于任何给定的同时有两个分子的过程,消除了在每个调查的情况下,一个阿伦尼乌斯的能量激活位于陪同替换高于1 - 2千卡/ g.-mol。消除因此一直较大的温度系数,所以温度的上升会增加的比例烯烃形成。”
这些文章是如此惊人。谢谢你这么多!
好的,很高兴你发现它们有用Minnoli !
可以这样E2反应的结果只有一个产品(vs主要和次要的产品)?如果是这样,这是怎么做的?
E2 -当然,因为它是由立体化学控制。一个很好的例子是在某些取代环己烷反氢只有一个位置(反式)离去基团。
E1(这篇文章的主题),最好的情况是,只有一个烯烃作为一个产品。例如C6H5-CH的E1反应(OH)甲基只会给一个烯烃。
否则,选择性是由烯烃之间稳定的差异,因为通常很小,70:30或80:20比率是常见的。
很棒的解释,到目前为止最好的笔记我曾经reffered有机化学。我很高兴我发现你的网站。非常感谢先生。
你好,詹姆斯,
伟大的工作。
你有了工作,它必须是。大部分的书用相反的方式。他们处理机制,然后支持它的反应。
困扰我的一件事是这些反应的名称。消除E1的反应称为单分子或消除一阶?
我喜欢首先提出证据和机制,就像解决一个谜。再保险:你的问题,我不认为这很重要。它只是E1机制。
在chlorocyclopropane chlorocyclobutane &chlorocyclopentane经历Sn1反应最快哪一个,为什么?
这是一个很好的考试问题!我邀请你去特殊焊接环丙烷环丁烷和推理出答案是否碳正离子会或多或少稳定在一个三人环或5环。
感谢你非常全面的解释我认为是一个复杂的机制。但是你对我使它容易得多。使用你的网站作为我的大多数有机化学考试的参考。:)谢谢! ! !
我真的不明白为什么替代产品也作为一个副产品。如果我们没有手性中心的分子?将相同的发生?请解决我的疑问和说明。谢谢你解释机制。你真的太棒了!
有一个中间的碳正离子可以接受命运。的命运是消除。另一种可能性是替换。加热时,一些替代产品将恢复到碳正离子中间体进行消除,导致这些替代产品,以消除产品的转换。
感谢你花时间来创建这些简单,容易理解,文章简洁轮廓手头的主题。bdapp平台真的,你帮助我很多我现在多教授。这些文章被无价的间距我有机化学期中考试。再次感谢,你美好的人类!
伟大的文章,它真的很有用!
一个问题,为什么水能够删除的H周期?
谢谢
弱碱水和氧气的孤对形式与H +新债券。碳氢键的孤对形成一个新的π键。
先生,如果我们使用哦,而不是H2O E1反应之后会发生什么
E2,最有可能。
由于-哦是强碱,对吧?
是的,因为HO -是一种强碱,它将E2途径而不是E1通道。
先生,
消除1-chlorobutane将给1-butene或2-butene吗?
谢谢你!
消除会删除一个质子的碳直接相邻的离去基团,所以C2。最初的产品是1-butene。
谢谢发布这些博客! !:):)这是真的帮助我真的学习和享受有机化学! !继续做这个,更多的人会喜欢这个主题的美丽。bdapp平台再次感谢! !