胺
保护组胺-氨基甲酸盐
最后更新:2023年2月9日|
保护组胺
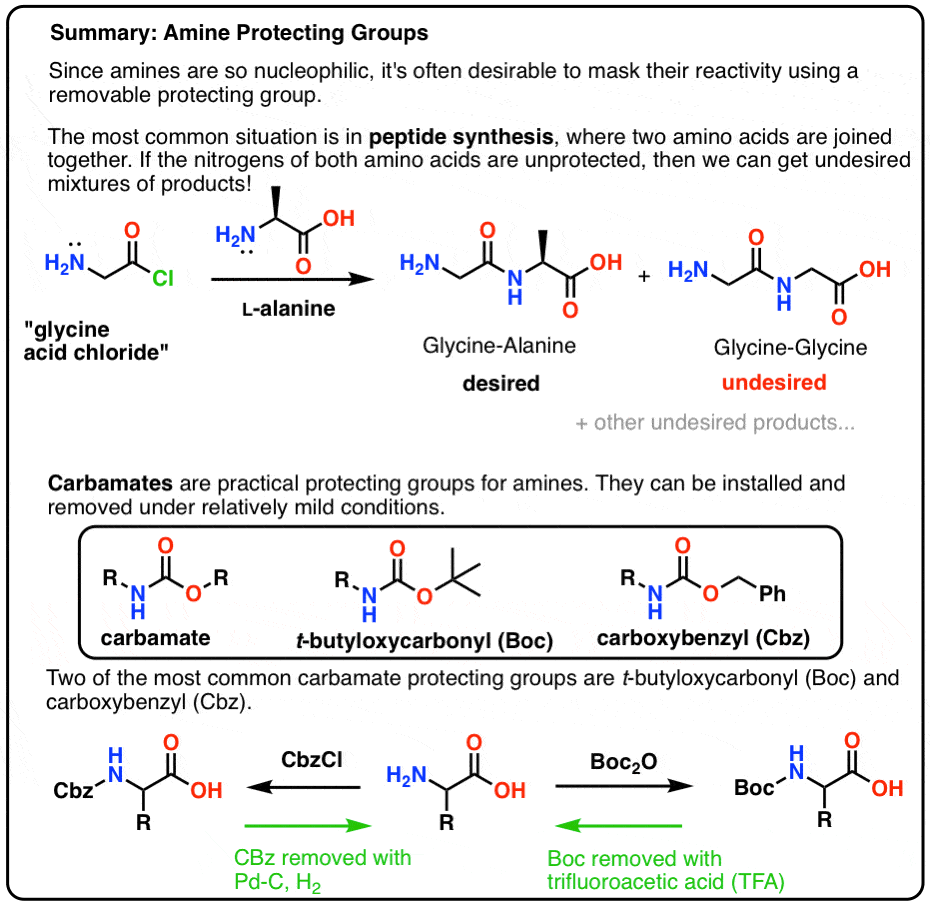
- 胺保护组织的合成至关重要肽。
- 氨基甲酸盐是有用的保护组织胺。他们可以在相对温和的条件下被安装和移除。
- 最常见的一种氨基甲酸酯保护组织是t-butyloxycarbonyl (中行)保护组。它可以删除与强酸(三氟乙酸)或热量。
- carboxybenzyl (卡马西平)集团苄可以删除组和使用催化加氢(Pd-C H2)
- fluorenylmethoxy (FMoc)集团与一个可以删除胺基础(如。R2NH)
- 如果存在多个保护组在相同的分子,它是有用的选择,这样他们可以被删除不同的条件(如酸性,碱性,加氢)。(我们有时使用“正交”这个词来形容这个属性)。
表的内容
- 介绍简单的肽合成
- 让我们混淆了一批Gly-Ala
- 一个非常糟糕的初步计划
- “听!这是什么垃圾?”
- NH的防护帽2
- 伴侣!用氨基甲酸酯,伴侣!
- 中行和卡马西平是蜜蜂的膝盖
- 安装和拆除的“中行”保护组
- 安装和拆除的卡马西平(或“Z”)氨基甲酸酯保护组
- 一个简单的肽合成使用氨基甲酸酯保护组
- 它会继续…
- 笔记
- (高级)引用和进一步阅读
1。介绍简单的肽合成
在最近一篇文章中(酰胺:合成、属性和术语我们经历了三酰胺的常用方法:
失踪的那篇文章是任何提及最有用的老老前辈酰胺合成人类已知的联系,我的意思吗肽。
一个肽键是我们给两种氨基酸的酰胺键连接在一起。
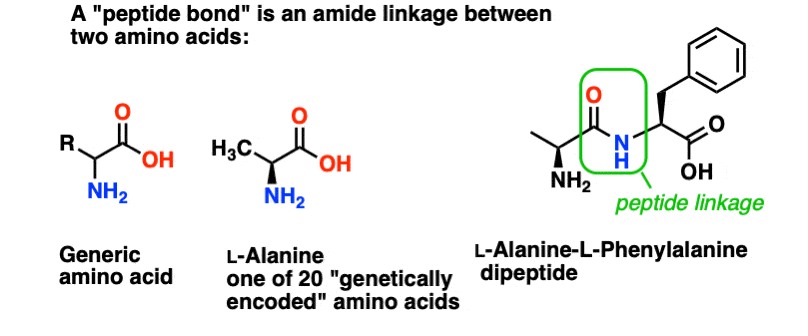
和氨基酸是重要的,因为…等。你已经知道为什么氨基酸是重要的,对吧?如果你现在不知道,阅读本文后回来。
2。让我们混淆了一批Gly-Ala
让我们试着申请我们的一些新发现的酰胺合成skillz试图建立一个真的简单的二肽,glycine-alanine。如果我们现在可以构建一个简单的二肽,我们可以用学习更复杂的我们学会了展示肽是由在后面的帖子。(看到帖子:介绍多肽合成你知道诺贝尔奖得主布鲁斯·梅里菲尔德合成胰岛素通过加入一个氨基酸在一起吗?是的,真的。
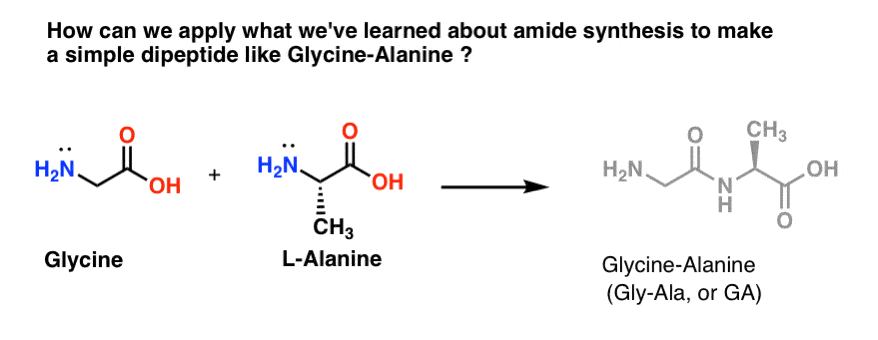
我们列出的三种方法进行酰胺,只有两个可能有助于形成肽键:1)酰氯的方法,或2)通过偶联剂合成DCC。(水解腈只提供主要的酰胺,R-CONH2多肽合成的,所以它不是一个选择。
3所示。一个非常糟糕的初步计划
我们第一次尝试多肽合成将涉及滚磨提出一个很天真的进攻计划,希望一切顺利。挂在人,因为它会变得混乱。
我们首先提出酸性氯化物的方法(或者是Schotten-Baumann反应,如果你喜欢合成Gly-Ala]。
向后看Gly-Ala二肽,我们的计划将会我们合成肽键通过丙氨酸与酰氯的反应来自甘氨酸:
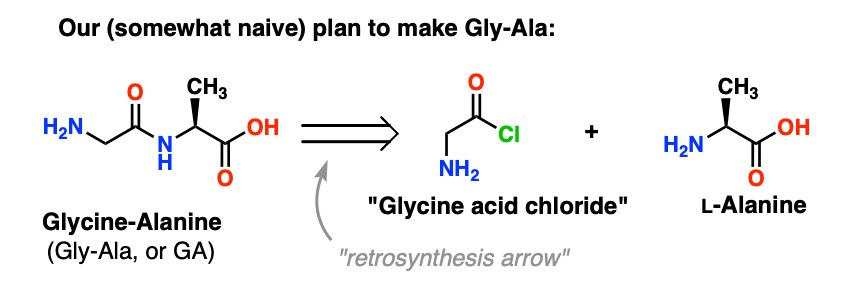
这个计划有一个轻微的问题。可能有点难发现。
让我们假设我们已经取得了甘氨酸*的酸性氯化物注1,我们有“甘氨酸酰氯和丙氨酸在同一瓶,还有一些多余的基地,以加快进程。(注2,省略了一个小细节re:氨基酸的两性离子性质)
我们将按正向的反应:
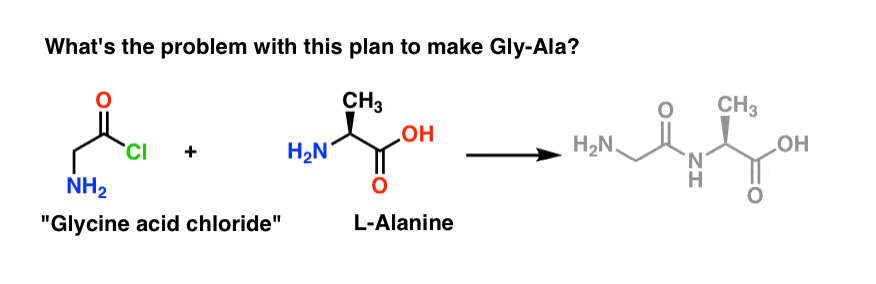
什么可能出错?
4所示。“听!这是什么垃圾?”
我们的计划是让甘氨酸的酸性氯化物溶液(相当于1 mol / l),然后拥有它耐心地等待在长颈瓶直到我们添加了一个摩尔相当于丙氨酸,于是将与亲核NH反应2丙氨酸。
我们的计划的问题是,我们没有处理的单分子“甘氨酸酰氯”——我们正在处理一些摩尔(6.02 x 1023分子)。和甘氨酸的酸性氯化物已经有一个亲核的NH2集团!
“甘氨酸酰氯”,不是一个稳定的分子,因为它可以反应本身。
这意味着,甘氨酸溶液酸性氯化物留给自己的设备将形成一个聚合物的甘氨酸,结构Gly-Gly-Gly-Gly…
甚至甘氨酸溶液酸氯丙氨酸的存在不仅会形成所需的Gly-Ala,而且Gly-Gly(附呈酰卤),可以继续执行更淘气亲核试剂,无论是g或者阿拉巴马州:
(不,没有区分北半球2“甘氨酸酰氯”从北半球2丙氨酸。他们同样反应。)
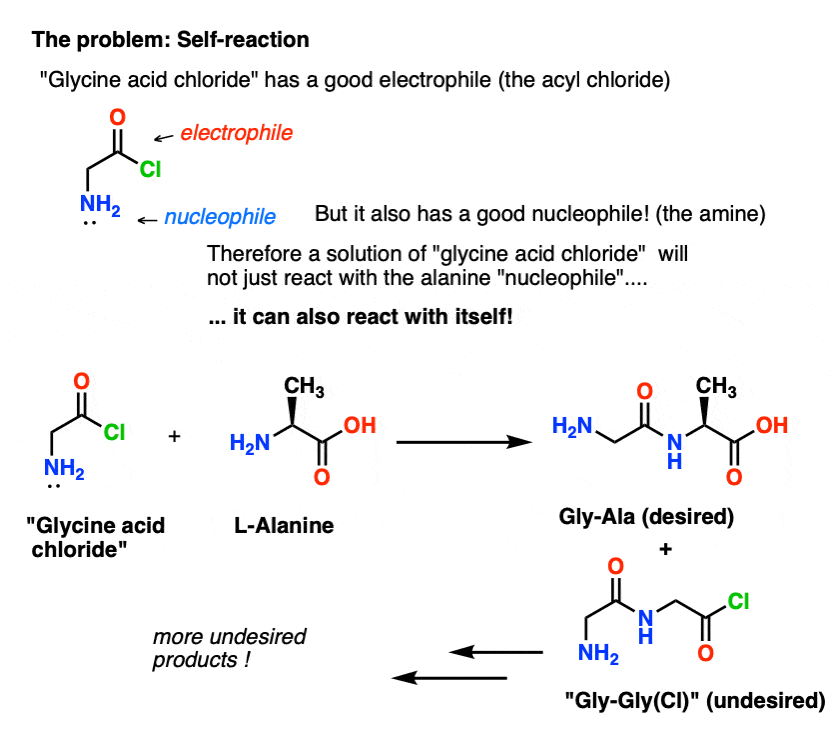
这里的教训是,当你有一个解决方案的一个分子包含一个亲核试剂和一个亲电试剂,它可以self-react。这个过程有一个名称,可能听起来很熟悉:聚合。
那么我们如何阻止这事发生吗?
5。NH的防护帽2
最好的方法是“帽”氮在某种程度上保护组(PG)使北半球2non-nucleophilic组。它还应该有以下属性:
- 轻松且有选择地安装
- 惰性到所需的反应条件(例如SOCl会2的酸性氯化物羧酸)
- 轻松且有选择地删除而不影响最终产品
这就是一个保护组织战略为我们合成的“Gly-Gly”的样子。我们安装一个保护组织(PG)甘氨酸,然后使酸性氯化物。PG应该选择如呈现氮non-nucleophilic(即它不会与酰氯反应)。
我们可以形成和未受保护的丙氨酸肽键,然后删除PG在温和的条件下。
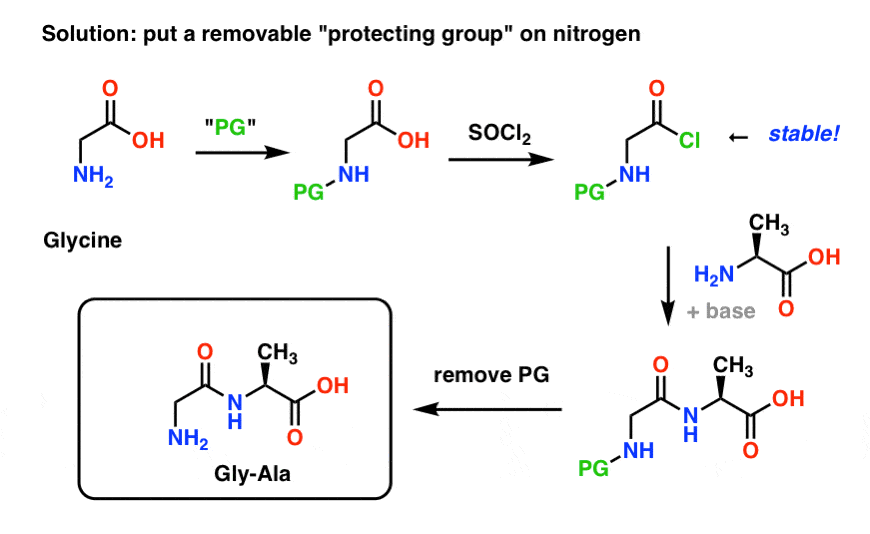
一个保护组织战略氮我们已经探索加布里埃尔合成使用phthalimide(你可以把phthalimide氮气保护)。这实际上已被用于合成Gly-Gly (“glycylglycine”)注2]!的问题之一,然而,相对恶劣的条件(充足的热量)都需要安装和删除phthalimide集团,这不是一个非常健康的生存环境敏感,很容易使外消旋手性氨基酸。
另一个潜在的选择是保护氮酰胺,但解理酰胺需要严厉的条件。此外,由于我们正在努力打造一个酰胺键(肽)无论如何,我们可能会选择性的问题删除——摧毁了村庄为了保存它。(注3]
6。伴侣!用氨基甲酸酯,伴侣!
最受欢迎的选择保护小组胺氮是氨基甲酸酯官能团。一个氨基甲酸酯看起来像的私生子酯酰胺、N和O侧翼羰基。
的氮氨基甲酸酯相对non-nucleophilic,此外,氨基甲酸盐:
- 很容易安装在氮
- 惰性的各种反应条件
- 轻松地删除不影响现有酰胺组
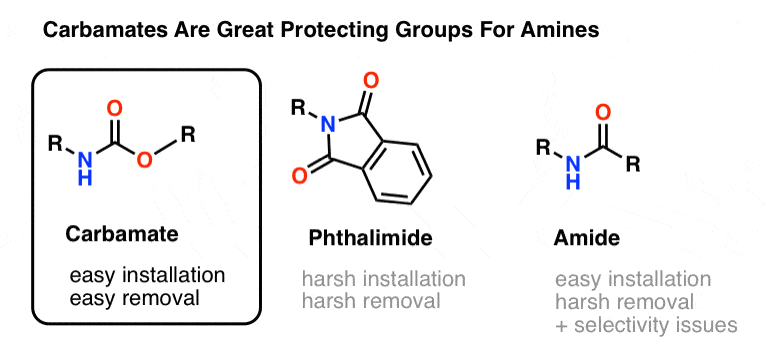
这使得它们适合我们的目的。
7所示。中行和卡马西平是蜜蜂的膝盖
两个受欢迎的氨基甲酸酯保护组织中行(t-Butyloxycarbonyl)和卡马西平(carboxybenzyl)。
就我们的目的而言,这两个保护团体或多或少可以被认为是等价的,是可以有效地用于多肽合成。
关键的区别是如何删除(即“去”的步骤)。选择一个或另一个成为至关重要的一旦你复杂的分子与多个保护组;这属于“先进的合成策略”的范畴,这是更多的主题组织3。bdapp平台(注意4]
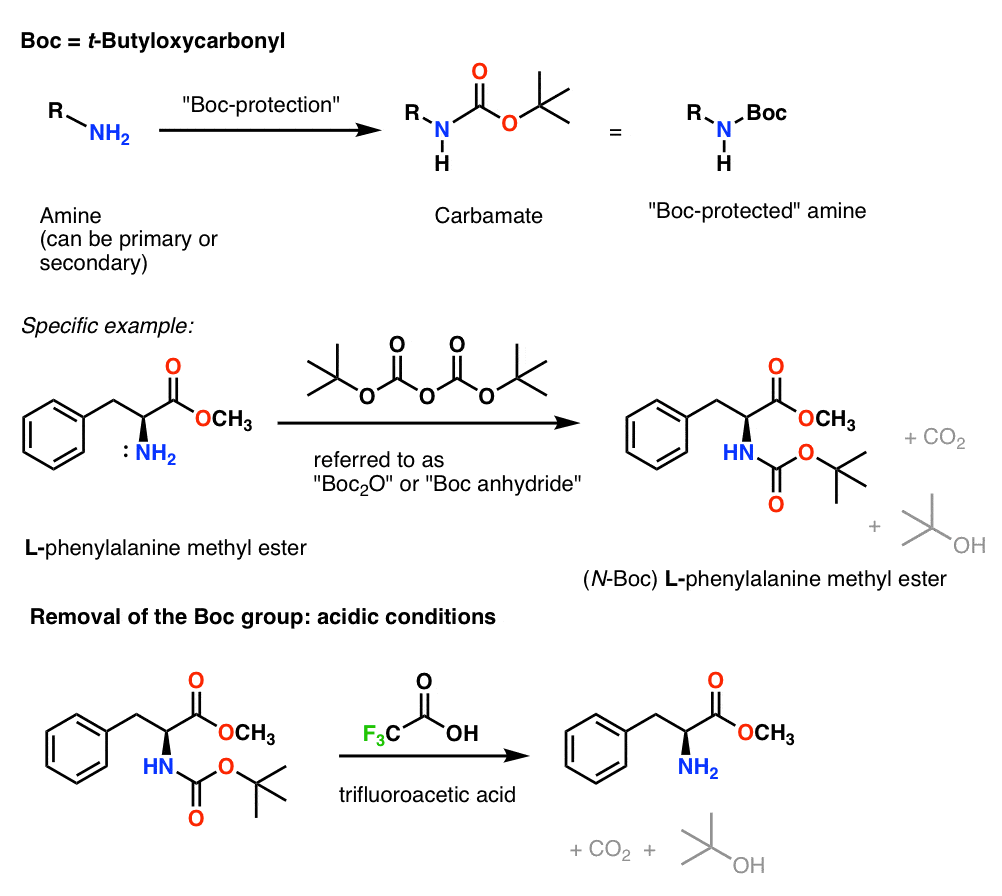
8。安装和拆除的“中行”保护组
与“中国银行中银集团通常是安装2O”(有时称为“中行酐”),并与酸被移除。通常的选择是“整洁”(即未稀释的)三氟乙酸(组织),弹出的中银集团非常干净,解放有限公司2和t丁酒精。
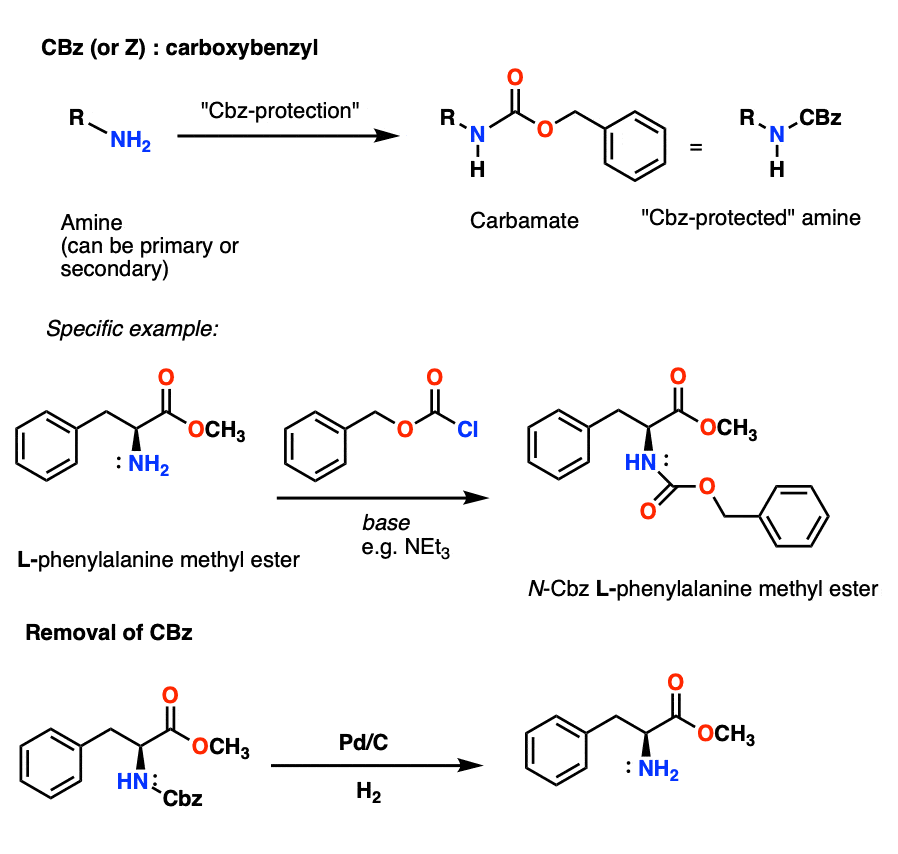
9。安装和拆除的卡马西平(或“Z”)氨基甲酸酯保护组
卡马西平组(有时进一步缩写为“Z”)可以安装CbzCl和温和的基础,通过催化氢化作用,通常删除(Pd-C / H2)。这是极其温和,在中性pH值的优势,使酸或独自base-sensitive官能团。
10。一个简单的肽合成使用氨基甲酸酯保护组
让我们回到多肽合成和应用这个保护Gly-Ala集团战略。
我们开始像丙氨酸的氨基酸。治疗与中行丙氨酸2啊,我们获得N-Boc丙氨酸保护。下一步是使用SOCl会形成酸性氯化物2。一旦形成,然后加入我们胺(例如L-valine)存在过剩的基地,形成关键酰胺键。最后一步给二肽是deprotect Boc-protected胺与三氟乙酸(组织)瞧!我们有二肽。
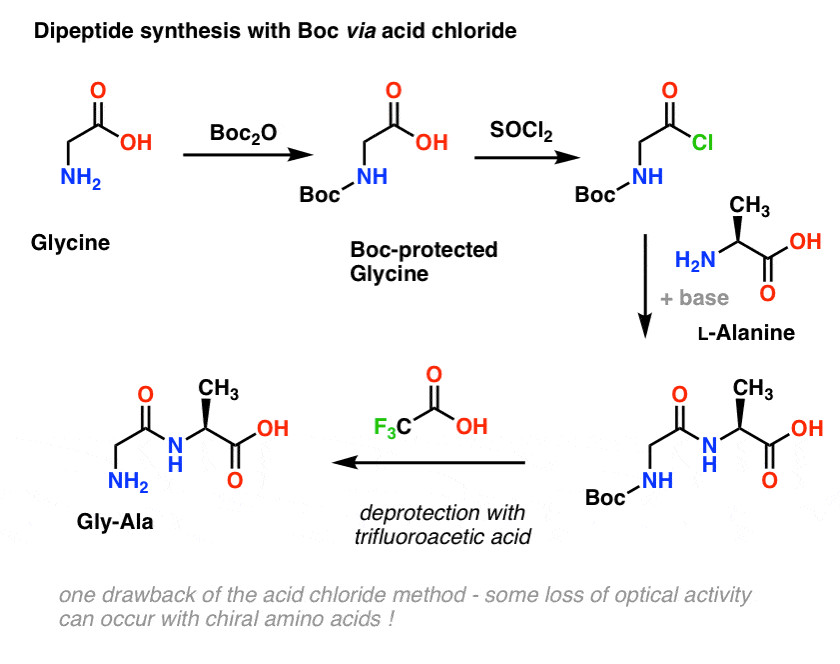
虽然这种方法可能好的纸上,在实践中使用酸性氯化物的一个问题是,手性氨基酸经常失去光学纯度通过这种方法,这一过程有时被称为“外消旋化”,但更正确地称为“差向异构化作用”(技术上更正确的,因为一个氢在一个手性中心倒)
由于手性氨基酸的生物功能是至关重要的,稍微温和的普遍使用,雇佣协议DCC或类似的耦合剂。
在这里,我们对待Boc-protected甘氨酸DCC激活羧酸。然后,我们把我们的氨基酸亲核试剂(丙氨酸),形成了二肽。如果我们想要隔离Gly-Ala二肽在这一点上,我们可以删除与组织中银集团。
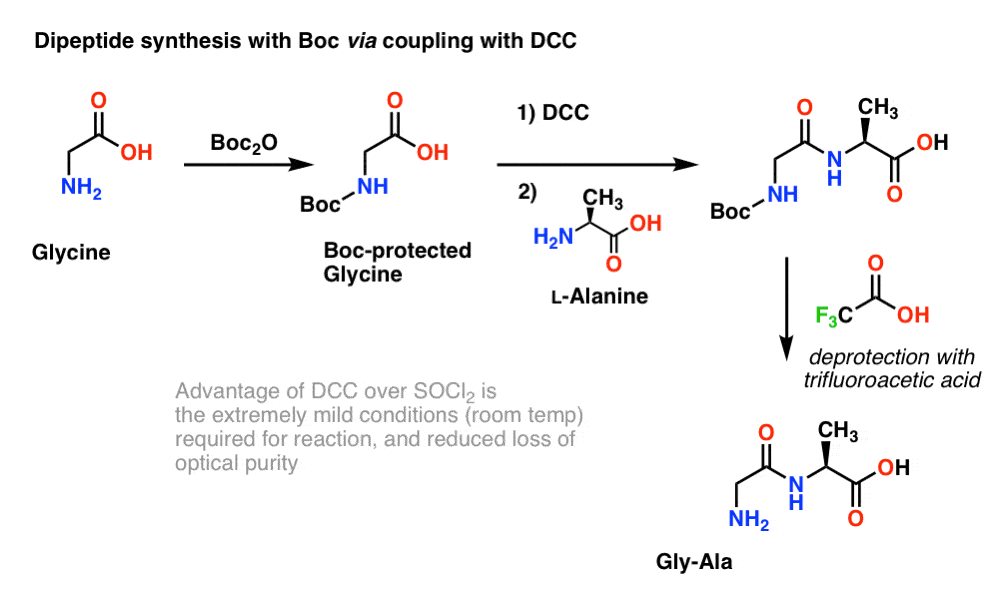
(注5关于这个方案)
11。它会继续…
请注意,如果我们想做一个tri-peptide,我们可以继续执行周期的增加DCC(激活羧酸)其次是添加新的氨基酸,肽建设一个单位在一个时间!
有一个特别有效的方法来构建长肽由布鲁斯·梅里菲尔德(在胰岛素的合成和应用等)称为固相肽合成,下次我们将会介绍我们关于这个主题。
笔记
“假设我们有一个船”。
甘氨酸(像所有氨基酸)本身就是一个两性离子。治疗与SOCl会甘氨酸2应产生酸性氯化物的质子化了的胺。这应该是相对稳定的解决方案,只要没有基地补充道。
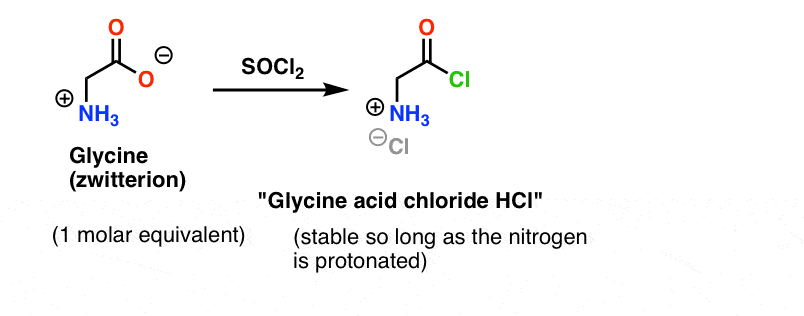
问题就在这里。因为我们的氨基酸亲核试剂(丙氨酸)也两性离子会发生,没有反应,直到多余的基地被添加到解放丙氨酸氮上的孤对。的基础后,我们有“甘氨酸酰氯和丙氨酸在一起的解决方案。没有明显的差异亲核性这两个物种的铵离子之间,每个人都将竞争与酰氯反应亲核试剂,导致的混合Gly-Ala Gly-GlyCl,然后Gly-GlyCl可以进一步与预设的各种亲核试剂反应在溶液中三,四和更高的肽。
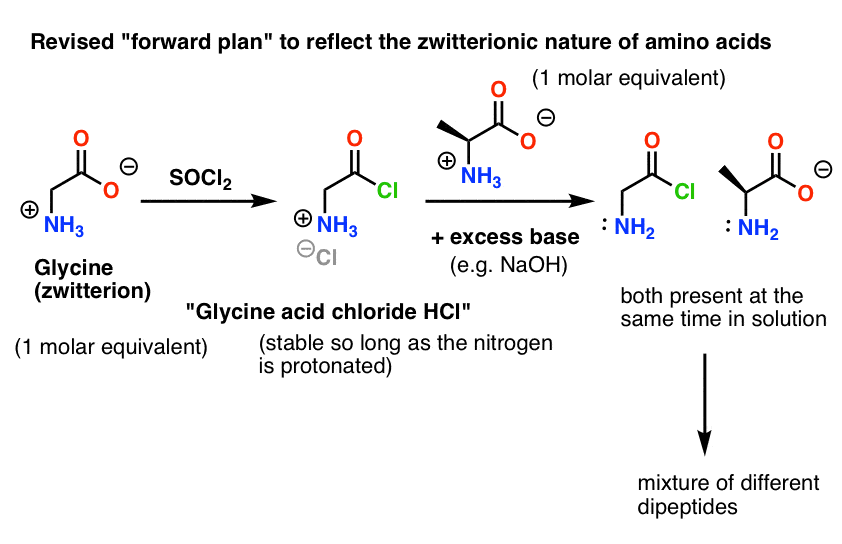
注2。约翰·希恩,我们见面早些时候的发明者DCC途中第一个合成青霉素,也使得phthalyl-protected Gly-Gly通过加布里埃尔合成:
注3。使用酰胺保护组的另一个问题是吖内酯的形成,从而导致差向异构化的手性氨基酸。也看到这个问题集。
注4。”正交保护组织”。在综合规划通常是至关重要的保护组明显不同条件下移动。这个属性通常被称为“正交性”
例如在接下来的二肽,我们有两个不同的氮保护组织——一个银行和一个卡马西平。通过选择“正交”保护组,每个氮可寻址——我们可以选择删除保护集团,和我们的合成可以从那里。这避免了进入一种情况我们有两个不受保护的胺,必须依靠一个比另一个更被动。这些方法很少工作!
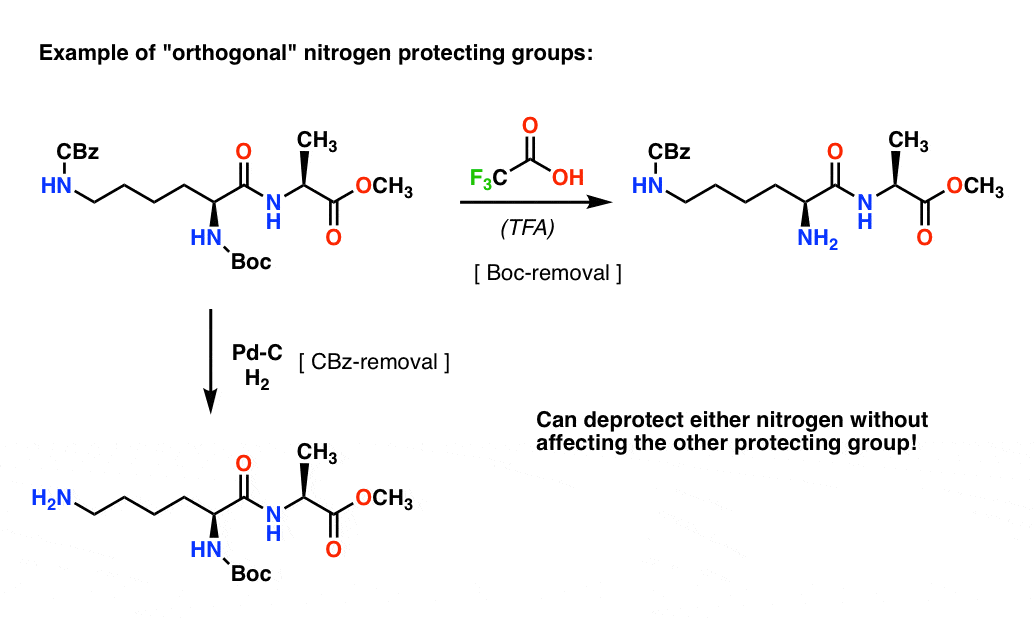
注5。注意,这里为了简单起见丙氨酸与自由描绘羧酸,但稍微更好的方法是使用甲基酯丙氨酸,以避免任何自耦之间的自由胺丙氨酸和自由羧酸。
(高级)引用和进一步阅读
氨基甲酸盐是有用的保护组织胺,最常见的是中行,卡马西平,-Fmoc。
- 乳房静脉《德国埃森der缩氨酸的合成
马克斯·伯格曼和列奥尼达Zervas
的误码率。1932年,65年(7),1192 - 1201
DOI:10.1002 / cber.19320650722
首次使用卡马西平(carboxybenzyl)保护集团1932年由马克斯·伯格曼和列奥尼达Zervas肽的合成,和有时缩写“- z”是为了纪念Zervas。 - 删除t丁和t BUTOXYCARBONYL保护组与三氟乙酸
机制,Biproduct拾荒者的形成和评价
Behrend f . Lundt尼尔斯·l·约翰森梅Vølund, Jan Markussen
j . Pept。普罗特。Res。1978年,12(5),258 - 268
DOI:10.1111 / j.1399-3011.1978.tb02896.x
在实践中,亲核食腐动物(如硫醇)通常添加到酸鸡尾酒deprotecting时(组织),因为去中行会给亲电叔丁基物种(如叔丁基三氟醋酸盐),可以与敏感反应残留物(例如Trp或半胱氨酸)。 - 长肽链合成的方法使用催产素的合成为例
杜米Bodanszky和文森特Vigneaud
美国化学学会杂志》上1959年,81年(21),5688 - 5691
DOI:1021 / ja01530a040
上半年的20倍th世纪,多肽合成技术是使用标准有机化学解决方案完成阶段。这是现在被称为牧民联盟(液相多肽合成)。du Vigneaud获得了1955年诺贝尔化学奖的作品表明,肽合成可以实现,使用正确的保护组织和合成策略的选择。 - 临时吖内酯环的外消旋化的形成与乙酸酐酰氨基酸衍生品
文森特·杜Vigneaud和柯蒂斯·e·迈耶
生物。化学。1932年,99年:143 - 151
DOI:10.1016 / s0021 - 9258 (18) 76075 - 4
使用酰胺保护组的另一个问题是吖内酯的形成,从而导致差向异构化的手性氨基酸。 - 肽的新的合成路线
约翰·c·希恩和维克多弗兰克
美国化学学会杂志》上1949年,71年(5),1856 - 1861
DOI:10.1021 / ja01173a095
约翰•希恩的发明者DCC在第一青霉素的合成路线,也使得phthalyl-protected Gly-Gly加布里埃尔合成。 - 一个新的形成肽键的方法
约翰·c·希恩和乔治·p·赫斯
美国化学学会杂志》上1955年,77年(4),1067 - 1068
DOI:1021 / ja01609a099
原始论文的合成肽债券/酰胺键使用DCC。 - 9-Fluorenylmethoxycarbonyl函数,一个新的base-sensitive amino-protecting组
路易斯·a . Carpino y和优雅
美国化学学会杂志》上1970年,92年(19),5748 - 5749
DOI:10.1021 / ja00722a043 - 9-Fluorenylmethoxycarbonyl amino-protecting集团
路易斯·a . Carpino y和优雅
《有机化学》杂志上1972年37(22),3404 - 3409
DOI:10.1021 / jo00795a005
-Fmoc保护小组的发现和开发胺增加了另一层正交性胺保护和去保护策略。-Fmoc集团基础不稳定,在多肽合成与哌啶20%通常是删除DMF。卡马西平是被加氢,中行进行脱酸,-Fmoc基地。
你好,
我注意到的立体化学苯丙氨酸在第一个二肽是错误的。
谢谢你的网络。
鲁本
非常感谢这个模块,超级有帮助!我想知道这些程序需要修改在处理涉及一种氨基酸的肽键的合成赖氨酸,有NH2组可以作为亲核试剂。有第二保护集团,需要添加,防止副反应羰基的亲核侧基之间的氨基酸?谢谢!
是的佐伊,绝对有。单独一个需要保护的赖氨酸氮,和理想情况下能够deprotect赖氨酸氮条件下,离开其他氮。官能团,可以删除,而不影响其他现有保护组织“正交”,从几何使用类比。这就是为什么大量的保护组织已经开发出来。
例如一个可以使用苄基保护组(:苄基)赖氨酸氮和删除它Pd-C / H2而不影响任何中行或FMOC保护组。人能deprotect FMOC与基地(哌啶)而不影响其他两个,或删除中行与强酸(组织)。
这回答了你的问题吗?詹姆斯
正交保护组,怎么可能来保护一个氮离开其他保护然后保护与一个不同的组。和你如何选择是否使用中行或卡马西平吗?
谢谢你!
通常的方法是保护氮(s)之前把他们一起在同一个分子。如果你在一个情景,在这个情景中你有两个化学类似胺,不得不选择性保护,这是一个规划问题。有很多变量取决于分子的细节,但几乎总是有方法!
无论你使用中行或卡马西平取决于其他官能团的分子。所需的酸中行去有时可以影响敏感的官能团的分子;卡马西平去温和得多。它会更容易给你更具体的答案如果你给我一个具体的问题。
如何保护谷氨酰胺侧链的简单和温和的保护组physilogical条件下没有变性蛋白质吗?
我不知道。我知道任何计划deprotecting谷氨酰胺sidechain体内。
为什么组织去保护步骤是最好的吗?其他酸呢?它需要非常低的pH值上班吗?谢谢
其他酸工作,比如冒泡盐酸气体通过解决方案。然而使用整洁(即未稀释的)组织是这样一个干净的反应,这通常是第一选择。你可以溶解你的反应物在dicholoromethane搅了,开瓶,走出一个吸管,降低整洁的组织方案,等待冒泡停止(异丁烯的副产品,即2-methyl-propene)和反应。这是非常容易做到。