羧酸衍生物
氢化铝锂(LiAlH4)减少羧酸衍生物
最后更新:2023年7月5日|
氢化铝锂(啦﹐LiAlH4为减少)羧酸衍生品
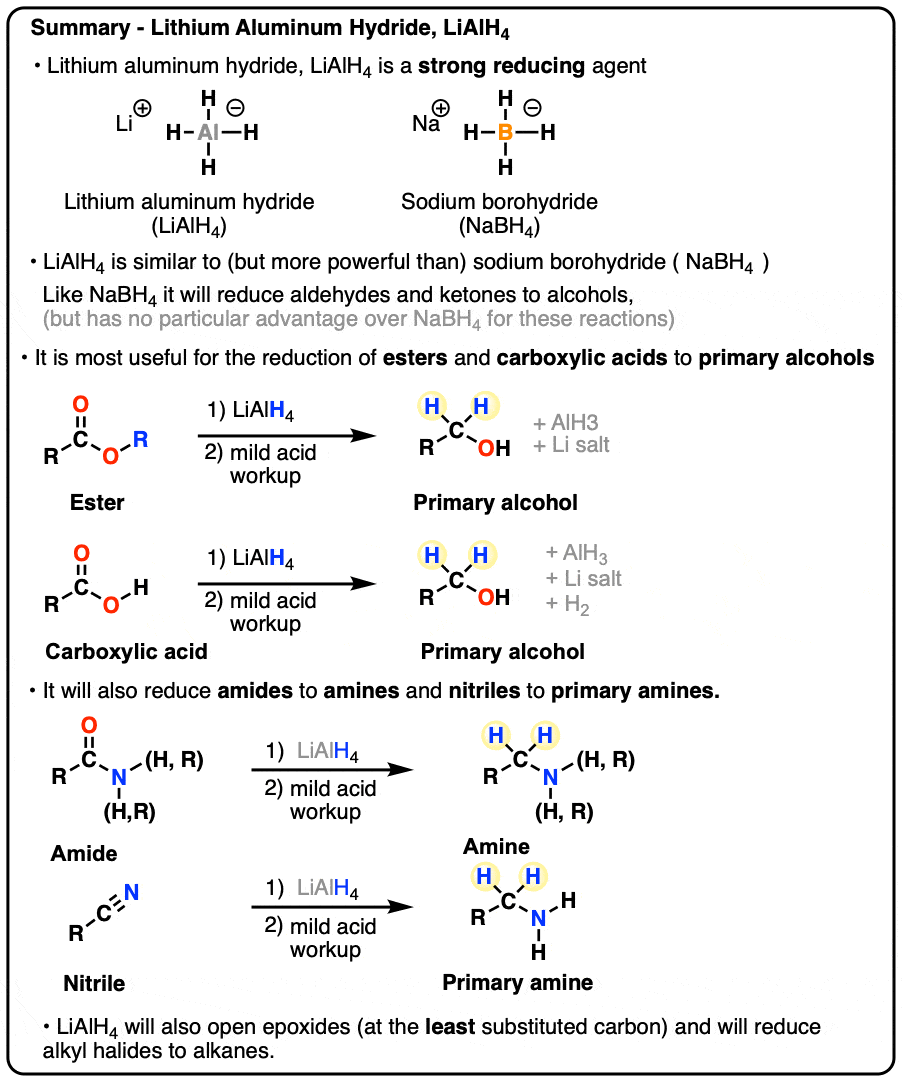
- 氢化铝锂(LiAlH4)是一个强大的还原剂类似,但比,硼氢化钠(NaBH4)
- 就像NaBH4氢化铝锂将减少醇醛和酮。
- 不像NaBH4,它还将减少羧酸,酯类、内酯、酸卤化物和酐主醇
- LiAlH4也会减少腈和酰胺胺
- 最后它可以打开环氧化合物以及减少烷基卤化物烷烃。
表的内容
1。氢化铝锂、LiAlH4
氢化铝锂(LiAlH4)是一个强大的还原剂与一个特定的效用羧酸衍生品。
如果你不熟悉是什么意思”还原剂“在有机化学中,可以找到进修在这里。(见文章-在有机化学氧化和还原。短的版本,还原剂形成的碳氢键而破坏切断债券)
你认为的路易斯结构LiAlH吗4看起来像吗?
 点击翻转
点击翻转
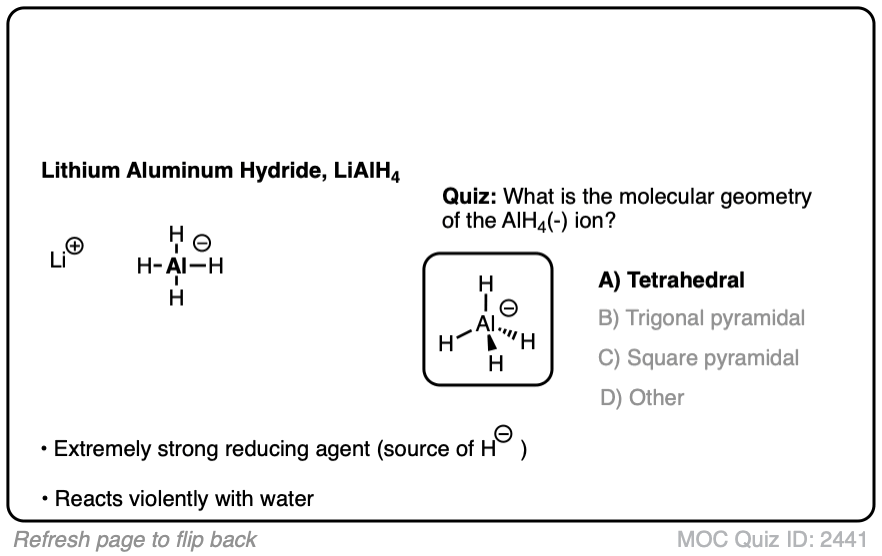
所有的试剂,LiAlH4最像硼氢化钠。(见文章-硼氢化钠(NaBH4醛和酮的还原反应))希望这个不应该是一个巨大的冲击,因为铝低于硼元素周期表是正确的。
这些试剂的一个关键属性是他们作为来源氢化物离子H(-)在他们的反应金属羰基合物和其他亲电试剂。
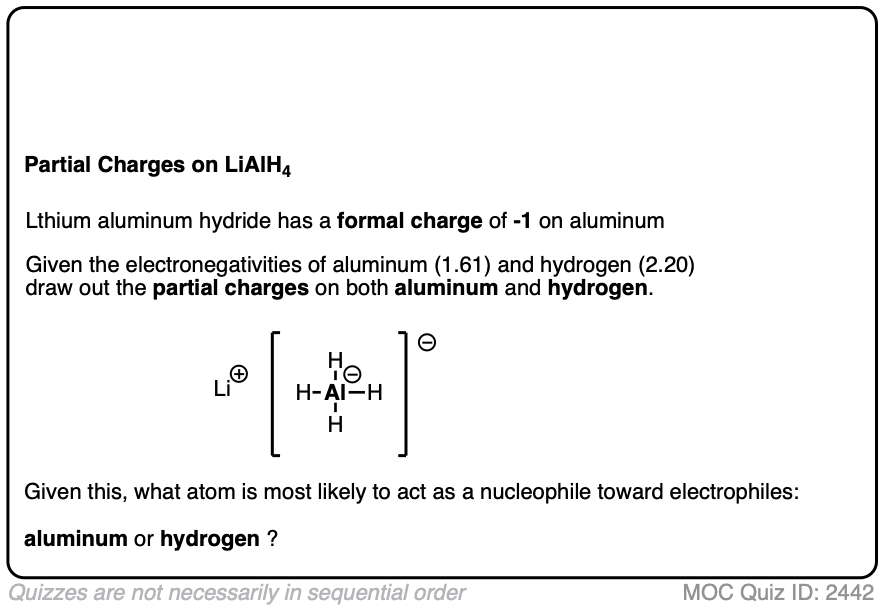
一个未经训练的眼睛,这可能看起来很奇怪,因为似乎负电荷铝。为什么会这样?
 点击翻转
点击翻转
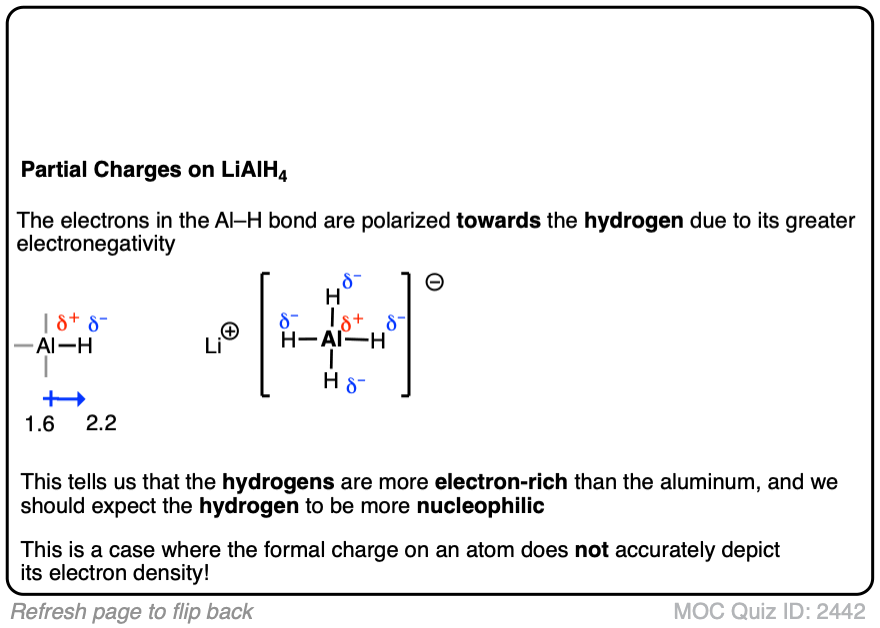
这可能是一个很好的机会来提醒自己形式电荷不一定是一样的吗电子密度。
- 氢的电负性是2.2。
- 铝的电负性是1.61
因此,尽管铝熊消极形式电荷(见文章-如何计算形式电荷),它是氢熊一个部分负(更大的电子密度)和铝熊收取部分正电荷(较小的电子密度)。
鉴于氢化铝锂和硼氢化钠像H(-)的来源,看看你能不能画一个合适的电子推动箭头LiAlH的反应4弱酸性的水。
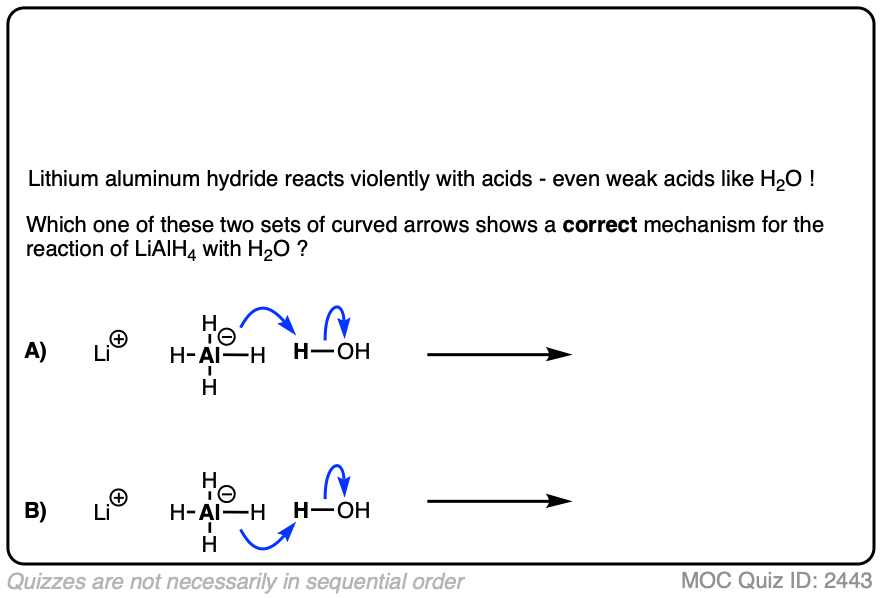 点击翻转
点击翻转
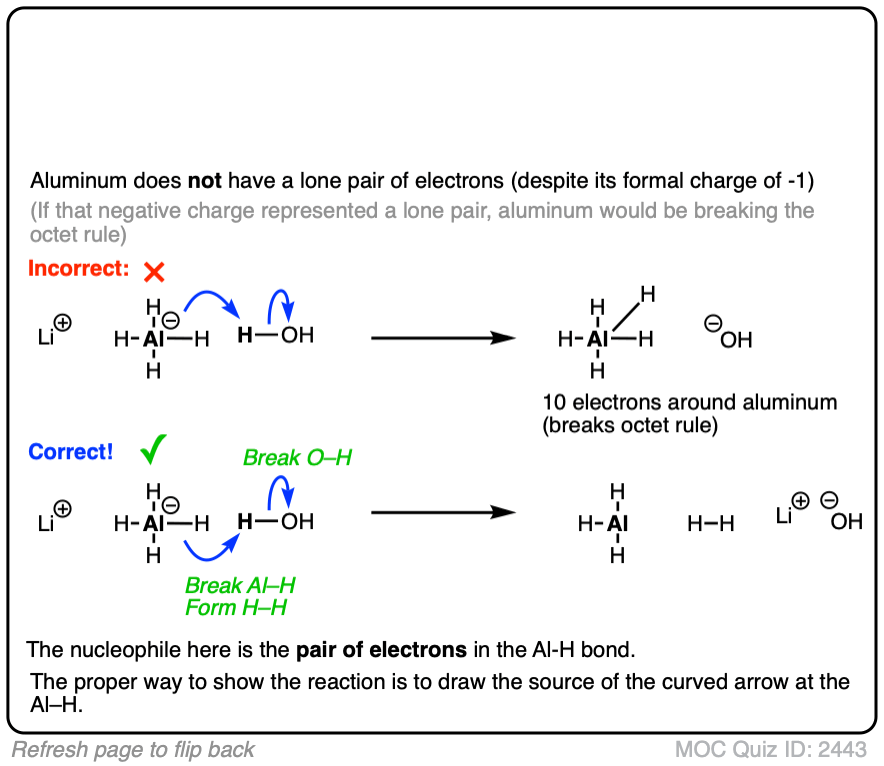
可能你希望成为一个更多的氢化反应捐赠者的离子——borohyride[黑洞吗4- - - - - -),或AlH4(-)。
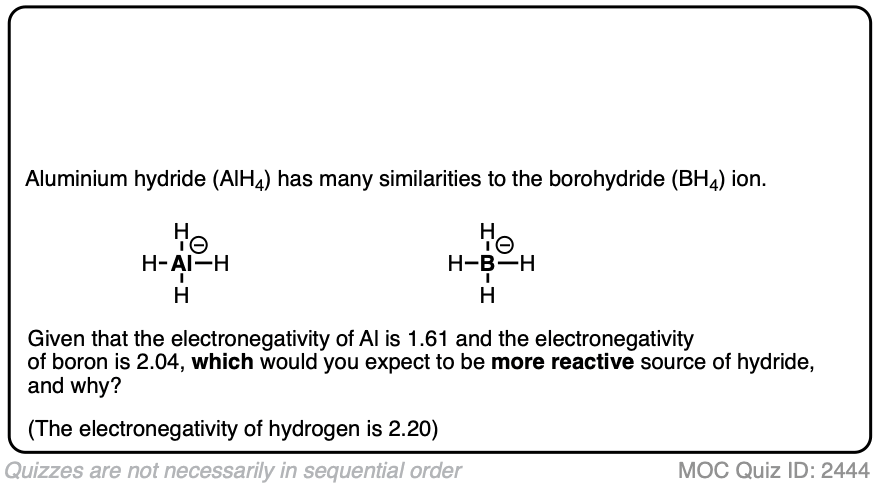 点击翻转
点击翻转
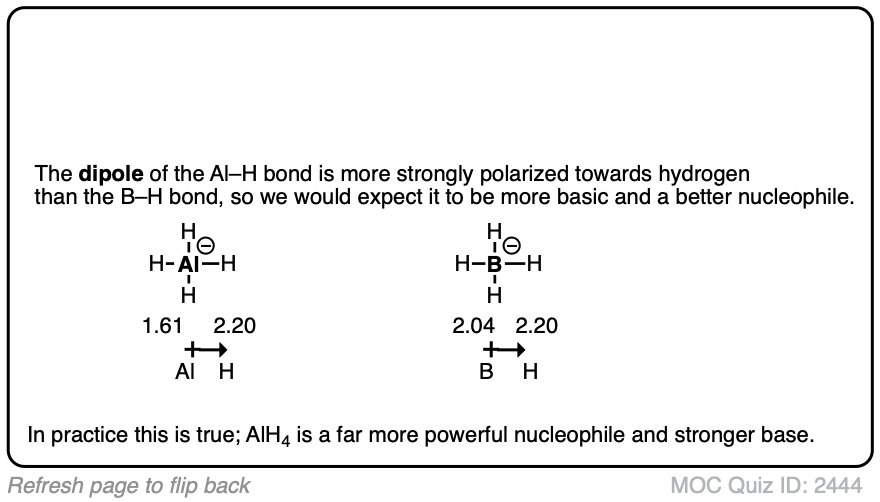
(有一点比这个答案。的抗衡离子也很重要。硼氢化锂(LiBH4)是活性比NaBH4。更多的在这注1下图)
2。NaBH4vs LiAlH4
LiAlH4将减少醛和酮一样吗NaBH4。
出于实际的原因(注2]NaBH4更方便的使用这些反应并使用LiAlH没有优势吗4除非你还计划减少其他官能团。(我的本科老师教授沃尔特Szarek喜欢说,“使用LiAlH4这个反应的就像使用大锤杀死一只苍蝇!”)。
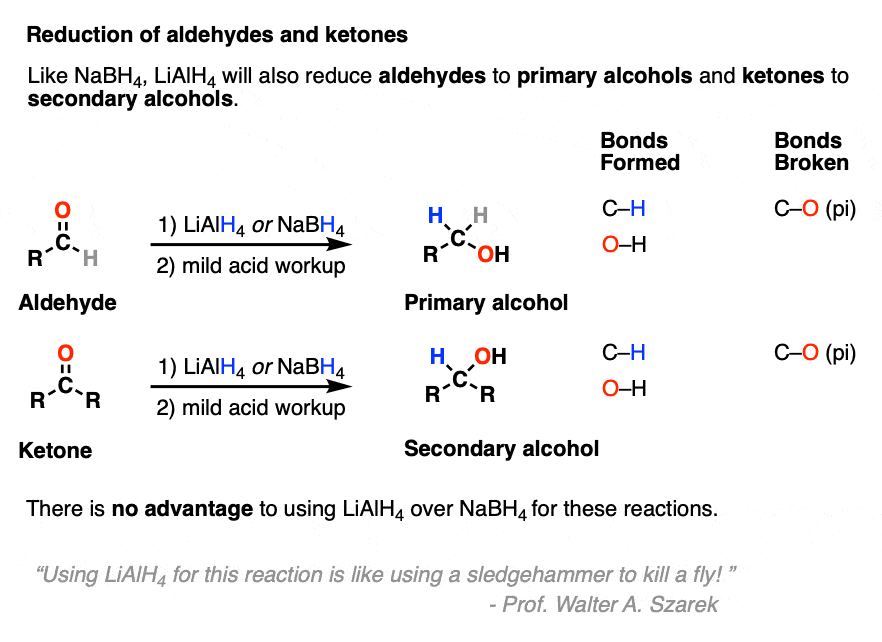
LiAlH4还将执行削减NaBH4无法做的,或者至少,他们要快得多。
一个关键的区别是在减少酯类来主要醇,这NaBH4缓慢(如果有的话)。
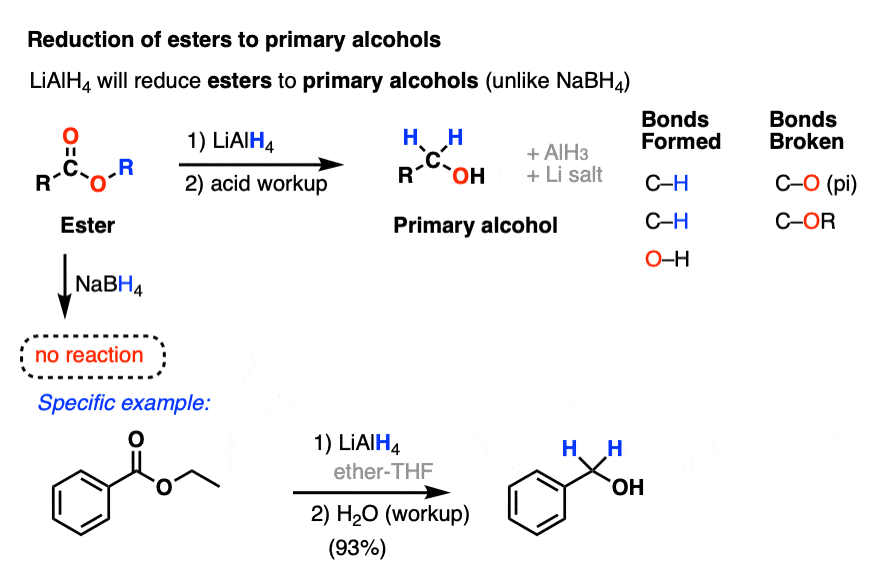
第二个反应,LiAlH4将执行,NaBH4不会减少羧酸主要的醇。
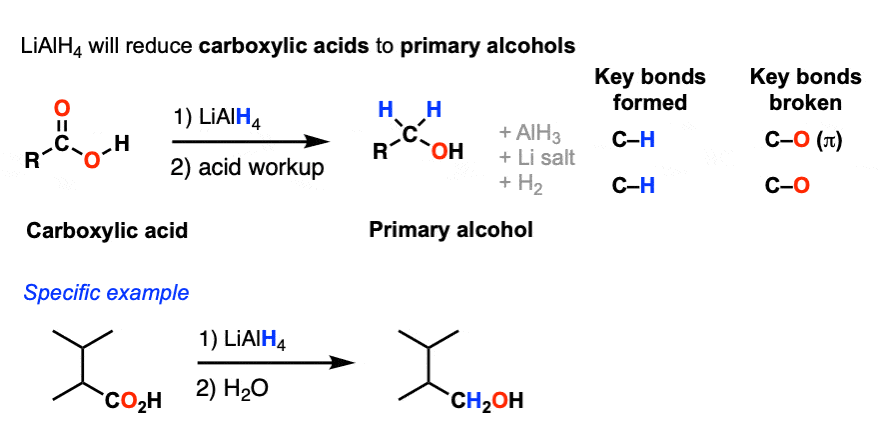
(参考在这里)
其他关键的反应包括
- 对初级醇酸卤化物
- 对初级醇酐
以及减少腈、酰胺环氧化合物,烷基卤化物(和更多的,我们不会封面)

3所示。减少由LiAlH羧酸4——机制
所以LiAlH的反应如何4与羧酸的工作吗?
让我们从最基本的开始。羧酸是酸的。氢化铝锂是强碱性的。
可能第一反应发生什么吗?
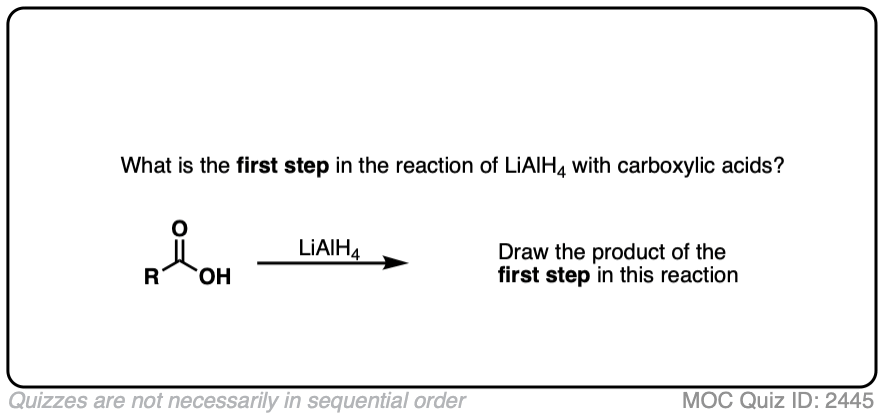 点击翻转
点击翻转
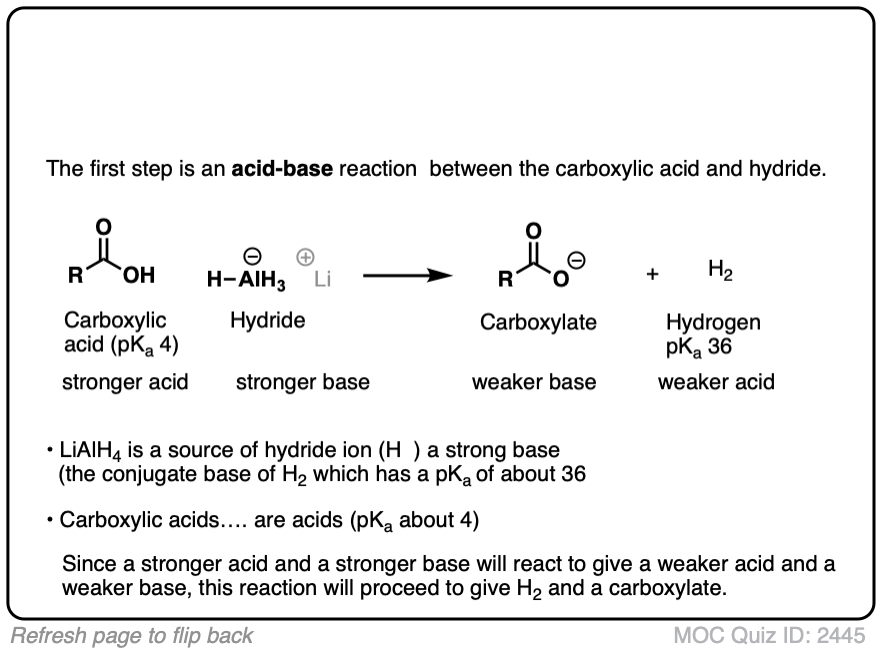
是的,酸碱反应。
记得pK一个H2,共轭酸氢化(H)大约36而pK一个的羧酸大约是4。由于酸碱反应时喜欢将转换为弱酸性较强的酸,这将迅速生成羧酸盐盐(共轭碱的羧酸)和氢气。(见文章:如何用pK吗一个表)。
酸碱反应LiAlH4往往是剧烈放热,并生成可燃氢气,除了。由于这些原因极其谨慎处理LiAlH时使用4这是从来没有排除任何长时间在板凳上,因为它会与空气中的水蒸气反应。火灾可以结果。(注3]。这是一个关键原因NaBH4通常用于简单的削减——在寒冷的气温中,它与酒精溶剂、反应缓慢,可控与LiAlH吗4。
在大多数的亲核试剂,形成的羧酸盐信号的反应。我们已经看到,羧化物不会接受大部分的亲核试剂。(见文章-亲核酰取代)
LiAlH4是一个例外。(注意4在第一步,从铝氢化物形成一个新的碳氢键,打破了切断π键。在第二步中,切断π键的生成,从而切断σ键的断裂。
亲核酰取代羧化物上通常是极其困难的,因为其具有强烈的基本性质的O (2 -)离去基团,但强有力的O-Al纽带和铝的强烈路易斯酸性字符可能极大地帮助。
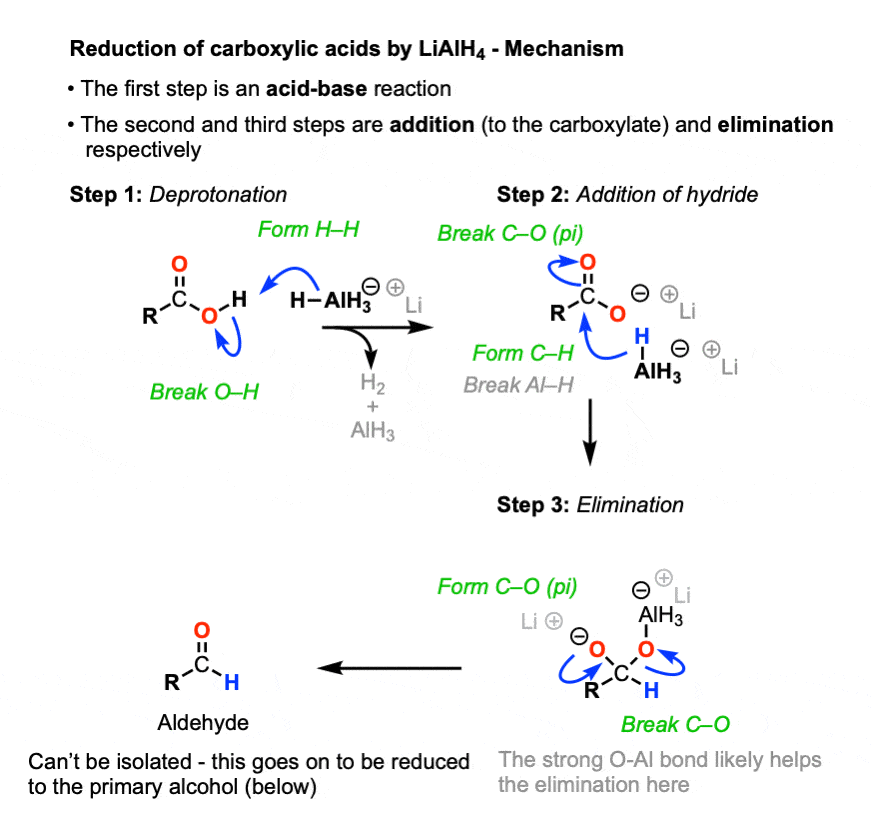
消除的结果在一个醛很快,经历另一个减少。理论上,LiAlH4有四个等价物的氢化物转移,所以它不会是错误的画AlH吗3氢化的来源。在实践中,过多的LiAlH4通常是使用,它很好画这一步发生的机制从另一个相当于AlH吗4(-)。
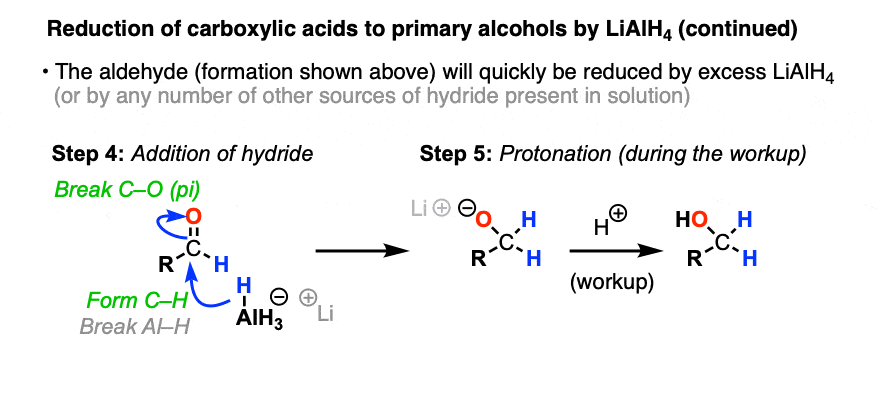
让我们的酒精回来了,我们执行淬火与水的反应,这使质子化醇盐并给出我们中性的酒精。
这是它是如何工作的,不管怎样!
在实践中,引起更复杂,因为铝盐乳剂唠叨,使分离困难,除非他们完全水解(只使用另一个理由NaBH4如果你能!)的费塞尔检查是行业标准,但是还有其他方式。(注3]
4所示。减少的机制由LiAlH酯4
LiAlH的反应机制4与酯类更加简单。
增加氢化酯(碳氢键形式,打破切断(π)]其次是消除醇盐(形式切断(pi),打破切断]了醛。
正如我们所看到的,LiAlH4不停止。它有足够的等价物的氢化物吃早餐醛,午餐,晚餐,剩下一点甜点。
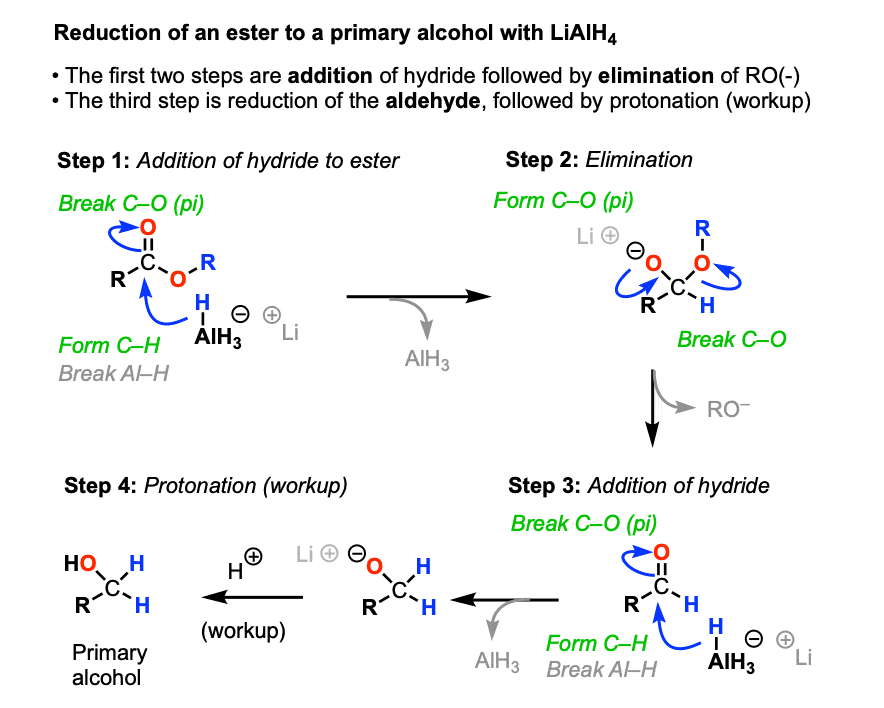
可以得到减少酯类停止在醛阶段通过添加某些群体的铝作为一个“大块头”。DIBAL(Di-isobutylaluminum氢化物,DIBAL- h)是一个典型的试剂用于这些目的。(见文章-Di-isobutyl氢化铝)
LiAlH4也会减少酸卤化物和酐通过机制主要醇相似吗酯类。
也可以执行部分减少酸卤化物醛通过使用相关的试剂LiAlH (Ot布鲁里溃疡)3(见文章-氢化铝锂三(t-butoxy))
5。减少酰胺LiAlH胺4
酰胺官能团的另一个类很难降低。
LiAlH4将减少amides amin然而,es。NaBH4不会触碰他们。
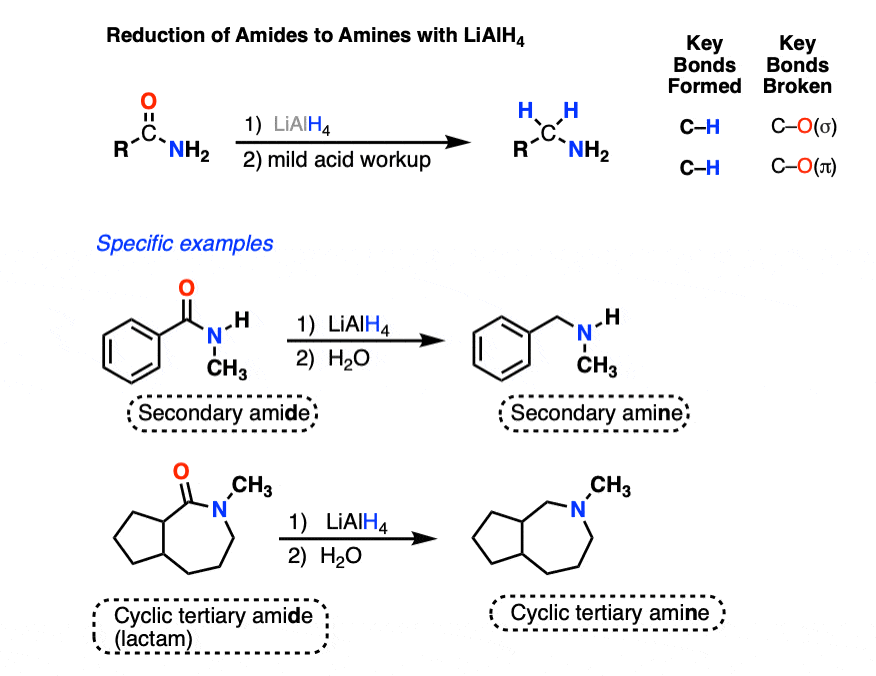
中小学酰胺氮氢键的弱酸性(pK一个17),将进行去质子化由LiAlH4给他们其次是减少共轭基地胺(使用如下所示的机制)。(看到去质子化,徘徊在这里和一个图像会弹出或单击链接]
(三级酰胺,缺乏酸性氢,会的不进行一个初步的酸碱步骤。)
酰胺还原的第一步是熟悉的除了氢化碳(碳氢键形式,打破切断π)给一个四面体中间。
第二步是亲核酰替换消除的薄弱的基础给一个新的π键。
这通常通过切断的形成发生(π)的损失离去基团。所以可能最初想切断π键是一个形式,消除R2N(-),给了我们一个中间醛。
但这并不是会发生什么!相反,它是切断键坏了,和一个氮π键形成,给一个iminium中间和一个醇盐离去基团。(注5)。
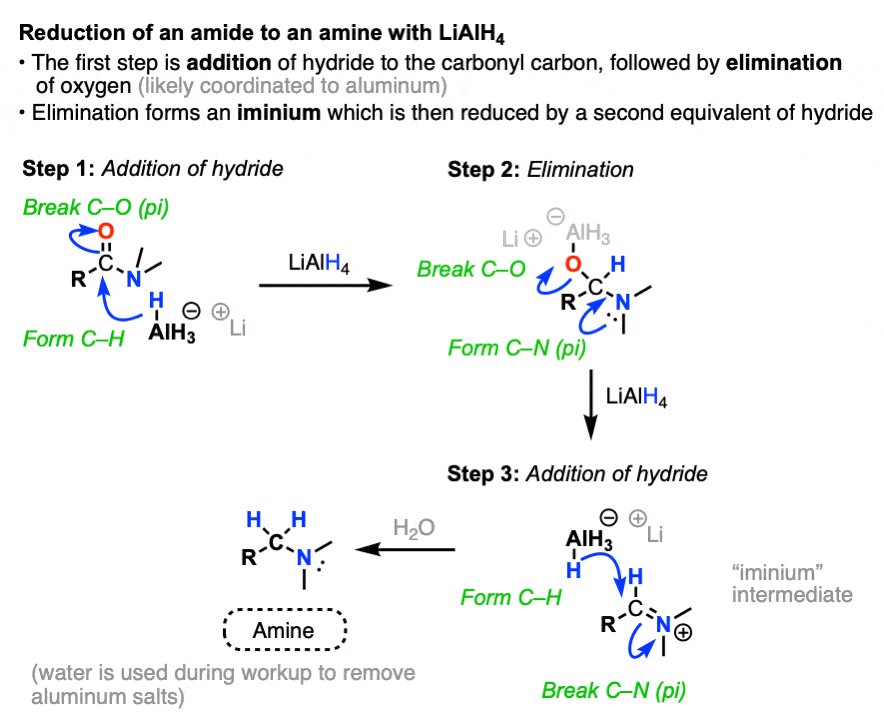
像醛,iminium中间不会持续很长时间的存在所有这些氢化物。
检查后获得的最终产品(去除铝盐)是一个胺。
的类型胺取决于酰胺前兆:
详细的有机合成过程中,点击在这里。
6。减少腈LiAlH一级胺4
打击,LiAlH4一直砸在每个功能性组我们扔在它的路径。它不能减少吗?
将在接下来的对手!
腈需要漂亮的强制条件下水解成羧酸或酰胺,和他们使用催化加氢还原需要高温(50 - 100°C)和氢压力(这裁判引用100 atm的H2)。
可以LiAlH4这样做吗?
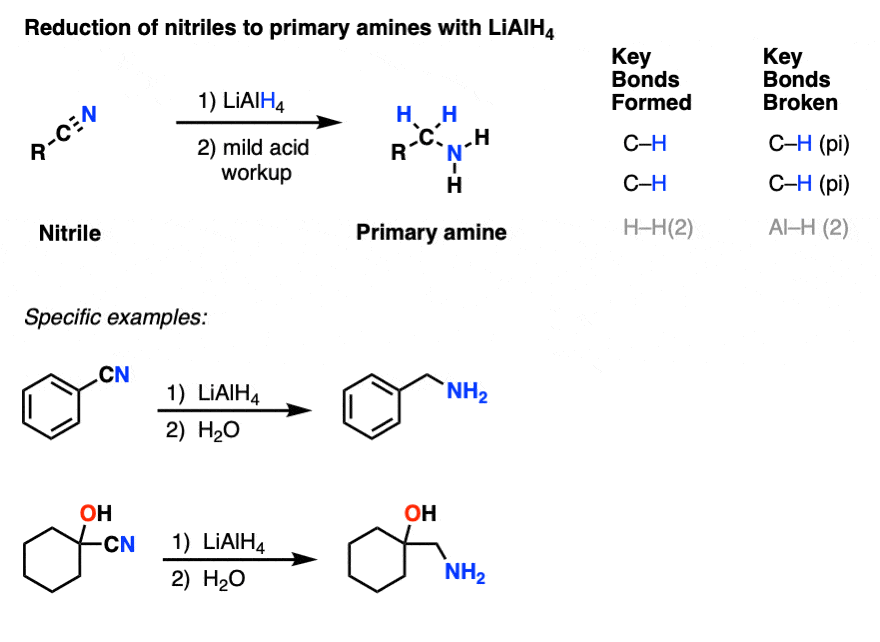
这里的第一步是另一个,这一次打破氮(pi)键,形成一个亚胺的物种。第二个添加氢化给出了带负电荷的氮中间主要是质子化了的胺在检查。
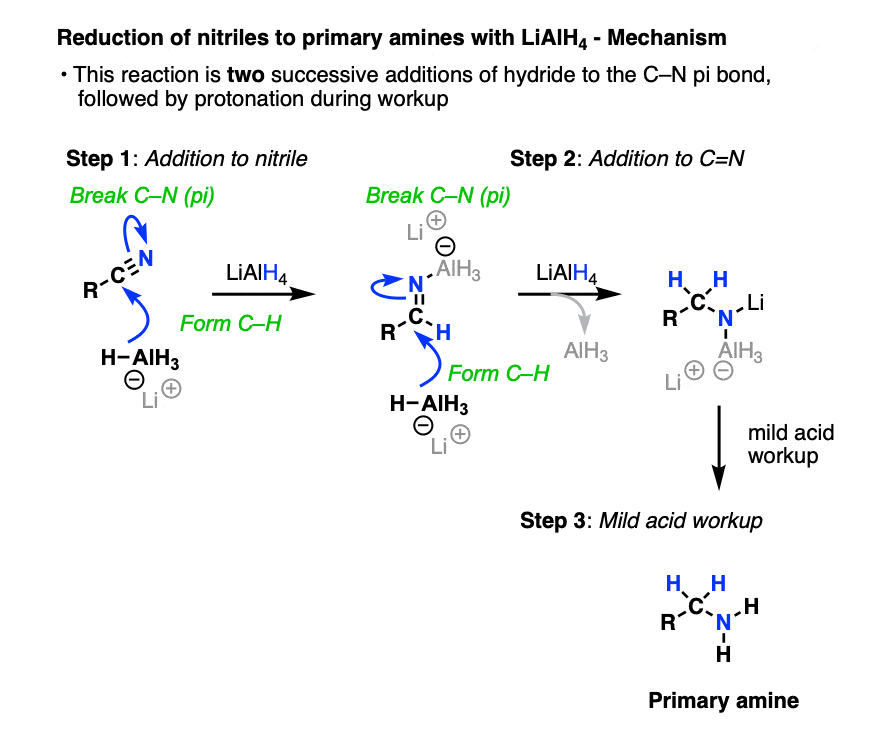
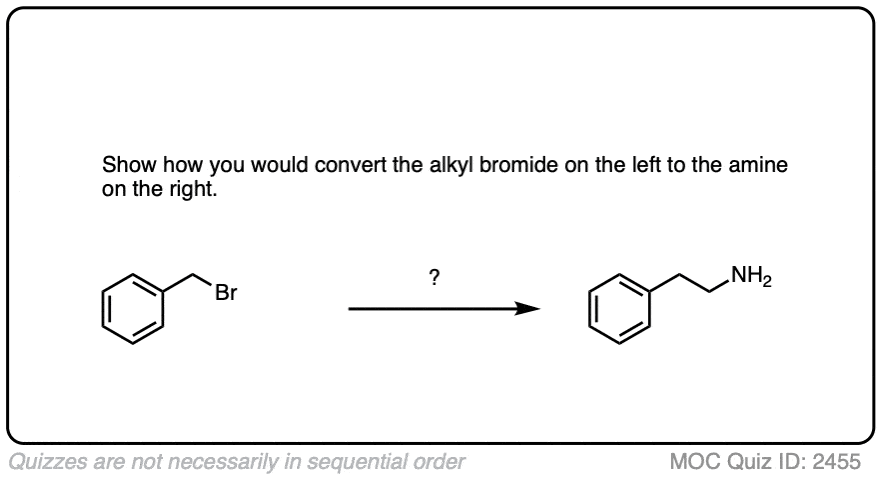
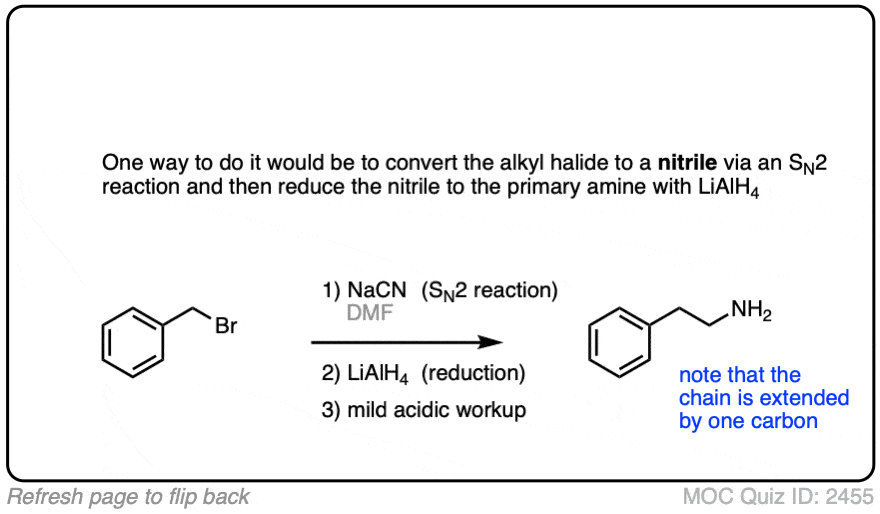
你可能记得,氰根离子CN(-)是一个很好的亲核试剂将执行年代N2反应烷基卤化物。所以执行一个年代N2其次是LiAlH4减少转换的一种方式烷基卤化物为chain-extended主要胺。
7所示。其他的反应LiAlH4
但是等等——还有更多!
- LiAlH4将会减少环氧化合物醇类,你能想到的是像一个年代N2的反应。像其他带负电的亲核试剂,它增加了环氧化合物至少取代碳。(见文章-环氧化合物的基础)
- LiAlH4也会在某些情况下,减少烷基卤化物烷烃,订单我> Br > Cl > F。
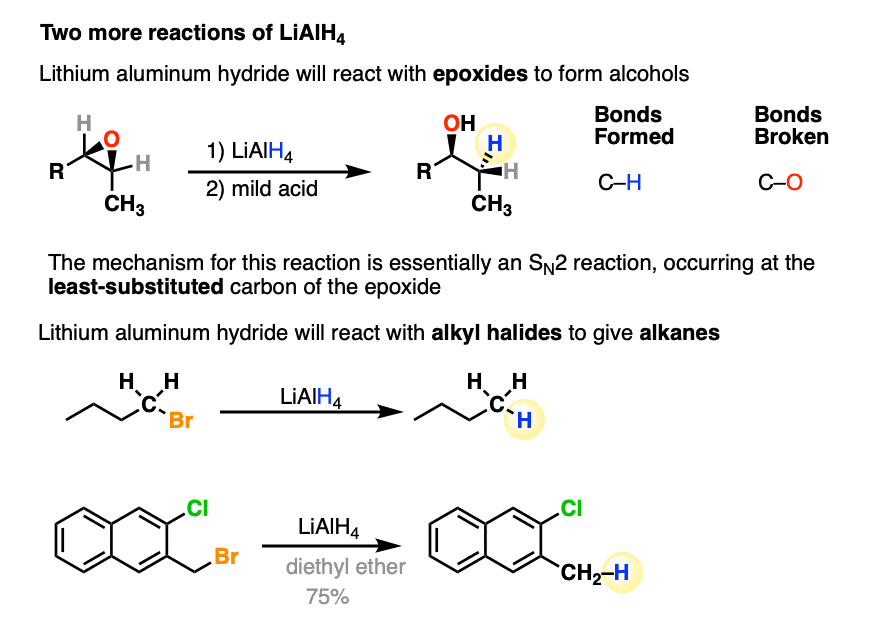
一个官能团LiAlH4将不触摸是醚。
8。总结
- LiAlH4的霸王龙减少代理。积极的,如果你的官能团绝对减少一夜之间,使用LiAlH4。这是一个通用hydride-adding强大的野兽,随时可用,相对便宜。
- 如果你需要一个还原剂,轻轻地逗氢化物分子与一个轻佻的触摸,用别的东西。
- 各种LiAlH温和的衍生品4如DIBAL和LiAlH (Ot布鲁里溃疡)3开发并更有选择性。
- 醛和酮的还原反应,硼氢化钠(NaBH4)非常好。
笔记
注1。LiBH4反应性比NaBH4由于越Lewis-acidic锂离子的存在。这有助于激活羰基对亲核攻击,就像质子化了的金属羰基合物更对的亲核试剂反应是中性的吗金属羰基合物。LiBH4不像LiAlH反应吗4,但它将减少酯类醇。
注2。下面是一些实用的喜欢的理由NaBH4对LiAlH4。
NaBH4通常是作为球团。排除空气中很短的一个时期,这些颗粒将从空气中吸收水和最终形成液体的小水坑,但不会自燃。NaBH4可用于冷酒精溶剂如EtOH和CH3没有事件哦。硼氢化钠减少的检查是非常简单的——通常只与饱和淬火铵氯和做它。
相比之下,LiAlH4是一个很好的灰色粉末形式尘埃云轻微扰动,和一个憋住气,避免在肺部。它反应暴力与水和醇类,最好使用干燥的溶剂。铝盐乳剂形成困难,在分液漏斗乏味,除非提取铝盐的水解与基础。通常的程序(费塞尔检查),如下所示。
减少使用n克LiAlH4一个仔细,一滴一滴地补充道
- n毫升的水
- n氢氧化钠溶液毫升的15%,
- 3n毫升的水
在搅拌15 - 30分钟这应该提供一个白色沉淀,可以过滤掉。
固体的另一个过程调用水合硫酸钠(芒硝,NaSO4•10 h2O)添加portionwise直到盐变成白色。(裁判)。
注3。一个人我知道(谁能保持无名)自己喜欢晚上工作到很晚。有一次他LiAlH重了4还原反应,离开了灰色粉在实验室重船的平衡。在某种程度上,在将其添加到他的反应之前,他决定在他的书桌上。有一个午睡不久之后他被烧焦的气味粗暴地唤醒塑料LiAlH自燃的4,消耗(4000美元)分析天平,他睡着了。幸运的是没有人受伤和实验室否则毫发无损。
注4。Al-O债券很强(128千卡每摩尔),因为铝空pi-bonding p轨道,实际的离去基团可能类似于O = AlH2(-),基本的量要少得多,说,O (2 -李)2
注5。的醛可以在一些条件下形成的。例如使用强劲还原剂super-hydride (tri sec-butylborohydride锂)在低温下醛可以获得。
一个特殊的类酰胺发现酰胺将接受mono-addition有机金属试剂(包括氢化来源)。这些反应工作,因为氮刘易斯包含一个基本的哟3组织可以配合金属和帮助稳定四面体中间,防止被淘汰。
注6。腈将进行部分减少使用吗DIBAL- h。他们也可以通过格氏试剂进行添加给酮水解后生成的亚胺。
注7。LiAlH4通常是通过减少AlCl的解决方案做好准备了吗3在醚氢化锂(LiH)。(参考)。
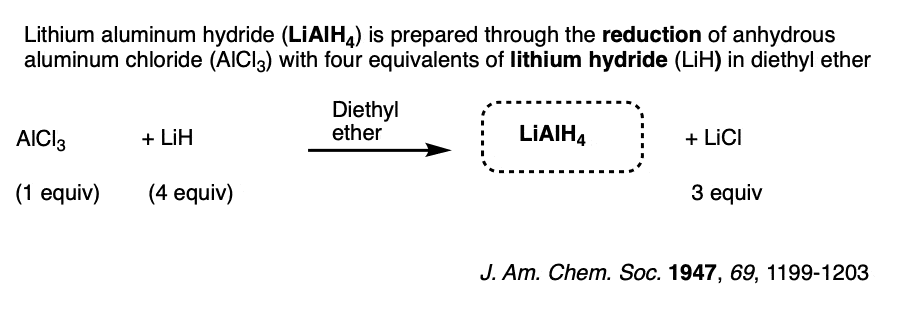
我们一般不认为不和LiH氢化物离子的好亲核试剂,但足够强大路易斯碱,它可以作为一个。
测试你自己!
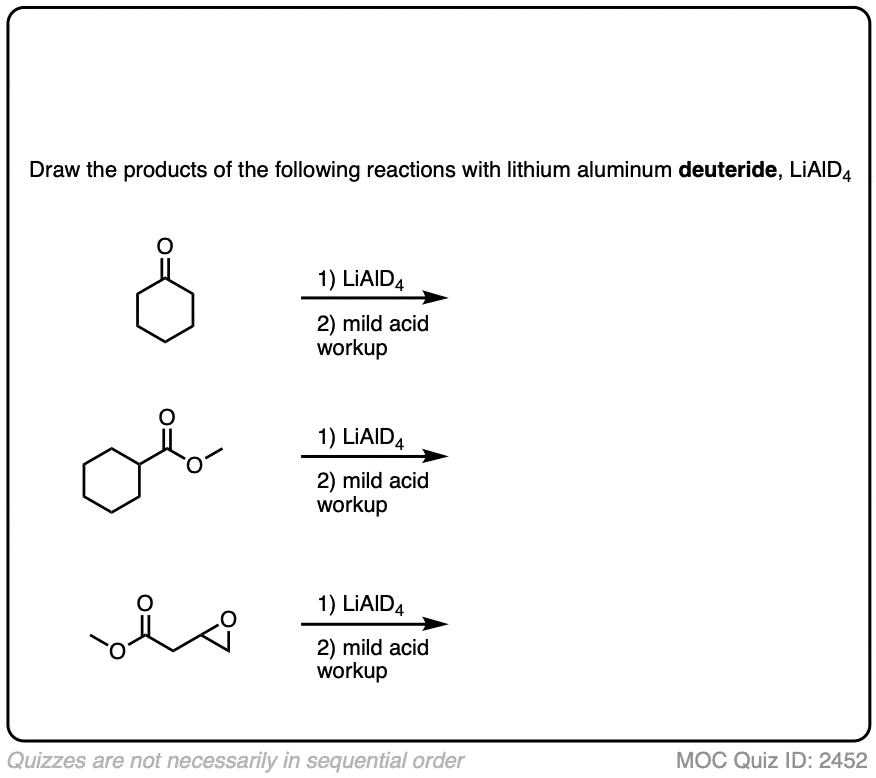 点击翻转
点击翻转
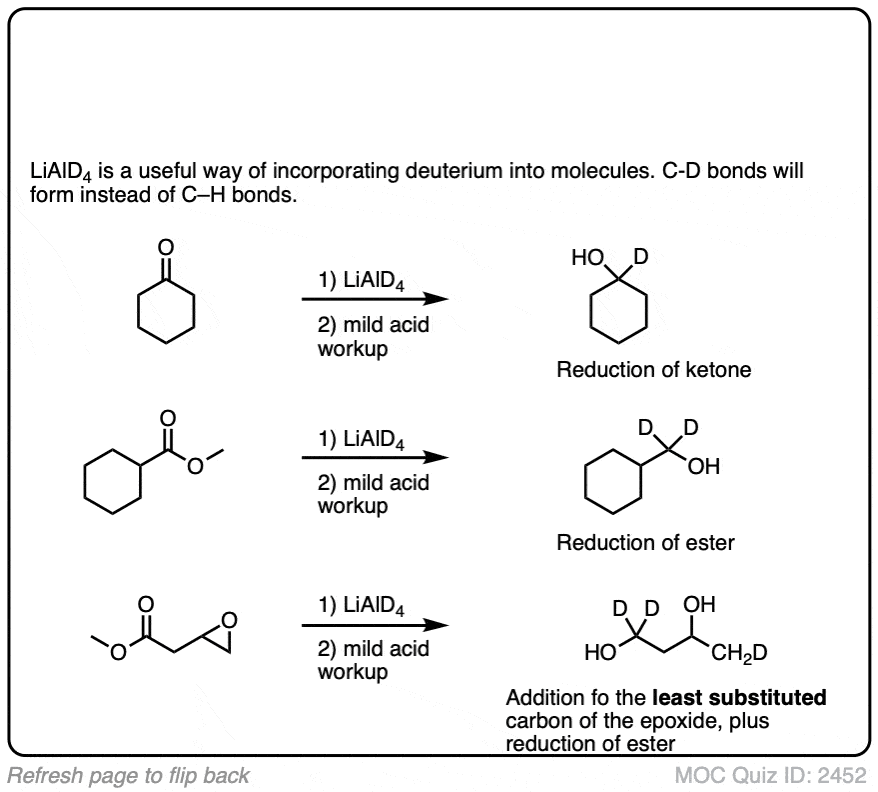
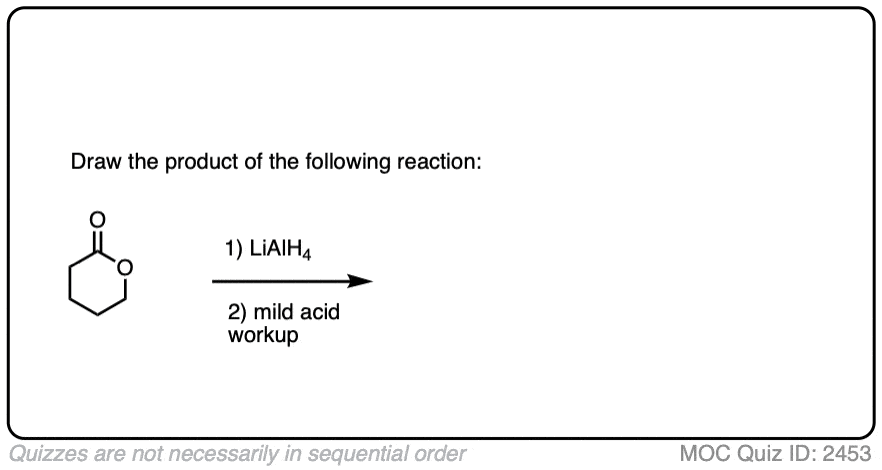 点击翻转
点击翻转
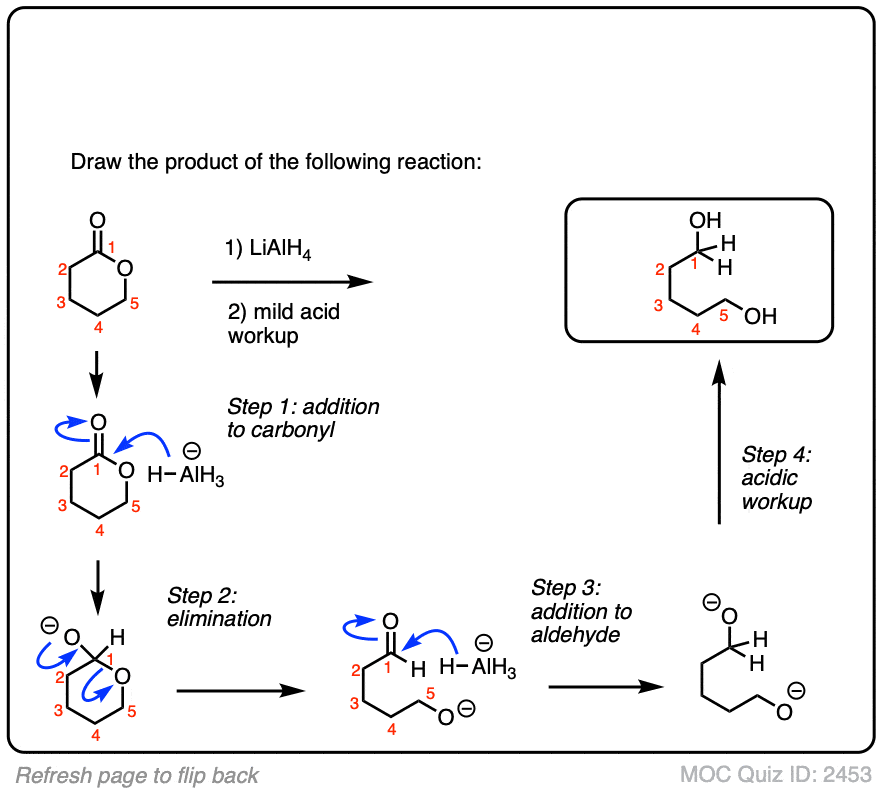
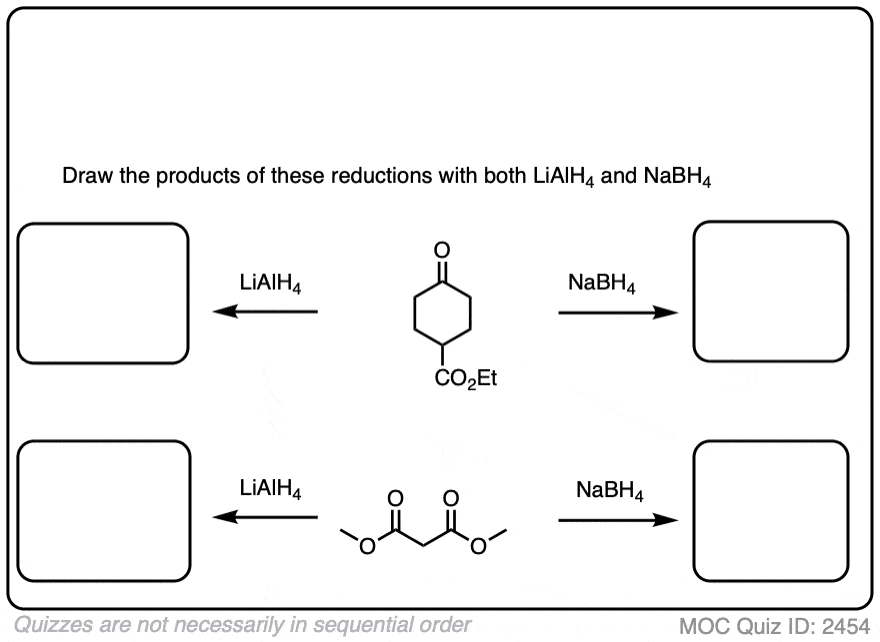 点击翻转
点击翻转
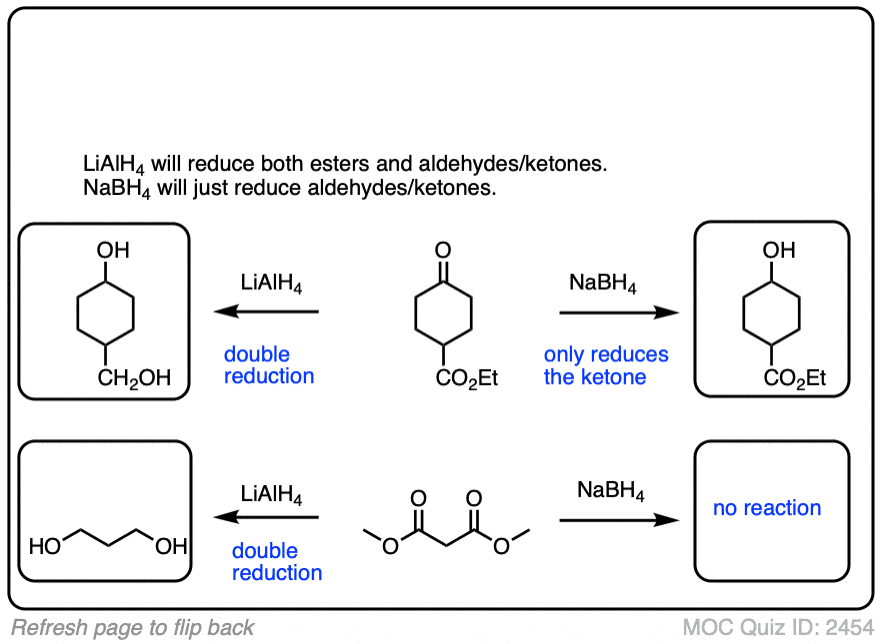
 点击翻转
点击翻转
(高级)引用和进一步阅读
减少更多的上下文本资料(PDF)减少代理从115年哈佛大学教授安德鲁·g·迈尔斯的化学课程是一个非常有用的概述
- 氢化铝锂、铝氢化物和氢化锂镓,和他们的一些应用在有机和无机化学
a . e . Finholt a . c .债券Jr .)和h·施莱辛格
美国化学学会杂志》上1947年69年(5),1199 - 1203
DOI:10.1021 / ja01197a061
第一个报告LiAlH做准备4,从AlCl3和典范。 - 减少氢化铝锂的有机化合物。醛,酮,酯类、酸性氯化物和酸酐
罗伯特·f·Nystrom和韦尔登·g·布朗
美国化学学会杂志》上1947年,69年(5),1197 - 1199
DOI:10.1021 / ja01197a060
早期论文LiAlH4覆盖与官能团的反应包含C = O双键。 - 经验教训─氢化铝锂火灾
克雷格•a . Merlic卡尔·j·费伯,Imke施罗德
ACS化学健康&安全2022年29 (4),362 - 365
DOI:10.1021 / acs.chas.2c00035
氢化铝锂颗粒不应该在研钵和研杵!本文描述了几种火灾发生时,这种治疗的结果。 - 2 -丙醇(1-PYRROLIDYL)
罗伯特·布鲁斯·莫菲特
Org。Synth。1953年,33,82年
DOI:10.15227 / orgsyn.033.0082 - 总(+)-calyculin的综合
大卫·a·埃文斯,詹姆斯·r·盖奇和詹姆斯·l·雷顿
美国化学学会杂志》上1992年,114年(24),9434 - 9453
DOI:10.1021 / ja00050a024
减少55在这个总合成甲基的选择性降低酯到一个酒精在一个使用LiAlH酰胺4。 - Daphniphyllum生物碱。15。总(+ -)。合成甲基homodaphniphyllate (+ -) -daphnilactone
克莱顿h .和罗杰b .最近,和金姆·麦克卢尔
《有机化学》杂志上1992年,57(9),2585 - 2594
DOI:10.1021 / jo00035a012
LiAlH4也可以用来减少内酯,消除循环结构。在本文中,减少内酯18影响使用LiAlH4,产生两个醇。 - 1,2-Benzenedimethanol
良Oi和k·夏普
Org。Synth。1996年,73年,1
DOI:10.15227 / orgsyn.073.0001
这个过程的第一步是邻苯二甲酸二乙酯的还原,2-benzenedimethanol LiAlH4 93%的收益率。 - N, N-Dimethylcyclohexylmethylamine
阿瑟和恩格尔伯特·Ciganek
Org。Synth。1959年,39,19所示。
DOI:10.15227 / orgsyn.039.0019
这个过程显示了减少叔酰胺三级胺与LiAlH4回流醚(15小时)。
我有一个疑问。如果过去rxn醇形成超过LiAlH4,强碱(H⁻), AlH3(路易斯酸)和李⁺做出更好的离去基团(-哦)。所以不应该这些好条件E2 E1cB较少或没有?