烯烃的反应
烯烃的稳定性
最后更新:2022年11月15日|
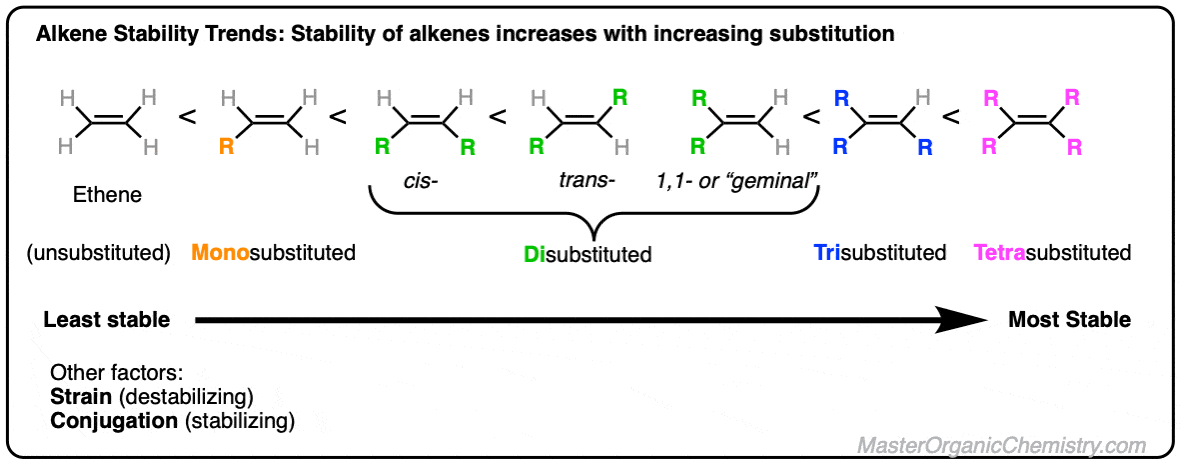
烯烃稳定(不稳定)
什么因素影响烯烃稳定?如果你已经研究了消除反应,毫无疑问你学到什么扎伊采夫规则——如何消除反应通常倾向于“更多的替代”烯烃。
在这篇文章中我们探讨如何增加替代碳的稳定性增加烯烃以及接合和应变的影响。
表的内容
- 烯烃的加氢作为衡量热稳定性
- 烯烃的稳定性增加而增加替换
- 加热一些单取代烯烃的加氢
- 的相对稳定顺式和反式-烯烃
- 由共轭烯烃稳定:共振能量
- 烯烃稳定性:总结
- 笔记
- 奖金话题# 1:为什么烷基取代稳定?
- 奖金话题# 2:反式-Cycloalkenes
- 测试你自己!
- (高级)引用和进一步阅读
1。烯烃的加氢作为衡量热稳定性
我们可能不会花费那么多讨论热力学在这里像在普通化学,有机化学,但这并不意味着这些概念刚刚消失!
我们之前见过的一个领域热力学数据的有用性是使用燃烧热数据来量化环应变。(参见:环烷-如何计算环应变]。环丙烷燃烧热的作品每CH 166千卡每摩尔2而不牵强附会的环己烷(燃烧的热量157千卡每摩尔每CH2]。“额外”燃烧热的环丙烷是归因于不稳定引起弯曲应变的碳碳键远离他们的理想角度109.5°。这是角应变。
另一个领域的有机化学热力学研究是有用的的稳定性烯烃。
Kiasatakowsky教授早在1935年,哈佛大学和同事发表的方法测量的加氢热乙烯(又名“乙烯”),因为它是通过在金属催化剂含有微细粒子吸附氢。(注1因为加氢,分子比,更温柔的说,燃烧,往往是更敏感的方法确定焓变的微妙差异。
在加氢反应,碳碳键坏了,和两个碳氢键形成。
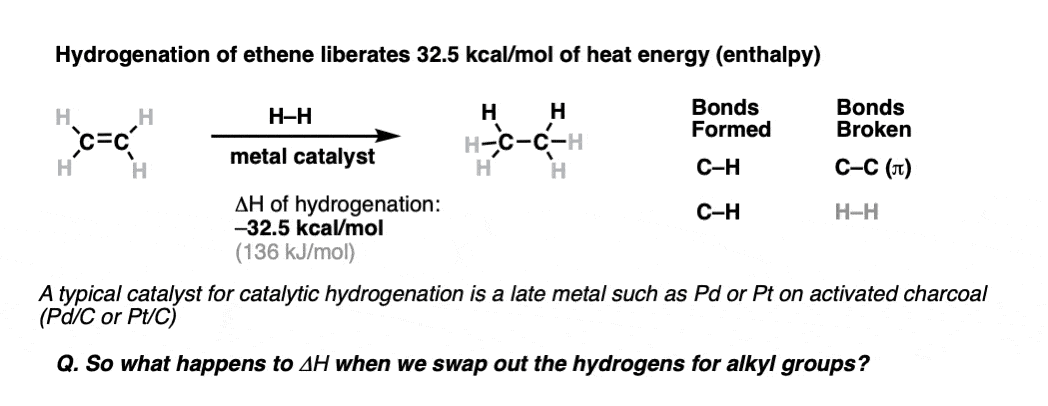
发现释放的乙烯加氢32.5千卡/摩尔(136焦每摩尔)的热量。(注2]
一旦获得了乙烯的加氢热,下一个逻辑步骤是衡量热形成的一个巨大的各种各样的烯烃,看看从数据模式出现。
2。烯烃的稳定性增加而增加替换
正如你想象的人发明了一种新的技术,Kiastakowsky进城,调查的加氢热一个巨大的各种各样的烯烃。(注3)在接下来的几十年,积累更多的数据,这可以很容易地获得(引用)从Web NIST化学书。
就我们的目的而言,六个替换模式在一个烯烃如果你计数乙烯)(7。
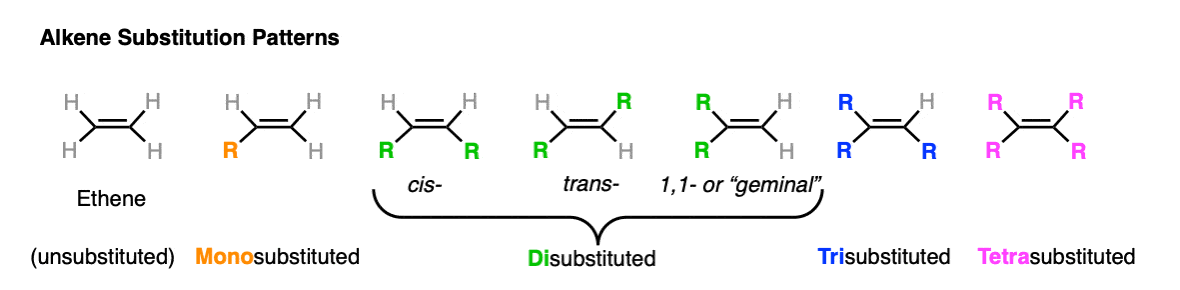
最值得注意的趋势是被发现加氢热减少随着碳氢键被替换成碳碳键。
这是什么的意思吗?
因为相同的债券形成和破碎的加氢反应,加氢热测量稳定每种类型的烯烃。
这意味着降低加氢,热的稳定性就越大烯烃。
可视化的方式“稳定”是比较势能,就像一个球变得越来越“不稳定”,增加高度。
所以我们真的说的是烯烃稳定增加而增加氢碳的替换。
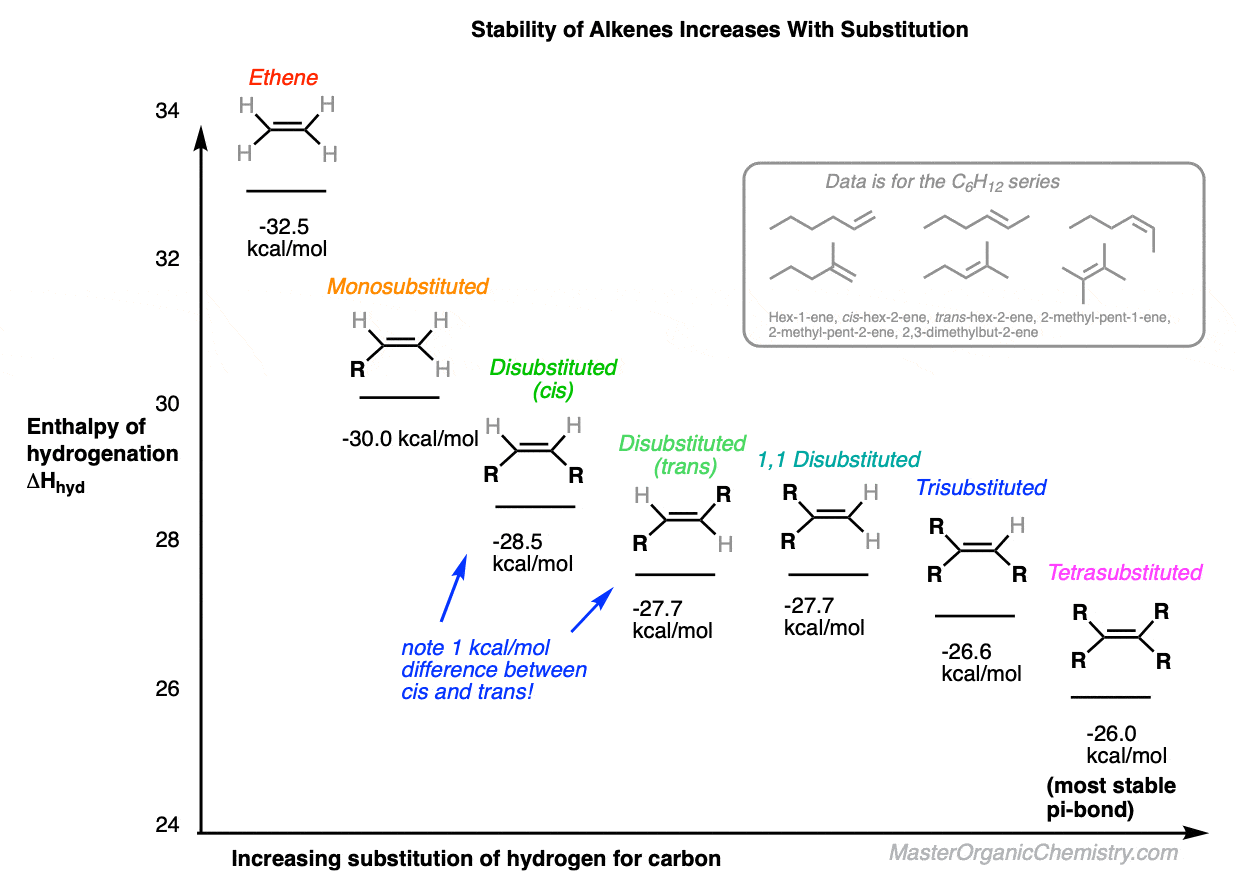
(上图为系列hex-1-ene使用加氢热数据,反式-hex-2-ene,独联体hex-2-ene、2-methylpent-1-ene 2-methyl-pent-2-ene, 2, 3-dimethylbutene,所有分享分子式C6H12。]
好吧,你可能会问。所以,为什么这发生了什么?
简短的回答是,替换烷基组的烯烃允许捐赠(完整的)碳碳之间的电子密度σ轨道和(空的)碳碳π*轨道。通常是不解决入门课程,所以我们会推动这个脚注解释到。(奖金的话题之一]
3所示。加热一些单取代烯烃的加氢
只是为了好玩,我们来看一系列mono-substituted烯烃。没有什么奇怪的,我们就从丙烯hex-1-ene。
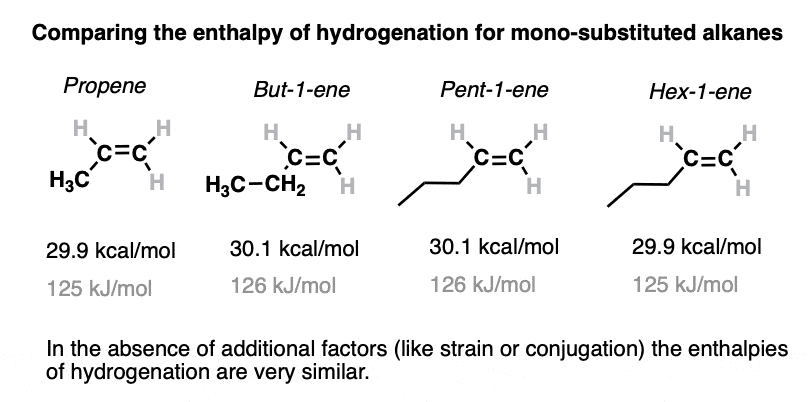
注意,加氢热相当一致的一系列的线性,non-branched,单取代烯烃。
4所示。的相对稳定顺式和反式-烯烃
那么双取代的烯烃吗?有三种类型(独联体,反式1、1-disubstituted),但让我们关心独联体和反式在这里。
现在我们都知道了独联体和反式烯烃应该有点稳定,因为在有何不同独联体烯烃举行的团体紧密(更多的应变!),反式- - - - - -烯烃他们是远。(好一段时间,让你的教练,叫它的名字:1,2-strain]
加氢热数据实际上允许我们量化稳定之间的差异独联体和反式烯烃。
例如,比较独联体- - -反式- 2 -丁烯,或独联体- - - - - -和反式hex-2-ene。稳定的差异大约是1千卡每摩尔,围捕慷慨。
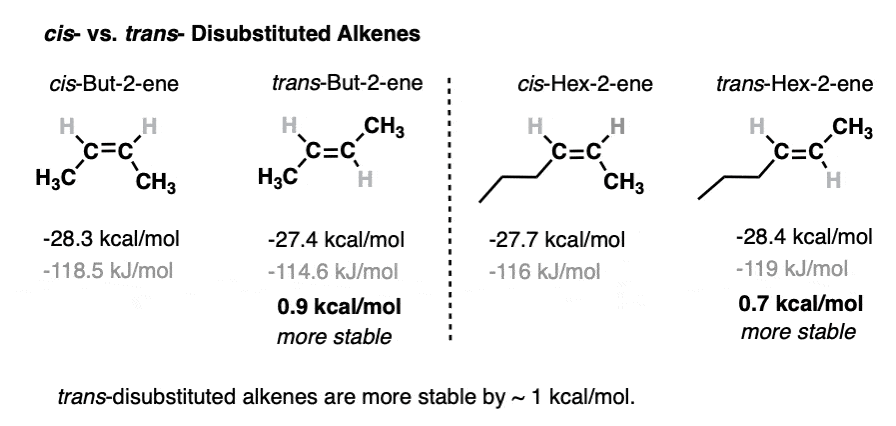
虽然1千卡每摩尔的区别可能看起来不是很多,这不是* *小-一个平衡在25°C, 1千卡每摩尔的差异会给你一个80:20比率的产品。(注意4]
一个很好的时间你可以选择疯狂喜欢的东西独联体- - -反式- - - - - -叔丁基乙烯。(不正确的国际命名,但肯定更生动独联体- - -反式- 2、2、5,5-tetramethylhex-3-ene]。
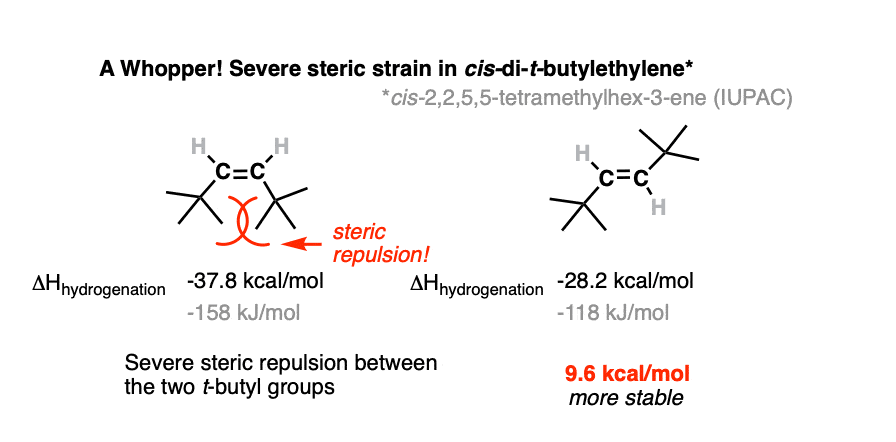
这是一个很多的压力。
5。由共轭烯烃稳定:共振能量
的稳定性烯烃也受到影响动词的词形变化。这是一个真正的另一章的主题(具体地说,知道了结合和共振),我们谈论π体系,但底线是p轨道在相邻的π键可以聚集形成更大的“pi-systems”,它提供了更多的“房间”电子游荡,降低他们的能量。(注5]
加氢热数据使我们能够量化共振稳定的影响。所以如何?
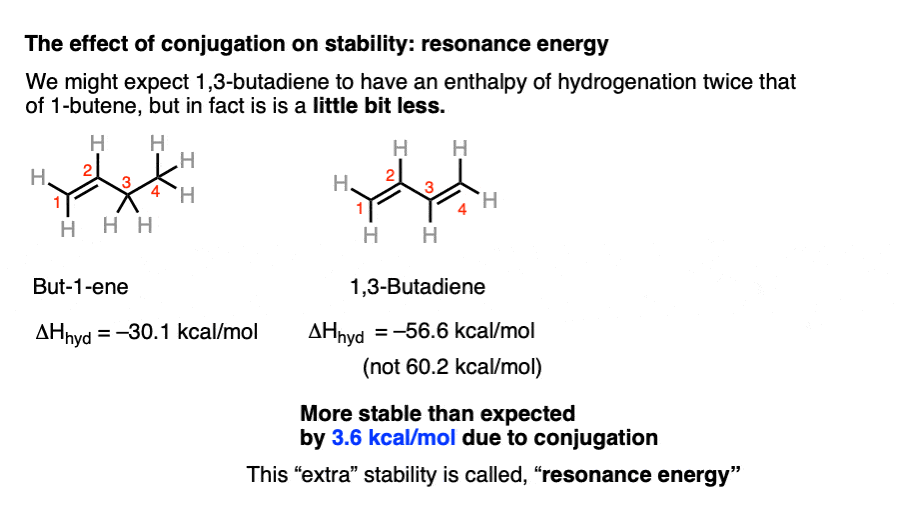
1 -丁烯。以上我们看到的加氢约为30.1千卡每摩尔。
添加一个双键,你可能期望加氢翻倍的热量。但它不!它实际上是一个少一些。56.6千卡每摩尔。的区别(额外的3.6千卡/摩尔额外的稳定)被称为“共振能量”。
最引人注目的例子共振能量的例子中发现“双键苯”,这有一个额外的稳定的能量36千卡每摩尔。这是一个确定的信号,这个分子发生了一些极不寻常的,这是更好的被称为“苯”。被称为“极不寻常”属性芳香性认股权证自己的一章。(参见:介绍了芳香性]
6。摘要:烯烃的稳定
三个关键因素影响的稳定性烯烃可以测量的影响,这些因素通过加氢的焓。
- 是一个重要因素替换模式。碳氢键被碳碳键取代,稳定的烯烃逐渐增加的顺序mono di(稳定)< <三< tetrasubstituted(最稳定)。
- 当加氢解放更多的比预期的能源替代模式,这是可能的一个标志应变。这是例证之间的焓差的加氢独联体- - - - - -和反式- - - - - -烯烃,那里的反式- - - - - -烯烃更稳定的1千卡每摩尔。
- 当加氢解放少比预期的能源替代模式,这是一个迹象表明,一些额外的因素是稳定的分子。常见的因素之一,动词的词形变化排名高。能量的差异之间的“预期”热氢化和加氢称为热计量共振能量。的共轭π键和一个额外的π键是“值得”2 - 3千卡每摩尔。
稳定的增加烯烃随着替代不仅出现在扎伊采夫规则,但后来也在当你学习热力学和动力学控制。
笔记
注1。这是一个铜催化剂,经过大量的试验和错误。的优势在燃烧热测量加氢热是一个更加敏感的技术用于测量小的能量。
注2。这个数字在1935年首次测量,重新度量界限1951年据我所知,还没有更新。看中的条目NIST Chembook为乙烯。
注3。标准的加氢热了NIST Chembook。
注4。实际上82:18在298 K。从δG = rt ln K,使用δG的1000大卡,T = 298 K, R = 1.987大卡/摩尔•K。
注5。如果你认为电子是波,大pi-system允许更长的波长,由于能量波长成反比,这意味着较低的电子的总能量。
和一个大感谢挪威海怪的稳定的双手稳定GIF。
附录1:为什么增加替代增加稳定?
所以为什么增加替换的吗烯烃增加其稳定性?这不是一个简单的问题来回答几句话入门的听众,和由于时间约束的典型答案你通常会从一个教练将从“很复杂”“超共轭现象”“混合轨道”。很少你可能得到一个莫图。
这里的统一原则是完整的轨道——即使是那些从单一债券可以捐赠到空(甚至反键)轨道,相互作用,这是稳定。
在乙烯(下图左)所有的碳氢键的平面烯烃,没有一个可以重叠的π键。
当添加一个甲基,说,在丙烯,其中一个碳氢键可以现在的pi-system对齐烯烃。碳氢键的一对电子可以捐赠到空π*轨道。
这可以通过“不共振”可视化,下面正确的,“共振”的形式显示断了碳氢键和一个新的碳碳π键。(引号来区分它从我们的传统观点只允许π键形成的共振和打破)。
这种基因混合结果的稳定分子。。尽管CH3在快速旋转,在任何给定时刻的至少一个碳氢键会有适当的几何与pi系统允许重叠。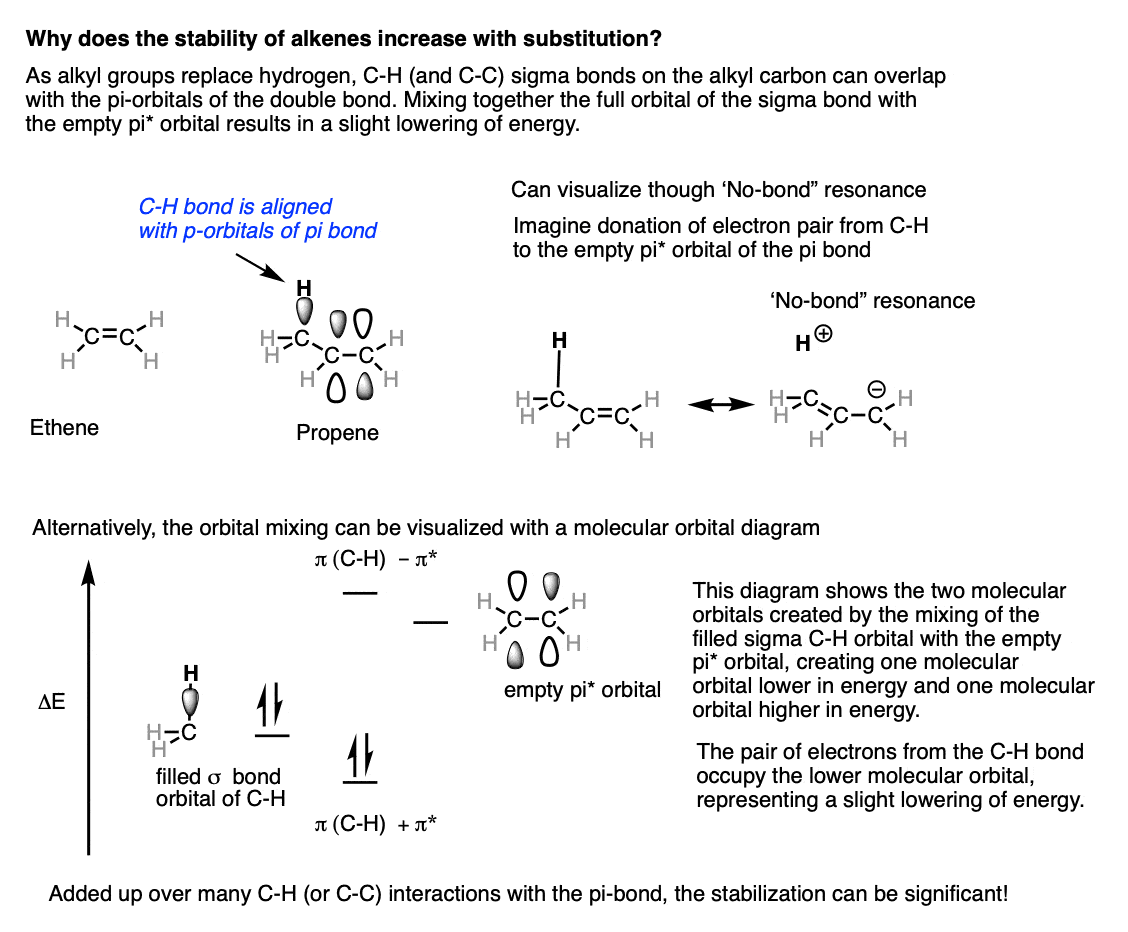
将略微延长碳氢键和碳碳π,加强碳碳σ。
附录2:反式-Cycloalkenes
99%的人读这将永远不会使用这个向下的脚注。
你会遇到在绝大多数分子,在环双键独联体。为什么?最生动的回答是试图使他们所提供的模型套件。
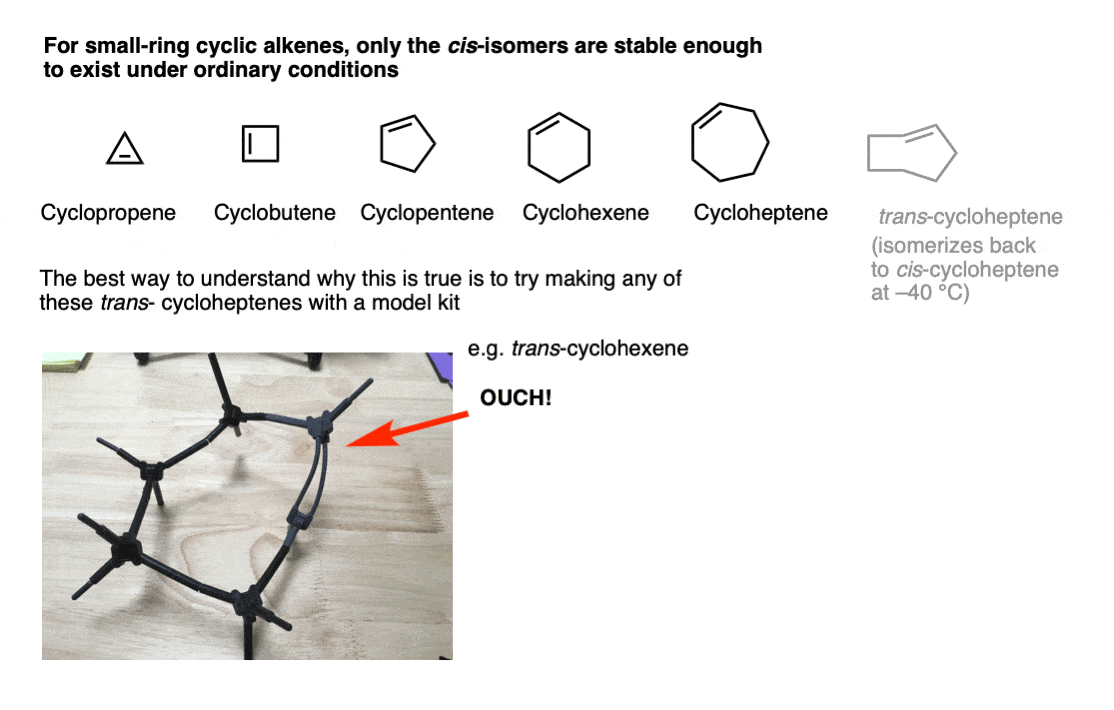
这是不一个快乐的双键。
然而在戒指的大小7,反式双键变得多是暂时性的稳定(尽管很短住在0°),和在一个环大小8有足够的floppiness环,其沸点可以测量[143°C !]。戒指大小超过8可以轻松容纳反式双键。
加氢的热量可以用来量化这些环的稳定性(请注意,这并不是全部,因为它没有考虑熵,并且会很大)。
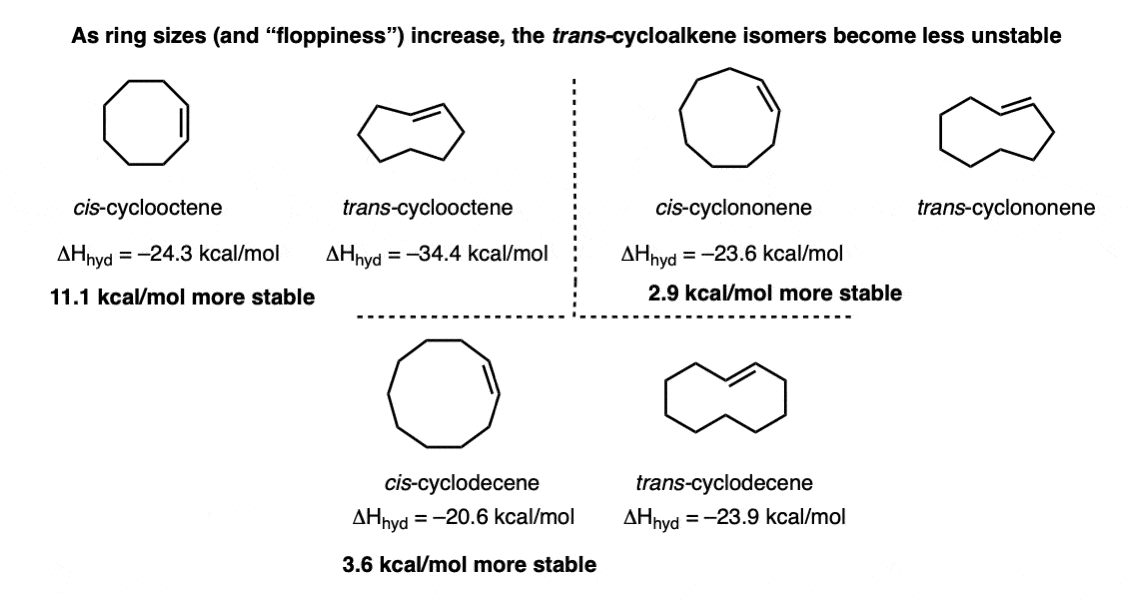
戒指大小11和12反式异构体实际上变成了更多的稳定(当允许与酸平衡),但回想一下,任何涉及平衡最终衡量δG的熵和δG还包括一个项(S)。事实证明,增加稳定性的主要因素的11 - 12,自己反式-cycloalkenes是他们更大的熵。看到这个引用。
测试你自己!
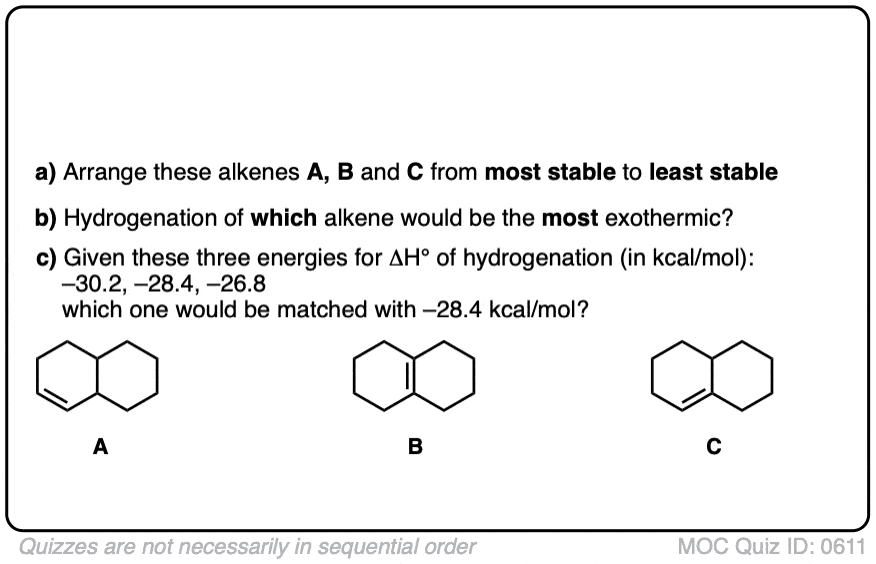 点击翻转
点击翻转
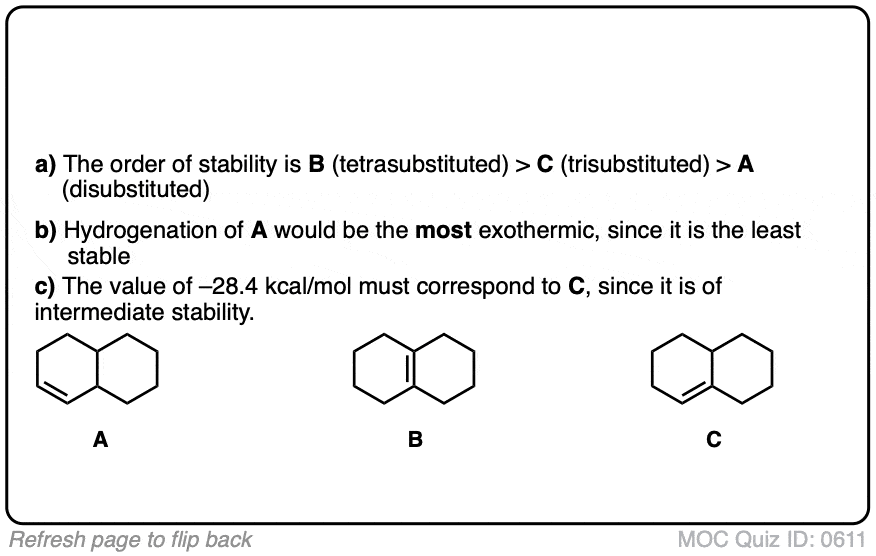
(高级)引用和进一步阅读
所有热氢化值引用在这里获得的NIST化学网络书。搜索通过CAS号永远不会失败。选择原始引用下面。
- 加热的有机反应。我的装置和乙烯的加氢热
g . b . Kistiakowsky h . Romeyn Jr . j . r . Ruhoff希尔顿·a·史密斯和w·e·沃恩
美国化学学会杂志》上1935年57(1),65 - 75
DOI:10.1021 / ja01304a019
Kistiakowsky教授的第一个(许多)论文有机分子的加氢热,他描述了设备在获得准确的加氢热数据所需的细节。结果站起来。 - 加热的有机反应。四、一些双烯和苯加氢
g . b . Kistiakowsky希尔顿·a·史密斯和约翰·r·Ruhoff w·e·沃恩
美国化学学会杂志》上1936年58(1),146 - 153
DOI:10.1021 / ja01292a043
包含的加氢热1,3丁二烯,苯,和其他不饱和分子,包括丙二烯(71.0千卡每摩尔)。 - 热氢化。第四,加氢部分独联体- - -反式-Cycloolefins1
理查德·b·特纳和w·r·tommeador一路
美国化学学会杂志》上1957年79年(15),4133 - 4136
DOI:10.1021 / ja01572a042 - 热氢化。第九。循环乙炔和一些杂项烯烃
理查德·b·特纳,公元Jarrett, p . Goebel和芭芭拉·j·马龙
美国化学学会杂志》上1973年95年(3),790 - 792
DOI:10.1021 / ja00784a025 - 的相对稳定性独联体- - -反式-CYCLONONENE、CYCLODECENE CYCLOUNDECENE CYCLODODECENE
阿瑟应付,菲莉·t·摩尔,威廉·r·摩尔
美国化学学会杂志》上1959年81年(12),3153 - 3153
DOI:10.1021 / ja01521a067
交流解决,当报道独联体- - -反式——cycloundecene(11)和cyclododecene(12人)允许平衡(通过加热催化TsOH)反式债券总价值青睐在平衡时(即有较低的ΔG)…即使反式十二碳烯有比它更高的焓(ΔH)独联体- - - - - -同分异构体。这是一个有益的提醒,焓(δH)只是吉布斯方程的一部分(ΔG =ΔH - TΔ年代),反式-cycloalkenes熵(S),这就解释了更高更大的稳定性。
那么为什么在环氧化反应,取代烯烃更反应?
是的,似乎有些矛盾的多取代烯烃是最被动的反应,如还有另外HX的烯烃环氧化反应。
与亲电试剂反应(如mCPBA)烯烃是亲核试剂。一般来说,更大的取代基的数量与烯烃,越亲核(富)。环氧化反应的过渡态有几个碳原子缺电子。更大的烷基取代烯烃的额外帮助捐赠电子可怜的碳原子的电子密度,降低过渡态的能量,导致更快的反应。
对不起,在分子轨道图为什么说π(碳氢键)+π*而不是σ(碳氢键)+π*分子轨道,当它是一个碳氢键σ键电子对捐赠?我又少了什么?
嘿,这是说“热氢化为一系列线性相当一致,(((non-branched)))单取代烯烃。“如果是支什么?假设比较稳定2-methyl-2-butene和2之间,2-dimethyl-3-pentene。我们需要仍然优先考虑取代基的数量最多的考虑?
2 2-dimethyl-3-pentene IUPAC命名不允许。它可以是2,2-dimethyl-2-pentene(三代的)或4,4-dimethyl-2-pentene(双取代的,可以顺式或反式)。
随便的,没有检查数据,我自信地说三代的烯烃是更稳定的反式双取代的1千卡每摩尔。
在这篇文章中给出的数据都是来自同一篇论文中,研究己烯的加氢的焓变。
https://www.sciencedirect.com/science/article/abs/pii/0021961487900589。
的加氢热偕的和反式相媲美的第一个小数位。
嗨,附录1,这是否意味着σ(碳氢键)轨道可以捐赠e -密度和ππ*轨道在C = C稳定吗?和捐赠到π*反键轨道,请问这会削弱C = Cπ键(因为我听说捐赠反键轨道削弱成键轨道)?非常感谢:)
嘿!轻微的修正,我抬起头来的数据qouted和偕的双键差不多稳定顺式键,不是一个反式债券。NIST给-117.8偕的氢化异丁烯,-118.5反式版本-114.5,独联体。
真讨厌。谢谢你带我的注意,我得考虑解决。