有机反应入门
稳定碳正离子的3个因素
最后更新:2023年3月22日|
碳正离子:性质、形成和稳定性
- 碳正离子是缺电子具有空p轨道的物质
- 由于缺少一个完整的八隅体并带一个正电荷,它们往往是公平的高能(即不稳定的)物种,通常被认为是短暂的中间体在许多化学反应中。
- 三个主要因素增加了碳正离子的稳定性:
- 增加…的数量相邻碳原子:甲基(最不稳定的碳正离子)<伯<仲<叔(最稳定的碳正离子)
- 相邻π键这使得碳正离子p轨道成为共轭pi系统的一部分(通过共振”)
- 相邻的原子孤这样就能给碳提供一个完整的八隅体。
- 相邻的吸电子基团不能给出孤对(如CF)3.,没有2)大大减少碳正离子的稳定性。
- 此外,碳正离子减少在稳定中有秩序烷基(最稳定)b>烯基>炔基(不稳定)
- 影响碳正离子稳定性的其他一些因素包括芳香性/反芳香性、平面性(桥头堡碳正离子不稳定)和涉及小环的特殊情况。
目录表
- 什么是碳正离子?
- 碳正离子的形成
- 稳定碳正离子的因素-取代
- 稳定碳正离子的因素-共振
- 应用碳正离子稳定性来理解反应
- 邻近孤对的镇定
- 共振和取代哪个更重要?
- 归纳影响
- 一些特殊情况
- 总结
- 笔记
- 测试你自己!
- (高级)参考资料和进一步阅读
1.什么是碳正离子?
带正电的碳原子带有三个共价键和一个空轨道,称为A碳正离子(或者更正式的说法是"正碳"离子,不过我们要用"碳正离子"[注1])
除了中心碳上的+1电荷外,绝大多数[注2]的碳正离子与中性离子非常相似硼化合物。

碳正离子和中性硼化合物通常都有
- 一个sp2-杂化中心原子
- 有6个价电子,
- 一个空的p轨道,
- 三角形的平面几何
- 键角是120°。
[我们是怎么知道的?x射线晶体学注3]
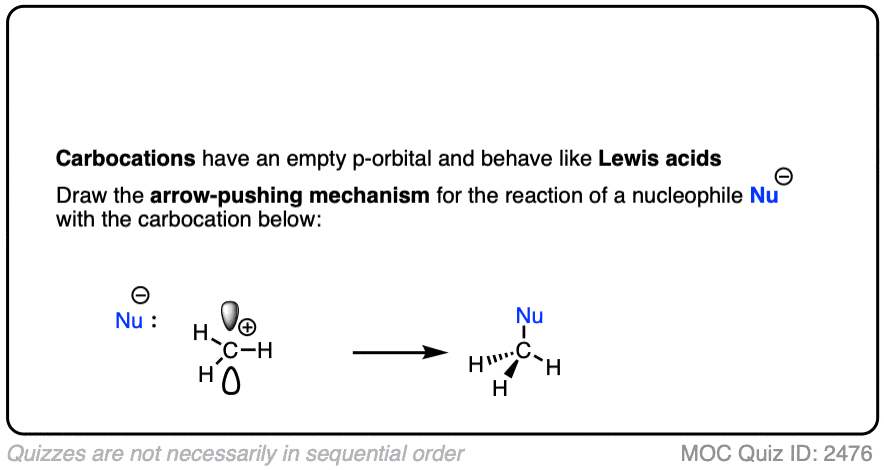
像硼化合物一样,碳正离子是缺电子的路易斯酸,很容易与路易斯碱结合,形成四面体3.杂化原子有一个完整的八层电子。
看看你能不能画出下面反应的曲线箭头。
 点击翻转
点击翻转
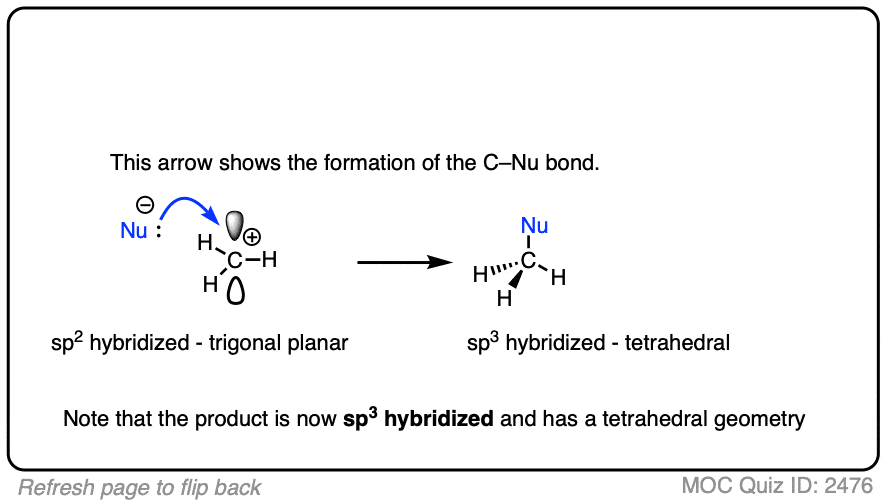
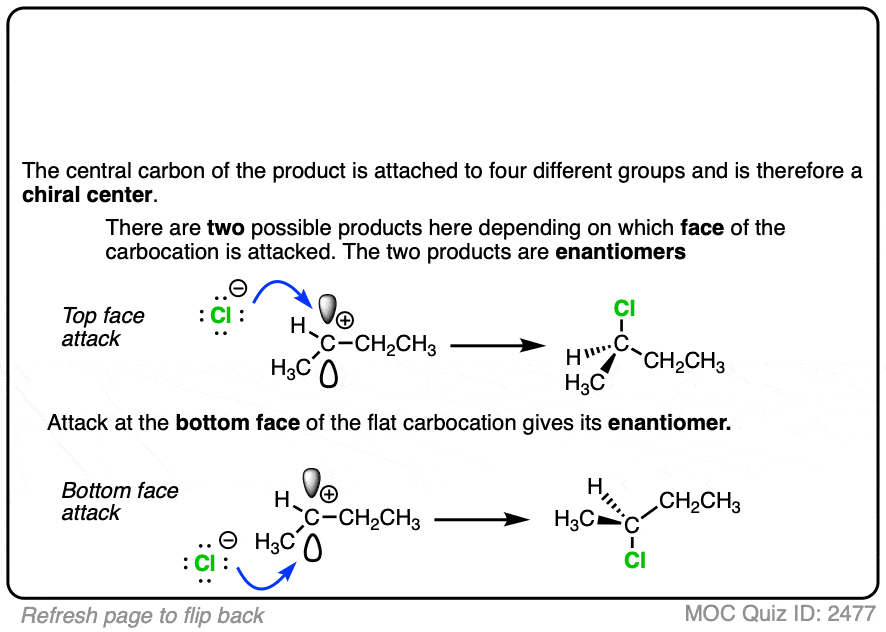
由于它们的三角形平面几何结构,碳正离子可以从空p轨道的任意面受到攻击。
要注意这可能会产生一对立体异构体的情况。
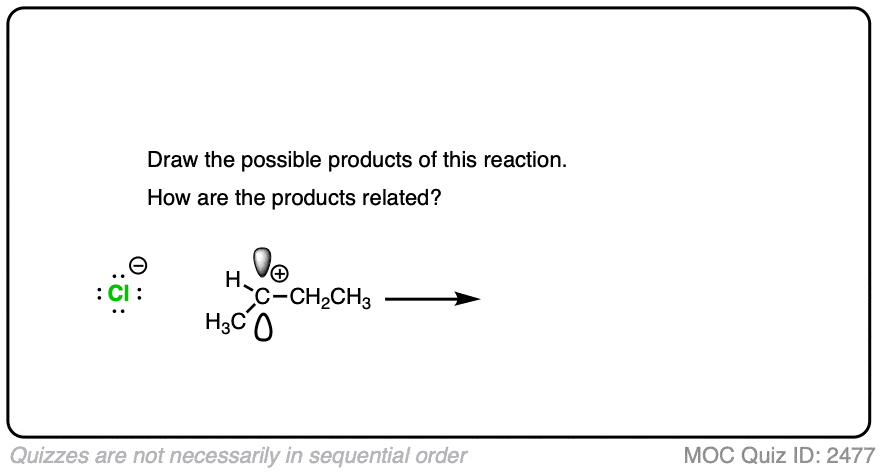 点击翻转
点击翻转
2.碳正离子的形成
碳正离子很重要中间体在许多反应中。(中间体,与过渡态相反,是反应中潜在的可分离物质,在反应坐标图中占据势能最小值。过渡态有部分键,寿命极短,不能孤立)。
由于碳周围缺少一个完整的八层电子并且带正电荷,因此碳正离子比中性碳化合物能量更高,也更不稳定。
一些涉及碳正离子中间体的突出反应是卤化氢(例如HBr, HCl和HI)的加成烯烃和单分子取代(SN1)和消除(E1)反应烷基卤化物。
在美国N1 /E1反应的第一步是损失a好离去基团(一般来说,一个非常弱的碱——见"什么是好的离去基团”)给出一个碳正离子。这通常在高极性溶剂中进行,如H2O或醋酸可以帮助稳定带电的碳正离子中间体。
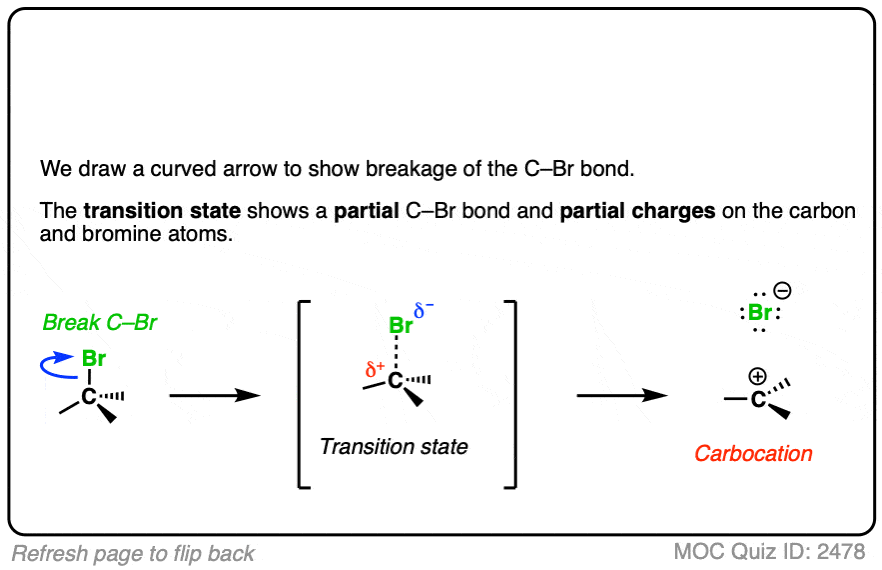
看看你能不能画出这个叔碳离子形成碳正离子的曲线箭头烷基卤化物,伴随着过渡态:
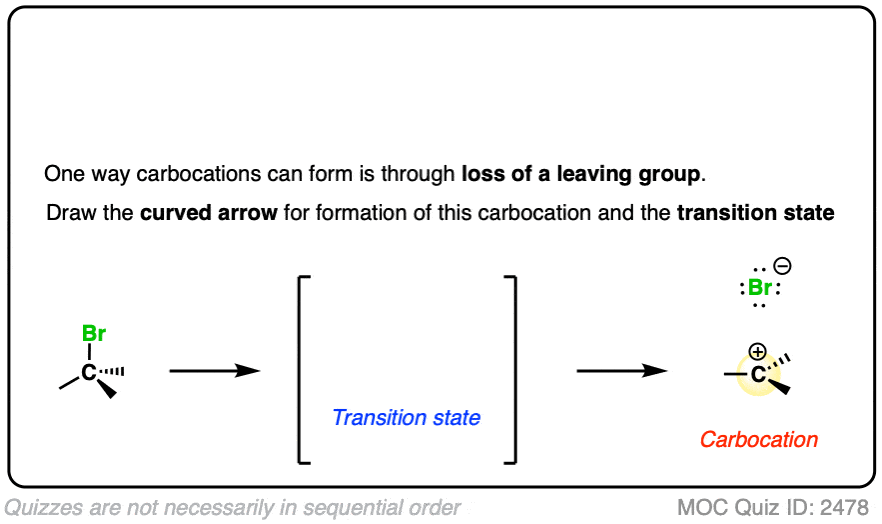 点击翻转
点击翻转
加入氢卤酸到烯烃,第一步是氢离子被C-C键上的一对电子攻击,生成碳正离子中间体。
看看你能否画出这个反应的曲线箭头推动机制和过渡态:
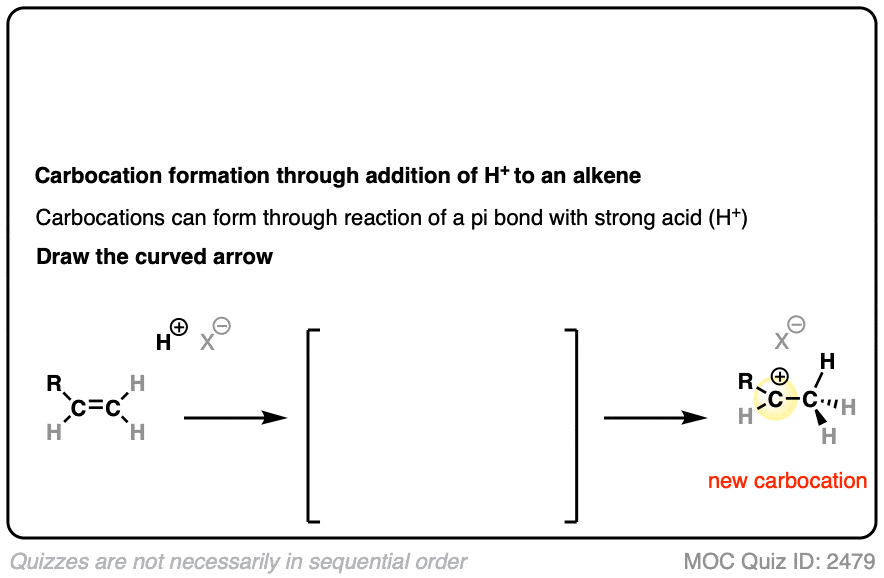 点击翻转
点击翻转
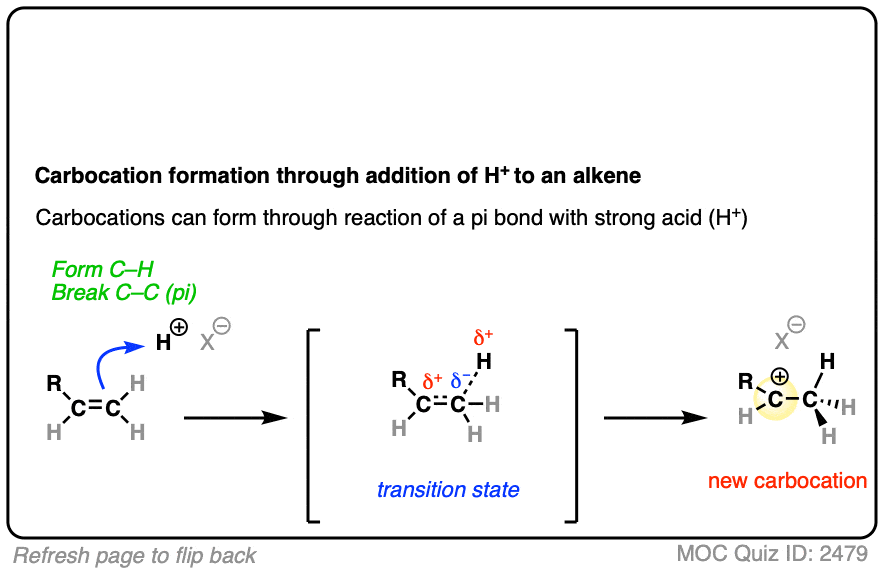
在这两种反应中,我们都是从能量相对较低的起始物质开始的,在通往碳正离子中间体的过程中,它会经过一个高能量的过渡态。
第二步,碳正离子与a反应路易斯碱在溶液中得到产物碳还是四面体,sp3.杂化。
这两个反应的反应坐标大概是这样的:
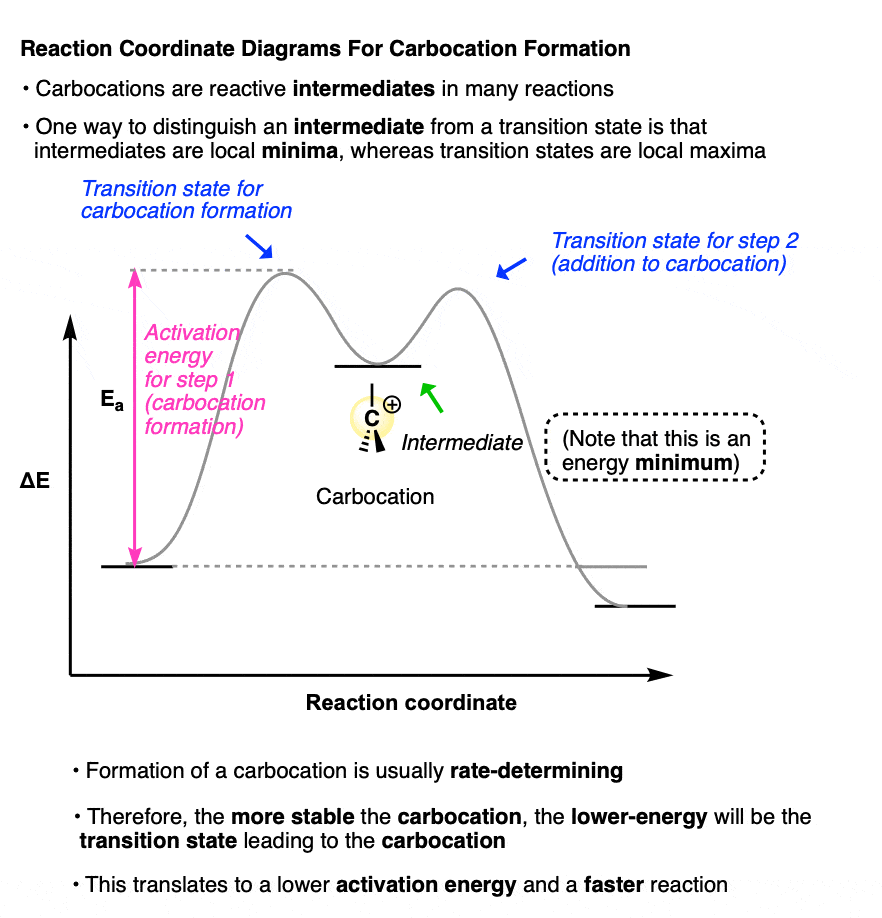
(注意碳正离子中间占据了一个当地的最低在这个反应坐标图上;这两个过渡状态是局部的maxima)。
为什么要提这个?
因为速率决定步骤每个反应都是形成碳正离子中间.
的更稳定的碳正离子中间碳正离子形成的过渡态能量越低,转化成活化能和一个更快的反应.
因此,如果我们了解控制的因素稳定碳正离子,这也能帮助我们理解为什么某些反应发生得很快,而另一些则不然!
3.稳定碳正离子的因素-取代
实验测量的稳定性[注意4]的碳正离子表现出以下趋势:
甲基(最不稳定)<伯<仲<叔(最稳定)
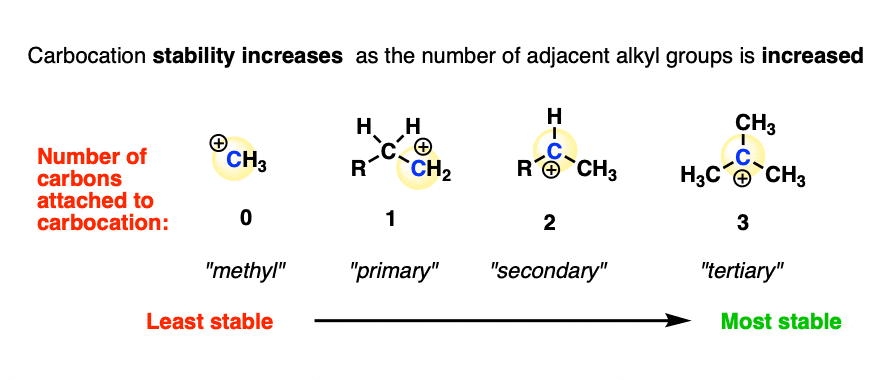
换句话说,碳-氢键被碳-碳键取代后,碳正离子的稳定性增加。
为什么?
碳正离子是电子贫乏的稳定通过邻居电子密度的捐赠电子的原子。
正如我经常告诉我的学生的那样,”当你很穷的时候,有富有的邻居是有帮助的”。
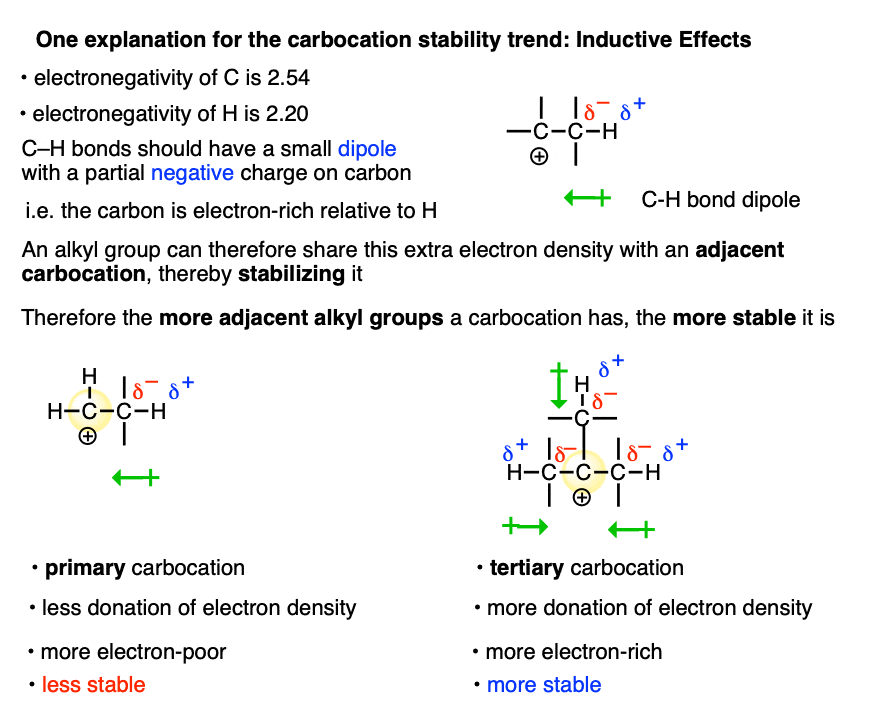
一种合理化这种趋势的方法是通过申请电感的影响。
碳的电负性(2.54)比氢(2.20)强。所以碳氢键有一个小偶极子碳带部分负电,氢带部分正电。
多个碳氢偶极子的电子密度可以相加。所以an的碳烷基一个基团会带一小部分负电荷,它可以给相邻的碳正离子,使它不那么缺电子。
当碳正离子直接连在氢上时,这是不可能的。
一个更令人满意的(一些!)解释来自于超共轭现象.
想象一下,把碳氢键(或碳氢键)上的两个电子和碳正离子的空p轨道排列在一起。然后想象一种“共振”形式,这些电子与p轨道共享,形成键(和氢离子)。
因为电子密度被分配给了空轨道,这应该是稳定对于空的p轨道(即碳正离子)
在本文中,我们没有足够的篇幅来讨论超共轭的所有含义,但它确实做出了一些可测试的预测,这些预测是通过实验证实的。[注5金刚烷基碳正离子的结构很有指导意义]
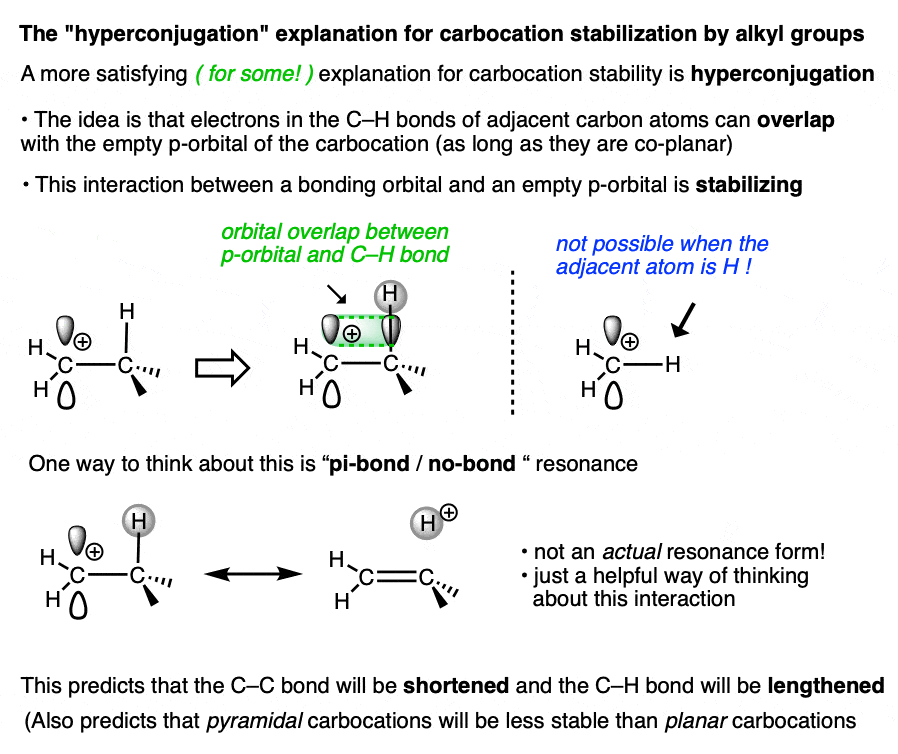
无论你喜欢什么理由,观察到的趋势都是一样的。的更多的代替的碳正离子,更大的它的稳定.
4.稳定碳正离子的因素-共振
有机化学中一个很好的工作原理是集中充电一般来说不稳定(高能)比稀释负责(低)注6]
我们以前见过的一个地方是极化率在美国,像碘离子I(-)这样的大阴离子比像F(-)这样的小离子更稳定,因为负电荷分布在更大的体积上。[这是造成H-I比H-F更大酸度的因素,也是造成H-I比H-F更大酸度的因素离去基团I(-)能力]
导致电荷“扩散”的另一个因素是“共振”。
在碳正离子中,比如n-丙基阳离子3.CH2CH2+),正电荷定位在一个碳上。
但是如果键是相邻到碳正离子,我们可以画出两种共振形式,正电荷在碳-1或碳-3上。
在共振杂化中,正电荷在这两个碳之间共享,每个碳的电荷密度为+ 0.5而不是+ 1.(这就是所谓的“共振离域”——电荷被涂抹在多个碳上)
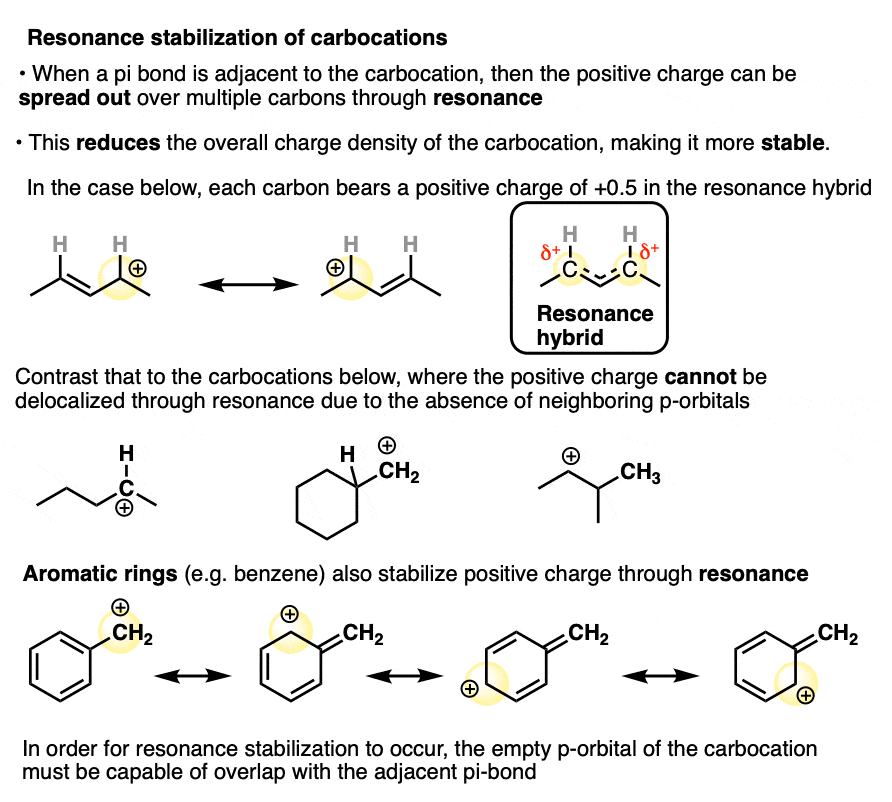
这种碳正离子(被称为烯丙基阳离子)相对于母体丙基阳离子是由许多测量证实的。[注意4]
当碳正离子与芳香环(如苯)相邻时,也可以看到类似的效果。这个碳正离子的稳定性,被称为苄碳正离子比“正常的”伯电碳正离子大得多。(事实上苄碳正离子和t-丁基正离子一样稳定,注意4)
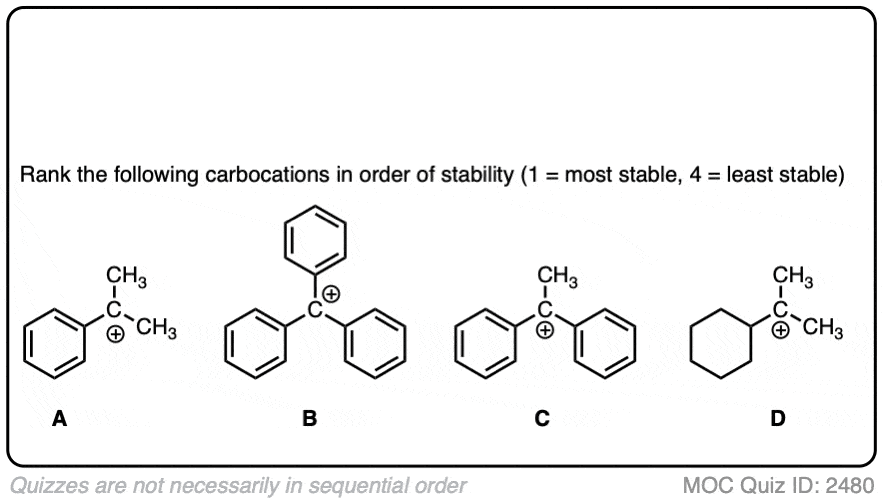
碳正离子的稳定性随电位共振形式的增加而增加。
例如,“三烷基”阳离子,Ph3.C(+)是非常稳定的,它形成一种结晶盐,可以放入瓶并无限期地储存在架子上。
 点击翻转
点击翻转
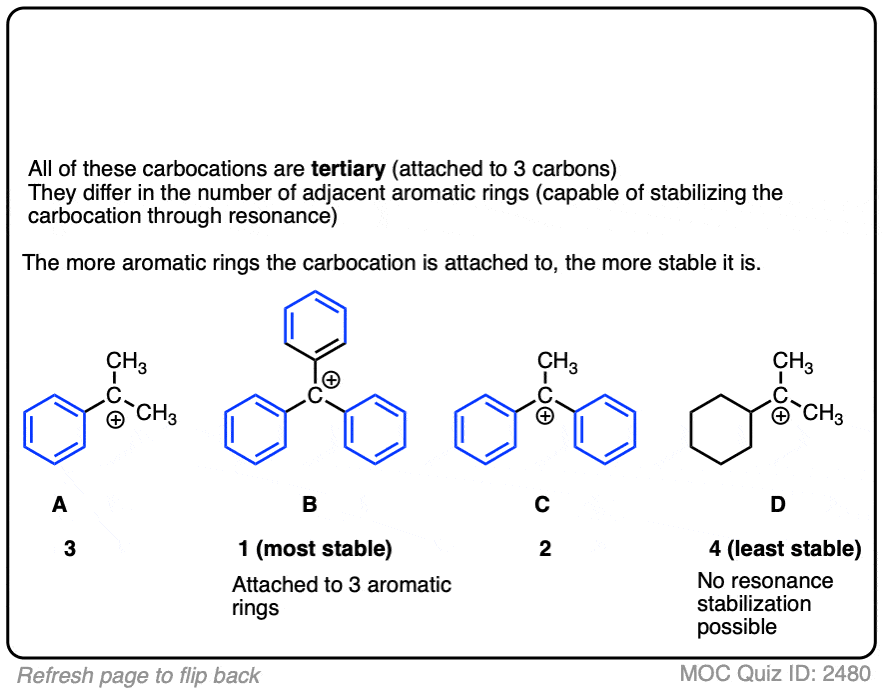
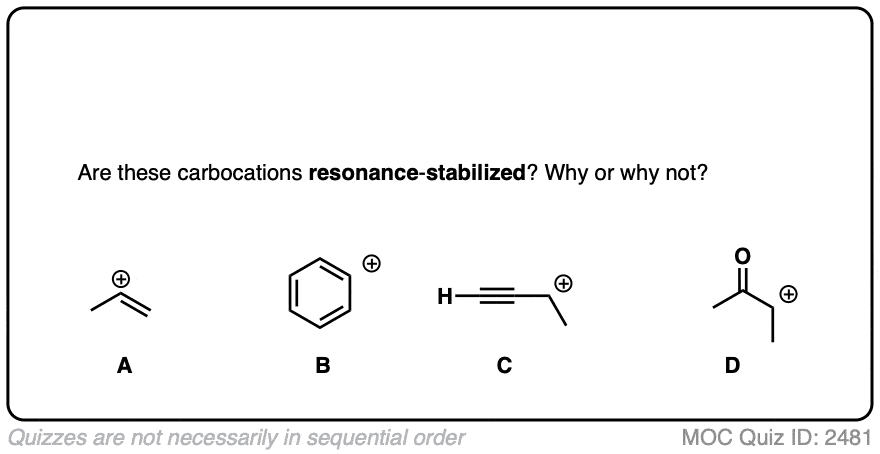
警告一句。为了使碳正离子通过共振稳定,碳正离子的p轨道必须能与相邻键的p轨道重叠。(参见文章-共轭与共振)
没有重叠就意味着没有离域,也就意味着没有增加稳定性。
通过回答下面的小测验来测试你对这个概念的理解。
 点击翻转
点击翻转
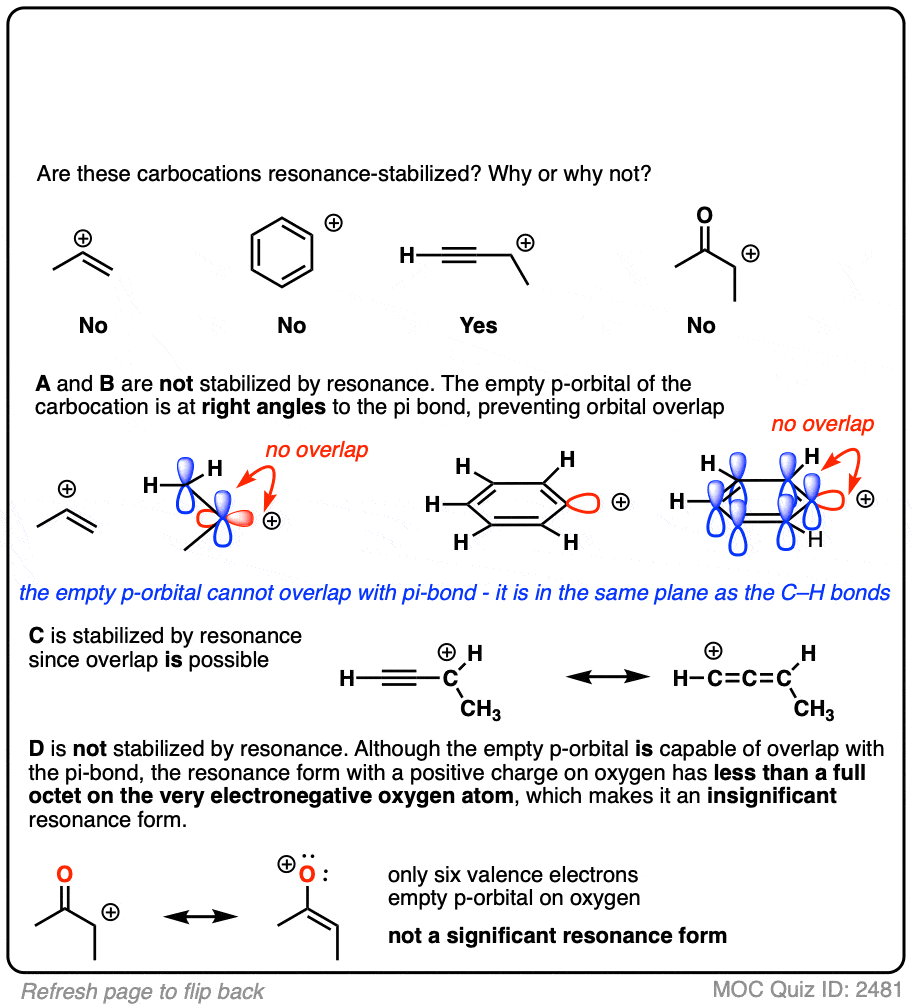
一个常见的错误是认为直接与键相连的碳正离子是共振稳定的。事实并非如此!键肯定是相邻到碳正离子。
另一种可能违反直觉的情况是碳正离子与C=O(或C=N)键相邻。有人可能天真地认为碳正离子是通过共振稳定的。
然而,如果你画出共振形式,你会发现,在形成C-C键和破坏C-O键的过程中,你最终会在氧上形成一个缺电子的物质,只有6个价电子。这种“共振形式”是如此高能量,以至于基本上对共振杂化没有贡献。
(像O这样电负性很强的原子在稳定负电荷方面很出色,但在稳定空轨道方面却很糟糕)
5.碳正离子稳定性在反应中的重要性
让我们回到碳正离子在几个关键的有机反应中作为中间体的作用上来。
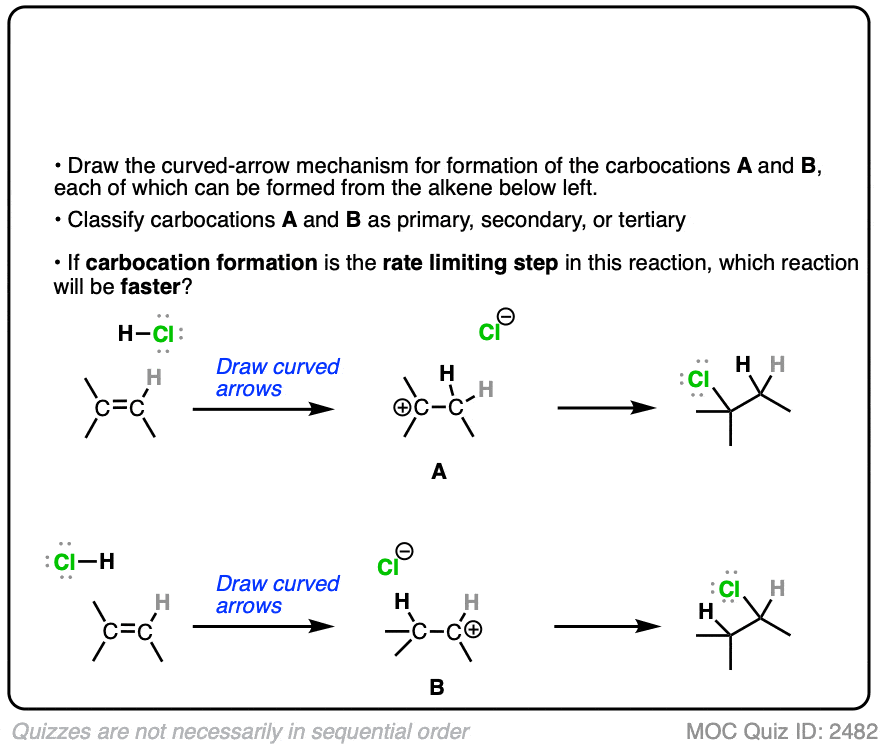
下面反应的速率决定步骤是质子化作用和H+键形成碳正离子中间体。
你认为这两种反应哪个更快?
 点击翻转
点击翻转
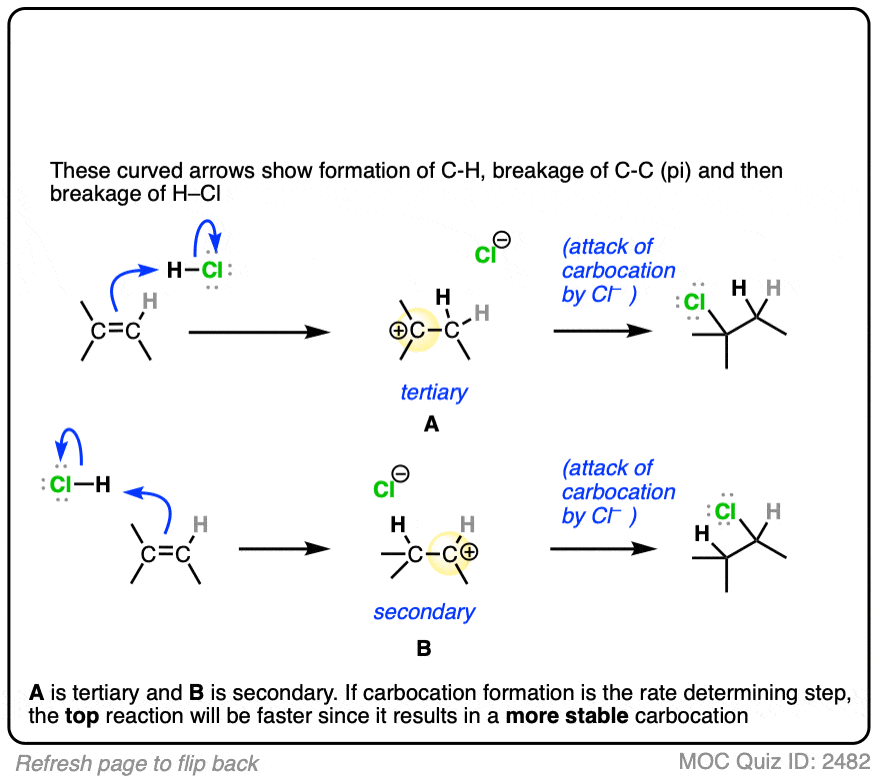
如果你回答正确,恭喜你!你已经表明你明白背后的原因马氏规则的像![参见文章-马氏规则的像]
让我们看另一个例子。
下面反应的速率决定步骤是a的损失离去基团形成碳正离子
这两个反应哪个进行得更快?
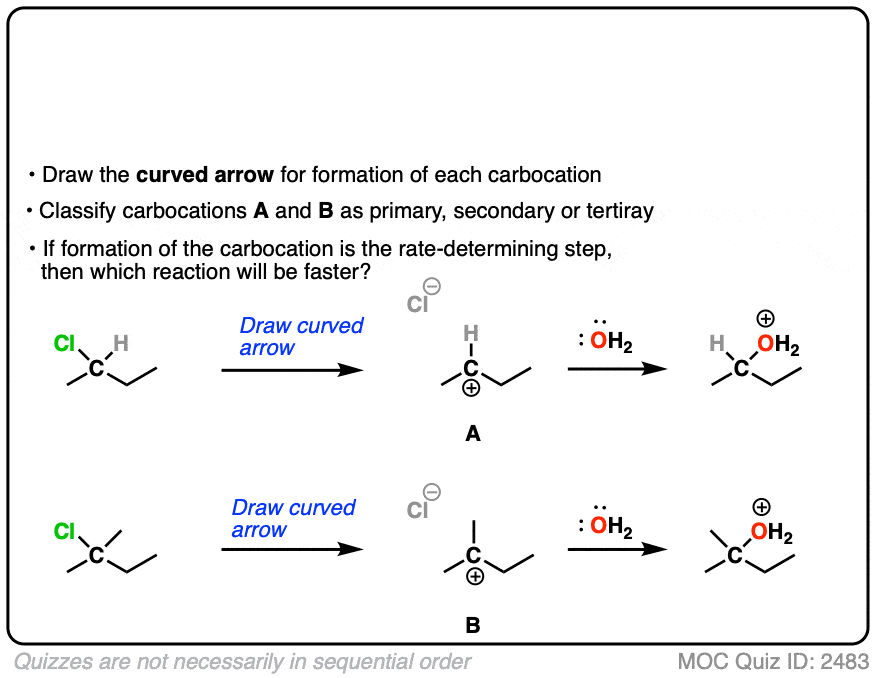 点击翻转
点击翻转
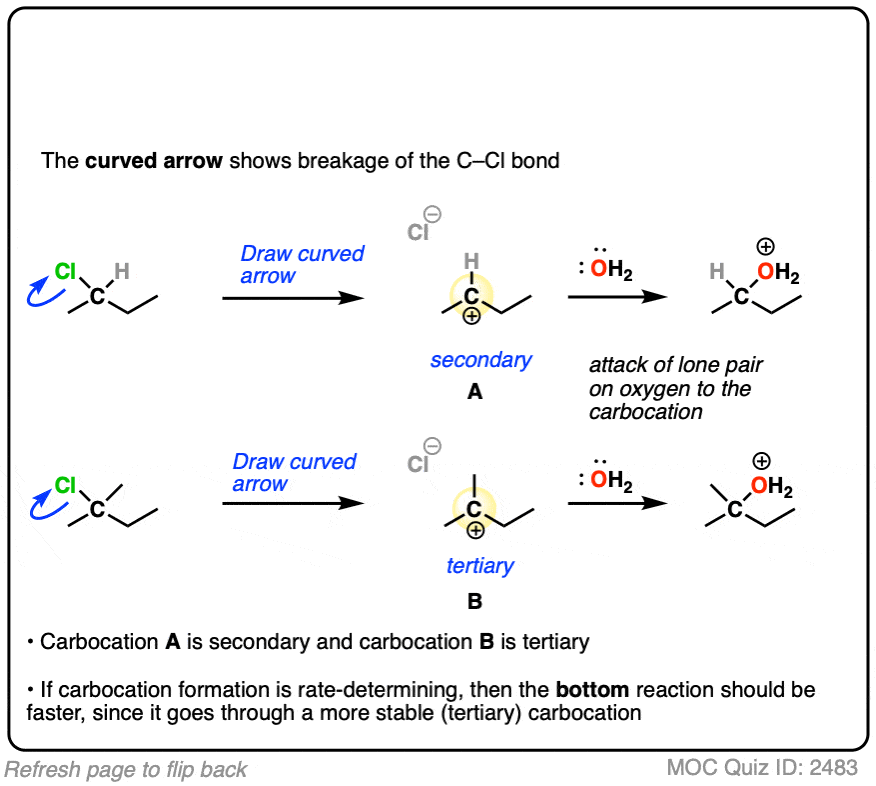
如果你回答正确,你就理解了决定反应是否通过S进行的关键因素之一N1,年代N2,E1或E2.(见文章:SN1/SN2/E1/E2 -底物)
6.稳定碳正离子的因素-相邻孤对
还有一个稳定碳正离子的因素我们还没讲到。
如果形成碳正离子相邻与带有孤对的原子(即a路易斯碱),然后这个原子可以把它的电子对给碳正离子,在这个过程中形成一个新的键。
这被称为“捐赠”(参见文章-π捐赠)
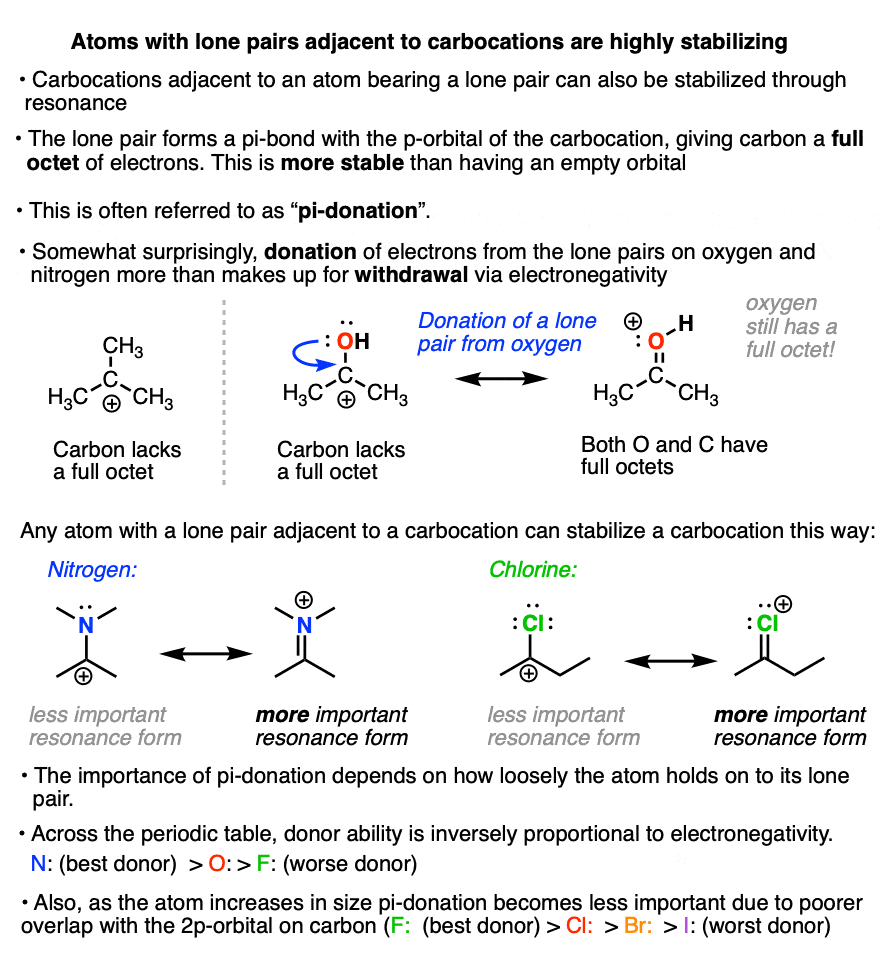
像氧或氮这样电负性很强的原子可以稳定碳正离子,这似乎有点违反直觉。
但是给予的最终结果是所有原子都有一个完整的八隅体,这是高度的稳定.(注意,尽管氧和氮会承受正式的带+1电荷,它们仍然有一个完整的八层电子!参见文章-如何计算形式电荷)
原子的孤对稳定相邻碳正离子的程度与其碱度成正比。原子碱性越强,给体越好。
在元素周期表的一行中,提供一对电子的能力与电负性成反比。所以,在其他因素相同的情况下,氮的孤电子对比氧的孤电子对更稳定,氧的孤电子对比氟的孤电子对更稳定。
会下来在元素周期表中,原子给出一对电子的能力与原子的价电子轨道与空碳的2p轨道重叠的能力有关。
一般来说,随着轨道大小的增加,轨道重叠(和提供能力)会增加减少.
所以氟比氯更适合给碳,氯比溴更适合给碳,溴又比碘好(碘的价电子轨道是5p和5s轨道,它们与碳较小的2p轨道不太匹配).
这是一篇关于碳正离子稳定性的文章,我想让它保持重点,但这一部分的内容非常重要,在整个有机化学中会一次又一次地出现。稍后您将看到一个应用程序-亲电芳香取代.
7.取代和共振哪个因素更重要?
所以影响碳正离子稳定性的因素有两个:取代(伯、仲、叔)和共振。
那么哪个更重要呢?
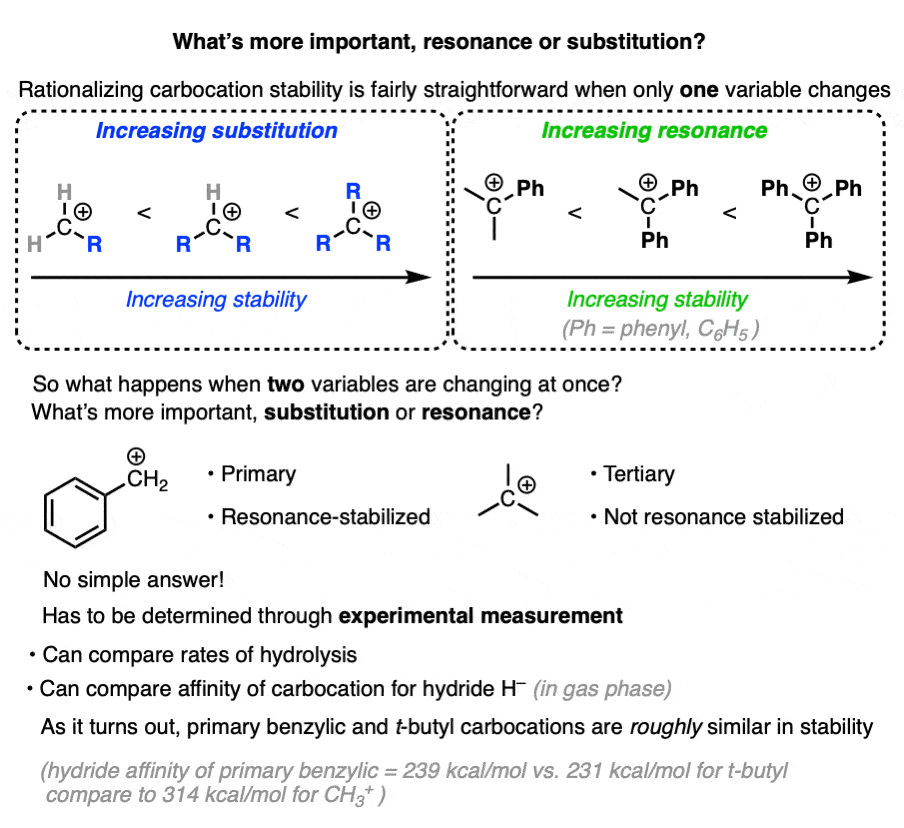
“他们这两个“重要”是我对这个问题的不回答。
回答这个问题的实际方法是看实验结果。
测量碳正离子稳定性的一种方法是取一系列相关的烷基卤化物和测量率它们在极性质子溶剂中水解的过程SN1很有可能。
这种方法的优点是它更接近实际的反应条件。缺点是它只适用于在S下形成的碳正离子N1个条件。)
另一种方法是衡量所谓的东西氢化物亲和力-碳正离子与一个当量的氢化物离子(H)反应所释放的能量- - - - - -).(虽然这可以应用于更大范围的碳正离子,但它实际上只适用于气相)。
伯苯基碳正离子的氢化物亲和力约为239千卡/mol,而a的氢化物亲和力为231千卡/molt-丁基碳正离子,所以它们的能量相当。
下面是一个包含一些值的表。看到注意4.
8.碳正离子不稳定的一些因素
既然给电子基团有助于稳定碳正离子,那么期望吸电子基团会破坏碳正离子的稳定就说得通了。
正如我们上面提到的,带孤对的电负性原子,比如O, N和F直接连着一个碳正离子会帮助稳定碳正离子通过捐赠。
出于这些目的,我不会考虑那些“吸电子基团”。
“吸电子基团”包括在内
- 碳原子附着在吸电子基团(如CF)上3.CCl,3.)
- 没有孤对的电负性原子(如NR)3.(+))
- 与a键成键的原子电负性更强原子(如C=O, CN, NO)2,所以2R,等等)。
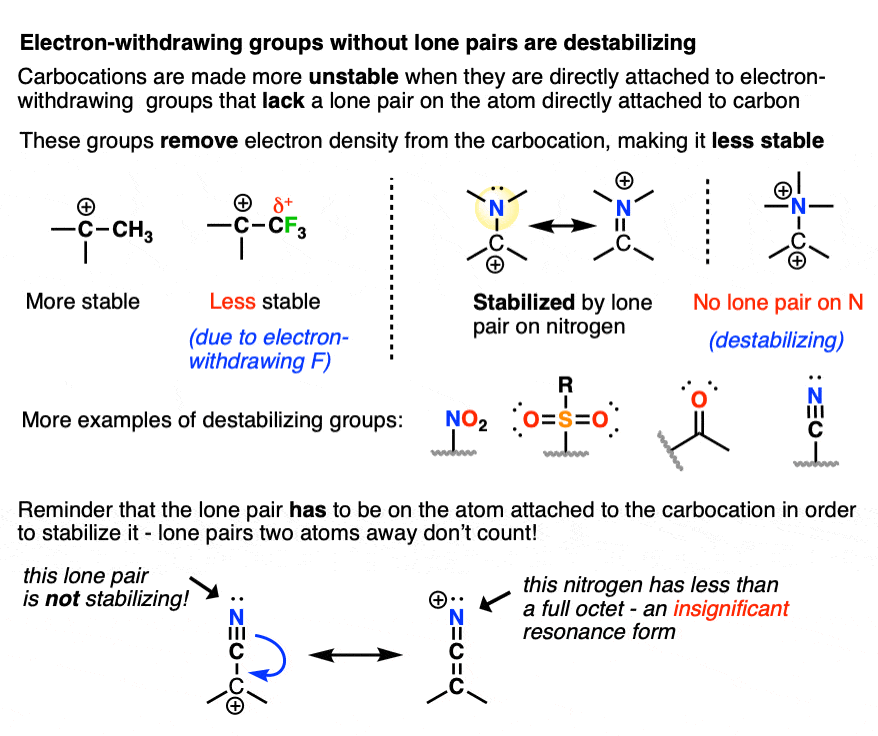
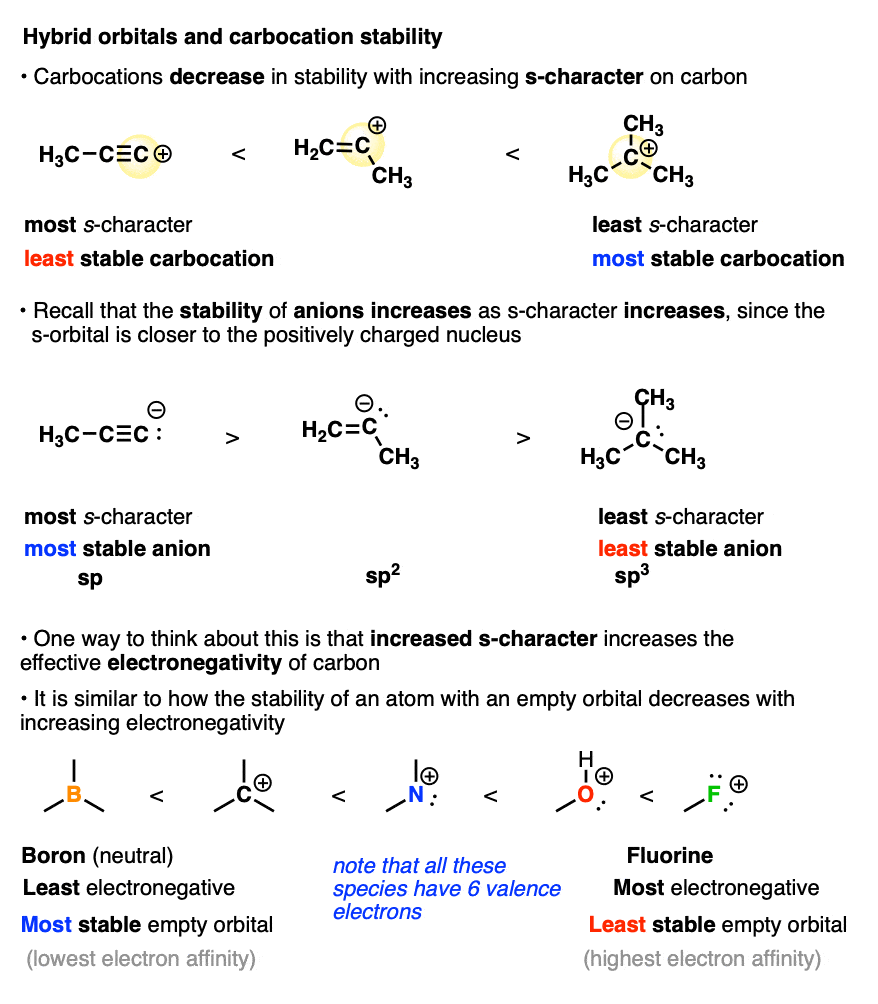
另一个使碳正离子不稳定的因素是碳原子中s字符的数量。
大家可能还记得炔烃碳氢键尤其酸性因为它们的sp轨道有50%的s轨道特征,而且s轨道离带正电的原子核更近,这有助于稳定电子的负电荷共轭碱(碳水化合物阴离子).
说到碳的稳定阳离子,这些都被扔进反向.
碳正离子的s型特征越多,空轨道离带正电的原子核越近。这使得碳原子核具有更大的有效电负性。随着s字符的增加,去除一对电子形成碳正离子变得越来越困难。(这可以通过测量氢化物亲合力或电子亲合力来量化)
桥头堡碳正离子也特别不稳定,因为它们不能达到理想的三角形平面几何形状,[请注意7小环上的碳正离子(如环丙基阳离子和环丁基阳离子)也是如此。[注8]
9.一些特殊情况
为了完整起见,我们可能应该提到最后一个因素,这是第二学期的话题,但对某些碳正离子的稳定性有很大的影响。
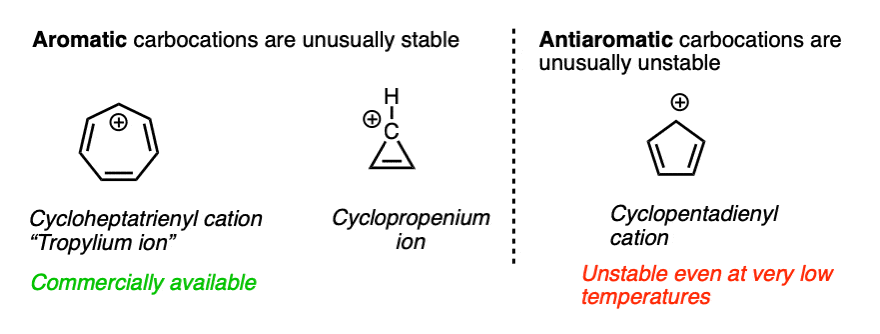
有些分子有特别的稳定的属性称为芳香性.(参见文章-芳香性规则)
一个相关的现象叫做antiaromaticity是谁造成了不寻常不稳定某些化合物的。(参见文章-抗芳香化合物和抗芳香性)
七三烯基(“tropylium”)阳离子,C7H7+是芳香由于其不寻常的稳定性,形成了一种稳定的盐,可以装在瓶子里出售商业.环丙烯离子3.H3.+也是芳香的,非常稳定。
另一方面,环戊二烯基阳离子,从表面上看应该是共振稳定的,实际上是anti-aromatic并且只能在非常低的温度下在精心控制的条件下短暂存在。
10.总结
[摘要]
笔记
注1.碳正离子的术语在历史上不以一致的方式使用。在现代用法中,带正电荷的三价碳被称为“碳离子”,而五元碳(在非常强的酸性溶液中观察到)被称为碳离子。
[F1-carbenium vs carbonium]
就我们的目的而言,“碳正离子”是指有三个键和一个空轨道的碳。
注2。一个突出的例外是乙烯基碳正离子。
[F2 -乙烯基碳正离子)
注3。用x射线晶体学测定了几种碳正离子的结构。
的结构t-丁基阳离子呈三角形平面结构(键角120°),C-C键长1.44埃。[裁判]
金刚烷基阳离子的结构也特别有趣。(Ref)
(F3-adamantyl碳正离子)
注4。实验测量了碳正离子的稳定性。
注5。金刚烷基碳正离子的结构具有指导意义。
注6。浓缩的电荷必须通过溶剂化来稳定。
请注意7.桥头堡碳正离子。
注8.小环
[气相稳定性并不总是与溶解速率相关]
测试你自己!
[Tfwo对映体X和y失去一个碳正离子。这两个物种有什么关系?
[在烯上添加质子]
(高级)参考资料和进一步阅读
参考文献
- 仲丁基阳离子的定量制备及重排焓
W.比特纳,E. M.阿内特和M.桑德斯
美国化学学会杂志1976年,98(12), 3734 - 3735
DOI:10.1021 / ja00428a072
本文介绍了一种新型的量热法来测量化合物的异构化热证券交易委员会-丁基阳离子变成叔超强酸溶液中的-丁基阳离子。由此得到的值为14.5±0.5 kcal/mol。 - 溶液中碳离子的稳定性。14.普通超强酸中碳正离子稳定性的扩展热化学标度
Edward M. Arnett和Thomas C. Hofelich
美国化学学会杂志1983年,105(9), 2889 - 2895
DOI:10.1021 / ja00347a060
本文给出了39种碳正离子的稳定性表,这些碳正离子是用生成热(在超强酸中由相应的甲醇电离)量热法测定的。 - 阳碳离子。由芳基羰基离子平衡导出的酸度函数(C0)
C. Deno, J. J. Jaruzelski和Alan Schriesheim
美国化学学会杂志1955年,77(11), 3044 - 3051
DOI:10.1021 / ja01616a036
碳正离子稳定性也可用p表示KR +,文中对其进行了定义。本文研究的碳正离子均为相对稳定的芳羰基离子。 - 中碳离子的氢化物亲和力乙腈和二甲亚砜解决方案
程金培,Kishan L. Handoo, Vernon D. Parker
美国化学学会杂志1993年,115(7), 2655 - 2660
DOI:10.1021 / ja00060a014
碳正离子的稳定性也可以用氢化物亲和力(R)来表示++ H- - - - - -- > RH)。本文所研究的碳正离子也是相当稳定的芳基碳离子,因为它们在两者中都是电化学测量的DMSO溶液或乙腈. - 甲基,乙基,异丙基和叔丁基自由基。对自由基及其相应的碳离子的热化学和结构的启示
A. Houle和J. L. Beauchamp
美国化学学会杂志1979,101(15), 4067 - 4074
DOI:10.1021 / ja00509a010
本文表三为基本的生成热烷基阳离子(甲基、乙基、异丙基和t-丁基),但是在气相。这些数字与解决阶段实验的直觉一致;稳定性从甲基->增加到乙基->异丙基- >叔丁基。 - 桥接或超共轭稳定碳正离子的x射线晶体结构
托马斯Laube
化学研究纪要199528(10) 399 - 405
DOI:10.1021 / ar00058a001
Laube教授对各种碳正离子的结构进行了非常有趣的比较和对比,包括金刚烷基碳正离子超共轭的非常明确的证据。C-C债券从1.528跌至1.431。C-C线从1.530延伸至1.608。100度角对110度角
化学通讯2022。58 12050
瓦格纳歌剧重排的故事。化学学报[J]
https://pubs.acs.org/doi/pdf/10.1021/ed077p858
奥拉——2001年。100年来的碳正离子及其意义。约21 66 59440-5957
好教程。
用最简单的方式解释科学是一门艺术。你做到了!
谢谢!
有机化学信息
很简单的理解化学的方法
你能解释一下如果我有一个苄基碳正离子和一个t-丁基碳正离子吗
哪个更稳定
由于苯基共振,1具有稳定性
第二句有9种可能的超共轭结构
请回答
亲爱的Jeetesh !你们应该知道共振比超共轭更明显也比超共轭更能稳定阳离子。
是的,伊克巴尔,共振主要是主导.....但这里已经发现t-丁基更稳定.....
库沙尔,你有推荐信吗?
莫里森·博伊德这样说。(http://www.chemicalforums.com/index.php?topic=33527.0)
正如一位评论者所说,替代的微小变化可能会打破平衡。
我没有实验参考资料,但在《有机化学中的电子流》一书中,保罗·斯卡德尔在第65页的“碳正离子稳定性排序”图表中声称,“叔正离子”比“苄基正离子”更稳定(苄基显示为伯离子,即两个H)。
我想叔苄基阳离子,sp2碳上有一个苯基和两个烷基,肯定比有三个烷基的叔阳离子更稳定(两者都有两个超共轭,但是芳香pi给体打败了第三个超共轭)。
仲苄基阳离子和叔烷基阳离子的区别就比较模糊了。
综上所述,碳正离子的稳定性可以从气相中氢化物的亲和力推断出来。参见《高级有机化学:Part A》第五版,由Carey和Sundberg编写,表3.10。第303页。氢化物亲和力越低,碳正离子越稳定。(苯基阳离子239千卡/mol VS t-丁基阳离子237千卡/mol)
我理解里奇的解释。这是令人满意的。谢谢你!
这是因为苯基不在一个平面上,为了发生共振,R基团应该在同一个平面上。这种化合物形状的变形是由于化合物中苯基的位阻作用造成的
这是个特例,t-丁基碳正离子更稳定.....
由于电荷离域,碳正离子苄更稳定。
好的解释,读了这篇文章就很容易理解
很高兴它对你有帮助。
伟大的文章。
好文章!
这篇文章真的帮了我很多!!i’很高兴你把它贴出来了
兄弟,你让这事简单点。你真的很棒!
哦,伙计,这真是太棒了。你告诉了我们学习时的每一个想法!我所有的疑虑都消失了!!n!n!n!
你能把碳正离子移位也加进去吗?
在重排系列中讨论过。
那"弯曲或伞形键"呢?你不认为弯曲的键参与了碳正离子的稳定性吗?
而ch3ch2ch2+和ch3ch2+是更稳定的碳正离子
都是主要的
前者具有较大的烷基,因此具有更强的诱导效应
而后者有更多的氢因此也就没有更多的超共轭结构。
这两个原因是相互冲突的......!!!!!
我们期望第一个是直觉但我们怎么能忘记超共轭比归纳效应更重要的事实呢?
都是伯碳正离子;它们的稳定性非常相似。丙基碳正离子可以通过氢化物移位重排生成仲碳正离子。
所以结论是丙基碳正离子更稳定....
因为它可以重新排列
不,一旦重排,我们讨论的是完全不同的碳正离子。
实际上我的主要问题是关于pinnacol和pinnacolone的重新排列。
H+攻击OH生成更稳定的碳正离子
那么它应该攻击哪个O呢?
哦哦
我我
CH3-C-C——C2H5
我我
甲基C2H5
哎呀,服务器省略了复合词中的空格,这把它搞砸了。
它是
(CH3) 2 C(哦)- C (OH) (C2H5) 2
非常感谢,这救了我的命。很感激。
我只有一点小问题。哪个更重要,共振稳定碳还是伯碳还是仲碳?由于这个事实,哪个更稳定,+CH2- ch =CH2还是CH3CH(+)CH3?提前谢谢你xD
好问题。在你引用的例子中,共振更重要。
谢谢。我现在正在准备下周的有机化学考试,这对我的学习很有帮助
很难找到阳离子稳定性的基本解释。谢谢!当然收藏你的网站。
这真是太有帮助了!有机化学很痛苦,其他有机学科有更多的解释吗?bdapp平台
比如光谱学,我真的需要帮助,可以使用像这个这样的好网站
谢谢。
你能解释一下为什么1,3,5庚-三烯碳离子(sp3碳上的+)比三苯基碳离子更稳定吗?
芳香性。看到的://m.deriinvest.com/2017/02/23/rules-for-aromaticity/
首先,谢谢你解释得这么好。
但是,你能告诉我,一般哪种效应更重要,归纳效应还是超共轭效应?
比如,如果有乙基碳正离子和2甲基丙烷碳正离子(伯碳正离子)哪个更稳定?
从超共轭的角度来看稳定性要强大得多,但从归纳效应的角度来解释它要容易得多。如果你学的是化学专业,我会花时间学习超共轭并将其应用到你的学习中。这是一个非常强大的概念。
嗨!谢谢你的帮助:)
我有一个问题。仲碳正离子会比伯碳正离子和卤素键更稳定吗?这是一个练习测试,我有点困惑
没有看到确切的例子很难说,但我猜后一种情况会更稳定,因为卤素可以提供一个孤对,分子上的每个原子都可以有一个完整的八隅体。这比有空轨道的自由碳正离子更稳定。
你能告诉我叔自由基、苄基自由基和烯丙基自由基的稳定顺序吗?
试着看看叔键、苄基键和烯丙基碳氢键的强度。因为碳氢键强度测量的是均裂劈裂,那么你就会得到自由基的稳定性。碳氢键越弱,自由基越稳定。
你好。我有一个问题我们是否可以说共振因子是更有效的因素,除非芳香性受到威胁?
你好,
我想知道你是否可以张贴这些样本问题的答案,请?我在做,但我没有办法检查它是否正确。
感谢,
助教阮
嗨,每种情况下,第一个碳正离子更稳定。这应用了我们学过的稳定碳正离子的3个因素。
叔碳正离子比仲碳正离子更稳定
烯丙基(共振稳定)碳正离子比非共振稳定碳正离子更稳定
与孤对原子相邻的碳正离子(氧)比不与孤对原子相邻的碳正离子更稳定。
希望这对你有所帮助
詹姆斯
大家好,为什么二级烯丙基碳正离子比叔碳正离子更稳定?谢谢你!
嗨,莫尼卡
有几个因素并不总是很容易通过观察来判断——我们需要做实验。比如我们知道碳正离子从伯离子到仲离子再到叔离子的稳定性都在增加。
我们还知道,如果碳正离子是共振稳定的,它们的稳定性会增加。
然而,哪个因素更重要呢?取代模式还是共振模式?
光看是不可能算出来的。我们必须做实验(我们确实做了!)[通过测量“电离率”]
这些实验告诉我们,二级烯丙基碳正离子比普通的(非共振稳定的)叔碳正离子稍容易形成。
为什么呢?问得好(这就是问题变得复杂的地方)。可能是因为邻近的p轨道提供的电子密度比邻近叔碳正离子的超共轭碳氢键提供的电子密度要大。
这些因素可以保持微妙的平衡。如果我可以打个比方的话,这有点像运动队。在足球比赛中,进攻和防守哪个更重要?嗯,它们都很重要。我们如何知道它们的相对重要性呢?通过玩大量的游戏,并试图通过查看数据来找出答案。幸运的是,在化学中,一摩尔的物质让我们有机会玩6 × 10^23个“游戏”,所以我们可以相当可靠地弄清楚这一点。
希望这对你有帮助!詹姆斯
对于像我这样的极客来说,有机化学一直是最令人兴奋和美丽的学科,所有这些文章都激励我更深入地研究这个学科。bdapp平台
阿门,兄弟
你好,詹姆斯,
谢谢你简洁的解释。我不是有机化学家,我有一个关于碳正离子稳定化的问题。你认为把碳正离子放在能稳定它的东西旁边可能会使它稳定吗?比如溶剂化效应,或者带负电荷的物质?比如静电稳定?
在这三个例子中,碳正离子是通过分子内效应稳定的,那么分子间稳定呢?
谢谢。
碳正离子在超强酸溶液中相对稳定。乔治·奥拉就是这样研究它们的,这帮助他获得了诺贝尔奖。http://www.nobelprize.org/nobel_prizes/chemistry/laureates/1994/olah-lecture.html
谢谢。
你好,詹姆斯,
我想向你请教一下。我一直在为这个问题绞尽脑汁,但我似乎还是不明白。
假设有两个仲胺。第一个取代基是丙炔(2-丙炔)第二个取代基是甲基。在第二个胺中,一个取代基是(吲哚-2-基)甲基(胺通过亚甲基连接到吲哚的2号位置),第二个取代基是甲基。现在,在这两种情况下,一个仲碳正离子在胺氮旁边形成。哪个应该更稳定?
在这两种情况下,氮通过给孤电子稳定了正电荷,但是炔基和吲哚基部分呢?我想它们都应该通过离域产生稳定作用但是哪一个能更稳定带电的物种呢?那归纳效应呢?他们应该在这个案例中扮演重要的角色吗?我很困惑……
嘿,詹姆斯……
为什么中间带正电的氧比碳正离子更不稳定
氧带正电的中间产物有两种。中间氧有一个完整的八隅体是可以的(通常来说比碳正离子更稳定)。中间产物中氧的八隅体小于一个完整的八隅体是非常不稳定的,因为一个电负性很强的原子(氧)如果小于一个完整的八隅体,就会有巨大的势能(因此不稳定)把电子拉向原子核。
带正电的氧是指一个带6个电子的电子。它是一个电负性更强的元素,所以会有更大的电子亲合力,把电子拉向原子核。非常不稳定的局势。
嗨!
我只是想知道,在叔碳正离子和共振稳定的碳正离子之间哪个更稳定?(就像第2条一样?)
谢谢你!好文章!
我没有找到任何关于碳不稳定的文章
稳定负电荷的一些因素:
//m.deriinvest.com/2012/02/27/7-factors-that-stabilize-negative-charge-in-organic-chemistry/
(CH3) 2-C + -COOH,这能共振吗?我的意思是有π和+ 5电荷共轭系统....但我在做一个问题,而这不是答案。
那么为什么它不能产生共鸣,请回答
共振形式最终会在氧上得到少于一个完整的八隅体,这是非常不稳定的。这不是一个重要的共振形式。
无共振稳定。如果打破C=O键,形成C=C键,就会留下一个只有6个电子的氧,非常不稳定。
这些例子的答案在哪里?
我想知道底部的应用问题是否有答案来检查我们自己??
你好,请问哪个碳正离子更稳定,(CH3)3C还是(C2H5)3C ?
如果烷基中碳原子数增加,它的+I效应会减小还是增大?
也许三乙基的稳定性会有一点提高。相应卤代烃的电离速率会告诉你。
那么如果一个仲碳正离子有一点共振稳定性而一个叔碳正离子(没有共振稳定性)哪个更稳定?(我的课本上说中学有共鸣……)
亲爱的詹姆斯:
我对-NH2 -OH没有问题,因为我们在EAS中建立了它们通常是给电子的。但我不明白为什么卤化物会稳定碳正离子。在所有的教科书中都说,3p和2p原子轨道的不匹配导致了共振离域的减弱,并赢得了卤化物的感应效应,使它们具有吸电子性。所以它减少了电子密度在芳香族反应中间产生了更大的正电荷。但是我们这里有相同的卤化物和相同的碳正离子(除了它不在环上)但是它现在提供了什么区别?谢谢!
“应用概念”的问题有答案吗?
非常感谢,先生!你对金钱和电子的比喻让这个概念变得简单多了!愿你拥有更多的力量!
非相邻的孤对原子有可能稳定碳正离子吗?在布朗的第八版《有机化学》中有一个问题,问为什么CH2CHCOOH (https://image.ibb.co/cdThRJ/structure_1.png) + HCl形成CH2ClCH2COOH而不是CH3CHClCOOH,因为仲碳正离子通常更稳定。我想知道你是否能让碳主链在自己身上卷曲(https://image.ibb.co/d6eBLd/structure_is_this_what_s_happening.png)所以羟基上的孤对可以帮助稳定伯碳正离子?
抱歉,这些分子模型里多了一个碳。原料的正确结构是(https://image.ibb.co/nOFkfd/structure_1.png),我提出的稳定碳正离子的正确结构是(https://image.ibb.co/cxTSty/structure_is_this_what_s_happening.png).
我想这也可能是一种共振结构(https://image.ibb.co/hj8Vfd/structure_contributing_resonance_structure.png).
可能发生的是分子内亲核攻击形成某种环。“Anchimeric援助”。
不管我在哪里上网,我总会在这里结束。你的教学方式太棒了,真是太棒了
我希望这种情况能继续下去!
如果伯烷基卤化物被邻近的氧原子稳定,它能发生SN1反应吗?或者碳正离子还会因为太不稳定而不能这样反应?
这取决于你对“邻居”的定义。如果氧直接连在同一个碳上(比如H3C-O-CH2Cl),那么氧就很容易和C形成π键,Cl-就很容易被取代。例如,见苄氧甲基氯。(这些东西往往不稳定)
如果你说的相邻指的是碳正离子相邻碳上的C= 0,那么它就不稳定。
你好先生!
我有一个问题。
哪个更稳定
苯基阳离子还是CH2(+)-环丙烷??
这是一个很好的问题,数据有些矛盾。环丙基甲基阳离子通常被认为比苄基更稳定。我正在寻找比March 5th ed. p. 222更好的参考资料,但其中的参考资料都是很好的,但有些模糊的评论。水解速率表明环丙基甲基阳离子更稳定。
然而,另一种回答这个问题的方法是看13c核磁共振来确定碳正离子的化学位移。化学位移越负,越不稳定。2-环丙基碳正离子的化学位移为-86.8 ppm, 2-苯丙基碳正离子的化学位移为-61.1,表明苯基具有更好的稳定作用。看到https://pubs.acs.org/doi/10.1021/ja00731a026
从气相解离能来看,叔丁基碳正离子比苄基碳正离子(238 kcal/mol)稳定约7 kcal/mol (232 kcal/mol),但取代基效应会大大改变这一数值。资料来源:March’s Advanced Organic Chemistry第5版。表5.2页224。
谢谢你,先生,你的文章非常有帮助,它们帮助我更好地了解我的宿敌O-chem
谢谢你! !
哪个碳正离子更稳定
甲基环丙基阳离子或环丙基阳离子
环丙基甲基。环丙烯基迅速重排成烯丙基阳离子。
环丙烯阳离子具有芳香性,可在瓶中保存。但是是否可以储存甲基环丙基阳离子,因为它更稳定。
你好,詹姆斯,谢谢你清晰的解释。
一个关于碳正离子的问题。我们说越稳定的碳正离子与亲核试剂反应越快。我们把热力学稳定性和动力学联系起来了吗?
嗨,成林,我假设你指的是第5节下的图像。
这些反应的总体动力学将由碳正离子的形成决定,这是限速步骤。通常碳正离子越稳定,其形成的活化能(“晚期”过渡态)就越低,反应的总速率就越快。
它不应被解释为碳正离子的稳定性与“秒”(即亲核试剂快速加到碳正离子上)步骤的速率之间存在关系。