醇、环氧化合物和醚
威廉姆森醚合成
最后更新:2023年7月9日|
所有关于威廉姆森醚合成
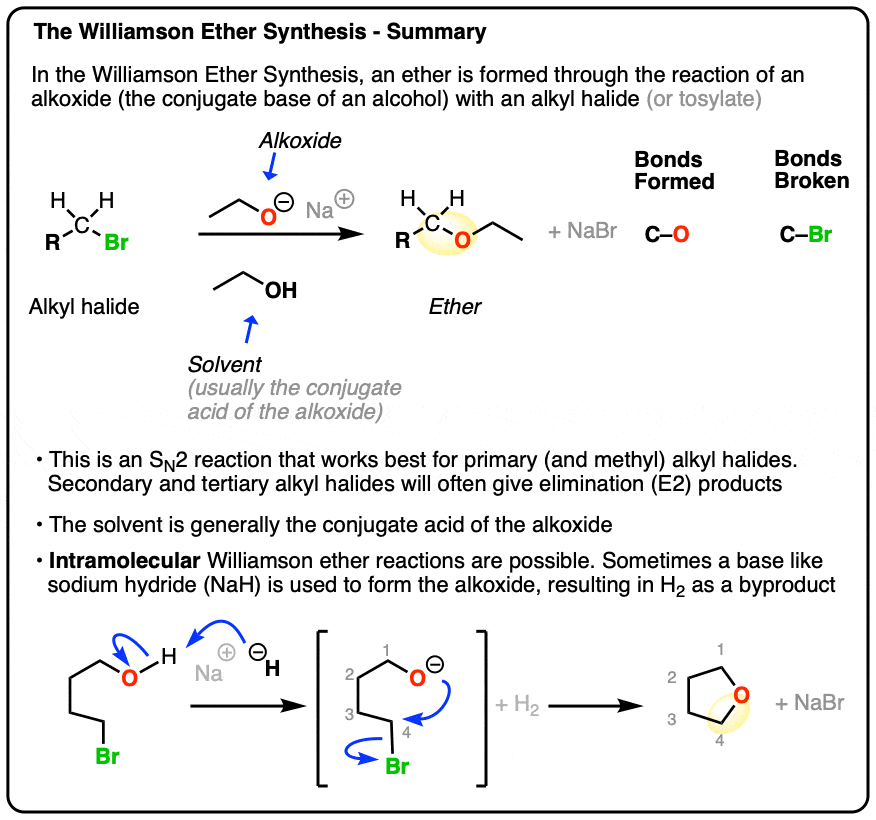
- 在威廉姆森醚合成,烷基卤(或磺酸盐,如甲苯磺酸盐或甲磺酸)发生亲核取代(SN2)由一个醇盐给一个醚。
- 作为一个年代N2反应威廉姆森最适合初级(甲基)烷基卤化物。二次烷基卤化物往往会接受被淘汰(E2)。三级烷基卤化物完全失败。
- 溶剂一般共轭酸的醇盐(例如NaOEt / EtOH),以避免形成在溶液中醇盐的混合物。有时基地像氢化钠(不)是用来形成醇盐,提供氢气(H2)作为副产品。
表的内容
- 威廉姆森醚合成是什么?
- 为什么我们使用R-O(-),而不是R-OH作为亲核试剂吗?
- 在威廉姆森醚合成烷基卤化物工作好吗?
- 从一个酒精:好的和坏的选择的基础
- 我们如何选择威廉姆森醚合成的溶剂?
- 摘要:威廉姆森醚合成
- (高级)引用和进一步阅读
1。威廉姆森醚合成是什么?
在最后发表,我们讨论了醇的酸碱性质。两个帖子前我们说,酸碱反应常常被用于“设置”替换和消除反应的醇。在这篇文章中,我们将讨论什么是最好的最后一点——的例子威廉姆森醚合成。
的威廉姆森醚合成是一个古老的反应,可以追溯到1851年,但没有被超越。那里不是一个简单的方式进行醚。
这是一个类型的反应我们已经见过很多次了——一个年代N2 deprotonated之间的反应酒精["醇盐”)和一个烷基卤,形成一个醚。(见文章:的年代N2机制)
请注意,我们形成和打破债券在碳——教科书的迹象替换的反应。
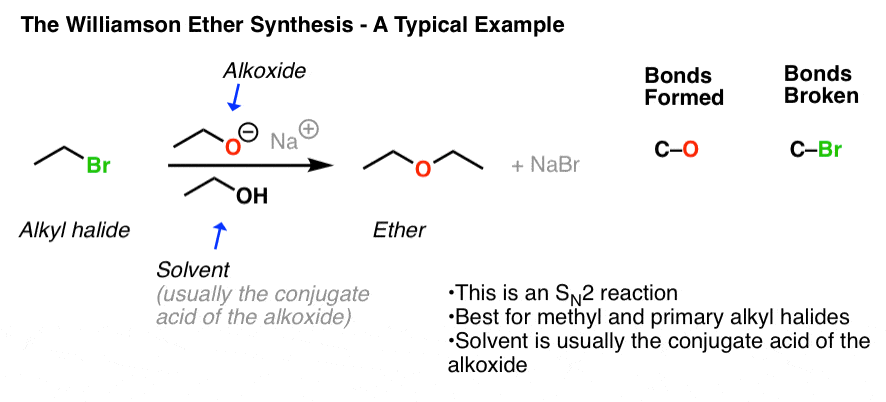
这是标准的反应。它的工作原理。但是仅仅通过观察一个“工作”的威廉姆森,我们只得到一半的照片。在这篇文章的其余部分我们会在某些方面,威廉姆森可能出错,并回答下列问题:
让我们挖的。
2。为什么我们用RO- - - - - -而不是卢武铉作为亲核试剂?
你可能会注意到威廉姆森的第一件事是我们使用的事实醇盐(罗- - - - - -)除了酒精(卢)反应。你可能会问,何苦呢?
不会卢武铉与一个反应烷基卤化物RO一样- - - - - -还是给我们一个吗醚吗?
答案回到我们谈到两年前的帖子:t他共轭碱总是更好的亲核试剂。罗的反应- - - - - -与一个烷基卤化物总是太多快卢武铉的反应,因为电子密度较高亲核试剂(氧气)。这就是为什么我们使用反渗透- - - - - -。(见文章:是什么让一个好亲核试剂?)
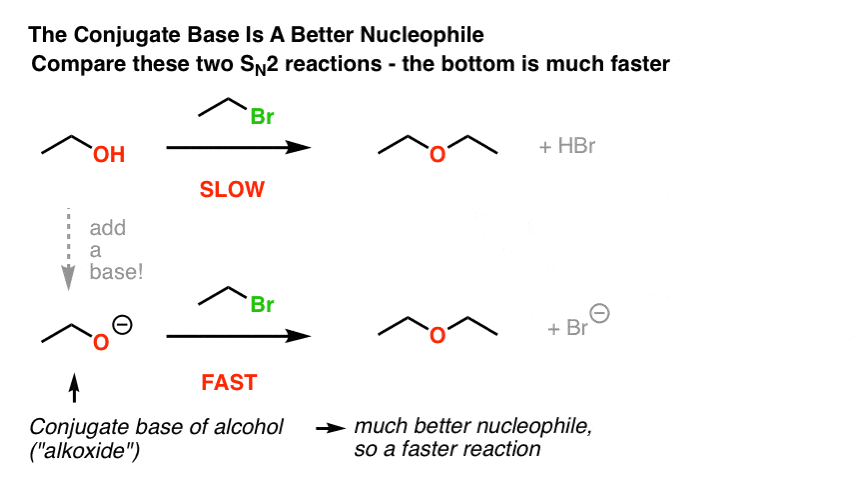
也有可能开始的酒精,添加一个基地给罗依- - - - - -,然后添加烷基卤化物(注意阴影部分]。下面我们会讲到。
3所示。在威廉姆森醚合成烷基卤化物工作好吗?(不)
在这里我们回到概念从中途Org 1重现在本章醇。
威廉姆森的醚合成是一个年代N2的反应。记住,自年代N2通过单步的反应所得亲核试剂对烷基卤化物执行一个“背后攻击”年代,“大障碍”N2反应位阻。
的速率N2甲基卤化物反应是最高的,那么主要,二级、三级(基本上不发生)。的同样的模式威廉姆森的存在醚的反应。
甲基和主烷基威廉姆森卤化物是优良的基质。
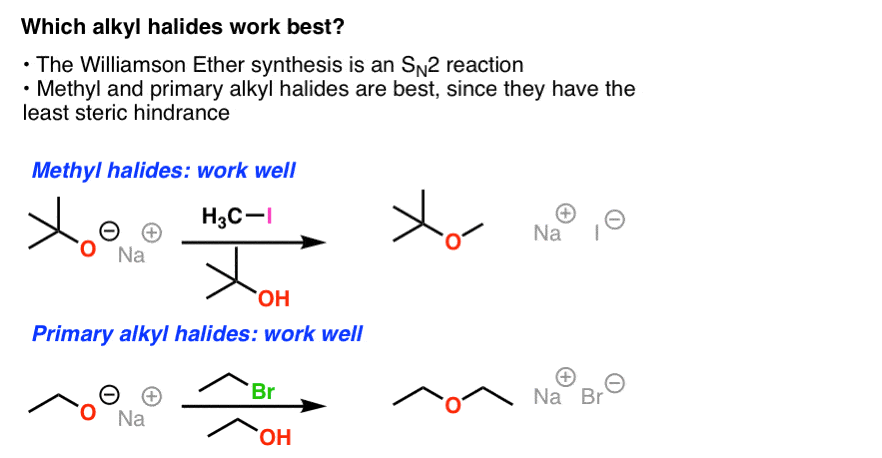
(一个例外:阻碍tert-butoxide阴离子(t-BuO)是较慢的执行N2比其他反应醇盐同行。这醇盐,也被强碱性,可能开始生产消除(E2)副产品当主烷基卤化物,特别是加热]。
因为醇盐强大的基地(记得pK一个醇是在16日至18日),与消除竞争(E2一旦]途径成为一个关注烷基卤化物变得更加位阻。
因为这个原因试图执行一个威廉姆森在次要的烷基卤化物有点比是一个主要问题烷基卤。
一种尝试的年代N2的青睐E2是使用一个极性非质子溶剂(如乙腈或DMSO溶液),将增加亲核性的醇盐。然而,如果加热E2很可能占主导地位。
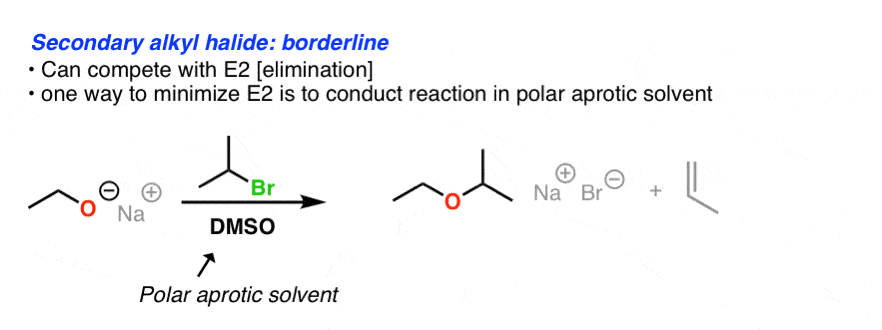
一个底物完全失败了威廉姆森的三级烷基卤化物。这应该是意料之中的,因为背后袭击一个叔烷基卤化物遇到巨大的位阻。而不是替代,消除反应相反,通过E2机制(看到帖子:E2机制)
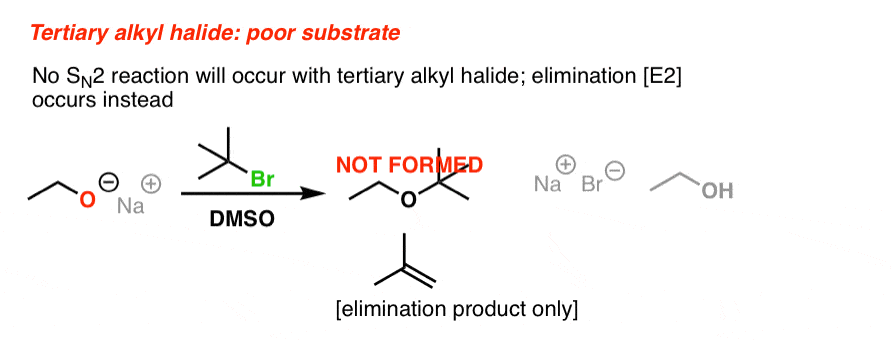
4所示。从一个酒精和添加基地——工作什么?
如前所述,威廉姆森的最常见的方法是显示醇盐基地被添加到烷基卤的存在共轭酸作为溶剂。
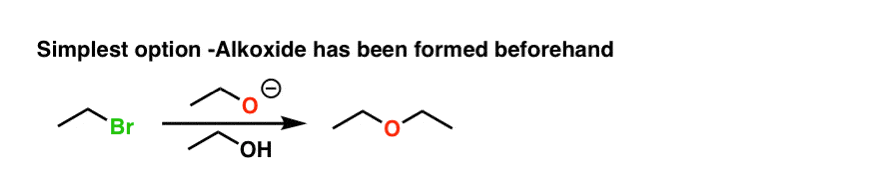
然而,也有可能开始的酒精(生成,添加基地醇盐),然后添加烷基卤化物。
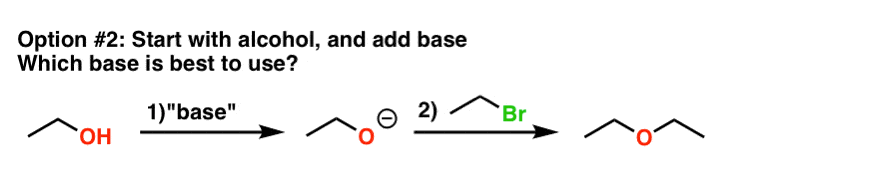
这里的问题是,我们应该用什么基础?
首先,不用说,实际上deprotonate必须足够强大的基础酒精。使用类似的Cl -或有数2(醋酸)不会做这项工作。理想情况下,我们希望至少一样强大的基础的东西醇盐,或者更强。
其次,我们需要担心副反应。这可能有助于反思这些反应是如何运行的。我们通常从一个烧瓶的开始酒精溶剂,添加基地,然后加入我们烷基卤化物。然后,当反应完成后,我们隔离产品。这意味着基它的去质子化后,其共轭酸在解决方案仍然是游泳吗,因此有可能与我们的反应烷基卤化物(把它搞砸的)。
这里有一个例子坏选择的基础:
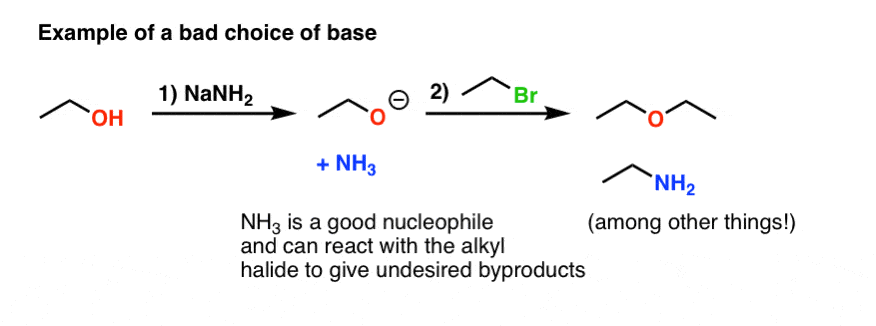
NaNH2当然是一个足够强大的选择基础deprotonate酒精。然而,在完成,我们有NH3在解决方案,这是一个足够好亲核试剂反应与烷基卤,给我们胺在我们的反应副产物。不理想!
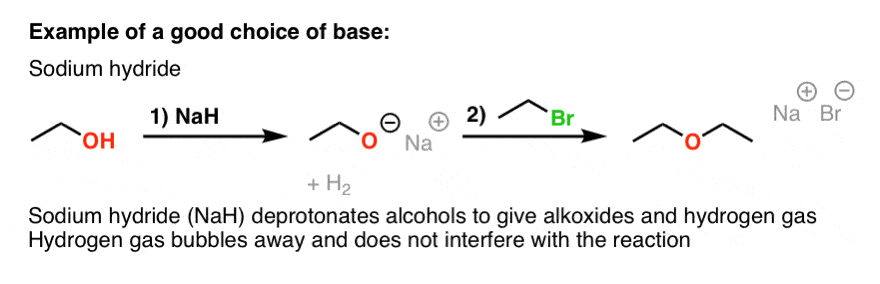
我们如何这样做的正确方法?有可能的醇盐直接从酒精,只需通过添加金属钠或钾,释放出氢。氢是完全无害的副产品烷基卤化物而言——它不会充当竞争亲核试剂,气体,只是泡沫的解决方案。后醇盐我们可以添加形成烷基卤化物。
不同(但更常见)的方法是添加氢化钠或钾(例如不或KH)。这同样的效果添加钠或钾金属——形式醇盐和H2——而不是强烈的额外奖金减少,一个潜在的担忧,如果我们处理复杂的原始材料,很容易降低。
5。我们如何选择溶剂在威廉姆森醚合成吗?
正如上面提到的,我们正常的溶剂的选择共轭酸的醇盐。(也有例外,我们可能会选择尝试如果竞争一个极性非质子溶剂E2是一个问题。
问题是,“为什么”?你搞懂了吗?
想象我们决定添加乙醇钠丙醇,然后加入我们烷基卤化物。会发生什么呢?
这将建立一个平衡!我们的“乙醇钠”也不会一直如此长时间——它可以deprotonate丙醇钠丙醇盐,随着乙醇。我们可以在理论上有一个混合物的乙醇钠和丙醇盐钠溶液,这可能导致的混合物醚产品。再一次,不理想。
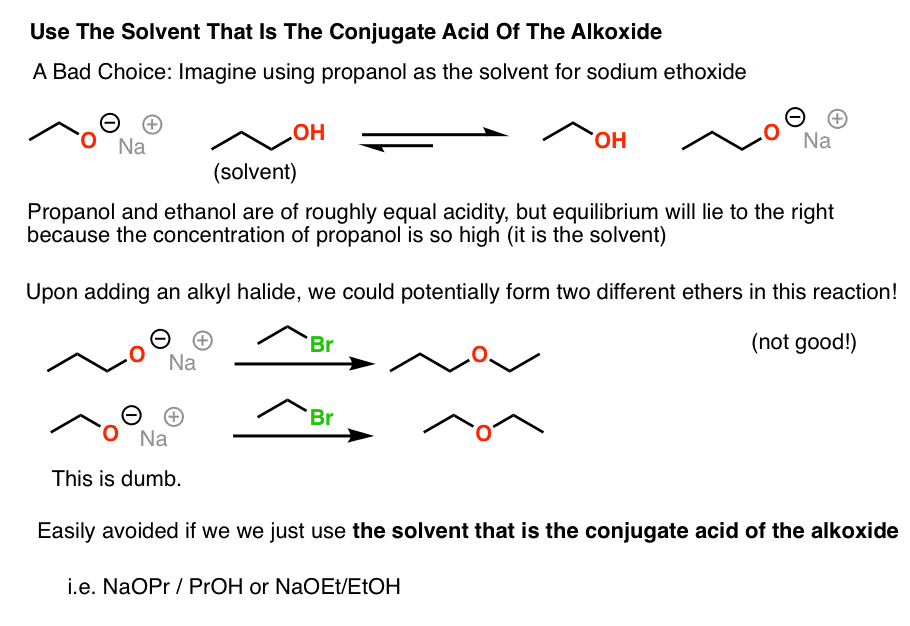
为什么给自己这个头痛?这是毫无意义的。出于这个原因,我们如果我们大大简化问题使用酒精溶剂是共轭酸的醇盐。
6。摘要:威廉姆森醚合成
这就是今天的威廉森说。然而,在下一篇文章,我们要考虑这个反应向后。从一个给定的醚,我们计划如何综合利用威廉姆森反应吗?
在下一篇文章- - - - - -威廉姆森醚合成:规划
笔记
- XLV。ætherification理论。
亚历山大·威廉姆森(1850),伦敦,爱丁堡和都柏林哲学杂志,和科学期刊,37:251,350 - 356,
DOI:080/14786445008646627
原来的威廉姆森纸。 - Equilenin 3 -苄醚
m . Hoehn克利福德·r·多恩,伯纳德·a·纳尔逊
《有机化学》杂志上1965年30.(1),316 - 316
DOI:DOI: 10.1021 / jo01012a520
本文的一个反应是一个典型的威廉姆森的保护反应酒精在dehydroestrone苄醚,使用苄氯。 - 总合成(+)7-deoxypancratistatin:一个激进的环化方法
斯坦顿·加里•e .凯克McHardy,杰瑞·a·聪聪
美国化学学会杂志》上1995年117年(27),7289 - 7290
DOI:1021 / ja00132a047
在现代有机合成中,用于威廉姆森反应保护醇反应的底物。常见的保护组织包括methoxymethyl(妈妈)和2-methoxyethoxymethyl (MEM)。妈妈保护工作在这个由凯克教授和同事总合成。
我也有过类似问题的above-bulky基地应该是一个可怜的亲核试剂,但一个真正强大的基地,所以引起E2反应,霍夫曼消除当适用于空间的原因。但教科书和这个网站还说,使用tert-butoxide离子是一种更好的选择做一个醚的SN2反应比说,叔卤代烷在这种情况下,只有消除产品。
但是,我猜你可能会做一个叔卤代烷醚SN1反应吗?当你在回应另一个评论说。教科书说的反应CH3ONa (CH3) 3 c-br给完全异丁烯。想这是一个实验的结果。
来源:
https://flic.kr/p/2ogyr3S
https://flic.kr/p/2ogxHyZ
NCERT化学课12
将反应tert-butoxide钠和氯乙烷给乙烯(E2)或乙基叔丁基醚(由于SN2)作为主要产品?
威廉森合成机制
你是对的,它不在那里。需要修复。它只是SN2。
感谢分享这些有用的细节。
如果产品是水不溶性,可以去除多余的基地通过注入水的反应;但是,我的产品是高水溶性,你有什么建议从多余的基础如何分离?(我使用K2CO3)
是你的产品溶于任何有机溶剂?方法之一就是淬火用饱和NH4Cl固定在底座的解决方案,然后添加相同量的盐水和提取。执行3提取提取和有机分子应该坚持这一层,而所有的盐将水层。
是否可以用氢氧化钠代替不作为基地的形成反应醇酚盐吗?
当然!之间有一个平衡醇盐和酒精,但仍将完成工作。最好是当溶剂的共轭酸醇盐(如埃托奥——/ EtOH)。
你好,非常感谢你的笔记,我发现他们真的很有帮助。
我有一个问题:在我的项目我必须形成一个苄基的酚醚保护。我使用奈,K2CO3 BnBr DMF在80 oc文学。这是威廉森合成醚形式通过Sn2吗?如果是的,那么为什么奈和K2CO3而不是一个更强大的基础?
奈使碘苄溴化苄。碘苄太不稳定的隔离。
苯酚的pKa是10。碳酸的pKa大约是6。pKa的区别是4。一个好的经验法则是,pKa差8或少足以让你参与的共轭碱。因此,尽管酸碱反应会喜欢碳酸一侧,会有足够的酚盐与碘苄反应。
我们可以请告诉我如果在威廉姆森醚合成SN1是可能的吗?。因为我们的老师今天说,否则会…,我学会了. .我12日标准的学生
通过SN1 * *醚形成是可能的。例如,叔卤代烷叔丁基溴化和溶于甲醇;你会得到一个新的乙醚,t丁基甲基醚。
然而这并不是技术上威廉姆森;威廉姆森涉及deprotonating酒精给一个醇盐,然后在与卤代烷反应给一个新的乙醚。这通过SN2反应所得。
最终“威廉姆森”这个名字不是很重要;更重要的是意识到醚可以通过SN1和SN2反应形成。
他的,我有一个之一。是可能的收益率主要酒精和二次卤有立体阻碍组织?。我试着用强碱在极性溶剂,但产量非常少与未反应的SM 6 - 7%。
的SN2仲烷基卤化物,特别是阻碍二级烷基卤化物,很可怜的。你为什么不把它使用二级和主要卤代烷醇盐吗?这将更好的工作。
你好,詹姆斯,
根据你下面的序列:
1)不
2)BnBr
是SN1或SN2机制?
谢谢你的回答
菲尔。
我没有看到你工作的分子,但我认为不就是deprotonate酒精,和BnBr反应生成的醇盐。
你好,我学到了很多在这个页面。但是,你可以给一些例子的共轭酸醇盐在选择溶剂。
你好!我有一个问题:为什么庚醇不能被氢氧化钠deprtonated ?
可以,只是,这将是高度可逆的。你可能会有一些溶解度问题以及庚醇在油腻的一面。尝试一种相转移催化剂。Tetraammonium氢氧化
杰出的演讲。
发现你的网页在帮助我的女儿为她找到好的信息来源的有机过程。
简洁但不简洁…
优点,缺点,比较,理由选择Reactant-Substrates试剂产量首选产品以及相关注意的“符号。
演示文稿完全充分填满我Golidlocks标准选择一个教授和教师。
不要小
不要太多,
完美的演讲
汤姆琼斯,D.D.S.
谢谢你!
我们可以使用K2CO3为基础,使醇盐吗?
不是一个伟大的基本使用,因为很弱。平衡极大地支持了酒精,而非醇盐。
它还取决于不可逆性,二氧化碳可以帮助的挤压;也许你需要那么alkyliodide…。
优秀的东西!化学世界需要作者喜欢你!这是如何传达一个信息。短和覆盖所有重要点. .
使用DMSO(非质子溶剂)将有利于E2而不是Sn2。应该使用质子,质子溶剂。
这是不正确的。非质子溶剂有利于SN2 / E2, DMSO溶液是一种有用的SN2反应的溶剂。这样想。极性质子溶剂氢键亲核试剂和阻碍其背后攻击。
“…它的去质子化,它的共轭碱仍然是游泳在解决方案…”
“这是non-nucloephilic”
“轻松避免如果我们只是…”
请适当的调整。
但是一个真正伟大的和有用的帖子,其实(像往常一样)。
很高兴这次的错误是次要的。谢谢你,一如既往。