醇、环氧化合物和醚
甲苯磺酸盐和甲磺酸
最后更新:2022年11月9日|
甲苯磺酸盐和甲磺酸
- 本身醇贫穷离开团体由于氢氧根离子(HO)是一个强大的基础
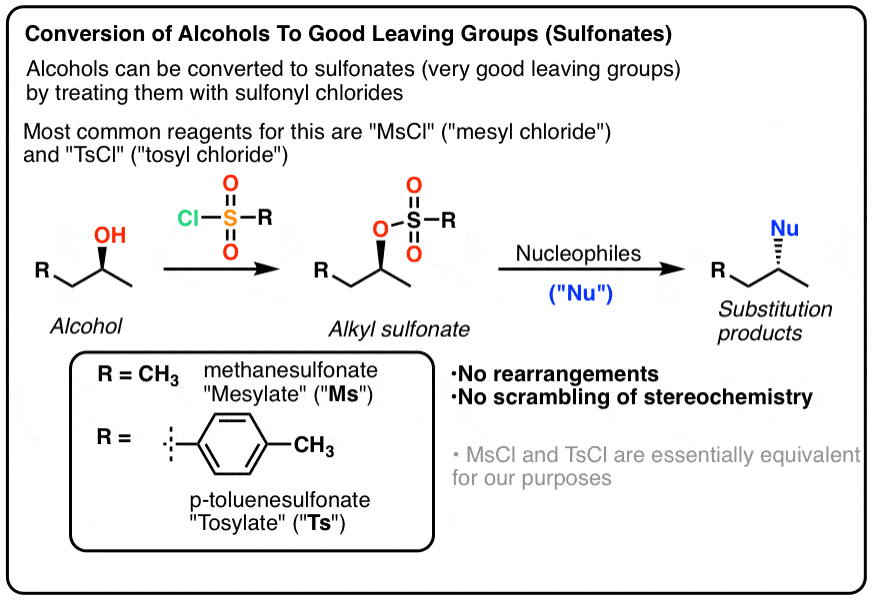
- 哦组可以被转换成一个更好的离去基团通过转换磺酸盐集团等p -toluenesulfonyl(“甲苯磺酰基”,简称Ts)或甲磺酰(“mesyl”,缩写为女士)
- 安装这些群体并不影响的立体化学酒精
- OTs和OMs组可以参与替换和消除反应。
表的内容
- 制造醇分成好离开组(第2部分)
- 一个好主意,实际上并不工作:硫酸离开组织
- 引入“甲苯磺酸盐”和“甲磺酸”
- 甲苯磺酸盐和甲磺酸是由醇吗
- 四个具体例子甲苯磺酸盐和甲磺酸的行动
- 摘要:甲苯磺酸盐和甲磺酸
- (高级)引用和进一步阅读
1。醇为好离开群体,第2部分
我们已经见过醇是可怜的置换反应的底物。主要的问题是,羟基是一种强碱,因此一个可怜的离去基团。
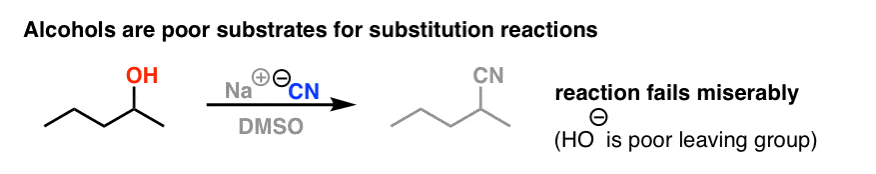
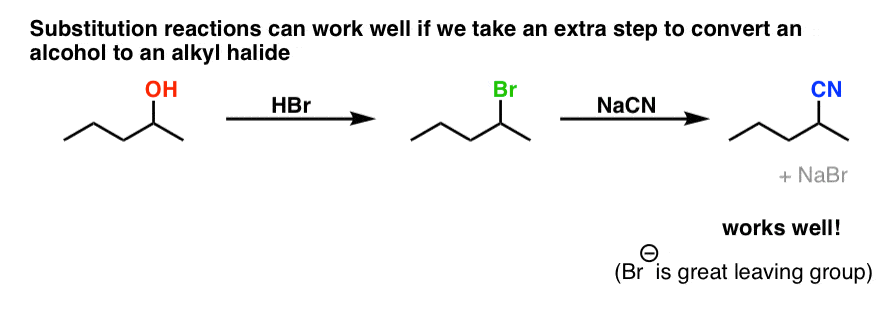
在最后发表我们看到,我们可以将醇转化为烷基卤化物通过添加强烈hydrohalic酸(盐酸,哈佛商业评论,嗨):强酸使质子化的R-OH给R-OH2+(更好的离去基团H2O),然后替换的卤化物离子可能发生。
与醇相比,烷基卤化物是伟大的基质对亲核取代反应。
不幸的是,这并不总是很好地工作。有两个主要问题。首先,在某些二级醇反应所得通过一个年代N1通路,从而导致重组。其次,这样做,我们可以最终爬任何存在的立体。例如,如果我们从一开始对映体在反应中,我们得到一些最终产品的外消旋化。
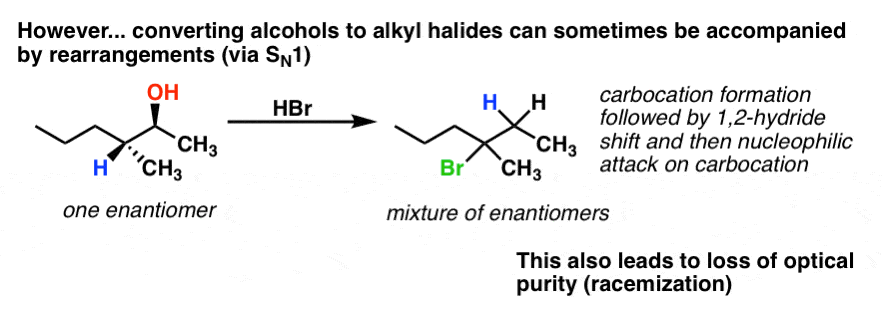
所以有一些其他方法将醇转化为离开团体没有这些问题好吗?
确定的东西!
2。一个好主意(实际上并不工作,)
我们都知道氢氧化物(HO)是一种强碱。但是,我们看到任何的例子疲软的基地和一个负电荷氧气?
是的!硫酸(H2所以4)是一种非常强烈的酸(pK一个3)及其共轭酸,OSO3因此,H,弱碱。这是由于两个关键因素——首先,移位的氧通过共振,其次,诱导效应氧的帮助重新分配。
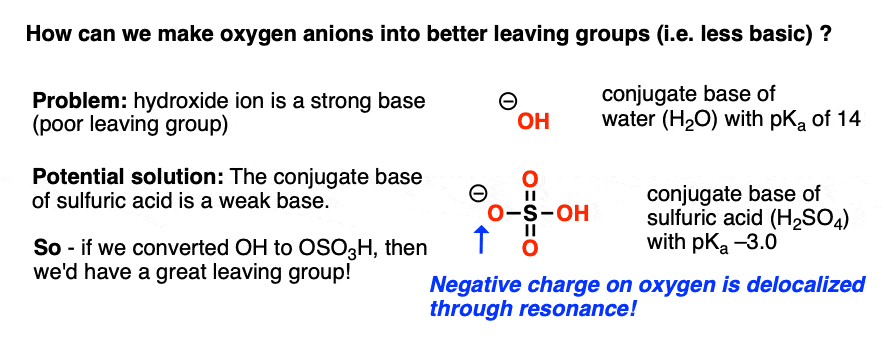
在完美的世界里,如果我们有一些的方式很容易把一个酒精(R-OH)成一个烷基硫酸氢(R -OSO3H),那么我们会有一个很好的方式进行酒精到一个好离去基团。
这个工作在实践中会如何呢?实际上它不工作很好!
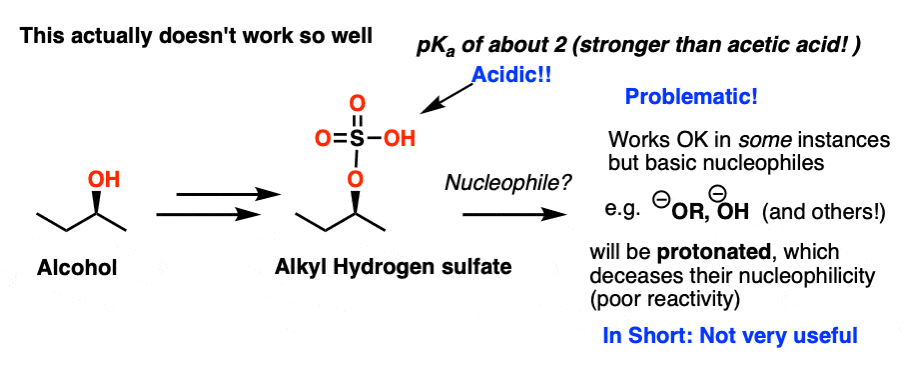
这并不是说- - - - - -OSO3H是一个贫穷的离去基团(这是一个伟大的离去基团)。问题是,许多亲核试剂非常基本的(记得-的共轭碱是一种更好的亲核试剂)和OSO3H仍非常酸性质子(哦组pK一个约2,使其更强大的比乙酸酸)。
底线是,如果我们添加一个基本亲核试剂,会发生酸碱反应而不是我们所期望取代反应。的亲核试剂将质子化了的到共轭酸(亲核性较弱)和任何替代的反应就非常慢了。不理想!
3所示。引入“甲苯磺酸盐”和“甲磺酸”
有一些方法解决这个问题吗?当然!只是一种替换哦组相对惰性有机硫的某种组(R组),没有一个酸性质子。
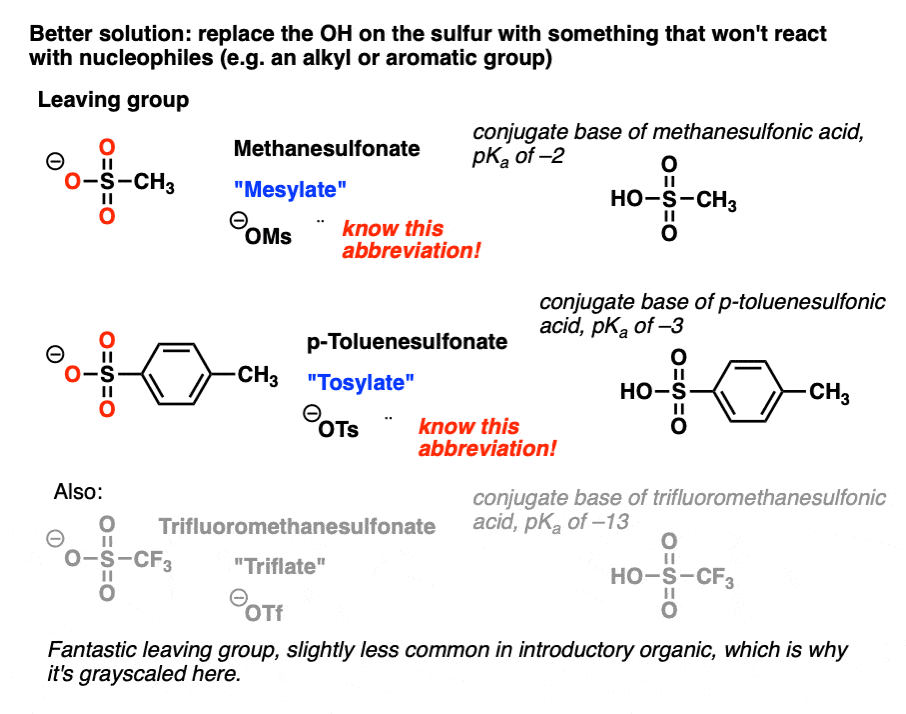
如果我们交换一个甲基(CH3)我们离去基团将- - - - - -OSO2CH3或“显示”(通常称为“甲磺酸”和缩写网络营销峰会。所有伟大的优点离去基团没有缺点的酸性质子与亲核试剂反应。
另一个流行的选择是使用共轭碱的p亚苄基酸,通常称为(“p-toluenesulfonate”)“甲苯磺酸盐”和缩写OTs。
这些组织本质上是相同的离去基团能力和对我们来说是可互换的。有些教科书更倾向于使用Ts,其他人使用女士并不重要,我们在这个阶段:他们都工作。
(第三种选择,常见于入门课程,是“triflate”(Tf)集团与三氟原子取代了三个氢原子在显示。的共轭酸trifluoromethanesulfonic酸,酸性更强的物种(pK一个-13年!),因为这个原因,triflate很“热”离去基团当连接到烷基组:喜欢离开自己的协议!更常用的芳香醇类和其他物种,不形成碳正离子容易)
4所示。我们如何从醇甲磺酸和甲苯磺酸盐吗?
所以我们如何应用呢?如果我们有一个酒精我们怎么把羟基甲苯磺酰基或mesyl组?
它是相对简单的。我们使用“mesyl氯”(MsCl)或“甲苯磺酰基氯”(TsCl)和中性酒精执行一个取代反应在硫,导致形成里和S-Cl破损。然后,去质子化的起诉酒精导致中性甲磺酸或甲苯磺酸盐。
请注意,立体化学是完全不变(不像例如,如果我们用氯)。当心——立体化学考试经常测试!
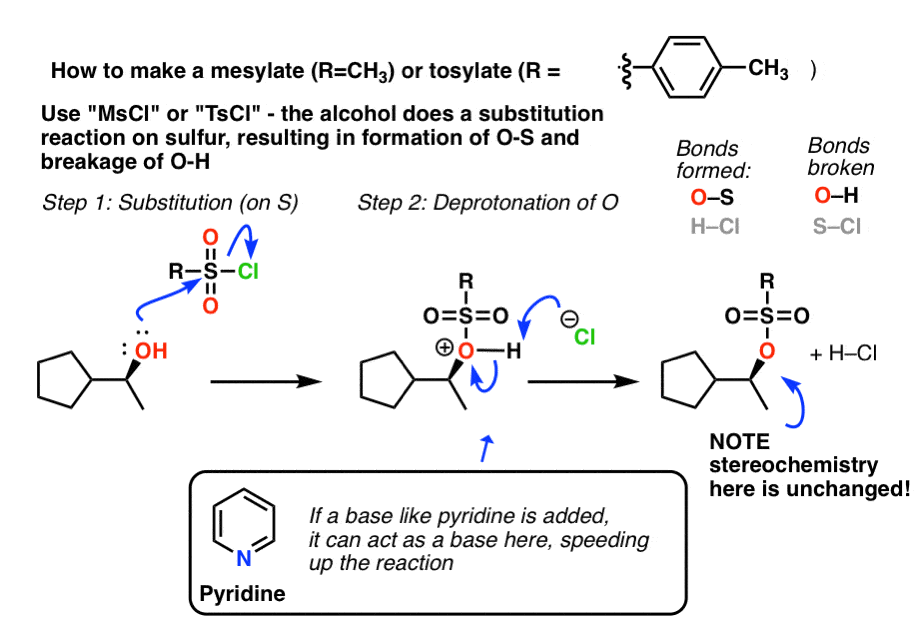
(顺便说一下,有时你可能会看到一个有机基地等吡啶还补充说,这有助于去除盐酸的过程形成的。]
5。四个具体例子甲苯磺酸盐和甲磺酸的行动
看到一些具体的例子让我们完成的Ts和女士在行动。因为它们包含好离去基团,烷基甲苯磺酸盐或甲磺酸可以执行所有的替换和消除反应烷基卤化物。几个例子如下所示。熟悉MsCl和TsCl缩写和扩展(例如“旷日持久”)的形式。
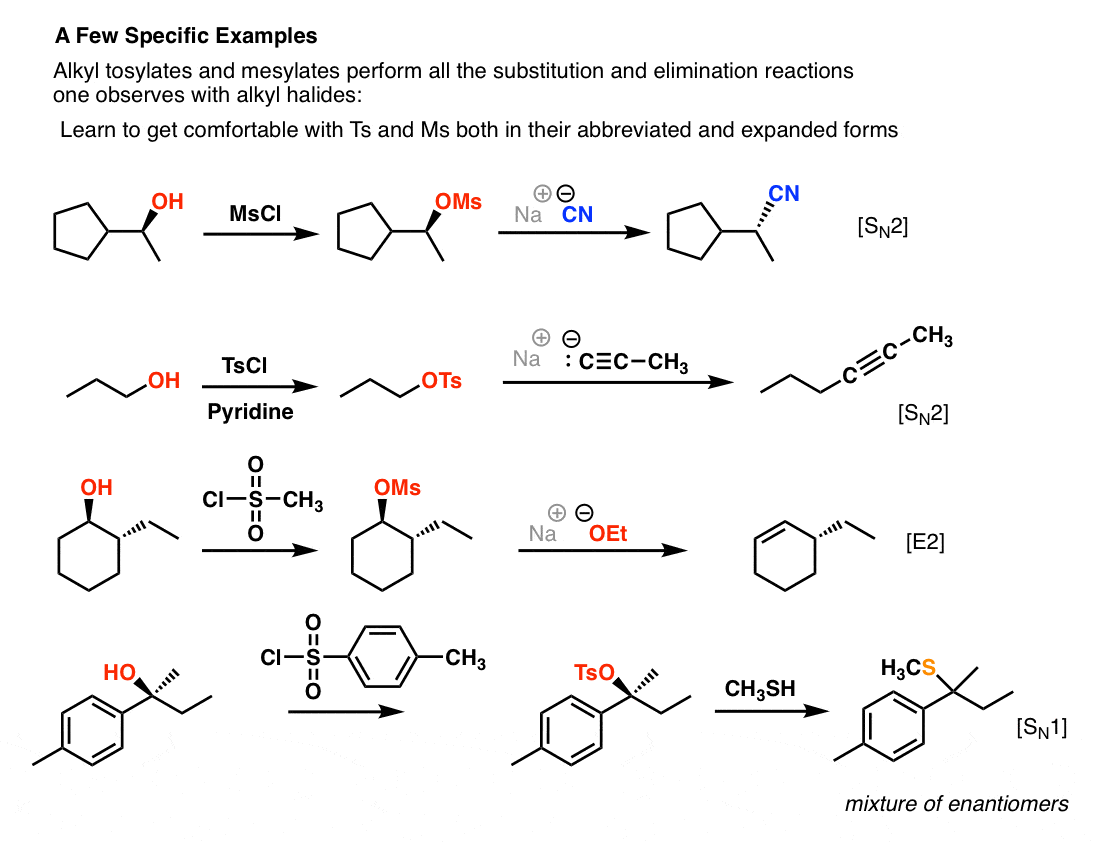
6。摘要:甲苯磺酸盐和甲磺酸
在最后两篇文章我们看到是多么有用的能够将醇好离开组织。在我们下一篇文章我们将讨论最后一个方法涉及到一些新的试剂,PBr3(包括其他磷卤化物)和SOCl会2。
在下一篇文章- - - - - -PBr3和SOCl会2
笔记
(高级)引用进一步阅读
- 在酯类p-TOLUENESULFONIC酸
斯图尔特还将就
有机化学杂志》上,1944年,09年(3),235 - 241
DOI:10.1021 / jo01185a005
早期对甲苯磺酰化参考斯图尔特还将就,在梅隆工业研究所(现在卡内基-梅隆大学)。 - 甲苯磺酰化的醇
乔治•w•Kabalka Manju Varma Rajender Varma, Prem c·斯利瓦斯塔瓦、小家具f·克纳普。
有机化学杂志》上,1986年,51(12),2386 - 2388
DOI:10.1021 / jo00362a044
本文介绍了一种改进的过程对甲苯磺酰化醇。除了p -toluenesulfonyl集团其他磺酸盐酯类从醇可以准备离开团体(如甲磺酸、brosylate triflate,三氟醋酸盐,nonaflate,等等)。两篇论文描述甲磺酸酯合成如下所述: - 动能和高活性显示出的光谱特性描述。离去基团影响solvolyses和评论偕的电子效应的影响SN1反应性
曼弗雷德·威廉·本特利Christl、拉尔夫·克姆加雷斯·卢埃林和约翰·e·奥克利
j .化学。Soc。,Perkin反式。2,1994年,2531 - 2538
DOI:10.1039 / P29940002531 - 钯催化的Buchwald-Hartwig氨基化和Suzuki-Miyaura交叉耦合反应的芳基甲磺酸
Pui应避开男人Wong白菜,应袁,洲明,口音太重绮邝
Synth。2015年,92年,195 - 212
DOI:10.15227 / orgsyn.092.0195
这个过程的第一步是mesylationp-t-butylphenol。 - 合成的一些小说trifluoromethanesulfonates和他们的反应酒精
查尔斯·d·比尔德,库尔特·鲍姆和Vytautas Grakauskas
有机化学杂志》上,1973年,38(21),3673 - 3677
DOI:10.1021 / jo00961a003
Triflate (-2CF3)酯类更比甲苯磺酸盐或甲磺酸反应,由于triflate阴离子是一个极好的吗离去基团。本文描述了各种triflate的合成酯类但是给没有提到为了安全考虑——这些都是强有力的烷基化剂和高度致癌。
有大约1.2装备的甲苯磺酰基氯在吡啶/深度贴图。产品是一个特戊酸甲酯衍生物(所以比其他的甲苯磺酸盐分子如果你明白我的意思)。色谱法在硅,用乙酸乙酯/正己烷洗脱液。我曾经尝试过使用细分化滤纸消耗多余的甲苯磺酰基氯,这似乎是一个有希望的途径,色谱法之前。
什么是最好的方法去除多余氯甲苯磺酰基反应混合物。我甲苯磺酸盐产品移动速度相同的色谱法对甲苯磺酰基氯化物。
多少多余TsCl你添加吗?的分子和什么样的溶剂系统你用?削减你的溶剂系统一点苯/甲苯与分离芳香族集团可能会帮助。
你好,我有一个问题关于甲苯磺酸盐和甲磺酸参与替换和消除反应的能力。我有一个二级甲磺酸/甲苯磺酸盐,我准备从相应的二级醇。邻碳我有一个质子,被认为是抽象在之前的反应。我怎么能预测倾向SN2 vs E2反应?这完全取决于你覆盖:列表。e衬底、溶剂、温度、亲核试剂吗?你能告诉我一些文学可能吗?我无法找到任何帮助。
提前谢谢。
在现实生活中,置换反应二次碳可能非常困难。你的底物与亲核试剂是什么?如果有任何位阻,如果在所有基本的亲核试剂,将很难避免消除作为重要的副产品。
Qestion,
谢谢你的文本是非常有用的。我想知道甲苯磺酰化酒精可以进行水吗?如果不是,哪些溶剂更好?
水是一个贫穷的溶剂,将水解氯甲苯磺酰基。我会找到一个非极性,non-nucleophilic衬底是溶于溶剂,如氯化溶剂或醚和使用它。
你好。
你能告诉我,请参考这些信息是什么?
谢谢你!
看到底部的新“引用”一节!:-)
你好,詹姆斯,
谢谢你的这些有趣的信息。我想知道是否甲磺酰组麦尔反应条件下是稳定的吗?事实上,我想实现麦尔反应在甲磺酸的存在保护酒精,你觉得如何?谢谢你!
详细回答你的问题是不可能的,因为你不提供一个结构。主要OMs活性而对亲核试剂叔OMs会进行消除。mesyl集团并不是真正想成为一个保护组。它很不稳定。我建议你在浪费你的时间和女士使用更健壮。TBS或OBn组怎么了?
的问题。非常感谢你的帖子和无尽的努力让人们学习有机化学欣然应评税。我有一个问题。如果这是一个很好的离去基团是在酸性环境。它需要先被质子化了的吗?因为我没有看到你在这篇文章中谈论。非常感谢。
我讨厌说,“看情况”,但这取决于。好离开组织薄弱的基地。如果提议的离去基团已经弱碱之前去质子化(例如TsO)然后质子化作用不会是必要的。但如果该离去基团不是弱碱(e。g HO)质子化作用将使它成为一个更好的离去基团。
你好詹姆斯,这是一个伟大的职位!只是一个问题:没有甲磺酸还含有酸性氢由于甲基?
我知道碳不是电负性,但这不是它的共轭酸,负碳离子在共振的电子对SO3的共轭酸稳定,与氢反应…有点像一个活跃的(我认为吗?)
你提出一个很好的观点。甲基甲磺酸可以问题如果您正在使用强大的基地,因为它是酸性。
先生我也曾在碳水化合物化学,但是我有一个问题,问题是当我想尝试甲苯磺酰化prymary酒精在开放的糖存在Py & TsCl反应不执行。
但是循环糖6 th prymary酒精存在Py & TsCl甲苯磺酰化,也执行,请先生帮我对你的指导,如何做到这一点prymary酒精在存在二级醇,甲苯磺酰化,二次酒精仍然相同。但prymary酒精反应&转换与甲苯磺酸盐产品。
我将非常感激你。
不可能回答没有更多信息,比如一个屏幕截图。
我想尝试Ph-OH TsO-Alkyl基地。
是工作吗?
烷基化的苯酚烷基甲苯磺酸盐应正常工作,这取决于烷基。主要将当然最好。
你好,詹姆斯,
好文章!
我发现一个小问题:这篇文章介绍了甲苯磺酸盐和甲磺酸不仅作为一种使醇成为好离开团体,还来哦,转换成一个更好的离去基团* *,让我们避免重组的问题,外消旋化* *…这究竟是如何发生的呢?
从我的理解,转换哦OMs / OTs下不允许我们避免这种问题可能SN1机制。
例如:
不会asume是正确的,酒精的反应通过SN1与哈佛商业评论显示在页面的开始也会导致重排和外消旋化如果一个是替换哦组OTs / OMs吗?
我之前看过它了(Clayden)作为一种哦,变成一个好的离去基团,给定一个亲核试剂与强酸相矛盾的。(例如:考虑到锂炔的导数,由deprotanating说炔BuLi;这可能与酒精反应之前treate TsCl /吡啶,给SN2产品;这将不会发生在强酸性环境中由于炔re-protonated)。试图上传图像的反应我引用(同样来自Clayden),但不能找到一种方法来这样做。
我认为这可能是一个更好的方法来呈现;提到避免re-arrangements和外消旋化,我认为这不是避免甲苯磺酸盐或甲磺酸。
很想听到你的意见!
奥尔多
嗨,阿尔多。也许我不够清晰。我想说的是,从噢OTs允许被转化为一个好的离去基团没有这里的中间形成+(和可能的电离- >重排)在这个过程中,与哈佛商业评论/盐酸一样。
我并不意味着暗示烷基甲苯磺酸盐不能进行重组。他们可以。
我只是想说这是一个温和的方式将醇转化为好的离开组织。
希望解释!詹姆斯
如何处理酚类和对苯二酚MsCl还是TsCl ?你能建议?
谢谢
Vinay
这是可以做到的。你的目标是什么?
你好先生,
我有1,5 -二醇与氯化mesyl想保护。我应该做些什么呢?
我不清楚如果你想形成mono -或di -甲磺酸产品。你搜索的文献吗?
伟大的文章关于酒精保护团体!我读高感兴趣因为我执行保护醇取代反应。分子我正在由一个二级acohol和次要的酰胺。这个想法是为了保护酒精OMs或OTs使它成为一个更美好的离去基团,然后与酰胺基反应并关闭(环化),形成一个结构2,5-substituted吡咯烷。
我思考正确吗?后你的向导的NH酰胺应该足够亲核cyclisation和OTs或OMs容易离开。我用吡啶加快反应。
结构:CH3-CH (OH) -CH2-CH2-C -NH-R (O)
R Ph值通常是一个组织或取代芳环。
谢谢你的帮助!
我会想象反应会工作得很好。甲磺酸盐,然后你会发现它会提前关闭,没有额外的工作。如果不是,那么deprotonate酰胺与强碱。
你好先生,
我正在经历上面的评论,我这里有一个查询,为什么三苯甲基氯是主要用于选择性保护羟基糖甙吗?
你好,莎拉,这是因为三苯甲基集团是非常巨大的。让它放在第二个酒精会与空间严重惩罚。
Thanku秀多先生
嗨,詹姆斯
如果吲哚和二级醇分子的一部分,那么任何选择性的机会酒精脱水,(酒精是次要的芳基酒精从苯环吲哚的一部分)
没有足够的信息。需要一个结构。
你好詹姆斯,谢谢你的回复。
结构如下
开始Ar-CH (OH) -CH2-CH2(吲哚)
产品Ar-CH = CH-CH2(吲哚)
或
开始Ar-CH (OH) -CH2-CH (ar和吲哚)
产品Ar-CH = CH-CH (ar和吲哚)
基于“增大化现实”技术是芳环
亲爱的先生,
我想做选择性mesylation伯醇,但在我的两个主要有酒精官能团和三级。
一些时间我只能选择甲磺酸能够获得产品。但是大部分时间我都醇mesylation。
你能给你的建议吗
我的建议是设计合成,区分这两种醇在早期阶段。使用正交保护组策略,继续前进。
嗨,詹姆斯
只是一个问题。如果有胺醇化合物或硫醇组,MsCl和TsCl攻击他们,而不是酒精吗?
谢谢你的工作。
硫醇和胺(特别是胺)可以与MsCl和TsCl反应。因为这个原因,当一个人试图合成一个给定的分子是非常重要的只有一个反应性官能团现在和其他人通过保护停用。试图选择性甲苯磺酸盐或甲磺酸分子有多个保护官能团是浪费时间。
亲爱的詹姆斯,
如果你缺乏基本的反应和胺组已经盐酸的盐吗?
谢谢你!
你需要添加一个基地释放质子化了的胺。
你好,詹姆斯,
TsCl醇类和胺的反应。你希望拿离去基团和甲苯磺酰化度是否相同?哪一个是容易处理醇或胺?
我不完全确定的问题是问。
如果问题是:“如果你有一个酒精和一个胺分子,哪一个会先与TsCl反应吗?”
答案是,胺,因为胺遥遥领先其他很多更亲核的数量级。
相对很难把Ts组从氮,因此不推荐作为保护组。
如果你能把你的问题说清楚然后我可以尝试不同的回答。
如果使用吡啶和三乙胺氯离子可以是亲核试剂和攻击的R组氧气?会有烷基卤化物的比例吗?
很好的问题。与烷基甲苯磺酸盐通常不是一个问题,尽管它可能是一个问题与烯丙基的甲苯磺酸盐(和甲磺酸! !)作为一个著名有机化学家(BMT)喜欢说,“氯离子是一个糟糕的演员! ! !“如果你真的偏执,你使用Ms2O (methanesulfonic酐)。
你好,谢谢你美好的解释!…有一个问题是,这将是一个问题mesilation免费的哦,如果我有另一个羟基化合物与三苯甲基集团已经保护吗?我只是需要更远mesyl转换成叠氮化,因为它离去基团。和其他需要保持主哦在这pricedure保护。任何建议请!谢谢你!
不,这应该很容易。Mesylation不会干扰三苯甲基组。你只是添加MsCl或Ms2O NEt3。
亲爱的先生,
我有一个问题,我复合糖分子敞开了大门,选择性地甲苯磺酸盐主要的酒精。我尝试了吡啶为基础,但我不能够得到产品。请给你的建议。
谢谢
我将有选择地tritylate三苯甲基氯的伯醇,保护其他醇与乙酸酐或TBS,删除与三氯乙酸三苯甲基组,然后主酒精转化为与TsCl甲苯磺酸盐。
最后两个例子,你给arcticle……有机会他们会不遵循提到机制……像在第三例E2,而是可以Sn2 . .吗? ?
真正好的文章!不过,一件小事:在文本中出现“trifluoromethylsulfonic酸”,我应该读“trifluoromethanesulfonic酸”,因为它确实在图片下面的段落。
固定!谢谢你,一如既往
存在的一些其他组织(如醛)这个反应的问题吗?醛与OMsCl反应吗?
在纸上,不,没有不好的应该发生。在实践中,醛易受空气氧化(在对方反应),通常保存在保护形式,直到需要。
呃…磺酰胺的形成是通过sulfene中间,不是SN1或SN2机制(SN2机甲,就像描述,不是指控)。
磺酸盐形成实际收益几乎完全通过sulfene状态,不通过中间。这篇文章有一个很好的概述(137页开始讨论sulfenes $ $)。
谢谢布兰登!
我不想去吹毛求疵的细节,但我的理解是,NEt3和更强的基地将生成sulfene,而吡啶和其他类似基地(如深度贴图)将增加硫和创建一个激活,收取中间(如深度贴图+酰卤)然后被酒精。(这就是为什么我离开了吡啶的机制:-))
我的理解是,吡啶/深度贴图作为基础与亲核试剂。基本字符生成sulfene,然后攻击第二个吡啶/深度贴图形成带电分子中间你指(这一步也deprotonates第一单元的吡啶/深度贴图)。
反应的性质可能会改变取决于磺酰氯的类型。例如,t-burylsulfonyl氯不能形成sulfene,而且必须通过SN1或SN2反应。这也是一个令人难以置信的可怜的亲电试剂,,在标准条件下它不与胺反应,需要一个怪异的氧化sulfinamide t-butylsulfonamide。
这很有趣(奇怪),因为TsCl或benzenesulfonyl氯和胺AFAIK反应没有任何问题。
我的朋友杰夫做了一些研究建议sulfenes认为深度贴图可能形成sulfene足够强大的基地,而吡啶不是。
“我认为,通过sulfene深度贴图可能会。碱度是接近NEt3比吡啶和在有机溶剂,它甚至可能是更基本的:因此维基百科,pKb的深度贴图MeCN是17.95(不能轻易找到DMSO值)。茶在DMSO是9,而吡啶是3.4在DMSO。”