焊接、结构和共鸣
介绍了共振
最后更新:2022年12月24日|
介绍了共振
最后一次我们讨论了如何使用电负性发现分子的电子密度,当忽略形式电荷。
但是我没有提到第二个关键因素,可以使电子密度的分析:的存在双键(π键)。在本帖里,我们将看到如何将偶极子的理解与“最佳”的理解分子π电子的分布将给我们一个电子在分子的整体图片。
(进一步的了解,由电子将帮助我们理解分子将参与反应。]
表的内容
- 应用电负性差异了解分子π键电子密度,简单的例子
- 两个情况下,“应用电负性差异”未能准确预测电子密度
- 可以画出两个,不同的路易斯结构酯阴离子和烯丙基阳离子
- 在这两种情况下,“真正的”电子密度反映的“混合”两个共振结构
- 笔记
1。应用电负性差异了解分子π键电子密度,简单的例子
但让我们从简单的东西开始。在许多情况下,一个分析电负性可以给你一个非常准确的电子密度在分子π键。这可以告诉你“偶极子”。
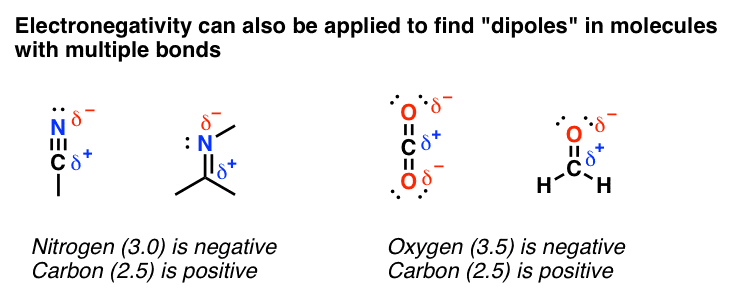
原子的电负性更强?这是一个将“delta-negative”。很简单。
顺便说一下,这种模式非常有效寻找这些分子的反应性网站。这里有两个例子。
看到H +是如何吸引部分-氧,和HO -吸引部分积极的碳。
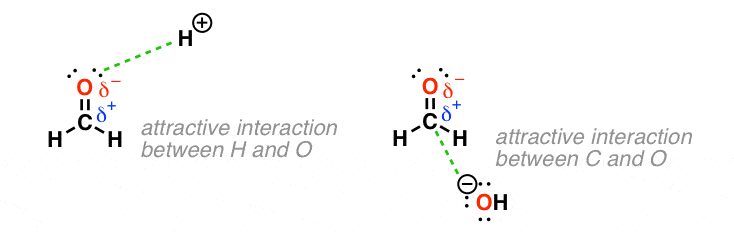
实验证明了我们的预测,带正电的酸(即“H +”)将在“负面”原子反应轴承电子(氧气在这种情况下),而氢氧化带负电(HO)反应在原子轴承部分正电荷(C在这种情况下)。
目前为止一切都很顺利。
到目前为止我们的模型的问题在于,它不允许在某些情况下我们做出准确的预测。
2。两个情况下,“应用电负性差异”未能准确预测电子密度:乙酸离子和烯丙基阳离子
经验的一部分作为一个科学家是看你很简单的,吸引人的假设/模型被实验证据撕成碎片(或缺乏)。
看看下面这两个分子。第一个分子的路易斯结构(“乙酸离子”)似乎告诉我们,一个氧比另一种更消极。
第二个分子的路易斯结构(烯丙基碳正离子)表明一个碳熊正电荷和其他人是中性的。
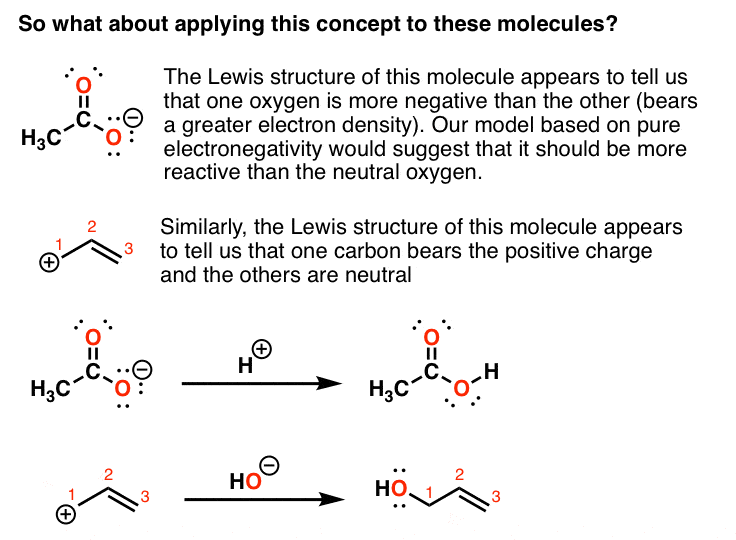
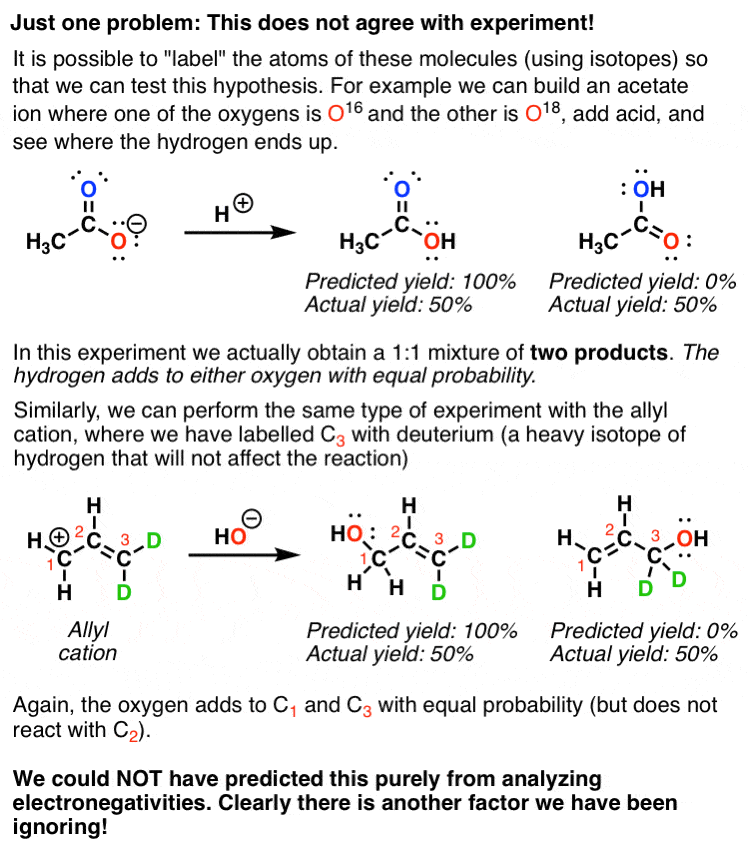
我们从这个模型预测,更多的“负面”会比中性反应氧,和同样的“正面”和中性碳。然而,如果我们测试这个模型通过使用标记化合物,我们发现我们的简单的模型与实验不符。
发生了什么第一分子(乙酸离子)每个两个氧原子与H +同样反应。
在第二个例子中,每个终端碳同样活性与亲核试剂。
3所示。可以画出两个,不同的路易斯结构酯阴离子和烯丙基阳离子
如果你仔细看可以画出两个,不同的路易斯结构对这些分子。
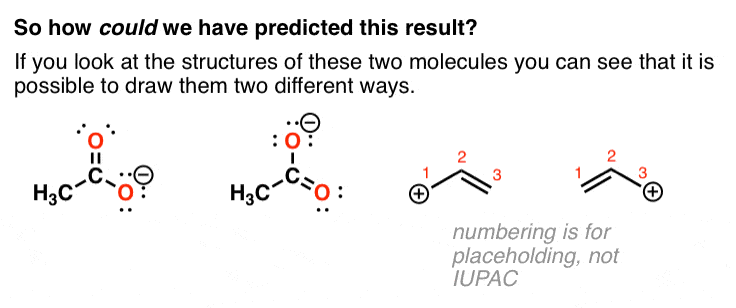
从上面的实验中,分子的行为好像是1:1的混合这两种化合物。(他们不是,但他们的行为!)
我们引入一个新的概念:共振
4所示。在这两种情况下,“真正的”电子密度反映的“混合”两个共振结构
- 当我们可以得出两个(或更多的)同一分子的不同形式只有在他们的位置电子,这些被称为“共振的形式s”(或“共振结构”)。
- 我们也可以说,这些形式是“在共振”。(有时又被称为共振“同分异构体”虽然在许多圈,这将得到一个推手不技术上同分异构体——他们只是不同的方式描述电子密度在同一分子)。
诱人的(和非常错误!)认为,这两种形式在彼此之间的“平衡”。避免常见的错误!
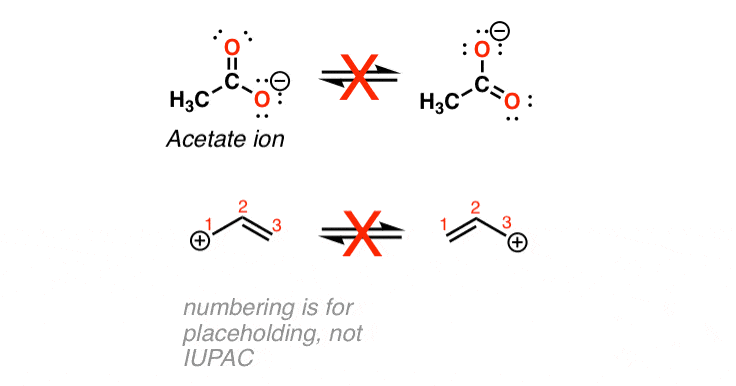
为什么这是错的吗?因为这是真的,碳氧双键的债券的长度和碳氧单键乙酸离子就会不同了。(1.21 vs 1.36埃)。
然而实验证据(从x射线晶体结构)告诉我们,每个键长完全相同的(1.26埃)。这个观察了无数共振同分异构体,如苯,碳酸盐岩,硝基和许多更多。
这意味着什么真正的醋酸盐离子的结构(和烯丙基碳正离子)是一个“混合动力“两个共振的形式。我们使用一个特殊的箭头来描述两种共振形式(双箭头)。
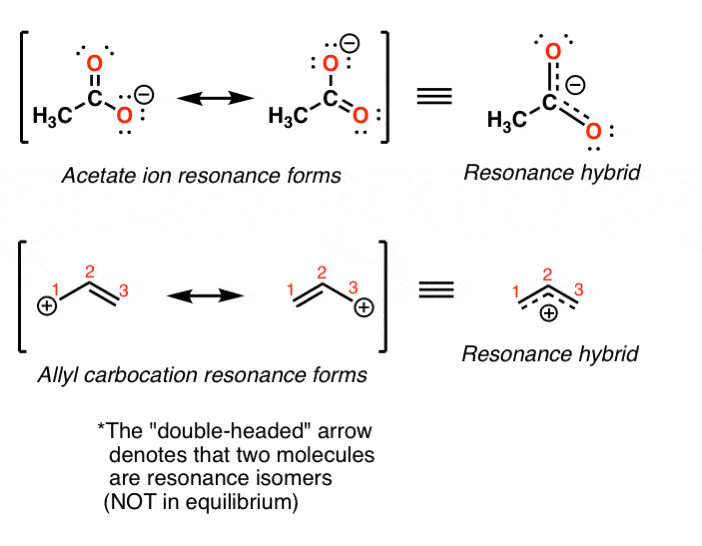
这意味着乙酸1的形式电荷的离子分布均匀两个氧原子之间。
和+ 1的形式电荷的烯丙基碳正离子是分布式的同样两个终端之间的碳原子。(注1]。
正如我们所见,形式电荷不能很好的反映电子密度,这里我们看到另一个例子,它是不准确的。
再次:电子密度是真正重要的理解分子的反应活性。路易斯结构和正式指控是不完美的指南完全描述分子中电子密度,但他们很有用在许多其他情况下,我们必须学会与他们的缺陷。
然而,理解偶极子的组合(电负性差异)和共振为我们将完成这幅画。
在下一篇文章我们将讨论另一个会计系统我们将使用来描述运动电子:弯曲的箭头形式主义。
在下一篇文章:介绍弧形箭头(2):弯曲的箭头!
我最喜欢的门外汉共振的解释:
http://www.reddit.com/r/chemistry/comments/dzvrm/i_tried_to_upvote_my_orgo_textbook/