家/化学平衡
普通化学复习
化学平衡
最后更新:2022年10月28日|
化学平衡
在化学、不可逆反应得到所有媒体:熟悉的火灾和爆炸,在YouTube上得到了很好的体现。问题是,并非所有的反应去完成。有时,可以一起反应,反应的产品再生起始材料,从而建立一个可逆的的反应。这些类型的反应在行动在我们周围,所以普通的我们没有注意。在任何给定的时刻,令人难以置信的数量的质子在我的健怡可乐(pH值3.39)与水分子交换,但由于没有净变化,这一过程几乎是看不见的。
在过去的主题“从创化学组织bdapp平台化学”,我们要谈论化学平衡,发挥了巨大的在有机化学的话题。您将了解的很多反应平衡反应,和这个概念超越了整数的化学反应过程,如底物与酶结合,甚至分子如何可逆地改变他们的三维结构。
化学平衡是什么呢?它为什么重要?什么意思说我们有化学平衡吗?
让我们从最基本的开始:
- 化学平衡只能发生在一个情况下有一个显著的反向的反应。
- 当建立化学平衡,没有改变反应物和生成物的浓度。
- 在平衡时,流程的δG等于零。没有动力。
可能最重要的你介绍在创化学平衡是通过酸碱反应。强酸盐酸的反应(HCl)与水产生水蒸汽(+),本质上是一个不可逆的反应。相比之下,弱酸乙酸(醋酸)后与水反应给H3O(+)和CH3COO (-),但反过来也可以发生反应。
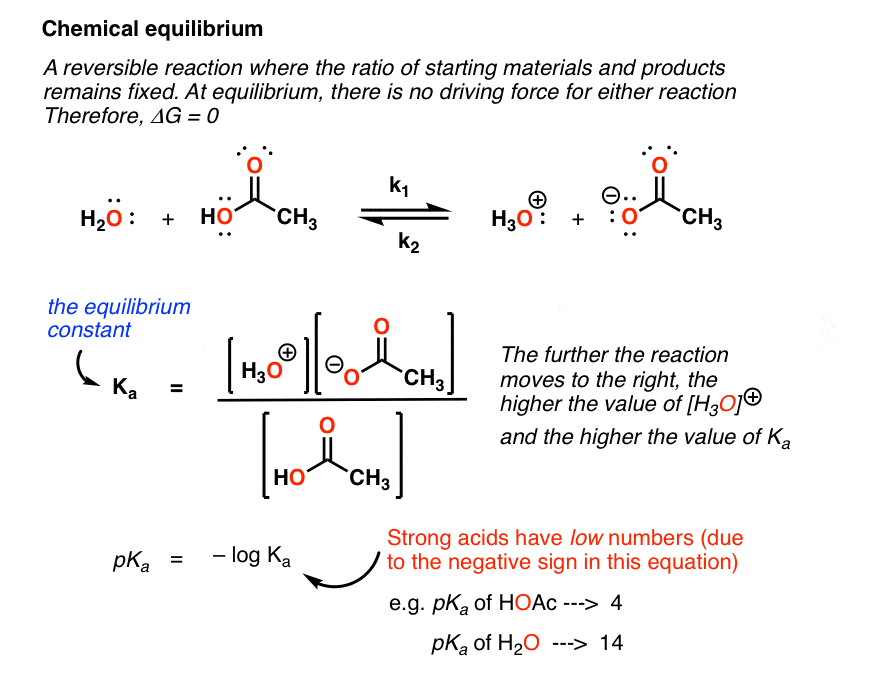
重要的是要注意,酸的相对优势来衡量这个平衡常数的值。这给我们提供了非常有用的措施pKa,等于这个反应的Ka的负对数。pKa是一个伟大的方式来比较不同的分子的相对酸度。随着分子的酸度增加,这个平衡将进一步推进,进一步向右。其结果是,强酸pka低(就像强酸溶解在水中导致低pH值)弱酸pka高。]
你可能不去想它,但化学反应平衡的操作你身边所有的时间在这样微妙的方式你甚至不通知。在每个罐的内部流行机你附近,例如,平衡水和(加压)之间建立了二氧化碳溶解在溶液中,形成碳酸;同时,分子碳酸分离为二氧化碳和水。
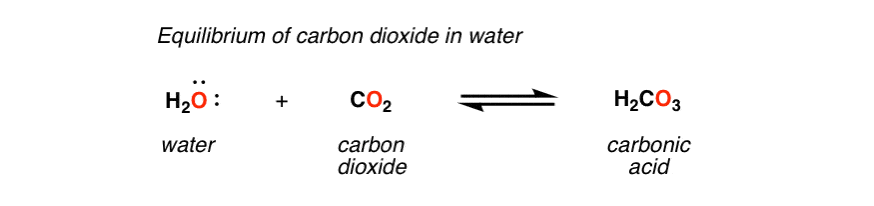
净二氧化碳浓度的变化,水,和碳酸:零
平衡常数可以用于确定ΔG。
在平衡时没有动力。ΔG的反应是零。有一个非常有用的数值平衡常数之间的关系和ΔG,叫做吉布斯自由能等温线方程我们可以用来求解ΔG(如果我们知道平衡常数)或平衡常数(如果我们知道ΔG)。
吉布斯方程:ΔG = rt lnK
在有机化学课上你会看到很多导致混合物的可逆反应的例子。一个具体的例子的研究构象,这是三维的分子通过可逆旋转形成的债券)。这是你如何使用方程求出ΔG,如果你知道凯西:

你甚至可以这个方程插入图形形式的关系(如果你能原谅蹩脚的Excel的技能)
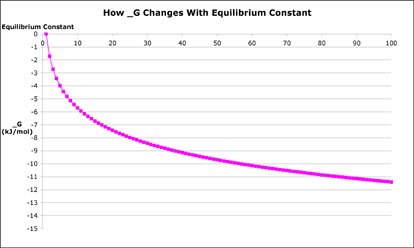
看起来多么陡峭的曲线的开始部分!很惊讶小反应的能量差异,给你一个9:1的混合产品。当你想想看,5.4焦每摩尔不是很多,比较碳氢键的强度,例如,430焦每摩尔。反应给你99:1比率,区别只有11.4焦每摩尔。
勒夏特列原理的原则
这是最后的关键概念对平衡。有机化学是一门实践的科学。我们经常关注将一个复合变换为另一个。我们经常想关闭了逆反应来提高我们的产量的产品。
我们经常可以找到一种方式操纵平衡为我们提供的产品,我们的欲望。你会经常听到这个描述推动反应。这是通过消除正向反应的副产品之一,因此防止反向反应发生。
这是一个例子。治疗一个醛胺生成化合物称为亚胺以及一个水分子。这个反应是可逆的;水可以与亚胺反应给我们的产品。
这是关键。如果你能找到一些方法来删除这里的水,你基本上关闭k2(逆反应)。那是什么要做整体反应?它将继续前进(向右)方向直至重新建立平衡。没有,因为我们增加了防潮珠。结果:一个产品,而不是一个混合物。
实际上,水可以通过几种方法,其中通过添加物质(称为干燥剂),将与水反应不可逆,因此将它从方程。硫酸镁(MgSO4)只是一个例子,它形成水合物。
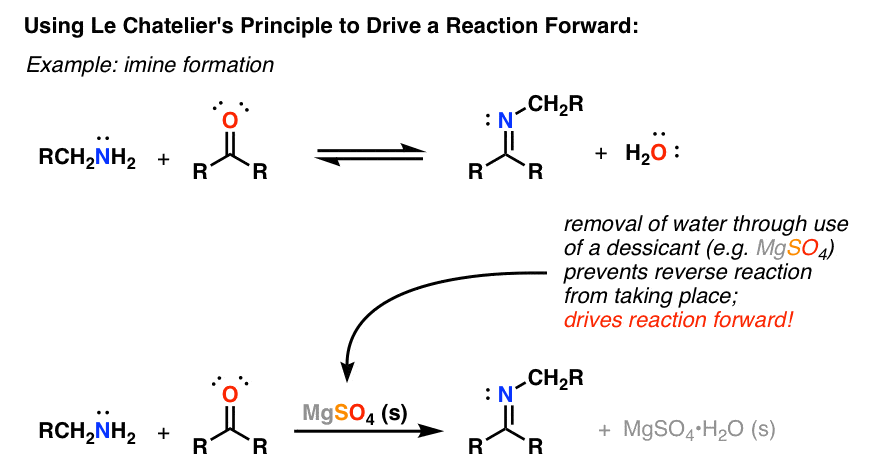
这个概念应该很熟悉你的名字:它叫勒夏特列原理。
你会遇到很多勒夏特列原理的例子在有机化学中,因为你会遇到很多的可逆反应(一些Org 1中,但是很多在Org 2)。
底线:如果你理解一个反应和它的产品,你可以选择条件,从而允许删除产品,将阻止一个平衡建立驱动反应,朝你想要的产品。
01焊接、结构和共鸣
- 我们怎么知道甲烷(CH4)是四面体吗?
- 杂化轨道和杂交
- bdapp.
- 轨道杂化和债券的优势
- σ键有六种:π键
- 一个关键技能:如何计算形式电荷
- 部分费用给线索电子流
- 四个分子间作用力以及它们是如何影响沸点
- bdappcom
- 如何使用电负性来确定电子密度(以及为什么不相信形式电荷)
- 介绍了共振
- 如何使用弯曲的箭头来交换共振形式
- bdapp1中国有限公司
- 如何找到最好的共振结构通过应用电负性
- 评估与负电荷共振结构
- 评估与正电荷共振结构
- 探索共振:Pi-Donation
- 探索共振:Pi-acceptors
- 总之:评估共振结构
- 画共振结构:3避免常见的错误
- 如何理解应用电负性和共振反应
- 债券杂交实践
- 结构和成键练习测验
- 共振结构的实践
02酸碱反应
03烷烃和命名法
04构象和环烷
05年有机反应的底漆
- 最重要的问题,当学习一门新反应
- 4反应的主要类Org 1
- 学习新的反应:电子移动如何?
- (为什么)电子流如何
- 第三个最重要的问题,当学习一门新反应
- 7因素稳定负电荷有机化学
- 7因素稳定有机化学中正电荷
- 常见错误:正式指控可以误导
- 亲核试剂与亲电试剂
- 弯曲的箭头(反应)
- 弯曲的箭头(2):最初的反面和最终的正面
- 亲核性与碱性
- 的三个类亲核试剂
- 是什么让一个好亲核试剂?
- 是什么让一个好的离去基团?
- 3因素,稳定的碳正离子
- 平衡和能量的关系
- 过渡态是什么?
- 哈蒙德的假设
- 格罗斯曼的统治
- 首先画丑陋的版本
- 学习有机化学反应:一个清单(PDF)
- 介绍加成反应
- 介绍了消除反应
- 介绍自由基取代反应
- 介绍了氧化裂解反应
06自由基反应
07年立体化学和手性
08年置换反应
09年消除反应
11SN1 SN2 / E1、E2的决定
12烯烃的反应
- 烯烃E和Z符号(+顺/反式)
- 烯烃的稳定性
- 加成反应:消除的相反
- 选择性与特定的
- 在烯烃加成反应的区域选择性
- 烯烃加成反应的立体选择性:Syn vs反加法
- 马氏的HCl烯烃
- 烯烃Hydrohalogenation机制以及它如何解释马氏规则的像
- 箭头和烯烃加成反应
- 除了模式# 1:“碳正离子通路”
- 重组在烯烃加成反应
- 卤化烯烃和Halohydrin形成
- 烯烃加成模式# 2:“三元环”的途径
- 硼氢化反应的氧化烯烃
- m-CPBA (meta-chloroperoxybenzoic酸)
- OsO4(四氧化锇)Dihydroxylation烯烃
- 钯碳催化加氢(Pd / C)
- 烯烃加成模式# 3:“协同”的途径
- 第四个烯烃加成模式——自由基
- 烯烃的反应:臭氧分解
- 简介:三个关键的家庭烯烃反应机制
- (4)-烯烃合成反应地图,包括烷基卤化物的反应
- 烯烃反应实践问题
13炔的反应
14醇、环氧化合物和醚
- 醇-命名法和属性
- 醇可以作为酸或碱(以及为什么它重要)
- 醇的酸度和碱度
- 威廉姆森醚合成
- 威廉姆森醚合成:规划
- 从烯烃醚,叔卤代烃和Alkoxymercuration
- 醇通过酸催化醚
- 劈理的醚酸
- 环氧化合物醚家族的离群值
- 的环氧化合物与酸
- 环氧开环与基础
- 卤代烃与醇
- 甲苯磺酸盐和甲磺酸
- PBr3和SOCl2
- 消除反应的醇
- 消除醇与POCl3烯烃
- 酒精氧化:“强大”和“弱”氧化剂
- 阐明酒精氧化反应的机制
- 分子内反应的醇类和醚类
- 保护组醇
- 硫醇和硫醚
- 计算一个碳的氧化态
- 在有机化学氧化和还原
- 氧化梯子
- SOCl2机制醇烷基卤化物:SN2和SNi
- 酒精反应路线图(PDF)
- 酒精反应练习题
- 环氧化物反应测试
- 氧化和还原练习测验
15有机金属化合物
16光谱学
17二烯烃和MO理论
- 有机化学2中会发生什么
- 这些分子共轭吗?
- 结合有机化学共振
- π成键和反键轨道
- 分子轨道的烯丙基阳离子,烯丙基自由基和烯丙基阴离子
- 丁二烯的π分子轨道
- 二烯烃的反应:1、2和1、4
- 热力学和动力学产品
- 添加更多的1、2和1、4二烯烃
- s-cis和s-trans
- Diels-Alder反应
- 循环二烯烃和Diels-Alder亲二烯体反应
- Diels-Alder反应的立体化学
- 一昼夜的桤木挂式vs Endo产品:如何分辨它们
- 在一昼夜的HOMO和LUMO桤木的反应
- 为什么Endo vs挂式产品青睐Diels-Alder反应?
- Diels-Alder反应:动力学和热力学控制
- 复古Diels-Alder反应
- 分子内一昼夜的桤木的反应
- Regiochemistry Diels-Alder反应
- 应对和克莱森重组
- Electrocyclic反应
- Electrocyclic开环和闭包(2)——六个或八个π电子
- 一昼夜的桤木练习题
- 分子轨道理论实践
18芳香性
19芳香分子的反应
- 亲电芳香取代:介绍
- 激活和去活化组织在亲电芳香取代反应
- 亲电芳香取代的机制
- 昊图公司,Para -和元董事亲电芳香取代反应
- 理解邻、对位、和元董事
- 为什么卤素昊图公司-帕拉-董事?
- 双取代的苯:最强的捐赠者“赢”
- 亲电芳香取代(1)——卤化苯
- 亲电芳香取代(2)——硝化、磺化
- 东亚峰会(3)——傅克酰化和傅克烷基化反应
- 分子内的傅克反应
- 亲核性芳香取代(NAS)
- 亲核芳香替代(2)-苯炔机制
- 反应在“苄基的“碳:溴化和氧化
- Wolff-Kishner Clemmensen,羰基和其他减少
- 更多的反应芳香Sidechain:减少硝基和拜耳威利格
- 芳香族合成(1)——“操作”
- 合成的苯衍生物(2)-极性倒转
- 芳香族合成(3)-磺酰阻断组
- 桦树减少
- 苯的合成(7):反应地图和相关的芳香族化合物
- 芳香族合成反应和实践
- 亲电芳香取代实践问题
我认为这应该是标准吉布斯自由能表达式而不是吉布斯自由能……标准吉布斯自由能是差异产品和反应物的吉布斯自由能
平衡常数的表达式相关的吉布斯自由能究竟是德尔·G .它的产品或反应物…不能自平衡系统del G = 0
对我来说这个澄清。谢谢你!
你为什么计算equilibirum反应的δG如果δG零平衡?有什么来计算?
这是一个奇妙的问题。
之间的区别是δG * *系统和δG°(形成的能量)的各个组件。
* *系统在平衡时,δG是零。没有净变化的能量。
如果平衡常数1(浓度=反应物的浓度)的产品我们也可以* *说,δG°(δG的生成)的产品相当于反应物。
但大多数时候,平衡常数(或降低)大于1(取决于哪个方向你画方程)。这意味着一个组件更* *比其他稳定,我们可以联系他们的相对稳定性通过吉布斯自由能平衡方程,δG°= RT ln k .如果我们知道平衡常数在给定温度我们可以重新排列方程解出能量的差异。
这说得通吗?