烯醇、烯醇化物
罗宾逊的环状结构
最后更新:2023年5月19日|
罗宾逊的环状结构
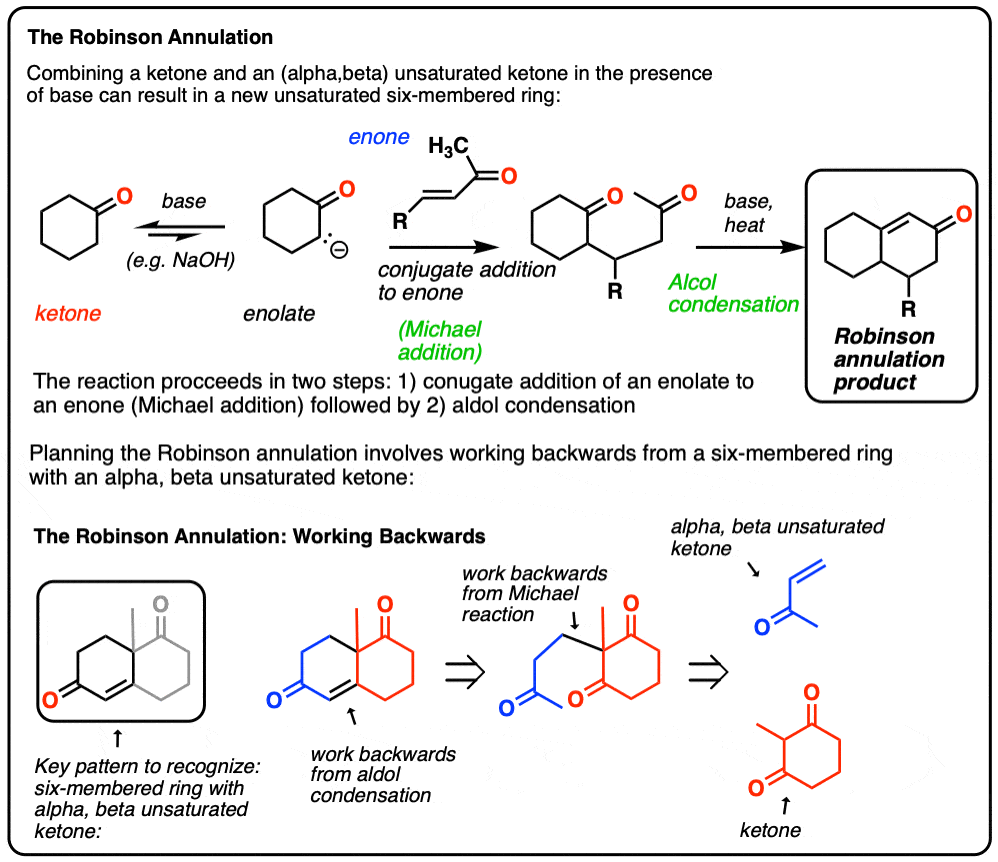
罗宾逊的环状物的名称是一个过程,结合前面学习的两个关键反应到一个时间序列。
反应开始迈克尔反应,紧随其后的是一个分子内醇醛缩合给一个新的包含一个六元环α,β不饱和酮。这篇文章进入所有的细节!
表的内容
- 回顾分子内反应
- 的醇醛缩合
- 的分子内醇醛缩合
- 五、六元环是青睐
- 迈克尔反应给1,5-Diketones
- 罗宾逊的环状结构
- 罗宾逊环状结构的机制
- 从产品逆向思考
- 好处:两个现代应用程序
- 笔记
- (高级)引用和进一步阅读
1。回顾分子内反应
有一些关于分子内反应经常旅行的学生。
从概念上讲,理解一个分子内反应并没有太大的不同理解当你系带,使一个循环的过程。
然而…。我看到学生进入考试认为他们知道反应冷,但是当突然面对的一个例子亲核试剂和一个亲电试剂在一起在相同的分子,他们冻结。
尽管这一事实完全相同的债券形式和休息!
没关系。有机化学似乎很抽象。它可以花时间去欣赏,所有这些符号我们画分子代理三维物体,并遵循他们的许多熟悉的原则!
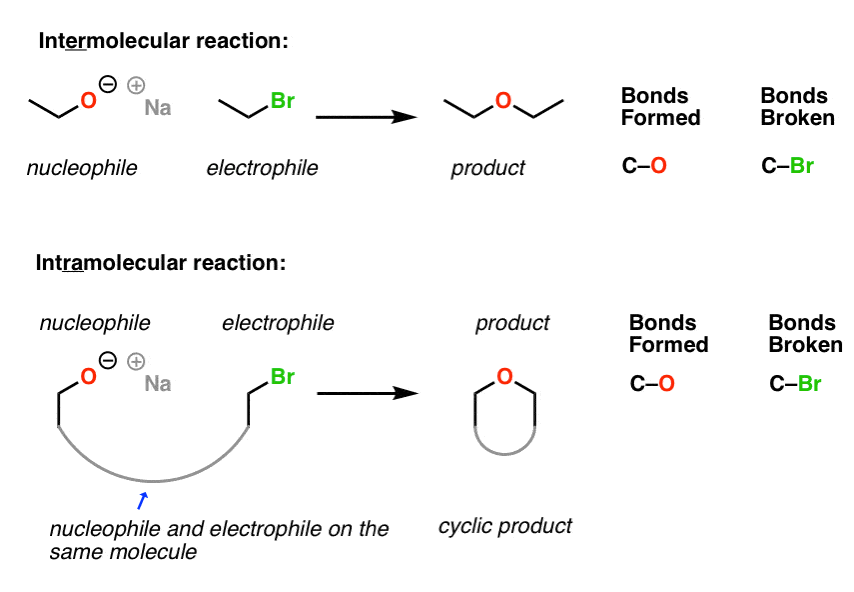
(以前的帖子:一个共同的盲点:分子内反应,分子内形成醚,分子内的傅克反应]
今天的醇醛缩合的分子内治疗,这是一个更大的过程称为罗宾逊环状结构。
再问:什么是醇醛缩合吗?
好的。快速回顾一下。
2。的醇醛缩合
base-catalyzed版本的醇醛缩合始于一个亲核的形成烯醇化物通过去质子化的“α碳”一个醛或酮,并在随后添加亲核试剂的亲电羰基碳的第二个醛或酮,形成新的碳碳键。
在加热时,产生的醇醛加成产品是deprotonated给一个新烯醇化物,然后取代氢氧根离子,导致碳碳双键伴随着水的净亏损(H2O)。(请注意这是一个消除通过的例子E1cb机制]由此产生的产品包含一个α,β不饱和酮(或醛)是醇醛缩合产品。
这张照片显示了结果的两个分子之间的醇醛缩合-丙酮(又名“丙酮”)。
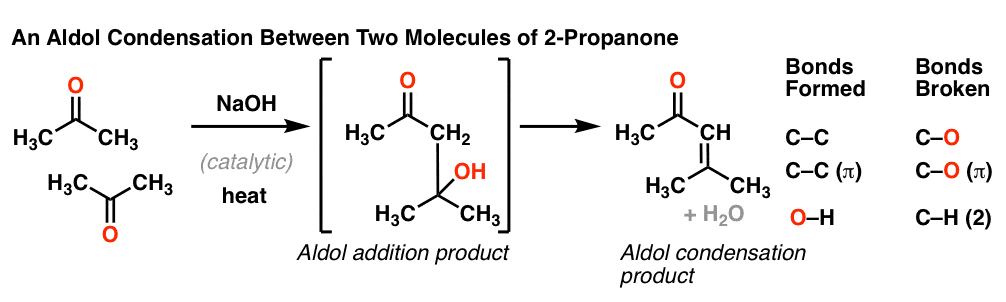
那么一个分子内的醇醛反应看起来像什么?截然不同?
3所示。的分子内的醇醛缩合
不,不是截然不同。实际上,我们需要做的就是两个碳氢键替换为一个碳碳键链接两个酮。就是这样!
现在我们的亲核试剂我们碰巧在同一个分子亲电试剂。所以,就像紧固带,当两个结合,我们获得一个“循环”,或者戒指。
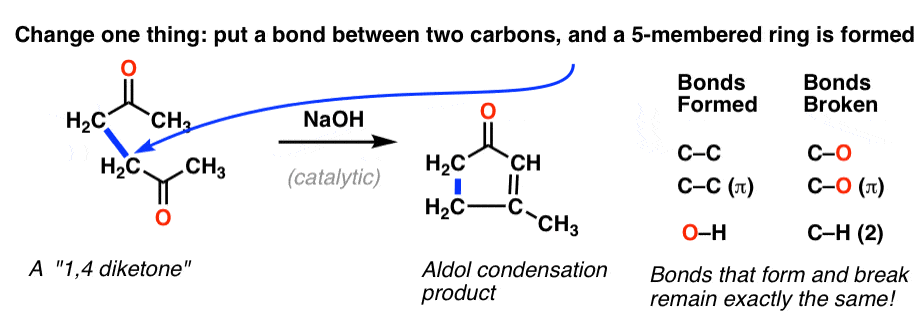
的机制是完全相同的。在基础治疗(如氢氧化钠)烯醇化物仍然形式,还增加了一个酮。和净亏损后的H2啊,完全相同的序列债券已形成和破碎。唯一的区别是,由于两个酮有关,我们现在有一个戒指!
4所示。分子内反应支持五年和六元环的形成
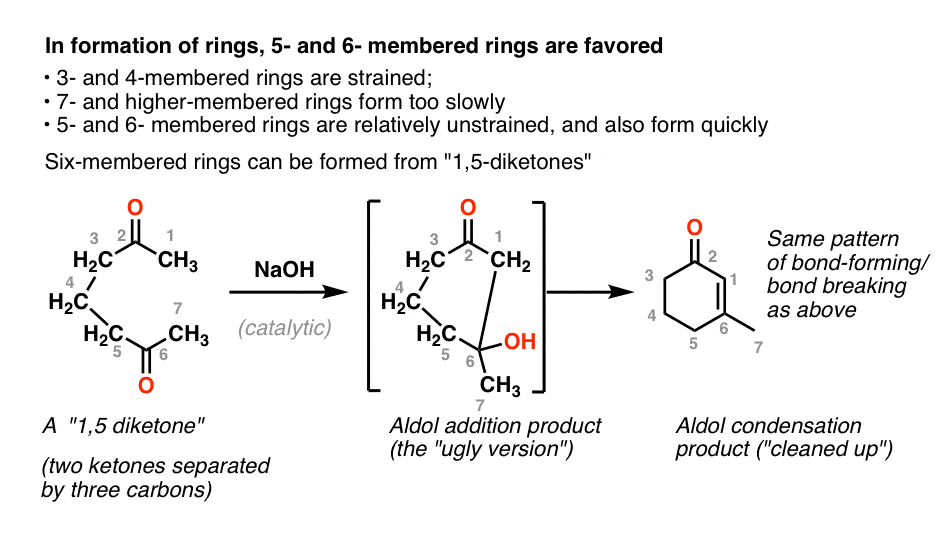
最好的候选人环会关闭五、六元环低环应变,结合合理的反应速率。
三,四元环往往遭受环应变。这不是不可能的3 -和4-membered环形式(分子内反应形成环氧化合物存在,毕竟-看到这篇文章),但在一个过程步骤是在平衡(因此潜在可逆的),这一过程形成了一个热力学不牵强附会的五年或六元环将支持在一个形成一个三或四元环。(注2]
7 -和higher-membered戒指慢形成由于较低的有效浓度亲核试剂附近的亲电试剂。
一个例子的形成六元环的分子内反应“1,5-diketone”如下所示。【注:这里的1和5不要IUPAC参考编号,但第二的事实酮从第一个是4个碳)。债券的模式形式,打破上面一模一样。
5。迈克尔反应给1,5-Diketones
我们已经见过的反应,使1,5-diketones:迈克尔反应。
回顾一下:迈克尔反应涉及的一个亲核的烯醇化物“贝塔”(β)碳双键的α,beta-unsaturated酮在这一过程被称为“共轭加成”或“1,4-addition”(吉尔曼的突出的反应试剂(organocuprates):明白了吉尔曼试剂:它们的用途]。这个结果在一个新烯醇化物。质子化作用的烯醇化物然后给出了1,5-diketone:
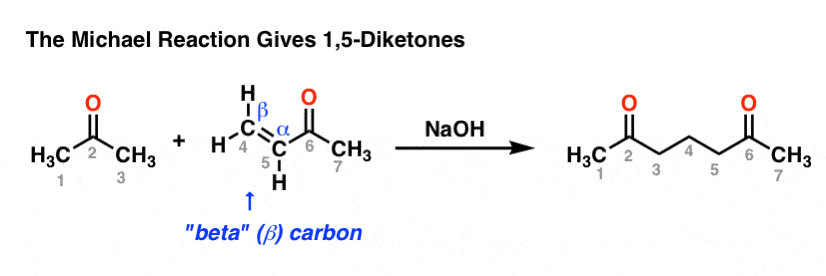
现在让我们一起加入这两个线程。在有机化学模式识别是一项关键的技能!
- 自1,5-diketones可以通过分子内醇醛缩合形成六元环…
- 和…1,5二酮可通过迈克尔反应…
- …而且,他们都需要相同的试剂(基地,如氢氧化钠)…
然后如果我们搅拌在一起会发生什么酮、一个αbeta-unsaturated酮,氢氧化钠,然后加热混合物?我们会得到一个分子内醇醛缩合产品?
是的!在一个1935年的论文罗伯特•罗宾逊和合作者威廉Rapson甲基取代的报道乙烯基酮和环己酮为一个产品用一个新的六元环包含α,β不饱和酮:
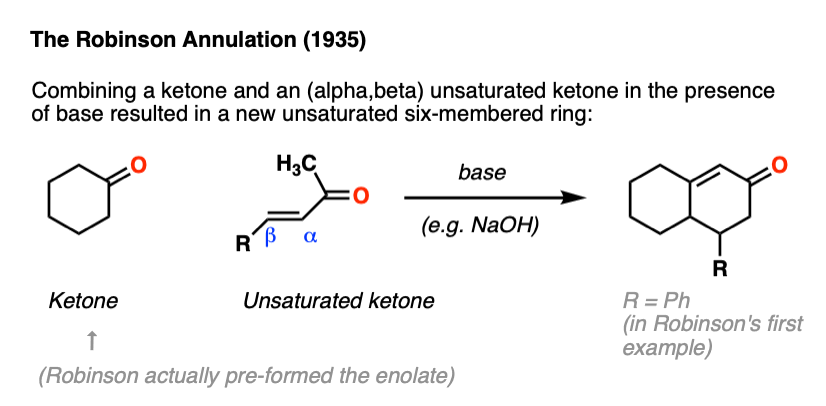
这被称为罗宾逊环状物,今天仍然发现使用。(注1]
迈克尔反应的过程开始和结尾给新环的分子内醇醛缩合。这是一个经典的例子串联反应(或级联),在最初的反应提供了一个连续反应的起始物料。
7所示。罗宾逊环状结构的机制
迈克尔反应段包括三个步骤:
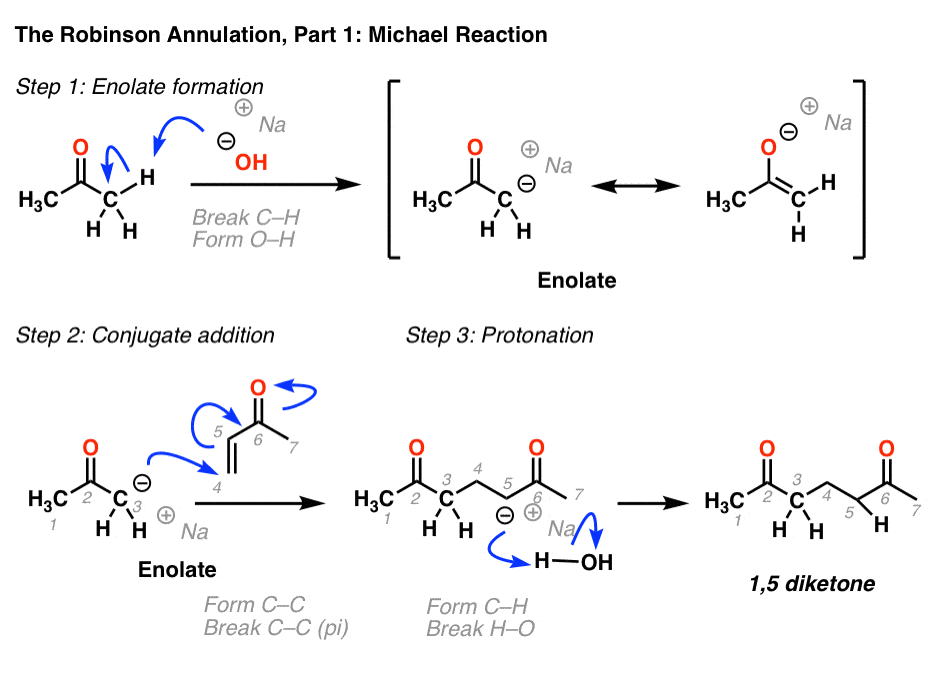
1,5-diketone由迈克尔反应成为下一段的起始物料罗宾逊环状物,的分子内醇醛缩合。
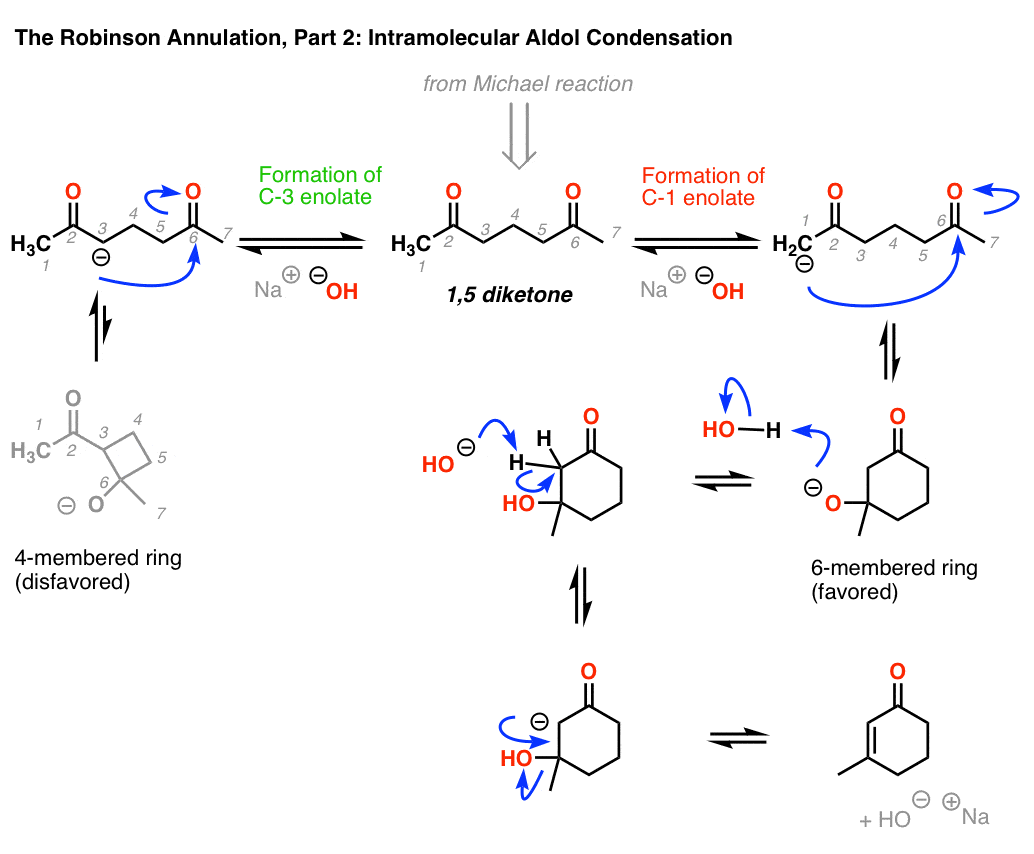
- 醇醛缩合始于去质子化的5-diketone给一个烯醇化物颈- 1上(注意,有两个烯醇化物,可以形成,在颈- 1和颈- 3(由于分子是对称的,这些是等价的,即和c - 5,分别)。然而,c - 3烯醇化物是一个终端;(紧张)4-membered环的形成是可逆的,和平衡最终会导致反应形成六元醇醛缩合产物)
- 的形成烯醇化物在颈- 1是紧随其后的是攻击酮五个碳,六元环。
- 质子化作用的带负电荷的氧气,其次是在相邻的碳去质子化,给出了一个新的烯醇化物。
- 这烯醇化物方法的氢氧根离子(HO)相邻的碳,形成新的碳碳双键,导致醇醛缩合产物。
8。罗宾逊环状物Retrosynthesis:向后工作
这是非常重要的是能够看罗宾逊环状结构的产物的结构和工作向后两个组件。
- 第一步是认识到关键模式在鲁滨逊的产物:一个六元环中含有一个双键毗邻酮(α,β不饱和酮)。
- 接下来,向后的工作醇醛缩合:所以在相反的方向上,打破C = C键和两个碳氢键(一端α碳的酮)和C = O键的另一端。
- 最后,工作向后迈克尔:打破碳碳键,和替换一个碳碳π键组件和一个碳氢键。
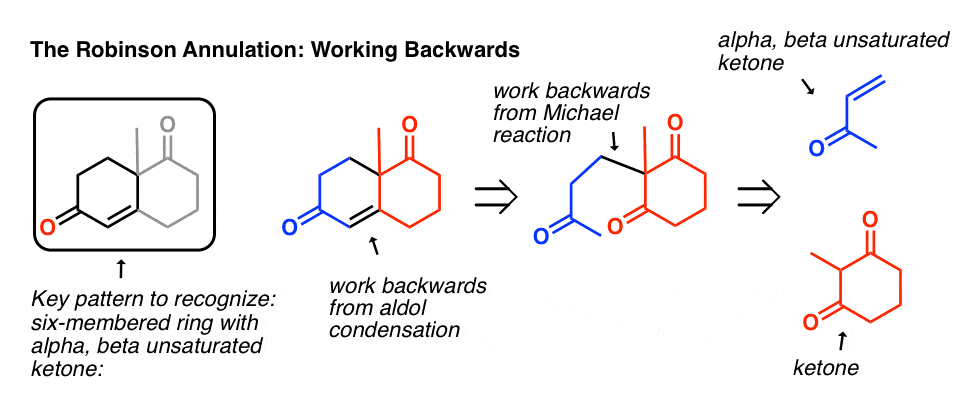
作为练习,尝试工作从下面的例子:
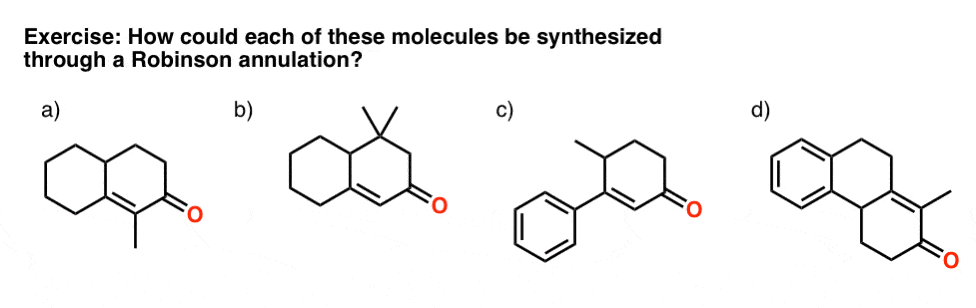
答案在这里(点击图片会弹出)。
这可能是足够的罗宾逊。
但敏锐,我提出两个应用程序的这个反应合成,尤其是应用于类固醇。
9。好处:罗宾逊环状结构的两个应用程序
您可能已经注意到,六元环使相当多的有机化学中露面。所以罗宾逊环状物发现的有用的应用程序。
一个著名的例子是发现在工业合成的类固醇激素雌激素酮前体的避孕药物的活性成分。
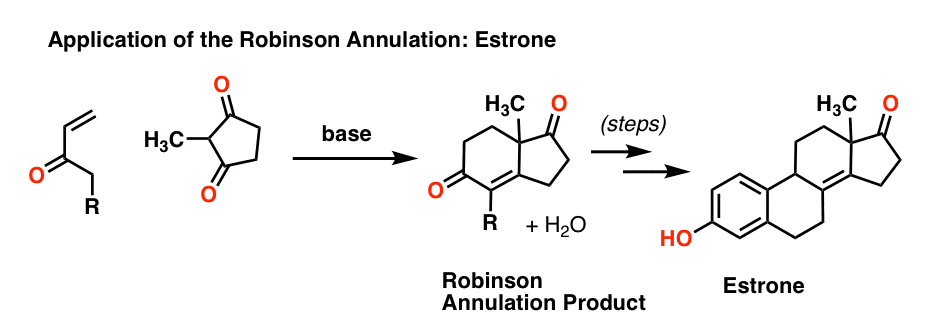
另一个例子是下面的分子的合成,称为Wieland-Miescher酮另一个有用的前体的合成类固醇和萜烯:
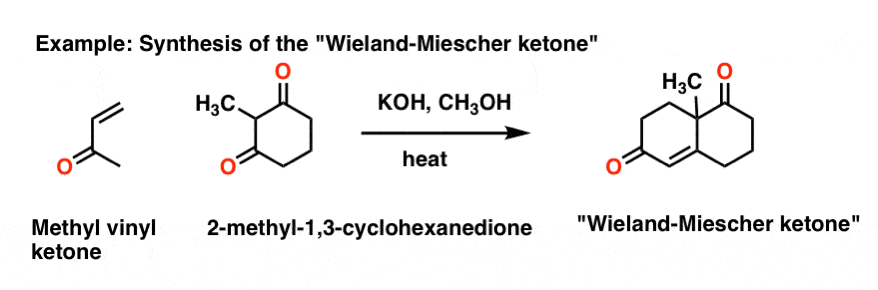
是什么让这个特别高收益的例子是pK一个二酮的约11,确保它将deprotonated选择性超过所有其他可能的alpha-carbons (pK一个~ 16)有助于确保迈克尔反应相对高产。此外,甲基在那个位置确保不能再deprotonated分子内醇醛缩合步骤。
在这一点上我要承认,上面的示例中,写的,有点欺骗。而(Michael)的第一步是通过氢氧化钾的使用,发现第二步可以实现使用催化(大约10摩尔%)吡咯烷或哌啶,经历一个enamine-promoted醇醛缩合。(有趣的练习:画出来)
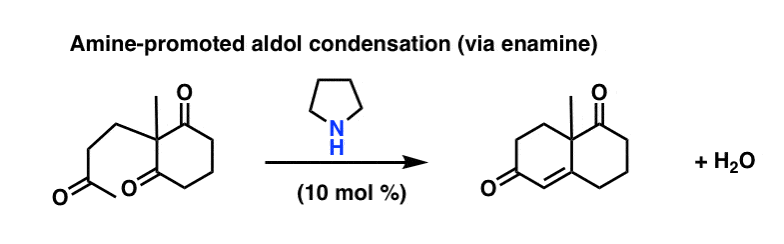
这里的关键之一是采用Dean-Stark陷阱由此形成的水作为反应的结果,推动反应完成。
有趣的事实。这个分子内胺催化醇醛缩合的发展实际上是一个关键的油石现代化学研究中最重要的领域之一。
1971年,Zoltan Hajos和大卫·帕里什有了一个好主意,使用(手性)L-proline取代吡咯烷(名字很奇怪Hajos-Parrish-Eder-Sauer-Wiechert反应导致一个光学活性的产品。这个结果或多或少地休眠坐在化学文献大约三十年,直到这2000年的论文巴尔巴斯、列表和Lerner的发展打开了闸门organocatalysis。
笔记
注1。即使在过去的几年中,罗宾逊环状物已经开发出来的新变化。一个拆分的例子从Toste实验室突出显示在这里。
注2。另一个关键因素是,环丁烯甚至更多的环应变(30千卡每摩尔)比环丁烷(26千卡每摩尔). .因此,形成4-membered醇醛缩合产物更是不可能的。
(高级)引用和进一步阅读
- 实验的合成甾醇类物质有关。第二部分。一个新的替换cyclohexenones的一般合成方法
威廉圣人Rapson和罗伯特·罗宾逊
j .化学。Soc。,1935年,1285 - 1288
DOI:10.1039 / JR9350001285
原始论文先生罗伯特·罗宾逊新合成方法措施,他应用总胆固醇和其它植物固醇的合成。 - 罗宾逊annelation反应的2 -甲基1,3二酮.beta.-chloro酮
a . Zoretic b Bendiksen, b . Branchaud
《有机化学》杂志上1976年41(23),3767 - 3767
DOI:10.1021 / jo00885a029
罗宾逊环状结构的一个例子提供一个实验过程——这应该是相当强健,因为工作是由两个大学生! - (S) 8 a-methyl-3、4、8、8 a-tetrahydro-1 6 (2 h, 7 h) -NAPHTHALENEDIONE
保罗•Buchschacher a·福斯特和j . Gutzwiller
Org。Synth。1985年,63年37岁的
DOI:10.15227 / orgsyn.063.0037
标题化合物的过程有机合成也被称为Wieland-Miescher吗酮中,一个常见的构建块的总合成类固醇和萜类化合物。 - 罗宾逊Annelation和相关反应
罗伯特·e·GAWLEY
合成1976年;1976年(12):777 - 794
DOI:10.1055 / s - 1976 - 24200
尽管本文可能会超过40岁了,仍然是一个有用的参考罗宾逊环状结构和相关的化学反应。
- 罗宾逊proline-catalyzed不对称环状结构的反应
汤米Bui,卡洛斯·f·巴尔巴斯III
四面体的信体积41岁的问题36岁,2000年9月,页6951 - 6954
DOI:1016 / s0040 - 4039 (00) 01180 - 1
氨基酸脯氨酸能促进罗宾逊环状结构,证明了本文的一个早期的例子是一个令人兴奋的新领域,organocatalysis。 - 总(−)-Anominine的综合
Ben Bradshaw Gorka Etxebarria-Jardi,约瑟Bonjoch
美国化学学会杂志》上2010年132年(17),5966 - 5967
DOI:1021 / ja101994q
非对称罗宾逊环状结构(2- >3)担任这个天然产物全合成的起点。 - 催化罗宾逊Annelations
克莱顿·h·和约翰·e·埃利斯约翰·e·McMurry安东尼•Coppolino
四面体信件,12 (52),1971年,4995 - 4996
DOI:10.1016 / s0040 - 4039 (01) 97609 - 9。本研究包含几个催化罗宾逊环状结构(使用H的例子2所以4)
由于詹姆斯先生!对我来说是一个新话题,但现在我懂了吗
这是一个详细的记录。
它清楚地解释并演示罗宾逊环状结构。好一个
第一次在这里评论。我可以知道如果使用鹳烯胺的迈克尔加成反应一步将导致更高的收益率的双环产品?我读过烯醇化物不是特别好的迈克尔捐助者所以他们将有利于羰基碳的攻击进行醇醛缩合而不是迈克尔反应。
难以概括。你计划在迈克尔加成α-β不饱和酮或αβ不饱和醛吗?如果你使用酮、共轭加成途径应该好(我将更加着重探讨醇醛如果是醛)。
记住,鹳烯胺你要让less-substituted烯胺,这是需要考虑的一个因素。
这是反应你会执行在实验室或这是“纸上”吗?
固定
你能请retrosynthetic罗宾逊环状物的答案吗?谢谢
感谢你如此详细的解释! !
这个网站已经相当惊人。这是一个比任何教科书更好的教学资源。罗宾逊在1935例中,R (Ph)应该是一个碳转移到正确的产品(见1935年引用)。
谢谢你,我很高兴你找到该网站有帮助。詹姆斯
在罗宾逊(1935)的例子中,R组应该在β碳(似乎在伽马碳产品)?
射击,将修复,谢谢你的正面。
抱歉延迟:在这里://m.deriinvest.com/wp-content/uploads/2020/12/supp-robinson-annulation-answers-compressed.gif
是的,就在这里://m.deriinvest.com/wp-content/uploads/2020/12/supp-robinson-annulation-answers-compressed.gif
你能发布答案罗宾逊环状结构问题吗?
请给我答案
谢谢你的伟大的页面!
你能把答案吗?
感谢你上传这样一个明确的职位罗宾逊环状物!我一直在到处都理解这个反应,但我从来没有发现好的,直到今天我看到了你的帖子!看起来这很最近的文章,所以我想我很幸运,现在看到这篇文章。希望你有一个很伟大的圣诞节,并感谢你分享这篇文章是免费的。:)
很高兴你发现它有用的珍妮弗!
我可以得到答案吗?谢谢!