家/3影响沸点的趋势
焊接、结构和共鸣
3影响沸点的趋势
最后更新:2022年12月14日|
找出沸点的顺序了解趋势。这里的关键考虑是沸点反映分子之间的力的强度。他们粘在一起越多,更多的能量将会爆炸气体到大气中。
有三个重要的趋势,需要考虑。
- 的相对强度四分子间作用力是:离子>氢键>偶极偶极子>范德瓦耳斯分散部队。这些引力的影响将取决于官能团。
- 沸点增加随着碳原子数量的增加。
- 分支沸点降低。
让我们来仔细:。
表的内容
1。趋势1:四分子间作用力的相对强度。
比较不同的丁烷酒精衍生品所示。分子的乙醚,C4H10啊,是在一起取向相互作用,出现由于极化切断债券。
比较乙醚的沸点(35°C)的异构体1-butanol(117°C)。的大大增加沸点是由于丁醇包含的事实羟基集团有能力氢键。
不过,丁醇苍白的引力与钠盐醚相比,哪个融化在一个非常高的温度(高于260°C)和分解才能变成一个液体和沸腾。
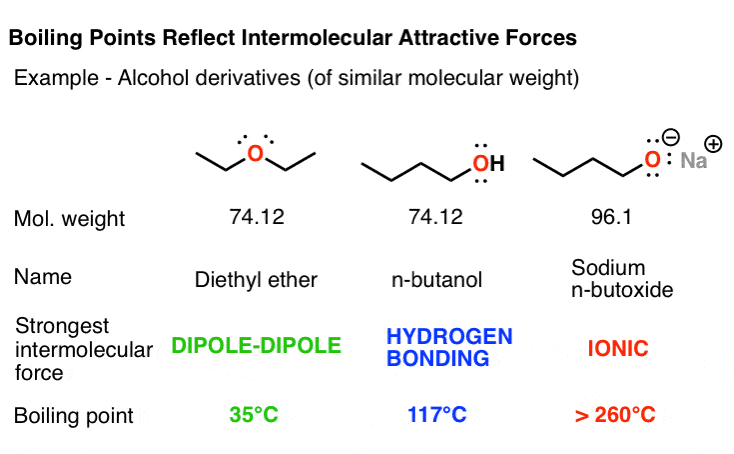
然后想想丁烷,C4H10,其中包含没有极性官能团。唯一个人丁烷分子之间的引力是相对较弱的范德华色散力。结果是,丁烷的沸点是水结冰的温度(0°C),甚至远低于乙醚。
故事的寓意:在分子大致相似的分子量,沸点将由官能团。
你可以告诉一个类似的故事类似的胺和羧酸的同分异构体所示。
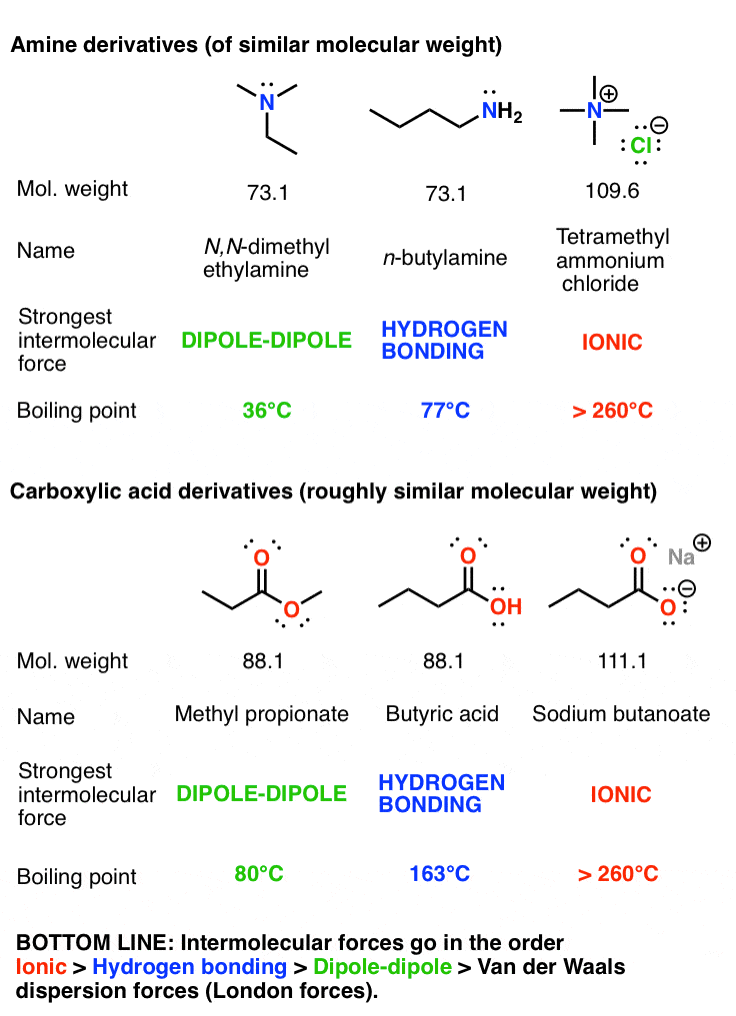
先前的讨论的4分子间作用力,看到一篇文章(四个分子间作用力以及它们是如何影响沸点)
2。趋势# 2 -分子与一个给定的官能团,沸点随分子量。
看看沸点增加分子量急剧增加在所有这些系列:
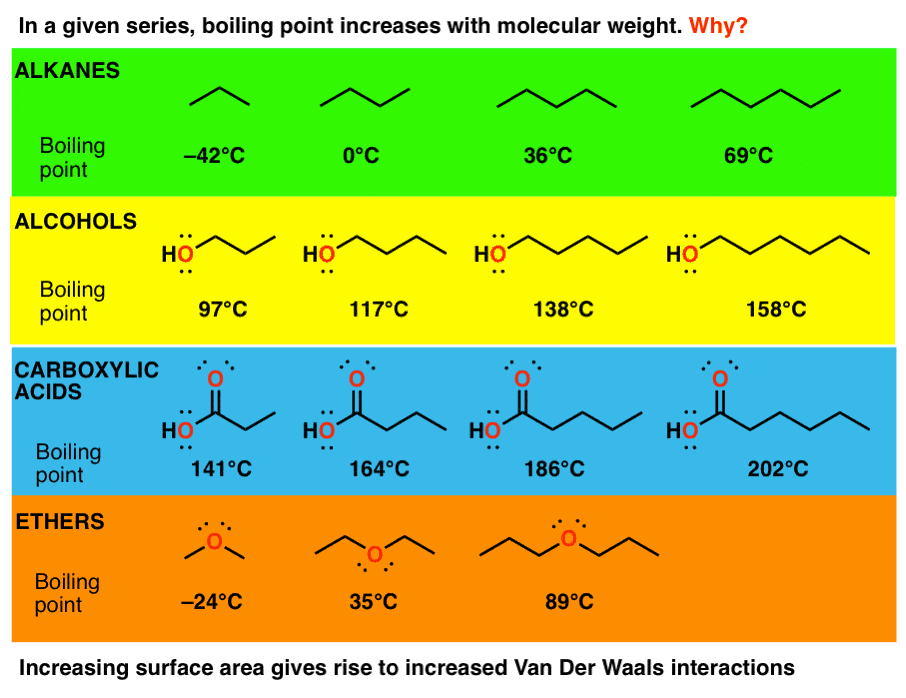
这是一个问题:如何,随着分子量的增加分子间作用力增加确切指的是什么?
这里的关键力作用是范德瓦耳斯色散力,这是与表面积成正比。所以当你增加的长度链,你也增加了表面积,这意味着你增加单个分子的相互吸引。
在一个直观的层面上,你可以比较这些长分子链的意大利面条,面条的时间越长,所需要的更多的工作把他们分开。随着链长度的增加,将会有地区,在那里他们可以排队彼此非常好。
个人,每个交互可能非常不值得,但当你把它们全部加起来除以链的长度,范德瓦耳斯色散力可以起到巨大的作用。
3所示。对称的作用(或缺乏)熔点和沸点
这是另一个的副产品的表面积依赖范德瓦耳斯色散力,棒状分子越多,他们将会更好的和债券。
采取另一个直观的面食的例子,粘在一起:意大利面或通心粉?spherelike分子越多,降低它的表面积和分子间范德华相互作用将越少。比较戊烷的沸点(36°C)和2,2-dimethyl丙烷(9°C)。
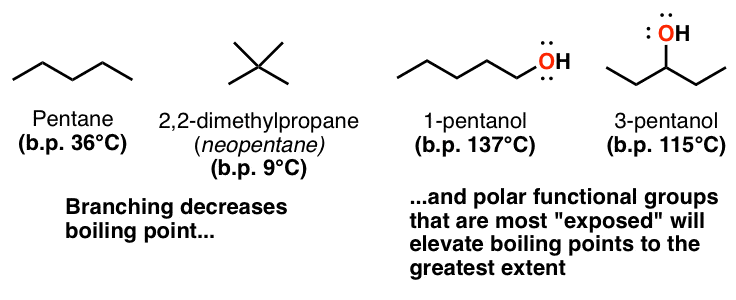
它还可以应用于氢键分子醇的沸点比较1-pentanol 2-pentanol 3-pentanol,例如。的羟基1-pentanol比在“暴露”3-pentanol(两侧是两个笨重的烷基组),所以它将能更好地与其同伴氢键。
总的来说,主要有三个因素需要考虑当面对一个问题关于沸点。1)分子分子间作用力将出现在什么?2)分子量比较如何?3)对称性比较如何?
最后一个小问题的道路(见注释回答)。
笔记
注:新!看看这个免费的3页讲义共同沸点解决考试问题!
01焊接、结构和共鸣
- 我们怎么知道甲烷(CH4)是四面体吗?
- 杂化轨道和杂交
- bdapp.
- 轨道杂化和债券的优势
- σ键有六种:π键
- 一个关键技能:如何计算形式电荷
- 部分费用给线索电子流
- 四个分子间作用力以及它们是如何影响沸点
- bdappcom
- 如何使用电负性来确定电子密度(以及为什么不相信形式电荷)
- 介绍了共振
- 如何使用弯曲的箭头来交换共振形式
- bdapp1中国有限公司
- 如何找到最好的共振结构通过应用电负性
- 评估与负电荷共振结构
- 评估与正电荷共振结构
- 探索共振:Pi-Donation
- 探索共振:Pi-acceptors
- 总之:评估共振结构
- 画共振结构:3避免常见的错误
- 如何理解应用电负性和共振反应
- 债券杂交实践
- 结构和成键练习测验
- 共振结构的实践
02酸碱反应
03烷烃和命名法
04构象和环烷
05年有机反应的底漆
- 最重要的问题,当学习一门新反应
- 4反应的主要类Org 1
- 学习新的反应:电子移动如何?
- (为什么)电子流如何
- 第三个最重要的问题,当学习一门新反应
- 7因素稳定负电荷有机化学
- 7因素稳定有机化学中正电荷
- 常见错误:正式指控可以误导
- 亲核试剂与亲电试剂
- 弯曲的箭头(反应)
- 弯曲的箭头(2):最初的反面和最终的正面
- 亲核性与碱性
- 的三个类亲核试剂
- 是什么让一个好亲核试剂?
- 是什么让一个好的离去基团?
- 3因素,稳定的碳正离子
- 平衡和能量的关系
- 过渡态是什么?
- 哈蒙德的假设
- 格罗斯曼的统治
- 首先画丑陋的版本
- 学习有机化学反应:一个清单(PDF)
- 介绍加成反应
- 介绍了消除反应
- 介绍自由基取代反应
- 介绍了氧化裂解反应
06自由基反应
07年立体化学和手性
08年置换反应
09年消除反应
11SN1 SN2 / E1、E2的决定
12烯烃的反应
- 烯烃E和Z符号(+顺/反式)
- 烯烃的稳定性
- 加成反应:消除的相反
- 选择性与特定的
- 在烯烃加成反应的区域选择性
- 烯烃加成反应的立体选择性:Syn vs反加法
- 马氏的HCl烯烃
- 烯烃Hydrohalogenation机制以及它如何解释马氏规则的像
- 箭头和烯烃加成反应
- 除了模式# 1:“碳正离子通路”
- 重组在烯烃加成反应
- 卤化烯烃和Halohydrin形成
- 烯烃加成模式# 2:“三元环”的途径
- 硼氢化反应的氧化烯烃
- m-CPBA (meta-chloroperoxybenzoic酸)
- OsO4(四氧化锇)Dihydroxylation烯烃
- 钯碳催化加氢(Pd / C)
- 烯烃加成模式# 3:“协同”的途径
- 第四个烯烃加成模式——自由基
- 烯烃的反应:臭氧分解
- 简介:三个关键的家庭烯烃反应机制
- (4)-烯烃合成反应地图,包括烷基卤化物的反应
- 烯烃反应实践问题
13炔的反应
14醇、环氧化合物和醚
- 醇-命名法和属性
- 醇可以作为酸或碱(以及为什么它重要)
- 醇的酸度和碱度
- 威廉姆森醚合成
- 威廉姆森醚合成:规划
- 从烯烃醚,叔卤代烃和Alkoxymercuration
- 醇通过酸催化醚
- 劈理的醚酸
- 环氧化合物醚家族的离群值
- 的环氧化合物与酸
- 环氧开环与基础
- 卤代烃与醇
- 甲苯磺酸盐和甲磺酸
- PBr3和SOCl2
- 消除反应的醇
- 消除醇与POCl3烯烃
- 酒精氧化:“强大”和“弱”氧化剂
- 阐明酒精氧化反应的机制
- 分子内反应的醇类和醚类
- 保护组醇
- 硫醇和硫醚
- 计算一个碳的氧化态
- 在有机化学氧化和还原
- 氧化梯子
- SOCl2机制醇烷基卤化物:SN2和SNi
- 酒精反应路线图(PDF)
- 酒精反应练习题
- 环氧化物反应测试
- 氧化和还原练习测验
15有机金属化合物
16光谱学
17二烯烃和MO理论
- 有机化学2中会发生什么
- 这些分子共轭吗?
- 结合有机化学共振
- π成键和反键轨道
- 分子轨道的烯丙基阳离子,烯丙基自由基和烯丙基阴离子
- 丁二烯的π分子轨道
- 二烯烃的反应:1、2和1、4
- 热力学和动力学产品
- 添加更多的1、2和1、4二烯烃
- s-cis和s-trans
- Diels-Alder反应
- 循环二烯烃和Diels-Alder亲二烯体反应
- Diels-Alder反应的立体化学
- 一昼夜的桤木挂式vs Endo产品:如何分辨它们
- 在一昼夜的HOMO和LUMO桤木的反应
- 为什么Endo vs挂式产品青睐Diels-Alder反应?
- Diels-Alder反应:动力学和热力学控制
- 复古Diels-Alder反应
- 分子内一昼夜的桤木的反应
- Regiochemistry Diels-Alder反应
- 应对和克莱森重组
- Electrocyclic反应
- Electrocyclic开环和闭包(2)——六个或八个π电子
- 一昼夜的桤木练习题
- 分子轨道理论实践
18芳香性
19芳香分子的反应
- 亲电芳香取代:介绍
- 激活和去活化组织在亲电芳香取代反应
- 亲电芳香取代的机制
- 昊图公司,Para -和元董事亲电芳香取代反应
- 理解邻、对位、和元董事
- 为什么卤素昊图公司-帕拉-董事?
- 双取代的苯:最强的捐赠者“赢”
- 亲电芳香取代(1)——卤化苯
- 亲电芳香取代(2)——硝化、磺化
- 东亚峰会(3)——傅克酰化和傅克烷基化反应
- 分子内的傅克反应
- 亲核性芳香取代(NAS)
- 亲核芳香替代(2)-苯炔机制
- 反应在“苄基的“碳:溴化和氧化
- Wolff-Kishner Clemmensen,羰基和其他减少
- 更多的反应芳香Sidechain:减少硝基和拜耳威利格
- 芳香族合成(1)——“操作”
- 合成的苯衍生物(2)-极性倒转
- 芳香族合成(3)-磺酰阻断组
- 桦树减少
- 苯的合成(7):反应地图和相关的芳香族化合物
- 芳香族合成反应和实践
- 亲电芳香取代实践问题
随着碳原子数量的增加他们的分子质量增加和vanderwalls引力增加,这将导致增加的沸点较高的烃链
什么导致了更高的碳氢化合物的沸点很高吗?
哪一个具有较高的沸点CH3OH或酒精
这是你可以很容易地查找!
我试图找出如果醋酸会蒸发干燥步骤中我的化合物治疗后的溶液与氢氧化钠,pH值约8
是你的水溶性化合物或有机可溶性?因为如果是溶于有机溶剂,可以避免担心这仅仅通过与类似的乙酸乙酯提取。
如果你的化合物水溶性和你通过旋转蒸发干燥/蒸馏、醋酸和水会蒸发与出口增速。最后你将氢氧化钠/ NaOAc盐。
谢谢你,詹姆斯。
剩余的用同样的例子(极端的你说的),如果我使溶液稀释醋酸完全沸腾在去除水的烧杯,烧杯仍将是什么?醋酸盐吗?
你想净化乙酸吗?
比如乙酸在水的稀释溶液。将bp乙酸在酸性酸碱或基本变化吗?
很难回答这个问题没有更具体的细节。
在极端的情况下,很容易回答。例如,如果水与强酸完全质子化了的* *,就H3O +。被指控化合物因此波动性很低(这就是为什么硫酸通常用于去除水)。同样的道理,当水是完全deprotonated氢氧化钠。
同样的将醋酸如果是质子化了的完全或完全deprotonated。盐不波动。
我怎么分离同分异构体与沸点
柱层析法是一种选择吗?通常的主要方法,除非你有很多物质分离。是有原因的炼油厂是如此之大,他们本质上巨大的蒸馏操作!
下面哪个更高的沸点吗?,为什么?
酒精和HOCH2CH2OH
计算官能团的数量氢键的能力。
为什么2-butyne BP高于1-butyne吗?
好问题。我不惊讶2-butyne熔点更高,更严格的(少自由度甲基乙基)相比,因此应该比1-butyne堆栈在一起更容易。我想在沸点相同的因素在起作用——刚性结构会导致更大的整体分子之间的表面接触,意思就是secu * tanu减去VDW强色散因素,意味着更高的沸点。
为什么酒精的沸点增加随着分子量的增加
增加表面积。表面积增加意味着更多的范德华相互作用,这将增加沸点。
等级以下预期从低到高沸点:乙炔、甲烷,Ne, H3COCH3。
首先问自己是什么分子间作用力的在每一个分子。
这是非常有用的,沸点,已经开始有意义的开始。之前找到这个我看课堂笔记和课本试图找出是什么让分子沸点不同,我不能找到一个好的答案。使用这个页面我能回答一个问题在我的任务。我要研究可打印表,以便下次更容易。
很酷,我很高兴你找到了有用的梅根。学习的趋势是关键!
有点困惑,不是沸点取决于分子的属性?因此,沸点升高只取决于粒子的数量在一个解决方案,不是这些粒子的性质?还是依数性因素只申请离子键——这就是为什么他们是如此之高沸点有机分子相比。
我们不应对溶质&解决方案,液体的沸点。每一个纯化合物有一个不同的沸点,取决于分子间引力。
你能解释为什么比戊烷乙氧基的乙烷沸点较低?
的沸点高甲氧基乙烷正丁烷相比?
这不是矛盾的吗?
这是一个非常狂野的事实,不是吗?你不会希望乙醚会比戊烷沸点较低。
非常感谢……它帮助很多。单是很神奇的。
酷。谢谢Sourabh。
巨大的资源,即使是有机老师!感谢您使内容简洁和容易理解!
在这里,我总结了一些沸点halobutane烷基链通过增加沸点秩序。的手,eazier看到增加的趋势不同的卤素原子甚至混合丁烷烷基链。
'c Perfluorobutane英国石油(bp): 7
丁烷bp: -0.5 'c
1-Fluorobutane bp: 32 'c
1-Chlorobutane英国石油(bp): 77 - 78 - 'c
1-Bromobutane英国石油(bp): 100 - 104 - 'c
1-Iodo-tert-butyl英国石油(bp): 118 - 120 - 'c
2-bromo-2-chlorobutane bp: 120 'c
2-bromo-1-chloro-2-methylpropane bp: 127 'c
1-Iodobutane英国石油(bp): 130 - 131 - 'c
1-Bromo-4-fluorobutane英国石油(bp): 134 - 135 - 'c
1-bromo-3-chloro-2-methylpropane bp: 153 'c
1-Bromo-3-chlorobutane bp: 154 'c
1,4-Dichlorobutane英国石油(bp): 161 - 163 - 'c
1-Bromo-4-chlorobutane英国石油(bp): 177 - 180 - 'c (80 - 82 'c / 30毫米汞柱)
1,4-Dibromobutane英国石油(bp): 195 - 198 - 'c (63 - 65 - 'c / 6毫米汞柱)
1-Chloro-4-iodobutane英国石油(bp): 201 - 201 - 'c (88 - 89 - 'c毫米汞柱)
1,4-Diodobutane英国石油(bp): 261 - 267 - 'c (147 - 152 - 'c / 26毫米汞柱)
辛烷英国石油(bp): 125 - 127 - 'c
1-Fluorooctane: 142 - 146 - 'c
1-chlorooctane bp: 183 'c
1-bromooctane bp: 201 'c
氯将如何影响烷基链的沸点为例1-chloro-octane比较辛烷?
和1-bromo-octane吗?
和1-bromo-8-chloro-octane吗?
谢谢,这是超级有帮助! ! !
很高兴你有帮助!
好,非常感谢你的宽宏大量,没有坚持一份工作。社会可能希望在一个更大的比你早一点选择…亲爱的教授James一件事,当我们讨论沸点时,我不得不说,等因素sterically hinderedness分子来场景或者我们不得忽视的影响。
让你知道我是在大学做助理教授,印度。张开双臂欢迎你和你的页面。
谢谢…你…非常可以理解。
非常感谢…
我想知道,如何在结晶物质含水量影响它的熔点。这个问题背后的主要原因是,合成苯甲酸后,发现其熔点高,我不得不给某些错误,增加%。验证水是存在于固体晶体,如果我能证明熔点高于预期由于存在水,产量增加%的错误将是合理的
水通常会导致抑郁的熔点,不提高。
为什么反式2 -丁烯但具有较高的熔点、沸点比顺式2 -丁烯低吗?这是由于偶极矩吗?
嘿,只是想阻止,说我是多么欣赏这网站。你有一个特殊能力呈现材料简洁,时尚可以理解的。我希望你是我的有机化学书的作者或我的教授,因为今年我已经自己有机化学教学使用你的网站和我的课本(讲师是可怕的)和接收在ochem + 1。谢谢你!
嘿,RJ,谢谢你commment,我欣赏你停止这么说。詹姆斯
为什么NO2沸点比二氧化硫吗?都是极取向作用,但二氧化硫有一个更大的偶极矩,更大的摩尔质量,和更大的表面积。我知道NO2是一个激进的、影响沸点吗?
我理解分支增加M。P但我不完全理解d原因. .
谢谢你!我在我的大学学习化学,这是非常有用的!我通常不喜欢和几乎不能理解化学但这很清楚和容易理解谢谢你:)
很高兴听到吉利安!谢谢你的评论!
我有一个小问题在理解熔点趋势……为什么以下熔点增加不平衡………。甲酸(m。p 8.4)然后乙酸(m。16页)…然后丙酸(m。-21页)……的n pentanoic acid (m.p -35)…………………It seems appropriate to understand boiling point trends which increase with molecular size as van der waals forces incrase but how does melting point trend works?
提前谢谢!
感谢!
我也把Orgo我和遇到一个问题我不明白。鉴于3醇:叔丁基,仲丁基,和正丁基各自沸点测量:82 c, 100 c, 117 c。4个碳,所有他们相同的分子量,同样的分子间作用力吗?其沸点值差异创造了什么?羟基的位置吗?
谢谢你的帮助!
将表面积的关键因素。线性链支化烷基组有更高的比表面积(更多的“球形”)和由于范德华力是成正比的沸点,线性烷基组应该有更高的沸点。
谢谢詹姆斯!非常有帮助。现在我清楚的概念。请保持发布这样的概念。
可读。Hurumph !
伟大的总结,真正reafable。我一直在努力掌握化学作为课程的一部分,我所做的。我发现这是最好的网站,谢谢你把东西从我真正理解!
谢谢杰基!
请告诉我为什么Butan-1-ol的沸点比butan-2-ol吗?
我不能没有留下你的评论。非常感谢:))我目前从事有机化学,这帮助了很多!
确定与左边的沸点最低的顺序:
= (CH3) 3 cch2ch2ch2ch2ch2c (CH3) 3
B = CH3CH2C (CH3) 2 c (CH3) 2 c (CH3) 2 ch2ch3
C = (CH3) 2 chch2c (CH3) 2 C (CH3) 2 ch2ch2ch3
所有三个具有相同数量的碳和相同数量的分支点。的帮助!
这不能解释沸点。
我学习我的DAT和这是一个神奇的审查和帮助…谢谢
太好了。很高兴你找到它有利于DAT尼基!
为什么分支在沸点烷烃低点…?
分支的能力降低分子的堆栈,降低其状态固体和其沸点较低。
如果我们有不同的化合物在milecular重量与巨大的差异
在这种情况下我们会比较两个不同的变量(链长*和*极性官能团),很难预测哪些因素更重要。我会寻找化合物的例子,你是好奇,比较它们的熔点和沸点。
这将有更高的沸点,C6H14或C2H5OH,为什么?
范德墙力意味着一样的偶极子诱导偶极力量?
可能是太迟了。但是没有,不是一样的。Dipole-induced偶极子是描述极性分子之间的引力(偶极子)和一个诱导偶极子(分散、伦敦、范德瓦耳斯)。看而不是一个孤立的力量(如disperson), dipole-induced偶极子是描述两个彼此吸引…暂时的诱导偶极子。
非常感谢你,我一直在寻找一些清晰和易于理解的趋势沸点这回答我这么多的问题!保持出色的工作。
我们只可以比较的分子大小和分子形状相似的分子或我们可以比较分子的大小和形状不同的官能团?例如我可以比较的大小和形状和庚烷戊酸吗?
这是很难比较两个变量(链长和官能团)。一般来说你只是想知道每个变量的影响。
你好感谢信息帮助很大,但我有一个问题。它关注有机化合物。说你有一个酮庚酮等。所以这种化合物的沸点应该相对较高,因为它有一个很大的表面积,这是一个极性分子偶极偶极有力量。现在的酒精丙醇等短链。酒精应该有一个更高的沸点,因为它有一个hygrogen债券。但丙醇分子更短链小表面积比庚酮。所以我们怎么能有更高的沸点哪一个?(在本例中庚酮沸点高于丙醇但我想解释为什么)。
嗨李尔,很难比较两个变量,因为它是很难衡量每个变量的相对重要性从第一原理(这就是实验)。例子中提到的,比较庚酮和丙醇是困难的,因为我们比较两个变量:链长度和极性官能团。从本文的关键结论是,如果所有变量除了一个是相同的,基于这些概念可以预测沸点。你会发现,考试通常会测试一个变量。
如果我们有一个分子氢键和烷烃。如果烷烃分子量大于氢键,而在沸点最高?
我不明白为什么辛烷比chloropentane BP更高。
你比较两个不同的变量;链长(8个碳和5个碳)和极性(氯是电负性)。很难预测沸点是如何当你改变多个变量的影响。
为什么亚兰的沸点比甲烷? ?(CH4 H更多债券)
高分子量是一回事。碳氢键不算作“氢键,因为碳不够电负性。地,h和F-H债券参与氢键。
这是很深刻的,但是我有一个问题我有一个问题比较戊烷和乙醚。基于的信息我已经看到它看起来像戊烷的沸点高于di-ethyl醚、基于实际英国石油公司,但你的信息告诉我,应该是另有乙醚取向作用,戊烷范德瓦尔部队。你能帮我清理的实际应该更高的BP和给答案的原因吗?
好点!我没有一个好的答案为什么戊烷的BP(36摄氏度)高于Et2O(34.5摄氏度)。有趣的是四氢呋喃的沸点(C4H8O)是66摄氏度,因为戒指给了它一个永久偶极矩。
戊烷具有较高的英国石油公司由于没有更多。C原子。
但丁烷bp低于乙醚由于你提到的原因
这个表我死记硬背OAT,帮助很多!谢谢!
这是一个神奇的引用可以简化属性影响沸点,可令人困惑的时候可以发挥作用的许多因素! !它更好的工作比我的教授,这本书真的很好,或者能够在阐明上述所有。感谢谁了! !
更多的例子!学生们会参考他们的做法。好网站!
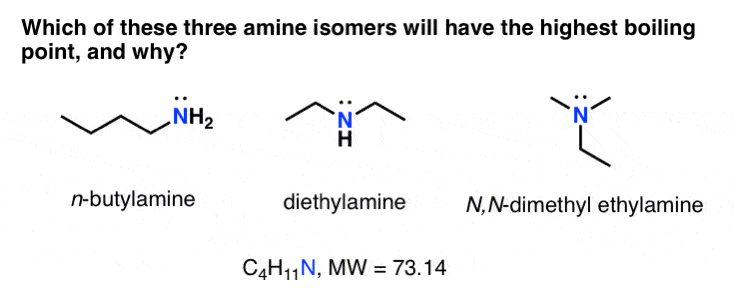
n-Butylamine >二乙胺> N, N-Dimethyl乙胺
有人能帮我这些物质的沸点,(比较)
甲基氨基,CH2 F2, CH3哦,CH3 CH2 CH2甲基
Ch3ch2ch2ch3 > ch2f2 > ch3oh > ch3nh2
烃(烷烃)沸腾pt温醇相比少了
谢谢。这篇文章很有教育意义的。
(1)为什么丁醇(bp - 117)有更高的沸点比butanamine (bp - 77.8)
(2)分子内氢键如何影响的沸点有机分子
好问题。很可能由于氮氧的电负性大(3.4)和(3.0)导致更大的偶极子,这意味着分子将有一个更大的力量把他们在一起。
谢谢,我发现我的问题的答案。一件事,,官能团如何影响沸点在大多数可以理解吗?谢谢
如果你专注于一件事,我寻找氢键等团体哦和北半球。这将显著提高沸点。
创化学1罪恶之城。这个网站真的很有帮助。这就像用一个更好的球员打网球;你只能从专业学习和获得更好的如果你想!谢谢!伟大的东西
回答问题:将最高沸点胺的氨基(最氢键)其次是NH然后右最远的分子。
这帮助我很多理解。我访问了很多网站,但是它是最有用的1…谢谢
很高兴你sumaiya发现它有用。
分支是如何影响熔点吗?
我得到分支减少英国石油公司由于表面积减少,因此减少范德瓦尔斯相互作用的机会。然而,对熔点它是如何工作的?当它是支很难堆栈,对吧?那么,熔点较低?
谢谢!:)
我认为分支导致更低的熔点,对于你提到的原因。
分支实际上增加的熔点分子,因为它减少表面积使其变得更加紧密。
然而,它降低了BP因为少Van de Waal能够发生的交互。
但国会议员的异丁烷小于丁烷。我在维基百科上搜索它
我有一个问题你指出本文的分支规则。不会增加分支的沸点会导致分子的形状被更多的球形和紧密。与紧密的分子,所以需要更多的能量把它分开因此,分支b.p应该增加。
更紧密会给它一个更高的熔点。但减少表面积会导致较低的沸点由于范德华相互作用降低。
你如何比较、议员和英国石油(bp)在同一分子,? ? ? ? ? ?议员给出4固体,bp 4液体……
我认为这是一个概念性的问题,,,b。p不意味着吸引,,,或者包装的分子,其物理性质,,,因此取决于交互b / w的分子化合物,,,现在,,,因为它在本质上是球形的,因此,接触面积减少,,,,,,因此,交互变得较弱,因此b。p降低………………
例如——我们有一杯水,,r有许多水,分子,,,在这里我们r abt不是,,,h-o债券,其abt b / w 2水分子的交互,,,,,,,窟我们通常说,分子间作用力………
希望你现在,清楚你的概念…………
1。离子键不是一个分子间作用力;它是一个分子内力吗?网络共价、离子、金属…无机化合物!
2。有一些被称为旋光异构。R和S对映体的mp和外消旋体的议员是不同的;重要的事情如果你掌握有机化学。
为什么不能是吗?我想主要是盐的有机化合物像Me4N + Cl -有很高的熔点与网络固体氯化钠或其他无机化合物并不是真正的“分子”本身。
谢谢你提到R / S,这是一个很重要的问题!
谢谢你!我在大学学习化学,这帮助了很多! !
谢谢,很高兴你发现它有用。
有人能帮我吗?比较boilnig点
NH3 b)过氧化氢c)水
CH4) CF4 b)亚兰c)
二氧化硅)水b)硫化氢c)
b > a > c
b > a > c
c > b > a
Shubham,我猜h20 bp高于氨。其他都是正确的。
硫化氢沸点比水要低得多。硫化氢不能形成氢键。
这取决于h-bonding不是力量nh3的程度可以形成3 h债券而水只能形成2
Utkarsh,我相信氨bp小于水…
1-H2O2。2-ccl4。3-h2o。
谢谢你!这也帮了我很多!