醇、环氧化合物和醚
消除反应的醇
最后更新:2022年11月9日|
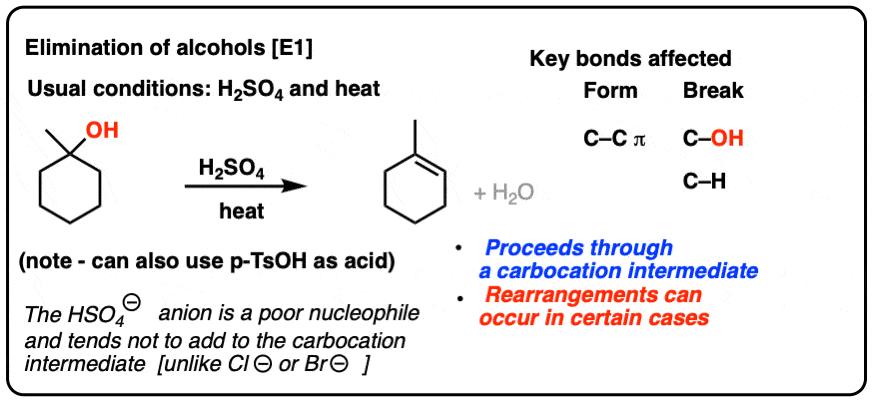
关于消除反应的醇(酸)
- 醇的羟基通常是贫穷离去基团。
- 然而,当处理强酸,R-OH转化成R-OH2(+)和H2O是一个更好的离去基团。
- 叔醇,H2O可以离开,导致碳正离子。
- 如果一个H等强酸2所以4或使用p-TsOH,最可能的结果消除,因为这些酸的共轭基地(HSO汽车贸易公司4- - - - - -和TsO- - - - - -)很穷的亲核试剂,可能增加碳正离子。
表的内容
- Hydrohalic酸(HX) +醇给替代产品…
- …但H2所以4,有H3PO4 TsOH给消除产品!
- 消除叔醇通过E1机制
- 为什么硫酸、H3PO4 TsOH给消除产品吗?
- 二级醇呢?
- 消除与碳正离子重排反应
- 其次是消除环扩张
- 主要的醇类和硫酸可以形成烯烃(通过E2)
- 摘要:消除反应的醇
- (高级)引用和进一步阅读
1。Hydrohalic酸(HX) +醇给替代产品…
之前(看到帖子:卤代烃与醇我们看到治疗酒精具有强大hydrohalic酸盐酸——认为,哈佛商业评论,或者嗨——导致的形成烷基卤化物。有三级酒精画的下面,这通过一个年代N1机制。质子化作用的酒精,那么H的损失2O形成碳正离子,然后攻击的亲核试剂碳正离子)。
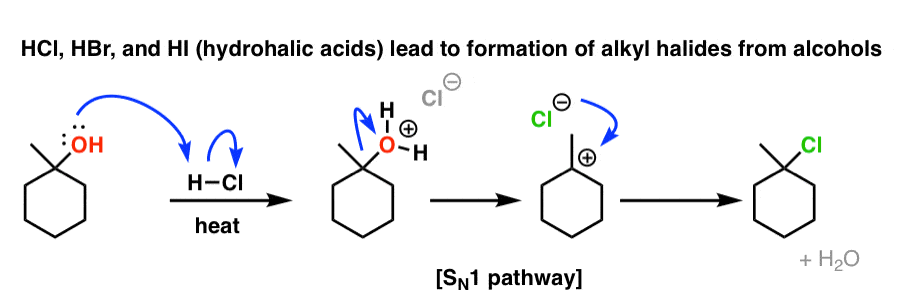
2。…但H2所以4H3阿宝4,TsOH给消除产品!
你情有可原,如果我们一个治疗酒精与H2所以4(硫酸)同样的事情会发生,和碳正离子会攻击(-)OSO3H阴离子使下面的产品。很合理的建议。然而在实践中,它不工作!
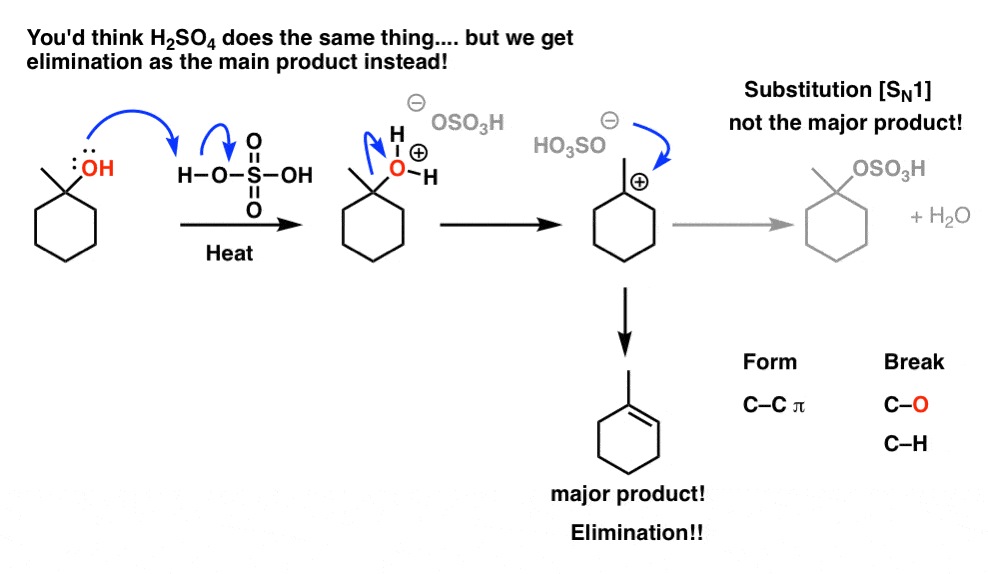
这里发生了什么?
首先,看什么债券形成和爆发。我们形成碳碳(π),c和碳氢键。(我们也形成H-O,水分子形成的副产品)。这是一个的模式消除的反应。
现在让我们问:如何这形成了吗?如果你仔细看,请注意,我们已经打破了碳氢键相邻碳正离子和形成新的碳碳π键的位置。是合理的建议,而不是攻击碳正离子形成新的替代产品,基地移除一个质子邻碳正离子和形成了烯烃。(碳相邻的碳正离子通常被称为“β(β)碳”。碳正离子本身是“α(阿尔法)碳”)。
3所示。消除叔醇通过E1机制
实际上我们已经见过这种类型的过程!这是一个E1的过程[消除(E),单分子(1)速率决定步骤)。您可能还记得,消除反应倾向于遵循”扎伊采夫规则”——我们总是最替代形式烯烃(或换句话说,我们把一个质子从碳附带最少的氢)因为烯烃稳定增加附加的碳的数量增加。
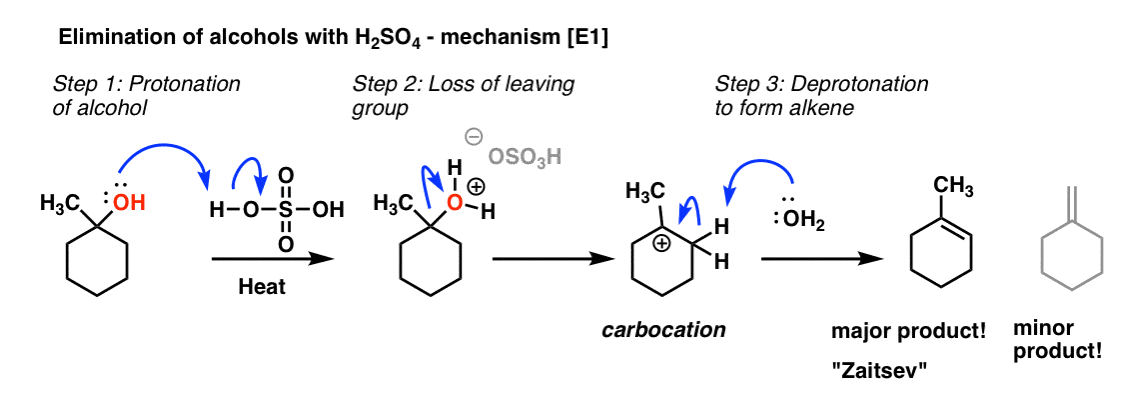
(顺便说下,你可能会问——为什么“热”?热一般倾向于支持消除反应。]
绝不是H2所以4做这件事的唯一的酸。磷酸(H3阿宝4)以及“除了酸”(p-toluenesulfonic酸)也倾向于消除产品形式。
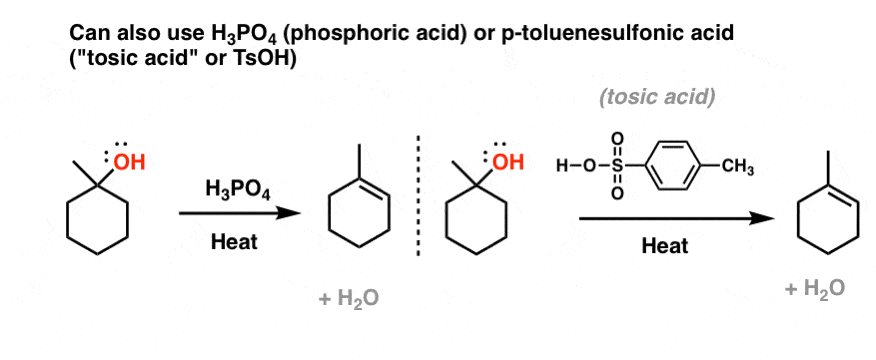
4所示。为什么H2所以4(或H3阿宝4或TsOH)给消除产品但HCl,哈佛商业评论,你好给替代产品吗?
为什么我们得到消除反应与H2所以4酸(或H3阿宝4或TsOH)而得到替换与盐酸反应,哈佛商业评论,和你好吗?
答案是,HSO汽车贸易公司的4-阴离子是非常可怜的亲核试剂,被共振相当稳定。在下面的图中,注意,负电荷的离域在三个不同的氧(TsO也是如此- - - - - -和H2阿宝4- - - - - -阴离子)。
相比之下,卤化物离子,负电荷不能分布在多个原子。其结果是,移位HSO汽车贸易公司选择的慢反应的结果4——作为一个亲核试剂相比去质子化碳氢键的基础,烯烃产品占主导地位。
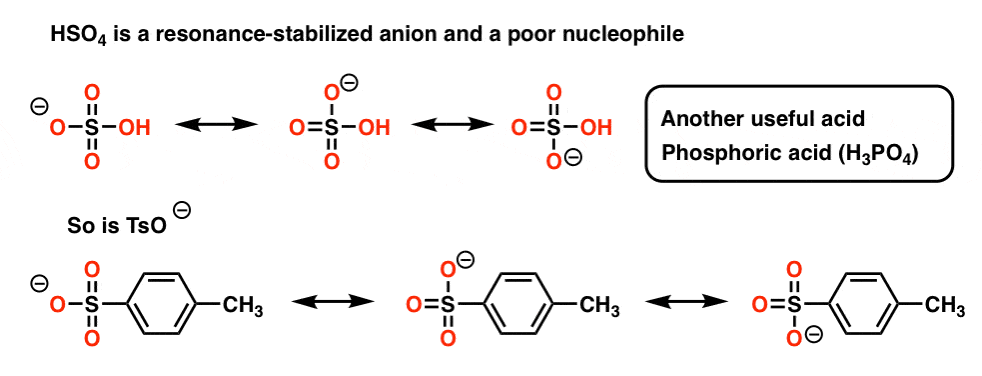
这里的底线是,加热叔醇与这些酸会导致损失的水(“脱水”)和形成的烯烃(消除)。
5。消除二级醇的反应呢?
加热二次酒精与硫酸或磷酸吗?相同的交易与三级醇:预计烯烃形成。正如所有消除反应,有两点要注意:第一,“大多数”代替烯烃(扎伊采夫)将占主导地位的产品,而且,别忘了反式烯烃将支持(更稳定)比独联体烯烃由于更少的空间应变。
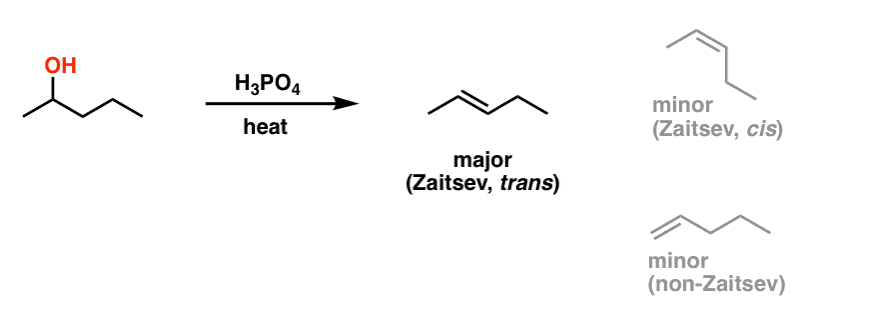
还有最后一件事要注意二级醇,虽然…就像一个糟糕的噩梦,他们回来了。
6。消除与碳正离子重排反应
我们看到与盐酸的反应,哈佛商业评论,嗨二级醇,我们必须小心碳正离子重排反应。如果能建立一个更稳定的碳正离子通过迁移的氢化邻(H)或一个烷基组,然后迁移将发生。
例如,治疗的酒精下面与H2所以4导致形成二次碳正离子,其次是氢化物转移给一个叔碳正离子,紧随其后的是去质子化哪个β碳导致最代替烯烃。
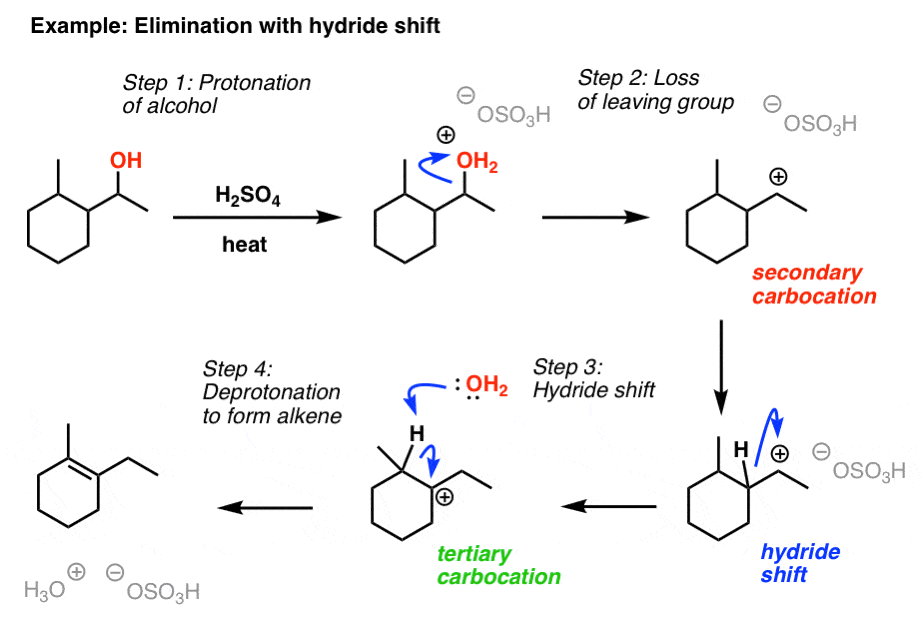
7所示。其次是消除环扩张
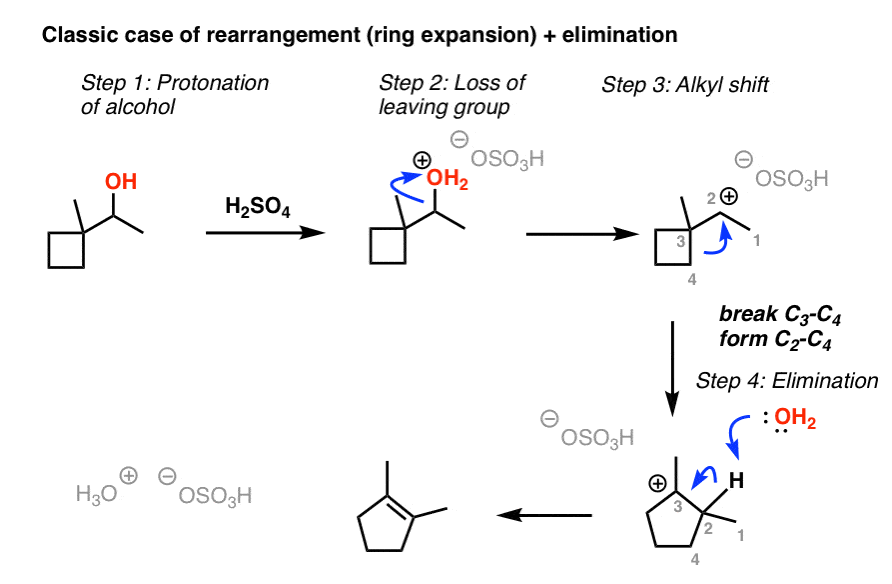
也有可能烷基发生转移给一个更稳定的碳正离子。紧张的一个经典例子是扩张环(如环丁烷)给少紧张环(如环戊烷)。
例如在下面的情况下的关键一步是同样的键断裂形成C2-C4键,导致一个新的(三级)碳正离子颈- 3以及不那么紧张的戒指。因为没有一个好的亲核试剂,消除发生在这样一个方式大多数代替烯烃就形成了。
8。主要醇类和H2所以4可以形成烯烃(E2)
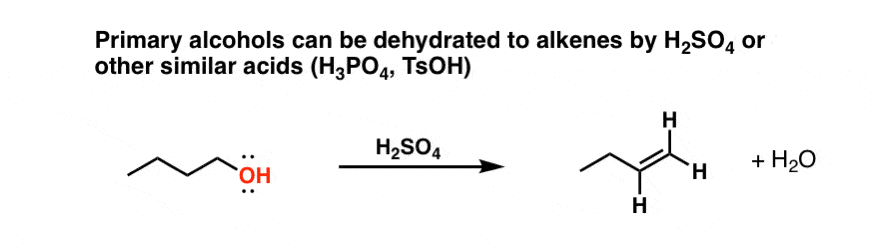
最后的一类醇关心是主要的醇。你可能会问:如果我们治疗伯醇(比如1-butanol)与强酸(如H2所以4,也会得到消除烯烃吗?
是的,烯烃这样就可以形成(连同一些形成对称醚(看到以前的文章])。这是一个例子。
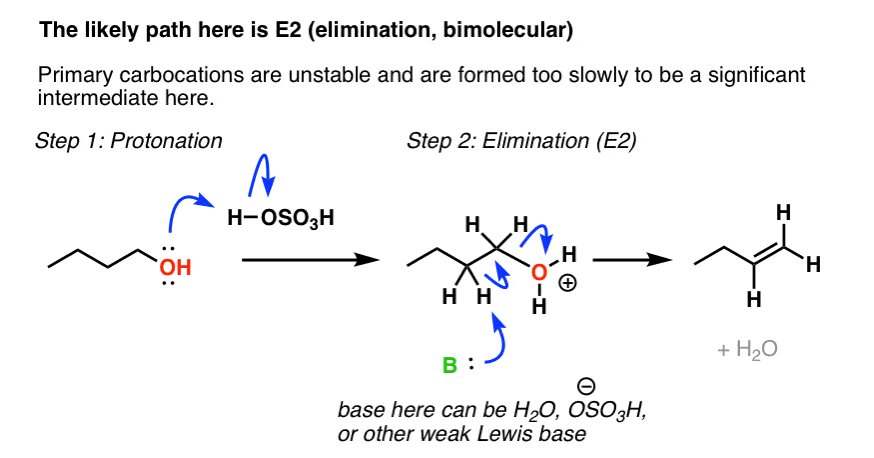
不过有一个条件:E1通路(主要形成碳正离子)不是最可能的路径。主要碳正离子往往是极不稳定的,更有可能通过一个反应E2机制的过渡态的能量会降低。注意这里发生了什么:首先我们使质子化酒精给好离去基团哦2+,然后弱碱(我离开模糊,但可能是H2啊,(-)OSO3H,或另一个分子酒精)可以打破碳氢键,导致形成的烯烃。
9。摘要:消除反应的醇(E1)
如果你看到一个三级二次酒精与H2所以4、TsOH或H3阿宝4(和特别是如果你看到“热”)认为:碳正离子形成紧随其后消去反应(E1)。
如果你看到一个更稳定的碳正离子可以通过迁移形成一个相邻H或烷基组,预计这种情况发生。
如果你看到一个主酒精与H2所以4、TsOH或H3阿宝4,预计对称醚形成伴随着消除形成烯烃。
下次…
到目前为止,我们已经学习了两种方式将醇烯烃:
- 将它们转换为好离去基团,然后添加基础步骤(2)
- 添加强酸与热(一步)
理想情况下,我们想用一个步骤。但强酸可以导致并发症(碳正离子重排、咳嗽咳嗽),我们可能会问:“没有一种更简单的方法”?
有!这是我们下一篇文章将介绍。
在下一篇文章:消除醇与POCl烯烃3
笔记
(高级)引用和进一步阅读
各种条件可能这个变换(酒精- >烯烃),所有这些涉及转换-哦更好离去基团。使用酸是最简单的方法来实现这一目标,的质子化作用-哦-哦2+,一个优秀的离去基团(水)。
消除与POCl3:
- 结构的影响的过程中磷酰氯-吡啶叔醇的脱水
罗纳德·r·萨奥尔
美国化学学会杂志》上1959年81年(18),4873 - 4876
DOI:1021 / ja01527a028 - 磷酰氯脱水的定向性和regiospecificity甾醇侧链醇
Jose Luis杜松子酒、基督教玛戈特和卡尔Djerassi
《有机化学》杂志上1989年54(2),369 - 373
DOI:1021 / jo00263a020
本文由传奇化学家卡尔Djerassi(发达炔诺酮,第一位女性避孕)描述POCl的选择性3- - - - - -吡啶脱水条件合成类固醇。它也有一个POCl一般程序3- - - - - -吡啶在实验段脱水。 - 一般线性方法融合triquinane自然产品。总合成(+ -)。-hirsutene, (+ -) -coriolin, (+ -)。-capnellene
Goverdhan梅赫塔斯瓦米。没吃,d . Sivakumar。Reddy,维拉。Reddy
美国化学学会杂志》上1986年108年(12),3443 - 3452
DOI:1021 / ja00272a046
本文通过教授Goverdhan梅塔(被认为是“印度e·j·科里”)演示了POCl的适用性3- - - - - -吡啶脱水在天然产物全合成。 - 3-methylcholestanols及其衍生品
d·h·r·巴顿a da s Campos-Neves和r . c . Cookson
j .化学。Soc。1956年,3500 - 3506
DOI:10.1039 / JR9560003500
本文由诺贝尔奖得主教授德里克·h·r·巴顿POCl3 -吡啶脱水(见p。3504 - 3505年在实验部分)。使用Brønsted酸: - 丁烯混合物的成分造成正常丁基醇的催化分解
威廉·g .年轻和霍华德·j·卢卡斯
美国化学学会杂志》上1930年,52(5),1964 - 1970
DOI:1021 / ja01368a030
虽然这似乎是一件容易的事情今天,研究核磁共振和gc - ms,在早期这并不是那么容易。丁烯转化为二,蒸馏,然后分析的二溴化三分量的混合密度、折射率、二阶速率常数与碘化钾的测定丙酮。比尔年轻和h·j·卢卡斯化学在南加州的发展作出了重大贡献——h·j·卢卡斯是一个加州理工学院的化学教授,和比尔年轻后来成为加州大学洛杉矶分校的化学教授和顾问扫罗Winstein教授的化学硕士(Winstein最终教授博士学位后加入加州大学洛杉矶分校的比尔年轻!)。 - 二、三级醇的脱水
阿尔伯特·l·Henne和阿尔弗雷德·h·Matuszak
美国化学学会杂志》上1944年,66年(10)1649 - 1652
DOI:1021 / ja01238a012
早期的纸了E1这个反应的性质,通过展示各种二级和三级醇的脱水给产品通过重排。 - 示踪剂研究醇。第二部分。氧18 sec.-butyl之间的交换酒精和水
c . a .横梁和d·r·卢埃林
j .化学。Soc。1957年,3402 - 3407
DOI:10.1039 / JR9570003402
本文提供了实验证据,更强的酸有利于消除在替换。哈米特酸度(-H0)中增加,形成碳正离子是越来越有利,促进消除在替换。硫酸酸和高氯酸强于氢酸(盐酸,哈佛商业评论,你好),这也解释了为什么硫酸是常用的烯烃从醇。 - 在稀酸反应n-butene和butan-2-ol。机制和中间的说明在消除二级醇的水合作用烯烃
Joost扫和弗里茨·s·克莱恩
j .化学。Soc。1960年,4203 - 4213
DOI:10.1039 / JR9600004203
作者用放射性标记研究的正向和反向反应(水化烯烃和消除酒精),以证明他们都通过一个共同的碳正离子中间体。 - 1的催化脱水的机理,2-diphenylethanol
唐纳德·s·诺伊斯,唐纳德·r·哈特和拉尔夫·m·波拉克
美国化学学会杂志》上1968年,90年(14),3791 - 3794
DOI:1021 / ja01016a034
有趣的是,在1的反应,2-diphenylethanol酸,中间形成碳正离子是快速、可逆的,和质子的损失烯烃速度决定。 - 取代基的影响1的催化脱水率,2-diarylethanols
唐纳德·s·诺伊斯,唐纳德·r·哈特和弗兰克b英里
美国化学学会杂志》上1968年,90年(14),3794 - 3796
DOI:1021 / ja01016a035
在这个反应,替换上的影响苯基环-哦是比替换的戒指。 - 可调,催化一步铋(III) Triflate与醇类反应:脱水和二聚作用
劳拉·e·Kolsi Jari Yli-Kauhaluoma,瓦尼亚Moreira
ACSω2018年,3(8),8836 - 8842
DOI:1021 / acsomega.8b01401
这个反应的现代变体使用路易斯酸。作者也表明,这些条件可以用于形成二聚体和简单的淘汰产品。二聚体形成的碳正离子反应烯烃。
你好詹姆斯,如果我有任何疑问在有机化学中,我观察到你的工作。我需要知道,主要的醇在酸催化消除产生任何重新安排产品。在这个网页(http://www.columbia.edu/itc/chemistry/c3045/client_edit/ppt/PDF/05_08_13.pdf),Butan-1-ol给2-butene作为主要的产品。在韦德小课本1-pentanol 2-pentene作为主要产品生产。
之间的替换和消除反应醇与酸或碱催化哪一个?
酸使哦更好的离去基团,自从新离去基团将较弱的基础水,不是HO (-)。
基地使哦更好的亲核试剂,由于RO(-)是一个亲核试剂比中性酒精卢武铉。
替换和消除反应可以催化醇酸。
你好。你介意告诉我酒精和Me2C机制(当地)2和p-TsOH(催化剂)?谢谢提前
这是一种形成一个循环从二醇醋酸酯。https://en.wikipedia.org/wiki/Acetonide
有将一个二醇转化为烯烃从上面提到的方法吗?
不是在一个步骤。有必要做一个减少一些。
然而,有一个反应称为Corey-Winter反应,降低烯烃二醇。https://en.wikipedia.org/wiki/Corey%E2%80%93Winter_olefin_synthesis
嗨,詹姆斯。只是想知道硝酸会导致同样的反应发生在硫酸或H3PO4 (E1 rxn) ?
快速回答:是的。
再答:是的,但是这取决于硝酸的浓度和类型的酒精。稀硝酸溶液本身的可能就行。浓硝酸包含一些NO2 +这是一个优秀的亲电试剂,酒精会增加,导致R-ONO2。如果酒精是主要或次要酒精,这可以氧化醛或酮,或开始。叔醇不氧化。
醇类的另一个问题:你听说过硝化甘油?这是由添加硝酸(以及一些硫酸)tri-ol甘油,导致潜在的爆炸性的效果。
因此我们通常只是坚持硫酸或H3PO4 !
詹姆斯
热稳定性与迁移能力:
我有这个疑问。不能找到一个解决方案。请帮助
消除2-methyl-2-phenylpropan-1-ol的产物是什么?
迁移的Ph值——比R更快,但将导致不稳定中间,反之亦然。
动力学和热力学控制的一个例子吗?
更合适的答案是什么?
这将是一个例子anchimeric援助(相邻组参与)。质子化作用后哦,苯基作为内部亲核试剂,导致桥中间。攻击的水桥中间给2-methyl-1-phenyl-2-ol,然后经历一个正常脱水给2-methyl-1-phenyl-1-propene
在什么情况下发生重排吗?当一个更稳定的碳正离子形成或有其他标准吗?
醇进行E2反应吗?因为它需要去质子化创建一个更好的离去基团,我认为不是但我不确定。
不是传统的E2反应。去质子化的羟基会使产生的物种(O)的离去基团甚至更糟!
关于第四张照片(消除醇硫酸-机制(E1)),为什么水deprotonate碳正离子在步骤3中?如果千瓦= 1.0 x 10 ^ -14然后不该H3O +的形成非常不利吗?
在最后一个例子,E2与伯醇反应,为什么2-butene(更稳定的烯烃)不是由1-butanol吗?
因为为了消除发生,碳氢键上打破旁边的碳碳轴承离去基团。离去基团在C1, C2 CH债券必须打破,C1和C2之间和债券形式,给1-butene。
只是想谢谢这清晰的解释。我很困惑为什么硫酸只是解释为形成E1 E2产品但不是SN1 SN2。不能在任何地方找到答案,直到我无意中发现了这个页面。
为什么我们使用硫酸的醇反应哈佛商业评论和我们使用H3PO4醇反应的嗨。为什么
他们应该是等价的。
如果你使用两个顺式或反式推论的哦?
很有可能你会得到一些环氧化物的形成,甚至形成酮/醛。取决于基质的结构。
当乙醇加热在140 * C在浓缩的面前。硫酸。这是一个β-消除反应吗? ?
可能形成的乙醚。
我认为二级醇可以接受E1和E2反应。在你的文章,你认为二级醇更喜欢E1机制。是真的只有一个仲碳可以重新排列给叔?是安全的说,否则,二级醇可以接受E1和E2 ?
酸的身份是很重要的。在硫酸的情况下或有H3PO4没有足够强碱发生导致E2反应。损失的水形成碳正离子其次是消除将支持途径。
注意,二卤代烃可以接受E2反应很好。醇的问题是,我们用强酸将哦,变成一个好的离去基团。如果我们增加一个强碱(执行E2),它只会最终中和这个物种。
重排而言,它通常只会青睐的处境更稳定的碳正离子会形成。这是正确的为二级碳正离子叔碳正离子的转换。事实* *可以重组叔碳正离子的发生,但通常只在他们的情况下会更稳定(如叔碳正离子共轭叔碳上)
对不起,我把我的电子邮件错误,再次发布我的问题。
为什么不是主要的SN2反应质子化作用后醇吗? ? ?水是一个很好的离去基团和初级碳不是阻碍,一个完美的SN2的秘方。就是HSO4——可以通过SN2攻击,为什么不呢?为什么取消?鉴于就是HSO4——每周基地。
就是HSO4——是一个非常可怜的SN2亲核试剂。
加上有热量参与反应的. .这是有利于消除反应…感谢u n随时纠正如果错了吗
感谢你的这些信息,但我有一个小问题…有消除和脱水的区别吗? ?
脱水具体是指水的损失。消除的这篇文章是指一个双键的形成。之间有重叠两个当脱水导致形成双键。
几天前我发了一条信息,但是这是抹去。这是再一次的:
——“…我们删除一个质子从碳附带最氢”;这是碳附带最少的氢!
-请检查酸的公式及其相应的阴离子在文本;一些看起来像这样:“硫酸酸(或H3PO4”(他们都写正确的图像)。
不知道为什么,没有文章发表评论。谢谢你的敏锐的眼睛,一如既往!