醛和酮
格氏试剂对醛和酮
最后更新:2022年12月1日|
格氏试剂:他们的形成、反应和反应机制

今天的试剂是大多数学生有经验在某一点或另一个。格利雅试剂是由金属镁的反应与烷基或烯基卤化物。他们非常好的的亲核试剂,与亲电试剂反应,如羰基化合物(醛、酮、酯类、二氧化碳等)和环氧化合物。他们也非常强大的基地,并将与酸性氢反应(如醇、水和羧酸)。
类似或相同:非常类似于organolithium试剂。
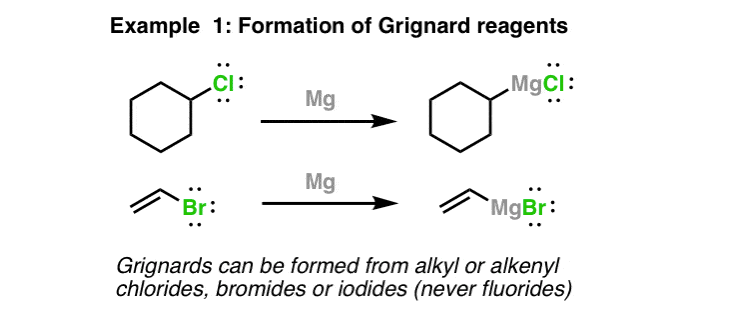
格氏试剂的形成
格氏试剂是由通过增加镁金属的烷基或烯基卤化物。卤可以Cl, Br,或者我(不是F)。这有点容易格氏碘化和陈词滥调,然而。注意这里发生了什么——镁碳之间的“插入”本身和卤化物。这卤“X”指当我们将格氏试剂称为“RMgX”。
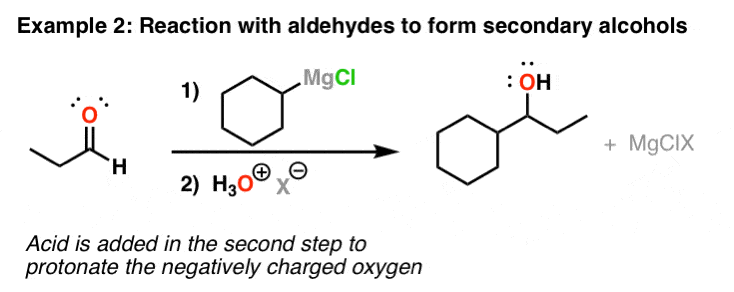
格氏试剂与醛的反应给二级醇
格氏试剂的最常见的用途之一是在醇与醛和酮的反应形式。在第一步中,格氏形成碳碳键。这导致一个醇盐(酒精)的共轭碱。形成了酒精,有必要增加酸的反应(所谓的“检查”步骤)。这是这里显示为“H3O +”(“X”只是抗衡离子,观众在这里)
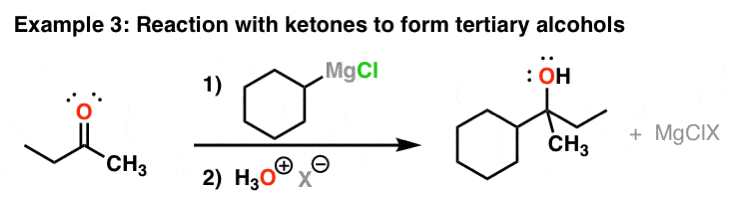
格氏试剂与酮的反应给叔醇
反应行为类似于针对酮。再一次,没有什么特殊的Cl -这一切都取决于你如何使格氏放在第一位。
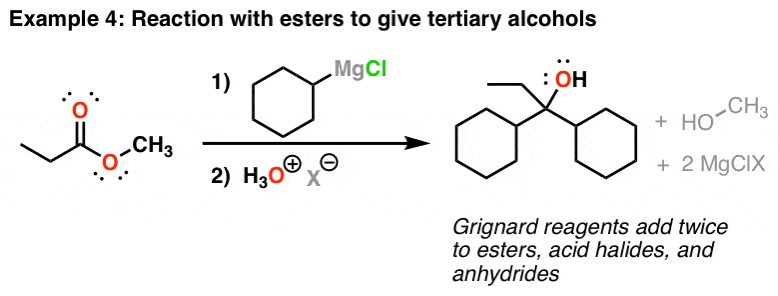
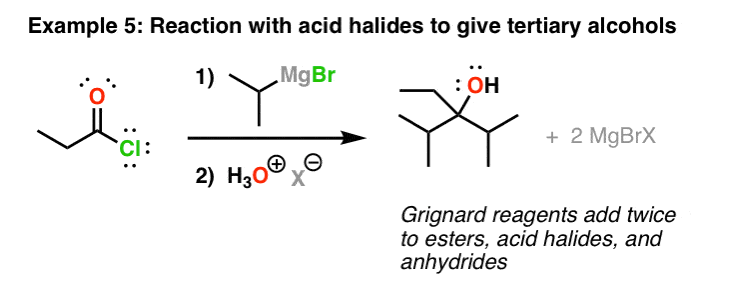
格里纳加酸酯和卤化物的两倍
格氏试剂也将增加酯。是什么让这些反应更复杂的是,他们添加两次。最终结果(后添加酸)是一个叔醇。这也是酸的卤化物(酰卤化物)和酐。一个值得注意的例外是羧酸(下图)。
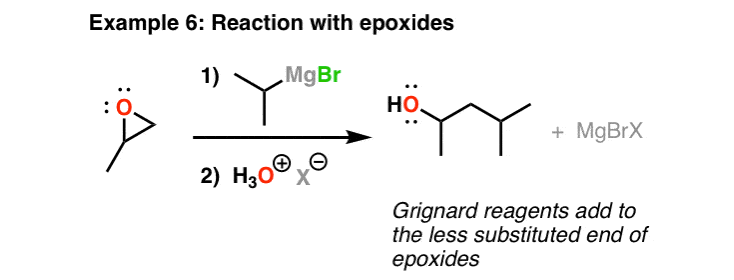
格氏试剂与环氧化合物
另一个重要的格氏试剂的反应是,他们将添加到环氧化合物形成碳碳键。一件事要记住的是,现在的趋势是增加了少替换的环氧—也就是说,位阻越小。你可以把这个反应本质上是类似的SN2反应。加酸后,酒精。
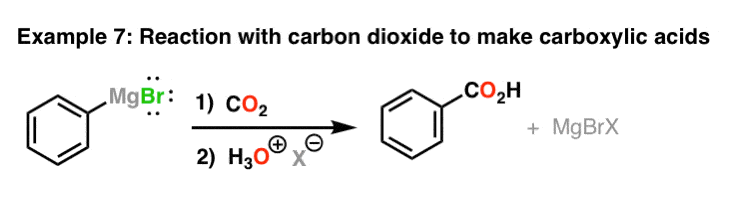
格氏试剂与二氧化碳的反应给羧酸
格氏试剂也增加二氧化碳(CO2)生成的羧酸盐,在一个类似于他们的反应与酮和醛的反应。后的羧化物转换为羧酸的酸(如我们的可靠的水蒸汽(+))。
格氏试剂是强大的基地——质子化作用(含重氢)
最后,由于格氏试剂本质上是烷烃的共轭基地,他们也极强的基地。这意味着有时酸碱反应可以与他们的亲核加成反应。一个常见的情况这个作物是当格氏试剂添加到羧酸。人们很容易忘记这一点羧酸…是酸的。这意味着,而不是添加羰基,他们与质子反应并形成羧酸盐的盐。
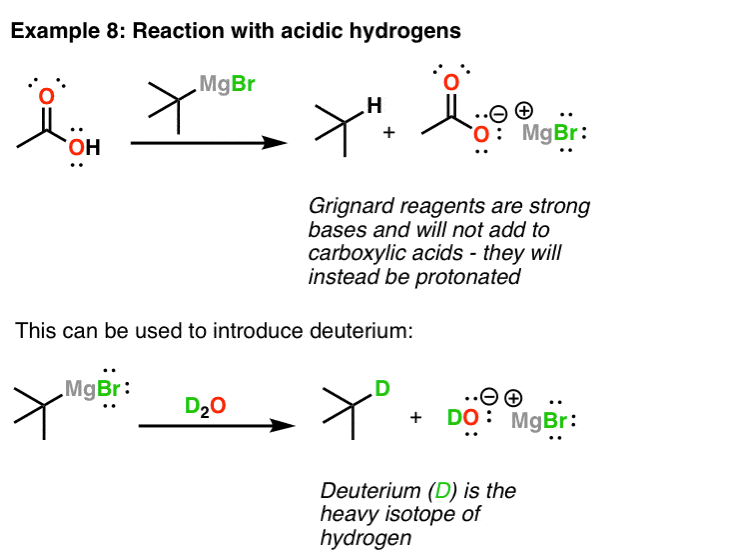
这也可以用于卤代烃转化为烷烃。首先你把它与镁,然后你把格氏强酸。这给你烷烃。您还可以使用该分子中引入氘(D) !第一步是让格氏试剂。第二个是治疗,格氏氘D2O等酸。这给你氘烷烃!
机制:格氏试剂对醛和酮
那么它是如何工作的呢?格氏试剂的关键其实是非常简单的。当你想到的相对电负性碳(2.5)和(1.1),镁碳和镁之间的债券极化对碳。这意味着碳比镁和电子丰富亲核!这是一个仔细的核查。
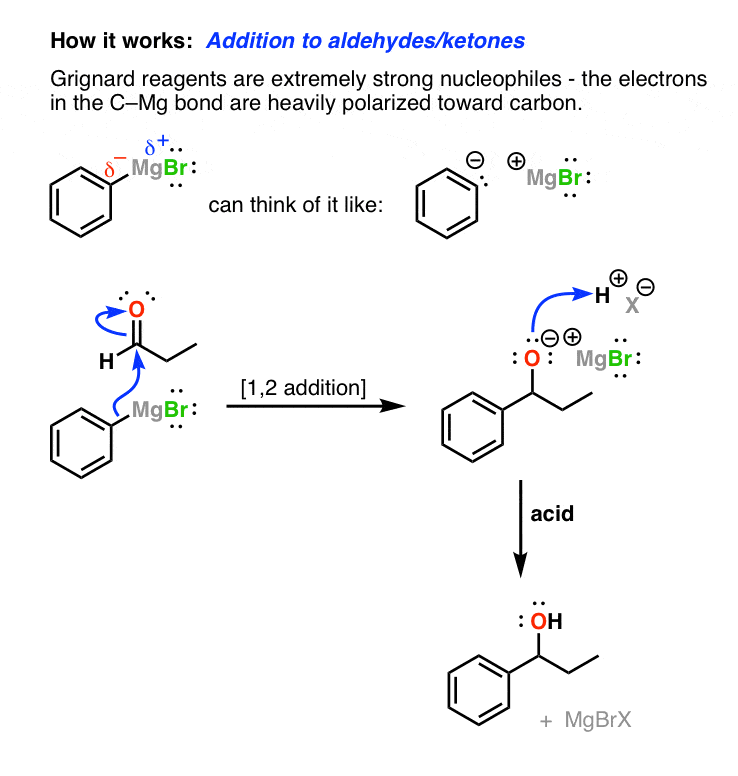
与醛类格氏反应,碳攻击羰基碳和执行一个1,加法,以醇盐。在第二步中,酸添加到给你酒。
(高级)引用和进一步阅读
- 格里纳,v . C。学会科学。1900年,130年,1322 - 1324
维克多格氏的原始论文描述一个酒精从碳氢化合物合成的新方法。 - 维克多格氏和保罗Sabatier:两个展示诺贝尔化学奖的得主
亨利·b·卡根
化学。Int。。2012年,51,2 - 9
DOI:10.1002 / anie.201201849
对于那些感兴趣的历史科学,这是一个历史的角度对维克多格氏和保罗的生活Sabatier,并提供洞察他们的生活,他们如何重要的发现,以及他们的工作的影响等。 - 机械活化制备活性镁切屑的格氏试剂
凯伦·贝克诉约翰•m•布朗,a . Jerome Skarnulis奈杰尔•休斯和安妮塞克斯顿
《有机化学》杂志上1991年56(2),698 - 703
DOI:10.1021 / jo00002a039
有时格氏试剂使用镁金属的形成可能是一个挑战,和激活金属表面的各种方法被开发出来,包括机械活化dry-stirring Mg切屑在惰性气氛下几个小时。
以下3篇论文机械研究格氏试剂的形成: - 格氏试剂的形成机制:捕获和Tetramethylpiperidine-N-oxyl烷基自由基中间体的反应
凯伦根,克雷格·l·希尔,Lynette m·劳伦斯和乔治·m·怀特赛兹教授
美国化学学会杂志》上1989年111年(14),5405 - 5412
DOI:10.1021 / ja00196a053 - 格氏试剂的形成机制。表面反应的性质
m . Walborsky Janusz Rachon
美国化学学会杂志》上1989年111年(5),1896 - 1897
DOI:10.1021 / ja00187a063 - 格氏试剂的形成机制。维模型计算与实验的比较产品的产量
约翰·f·buying Garst和布莱恩·l·斯威夫特
美国化学学会杂志》上1989年111年(1),241 - 250
DOI:10.1021 / ja00183a037 - 4-METHOXY-4′-NITROBIPHENYL
k . Stille安东尼奥·m·Echavarren罗伯特·威廉姆斯,和詹姆斯·a·亨德里克斯
Org。Synth。1993年,71年,97年
DOI:10.15227 / orgsyn.071.0097
第二步在这个过程包括的合成p -anisylmagnesium溴化,可以准备一个棘手的格氏试剂,需要特殊的激活与碘甲烷毫克。
你好,
我只是想做格氏反应是放热的,自发反应。此外,氧化/还原反应热力学反应(δG = nf(δ)E)。因此,我可以得出结论,做出格氏反应热力学控制吗?
这个感觉反直觉以来形成的有机金属化合物活性和更不稳定得多卤代。
我希望你能开导我,我错在哪里。
感谢你的伟大的工作。
嗨——这是放热,热动力青睐。
热力学控制是当你可以选择的产品分布平衡混合物通过改变温度。没有格氏产品和原料之间的平衡。
你怎么回氯苯转化为苯?你能做到通过格氏试剂吗?
是的,工作,就像做lithium-halogen交换(如t-BuLi)和淬火水
问候!首先感谢您创建这个网站!
醛和酮也是酸性的,如:,acetone can act as an acid, so why don’t they give acid-base reaction with Grignard reagent. Is it because it is a weak acid? Are there any priority order like when will acid-base reaction occur and when nucleophillic addition? Thank you for your help!
问候!首先非常感谢你创造这样一个美妙的网站!
环己烷可以用作格氏试剂溶剂?我的教科书不能说,可以的原因什么?它似乎没有任何酸性的氢。
谢谢!
如果有什么都喜欢醛酮酯酸卤化物在同一化合物,先将反应吗?
这将是一个非常糟糕的合成设计,因为它是不明智的有这么多官能团存在在同一分子。但在这些醛可能是最活泼。
的产品是什么格氏试剂的反应和烷基卤化物吗?
通常不会解决你所希望的方式(即替换)。电子转移其次是减少烷基卤化物和消除都是常见的反应。取决于烷基卤化物的身份和替换模式。
即使有铜酸盐(吉尔曼试剂)让取代反应在仲碳可以非常具有挑战性的工作。
为什么不该羧酸与格氏反应? ?
他们deprotonate羧酸,但不要进一步反应。由此产生的O(-)是一个很强的π捐赠者的羰基碳,这大大减少了其亲电性。然而Organolithium试剂做添加羧酸。
格氏试剂的反应与酒精(zerevitnov)的反应不是这里…。剩下的内容很好。
这只是一种酸碱反应。
格氏试剂与烷烃反应吗?
绝对不可能,除非我们讨论酸性末端炔烃等碳氢键,或环戊二烯。
嘿,詹姆斯,今天我遇到了这个问题https://tinyurl.com/y489es2g上面写着“如果CH3MgBr摄入过量,则会消耗多少摩尔的CH3MgBr反应”
我解决了它,得出的结论是,只有2摩尔CH3MgBr是必需的,但是答案是第三方物流尽快帮助我。
1)寻找酸性质子(如醇类)。看到任何?我做的事。他们将执行一个酸碱反应。
2)酸氯。多少的格氏反应吗?
总= 3
如果在格氏反应和H3O +补充说,还有另一个H +和热添加吗?这个反应会是什么样子?
为什么你要这么做?难道你想完成你的检查和净化之前添加更多的酸?
如果在格氏反应和H3O +补充说,还有另一个H +和热添加吗?这个反应会是什么样子?
它没有意义添加H3O + H +,因为H3O +代表水检查,你会加热两相的混合物。
但是我认为你的意思是,一旦执行检查,你得到一个酒精。如果你热酒精和酸,你可能会得到某种消去反应。
可以用类似dihydropentalene格氏反应吗?
会发生什么,如果我们两个摩尔的格利雅(在第一次袭击我相信这将使芳香一侧)?
听起来像你要求考试问题的解决方案。确定。这是一个强大的基础。在两个对等的情况下,我认为你应该检查结果结构将从删除两个质子和计数结果π电子的数量。
你好詹姆斯,我有一个问题在我心中已经很长一段时间以来我开始ochem II。为什么我们从未看到格氏反应与α氢酮类和酯类,而不是选择攻击中的羰基取代反应尽管pKa理论上允许这样的去质子化的差异是可能的(pKa 50 vs pKa ~ 20到25)?
嗨,乔恩。*能*发生酸碱反应,但通常只在酮有很多位阻。
部分源于为什么酸碱反应快的区别在杂原子(例如哦)相对于碳。(又名“运动”的原则)
酸碱反应等杂原子哦快,因为很少有重组的去质子化后原子周围的债券。
相比之下在一个α碳,碳从sp3 rehybridize sp2,这就意味着其他两个碳氢键移动。
另一个微妙的因素是,酸碱反应的α碳酮要求与碳氢键羰基的π体系(这样去质子化导致共轭阴离子)上。对于发生酸碱反应,反应物之间的碰撞与α碳的碳氢键被正确的构象。没有这样的构象为反应屏障C = O键和假设没有妨碍格氏羰基的方法(即没有位阻)的反应应该很快。我知道这听起来有些简短,但它是一个试图向后合理化为什么酸碱反应是相对缓慢的在这个实例中。
为什么当完全形式gignard试剂然后剩下mg金属颜色是黑色的吗
有可能使用的有机化合物合成格氏氮气或氧气吗?
氧气,是的,尽管它应该是保护作为一个醚和没有地。氮也可能,但在复杂基质通常是容易做金属卤素交换。
什么X表示在格氏与二氧化碳的反应吗?这是一个氢卤化物或任何酸工作吗?
的抗衡离子形成的格利雅从一个烷基卤化物(例如Cl - Br -,我)
为什么格氏并不与烯烃反应但reaxts乙炔吗?
乙炔碳氢键质子更酸。
可以用grigard烯烃反应试剂吗?像没有形成格氏但后形成能与烯烃反应吗?
简短的回答是否定的。一个碳碳π键的electons烯烃碳之间的相对平等,共享结果碳都没有任何明显的部分正电荷。烯烃是稳定。相反,C = O键,碳部分正面和氧部分负面;格氏试剂更被动的在这种情况下。
酮和醚有酸性氢不该那么为什么格氏试剂与酮而不是醚反应吗?
RMgX + R ' OR ' - - > ROR + MgX(或“)
上述反应发生吗?
如果它发生,那么为什么格氏试剂放在干燥醚?
格里纳绝对不与醚反应。这就是为什么他们用作溶剂。至于酮…你需要重读这篇文章。
格利雅肯定是在我的列表的最喜欢的反应。我仍然认为桑德迈尔和clemmensen将在战斗中获胜。
对于格氏反应,你会如何执行反应如果你有MgBr-cyclohexane然后与乙醇反应溶液酸吗?
格氏乙醇只会使质子化,环己烷。
做格氏试剂与任何来源的质子反应给酒精吗?
烷烃,而不是酒精。
加热格氏试剂甲醇给什么?
它会给杀死你的格氏酸碱反应。
你好,我买了你所有的指导和应用,但是应用程序不是更新自2012年以来,虽然化学肯定没有改变orgo课程,我不购买支付,我很好奇如果在未来将会有任何更新。
更新!
二氧化碳可以格氏攻击两次,因为碳羧酸盐初始格氏攻击后仍有积极的三角洲费用?和随后的质子化作用创建偕的?
不,只有一次。攻击羧酸盐不会发生——羰基碳相当丰富电子由于捐赠的羧酸盐电子(π捐赠)
嘿我明白当你添加h30 +,但是如果您添加只是用水呢?
同样的事情!水是足够强的酸使质子化醇盐。(额外的细节,随时跳过:这将形成HO,卢武铉。为什么不反应可以反过来说,由于卢武铉是相似的酸强度的水吗?关键是要添加大量过剩的水。自会有一个更大的浓度的水,平衡驱动器酒精。)
我们最近做了一个格里纳合成在实验室使用乙醚作为溶剂,它说,反应是沉淀的阴沉和泡沫的迹象出现在镁但是我不知道什么样的气体这些泡沫会…他们是乙醚吗?
也许,是的。醚的沸点很低,格氏的形成产生的热量。
trimethylborate和格氏反应
这将使boronic酯,铃木反应的前体。
如果Gringard试剂是好的亲核试剂为什么它不参与SN类型提出今后
好问题。它会启动电子转换类型反应,最终导致乳沟的r×卤素(X)债券。格氏往往是集群解决方案,所以他们更可能出现位阻比。解决办法是把它们制成organocuprates(吉尔曼试剂)使用CuBr或类似的。然后SN2反应(特别是在主基板)很好地工作。詹姆斯
格氏试剂与乙醇的反应是什么?
它将被质子化了的乙醇,摧毁了格氏试剂和形成醇盐!
感谢你的工作在这些页面!你能谈谈如何格氏试剂与羧酸盐盐反应,与羧酸吗?他们会没有反应?我被要求展示的产品羧化物盐(乙基butanoate)和甲基格氏水检查紧随其后。我的猜测是盐和格氏反应不会(因为这些盐很稳定)和水会使质子化形成羧酸。想法吗?
他们不会做出反应。Organolithium物种,但是;可以治疗羧酸盐alkyllithium和获得一个酮。
你的回答听起来正确给我。
“格雷格甘松添加了一个相当于3 4-epoxy-4-methylcyclohexanol(图1)甲基溴化镁的乙醚溶液,然后加入稀盐酸。他预计该产品将是一个二醇(图2)。他没有得到任何预期的产品。他得到了什么产品?”i have tried everything for the answer i cannot figure it out
听起来像它只是deprotonated 1位置的羟基,假设你的底物是3,4-epoxy-4-methylcyclohexan-1-ol。醇盐可能然后打开,环氧产品我不能名字,但应该看起来像个dicyclohexylether甲基和昔日的环氧哦的环α醚键。所以没有从格氏打开二醇环氧化物因为-哦太酸性质子CH3MgBr的存在。
唔,或者你可能会得到一个很酷的分子内攻击如果你把衬底椅式构象让O -攻击环氧化物。我不知道。值得建立一个模型或画出来。如果你正在运行一个非常稀溶液的衬底,其中两个分子发现对方是一个非常罕见的前景,分子内可能会赢。
在分子内的情况下,但是,最终你会开放更多的环氧替代的一面得到两个5环分享C-O-C桥(得为这个模型!)而不是4 + 6…我想…
如果你试图使用格氏化学合成产品,和格氏反应物(R-MgBr)也包含一个醛酯和其他反应物,将格氏反应可能的反应与自身之前与醛的反应?
是的,它将反应本身。这就是为什么你需要保护组织可以进行格氏除了如醛、酮、酯类。虽然对于酯保护他们,不能让他们和醇氧化反应完成后。
氟为什么不参与格氏试剂呢? ? ?
氟键太强大而减少了镁。
因为在卤素和氟氟原子是最小的元素与碳原子形成共价键强为了打破这样的债券必须应用因此有力的条件
你好詹姆斯,
自从格氏试剂deprotonate酒精。
会影响与格氏反应醛生产二次酒精?
格氏之外单独生成醇盐。一个单独的酸检查有必要使质子化二级醇的醇盐。
做碳正离子中形成醛和酮的反应与格氏试剂stabalize 1-2methyl转变或氢化物转移? ? ?
期间不形成碳正离子与醛/酮格氏反应。
讨论了利用格氏试剂在有机合成。
如何可以反应之间的1、2不饱和酮和格氏试剂吗?
非常感谢你的信息
我最近遇到了有趣的反应之间的格氏试剂和丙炔氯化物(终端)。SN2′替换给艾伦新碳碳单键,连同一片混乱造成的其他东西去质子化的终端炔…包括古老的烷叉碳烯,也许我最喜欢模糊的中间的有机化学!
http://pubs.acs.org/doi/abs/10.1021/jo00401a020