光谱学
紫外可见光谱法:羰基的吸光度
最后更新:2022年10月31日|
紫外可见光谱的金属羰基合物(C = O债券)
紫外可见光谱法不仅仅是碳碳π键。切断π键能吸收紫外线!
表的内容
1。一个快速回顾一下我们目前学到的紫外吸收
在我们的最后发表我们表明,分子与碳碳π(π)债券在紫外可见吸收光区域,促进电子(粘结)π轨道(反键)π*轨道。
我们看到
- 所需的能源转换的程度主要取决于动词的词形变化(即连续π键的数量,粗略地讲)。
- 一个烯烃很少或根本没有动词的词形变化(如乙烯、CH2= CH2)具有大能源缺口(ΔE)之间的成键和反键轨道,它要求更有活力(光波)光子激发。乙烯,最大吸光度发生在约170海里,在紫外线地区。
- 随着共轭的增加,能源缺口ΔE减少,推动最大吸光度的波长(λ马克斯)向可见(更少的高能光子,长波长)。例如,β-carotene(橙色胡萝卜色素)11个共轭π键,吸收可见光(λ马克斯= 470海里)。
因为邮局是这么长,我们还没开始解决一个关键问题:这是否适用于其他类型的π键吗?
例如,C = Oπ键也吸收光线在紫外/可见区域?
- 简短的回答是:是的。
- 中型的回答是:是的,但是主要的过渡感兴趣的并不是一个介子*过渡略有不同。
长一点的回答. .好吧,这是长期的答案。
2。吸光度的C = O债券表现出最大的约300海里
让我们先从最简单的一个化合物的C = O邦德:丙酮,否则称为丙酮。
问题:丙酮吸收紫外线或可见光吗?
答:那还用说。这是丙酮的紫外可见吸收光谱(丙酮)。
(关键信息收集的频谱有一个吸光度最大的约275海里在紫外线。)
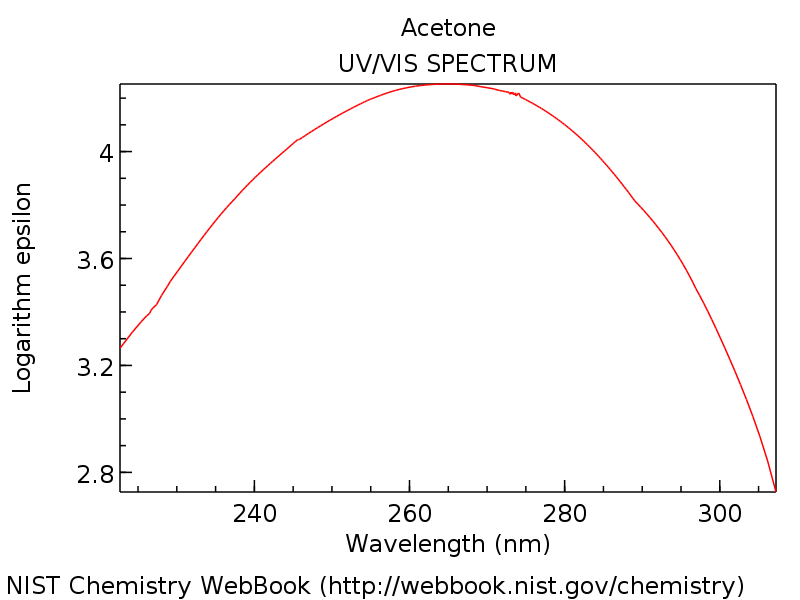
如果你有一个非常好的记忆力你可能记得上次发布(或从我上面介绍)乙烯吸收马克斯(CH2= CH2)约170海里。
一个吸收约275海里意味着更长的波长因此更少的精力充沛这种转变所需的光子。
这像不奇怪吗?
如果有的话,C = Oπ键更强的比C = Cπ键。你可以查一下。难道你合理期望* *能源需要从圆周率(π)促进电子π*(π*)?
到底发生了什么事?
现在:我们会看到,在那里是ππ*(π→π*)过渡丙酮紫外线,但这高峰在275海里不是一个ππ*跃迁。这是一个从一个非键轨道(n)过渡到π*轨道(n→π*)。
3所示。羰基(C = O)组织倾向于显示弱吸光度(约)300海里,对应于非成键轨道和π*轨道之间的转换
哈吗?让我们看一个简单的分子轨道图丙酮。
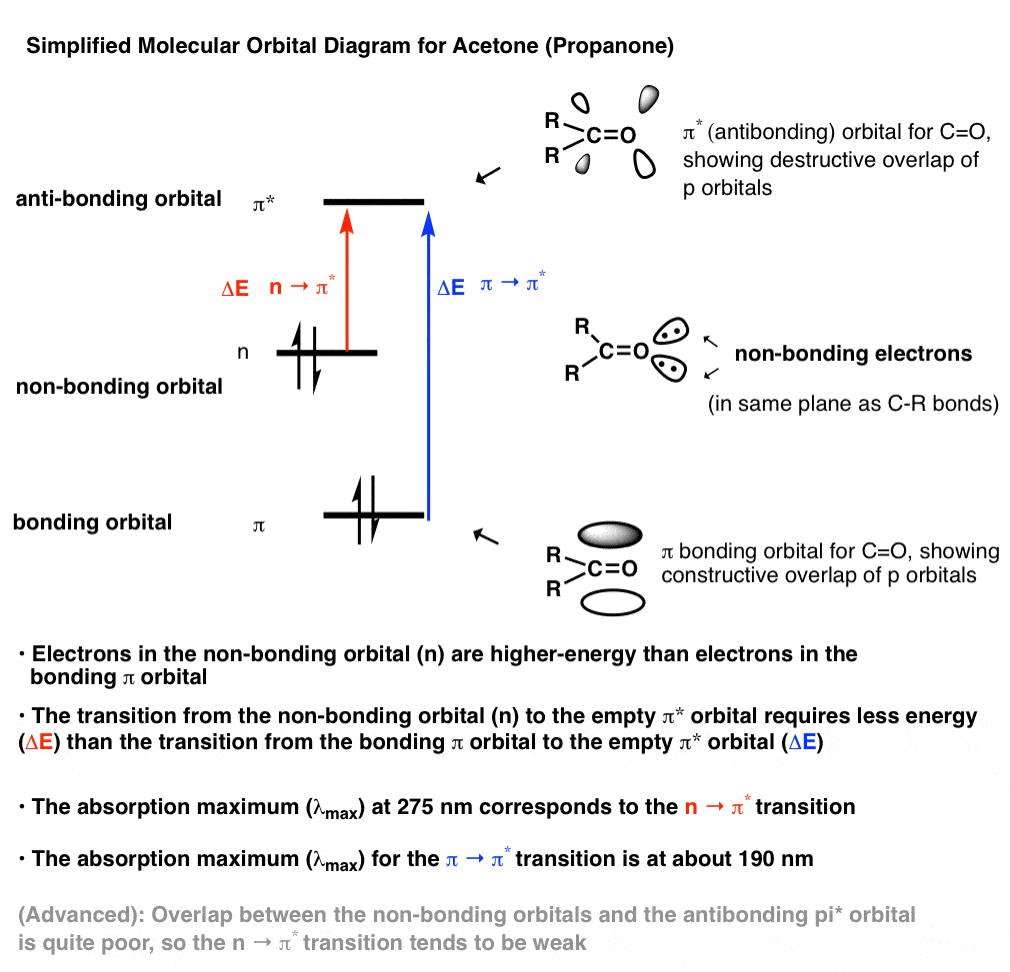
[这是一个简化的画面。更详细的莫图,还包括一个更彻底的讨论性质的非键轨道,我强烈推荐Reusch在线教科书条目。]
一些重要的注意事项:
- 羰基组包含非成键电子在能量之间的成键轨道中间π轨道和反键π*轨道。这些轨道缺席在典型的烯烃如乙烯(CH2= CH2][注1]
- 更高的能源,电子之间的转换的非键轨道π*轨道ΔE较小,因此在长波长吸收。
- 正是这种(n→π*)过渡负责高峰在275纳米左右。
4所示。关于ππ*转换为C = O ?
ππ*跃迁呢?也不会发生吗?
很高兴你发问。如果你快速回顾的紫外可见吸收光谱丙酮,上图中,您会注意到,x轴切断240海里左右。有一个原因(mwah-ah-ah)。
如果你缩小,你会发现有一个更强大的过渡约190海里。(我去寻找一个体面的全尺寸的紫外光谱丙酮如下图,是我能找到最好的。我没有这张照片,它不是我的知识产权。我发现它在这里。]
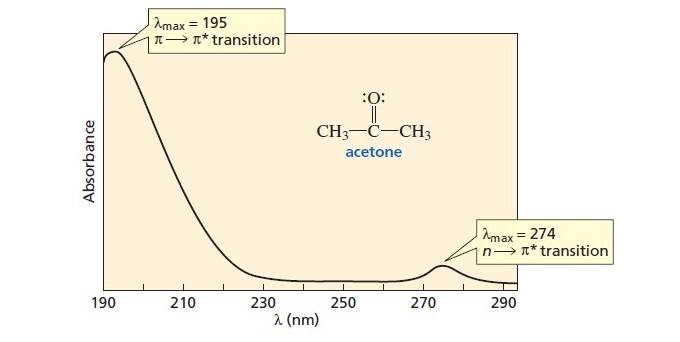
事实证明,“峰”275海里(n→π*)我们看是一个无意义的事旁边(π→π*)山约为195纳米的更深层次的紫外线。
换句话说,(n→π*)在275纳米过渡,我们花了很多时间讨论很弱的相对于(π→π*)过渡。(有时一个术语称为“εε”是用来表示这种差异大小的吸收)。
这是为什么呢?这与差异轨道重叠。为了使电子从一个轨道到另一个过渡,必须满足两个条件。
- 首先,正如前面所讨论的那样,轨道与光子ΔE适当的能量。
- 第二,必须有意义重叠在太空轨道之间。我们一般不讨论这个(π→π*)和(σ→σ*)转换,因为每一对成键和反键轨道占用相同的区域空间。如果你回顾图的位置n轨道丙酮π*轨道的位置相比,你可能会注意到他们基本上成直角。可怜的轨道重叠意味着即使电子有足够的能量ΔE过渡,过渡明显不太可能发生,因为受激电子将不太可能被占据的空间对应的高能轨道。(额外的细节:您可能还记得,轨道三维卷,遇到一个电子的概率是95%。因此,有是一些外部的电子密度卷我们通常考虑“轨道”)
5。羰基也参与接合
金属羰基合物也可以参与与碳碳共轭π键。这将导致增加整体λ马克斯的分子。例如,的吸光度烯烃2 -甲基pent-2-ene低于200海里,π→π*吸光度4-methyl pentane-2-one(下图)。
亚异丙基丙酮,烯烃和C = O组相互结合,吸收最大移向长波长228 nm。这类似于不同乙烯(174海里)的吸光度和丁二烯(217海里)。
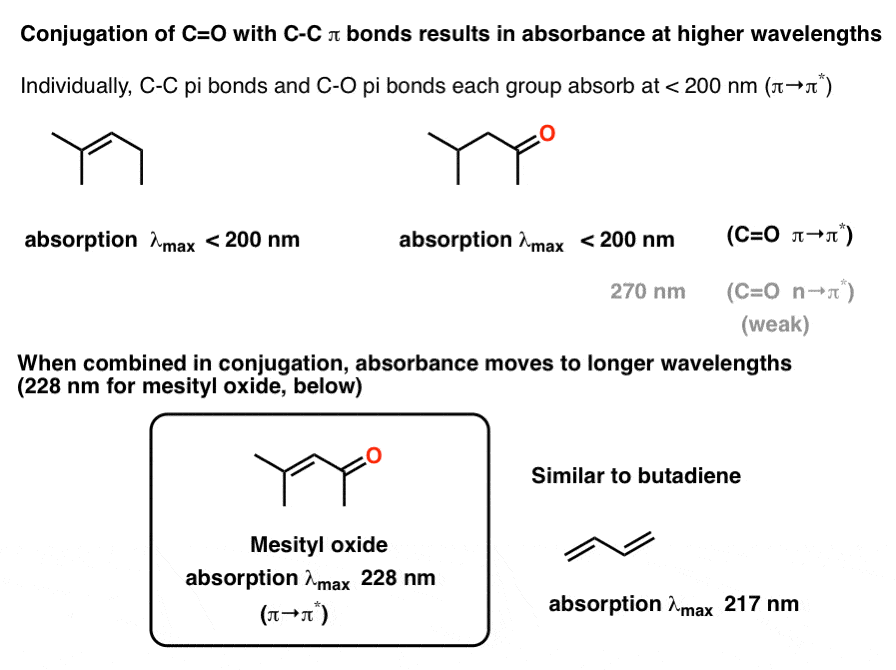
请注意最大吸光度可以敏感的身份溶剂以及取代基上的身份烯烃。(注2]。
6。摘要:羰基的紫外可见光谱
吸光度在270 - 300海里的粗糙的邻居是常见的分子包含一个C = O组(如酮和醛),这对应于一个(n→π*)过渡。
这些吸光度往往弱,相对于(π→π*)转换。不过,观察这个吸光度可以未知化合物的结构测定的重要线索。
在接下来的文章我们将进入实际使用紫外可见的细节结构的决心。
(再一次,更深入看C = O吸光度的主题,bdapp平台Reusch。我们浏览这里的表面,但这对我们来说已经足够了。)
笔记
注1。应该注意的是,非键轨道是在物种如烯丙基阳离子、烯丙基阴离子和其他离子的奇数π体系。
注2。为金属羰基合物,一般更多的极性溶剂导致更高的λ马克斯值一样,取代基的存在(如甲基)烯烃。
额外的话题:偶氮染料
因为我们在这个问题上,让我们简要地探讨bdapp平台另一个系统,两个n→π*和π→π*转换观察:偶氮染料。
偶氮染料的,没有具体知道你可能见过一百万次什么他们是。
例如,公路标志的黄色?这是颜料黄10。

偶氮染料中常用的染色纺织品、塑料、和许多其他物质不用于人类食用(他们通常禁止作为食品添加剂)。
偶氮的化合物的重要结构特征是一个N = N键。最简单的偶氮的化合物之一偶氮苯,每个氮是一个芳环连接。轻微的修改苯环分子可以大幅修改的颜色。苯胺黄,发现于1861年,是第一个偶氮复合找到商业使用染料,和无数的衍生品偶氮苯的合成。的合成是通过重氮耦合——我们不会进入这里。
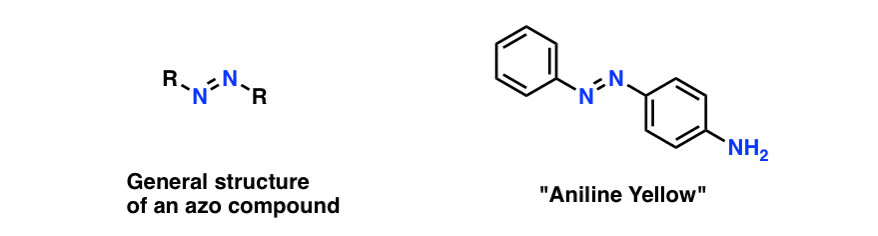
这是苯胺黄的紫外可见光谱,由ChemTube 3 d计算。
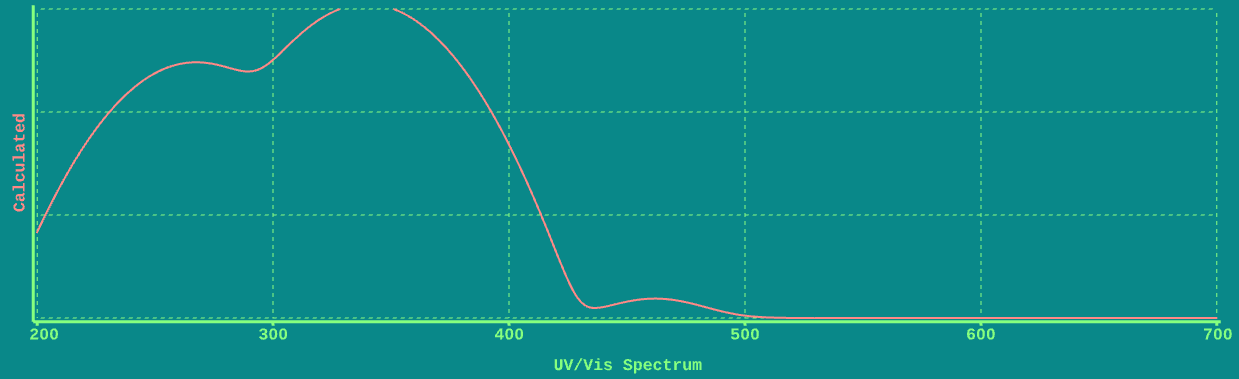
注意它是如何定性类似于丙酮:左边一个强大的吸光度(对紫外线)和弱吸光度右侧(向可见)。
相比丙酮然而,弱吸光度在260 nm,苯胺黄的弱吸光度光谱中的可见光区域约460海里。这个吸光度在460 nm负责苯胺黄的颜色。
通过类比丙酮,疲弱的过渡是一个(n→π*)过渡和强劲的过渡约360纳米是一个π→π*跃迁。
光异构化
更有趣的关于偶氮苯及其衍生物(例如苯胺黄)的现象光异构化,吸收特定频率的光会导致的异构化的反式同分异构体,独联体同分异构体,反之亦然。
吸光度的紫外线反式偶氮苯(π→π*跃迁)导致异构化独联体偶氮苯。相反,吸光度的可见光(蓝光)独联体偶氮苯(n→π*跃迁)导致转换回反式同分异构体(离开独联体偶氮苯在黑暗中,这一过程称为热放松)。这个过程的机制还没有完全解决。
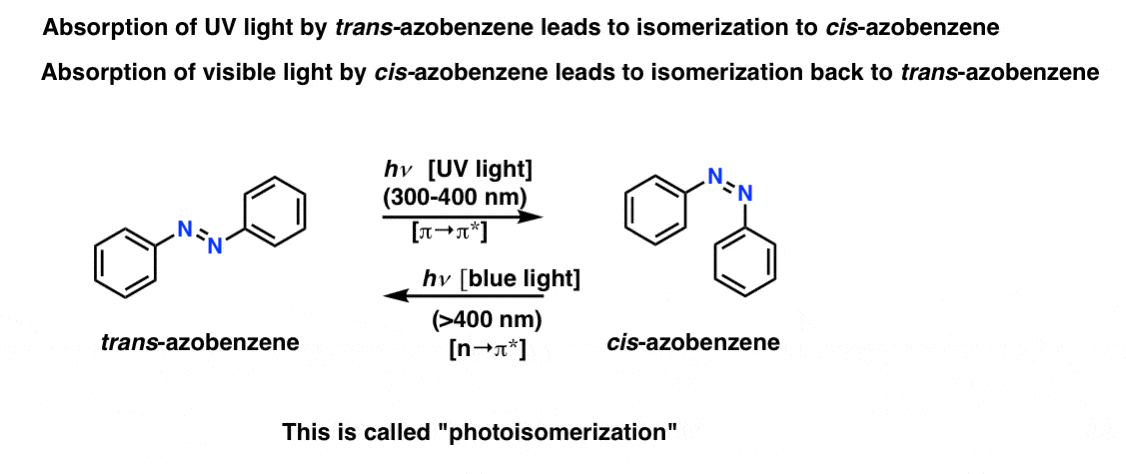
很整洁,你可以针对一个特定的异构体仅仅通过改变光的频率。
很好。了学习的乐趣。
丙酮光谱显示的链接λ马克斯在195 nm似乎并不存在。一般的页面。你有一个更新的链接或链接显示吸光度在195海里吗?
就像我说我找不到原来的,我联系到一个页面并没有知识产权。
另一个源可能是这里,NIST的网页:
https://webbook.nist.gov/cgi/cbook.cgi?ID=C67641&Units=SI&Mask=400 UV-Vis-Spec
你好
我有一个问题plx…的紫外线vis soectrum acetobe我们只考虑两种类型的过渡ππ*或nπ*。我的问题是σ键也存在于羰基,同样可能存在σ* n之间的过渡。那么为什么我们只考虑两种可能的转换?为什么我们不考虑其他转换由于σ键?
好解释。
相关的问题;
如何结合有助于增加共轭化合物的λ马克斯?
见本系列之前的文章://m.deriinvest.com/2016/09/16/introduction-to-uv-vis-spectroscopy/
伟大的讨论话题! !
问题偶氮黄染料。当我抬头cis黄色偶氮的吸收光谱在互联网上,我看到吸收峰~ 420远低于峰值进一步到紫外线,这将会为一个n - >π明星转变为你解释的原因,但更强的吸收光波的λ马克斯cis实际上是在更短的波长比反式。我希望相反的考虑到空间应变两个苯组的顺式构象和贫困p轨道的重叠
相关的问题:我认为n >π明星转型导致削弱n = n双键就像π>π明星转型,从而使顺反异构化照片吗?
谢谢!
很有帮助我修订有机光谱…
很高兴听到它泰森。谢谢!
非常感谢。最清楚的是我读。美丽的工作!
这是一个非常有用的教训的紫外吸光度与轨道过渡。我是一个高中的化学老师,我学到了很多!
很棒的史蒂夫!谢谢你让我知道!