二烯烃和MO理论
分子轨道的烯丙基阳离子,烯丙基自由基和烯丙基阴离子
最后更新:2023年1月17日|
如何绘制分子轨道的烯丙基阳离子,烯丙基自由基和烯丙基阴离子吗
画的π分子轨道系统烯丙基(3共轭p轨道)有点像建设:先建殿(轨道),填补它与人(电子)。
- 当两个p轨道的π键可以用p轨道重叠在一个相邻的碳,由此产生的“pi-system”包含3 p轨道被称为烯丙基π体系
- 的烯丙基阳离子有3个p轨道和两个π电子
- 的烯丙基自由基有3个p轨道和三个π电子
- 的烯丙基阴离子有3个p轨道和四个π电子
- 画出每一个系统的分子轨道可以逐步地完成。
- 的最低分子轨道(π1)将所有三个p轨道与相同阶段和零节点
- 的高能分子轨道(π3)将有三个p轨道相反阶段和两个节点。
- 中间能源分子轨道一个节点中心原子。
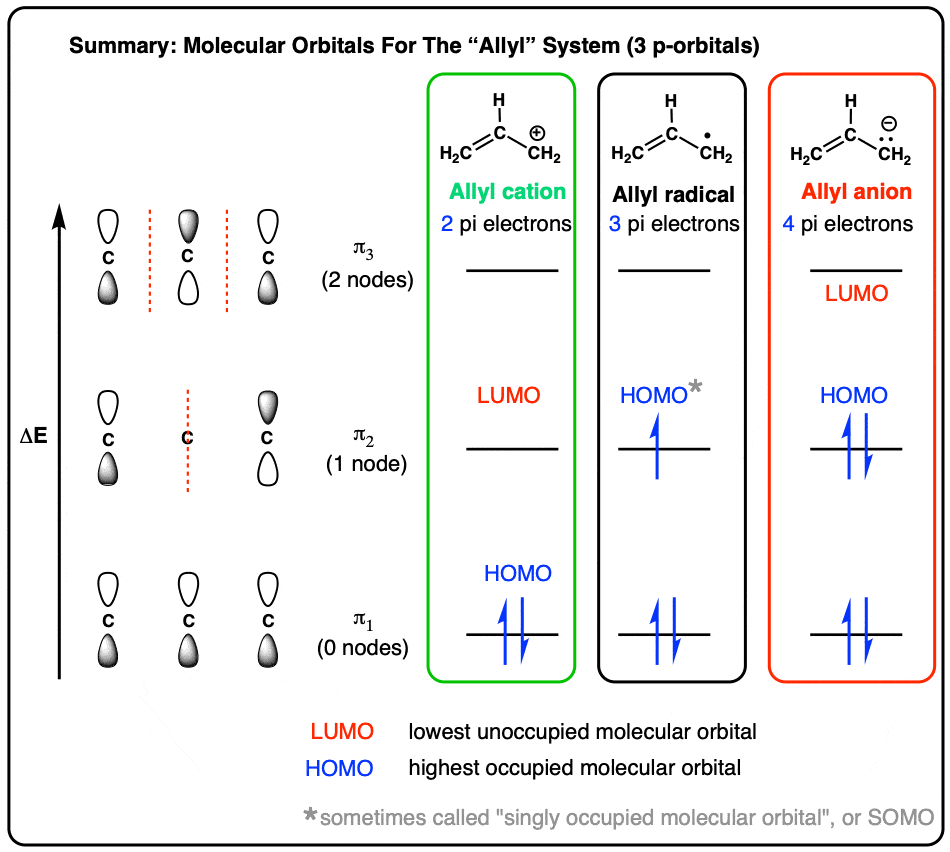
- 一旦分子轨道图,下一步是装满π电子:两个烯丙基阳离子,三个烯丙基自由基,四个烯丙基阴离子。
表的内容
- 快速回顾一下:为一个简单的π键分子轨道
- 的规则建立π分子轨道
- 烯丙基阳离子、烯丙基自由基和烯丙基阴离子
- 烯丙基的分子轨道系统(N = 3)
- 棘手的烯丙基的中间轨道系统
- 分子轨道的烯丙基阳离子(2π电子)
- 烯丙基自由基的分子轨道(3π电子)
- 分子轨道的烯丙基阴离子(4π电子)
- 结论:丙烯体系
- 笔记
- (高级)引用和进一步阅读
1。快速回顾一下:为一个简单的π键分子轨道
在过去,我们显示如何构建一个分子轨道(MO)图一个典型的碳碳π键。
我们发现:
- 分子轨道的数目与原子轨道的贡献。的重叠两个原子(p)轨道了两个分子(π,或π)轨道
- 最低分子轨道在p轨道的贡献的所有阶段相同的方式保持一致。换句话说,没有节点在p轨道之间。
- 能源与节点的数量增加(就像驻波)。高能分子轨道的一个节点,在p轨道改变了彼此之间的阶段。
π键的分子轨道是这个样子:
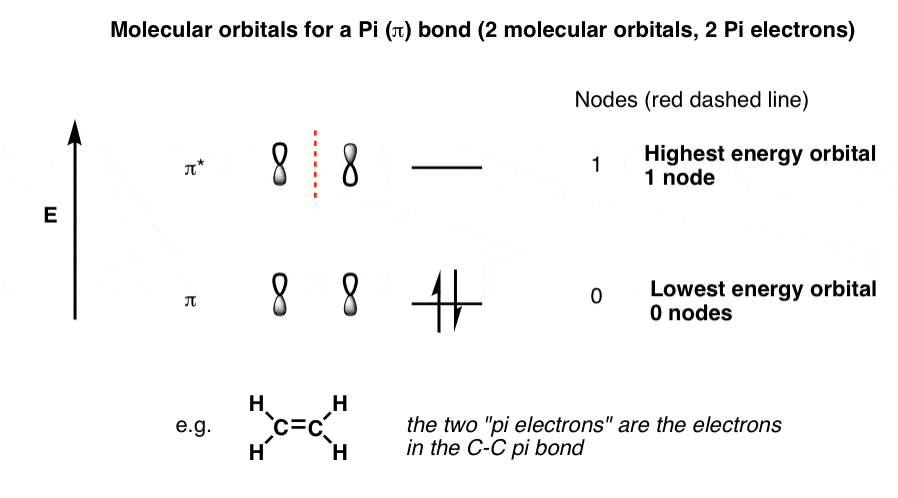
画出一个π键的分子轨道似乎很简单。但是如果我们添加一个分子轨道图第三p轨道的贡献?如果我们有一个相邻的双键,贡献2 p轨道,给我们总共4共轭p轨道吗?理解发生了分子轨道将使我们能够理解他们的能量,和(稍后我们会看到)他们的反应。
2。概括的规则建立π分子轨道
我们可以使用建设过程中的经验教训π键的分子轨道向建立更大的推广(线性)pi系统包含N分子轨道。(注1]
- 系统的N原子obitals我们将分子轨道
- 最低轨道总有零节点(所有phase-aligned)
- 会的最高能级一个节点
- 水平之后,两个节点,
- 等等,到最高的能量水平,n - 1节点(所有的交替阶段)
两个关键的经验教训,真的。首先,p轨道的数量告诉你π轨道的数目。第二,最低和最高能量的轨道是最简单的画:能量最低的阶段都对齐,和最高能量的阶段交替。我们将使用这个泛化。
这让我们更上一层楼。三个分子轨道。我们称之为烯丙基系统。我们走吧!
3所示。烯丙基阳离子、烯丙基自由基和烯丙基阴离子
你听说过甲,乙,丙,丁;我们的名字三碳单元H2C = CH-CH2是“烯丙基”。烯丙醇,例如,H2C = CH-CH2哦。
现在你可能遇到的烯丙基阳离子,烯丙基自由基,或烯丙基阴离子吗?也许你已经知道了烯丙基阳离子是“共轭”上碳正离子,或烯丙基自由基是“共振稳定”激进?
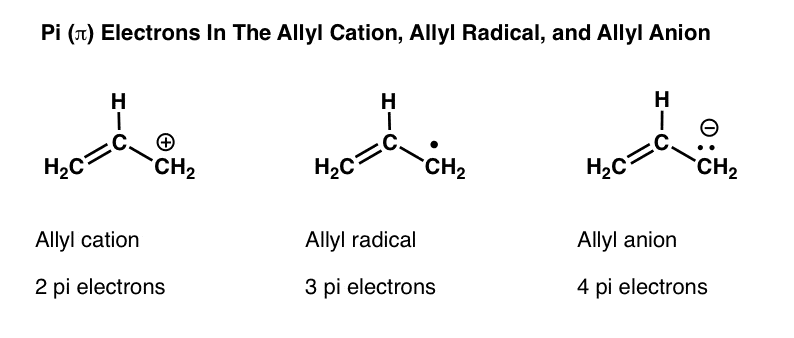
在这些“π系统”的烯丙基碳有一个可用的p轨道共轭与相邻的π键。另一种说法一样的烯丙基碳是共振的π键,这样,我们可以画出每一个分子的共振结构。我们不会再这样做了:我们覆盖这两个帖子前,在这篇文章中结合和共振——如果你需要复习,回去读表演结合,共振,轨道重叠。]
由于烯丙基系统有三个p轨道的接合,π分子轨道会有多少?
三。(N = 3)
下一个问题。将这三个π分子轨道是什么样子的呢?说你问以下问题:
“画的烯丙基阳离子分子轨道,烯丙基自由基,和烯丙基阴离子。”
(一种常见的足够的考试问题,信不信由你!)。
你会如何处理?
激进,烯丙基阳离子和阴离子所有使用相同的框架的分子轨道。他们只π电子的数量他们拥有不同(分别为2、3、4)。
知道,我们可以把这个问题分成两个阶段。
- 第一个自己,画出轨道。
- 第二,填充适当数量的π电子的轨道。
让我们这样做。
4所示。烯丙基的分子轨道系统(N = 3)
首先画出最低和最高能量轨道
我们将开始通过轨道。这两个简单的画是最低和最高能量轨道,所以让我们先做这些。
- 的最低分子轨道将完全对齐的阶段在p轨道,以及它们之间零节点。让我们称之为“π1”,最低π分子轨道。(我们可以另外画上面的“阴影”阶段:它相当于相同)。
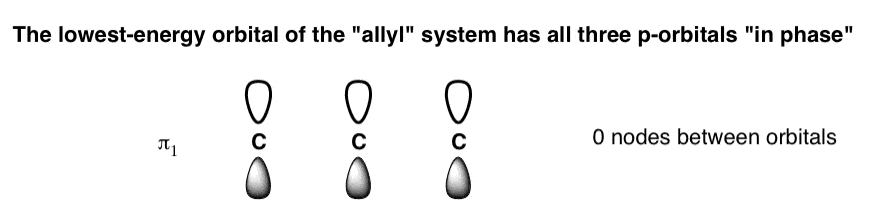
- 的高能分子轨道也很容易画:所有阶段交替,给它(n - 1) = 2节点。我们可以称之为“π3”,高能π轨道的三个。节点是标有红色线。
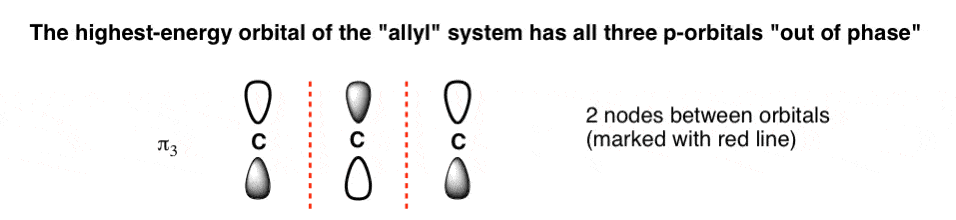
5。棘手的烯丙基的中间轨道系统
关于中间轨道,π2吗?它应该有一个π之间能量节点,中间1和π3
把一个节点在哪里?如果你像我一样,你的第一个诱惑图之间的轨道可能会将一个节点的一个碳,给轨道,看起来像这样:
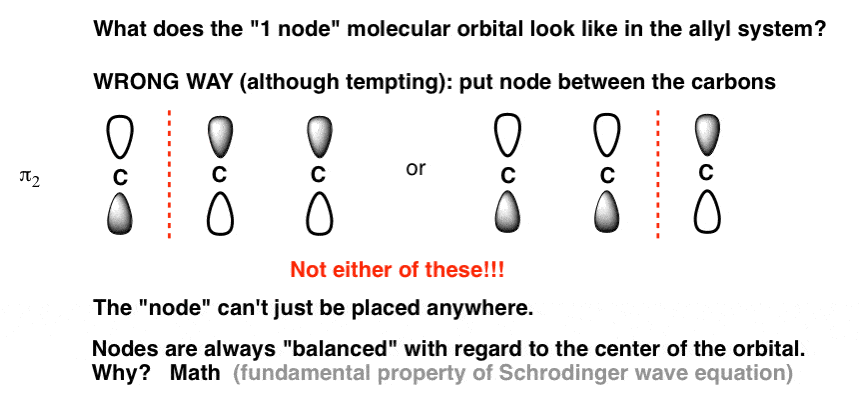
它实际上是不正确的!
为什么?这是个好问题,答案并不明显。事实证明,因为薛定谔方程的数学的工作方式,节点总是“平衡”对轨道的中心。节点不能被放置在任何地方;当一个节点,它必须在中心。(顺便说一下,这是密苏里州的普遍特征就是轨道的贡献的数量是奇数,例如N = 3, N = 5, N = 7…第一个节点将在中央碳。)
中间的节点!
这意味着该节点直接在中间的碳。
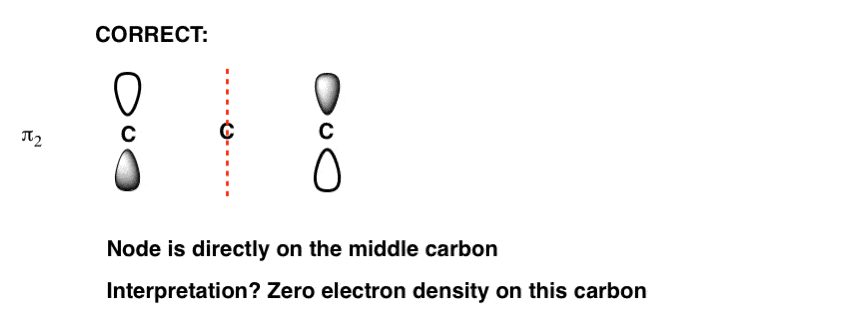
很奇怪,对吧?这到底意味着什么呢?这意味着在分子轨道上电子密度为零,中央碳。我们不需要进一步的细节对于我们的目的,但我包括注意反应给了我们一些线索。(注2]
现在,如果我们安排这些轨道由能源(最稳定的底部),我们得到下面的烯丙基系统的轨道图。
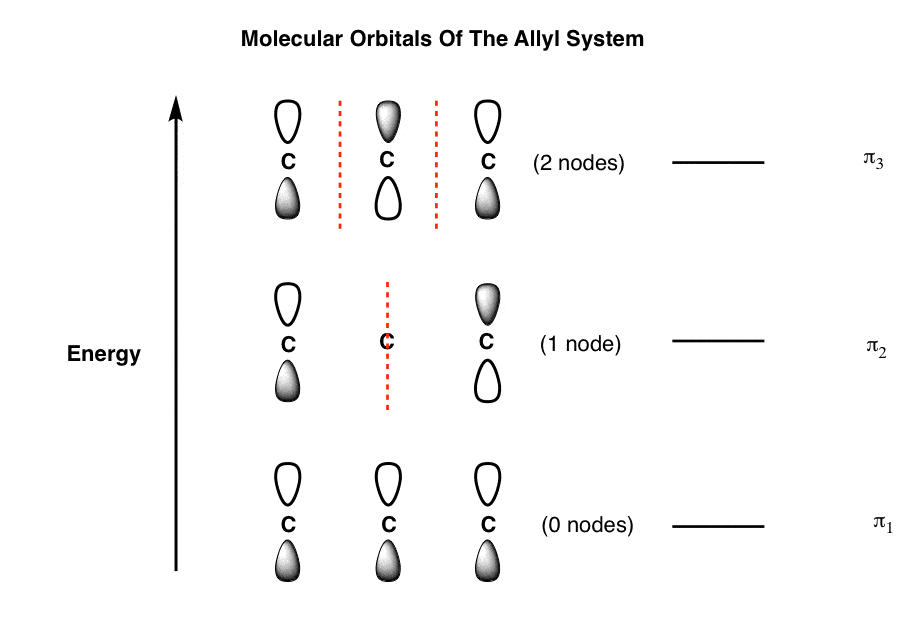
这是轨道在烯丙基系统的框架。这不是具体的烯丙基阳离子,激进,或者阴离子,因为这三个物种具有π电子的数量不同。
现在,让我们来填充电子的轨道。
6。分子轨道的烯丙基阳离子(2π电子)
烯丙基阳离子我们总共有2π电子:在下面的共振形式中,我们看到两个电子π键,和零碳烯丙基。
当我们填充烯丙基轨道有两个电子,建筑从一楼,我们得到了以下几点:
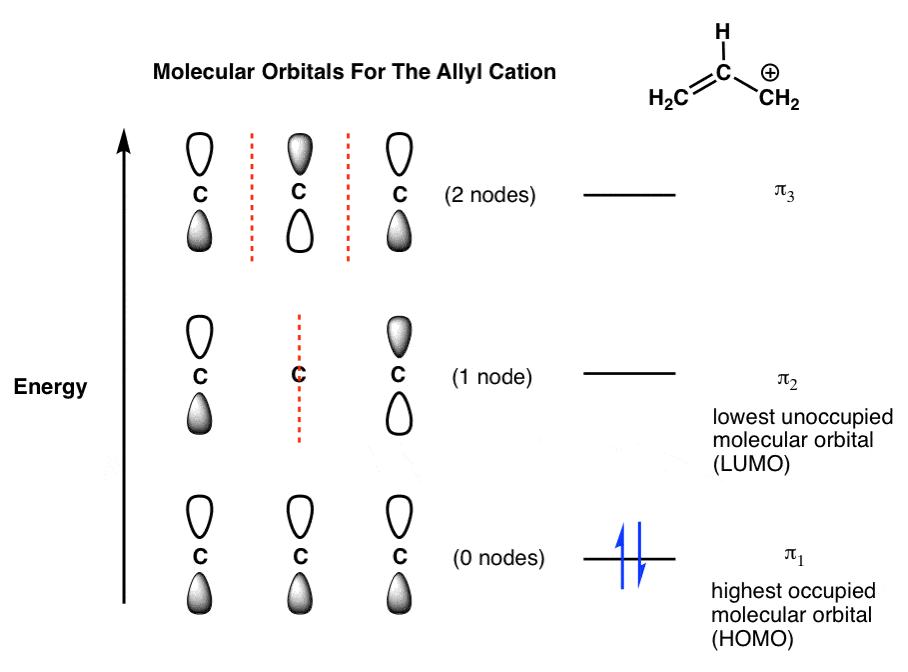
注意,“最高占据分子轨道的烯丙基阳离子是π1——最低轨道系统中。最低未占据的分子轨道是π2。
我们通常缩写术语“最高占据分子轨道”HOMO和LUMO“最低未占据分子轨道”。他们通常被称为“前沿”分子轨道,在大多数的行动发生在反应,我们会看到在未来的文章中。
7所示。烯丙基自由基的分子轨道(3π电子)
烯丙基自由基呢?这里我们有3π电子:两个π键,和一个在装第三个p轨道。
我们把第三个电子?当然,这个比率在轨道。成π2它!
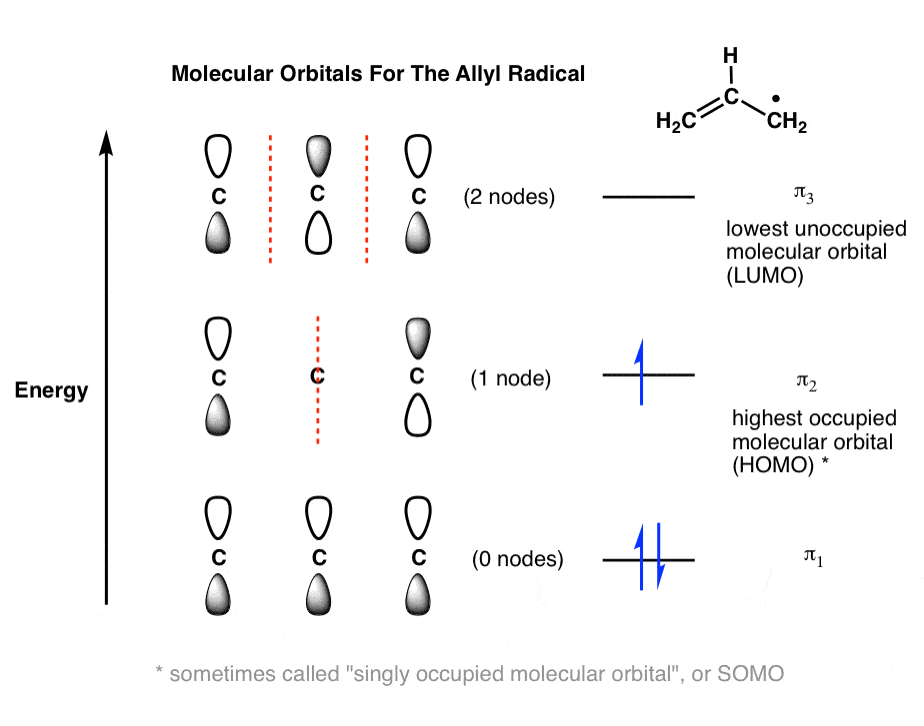
这给了我们一个装π2,这是我们的新“人类”,和π3现在变成了我们的“LUMO”。(我不想增加混乱,但有时候装这样的分子轨道被称为“单独占据分子轨道”,或SOMO。不是在这个阶段非常重要]。
8。分子轨道的烯丙基阴离子(4π电子)
烯丙基阴离子呢?这里有4π电子:两个π键,和两个更多的终端上的孤对碳。这充满了π2。
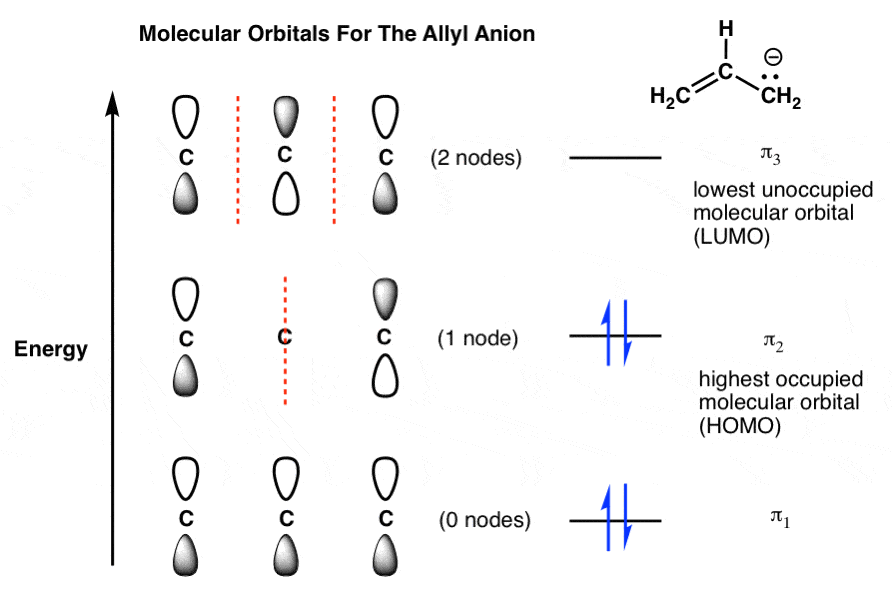
我们人类是π2和我们的LUMO仍然π3。
这令人满意地显示了烯丙基阳离子分子轨道,激进和阴离子。
9。结论:丙烯体系
在这里,我们显示如何扩展分子轨道我们学到的一般原则建立π键的分子轨道(N = 2)对烯丙基系统(N = 3)。要点如下:
- N原子p轨道产生Nπ分子轨道
- Nth分子轨道将n - 1节点。(如第三MO的烯丙基系统(3 - 1 = 2)节点。
- 当被要求画分子轨道,一个好的经验法则是从最低开始,高能分子轨道。最低分子轨道节点为零(所有p轨道阶段)和高能分子轨道(n - 1)节点(所有p轨道的阶段)。
- 不要添加电子系统,直到你首先画出所有分子轨道。
在接下来的文章,让我们来看看butadienyl系统的分子轨道(N = 4)。
笔记
注1。“N的经验法则th分子轨道将n - 1节点”最好适用于线性分子。循环分子(如苯)遵循同样的一般原则,但由于对称“节点飞机”。例如苯的最低能量莫零节点,但最高能级苯是“双重退化”意味着有两种方法可以画一个节面。更多的在这里。我们将讨论在一个单独的文章。
注2。(一个先进的注意:一个结果的节点在π的中心2是中间的激进的电子密度为零碳(c - 2)。这是符合我们所观察到的所有关于烯丙基自由基的反应——他们反应终点(颈- 1或颈- 3),和从来没有中间的碳(c - 2)。]
注3。这是最后一个(高级)脚注,只有极其好奇应该看看。它显示3烯丙基的分子轨道系统通过相互作用形成的2π分子轨道p轨道。这导致降低π轨道的能量(导致一个稳定的能量E)和提高能源的π*轨道。p轨道的能量保持不变;中间能源之间的成键和反键,它被称为“非键分子轨道。
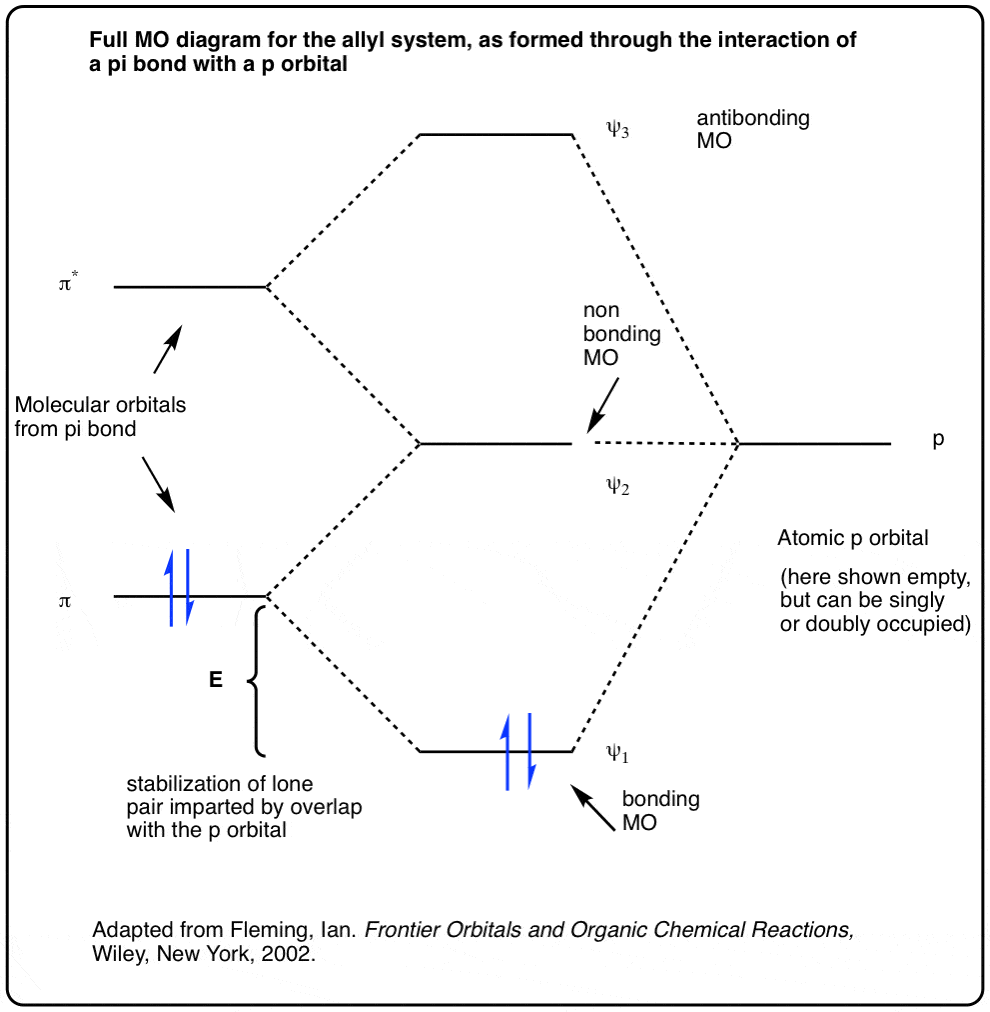
改编自伊恩·弗莱明的优秀“前沿轨道和有机化学反应”。
(高级)引用和进一步阅读
这个话题覆盖在一些教科书和最好的关于这个主题的信息来源是书。
- Streitwieser heathcock。,小。分子轨道理论的有机化学家;威利:纽约,1961年。
- 弗莱明,我。前沿轨道和有机化学反应;威利:纽约,1991年
- Streitweiser,小a。补充表的分子轨道计算,卷2;帕加马新闻:牛津大学出版社,1965年
- 立体化学路径的识别轨道相互作用
Kenichi福井
的化学研究1971年4(2),57 - 64
DOI:10.1021 / ar50038a003
本文论述了丁二烯的分子轨道的上下文中前沿分子轨道理论和“Woodward-Hoffmann”规则。福井教授获得了1981年诺贝尔化学奖罗尔德·霍夫曼教授为他贡献的发展前沿分子轨道(FMO)理论。 - 2。考试的能量对双键的同面性的偏好。比较丁二烯、丙烯醛和乙烯胺
肯尼斯·b·Wiberg罗伯特·e·罗森博格,和保罗·r·拉
美国化学学会杂志》上1991年,113年(8),2890 - 2898
DOI:10.1021 / ja00008a016
本文探讨了密苏里州的丁二烯和乙烯胺和丙烯醛等电子的分子。丁二烯有障碍旋转沿C2-C3债券,由MO理论预测。
我困惑莫图之间的烯丙基系统使用原子p轨道,得到完整的莫图过去。
第一个显示的三能级和阶段p轨道。第二个用电子填充它。
这是第二个因素,最终确定哪些3π分子轨道的最高占据分子轨道(HOMO)或最低未占据分子轨道(LUMO)。
这个网站正在迅速成为我最喜欢的餐馆之一。我喜欢看到这样的复杂主题解释如此有效!bdapp平台
我假设我丢失的东西明显还没能找到这个问题提出了其他地方,所以我希望读者能够帮助我。
我觉得找到一个原子的杂交,可以使用空间数量的σ键+ #(#孤)。烯丙基阴离子但如果我们这样做,我们得到的SN 4(1和3σ键),对应于sp3杂交。但如果是这样的话,我们就不会有可用的p轨道共振结构给我们…
正确的。将在一个孤对sp3杂化轨道,和相邻的sp3 orbtial p轨道的重叠并不是那么好。Re-hybridization sp3轨道的p给较低的能源结构。
激进的阳离子,阴离子烯丙基的碳原子,这是最稳定的能量?我已经找,但我似乎无法找到答案吨。
很难比较的相对稳定性阴离子,阳离子和自由基。真的就像拿苹果,橘子和香蕉。更容易比较阴离子相对于其他阴离子,阳离子其他阳离子,等等。
我的意思年底C1和C3碳原子先生,对不起,稍事休息
先生,我有一个问题要问你(似乎是愚蠢的). .烯丙基阴离子或激进的系统,据说两个电子分别在离子和一个电子激进(指非成键轨道)是由碳原子(C2和C3)结束共享. .怎么可能,如果它们之间有中间节点碳?请明确我怀疑先生
谢谢提供如此详细的回答和解释在一个简单的方法:)
先生,烯丙基的分子轨道图的系统,我们可以对烯丙基的阳离子的稳定秩序,激进和阴离子吗?
凭什么我们决定这个订单吗?
很难比较的相对稳定性阴离子,阳离子和自由基。真的就像拿苹果,橘子和香蕉。更容易比较阴离子相对于其他阴离子,阳离子其他阳离子,等等。
非常感谢先生对这些可爱的解释!
谢谢你你的快速反应。你是对的,我的意思是丙二烯和我很熟悉它的结构。我想知道的是是否分子轨道由原子轨道将独立存在,他们是否也会互相垂直。
是的,他们将独立存在,是的,他们将互相垂直。本质上他们像两个独立的π键。
我想知道如果丙二烯分子轨道与1类似,3丁二烯。我知道丙二烯结构扭曲,但我不明白为什么没有一个网站提它的分子轨道。我理解这篇文章很好,但我只是好奇丙二烯由于某种原因。你能请帮助我了解这个吗?
你的意思是,“丙二烯”?它有两个π键成直角。//m.deriinvest.com/2015/01/13/chiral-allenes-and-chiral-axes/
真正伟大的解释!
好的,谢谢彼得,很高兴你有帮助!
非常感谢先生很有用的帖子……容易理解,但难以找到在普通教科书。