胺
一些反应的叠氮化
最后更新:2022年9月21日|
叠氮化离子:结构、属性和置换反应
表的内容
- 叠氮化离子是一个伟大的亲核试剂
- “蒙面”胺有机叠氮化物
- 在发射台爆炸
- 亲核酰取代与叠氮化盐:酰基叠氮化
- 重排的酰基叠氮化:库尔修斯重排
- 叠氮化的亲核试剂的例子:环氧打开和共轭加成
- 笔记
- (高级)引用和进一步阅读
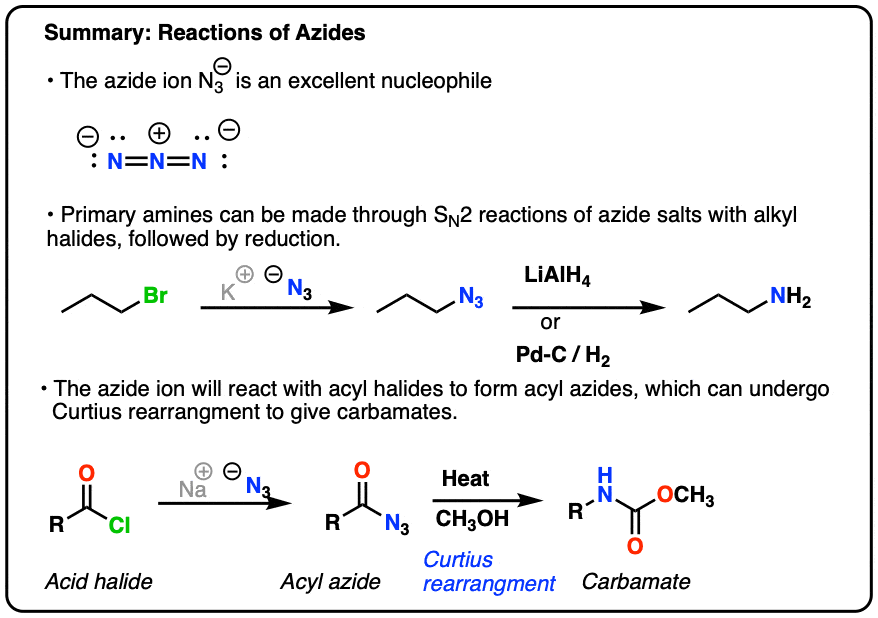
1。叠氮化离子是一个伟大的亲核试剂的年代N2反应
的叠氮化离子(N3- - - - - -)是一种化学实体,相貌平平奇怪。

- 连续三氮吗?检查
- 两个负电荷和正电荷,净电荷的1 ?检查
- 稳定吗?检查(只要是温柔地对待)。
事实证明,叠氮化离子能形成碳氮键的非常有用的亲核取代反应。
叠氮化离子是共轭碱叠氮酸、环3。尽管只有弱碱性(pK一个接下来的3只有4.6)N3是一个非常好的亲核试剂——根据一项措施,比任何更亲核胺(看到帖子:胺的亲核性)。不难解释这可能是当你停止去想它。有四个亲核孤局限于一个很小的体积,一个碰撞的可能性亲电试剂结果在一个反应是远远高于一个胺与笨重烷基组,举个例子。
你能想到的N3- - - - - -精益,意思是,nitrogen-tipped导弹将其负载到碳迅速,高效,没有明显的副反应。
在年代N2反应,主要和次要烷基流离失所的卤化物和磺酸盐很容易N3- - - - - -,导致烷基叠氮化:
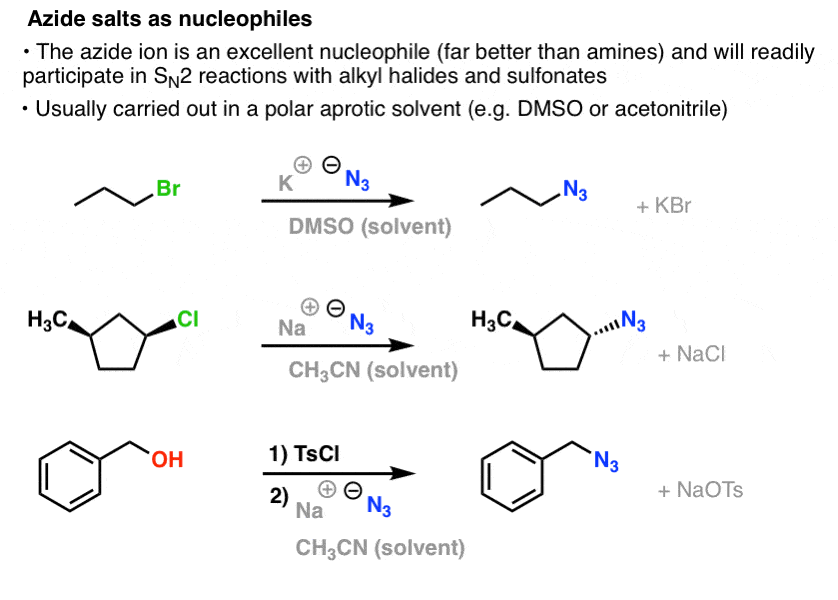
通常的程序是使用叠氮化盐,如南3或KN3用适当的烷基卤化物在极性非质子溶剂等乙腈(CH3CN)或二甲亚砜(DMSO溶液)。
叠氮化有机产品是相当稳定的,即使他们看起来有点奇怪。一些人甚至发现使用药品(例如AZT,低于右)或有用的调查研究化学生物学。(注1]。
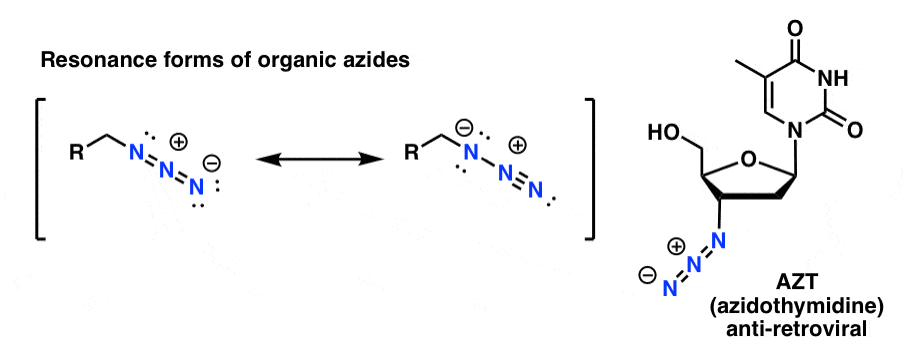
有机叠氮化物的对我们来说最有用的特性是他们作为“蒙面”胺。
2。有机叠氮化“蒙面胺”
注意上面的共振形成一个氮与氮之间的三键。如果处理还原剂,如LiAlH4甚至催化加氢(Pd / C, H2)可以减少有机叠氮化物主要胺,解放N2在这个过程中。
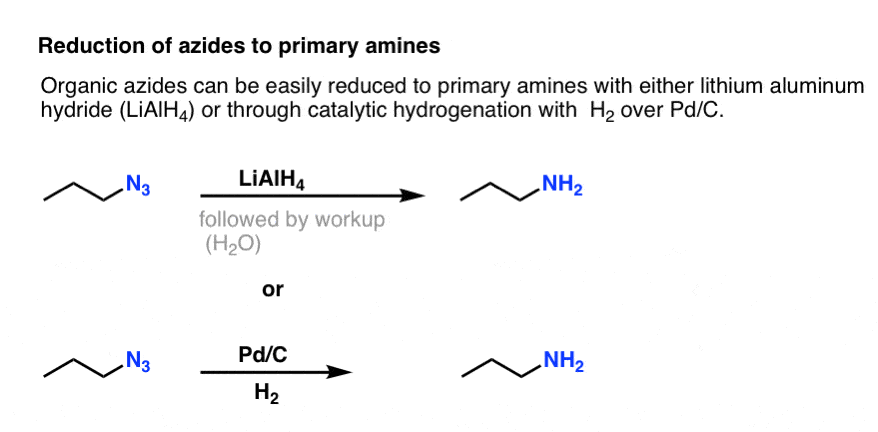
之前我们已经探讨了加布里埃尔合成作为主要的路线胺(看到帖子:加布里埃尔合成叠氮化),但是这条路是优越的,因为可以减少的胺在温和的条件下(如加氢)。这些高温的乳沟phthalimide肼可担心的。
我们也看到,使主胺通过直接的治疗烷基卤化物与NH3通常不会导致所需产品,因为胺有多次Cookie-Monster-like趋势做出反应烷基卤化物:自胺产品往往比反应物更亲核的,很难得到的胺在咀嚼烷基卤化物。(看到帖子:胺的烷基化]
3所示。在发射台爆炸
如果N3是一个“nitrogen-tipped导弹”,正如我们以上评论,值得回忆当导弹不小心处理:它本质上是一个炸弹。
南3和KN3是白色粉末,可以无限期地存储在室温和舀出在板凳上了。
但是,当加热或受到冲击bdapp平台一切都不一样了。同样暴露这些叠氮化盐酸,形成潜在的爆炸接下来的3。
和南3和KN3是不错的叠氮化!如果混合金属盐的铅、汞、镉、锌、银、或者更爆炸性叠氮化物化合物的结果。这些金属叠氮化物接触爆炸物,其中一些非常敏感的,他们会引爆如果有人放屁20英尺大厅。一些疯狂的化学家甚至让这些事情故意,但我们不会旅行接近爆炸半径的主题随时在这个博客上,。
南3和KN3应在合理使用稀释浓度,制备规模的爆炸盾后面,顺便和从不使用CH2Cl2溶剂,从而导致爆炸diazidomethane。
现在,有的时候突然爆炸氮气是有用的——而且可能挽救。你可能已经花了你一天的一部分接近叠氮化钠而不自知。这是因为南3是为数不多的几个推进剂发现使用在安全气囊;一旦触发一个加速度计,引爆NaN3分别由N2天然气超过每小时200英里,充气袋的1/25秒。(注3)
叠氮化盐,太棒了!
(但不要这个人):
底线:年代N2之间的反应烷基卤化物或与叠氮化磺酸盐合成主要可能是最好的方法胺从烷基卤化物。这总比加布里埃尔合成。
4所示。亲核酰取代与叠氮化盐使酰基叠氮化
的年代N2反应并不是唯一的取代反应我们探索。也有亲核酰替换。一个羰基附加到一个好的离去基团(如一个酰氯或酸酐)一个适当时将进行替换亲核试剂是补充道。
在第一步的机制亲核试剂(ν)攻击羰基碳,形成C-Nu和打破切断(π)。这产生了一个四面体中间。在第二步中,切断π键生成,和碳- (离去基团)键坏了,导致亲核酰替换产品。
这是一个亲核酰的例子取代反应酰氯与N3离子给一个酰基叠氮化:
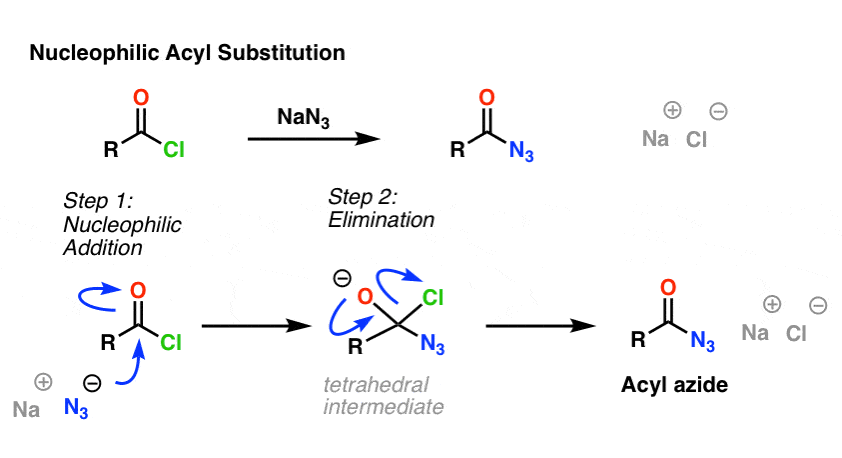
5。重排的酰基叠氮化:库尔修斯重排
酰基叠氮化的最常见的用途是,加热后,他们重新安排给异氰酸酯的反应称为库尔修斯重排。(看到帖子:霍夫曼和库尔修斯重组]
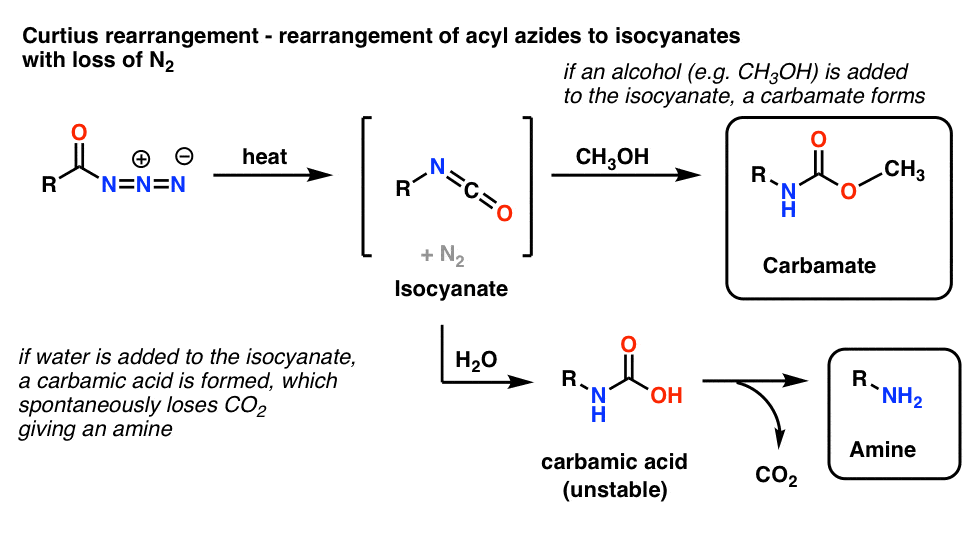
为什么这是有用的呢?这是方法之一。
有很多方法使芳香族羧酸,但不是那么多伟大的芳香环上形成碳氮键的方法。说你有苯甲酸(如p-methylbenzoic酸),但需要形成芳香(保护)胺。库尔修斯协议代表了一个很好的方式形成新的碳氮键的环,而无需求助于硝化+减少。
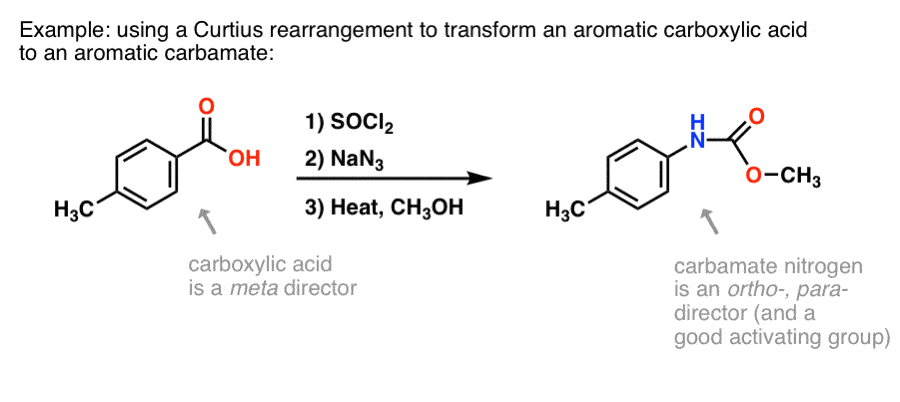
(以这种方式有点类似于一个等效的氮Baeyer-Villiger氧化)。
6。叠氮化的亲核试剂的例子:环氧打开和共轭加成
叠氮化离子的两个应用程序亲核试剂包括开幕式环氧化合物(在本质上是一个年代N2过程——注意反转配置)和共轭加成在α,β不饱和酮:
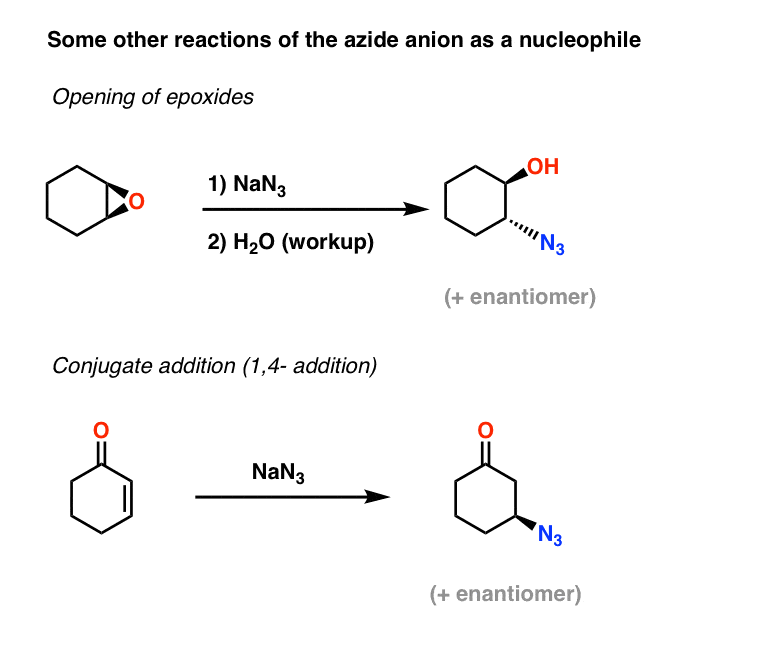
笔记
注意1.叠氮化-炔烃环加,或者说“点击”化学
有机叠氮化的一个有趣的和有用的应用程序,还没有进入介绍有机化学教材(但可能会在不久的将来)是一个过程在技术上被称为“copper-catalyzed azide-alkyne环加成作用”,但更常见的是被称为“炔烃叠氮化点击反应”。
当一个终端炔烃对待一个铜催化剂在有机叠氮化物的存在,环加成作用迅速的结果,形成一个1,2,3-triazole。
我们不会深入细节,但这种措施反应涉及6π电子的表兄Diels-Alder反应(nitpckers将正确地指出,copper-catalyzed版本不是技术一致的过程,但是non-catalyzed版本)
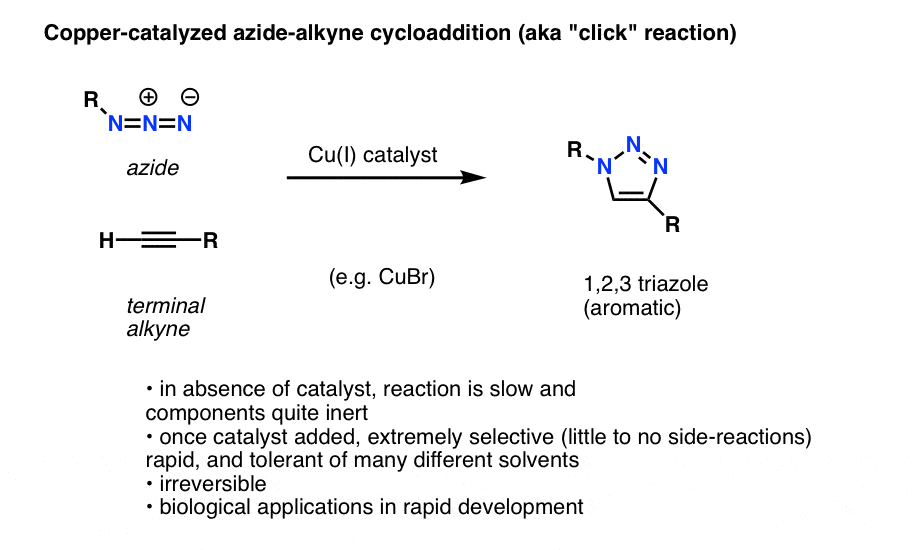
的反应是值得注意的几个原因:
- 反应性伙伴(终端炔烃和有机叠氮化物)相对惰性在缺乏催化剂在大多数情况下。
- 一旦添加铜,反应非常迅速在温和的条件下,发生在各种溶剂(包括水)。
- 这是非常有选择性的在这种情况下,炔烃叠氮化和合作伙伴只有相互反应,不可逆转。
- 产品、三唑环芳香族和稳定
这是被称为“点击“反应其发起者之一,夏普,因为它是最接近的事情之一化学家有反应,就像光滑的“点击”两个免费乐高积木。
什么使得这个反应特别有用的是叠氮化和迟到了炔烃合作伙伴可以安装在分子生物学的兴趣,和“点击”在一起。
例如:
- 把一个乙炔的5′位置的叠氮化糖和3′位置已被用来制造“点击”DNA,三唑取代了有机磷的地方。(链接]
- 难以置信的是,一组“点击”DNA,把它放到人类细胞,并设法得到它通过信使RNA转录。(链接]
- azide-containing AZT(上图)掉了转录机器。一些聪明的人发现了一种方法应用叠氮化-炔烃点击向快速基因组测序反应,称为ClickSeq的技术。(一个非常可读的账户,礼貌的在管道]
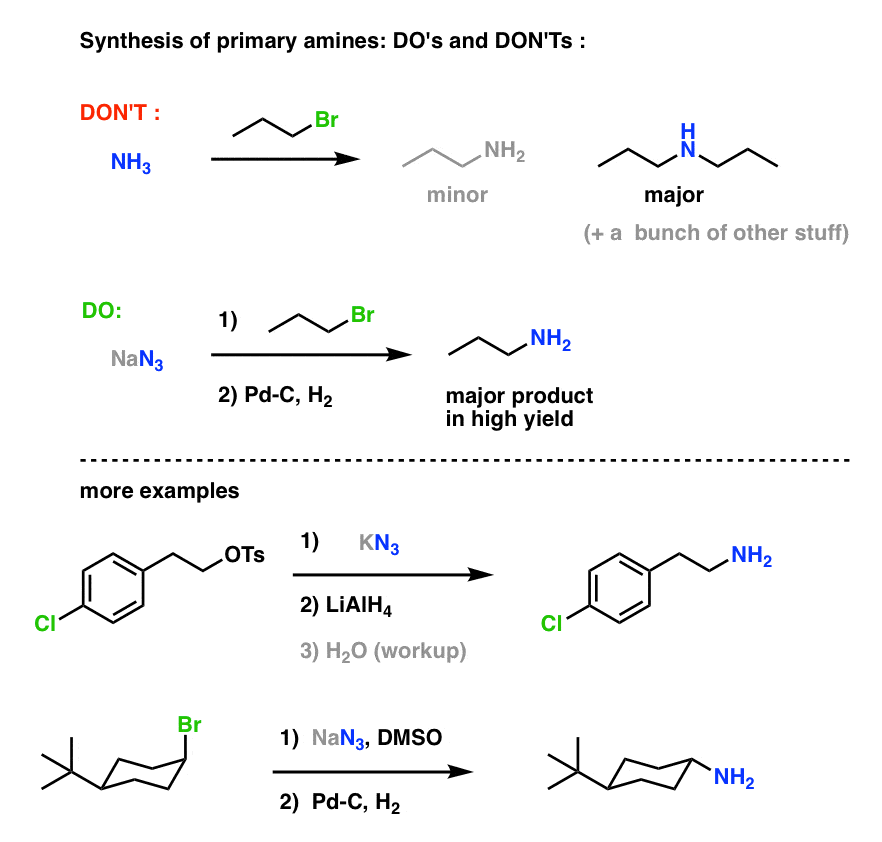
,注2。主胺合成“守则”:
注3。中国人在1990年代早期使用叠氮化钠,然后搬到四唑铵硝酸。
铵硝酸是十分之一的价格四唑,阿帕姆,也回顾了产业专利。但铵硝酸有一个重要的缺陷,他说让其他空气袋制造商放弃:铵硝酸不同密度的五个阶段,很难保持稳定。一个推进剂用铵硝酸将膨胀和收缩与温度变化,平板电脑最终会分解成粉末。水和湿度会加速这个过程。粉燃烧比平板电脑更快,所以一个气囊的推进剂崩溃可能会部署太积极。控制爆炸就发生爆炸。“每个人都下降一定的道路,只有中国人走另一条路,”约亨•Siebert说关注气囊行业自1990年代以来,现在JSC汽车咨询董事总经理。“如果你读的会议论文,你可以看到人们说,“不,你不能。是很危险的。”
弹片从错误的全球安全气囊已造成13人死亡,和超过100人受伤。
2017年6月25日,面临超过110亿美元的债务,中国人申请破产。
(高级)引用和进一步阅读
叠氮化是有用的在有机合成、叠氮化化学的一大亮点是下面的引用。
- 亲核的叠氮化反应的离子在不同的溶剂
Thanh Binh表象,赫伯特·迈尔
理论物理。Org。化学。2006年,19(11),706 - 713
DOI:10.1002 / poc.1063
教授赫伯特·迈尔(LMU,慕尼黑,德国)花了他职业生涯的贡献量化的基本物理有机化学亲电性和亲核性和发展规模,比较不同的亲核试剂的反应性与亲电试剂。 - 的SN2位移在2-norbornyl brosylates
克劳斯Banert和沃尔夫冈Kirmse
美国化学学会杂志》上1982年,104年(13),3766 - 3767
DOI:1021 / ja00377a057 - 一种改进的合成叠氮胸苷
即Balagopala, a . p . Ollapally & h·j·李
核苷、核苷酸和核酸1996年,4,899 - 906
DOI:10.1080 / 07328319608002136
叠氮化可以作为亲核试剂的年代N2反应。Ref。# 3显示了使用叠氮化离子的合成AZT(叠氮胸苷)。的转换1来5通过3ref。# 3使用Mitsunobu反应,它允许位移的一群-哦亲核试剂反演的配置。 - 减少有机叠氮化物为主胺用氢化铝锂
h·波伊尔
美国化学学会杂志》上1951年,73年(12),5865 - 5866
DOI:10.1021 / ja01156a507
减少有机叠氮化物为主胺是一种方便的方法,主要的合成胺,否则很难合成选择性的标准方法。 - 金属叠氮化物的爆炸敏感性的影响
p·g·福克斯
j .固态化学。1970年,2(4),491 - 502
DOI:10.1016 / 0022 - 4596 (70)90043 - 5
调查南的冲击敏感性3,TlN3和Pb (N3)2。 - 库尔修斯的反应
史密斯,p . a S。反应。1946年,3,336年
DOI:10.1002/0471264180. or003.09
老库尔修斯反应但全面审查,其中包括发现的历史重排,底物范围,限制,相比其他类似的反应,和实验过程。 - 合成方法和反应。121年。碘化锌催化制备芳酰基叠氮化与芳酰基叠氮化氯化物和三甲基硅烷基
k·苏利耶普拉卡什,Pradeep s艾耶马苏德Arvanaghi,和乔治·a . Olah
《有机化学》杂志上1983年48(19),3358 - 3359
DOI:10.1021 / jo00167a051b
一个方便的程序准备芳香从诺贝尔奖得主乔治·A·Olah教授芳基叠氮化。这些可以用于库尔修斯重组。
环氧开放和共轭加成:
- 环己烯亚胺(7-AZA-BICYCLO[4.1.0]庚烷)
伊恩·d·g·沃森,尼古拉斯Afagh和安德烈·k·yudi
Org。Synth。2010年,87年,161 - 169
DOI:10.15227 / orgsyn.087.0161
这是一个特别有用的程序,因为它是将环氧化合物转化为NH-aziridines施陶丁格反应(环氧化合物的氮模拟)。合成可能会非常棘手,但提供了更多的细节在这里可以复制,拟合的一种程序有机合成。 - 胺叠氮化催化添加离子α,β-Unsaturated羰基化合物
David j . Guerin Thomas e . Horstmann和斯科特·j·米勒
有机的信1999年,1(7),1107 - 1109
DOI:10.1021 / ol9909076
这篇文章很有趣,因为它代表了早期的形式organocatalysis,可能是通过亚胺或收益iminium离子中间。不幸的是没有使用这个词在本文——这些作者可以击败了麦克米伦教授下手! - 点击化学:多元化的化学功能从几好反应
Hartmuth c·m·g·芬恩博士科尔布教授巴里•沙普利斯教授。
Angew化学。Int。。2001年,40(11),2004 - 2021
DOI:10.1002 / 1521 - 3773(20010601)赛40:11 < 2004::AID-ANIE2004 > 3.0.CO; 2 - 5
Cu-catalyzed环加成反应的叠氮化炔烃被称为“点击”反应由诺贝尔奖得主教授k·夏普(斯克里普斯研究所的拉霍亚,CA)由于其简单性,高产量,快速动力学、兼容性范围广泛的条件和基质。如果紧张Cu-free反应也是可行的炔烃使用(如cyclooctynes)。
谢谢你解释氯或酸酐可能导致替换发生并创建酰基叠氮化。既然你提到它,我想了解不同的应用程序为氯化物和酐作为供应链性能的化学物质的过程。有意思的是读你的文章,了解更多关于叠氮化化学反应,所以感谢分享!
非常感谢这些有用的信息。特别是新合成方法和危险。
很高兴这是有用的吉恩·克劳德。
很好,谢谢你给简要回顾叠氮化反应