置换反应
极性质子?极性非质子?非极性吗?关于溶剂
最后更新:2022年12月6日|
极性质子与极性非质子与非极性:在有机化学溶剂
我交谈过的很多学生对溶剂有问题。
在反应溶剂会导致相当大的混乱,因为他们上市的试剂反应,但通常不参与反应本身。老实说,很多教师(包括我自己)都不到一致时,包括溶剂和不的时候出现。所以整个运动能遇到有些武断的:当你知道包括溶剂吗?
表的内容
1。溶剂是什么?
让我们后退。溶剂是什么?
溶剂是液体作为反应介质。它可以用于两个主要目的:
- (Non-participatory)解散反应物。还记得“像溶解”吗?极性溶剂最适合溶解极性反应物(如离子);非极性溶剂最好溶解非极性反应物(如碳氢化合物)。
- 参与:之源酸(质子),基地(删除质子),或作为亲核试剂(捐赠一个孤对电子)。唯一的溶剂类这是你通常需要担心极性质子溶剂(见下文)。
2。极性溶剂有大的偶极矩。非极性溶剂有小或偶极矩为零
好的。所以“极地”和“极性”是什么意思?
- 极性溶剂有大的偶极矩(又名“部分费用”);它们包含债券之间的原子有不同的电负性,如氧和氢。
- 非极性溶剂包含债券原子之间类似的电负性,如碳和氢(认为碳氢化合物,如汽油)。原子之间的债券和类似的电负性缺乏部分费用;这没有使这些分子“极性”。
有两个直接测量极性的方法。一个是通过测量一个常数称为“介电常数电容率。介电常数越大,极性越大(水=高,汽油=低)。第二个来自直接测量偶极矩。
极性是一个连续体。虽然我们都同意戊烷是“极性”,和水是“两极”,有边缘案例如乙醚、二氯甲烷、四氢呋喃(四氢呋喃)有极性和非极性的特点。在紧要关头,一个好的经验法则分界线“极地”和“极性”是与水混溶。乙醚和二氯甲烷不与水混合;乙腈,四氢呋喃,DMSO DMF、丙酮和短链醇。
3所示。“质子”溶剂地或氮氢键和能与自己形成氢键。“非质子溶剂不能氢键捐助者
有一个最后的区别,这也会造成混乱。一些溶剂被称为“质子”,被称为“质子”。是什么让“质子”溶剂,溶剂呢?
- 质子溶剂地或氮氢键。为什么这个很重要?因为质子溶剂可以参与氢键,这是一个强大的分子间作用力。此外,这些地或氮氢键可以作为质子(氢离子)的来源。
- 非质子溶剂可能有氢的某个地方,但他们缺乏地或氮氢键,因此不能氢键与自己。
4所示。非极性的年代olvents几乎没有偶极矩
这些溶剂介电常数较低(< 5)和没有良好溶剂指控物种如阴离子。然而乙醚(等2O)是一种常见的格氏反应的溶剂;其孤刘易斯基本和可以帮助Mg阳离子溶剂合物。
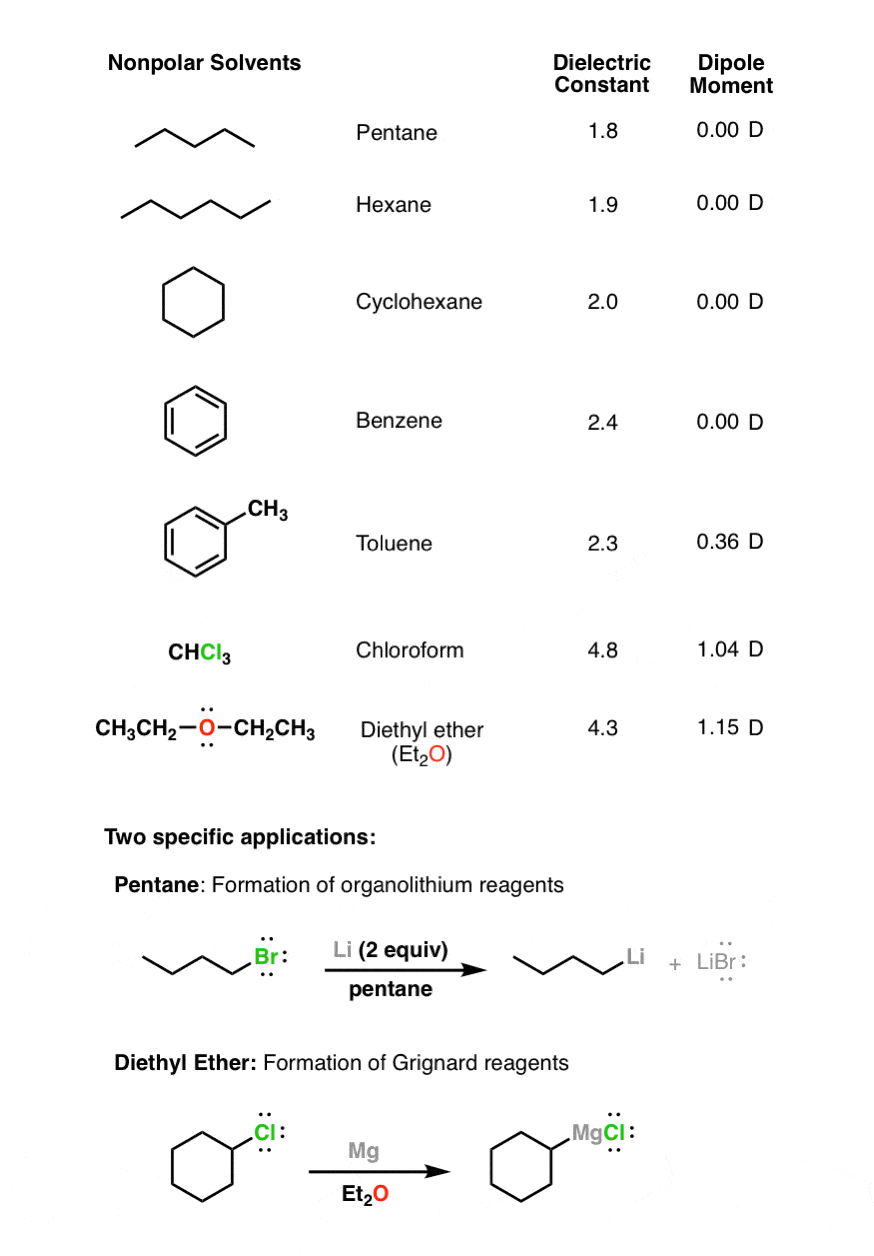
5。“边缘”极性非质子溶剂有小偶极矩和低(< 10)介电常数
这些溶剂介电常数适度高于非极性溶剂(5 - 20)。因为他们中间极性的好“通用”溶剂广泛的反应。“质子”,因为他们缺乏地或氮氢键。对我们来说他们不参与反应:他们只作为媒介。
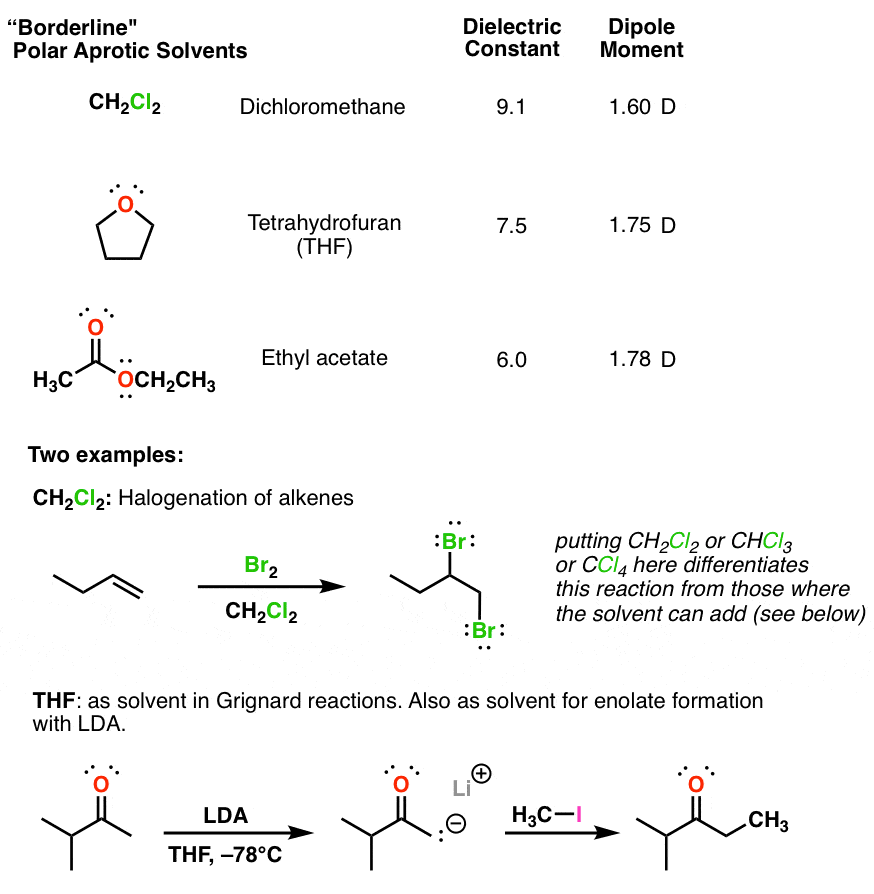
6。四个关键极性非质子溶剂与大(> 10)介电常数
这些溶剂都有大的介电常数(> 20)和大的偶极矩,但他们不参与氢键(无地或氮氢键)。高极性允许他们解散指控物种(如各种阴离子作为亲核试剂(例如CN(-),(-),等等)。氢键的缺乏意味着这些溶剂的亲核试剂是相对“自由”的解决方案,使他们更被动。对我们来说这些溶剂不参与反应。
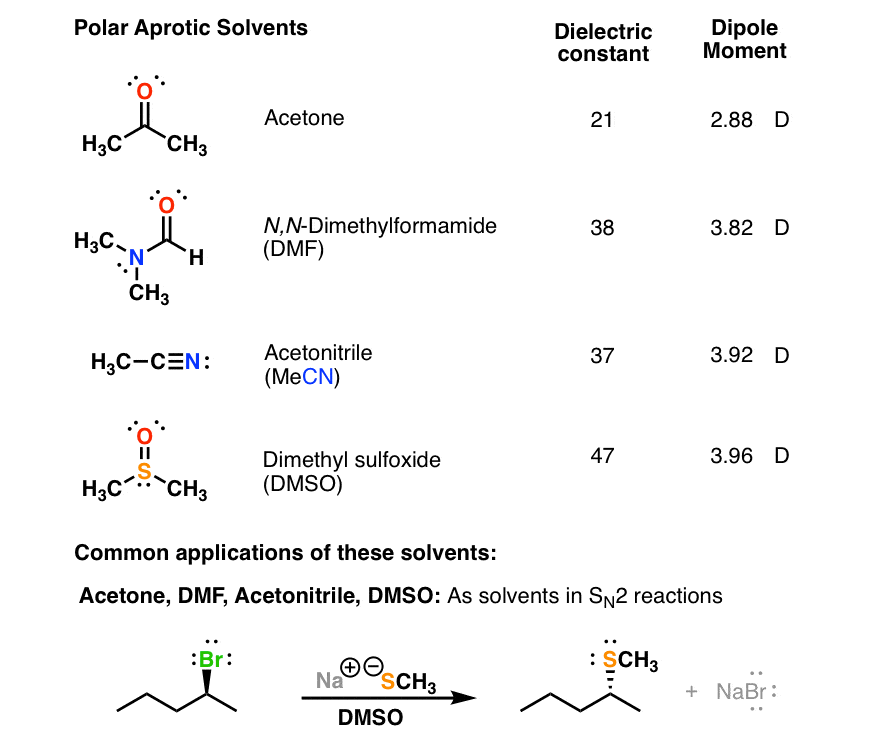
7所示。极性质子溶剂:一个表
极性质子溶剂往往有高介电常数、高偶极矩。此外,因为他们拥有地或氮氢键,他们还可以参与氢键。这些溶剂也可以作为酸(质子来源)和弱的亲核试剂与强大的亲电试剂(形成债券)。
他们最常用的溶剂共轭基地。(如H2O是用作HO溶剂(-);EtOH用作溶剂环氧乙烷(-))。
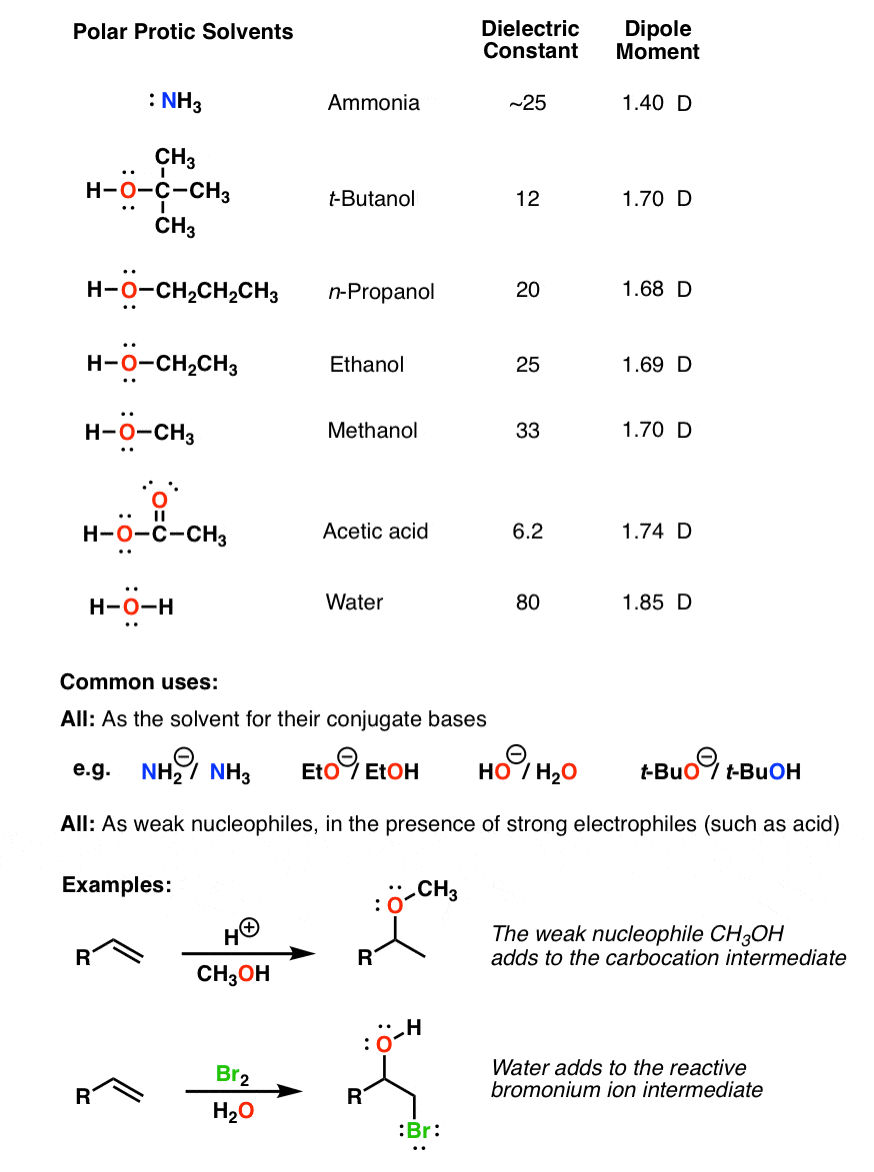
这些类型的溶剂是目前最可能参与反应。有许多例子(太多的列表),水等极性质子溶剂,甲醇,乙醇或可以作为亲核试剂的反应,通常当一个强大的亲电试剂(如酸)。所以如果你看到这种类型的溶剂,注意。
数据来源:维基百科
是的,我的意思是如何物理上独立的实验室
谢谢
我们用分液漏斗。极性和非极性溶剂通常不混合。
2022年11月24日
如何分离极性溶剂与非极性溶剂
你的意思是单独的在物理上独立的实验室,或者你的意思是单独的在“区分”?
最重要的差异区分极性溶剂:寻找地债券,因为他们将有氢键(O比H和将会有更多的电负性很大部分负电荷在氧气和氢很大部分正电荷)。第二个最重要的区别:寻找债券,那里是一个大型的电负性的差异,如C = O在丙酮和DMF, S = O在DMSO, CN在乙腈。
非极性溶剂(碳氢化合物)只有碳氢键。
关键测量寻找所谓的“介电常数”,这是大,极性分子和非极性小分子。
这是非常有利于清晰地理解. .谢谢你
嗯,我想我有一些贡献的偶极矩DCM和氯仿。问题是,这两个是四面体的结构与键角= cos-1(-0.33) = 109.5度。现在,如果你有一些想法关于向量,然后你会意识到,四个向量保持在这个角度给净= 0。但是很有趣的是,三个这样的向量的合成等于其中一个向量,只是方向相反。所以,在氯仿中,三个cl实际上导致偶极矩,就好像它是一个cl。然而,在DCM的情况下,这两个cl贡献,如果有2 cos(54.9度)cl = 1.15 cl
总之,使用向量代数:
在CHCl3 =偶极子eqv。1 cl
在以结构=偶极子eqv。1.15 cl
伟大的评论。非常感谢。应该想到这一点。
溶剂与氨基或NHC更糟吗?
NHC吗?
我有一个疑问:
当极性质子溶剂作为溶剂的共轭碱,共轭碱将最强的基地/亲核试剂,溶剂吗?
谢谢!
我在看己烷中的各种溶质的溶解度。己烷是极性应该溶解非极性溶质但我相信乙酸乙酯是极地但在己烷混相。你能帮助我了解这是为什么?
乙酸乙酯极性比己烷,但与其说这是与水混相。这是一个极性有机溶剂。
嗨,这真的帮助我的科学展览项目。非常感谢! ! ?
好的!谢谢Malak。
所以非常有帮助。谢谢你花时间来开发和发布!
好的,谢谢伊莎贝拉。高兴是很有用的。
你好,请我有一个问题:
关于离子的溶剂化作用;为什么水溶解K +离子例如甲醇多吗?
鉴于:稳定常数K +复杂的水溶剂是100,而在甲醇溶剂就1000,000
所以有更多的从水中溶解效应导致减少复杂的形成
(超分子化学课)
所以它是正确的说,极性质子溶剂SN1反应形成稳定的碳正离子,极性非质子溶剂溶剂合物不亲核试剂的SN2反应从而维护其有效性?做极性质子溶剂溶剂化物SN1的亲核试剂,如果是这样,为什么这是重要的?
为什么F -氢键与极性质子溶剂比我- ?
看看氢氟键债券(135千卡每摩尔)远强于设定h债券(70千卡每摩尔)。负电荷更集中在F。
教授,
你知道在哪里找到信息有机极性溶剂的电击穿电压吗?
这是唯一科学的信息我无法找到在50多年的独立研究中,假设我知道我正在寻找. .
谢谢你!
最好的问候,
吉姆Andrakin
好问题吉姆。在这里我没有任何特殊的洞察力。
你好,
我猜你终于向我解释这一趋势我观察不知道为什么。我也经常遇到这样的情况,人们会使用一个acid-alcohol作为溶剂(如HCl-EtOH)解决方案。
如果我得到你的句子:“有许多例子(太多的列表),水等极性质子溶剂,甲醇,乙醇或可以作为亲核试剂的反应,通常当一个强大的亲电试剂(如酸)是礼物。”
然后使用一个acid-alcohol混合物作为亲核试剂溶剂允许在环境稳定溶解离子的某些更低的价。这是在HCl-EtOH代替盐酸的好处吗?
经常发生的是,酸会使质子化一个酒精和把它变成好的离去基团(R-OH2 +)。后损失的水溶剂可以作为亲核试剂。
将DMSO溶剂极性aprotric仍然能够氢交换?
说我想测量红外或氘DMSO VCD的葡萄糖,我能够这样做,而不必担心氢交换?否则我将不得不首先氘哦债券形式葡萄糖。
氘DMSO不会交换质子哦组的葡萄糖。氘都附着在碳。
如何决定是否在反应中使用的溶剂能参与一个或一个non-participatory ? ?
大多数时候,参与式溶剂将地债券可以deprotonated后作为亲核试剂。
不错的讨论。丁醇是极性(我的意思是,它可溶于水)。
你怎么把ff的顺序与增加极性溶剂(乙醚、丁醇、氯仿和乙酸乙酯)
如果你搜索“水溶解度”所有你提到的溶剂,你会发现丁醇是最比他们都溶于水。它是迄今为止最极性的。
为什么丁基纤维素溶剂与水混相? ?
谢谢你!但是如何确定哪些物种将作为neucleophile吗?溶剂或其他neucleophile ?
如果你有一个非常被动的亲电试剂像碳正离子,和溶剂,可以与碳正离子反应水或醇等溶剂将出现在巨大的过剩相对于其他亲核试剂。所以基于浓度,人们会预计溶剂作为亲核试剂反应。
如何比较有2极性质子溶剂的强度吗?
介电常数是一个很好的指南。
二苯醚是极性?或极?
它在室温下是固体。不是最实用的溶剂。
丙二醇是什么?甘油怎么样?
极性质子。丙二醇羟基。
我有一个问题。为什么极性质子溶剂异丙醇与环己烷和乙腈混相,但环己烷和乙腈混相吗?更普遍的是,我明白了为什么“像溶解极性质子和极性非质子交互,但是为什么会有一个非极性相互作用环己烷和极性质子溶剂异丙醇,但是没有反应(nonmiscible)环己烷非极性和极性非质子之间的乙腈吗?
谢谢!
记得乙腈有N原子所以h N分子间的相互作用是可能的,因此氢键。规则是帮助完成一个特定的推理但他们开发不解释的东西是如何工作的,而是来简化我们思考如何解决问题。极性非质子溶剂的根本原因可以和封装离子周围的Sn2反应是因为氢键可以用离子在溶液中互动很好。只要1 HCN可以对齐,这样O原子分子在异丙醇在HCN和H原子附近亦然异丙醇N原子HCN和H原子之间的氢键是溶剂化作用的主要驱动力,因此混溶。
希望这个有帮助。
感谢您使非极性溶剂更清楚。现在更多的意义后,看着你列出的所有化合物。所以非极性溶剂通常不会有氢键吗?看着氯仿后,溶剂极性因为电荷必须均匀地分散在三个氯原子,对吧?
嘿,卢克-
“极性”是一个连续体。测量极性的方法之一是通过一个称为“介电常数”。水有很高的介电常数,而非极性溶剂如己烷具有非常低的介电常数。
对我来说,一个有用的“硬线”对极性溶剂是否与水混相,如甲醇,乙醇,DMSO, DMF,四氢呋喃,都与水可溶混的,相当“极”。
溶剂如乙醚、己烷、二氯甲烷、氯仿,不溶于水的,通常被划分为“无极”。是的,你是正确的指出其中的非溶剂氢键。
这并不是说,没有一些极地方面一些溶剂——例如氯仿有偶极矩,乙醚一样,所以他们比,极地说,戊烷。
我希望这有助于一点!詹姆斯
你好,
我现在反应有点毛病,我希望你能帮助我。有什么方法,水解反应可以在其他溶剂proctic执行?我一直在与丙二醇或甘油,但他们似乎不工作以及水。
由于先进的!
丙二醇,甘油是质子。
嗨,詹姆斯!
首先,恭喜你的网站!太棒了,非常经验。
我需要一些帮助你应用这一概念解释道。我不是一个化学家,但是我需要这些知识在有机化学液相色谱(UFLC-MS / MS)使用C18 quanitfy原花青素(极性化合物)硅习题答案。年长的出版物提到甲醇+酸化什么作为流动相,最新的使用乙腈+水酸化。专业材料建议替代的乙腈甲醇由于成本降低,对于我来说,我只有随着年级女士metanol作为高效液相色谱级(ACN)。两者都是极地但ACN极性非质子和metanol极性质子。虽然他们的介电常数非常相似(也许这就是为什么一些研究者建议更换),我应该期待一个巨大的差异在量化由于可能的结合使用甲醇?
瓶子为什么氯仿保存在琥珀的颜色?
使用琥珀瓶减少任何光化学降解的机会,可随着时间的推移发生。
嗨
如何轻松地找出极性质子和极性非质子?
它有一个哦任何地方或NH组吗?如果是这样,这是极性质子。
詹姆斯博士和其他人,
你能解释一下如何助溶剂的工作吗?如xylene-methanol或xylene-DMSO在特定的比率?你有任何引用混合溶剂是如何工作的以及如何确定他们的比率?
和二甲基甲酰胺是偶氮二异丁腈高度可溶吗?如果你把这些,然后添加聚苯乙烯,将化合物溶解聚苯乙烯?
AIBN溶于DMF,是的。这是一个自由基引发剂。我认为你描述的反应是聚苯乙烯苯乙烯自由基聚合的形式。
有时两相溶剂使用e。g四氢呋喃/水。为什么会出现这样的情况?
四氢呋喃和水是混相。这是一个有用的溶剂系统当你想使用水溶性试剂,像LiOH有机分子的存在。例如hydroylsis酯通常做在1:1四氢呋喃/水
链接…http://chemwiki.ucdavis.edu/Organic_Chemistry/Reactions/Substitution_Reactions/SN2/Nucleophile
你怎么能确定极性与非极性溶剂?
我想知道乙二醇的极性?极性或非极性溶剂吗?乙二醇的介电常数是什么?
有人知道这些吗?
请帮我在这. .谢谢
乙二醇是一种极性质子溶剂,因为它哦。根据这个网站,乙二醇的介电常数为37.0。https://www.engineeringtoolbox.com/liquid-dielectric-constants-d_1263.html
方法使用删除所dimethayl甲酰胺?
使用的方法史密瑟斯,穆南加。https://www.chem.tamu.edu/rgroup/gladysz/documents/nmr6.pdf
这将为更好的SN2机制?水或哦?有极性质子和为这种类型的机制不是最好的吗?那么他们在反应的速率相等。
更好的作为亲核试剂吗?HO -因为这是一个更强的亲核试剂。溶剂的选择最好是乙腈或DMF或其他极性非质子溶剂如果你想促进SN2。
当用金属钠治疗碘甲烷,乙烷,形成反应发生在醚作为溶剂! ! ! ! ! ! !为什么会这样? ? ? ?
嗯,这可能是几种不同的方式发生,但一个途径是还原形成甲基阴离子替代紧随其后。另一个是甲基的形成和随后的耦合的两个自由基(终止)。维尔茨耦合。不是一个非常高产的反应
最激进的合成溶剂是什么?
碳春节是伟大的,如果你能找到它。漂亮的高沸点。
精制的产品曾经向我描述“solvent-solvent”。
詹姆斯博士,你能开导我什么这可能意味着其溶解能力的各种类型的化学堵塞?
谢谢,
罗伊
詹姆斯,你能解释一下为什么哈佛商业评论的烯烃不使用烯烃的极地,质子溶剂?为什么质子?
对不起,没有使用过氧化物。
嗨罗杰-免费的速率限制步骤将形成碳正离子。速度将会提高如果我们使用溶剂具有高介电常数(即极性)。溶剂介电常数高的也往往是极性质子溶剂(如甲醇)。然而,哈佛商业评论极性质子溶剂并不是一个要求。
我会谨慎使用极性质子溶剂,因为它可以作为亲核试剂,捕获的碳正离子。
这是一个例子,二氯甲烷作为溶剂:
http://www.orgsyn.org/Result.aspx?ga=na
我3月的先进典型有机化学没有提到溶剂HX加法。
四氢呋喃也适合格氏反应的溶剂
如此的感谢! !你岩:)。
乙醚是极!!!
它比碳氢化合物极性,但仍与水不混相。因此我将它作为一个非极性溶剂。
这是我超级浓密的更好然后vollhardt课本>。<非常感谢!
有人能显示材料的抗蜡(碳氢化合物)? ?
使用极性质子溶剂增加反应速率的对吧?嗯,我想知道如何使用1型或2型?
请告诉我为什么sn1反应发生在辕马溶剂和sn2反应发生在非辕马溶剂
我认为这是因为sn1由偶极稳定的碳正离子与溶剂的相互作用。在非极性非质子溶剂,sn2反应更好,因为亲核试剂并不妨碍了偶极子与溶剂的相互作用,可以攻击碳更容易。
哦”在极性非质子溶剂,sn2反应…”
我需要睡眠。学习了一整天
氯仿不是一个非极性溶剂。这是极性的。
你似乎很有信心。氯仿和水混合吗?:-)
记住,极性/非极性是一个连续体。
你好,
据我所知,Hexafluoroisopropanol (HFIP)为聚合物是一种很好的溶剂,即使它是极性质子溶剂。
但凭直觉我不明白它是如何工作的。
请帮我解释一下。谢谢你!
HFIP我所知的最好的特性是可以溶解极性在极性分子的非极性分子或极性。我用它制作聚酯和蛋白质之间的聚合物混合。但我不知道它是如何工作的,因为我是一个生物学家,化学家。如果有人知道,请给我一些解释。
干杯
嗨
请告诉我为什么不甲基转移bt methanide写道。然而CH3轴承负像苯charg一些其他的例子。
嗨
是极性的导电性变化如何?如果电压高,极性非质子溶剂可以电解?
我有一个问题关于醋酸的低介电常数。相比其他极性质子溶剂的介电电荷很低但当做同样的比较它的偶极矩是极高。这是为什么呢?
伦大问题。如果你看这一趋势在上面的表中注意到有两个O的醋酸,剩下的只有一个或一个N原子。偶极矩低因为HO和公司债券之间的流离失所的指控在乙酸可以抑制或稳定生成的部分费用。一个偶极子向量点远离对O H和另一点远离对O . C和- HO的向量是积极的公司最近向量因此感生电荷的抑制。
至于高偶极矩,记住(我必须看这个,哈哈)u = E r * q *,
在哪里
u =偶极矩向量
E =一个总和
q =级的指控
r =净电荷的向量
这将导致费用之和的结论,问在醋酸包含两个高度原子的电负性比问小醇中只包含一个高度electroneative原子。因此,较大的偶极矩在醋酸但较小的水这是偶极子向量是对齐的方式增加了向量的大小和结果在高1.80 d。
希望这个有帮助。
我所知道的是,这一切都取决于你想要的内容的极性溶剂。如果你想运行一个极性的内容,运行它的极性溶剂的极性是确定的交互。所以极极性和非极性非极性。
这是最有效的运行之间的溶剂极性和非极性溶剂,为什么?
这是一个很难回答的问题但没有具体指明。
你能明确你想要运行的溶剂
的例子使用的溶剂是什么我需要帮助的时候,确实是很有帮助的。那些将感兴趣区域扩大。谢谢你!
当溴也加入氯仿和溴加入二氯甲烷吗?
我相信你的引用是一个“溴测试”涉嫌饱和碳氢化合物。如果添加溴氯仿,我相信溴应该保持双原子元素的颜色因为氯仿是饱和,因此不会反应,它应该与DCM相同的反应。
詹姆斯,你的工作关于这个主题(溶剂)非常惊人。许多学生感到困惑的质子溶剂/非质子极性/非极性。很棒的工作。谢谢你!你的帽子。
一些观察:
——第五段:“用极性溶剂溶解指控物种(如氢氧化钠),但不要用它来溶解”(这里的句子结束)-溶解什么?
——段落在极性非质子溶剂,最后一句话:“对我们来说这些溶剂不参与反应”——点失踪的最后一句话
-以上反应极性质子溶剂不C原子的立体化学的产品被逆转?
否则,像往常一样伟大的工作。
谢谢,我很高兴你发现了立体化学的例子。重要的确保反演存在!
如果你理解为什么嗨酸性比高频电负性强,尽管氟二氯甲烷的你不会有问题,更比氯仿极地,尽管更多的电子退出群附着在碳,债券-强度是一个关键,更快的bondbreaking打赌的极性溶剂在反应pertake。请注意这是限于极性。
没错,从未想过比较酸强度和极性的溶剂。酸/碱强度与亲核性趋势相比更有用。
我摸不透的东西:为什么DCM的偶极子的氯仿小于?撤销三个Cl不应该超过两个?我觉得我缺少一些东西,但是我不能把我的手指…
我也不明白。
由于偶极矩是基于大小和电荷分离,我想原因是3 C-Cl债券彼此抵消超过2 C-Cl债券。如果我没弄错的话,我认为氯甲烷(CH3Cl)具有更高的偶极矩比DCM和氯仿。
你是正确的,我发现这是1.9 D。http://en.wikipedia.org/wiki/Chloromethane_ (data_page)
在代数我不是世界上最好的,但我认为三个C-Cl矢量和偶极子将导致更大的整体的偶极子只是一个C-Cl债券。也许,碳氢键提供额外的电子密度,允许更大的整体分子的极化。
三个C-Cl债券是指向不同的方向
认为通过向量
我认为这是因为碳2 p2电子被更多的氯原子之间共享氯仿有较弱的偶极矩之间的比DCM C-Cl债券。所以你有一个更大的偶极矩在扩张型心肌病。偶极矩的氯甲烷是1.09,DCM 1.04是1.60和氯仿。氯甲烷我想象一个氯不够足够强大的形成一个大的偶极矩。
进一步化学:画出分子轨道图可以帮助,因为它将显示哪些电子输入子shell将显示你如果进入一个更高或更低的能级。
如果你让这三个物种的各自的碳正离子通过删除1氯原子和比较稳定,显然ch3 +是最稳定的,这意味着氯甲烷将最有可能是两极分化。
实际上,CH3 +会至少稳定。别忘了,Cl可以捐一双电子形成π键。
@James,但随着Cl是第三周期元素C是第二周期,我不认为他们的p轨道重叠很好由于大小差异,在这种情况下我们必须喜欢在共振诱导效应。
F虽然你的观点可能是有效的,它可以验证如果Fluoro-methanes的极性是相反的顺序氯甲烷代替。
你也失踪的事实有一个额外的氢原子在DCM和氯仿。因为氢比低碳偶极矩是阳性的。例如,CCl比较盐酸之间的电负性和债券。尽管这种差异很小的偶极矩的影响是明显的。
氯仿1 H 1.9 d
二氯甲烷2 H的1.6 d
氯甲烷3 H ~ 1.1 d
希望这个有帮助。
我认为这是因为氯仿三个氯原子的诱导效应抵消了大部分的外部负偶极子与扩张型心肌病时,只有两个氯原子撤回电子,因此更少的诱导效应的取舍。
回到矢量和,的人。如果你在笛卡尔图以结构和CHCl3,这样整体偶极子将指向的值- y(垂直向下,传统上),然后C-Cl债券比CHCl3以大- y值。简单的几何将从X轴如下35º角以CHCl3,只有15º低于轴。很难描述,但如果你建立一个分子和想象在笛卡儿坐标系统,你会没事的。
如果你真的尝试相同的向量和法律就清楚了
是的,我认为这是一个几何问题
其没事3 Cl -电子密度…撤军。但它们将在不同的方向……dipolemoment是一个矢量,应该subjcted向量添加,你知道在亚兰DP = 0…有4 cl -离子是0…。因为他们在不同的方向…。3 cl -离子将尽可能由于空间排斥力。所以他们把differrnet方向…。像一个大盒巧克力被孩子们在所有的方向。