焊接、结构和共鸣
如何使用电负性来确定电子密度(以及为什么不相信形式电荷)
最后更新:2022年12月31日|
如何确定部分费用
最后一次我们说过的“货币”是电子化学和电子原子间的每一个反应是一个事务。这意味着,如果我们真的想理解的反应,我们必须了解电子(并不是)。
有两个因素采用时这样做。第一个是电负性。这就是今天的帖子:使用电负性来确定电子密度。(第二个是共振,在下一篇文章中)
我假设你知道如何画路易斯结构,了解电负性的概念形式电荷以及能够解释图纸,但就是这样。如果你不是在那样的层次,并阅读了这些概念。
表的内容
1。我们怎么告诉电子在哪里吗?首先,画路易斯结构
好的。让我们开始第一个问题:我们如何告诉电子在分子吗?
第一个技能是能够吸引合适的路易斯结构的分子。在有机化学取得成功你绝对需要这样做在你的睡眠。路易斯结构应该占所有原子周围的电子,包括隐藏的孤对电子,如果适用。让我们看看。
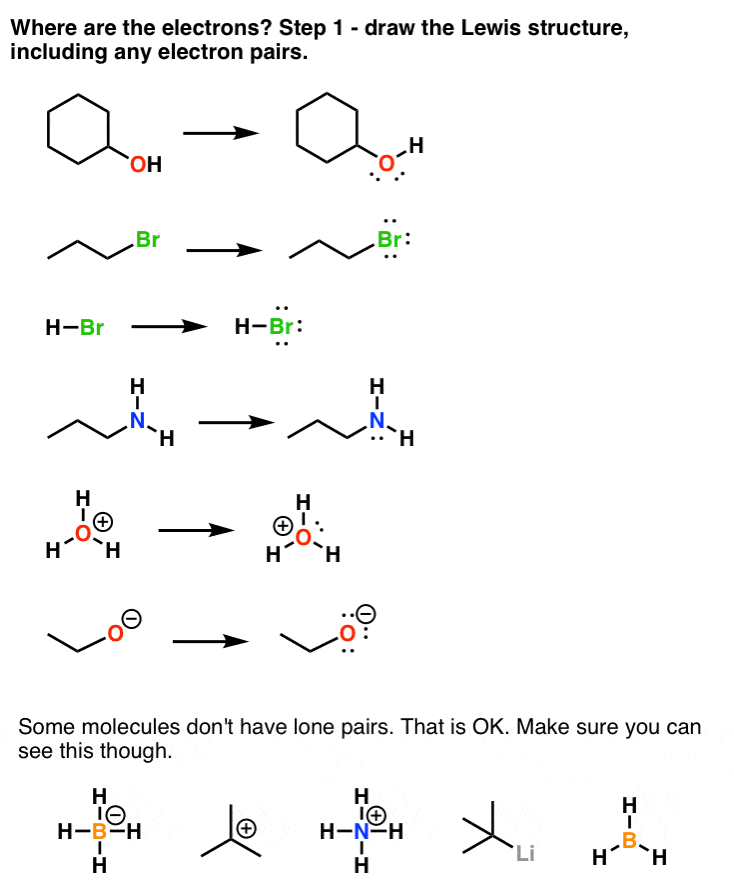
2。其次,应用电负性来确定部分费用
第二个技巧在于能够适用电负性来确定部分费用在债券。
看,我们的图纸的化学结构有时会得到的是什么真正的电子。
如果我们只注意到图纸本身,原子之间的线我们画——“共价键”两者之间共享的电子对同样。
然而,理想化的共享电子之间的差异在共价键与现实不同的电子密度,打个比方,就像一个乌托邦式的社会主义worker-state之间的区别,和苏联。
记得电负性——一个排名的一个原子对电子的“贪婪”,换句话说吗?键,将会有更多的元素的电负性更大份额的电子,和部分负反映这个更大的电子密度。电负性元素将有部分越少积极的向反映缺乏电子密度。
让我们看一些简单的分子和分析通过比较相对电负性偶极子的债券。
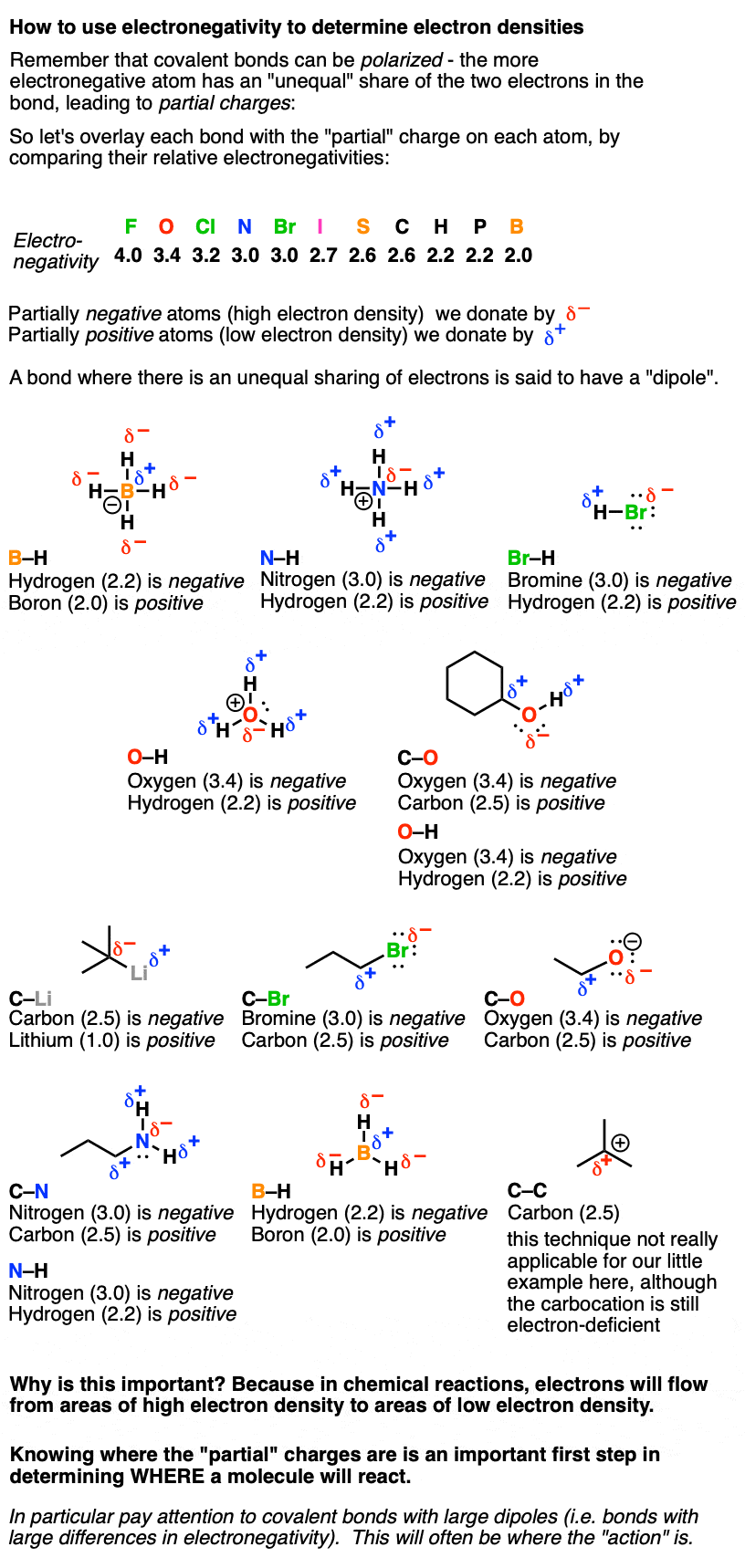
为什么它是重要的去通过所有这一切吗?因为在化学反应中,电子会从高电子密度的区域流向低电子密度的地区。知道部分费用是重要的第一步确定的分子反应。共价键与大偶极子(即大电负性的差异)值得关注:看频繁,这将是“行动”在哪里。
“坚持”,你可能会说。“我认为电子密度是反映在他们的指控,在H3O +,男朋友4- - - - - -,NH2- - - - - -不不不不不!”。这是第一个真正的弧线球,扔在有机化学的你,和一个不断给学生适合。
3所示。电子形式电荷是不一样的密度,
“形式电荷”给了我们一个难题。当一个分子熊电荷(或正面或负面),用于记账,我们不得不表示一个原子作为“轴承”。然而重要的是要意识到这种“记账”是不一样的电子密度,这是反应性的真正来源。当然,有很多分子中电荷的例子实际上* *代表的电子密度。但话又说回来,有很多相反的例子,像黑洞一样4(-),在北半球4(+),H3O(+)和其他人。
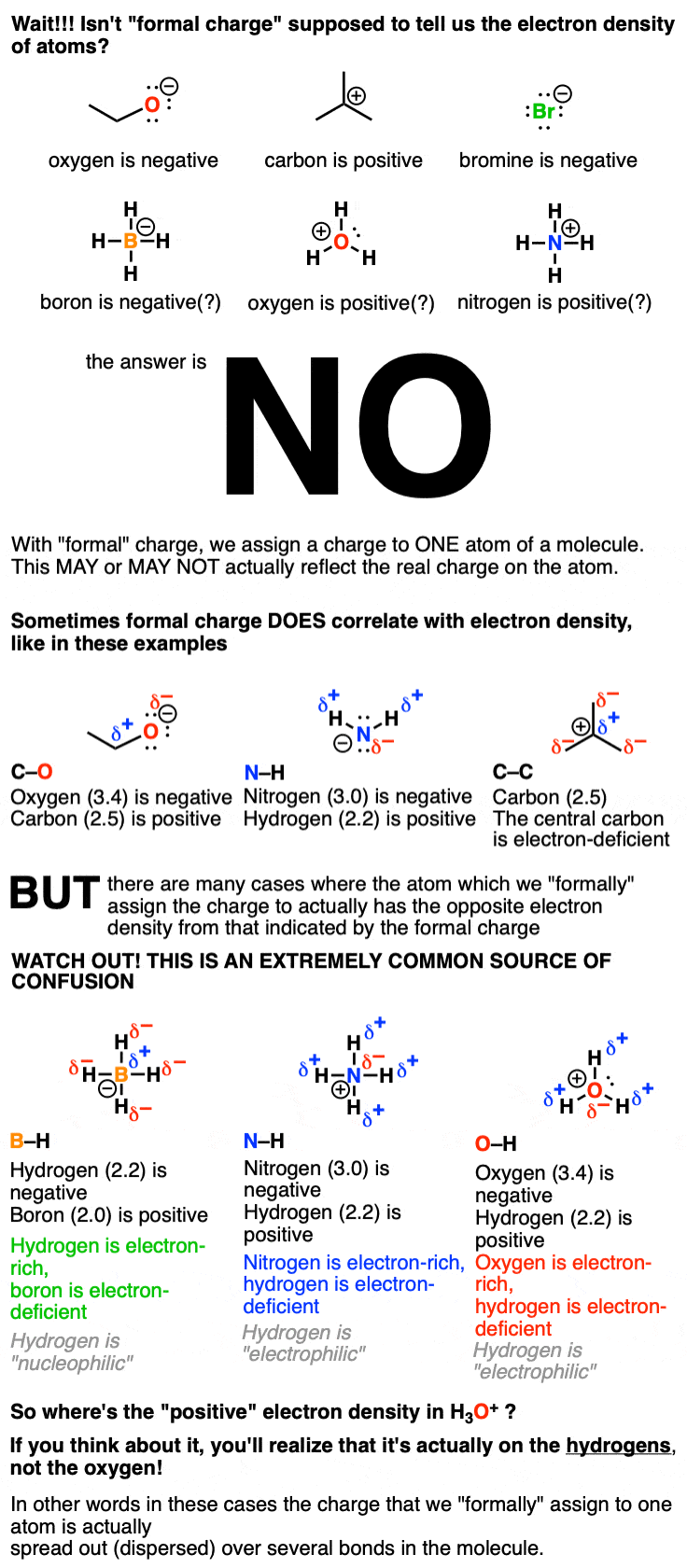
确保你理解这一点,因为它可能很难得到你的头在第一次。
在H O3O +可能有一个“正式”的+ 1,但是它实际上是最富电子(带负电荷)原子在分子!
所以尽管分子H3O(+)的费用+ 1,正电荷实际上是不在氧气本身,但“分散”-分散在分子,特别是在氢。点击这里查看势能图H3O (+))。然而,对于“簿记”我们分配一个+ 1的氧气,因为潜在的假设是原子间键的图,电子平均分担。
4所示。底线是:使用相对电负性,而不是正式的指控,确定电子密度
底线:如果H3O(+)与一个电子反应物种丰富,这些电子将去氢(因为它们是电子差),不氧气! !
如果你使用形式电荷来确定电子密度在定期会完蛋了。
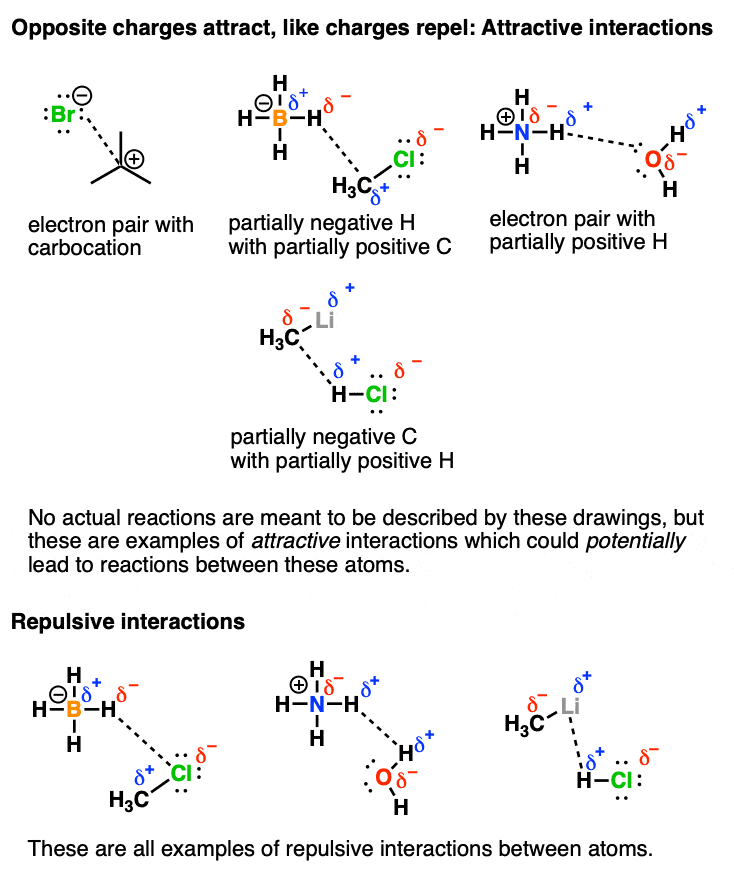
注意在第三张幻灯片的最后一部分我把一些新单词——“亲电”和“亲核”分别表示“electron-poor”和“富”。稍后将详细介绍这些。
这是一款优秀的在线资源的主题有机化学中静电势从里德学院。
在下一篇文章:介绍了共振
f - 4.0
0 - 3.4
cl - 3.2
n - 3.0
然后在逻辑上cl的电负性也比N H键(形式)
还应该形成H键。
但它不是。为什么? ? ? ? ? ? ?
它形成氢键,他们只是相当薄弱。可能由于贫穷轨道重叠H和Cl比发现H和F (3 p和2 p)
例如埃里克·雅各布森的研究项目涉及使用非常弱的氢键催化剂之间的相互作用(如尿素酶)和氯。它必须使用非常non-coordinating溶剂,这样他们不干扰这些弱相互作用。
嗨,詹姆斯
在过去的图我看你描述NH4 - 3之间的交互。我找不到任何信息NH4 +离子,这是一个错误或者有其他的意思吗?请帮我澄清这种化合物,谢谢!
晚,但这是一个错误。将修复。谢谢你!
有趣,有用。但是,说提斯水合氢离子的氧气是partiall负是不正确的。比H部分不太积极,但它不是负面的。氧亲核试剂不攻击的重要原因是,这导致热力学冷宫中间体形式电荷/八隅体规则的原因。
我不知道乔丹。的电荷分布地图H3O +和寻找蓝色区域(正电荷)。他们都是氢。http://www1.lsbu.ac.uk/water/hydrogen_ions.html
亲核试剂*能*攻击氧气,如果它是连接到一个像样的离去基团。例如,看看hydroboration-oxidation的迁移步骤。关键是氧气必须有一个低洼σ*轨道,可以攻击亲核试剂。这不是现在在H3O +因为亲核试剂必须解放H -,虽然这特定点有点超出了手头的话题。
嗨,詹姆斯!
这个话题确实是令人困惑的。我没有任何问题,电子流和电路类比。似乎总是让我尽管是电线在哪里,他们不是——坚持类比。
我觉得我得到一个掌握。当我重读这篇文章,我注意到你提到的债券重叠和共振。所以,基本规则是“线”通过电子迁移是有限的严格轨道重叠?因此,默认情况下是真的,移民也仅限于债券本身,除非有关的两个轨道在别处也有重叠?
有一个基本的规则集时使用确定的部分指控传播?我寻找的是一个心智模型的电路与一个特定的分子,这将是类似于构造图,但线表明它们是如何“连接”。
谢谢!
嗨。你提到的每一个反应是原子之间的电子交易。这是否意味着所有的反应有一个氧化还原的性格?
不一定,因为在一个物种的过程中提供一个电子对,受体分子可能开除一个物种轴承一个孤对电子。酸碱反应是一个简单的例子。氢氧化钠和盐酸反应的羟基捐赠一对电子H,但Cl接受一对电子(从氯键)。氧化和还原都没有发生。这也是真正的取代反应。
这是极其经验我有很多困惑与形式电荷……………谢谢这个网站“世界上最好”…就像cm朋克
u有写小心极其混乱如2应该是氮源是电子丰富而不是氧
固定的。谢谢你!
你好,詹姆斯,
感谢你进入“挑剔的细节深度”和重复的概念在这篇文章中,我不知道如果这是真的,但我相信学生已经与细节和混淆斗争看到两个类似的事情在化学之间的细线,找到更好的/享受当老师对待我们就好像我们是“不废话吗”——至少我做,可以充满清晰的信息。(我希望有意义)。我写这多谢谢先生。
谢谢你的有用的帖子!一个问题——在过去的图你描绘的互动李(+)和(+)H,但也可能是一个有吸引力的互动李(+)和(-)Cl吗?这将是更多的有关在被动的情况下?
有可能,是的,但是碳氢交互更重要。我们稍后当我们谈论亲核性、亲电性。
伟大的詹姆斯显然讨论形式电荷的电子密度之间的区别。你有解释和合适的例子很佳otherwebsites书并没有这样做。
有什么方法可以求出分子的HOMO和LUMO对于电子密度吗?
不知道如何回答这个问题。如果你能确定一个分子的HOMO和LUMO,你确定活性成分。电子捐赠的人类将从(亲核试剂),和LUMO就是电子将被接受(亲电试剂)。很难概括现阶段因为有3种的亲核试剂——孤对,π键,σ键,还有三个主要类型的亲电试剂:p轨道,π*反键轨道,和σ*(反键轨道)。
至少在这篇文章中我可以告诉你,如果我们只是谈论孤的人类,高能(大多数活性)孤将原子的电负性最低。这就是为什么H3C -比H2N反应活性比HO -,等不占溶剂效应。
如果我们谈论的是σ*的LUMO轨道(我还没有谈到π轨道),最大的“叶”σ*将发现更多阳性原子的偶极子。
无可否认,这是一个非常粗略的治疗。为了知道HOMO和LUMO(精力)更有把握可以计算能量使用高斯这样的包(超出了我们讨论的范围)或从实验结果推断。
好文章!你总是帮助我找出很多东西! ! !
谢谢!
另一个伟大的文章!我期待其他系列。
区分形式电荷和电子密度是一个重要的一个,和可悲的是似乎是教师和课本都经常被忽视的一点。我记得感到困惑,直到我开始考虑电负性:
“嗯…H3O +有+ 1中的O fc…但它也有最高的EN…这意味着它很可能要拉甚至* *电子密度H的试图减轻+ 1”。
(我知道我上面写的不是技术上准确,但它帮助我记住了fc和电子密度的区别以这种方式思考。)