焊接、结构和共鸣
我们怎么知道甲烷(CH4)是四面体吗?
最后更新:2022年12月13日|
什么告诉我们有关碳的价电子成键在CH4吗?
(提示:因为CH的偶极矩4是零,答案是,“不够”)
是否2 s轨道配置的碳22 p2,那么我们如何使用这些信息来计算出轨道的安排在一个简单的有机分子像甲烷(CH4)?
事实证明,甲烷是四面体,4 =键角为109.5°和4等于债券的长度,也没有偶极矩。
这带来了两个问题。首先,我们如何知道,CH4四面体吗?其次,我们如何调和这电子配置(2 s22 p2),这一事实四个等于碳氢键?
这就是这篇文章。
表的内容
- 价电子的电子排布的碳是2 s22 p2
- 我们可以使用这些信息来计算出结构的甲烷(CH4)?(剧透:没有)
- 也许甲烷(CH4)是广场平面?
- 证伪CH的广场平面结构4(1874)和四面体结构的建议
- 1874年四面体碳:不是一个流行的想法
- 轨道涉及什么?
- 笔记
1。价电子的电子排布的碳是2 s22 p2
在我们的原子轨道的审查我们看到,轨道的配置价电子碳是2 s22 p2如下所示:
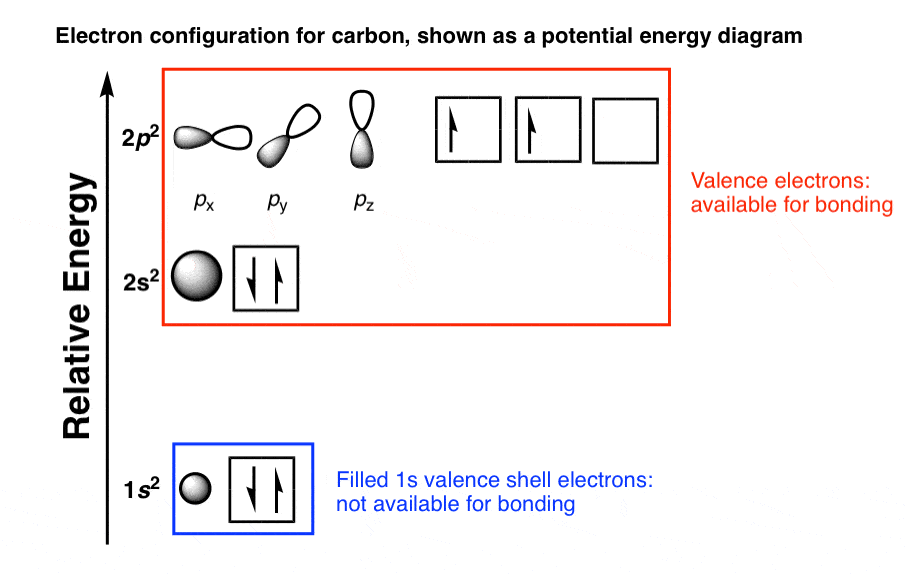
自从2 s轨道的能量低于2 p,这是第一。这意味着2 s轨道有两个电子,和一个电子的两个3 2 p轨道。还有一个空2 p轨道。
(此外,还有两个电子“内壳层”1 s轨道,不用于成键)。
2。我们可以使用这些信息来计算出结构的甲烷(CH4)?(剧透:没有)
目前为止一切都很顺利。这是好如果我们只是谈论孤立的碳原子。
但为了成为真正有用,我们需要能够与碳的轨道的结构和结合实际的有机化合物。
最简单的有机化合物是甲烷,CH4。让我们把四个氢原子进入图片并尝试应用我们所学到的知识提出一些假设这个分子的成键。
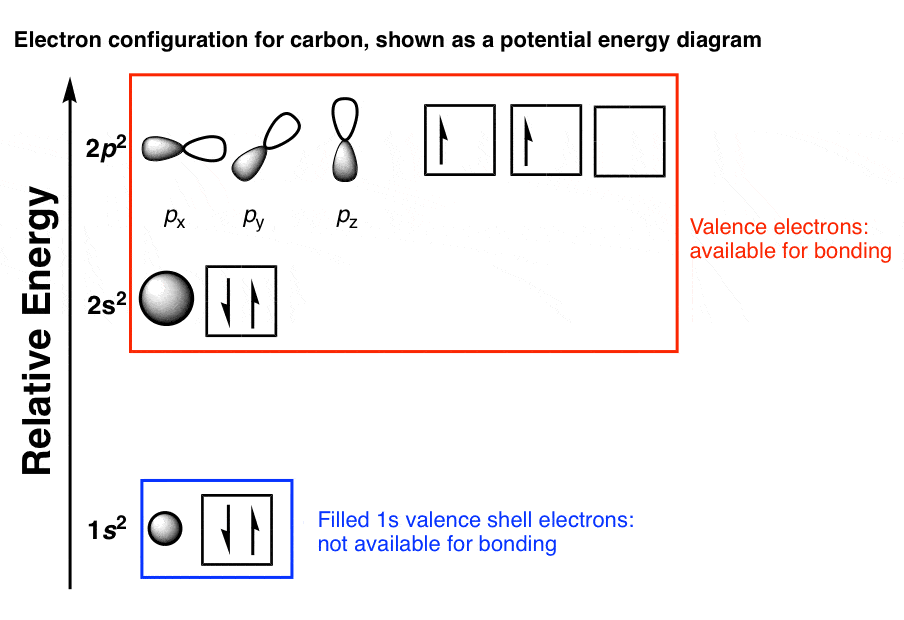
3 p轨道碳都是在90度,在x, y和z轴。
难道我们希望甲烷的结构将有三个碳氢键为每个p轨道彼此(90度),然后第四个碳氢键连接到2 s轨道?由于对电子排斥,也许我们应该把碳氢键的最大距离其他碳氢键;这将使一个H-C-H键角为135°。
这种逻辑会给这样的结构:
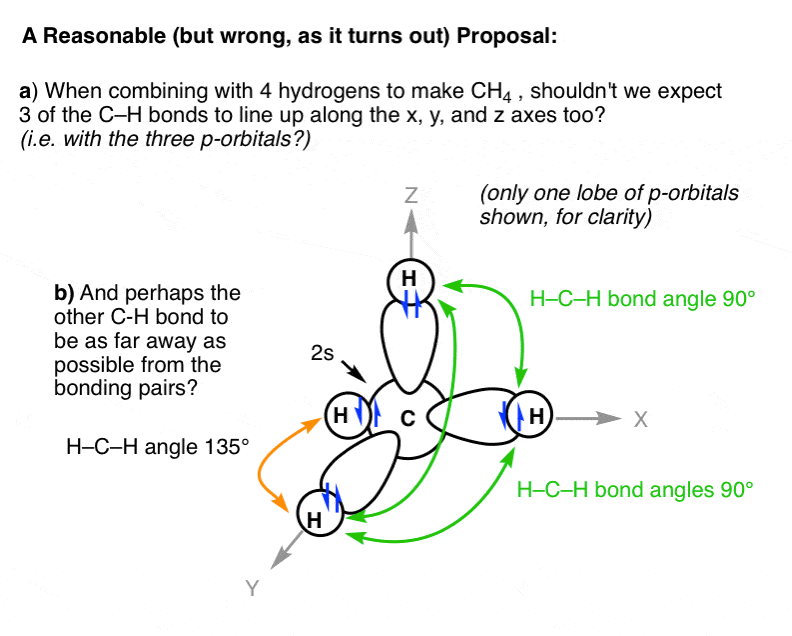 事实证明,它可以表明,这一建议是错误的。
事实证明,它可以表明,这一建议是错误的。
为什么?
偶极矩。
回想一下,每个碳氢键都有小偶极子由于电负性的差异之间的H C(2.5)和(2.2)。我们期望C部分消极和H部分积极。
- 如果上述结构准确描述甲烷的结构,我们期望甲烷有3个长碳氢键(2 p轨道)和一个短的碳氢键(2 s轨道,它是接近原子核)
- 此外,我们预计3 H-C-H键角为90°和一个H-C-H键角为135°。
- 当矢量的碳氢键偶极子被添加在这个结构,他们会不都消掉了。
- 因此,我们将会观察一个小,但对CH可衡量的偶极矩4。(注1]
然而,测量偶极矩CH4是零。因此这不能正确的结构。
这告诉我们,所有的键长和键角甲烷是相同的。
3所示。也许甲烷(CH4)是广场平面?
好的,你说。如果所有碳氢键的长度和角度,为什么不能CH4下面的结构,所有的键角为90°和CH4是平的,在平面上的页面。(我们称之为结构“广场平面”)。

这是事实上的多数意见安排债券碳直到大约1880左右。非常杰出的化学家等贝采里乌斯去他们的坟墓没有理由怀疑甲烷除了持平。
然而,我们现在知道这是错误的。为什么?
4所示。证伪CH的广场平面结构4(1874)和四面体结构的建议
如果甲烷被修改以便中央碳连着四个不同的基团,分子可以存在2种不同的异构体重叠镜像(这就是所谓的“光学异构”和后来的课程)。
这是可能的,如果安排在中央碳四面体4组,但是不如果分子广场平面。例如,甲烷衍生bromochlorofluoromethane周围有四个不同的组碳,可以分为两个不同的异构体在不同的方向旋转平面偏振的光。(稍后我们将看到,这些同分异构体被称为“对映体”)
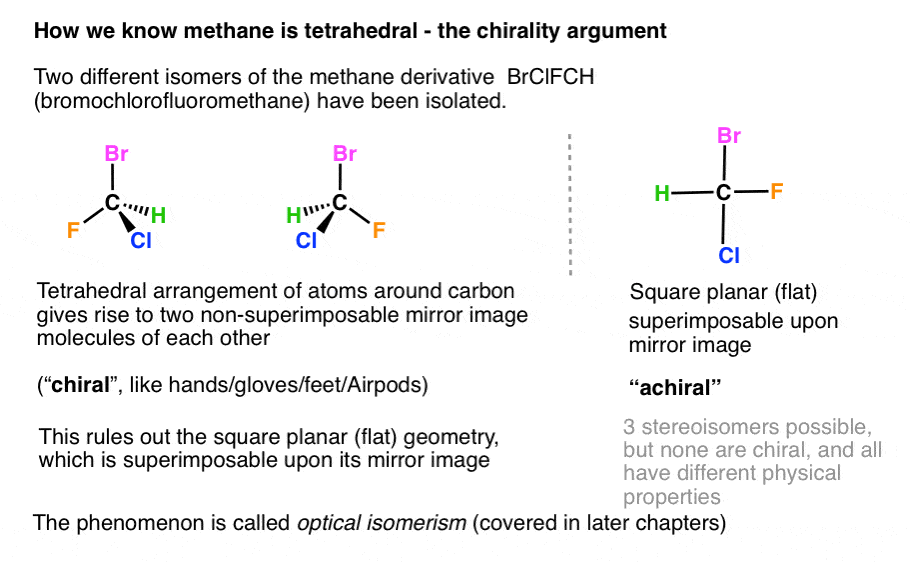
这个观察排除广场平面结构。如果碳方形平面,分子将持平,和自己的镜像重合,且只有一个异构体可能。
即范霍夫兽医学院,一个研究员在乌得勒支,是最早解决三维碳的可能性。在他的“La Chimie在空间”(1874年)他指出,原子在空间的排列具有重要实际后果——这一点已经完全忽视了这一点。范霍夫显示四面体排列的四个不同的团体在一个碳原子(他称为“不对称碳”)会产生两种不同的异构体,此外,这可以解释为什么酒石酸(两个不对称碳原子)中存在三种形式(+、-、和内消旋)。(源]

范霍夫的工作——应该注意的是纯粹的理论——在某些圈子里很不受欢迎。
5。1874年四面体碳:不是一个流行的想法
著名的德国化学家赫尔曼·科尔伯曾经这样说:

范霍夫飞往斯德哥尔摩,在飞马座接收第一个1901年诺贝尔化学奖。(注2]
无可争议的证据为碳原子周围的四面体排列的债券是在1913年布拉格钻石使用x射线结晶学的结构决定的,发现它与C-C-C四面体网络的碳原子键角109.5°。
6。轨道涉及什么?
我们现在合理化四面体的原子排列在甲烷是由于相互排斥的结合对电子(或称。VSEPR理论)。
这并不是帮助我们理解轨道然而,参与成键。
如果我们接受氢在甲烷是四面体的安排,然后我们如何描述成键轨道的甲烷,鉴于我们所知的几何年代和p轨道?
毕竟,2 p轨道都是在90度,但甲烷的键角是109.5°。
此外,我们如何解释,每一个在甲烷4债券相同的长度吗?发生了什么2 s轨道,例如?
碳氢键的电子被认为是在吗p轨道或年代轨道?还是别的?
事实证明,传统的治疗方法是处理碳是周围的债券杂化轨道。
在下一篇文章。
笔记
注1。注意,mono-deuterated甲烷(CH3D, D是氘,氢的重同位素)有一个小的偶极矩测量。(裁判]
注2:需要注意的是,范霍夫的物理化学诺贝尔奖是为了表彰他的贡献,不是有机立体化学。
我感谢这个页面覆盖范霍夫“原子的空间排列”的历史视角。值得一读。
从同一来源:范霍夫的四面体模型(从莱顿科学博物馆的历史;源]

从同一作者,一些历史视角科尔伯/范霍夫争吵:
显然科尔伯被愚蠢的放纵和恶意的。他也是目光短浅,他猜错了。我们可以轻松地欣赏,他得到了在历史上是他。
面临的挑战是适当尊重不可或缺的贡献他拥护的态度对化学的发展。坚持接近仔细的实验观察,化学已经(现在也是)。科尔伯试图保持科学生产,智力的路径。
看到有机化学简史(幻灯片35和36):http://ursula.chem.yale.edu/ chem220 / chem220js StudyAids.html #历史
如果我没记错的话正确,a·w·霍夫曼是给这节课的时间,李是格兰特在1865年投降。
非常感谢。我从你的网站受益。
我相信,一个方形平面的概念与4种不同碳substiuents只有一个异构体并不准确。是的,镜像是和原来的一样,但切换两个取代基将提供一个不同的异构体。
正方形平面几何,然而,将二氯甲烷和类似的分子存在两个同分异构体(顺式和反式),也会增加可能的异构体分子的数量超过1立体化学的中心,打破了2 ^ n规则。
作为一个旁观者,我想说,自2014年以来我一直在使用这个网站,我觉得这是令人惊叹的,所以谢谢你的奉献精神。
这是一个很好的观点。正方形平面碳有4种不同的取代基可以* 3 *同分异构体(试试),所有的立体异构体,但没有一个对映体。