酸碱反应
在有机化学酸碱反应
最后更新:2022年12月29日|
介绍了在有机化学酸碱反应
既然我们已经描述了如何找出电子在分子,稳定的因素负电荷和正电荷,进入了曲线箭头形式主义反应,我们就可以开始进入更详细的一些有机化学的重要反应。
让我们先从酸碱反应。
表的内容
- 每一个酸碱反应的四个组件
- 是什么让一种酸碱反应有利?(提示:这与共轭碱的稳定性)
- 分子的酸度直接相关的能力共轭碱稳定负电荷
- 任何因素稳定的共轭碱将导致酸度的增加
- 酸碱反应,从一个更不稳定(例如更基本的)阴离子更稳定(即基本)阴离子是积极有利的
- 笔记
1。每一个酸碱反应的四个组件有机化学
在第一篇文章引入酸碱反应,我只是说,首先要做的就是找出打破债券形式和债券,并承认这四个组件。像这样。
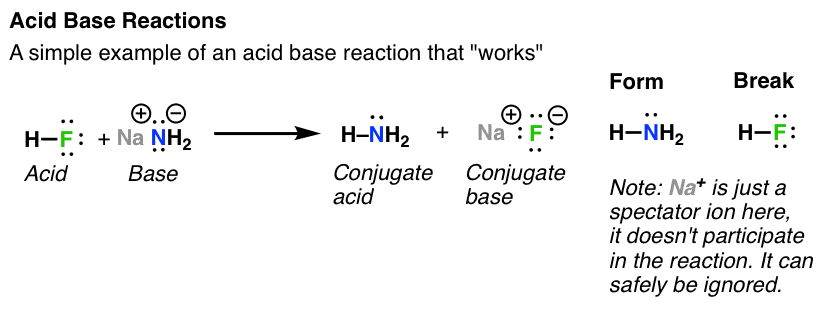
这是在有机化学酸碱反应的模式:我们交换氢两个原子之间。实际上,由于氢不带任何电子,当这种情况发生时,我们的技术交换氢离子(质子)。我们每个物种的名字:
- 失去了H +叫做的分子酸
- 的分子H +称为收益基地
- 在获得H +,成为基础共轭酸
- 失利后H +,酸变成了共轭基地。
2。是什么让一种酸碱反应有利?(提示:这与共轭碱的稳定性)
虽然这有助于我们认识到模式,它并没有真正帮助我们回答“为什么?”。例如,为什么上面的反应继续进行,但下面的反应不?毕竟,这也是技术酸碱反应。
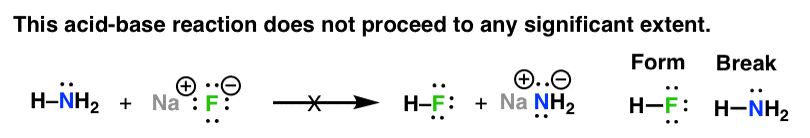
现在我们可以回头开始解决这个重要的问题。
让我们先从一些简单的例子。这里有四个样品酸碱反应。如果你读到负电荷的稳定之前,您应该能够衡量的更有利的哪些是更有利的。(现在随意忽略向后箭头)
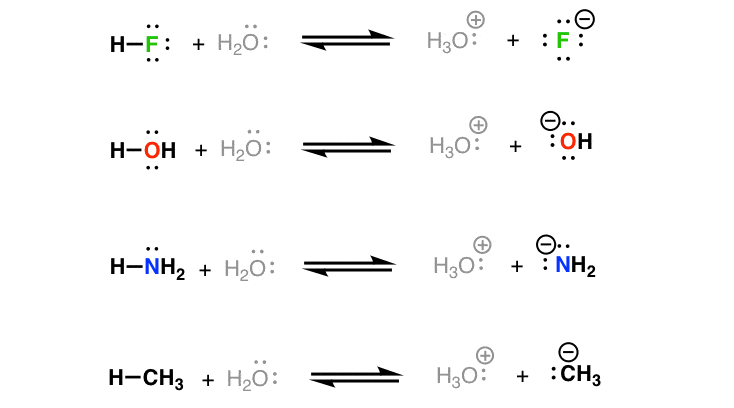
3所示。分子的酸度直接相关的能力共轭碱稳定负电荷
让我们看看这个,想想看:
- 在每一个反应,分子在最左边是酸,这是捐赠一个质子水(基地),形成H3O (+) (共轭酸)和阴离子(共轭碱)。
- 注意费用变化:在每种情况下,共轭碱比酸,更多的负面和共轭酸比基础更积极。这总是对酸碱反应。
- 由于每个反应包括H2O和H3O (+)唯一的区别每个反应之间的身份酸和共轭基地。
- 在其他条件保持不变的情况下,中性分子是更稳定的比它的共轭碱(自然寻求最小化费用)。中性分子之间的稳定的差异(左边)相比是微不足道的稳定带电分子之间的差异(右边)。
- 因此,理解的因素稳定负电荷将会是关键了解哪些是最有利的,哪些是最有利的。
如果你回想一下稳定因素负电荷,因为我们从左到右在元素周期表中我们得到了这一趋势:
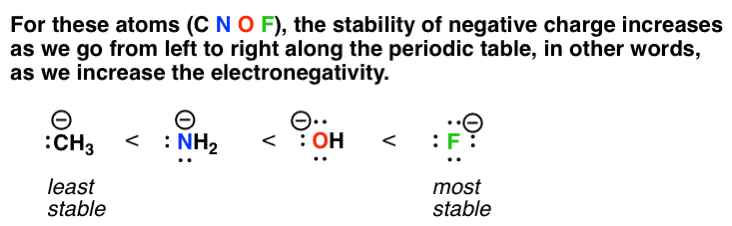 这四种物种,氟离子(F -)大多数稳定。
这四种物种,氟离子(F -)大多数稳定。
因此,上面列出的所有四个物种的反应,我们应该期待氢氟键是大多数可能放弃其质子形成它的共轭碱,F (-)。换句话说,氢氟键是最酸的因为它的共轭碱最好的能力来稳定负电荷。
这四种物种,CH3(-)至少稳定。
因此我们应该期待列出的所有四个物种H-CH3是至少可能放弃其质子形成它的共轭碱,CH3(-)。换句话说,H-CH3是酸性的。
4所示。任何因素稳定的共轭碱将导致酸度的增加
让我们重复这个过程,在不同的形式。
- 一个物种的酸度直接相关稳定它的共轭碱。
因此任何因素稳定共轭碱(具体来说,电子对的共轭碱)将导致一个增加在酸度。
哪些因素稳定负电荷,因此会导致酸度的增加?有七个:电荷,电负性,极化率,共振,归纳影响,轨道和芳香性。(见文章-七个因素稳定负电荷有机化学中)
每一个趋势导致负电荷的稳定直接影响酸度。更具体地说,稳定负电荷将使共轭酸酸性更强。
5。酸碱反应,从一个更不稳定(例如更基本的)阴离子更稳定(即基本)阴离子是积极有利的
所以对于反应顶端,我们要从一个更不稳定阴离子(H2N- - - - - -)更稳定的阴离子(F- - - - - -)。这是大力优惠,像水往低处流。这反应所得。
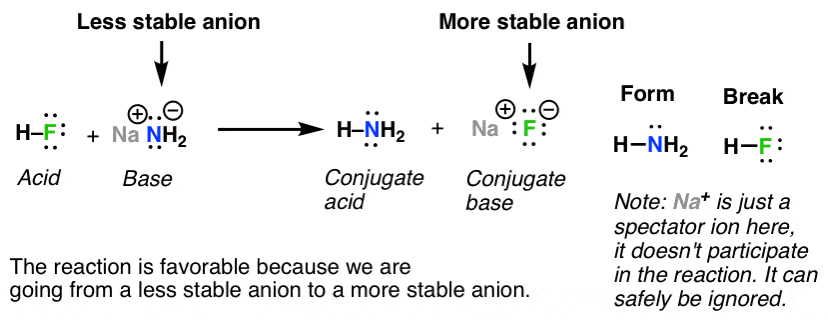
需要从一个相反的反应更稳定的阴离子(F- - - - - -)不稳定阴离子(H2N- - - - - -)。这是大力不利,不满意。

当然这是目前仍然很模糊,我们可以更准确,我们会看到。下一篇文章中,我们来看看这些相同的反应从一个稍微不同的角度。
在下一篇文章:酸性越强,较弱的共轭碱
为什么水作为酸或碱?如果1×10 - 14千瓦的水,不会形成H3O +和OH -非常不利的?
我相信你的氨产品可能有额外的一对电子:)
哦,是的。尴尬。固定的,谢谢!
读到这里我意识到有机我上个月的一大教训在稳定的因素一个负电荷。我有一种感觉,电子和他们的收费是有机的最重要的因素,但是阅读这篇文章让我退后一步,理解更大的图景。谢谢你!
对于最后一个例子,你的意思是你的反应是不利的b / c从一个更稳定的离子不稳定阴离子吗?
是的!完全正确!