有机反应的底漆
平衡和能量的关系
最后更新:2023年8月3日|
一千卡每摩尔实际上是很多的
本文讨论了平衡常数之间的关系K和能源ΔG的差异,探讨了方程的一些应用程序对各种有机化学中例子。
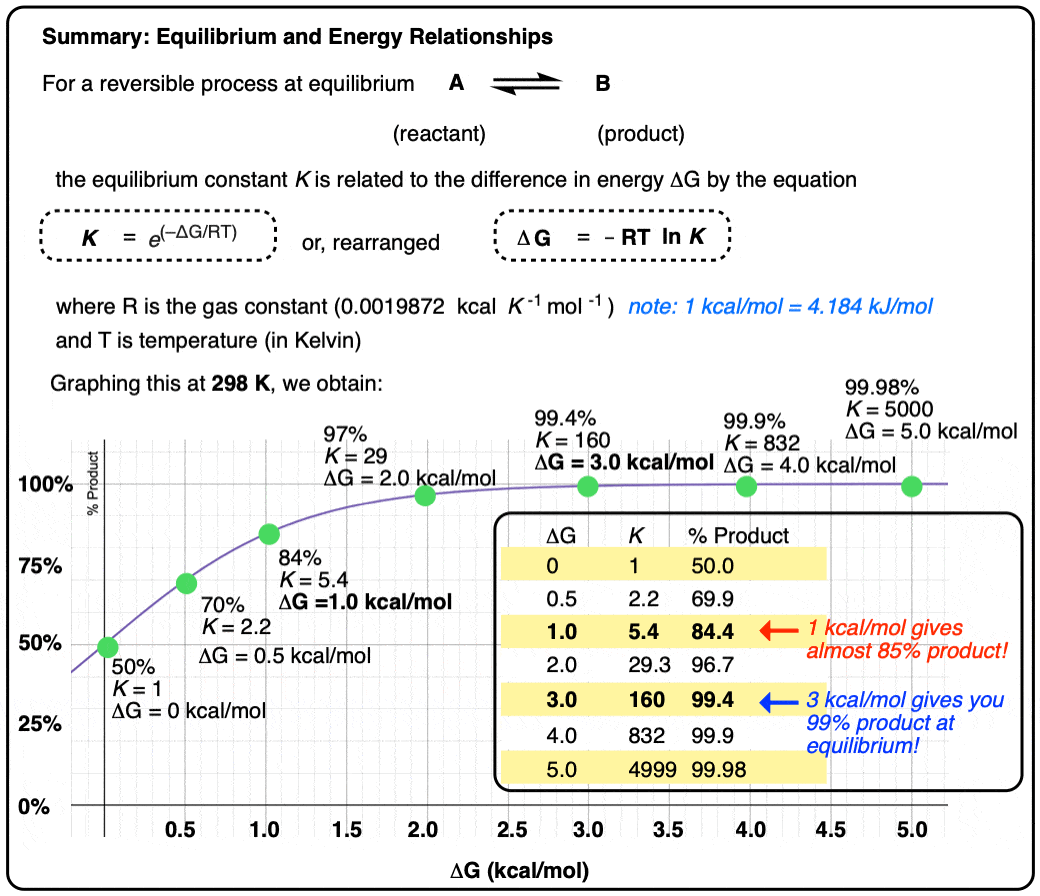
- 吉布斯能量的差异ΔG两个物种之间的平衡和平衡常数有关K根据方程
ΔG = rt lnK
- 其中R是气体常数(0.001987千卡K1摩尔1)(我们将使用千卡每摩尔- 1千卡每摩尔= 4.184焦每摩尔)
- 和T温度(开尔文)
A和B两个物种的存在为50:50的比例均衡对应于一个平衡常数K =1,一个能量差ΔG 0千卡每摩尔。
不是非常令人兴奋!
然而,图形一系列ΔG值与平衡常数K,让我们看到一个相对少量的能量(1千卡每摩尔)在室温(298 K)就足以提供一个84:16产品比反应物。所以1千卡每摩尔是真的很多!
相反,如果你知道ΔG能量差异,可以计算平衡常数K通过重新整理方程为:
K=e(-ΔG / RT)
下面的文章也讨论这些后果和一些测验,你可以练习做涉及各种计算K在不同温度和ΔG。
表的内容
- 计算产品比例均衡的产品
- 从平衡常数计算能量差异(ΔG)
- 1千卡每摩尔实际上是相当多的
- 计算平衡常数K当你有能量差(ΔG)
- 更好的选择性“免费”通过降低温度
- 应用程序-环己烷“值”
- 应用程序-烯烃反应
- 应用程序——取代反应
- 应用程序-酮烯醇互变异构
- 总结
- 笔记
- 测试你自己!
- (高级)引用和进一步阅读
1。计算产品比率反应的平衡
假设我们有一个可逆的过程(注1反应物之间)一个和一个产品B。
- 平衡常数K= (B]/ [一个]在方括号的浓度一个和B在平衡(mol / L)。
- 例如,一个平衡常数K5.4意味着有一个5.4:1比例产品开始材料的平衡。
- 自K最终只是一个比,我们可以计算出产品的数量除以5.4(5.4 + 1)给0.84 B的结构百分比,因此只是任何剩余的金额(0.16)。
- 我们可以计算产品的贡献B整体平衡常数除以混合物K通过(K+1)

时的浓度一个和B是相等的,平衡常数K等于1的数量B在混合=K/ (K + 1)在本例中是1 /(1 + 1)还是0.5
 点击翻转
点击翻转

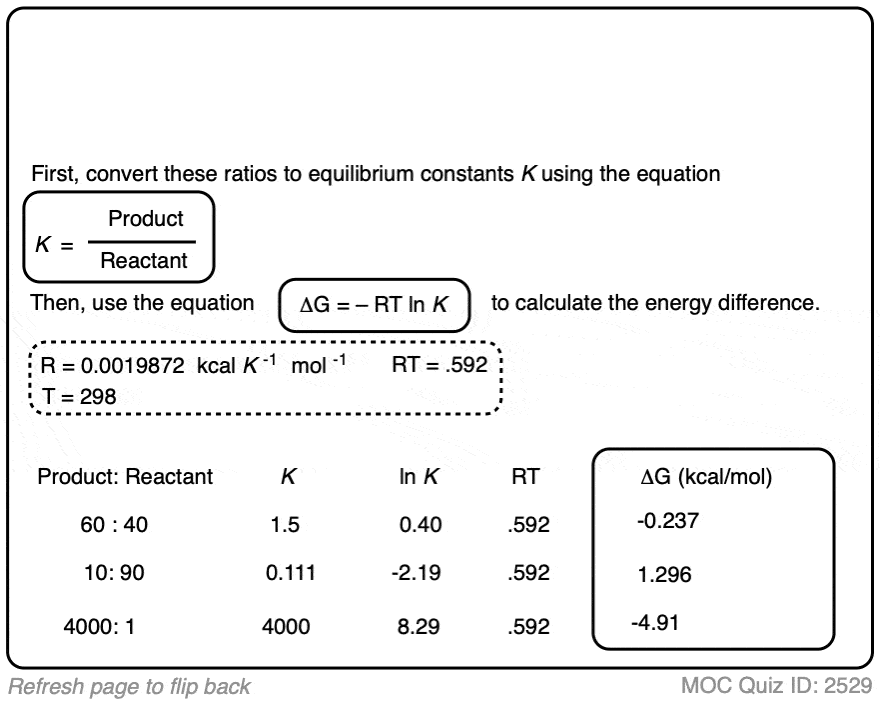
2。从平衡常数计算能量差异
平衡常数K有关的差异ΔG两个物种之间的能量方程:
lnK= -ΔG / RT
- 其中R是气体常数(0.001987千卡K1摩尔1)(回想一下,1千卡- 4.184 kJ。我们倾向于使用千卡每摩尔因为千卡单位只是如此方便有机化学(见文章为什么有机化学家使用千卡吗(注2])
- 和T温度(开尔文)
现在我们可以重新安排这个方程
ΔG = rt lnK
这意味着,如果你可以测量平衡常数对于一个给定的转换在一个特定的温度,你可以用它来计算相应的能量差ΔG。这是非常有用的!
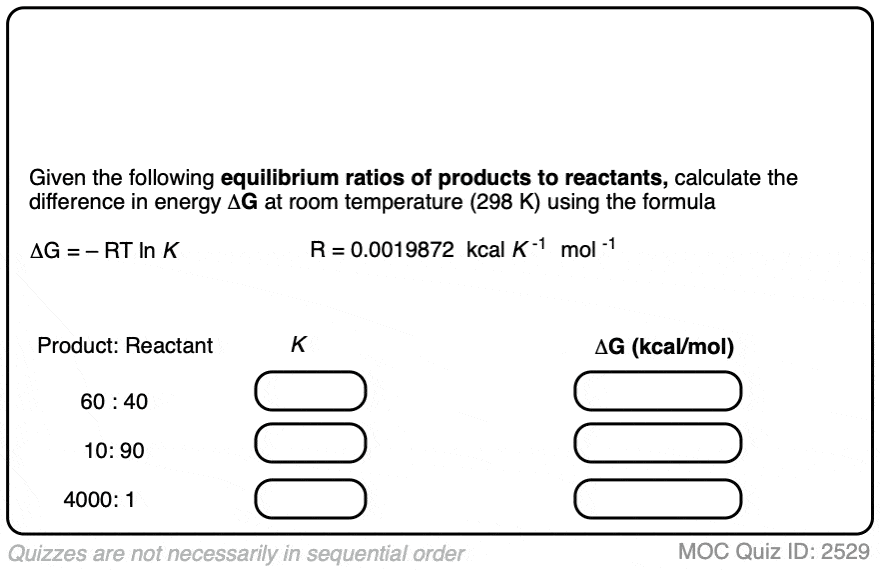
在室温(298 K),使这些值的表是这样的:

在下面的测试实践做一些计算。
 点击翻转
点击翻转
3所示。1千卡每摩尔实际上是相当多的
从上面的表中,值得指出的是,一个1千卡每摩尔不同能量给你相当多的选择性。
图形产品比率和δG在298 K,给我们如下图:
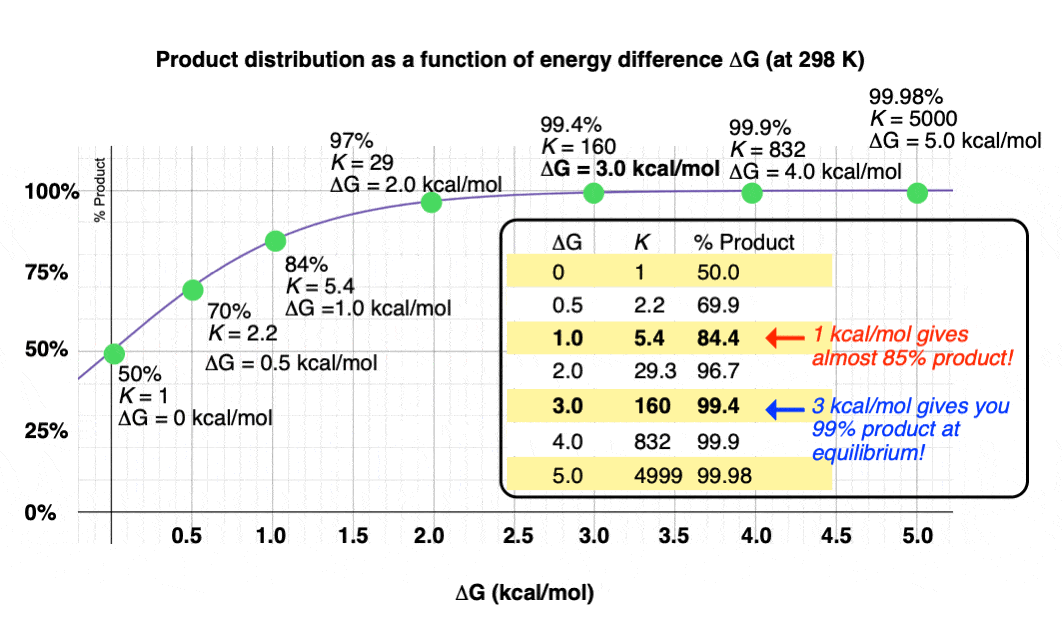
仅1千卡每摩尔让你的能量差一个84:16产品的混合物。这是很好的选择性能量差如此之少。
相信我当我说很多时候,化学家们很乐意接受84:16比的产品!
当你考虑到1千卡每摩尔是一个高度差超过互动的能量消耗乙烷(见后乙烷的交叉与重叠构象这似乎是一个很好的交易!
如果我们提高能量差一点点3千卡每摩尔,我们克服99:1产品的选择性。这是优秀的。(注3]
4所示。从能源的差异计算平衡常数
我们可以用这个方程在相反的方向。
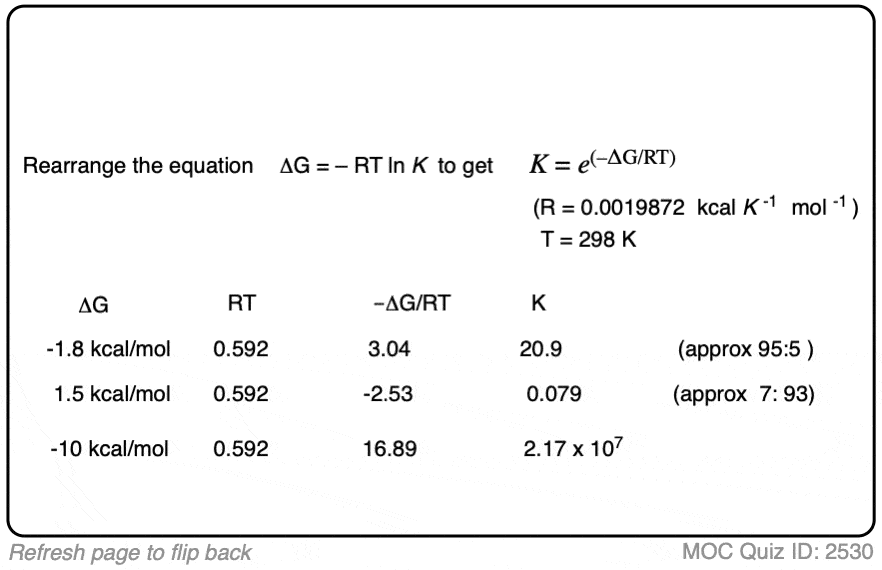
如果我们知道能量差ΔG,我们可以计算平衡常数K通过重新整理方程为:
K=e(-ΔG / RT)
当两个物种之间的能量差异零,这对应于一个平衡常数K= 1
当能量的差异仅仅是1千卡每摩尔平衡常数在室温(298 K)是5.4。
这就会突飞猛进K = 5000的能量差5千卡每摩尔在298 K。
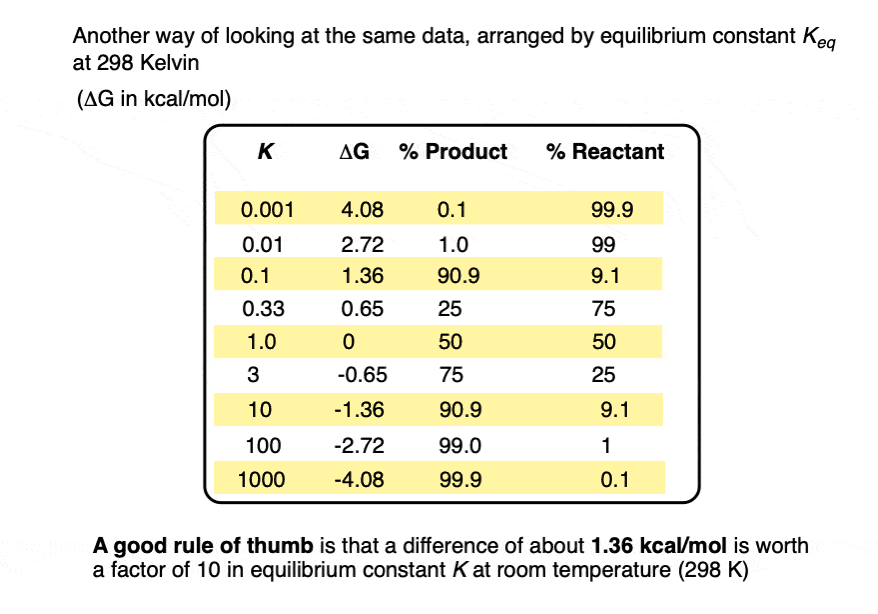
一个有用的经验法则是,每个变化的能量1.36千卡每摩尔的结果在一个数量级(10×)增加平衡常数K。(注意4]
 点击翻转
点击翻转
5。更好的选择性“免费”通过降低温度
直到现在我们已经考察自由能之间的关系和平衡常数在室温(298 K)
平衡常数温度时发生了什么变化?
K=e(-ΔG / RT)
随着温度小,平衡常数K去向上。(假设一个自发的过程(负ΔG))
换句话说,对于一个给定的能量差(例如1千卡每摩尔)选择性为产品增加。
比较过程的趋势平衡常数和ΔG 1千卡每摩尔在室温(298 K),水的冰点的温度(273 K)和现成的干冰——丙酮冷水澡(-78°C或195 K)。
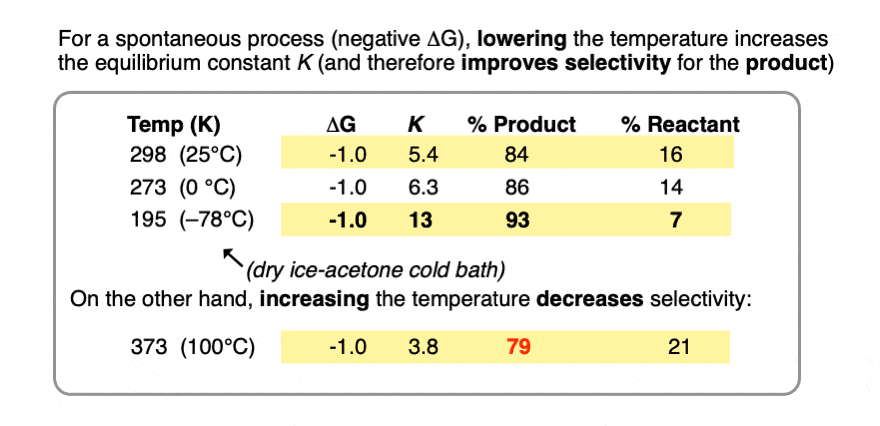
反应在极低的温度下运行(-78°C)给了我们一个平衡常数K= 13提供93:7比率的产品,在室温下与84:16。
与之形成对比的是,执行相同的过程水的沸点的温度(100°C或373 K),使产品的比例79:21和平衡常数K3.8。
所有其他条件不变的情况下,如果你想最大限度的选择性平衡所需产品,运行它的最低气温可能仍然会给你一个可以接受的水平。
那么问题是什么呢?前面的句子的最后一部分提供了一个线索。我们支付的价格运行在较低的反应温度是它慢。
另一个因素,需要注意的是,运行一个反应在足够低的温度可能会关闭这两个物种之间的平衡。这未必是一个选择性的问题(见文章热力学与动力学控制),但只要注意,用吉布斯方程假设两个物种都处于平衡状态。
6。应用程序-环己烷“值”
如果“1千卡每摩尔确实是很多毕竟”,这仍然会让很多人迫切和重要的问题:
那又怎样?
好吧,好吧。让我们把这一点具体的遵循了一些具体的例子。
首先:环己烷椅子翻转。
环己烷采用“椅子”构象和两个“翻转”椅子之间互换的形式,所有轴向取代基取代基成为赤道和赤道轴。这两个构象处于平衡状态。(见文章——环己烷椅子翻转]
当一个取代基环己烷存在,与取代基的构象赤道的立场是较低的能源比取代基的构象轴向(很大程度上是由于取代基之间的“笨拙的交互”——立体交互和碳氢键环己烷环)
测量两个矫形器的比例(核磁共振-核磁共振是一个方便的工具)允许我们计算平衡常数K从那里,我们可以计算在能源ΔG的区别。
例如,在室温下1-methylcyclohexane存在95:5赤道和轴向矫形器的比例,这对应于一个平衡常数为17.6和1.7千卡/摩尔的能量差。
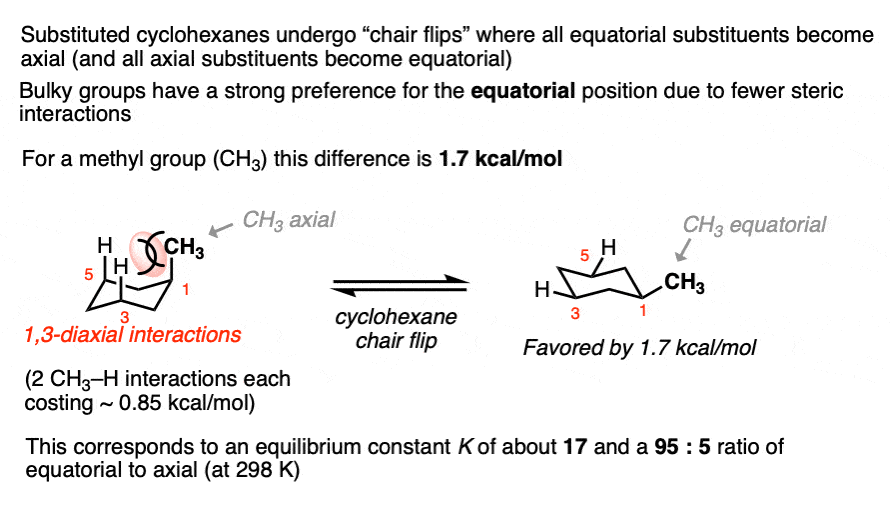
这个值是1.7千卡/摩尔通常被称为的“值”CH3组。(见文章-环己烷的值)。
许多的值(能量差异)对各种取代基环己烷测量和列表。例如,O-CH的一个值3组是0.60(更少的倾向于比CH赤道的位置3)和一个值t丁组是4.9(极强的偏爱赤道的位置)。
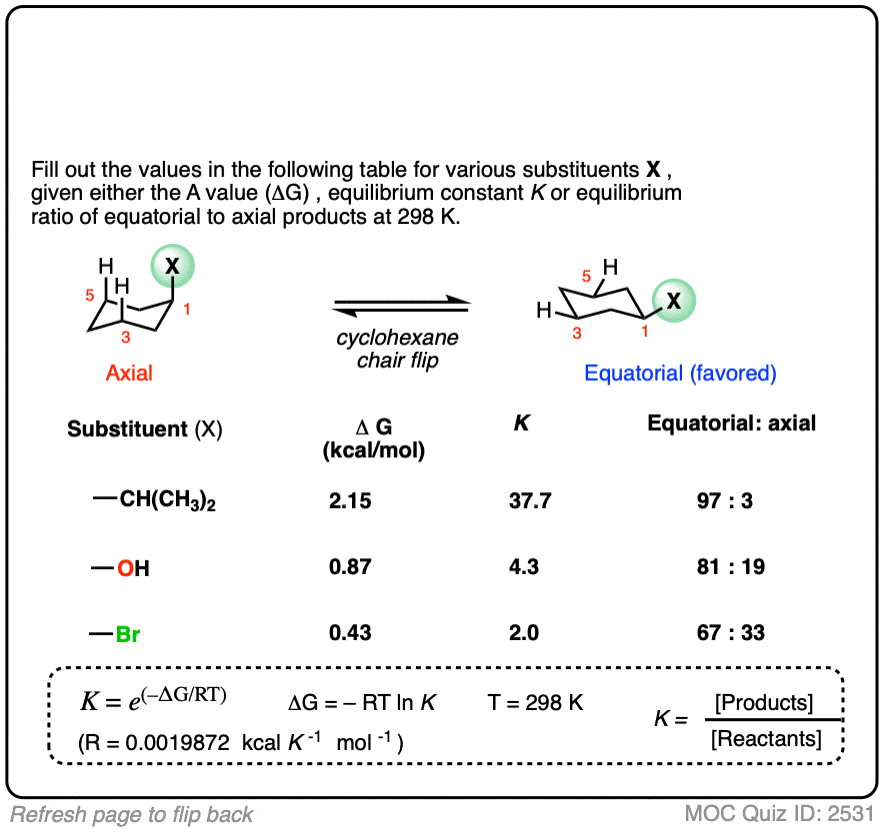
在下面的测试,填写完整的表格提供的信息:
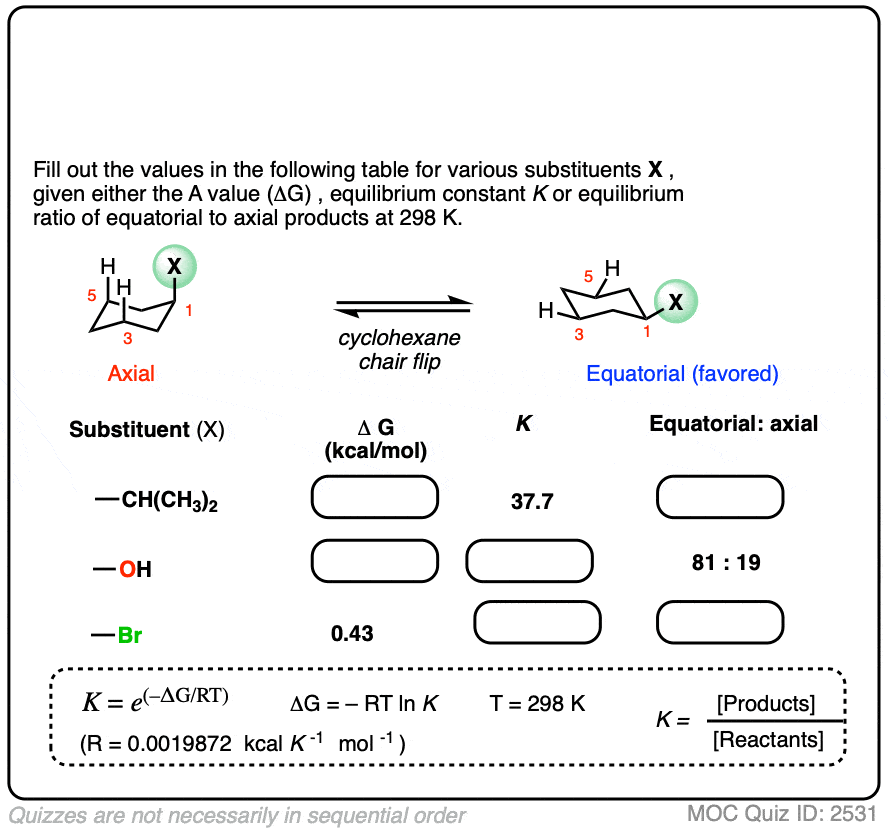 点击翻转
点击翻转
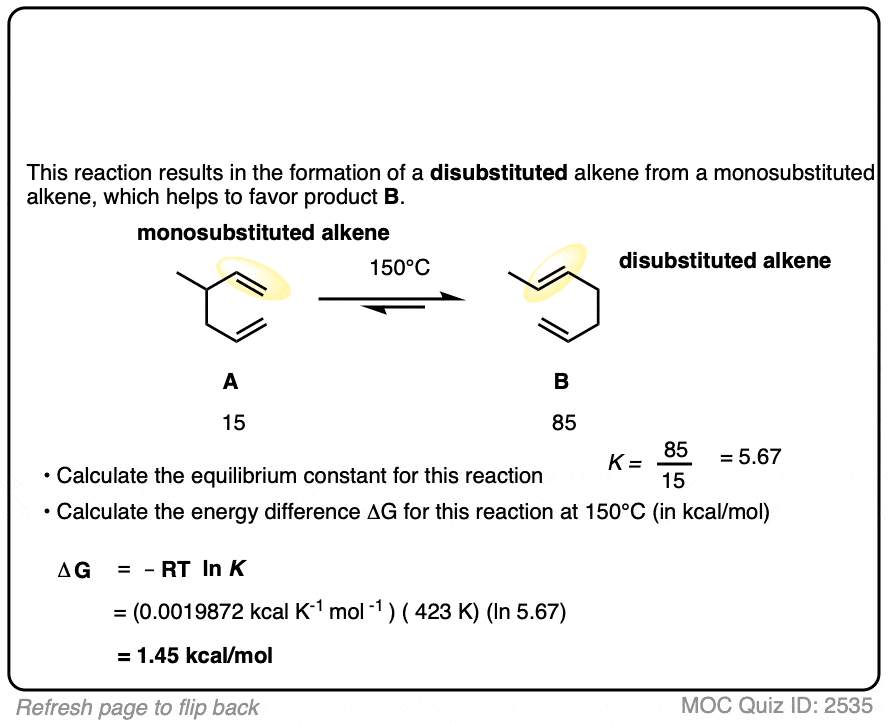
7所示。应用程序-烯烃反应
这是另一个例子也开始出现在有机化学2对大多数学生。
反应的具体细节并不重要对我们来说这是哈佛商业评论1,三丁基。在这篇文章的更多细节1、2 - 1、4-additions二烯烃。)
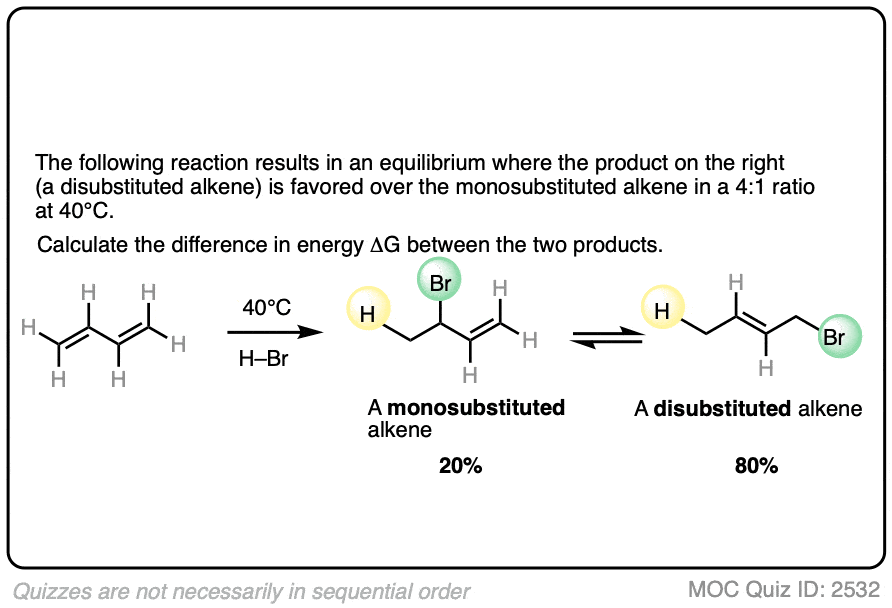
什么是重要的是,在一个反应的结果平衡两种产品形成的4:1比例支持呢双取代的烯烃的种烯烃。
使用这些信息,您应该能够计算不同的能源(ΔG)之间的两个产品当执行这个反应在40°C。
 点击翻转
点击翻转
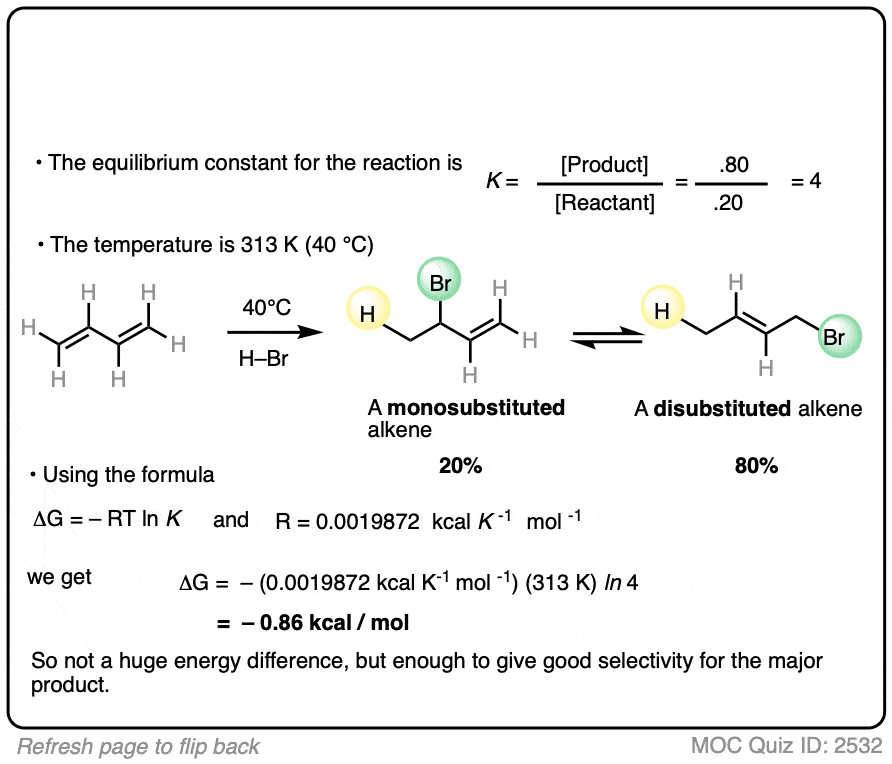
您可能已经了解到烯烃稳定性随替换,这是扎伊采夫规则的消除反应的基础。(见文章扎伊采夫规则)。这不是一个消除反应,但显示了同样的原则在起作用:取代烯烃更青睐。
有趣的是,单取代和双取代的烯烃之间的能量差异不是那么大见文章:烯烃的稳定性),但如本例中所示,可以导致很好的选择性的主要产品。
扎伊采夫的最终规则是基于能量的差异只有1千卡每摩尔左右!
8。应用程序——置换反应
我们也可以应用这些关系置换反应。
取代反应,就我们的目的而言,是一个债券形成和破碎在同一个碳。与酸碱反应,通常是作为平衡,置换反应往往是不可逆转的。(注5]
对于许多实际的卤代烃的亲核取代反应,能量的差异ΔG已经计算10至20千卡每摩尔。(裁判]
(这反映了切断更大的键的强度,碳氮,或碳碳债券相对于C-Cl, C-Br,或我债券以及更低碱度Cl (-), Br(-),或者我(-)离去基团相对于大多数的亲核试剂)。
使用其中的一个实验确定不同的能量计算平衡常数K是一个有用的练习。
在下面的练习中,计算反应的平衡常数之间的氢氧化钠和CH3Br在298 k给定不同的能量大约是16个千卡每摩尔。(裁判]
 点击翻转
点击翻转
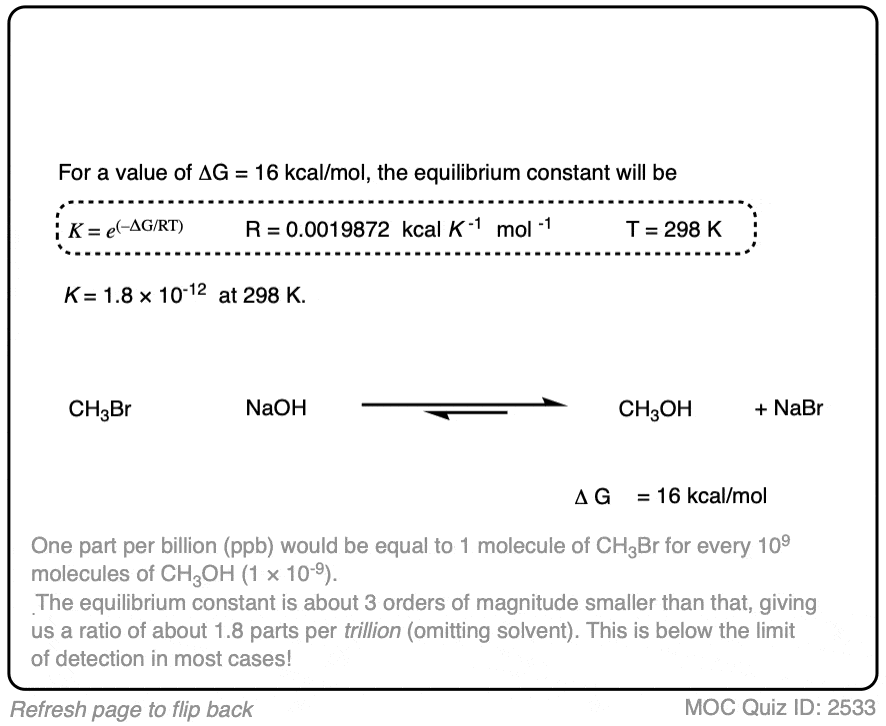
9。应用程序——Keto-Enol互变现象
我们的观光之旅的大二学生有机化学使用这个概念。无论如何,这是另一个例子应用平衡常数之间的关系和能量差异。
醛和酮,在平衡结构异构体称为他们的烯醇的形式。这个过程被称为keto-enol互变现象。(有关更多信息,请参见本文-酮烯醇互变异构)。这个反应的细节不关心我们这篇文章的目的,我们真的只会关注平衡常数和能量差异。
酮的比例:烯醇取决于许多因素,主要与羰基化合物的结构,尽管溶剂也可以发挥重要作用。
对于大多数的醛和酮,平衡强烈倾向于酮形式。例如,环己酮,平衡常数K形成的烯醇是2.0×10- - - - - -6。所以每个分子的烯醇酮数量的约一百万倍。
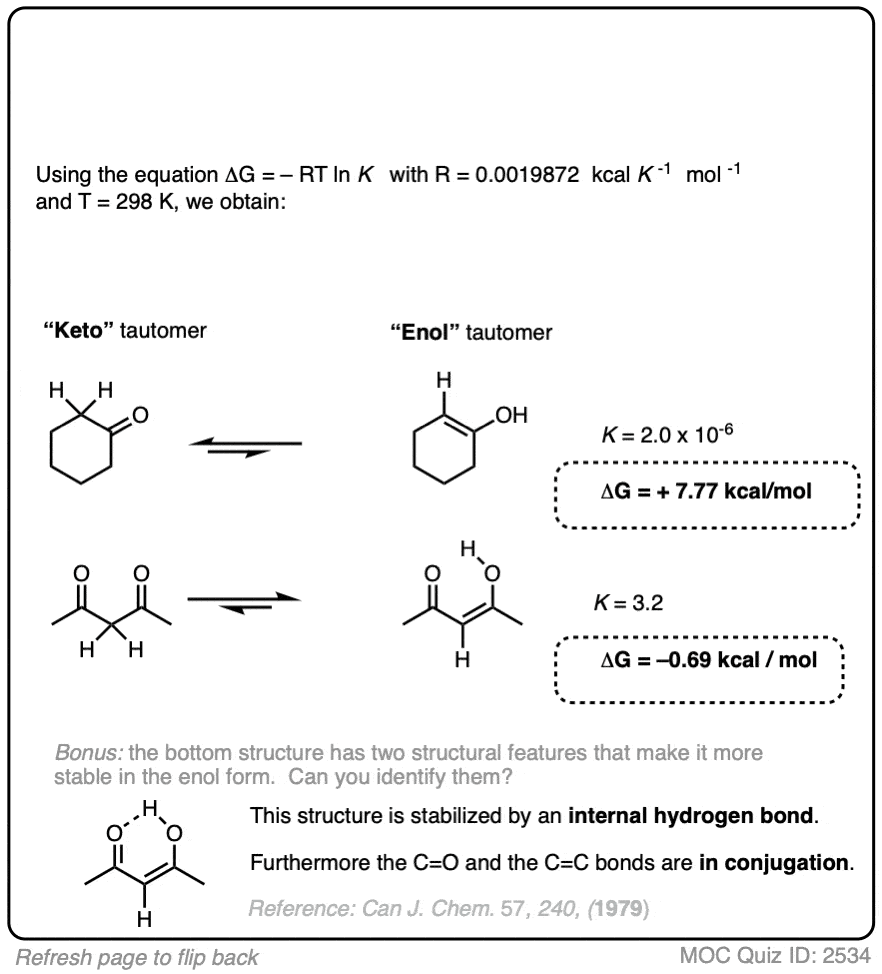
我们可以使用平衡常数,结合温度T计算之间的区别在能源ΔG酮和烯醇形式。
试试下面的练习中的两个例子:
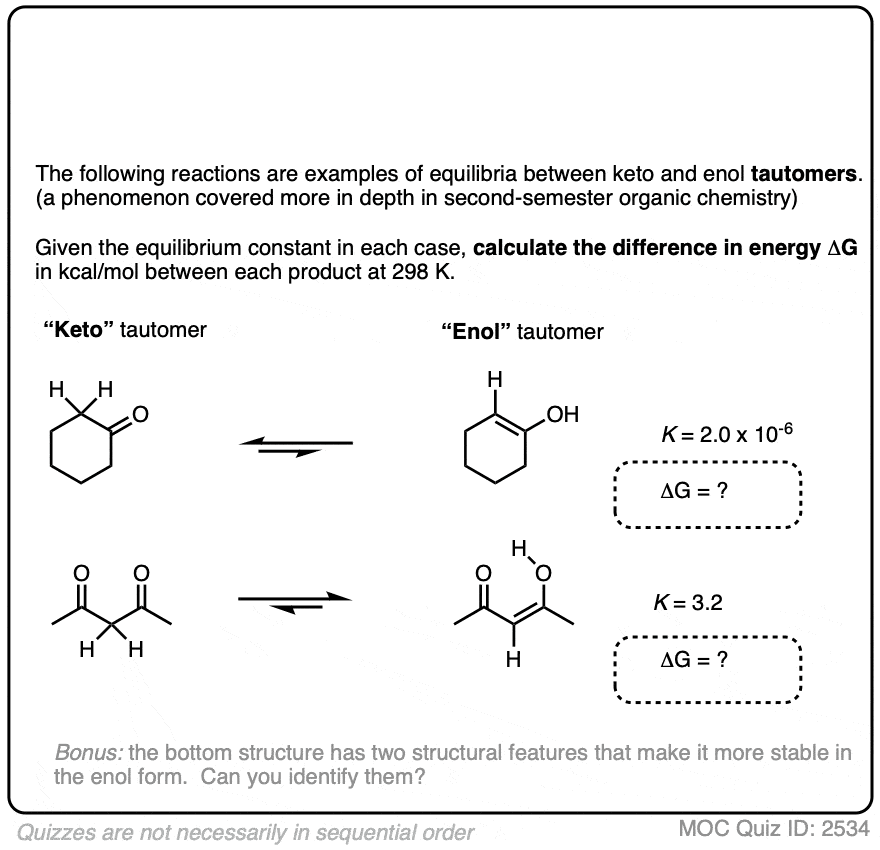 点击翻转
点击翻转
10。总结
在我们去之前,我应该强调,仅仅因为一个产品不是不一定使它的平衡不重要的。在许多情况下的反应,形成一个产品通过一个不利的平衡,但一旦形成,该产品是高活性在随后的反应,最终整个起始物料消耗。(一个典型的例子是去质子化酯的醇盐克莱森缩合- - - - - -见文章。注6)。
让我们总结一下要点。
- 平衡常数K两个物种之间能源ΔG有关他们的区别。知道一个值可以计算。
- 的能量差1千卡每摩尔听起来并不很多,但足以产生84:16比率在室温下的产品。改变三千卡每摩尔的能量足以产生一个99:1比率。
- 在较低的温度,平衡常数增加给予更大的选择性。
- 更高的温度减少选择性。
- 平衡常数之间的关系和ΔG介绍有机化学中可以应用在许多方面,包括(但不限于)取代环己烷(a值),烯烃,亲核取代反应,keto-enol互变现象。
笔记
注1。这里我说的“过程”,包括反应现象也像构象变化(如环己烷椅子翻转)。“过程”是一个很好的模糊词涵盖所有基地。
注2。为什么使用千卡?它只是发生在有机化学,因为很方便很多化学现象发生在从1 - 100千卡每摩尔,这使得值更容易记住。
例如,100千卡每摩尔的值对应于一个更强的键离解能量单键,乙烷的碳氢键离解能。
1千卡每摩尔的值对应于最低的一个相互作用的有机化学家经常考虑,两个重叠的扭转应变在乙烷碳氢键。(见文章:乙烷的交叉与重叠构象]
天平的一端,你有一个非常高能过程(碳氢键断裂),另一方面,一个非常低能交互(高度差排斥),和大量的其他现象。
只是容易,精神上,使用1 - 100的规模要比使用4.184到418.4范围内。可能不是这样在其他领域的化学,有机化学,千卡每摩尔方便。把,公制!
注3。一旦99:1产品开始变得很难精确测量小的数量的产品是因为我们的大部分技术用于确定产品比率涉及确定山峰下的面积在NMR(核磁共振)光谱或高效液相色谱(高压液相色谱)色谱和小山峰下的面积从基线噪音开始变得难以分辨。
如果“1千卡每摩尔是很多”,它是公平地说,“足够3千卡每摩尔”建立一个选择性的过程。
注4。这种关系是明确提到的优秀教材”现代物理有机化学“Anslyn和多尔蒂。强烈推荐上年有机化学专业和研究生。
注5。亲核取代反应更经常发现时可逆的亲核试剂与离去基团都是很弱的基地,也有类似的pK一个值。替代卤代烃和卤离子之间的反应是一个例子(例如CH3CH2Br +奈- > CH3CH2我+ NaBr)。
注6。在酸碱克莱森缩合反应是冷宫约8 pK一个单位和仍然运转良好。然而,是有限度的。一个不错的经验法则(从格罗斯曼的艺术写作的合理反应机制)是治疗反应的平衡常数1010以上基本上是不可逆转的。
测试你自己!
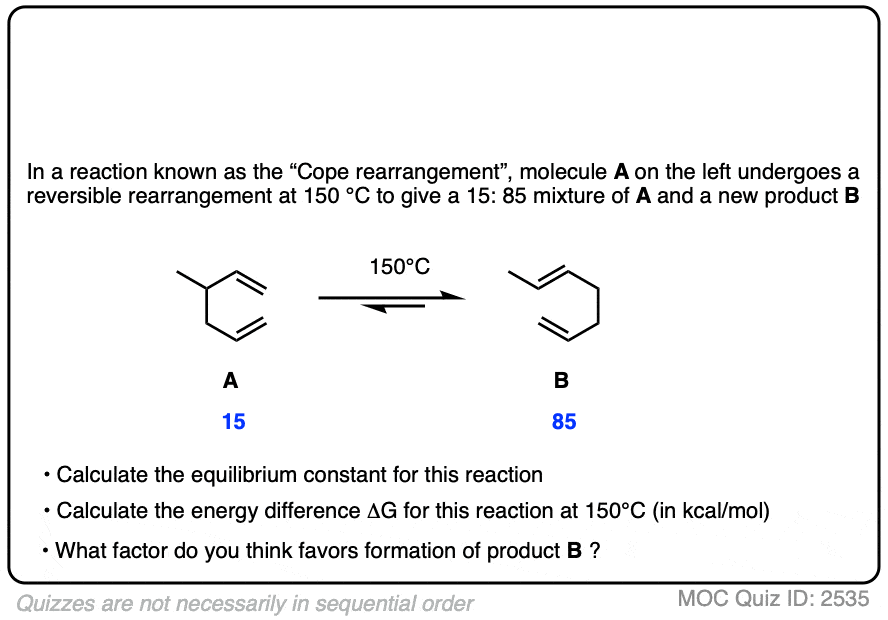 点击翻转
点击翻转
(高级)引用和进一步阅读
引用
- 相邻的碳和氢。第十九。t-Butylcyclohexyl衍生品。定量构象分析
美国Winstein和n·j·霍尔尼斯
美国化学学会杂志》上1955年77年(21),5562 - 5578
DOI:10.1021 / ja01626a037
一个关键论文引入“值”的概念,尤其是研究t丁基取代环己烷。 离子反应的机制。热离子置换反应
r . a . Ogg
反式。法拉第Soc。,1935,31日,1385 - 1392
DOI:10.1039 / TF9353101385
置换反应的热力学研究,发现乙醇烷基卤化物的反应,酚盐、醋酸、氢硫化物、氰化物、硫代硫酸盐和亚硫酸盐离子都是放热的10 - 20千卡每摩尔。
评论
评论部分