二烯烃和MO理论
应对和克莱森重组
最后更新:2023年2月14日|
表亲Diels-Alder:应对重排和克莱森重排
- 应对重排和克莱森重排pericyclic反应在同一家庭的Diels-Alder经过循环,6-electron协同过渡轨道对称性的州和遵守规则。
- 在本文中,针对学生在介绍有机化学课程中,我们将介绍这两个反应的例子,机制和应用。

表的内容
- 应对重排:例子和机制
- 应对重排是一个平衡
- 与环Cope-ing应变
- 的Oxy-Cope重排
- 克莱森的Rerrangement
- 克莱森重排的烯丙基苯基醚
- 氨基酸生物合成的克莱森重排
- 摘要:应对和克莱森重组
- 笔记
- 测试你自己!
- (高级)轨道对称性的应付和克莱森
- (高级)合成Periplanone B
- (高级)引用和进一步阅读
1。应对重排:例子和机制
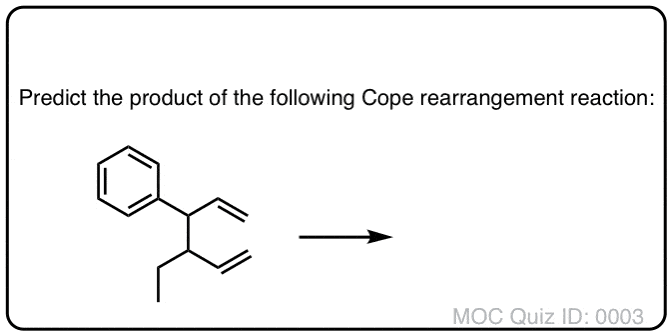
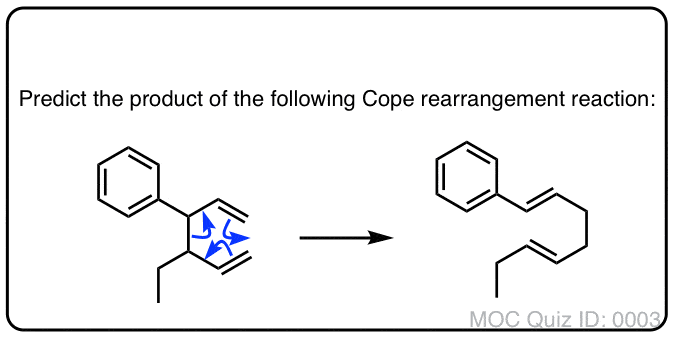
下面的反应被称为应对重排。在这个反应中,一个加热1,5-diene 150°C的温度(或更高版本)于是起始物料给重新安排产品。

Ta-daa ! !
上面的例子是最简单的例子(“堕落”应对重排)向本身只是重新排列。
如果你被这个判断应对重排反应(像我一样,一次)你会原谅来的结论变态的无用的。相信我当我说它不是。(请注意]
让我们检查和打破债券形式:
- 两个碳碳π键形成碳碳σ键(+)
- 两个碳碳π键断裂(加上一个碳碳σ键)。
那么它是如何工作的呢?
像Diels-Alder反应,应对重排属于一个大家庭的反应称为“pericyclic”反应。共同应对重排穿过,没有指控中间体环过渡态。

应对重排也是一个单键转移的“重排的例子一个σ键(及其取代基)交换末端共轭π系统(注1]
2。应对重排的产品是处于平衡状态的原始材料
应对重排的产品也将成为1,5-diene,因此能够接受相反的反应。
因此反映出产品的分布平衡起始物料和重新安排产品。
在简并应对重排(上图)看看正在发生什么是不可能的,因为起始物料是一样的产品。(注2——有一个解决这个问题的办法使用isotopically碳“标签”]
所以平衡怎么可能倾向于一些实际上,你知道,有用的吗?
还记得扎伊采夫规则吗?(即。”代替烯烃赢了”)。烯烃稳定略有增加(例如,约1 - 2千卡每摩尔)连续碳氢键上烯烃取而代之的是碳碳键。
1 - 2千卡每摩尔可能听起来不算多,但是这足以推动一个反应很好地前进!
在简单的情况下,就把一个甲基双取代的结果重新安排产品供给烯烃而不是单取代烯烃。结果是一个产品的85:15混合物(5:1)。(注3]

的例子开始,由阿瑟应付和伊丽莎白·哈迪在1940年,有一个三代的烯烃重新安排一个tetrasubstituted烯烃这也是与一个接合酯和一个腈。这是获得作为一个单一的产品。(注意4]
3所示。与环Cope-ing应变
应对重排,真的将自己的肘部的规模对形成一个产品有一个碳碳σ键,是一个紧张的环系统的一部分。这重排”独联体-divinylcyclopropane”发生低于室温。(注5]

仔细看!尽管有些奇怪的反应,它的债券形式相同的模式和休息!
化学家们已经采取这些strain-driven应对重组更疯狂的极端。这是没有”牛”有一个分子没有固定的结构,因为它的不断Cope-ing本身。(注6]
4所示。的Oxy-Cope重排
在上面的例子中我们看到,即使是一个卑微的颈- 3甲基是足以应付重排产品有用5:1比例。
沿着这些线路,据报道到,伟大的教授杰罗姆Berson(琼斯和他的博士后梅特兰教授,纽约大学和教科书的名声)在1964年的应付重排3-hydroxy取代1,5-diene导致烯醇产品。

如果你认为——回家硼氢化反应和炔烃oxymercuration,你可能会记得,烯醇不会呆很长时间。
通过一个过程称为酮烯醇互变现象,烯醇经历rearangement变成酮(或醛,取决于原料的结构)导致不可逆的形成我们称之为“γδ”不饱和醛或酮。(看到帖子:Keto-Enol互变现象)
酮烯醇互变现象是一种平衡,通常更喜欢酮形式由于切断π键的强度与碳碳π键。(请注意7]。至少在一个情况下,平衡测量约为105支持酮)
像应付重排,Oxy-Cope仍然需要大量的加热。(Berson-Jones的一个例子涉及加热密封管在320°C。) (注8如何让这个更快]
5。克莱森的重排
应对重排的表兄是一个过程(1912)被称为“稍显陈旧克莱森重排。(是的,这是相同的路德维希·克莱森负责克莱森缩合)。这也是一个pericyclic反应。
在克莱森重排乙烯基烯丙基醚加热给γ、δ(γ、δ)不饱和羰基。

- 碳碳σ键,碳碳π键,切断形成π键。
- 两个碳碳π键坏了(和切断σ键)。
如果我们比较债券的能量与形式的债券,我们看到,我们交易相对较弱的碳碳π键(约65千卡每摩尔)相对强劲的碳氧π键(约85千卡每摩尔)获得约20千卡每摩尔。
(碳碳σ键的键离解能和切断σ键大致相同(大约85千卡每摩尔所以他们基本上抵消了)
反应在产品约20千卡每摩尔(~ 85焦每摩尔)比反应物更稳定是对所有的意图和目的不可逆转的。这只是一个特性使克莱森重排所以有价值。注意9]
那么它是如何工作的呢?从arrow-pushing的角度来看,它看起来很像应付重排!

我们不会进入这里的克莱森重排的立体化学,但足以表示,通常遵循一个非常可靠的模式,使其立体选择合成的主力。(注意10]
6。克莱森重排的烯丙基苯基醚
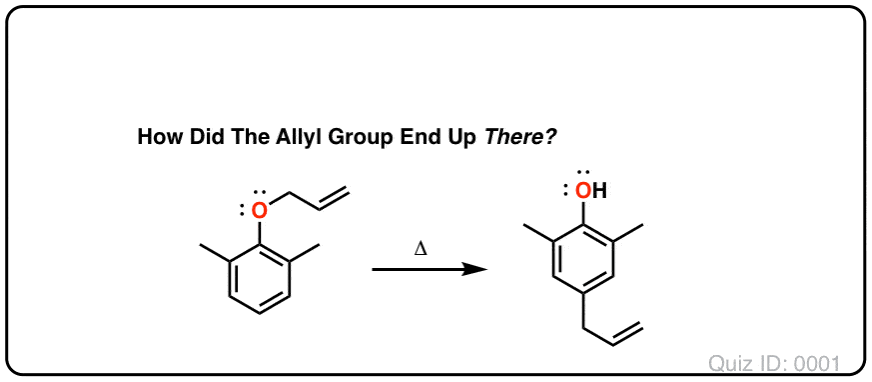
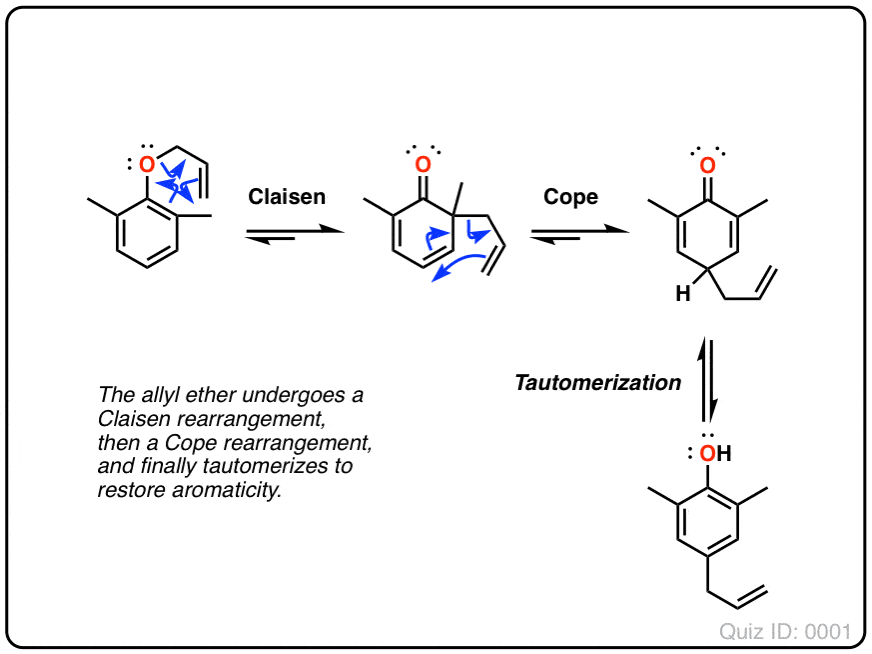
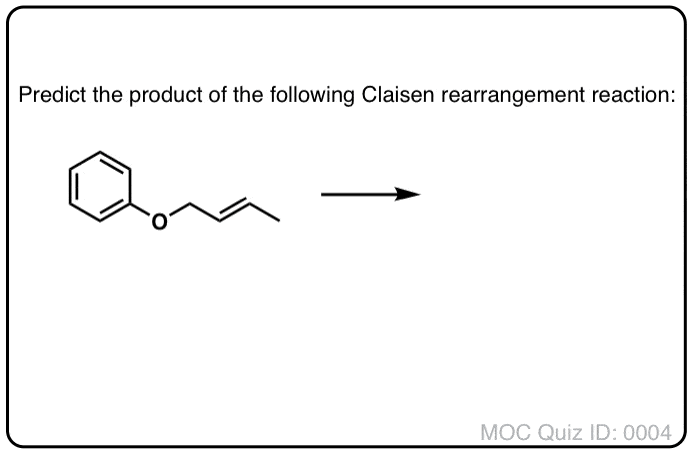
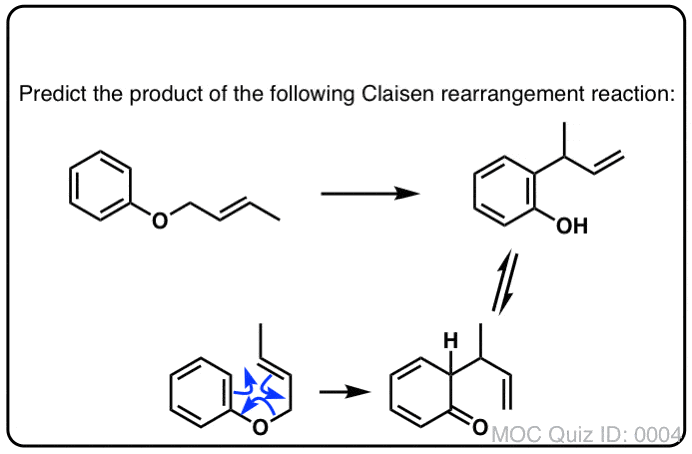
芳香pi系统也可以参与克莱森重排。加热烯丙基苯基醚(注意11)导致克莱森重排导致γ,δ不饱和内酯。

尽管克莱森重排停止,第二个反应立即发生(并不能停止)。
如果你所投保的芳香性,那么你会意识到克莱森重排不再的产物芳香;sp的3碳连着4σ键使接合在环。
凑巧的是,这是另一个酮的机会烯醇互变现象,提高它的头,虽然这一次的驱动力是相反的方向(从酮烯醇)!原因是由芳香性的稳定(共振能量> 30千卡每摩尔)超过弥补了较小的不同能量(请注意7酮和之间的)烯醇形式。
会发生什么如果昊图公司立场是屏蔽了吗?看你能不能找出这个有趣的(嘿)机制。

7所示。克莱森的重排
事实证明,克莱森重排的发生在生物体中。如您所料,而不是忍受加热到150°C,自然发现了一种方法和一种酶催化反应。
下面是画的重排chorismate prephenate。这个反应是由酶催化chorismate变位酶,导致速度加速度约106。注意债券的模式形成和破碎的——尽管这些分子,有些时髦的外观完全相同的模式bond-breaking和bond-forming发现在上面的反应。

为什么这是生物合成途径重要?这是一个关键的一步莽草酸途径负责生物合成的必需氨基酸色氨酸、苯丙氨酸和酪氨酸。这个途径并不在动物(包括人类)——这就是为什么我们必须获得这些氨基酸膳食来源。
8。摘要:应对和克莱森重组
我们只是几乎无损的表面处理和克莱森重组,但对于大多数学生在导论课程,这就足够了。
- 像所有pericyclic反应,应对和克莱森重组的bdapp平台Woodward-Hoffman规则轨道对称性有关。应付的轨道对称性和克莱森重组可能是超出了大多数入门课程材料但办理附录下面
- 同样的立体化学的细节,包括椅(有时船!)的几何过渡状态被忽视了。好一段时间,看看经典Doering-Roth实验。梅特兰琼斯在他还讨论了他们教科书。
- 处理的应用和克莱森合成举不胜举。超过15克莱森重排的变体存在,和一些最近才被开发出来。有机化学是一个生活和活动纪律,新的发现不断发表!
笔记
的活化能应对的是33千卡每摩尔。的活化能克莱森重排的约30千卡每摩尔。(参考文献]
注1。IUPAC定义了一个“单键转移的重排“作为一个pericyclic反应涉及新σ键的断裂和形成π的总数和σ债券不改变。
注2。人们可以观察的“堕落”应对重排13C NMR如果要安装一个13C标签的一个终端烯烃原子的5-diene(说,颈- 1在我们的图)。的位置平衡的解决可以通过观察监测的外观13C标记亚甲基(CH2)组。
注3。用吉布斯自由能关系(ΔG = rt ln K),比150°C的85:15对应的能量差为1.5千卡/摩尔。不需要太大的能量差推动平衡一个有用的比!
注4。最初的报告在应对重排阿瑟应对和伊丽莎白·哈代:

注5。只有独联体- - - - - -divinylcyclopropane将很容易。的反式二乙烯基环丙烷必须加热到190°C,以重新排列自环丙烷需要片段。(江淮1972 94 5910]
注6。Bullvalene(下图)分子没有固定结构。生活是一系列的应对重组;所有碳原子化学位移等价的。

注7。迈威尔公司测量了平衡常数约为105所以通过吉布斯方程这将把能量差约为7千卡每摩尔。
注8。这似乎抑制了反应的应用程序,而是十年后埃文斯和Golob发现用氢化钾治疗起始材料把Oxy-Cope重排成超光速推进装置,降低活化障碍太多(大约10 - 15千卡每摩尔)反应可能发生在室温或以下。这是现在被称为“阴离子Oxy-Cope重排”。的有趣的例子Oxy-Cope导致蟑螂性信息素的合成periplanone B,看到附录。
注意9。从综合的角度来看,一个微妙的特性,使得克莱森重排有用的是它交易债券相对容易使(切断)债券相对困难(碳碳)在一个可预测的方式。(例如我们学到几个方面通过切断债券威廉姆森醚合成,添加醇类烯烃和炔烃以及各种其他进程)。
注意10。一个迷人的细节克莱森重排是立体化学信息的转移。如果切断债券和双键立体选择的方式构造(s) (E或Z)那么这个几何可以传送到新的手性中心的形成有可预测的立体化学。这尤其发达爱尔兰酯烯醇化物克莱森重排。
注意11。很容易由威廉姆森醚合成,对吧?
测试你自己!
 点击翻转
点击翻转
 点击翻转
点击翻转
 点击翻转
点击翻转
 点击翻转
点击翻转
(高级)轨道对称性的应付和克莱森重组
pericyclic反应,因此Diels-Alder反应的亲戚,你图轨道对称性所出现的地方让我们解释处理和克莱森重组“热允许”。
最简单的方法想出这些反应的轨道是想象他们两个烯丙基片段相互结合。如果我们认为人类的烯丙基自由基(我们讨论它在这里)人类的分子轨道终端叶反相,该中心是一只长相怪异的点(因为一个节点通过中央碳)。

如果你把两个烯丙基自由基这种方式轨道排列好。我们没有进入细节处理过渡态的几何形状,但它往往是一个比作物种,这就是为什么它是这种方式所吸引。
我们一直很简单。应对的机制仍在调查,还有通路的过渡态真的像两个烯丙基自由基的组合!
(高级)应用氧处理的合成:蟑螂性信息素
正如上面提到的,哈佛大学的大卫·埃文斯和他的合作者a Golob报道1975年oxy-Cope重组显著如果羟基deprotonated加速条件下的地方醇盐离子与由此产生的反离子弱协调。这导致了许多令人兴奋的天然产物合成的冒险。
一个相当简单的方法是添加一个设置乙烯基格氏试剂β,γ不饱和酮,紧随其后的是轻微的加热。在下面的案例中,60°C是足够的!
蟑螂信息素的合成periplanone B教授斯图亚特·l·施赖伯(现在耶鲁,哈佛大学)和研究生康拉德Santini Woodward-Hoffman规则是一个主类。

它始于一个光化学[2 + 2]环加成作用使二环环系统。添加一个乙烯基格氏设置阴离子Oxy-Cope[3 3]单键转移的重排导致一个高度紧张的环丁烯。这经历热electrocyclic开环给随后的二烯环氧大蟑螂信息素。
好玩的部分。
信息素合成,施赖伯然后Santini着手寻找蟑螂在耶鲁大学化学楼的地下室:

感觉一定是什么。
大量的引用,只是因为这些反应都是真正有趣的和有用的。
- 替换的引入乙烯基组。诉涉及迁移重排的烯丙基集团在3个碳系统
阿瑟和伊丽莎白·m·哈迪
美国化学学会杂志》上1940年,62年(2),441 - 444
DOI:10.1021 / ja01859a055
最初报告的反应被称为重排。应对重组及其变体(如oxy-Cope和阴离子oxy-Cope重组)(3 3)单键转移的重组。这是一个协调一致的反应和是一个平衡的过程。这是教授亚瑟粘土处理命名,他是麻省理工学院的一位教授。美国化学学会命名的奖项,亚瑟应付和处理学者奖,跟随他。 - 两个烯丙基自由基的重叠或四中心过渡态的重排
w·冯·e·林根R w·罗斯
四面体,1962年,18,67 - 74
DOI:10.1016 / 0040 - 4020 (62)80025 - 8
在这个经典研究中,冯林根和罗斯提出了一个六元环比作美国的过渡状态应对重排重组的基础上非对映的前兆。以下论文Oxy-Cope重排。这变种提供了热力学水槽,因为重组的结果烯醇,发生互变现象酮/醛,提供一个热力学驱动力。 - 酮的合成3-Hydroxy-1热异构化,5-hexadienes。的Oxy-Cope重排
Jerome a Berson琼斯和梅特兰
美国化学学会杂志》上1964年,86年(22),5019 - 5020
DOI:10.1021 / ja01076a067
这是第一篇论文描述了重排,是“Oxy-Cope”一词的起源,是作者提出的。 - 逐步Oxy-Cope重排的机制
Jerome a Berson和梅特兰。琼斯
美国化学学会杂志》上1964年,86年(22),5017 - 5018
DOI:10.1021 / ja01076a066
Oxy-Cope的一个变体阴离子Oxy-Cope重排,它使用产生的基础醇盐,它生成一个烯醇化物离子重排后,允许显著降低温度相比,传统的处理或Oxy-Cope反应。 - (3、3)单键转移的重组,5-diene醇盐。强大的加速的影响醇盐取代基
d·a·埃文斯和a . m . Golob
美国化学学会杂志》上1975年,97年(16),4765 - 4766
DOI:10.1021 / ja00849a054
上的第一个出版阴离子Oxy-Cope重排。开创性的。 - 宏观展开方法:中等环合成基于八单元环扩张过程
Paul a .前进,斯科特m cn。Sieburth约瑟夫•j . Petraitis苏尼尔•k•辛格
四面体1981年,37(23),3967 - 3975
DOI:10.1016 / s0040 - 4020 (01) 93271 - 5
一个应用程序的阴离子Oxy-Cope重排合成的重点,从实验室的教授Paul a .前进(现在在斯坦福大学)。 - 超级Umlagerung冯在C高烯丙基苯酚allylathern应承担phenole
l·克莱森
化学。的误码率。1912年,45(3),3157 - 3166
DOI:10.1002 / cber.19120450348
第一个报告(3 3)烯丙基的热重排苯基醚,随后被命名克莱森重排后发现,路德维希克莱森。 - 的重排乙烯基烯丙基醚
查尔斯·d·赫德和麦克斯韦·波拉克美国化学学会杂志》上 1938年 60(8),1905 - 1911
DOI:10.1021 / ja01275a051
利用热化学测量,烯丙基的重排乙烯基 醚给allylacetaldehyde被发现的约24千卡每摩尔(100.6焦每摩尔)在这项研究。 - 克莱森重排的机制:似曾相识
布鲁斯Ganem
Angew。化学。Int。。1996年,35(9),936 - 945
DOI:10.1021 / anie.199609361
审查机制的克莱森重排,溶剂效应、催化、立体效果,酶催化。 - 克莱森重排过去九年
安娜·m·马丁·卡斯特罗
化学评论2004年,104年(6),2939 - 3002
DOI:10.1021 / cr020703u
克莱森重排的全面审查,大量的例子证明这个反应的底物范围和应用化学。 - 5β-cholest-3-ene-5-acetaldehyde
爱尔兰和d·j·r·e·道森
Org。Synth。1974年,54,71年
DOI:10.15227 / orgsyn.054.0071
的一个例子涉及串联克莱森重组的过程。这是来自有机合成可靠来源的独立测试有机化学过程。经典的几个变种克莱森重排了——两个最受欢迎的是如下: - 简单的立体选择版本的克莱森重排导致反式三代的烯键。角鲨烯的合成
卢修斯Werthemann威廉•约翰逊夏天威廉·r·巴特利特,蒂莫西·j·Brocksom Tsung-Tee李·d·约翰·福克纳和迈克尔·r·彼得森
美国化学学会杂志》上1970年,92年(3),741 - 743
DOI:10.1021 / ja00706a07411
加热一个烯丙基的酒精过量的三烷基乙酸存在微量的弱酸orthoester混合。从力学上看,orthoester失去酒精生成烯酮缩醛(3、3),经历了一个单键转移的重排给g, d-unsaturated酯。这是众所周知的Johnson-Claisen orthoester重排之后,它的开发者,w·s·约翰逊教授,斯坦福大学化学系。 - 克莱森重排的烯丙基酯类
罗伯特·e·爱尔兰和理查德·h·穆勒
美国化学学会杂志》上1972年,94年(16),5897 - 5898
DOI:10.1021 / ja00771a062
烯丙基三甲基硅烷基烯酮的重排缩醛树脂由的反应烯丙基的酯与TMSCl烯醇化物。这被称为Ireland-Claisen(甲硅烷基烯酮缩醛)重排,开发人员后,教授罗伯特•爱尔兰。这种反应是温和得多的优势条件是可能的。 - 拆分克莱森重组:开发的第一代不对称Acyl-Claisen反应
Tehshik p Yoon和大卫·w·c·麦克米伦
美国化学学会杂志》上2001年,123年(12),2911 - 2912
DOI:10.1021 / ja015612d
这是克莱森重排的现代发展的一个例子。这是教授的论文之一麦克米伦(普林斯顿大学)已经发表在不对称克莱森重组的面积。
非常感谢这个出版这一课。我学到了很多。