首页/亲核试剂攻击亲电试剂
有机化学学习小贴士
亲核试剂攻击亲电试剂
最后更新:2021年3月27日|
我的博士生导师的博士生导师曾被引用过一句话:基本上,所有有机化学反应都归结为亲核试剂攻击亲电试剂”。
想想看。当你扩展你的概念亲核试剂除了那些会反应的物种烷基卤化物SN2反应包括芳烃和烯烃你在有机化学入门课上学到的几乎每一个反应都遵循这个原则。
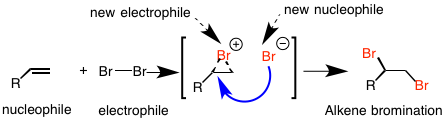
溴化:亲核试剂(烯烃)攻击亲电试剂(溴)给一个新的亲电试剂(bromonium离子)和一个新的亲核试剂(溴离子)进一步反应,得到相邻的二溴。说到这个,看看所有的烯烃加成反应:烯烃(亲核试剂)加上亲电试剂BH3,硫酸,Hg (OAc) 2,OsO4臭氧等等。
Friedel Crafts反应和相关反应是另一个例子:亲核试剂(芳)攻击亲电试剂(烷基或通过添加FeCl3或AlCl3生成的酰基碳正离子)。

看看Aldol反应:亲核试剂(烯醇化物)攻击亲电试剂(醛).烯醇酯是多功能亲核试剂。这是掌握的挑战之一羰基化学是理解亲核烯醇酯和亲电烯醇酯的“味道”金属羰基合物控件旁边的功能组会在调整时发生变化金属羰基合物.

甚至Diels-Alder反应也可以在这种情况下考虑:diene (亲核试剂)攻击双恋者(亲电试剂).

用更专业的术语来说,在所有这些例子中所描述的都是由轨道中占据最高的分子轨道(HOMO)重叠而形成的新化学键亲核试剂具有最低的未占据分子轨道(LUMO)亲电试剂.简而言之,有机化学中大多数反应的本质是电子从富电子(亲核)位点流向低电子(亲电)位点。
你能想到任何例外吗?
01键合、结构和共振
02酸碱反应
03烷烃和命名法
04构象和环烷烃
05有机反应入门
- 学习一种新反应时最重要的问题
- 组织中的4类主要反应
- 学习新的反应:电子如何移动?
- 电子如何(为什么)流动
- 学习一个新的反应时要问的第三个最重要的问题
- 有机化学中稳定负电荷的7个因素
- 有机化学中稳定正电荷的7个因素
- 常见错误:形式上的指控会产生误导
- 亲核试剂和亲电试剂
- 曲线箭头(用于反应)
- 弯曲箭头(2):最初的反面和最后的正面
- 亲核性与碱性
- 三类亲核试剂
- 什么是好的亲核试剂?
- 什么是好的离去基?
- 3个稳定碳正离子的因素
- 碳正离子不稳定的三个因素
- 什么是过渡态?
- 哈蒙德的假设
- 格罗斯曼的统治
- 先画丑的版本
- 学习有机化学反应:核对表(PDF)
- 加成反应简介
- 消除反应简介
- 自由基取代反应导论
- 氧化裂解反应导论
06自由基反应
07立体化学和手性
08置换反应
09消除反应
11SN1 SN2 / E1、E2的决定
12烯烃的反应
- 烯烃的E、Z表示法(+ Cis/Trans)
- 烯烃的稳定性
- 加成反应:消去的反义词
- 选择性vs.特异性
- 烯烃加成反应的区域选择性
- 烯烃加成反应的立体选择性:Syn与Anti加成
- 烯烃中盐酸的马氏加成法
- 烯烃加氢卤化机理及其对马氏规则的解释
- 箭推和烯烃加成反应
- 添加模式#1:“碳正离子途径”
- 烯烃加成反应中的重排
- 烯烃的溴化
- 烯烃的溴化反应机理
- 烯加成模式#2:“三元环”途径
- 硼氢化反应——烯烃的氧化
- 烯烃的硼氢化氧化机理
- 烯烃添加模式#3:“协同”途径
- 溴离子的形成:一个(次要)推箭困境
- 第四种烯烃加成模式-自由基加成
- 烯烃反应:臭氧分解
- 概述:烯烃反应机理的三个关键家族
- 钯对碳(Pd/C)催化加氢
- OsO4(四氧化锇)用于烯烃的二羟基化
- 间氯过氧苯甲酸
- 合成(4)-烯烃反应图,包括卤代烷基反应
- 烯烃反应练习题
13炔的反应
14醇,环氧化合物和醚
- 醇。命名法和性质
- 酒精可以充当酸或碱(以及为什么它很重要)
- 醇类-酸性和碱性
- 威廉姆森醚合成
- 威廉姆森醚合成:规划
- 烯烃、叔烷基卤化物和烷氧汞的醚
- 醇通过酸催化合成醚
- 醚与酸的裂解
- 环氧化物-醚家族中的异类
- 用酸打开环氧化物
- 环氧环开口与基地
- 从醇中制取烷基卤化物
- Tosylates和Mesylates
- PBr3和SOCl2
- 醇的消除反应
- POCl3消除醇生成烯烃的研究
- 酒精氧化:“强”和“弱”氧化剂
- 揭开酒精氧化机制的神秘面纱
- 醇和醚的分子内反应
- 酒精保护团体
- 硫醇和硫醚
- 计算碳的氧化态
- 有机化学中的氧化与还原“,
- 氧化梯子
- 醇制卤代烃的SOCl2机理:SN2 vs SNi
- 酒精反应路线图(PDF)
- 酒精反应练习题
- 环氧反应测验
- 氧化还原练习测验
15有机金属化合物
16光谱学
17Dienes和MO理论
- 有机化学中会发生什么
- 这些分子是共轭的吗?
- 有机化学中的共轭与共振
- 成键和反键轨道
- 烯丙基阳离子、烯丙基自由基和烯丙基阴离子的分子轨道
- 丁二烯的分子轨道
- 二烯反应:1,2和1,4加成
- 热力学和动力学产物
- 更多在1,2和1,4添加到双烯
- 顺式和反式
- Diels-Alder反应
- Diels-Alder反应中的环二烯和亲二烯
- Diels-Alder反应的立体化学
- Exo vs Endo产品在Diels Alder:如何区分他们
- Diels Alder反应中的HOMO和LUMO
- 为什么Endo vs Exo产品在Diels-Alder反应中更受青睐?
- Diels-Alder反应:动力学和热力学控制
- 复古Diels-Alder反应
- 分子内Diels Alder反应
- Diels-Alder反应中的区域化学
- Cope和Claisen重排
- Electrocyclic反应
- 电循环环开启和关闭(2)-六(或八)π电子
- Diels Alder练习题
- 分子轨道理论实践
19芳香分子的反应
- 亲电芳香族取代:简介
- 亲电芳香族取代反应中的激活和失活基团
- 亲电芳香族取代反应机理
- 亲电芳香族取代中的邻位、对位和元位董事
- 理解Ortho, Para和Meta director
- 为什么卤素是正对位的?
- 双取代苯:最强电子供体“胜出”
- 亲电芳香族取代(1)-苯的卤化
- 亲电芳香族取代(2)-硝化和磺化
- EAS反应(3)- Friedel-Crafts酰基化和Friedel-Crafts烷基化
- 分子内Friedel-Crafts反应
- 亲核芳烃取代(NAS)
- 亲核芳香族取代(2)-苄基机制
- “苄基”碳的溴化与氧化反应
- Wolff-Kishner, Clemmensen和其他羰基还原
- 芳香族侧链上的更多反应:硝基还原和拜耳Villiger反应
- 芳香族合成(1)-“操作顺序”
- 苯衍生物的合成(2)-极性反转
- 芳族合成(3)-磺酰基阻滞基团
- 桦树减少
- 合成(7):苯及相关芳香族化合物的反应图谱
- 芳香族反应与合成实践“,
- 亲电芳香取代的实践问题
很抱歉这么晚才在一个老话题上发表文章。基本上我是一个生物化学的学生,谷歌总是帮助很多,我经常上你的网站,这是非常有帮助的,所以谢谢你。我读了这篇文章,一生都无法停止思考“亲核试剂攻击亲电试剂”的事情。我知道大多数反应都是这样发生的,但是亲电取代/加成呢如果这两种反应是一样的。我知道像碳正离子这样的阳离子一般不存在因为它们不稳定,只能在亲核作用下形成,最近几节课这个问题一直困扰着我因为我注意到的都是一些负电荷攻击一个正电荷我这辈子都想不出任何例外。那么亲电取代在这个过程中处于什么位置呢?是不是在亲电机制中,溶剂对分子做了什么让分子先变成阳离子然后亲核试剂攻击?能不能说亲电取代和亲核取代基本上是对等的?那到底有什么区别呢?谢谢!
你网站的忠实粉丝。
关于弗里德尔·克拉夫特酰基化反应中酰基阳离子中间体的几何结构还有一个问题。既然一个共振结构是线性的(碳与碳的三键结合),而另一个共振结构在这里被描述为“弯曲的”(碳与碳的双键结合),你认为共振杂化物是线性的、弯曲的,还是介于两者之间?
你好,乔纳森!
你提出了一个很有趣的问题。请允许我对这场辩论发表意见。
酰基离子的线性共振结构是氧鎓离子:正电荷定位在氧原子中。氧的电负性很强,比碳的电负性更强。因此,氧离子阳离子很难稳定(尽管自然界中有这样的例子——花青素),因此这种共振结构对共振氢化物的贡献应该很小。
我认为共振杂化的角度会比典型的sp2碳的120度角大一点。
恐怕我不同意。为什么分子会选择弯曲?它可以是sp杂化和线性的,把正电荷放在碳的p轨道上,使C-R sigma键能量更低,因为它有更多的s轨道,或者它可以是sp2杂化和sp2轨道上的电荷。在我看来,对于非酰基阳离子来说,空间和电子的惩罚不是线性的。