SN1 SN2 / E1、E2的决定
决定SN1 SN2 / E1 / E2(4) -温度
最后更新:2022年11月29日|
快速确定N '肮脏的指南SN1/SN2/E1/E2第4部分:温度的作用
快速N的肮脏的指南SN1/SN2/E1/E2包括分析四个关键变量,为了他们的重要性。
今天,我们会解决最后一个变量来考虑:温度。
之后如果你一直到目前为止,您可能已经注意到,此时我们应该能够区分所有情况SN2是喜欢E2(反之亦然),但仍留下这个难题:当碳正离子形成时,我们如何确定SN1或E1产品喜欢吗?
如果你需要这些反应进修,阅读这些回来:
我们如何确定SN1和E1将主导一次碳正离子形成了吗?
首先,注意第一步的SN1和E1反应是相同的:失去一个离去基团给一个碳正离子。自这两个反应进行通过相同的中间,在实践中混合物的这两个SN1和E1产品会发现每当反应通过吗碳正离子(在可能的情况下]。
鉴于此,然而,我们仍然要根据经验告诉我们什么类型的产品在大多数情况下应该是主要产品。
然而,回想一下,消除反应的热量(见文章:消除反应的热量)
在这种情况下,取代反应和消除反应在相互竞争,提高温度会增加消除产品的数量。
这是一个代表性的例子:
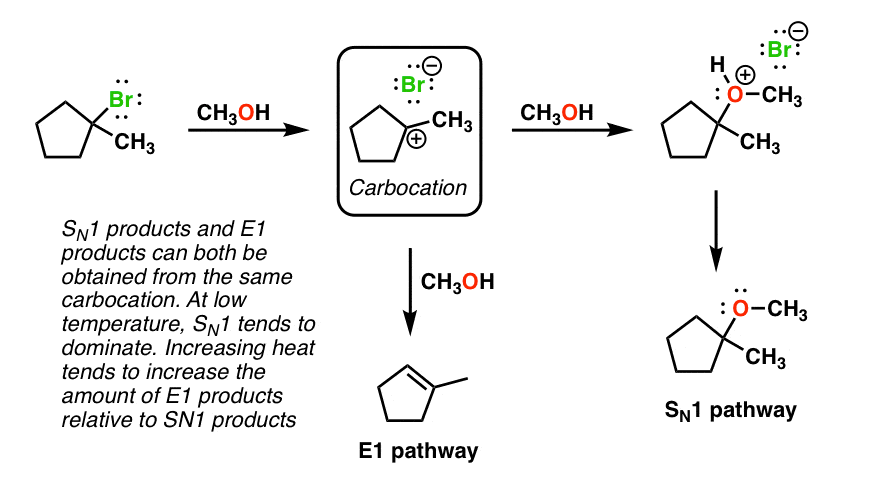
- 溴离子从三级的损失烷基溴化底物导致的形成三级碳正离子(稳定,因此没有重排]。
- 在低温度,SN1通路(上图)主导;碳正离子受到CH3哦,失去质子给紧随其后醚产品。
- 通路(底部E1)——清除附近的氢碳碳正离子,小在低温度(注意多取代的形成烯烃在这里,扎伊采夫规则在行动]。
- 然而,随着温度的增加,大量的消除相对于替换应该逐渐增加。
这将导致以下快速N '脏的经验法则。
如果“热”是指出,反应将有利于E1 / SN1
快速N '脏规则# 6:
(注意:在这些反应模式应用于衬底之前,一定要检查形成碳正离子。如果一个更稳定的碳正离子可以通过氢化或形成的烷基转变,先做这个重组!)
让我们回到我们一直在做的例子。
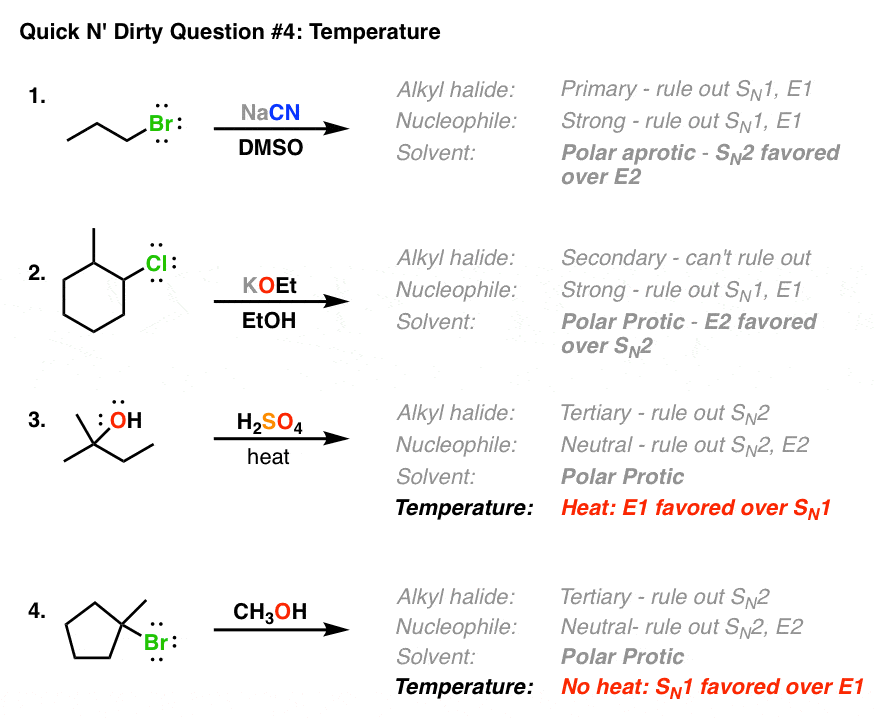
- 第三个病例——H2所以4一个三级酒精——是形成碳正离子的情况没有好亲核试剂(看到后消除醇与酸]。这一事实热正在应用有助于进一步平衡对小费了吗E1主要在SN1。
- 第四我们有一个例子三级卤化物(这将形成一个稳定的碳正离子吗)在一个极性质子溶剂(将有助于稳定碳正离子中间体),热是不表示。
- 因此使用Quick N '脏规则# 6,我们可以这样说SN1产品将占主导地位。(E1产品形式,但是他们不会是重要的产品]。
这确实是一个快速N '肮脏的规则。这不是应用均匀和有很多例外。你的里程会相差很大。(注1]
在下一篇文章我们将总结所有快速N的肮脏的规则决定的反应SN1/SN2/E1/E2。
在下一篇文章:总结性的快速N的肮脏的指南
——快速结束- - - - - - N '肮脏的讨论
笔记
注1。我恼火的缺乏硬数据可用时声明的SN1/SN2/E1/E2的决定。维勒引用的“可怕的和无限的灌木丛…也许害怕进入哪一个”似乎是适当的。我希望看到控制实验与各种基板运行在相同的条件下,清晰地描述每个变量的影响。我没有见过这个。任何本科实验室有一个渴望执行这个宝贵的公共服务?
一个区别“真正的”化学和化学“考试问题”
上面的文章与其说是了解有机化学的一些方面是如何回答一些武断的问题从课本或考试。为目的的理解有机化学,这足以知道热有利于消除反应。知道如何回答为目的的一种特殊的问题在考试中,这当然会取决于考官。存在很大的不同。然而,我将与你分享一个共同的观察,我见过2.5年看到考试来自全国各地。
首先,背景。在实验室,这是非常常见的加热反应让他们走在一个合理的速度,比如在这个例子中(从3月的高级有机化学第五ed;库珀·等。j .化学。Soc。1948年2038:]
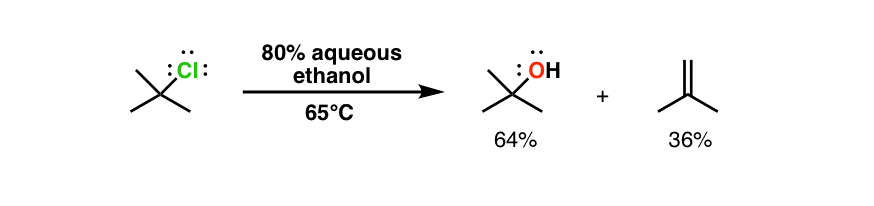
然而,在考试中老师,由于各种原因,包括善意的愿望不是压倒学生——往往会忽略一些数据。为了考试,如果上述反应是写成一个问题它会看起来像这样:
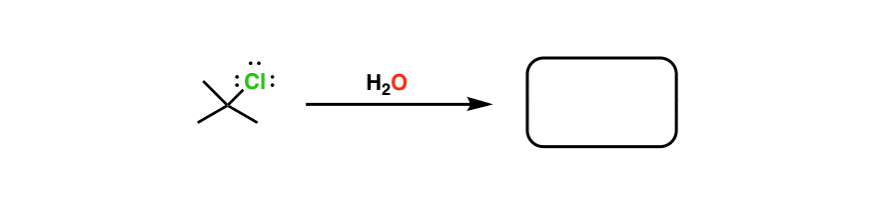
注意省略了“热”,这是符合的最小努力原则。预期的答案在这个实例将t-BuOH,产品的SN1的反应。根据问题的措辞,一些老师也会坚持E1产品被吸引。
这是观察我看到在许多(但肯定不是全部)课程。如果“热”这个词写在考试问题,这通常是一个线索的教练一个消除。在接下来的反应,例如,问题点消除(2 -甲基丙烯)的主要产品。
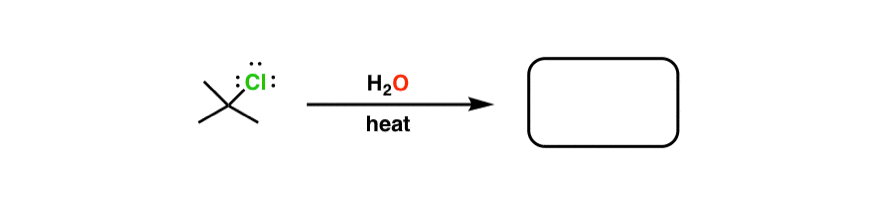
如果你是一个学生,你的目标是回答一个特定类型的问题在考试中正确,我建议你仔细检查这个问题和你的教练,让他们回答。在全国范围内这种做法存在巨大的矛盾。
挣扎在SN1/SN2/E1/E2吗?我们的Org 1总结表(PDF)在决定包含一个整版的流程图SN1/SN2/E1/E2总结,以及两个页面替换和消除反应,除了许多其他组织1主题。
你好詹姆斯,令人印象深刻的在这个网站工作。在这个页面,我想最后两个图在笔记中截面序列。热不是省略这个词叙述说,反之亦然。(也许我误解了你的意思!)
你是正确的。固定的。非常感谢你兰!
这个网站是不可思议的,我从未把它谢谢你先生
途径我们如果反应的问题发生在“温和热”;E1或SN1吗?
我会假设“温和热”有一个目的,是推动对E1。
为什么Br被认为是强亲核试剂在第二和中性在过去的例子吗? ? ?
谢谢你!
在第二个例子中“亲核试剂”是KOEt指控,因此“强劲”(根据我们的“快速N“脏”规则)。在第四个例子的亲核试剂是CH3OH是中性的(因此“软弱”根据这些规则)。
包含Cl的物种(第二个例子)和Br(第四)被称为“基质”。
我想知道什么是高和低的温度范围。
它是模糊的。但“热”通常指加热解决其沸点(“回流”)和最典型的沸点溶剂对我们来说是60 - 100°C。
它对我很有帮助。
读完之后,我也能够决定的反应就像通过sn1 / E1或sn2 / E2。
这是目标。如果它是帮助你,我很高兴。
亲爱的詹姆斯博士
你主要讨论二级三级碳。alilic和benzilic碳。将主benzilic碳像主碳?
烯丙基的和苄基的碳将会更容易通过碳正离子通路(SN1 / E1)比一般主要碳。如果一个带电的亲核试剂,使用快速N '肮脏的规则我就普遍预计通过SN2替换,如果亲核试剂是中性的(或使用溶剂作为亲核试剂)SN1和E1通道开始变得可行,特别是热。
温度是一个很好的例子,添加硫酸伯醇。在413 k,消除发生形成烯烃,但在443 k,醚是由SN1。感谢你的这些经验规则。很有帮助!
将sn1进行三级卤化物的反应与乙醇在25摄氏度?
如果你的问题是与考试相关的问题,答案可能是“是的”。应用快速N '脏规则、三级排除SN2乙醇(中性)排除E2, E1和室温规则。这使得SN1。
如果你的问题是有关一个真实的反应,我的建议是去3月先进的有机化学和查找“溶剂分解率”来了解如何快速。
应该打破C-Br债券的温度吗?
那是不可能的回答没有更多的信息。
了不起的工作!真正的钱
我认为它应该是“在第四个例子中我们有一个叔卤”而不是“在第四个例子中,我们有一个叔醇”。
谢谢你!
我只是想谢谢你的很棒的网站,和方法的解释的概念。我在本章好几天,阅读你的指示,和规则,我理解这个概念在一个小时!实际上我正确回答问题。谢谢你!
哦,哇,这是伟大的萨因。很高兴听到它。记住这些快速N的肮脏的规则,只是一个开始的好地方。
如果我们有叔卤代烷、水或酒精和22摄氏度是什么反应?E1和E2吗?
可能SN1 -叔烷基卤化物(不是SN2)和弱亲核试剂(水或酒精)(没有E2)在缺乏热量。
应用快速N '脏规则:叔卤代烷SN2规则。水/醇E2规则。室温排除了E1。为什么不SN1呢?