有机反应的底漆
7因素稳定有机化学中正电荷
最后更新:2022年8月23日|
稳定的正电荷在有机化学:7个关键因素
澄清一下:如何确保你熟悉形式电荷可以误导在你读这篇文章。这些因素确定“真正”的正电荷的稳定性(即低电子密度),而不是“正式”正电荷。
讨论之后7因素稳定负电荷,它将意义谈论7因素稳定正电荷。
表的内容
- 稳定正电荷在有机化学的重要性
- 因素# 1:正电荷的增加来增加不稳定
- 因素# 2:原子的电负性越低,就越能更好稳定正电荷
- 因素# 3:原子的极化率越大越好它可以稳定正电荷
- 因素# 4:共振稳定——将正电荷分配在一个更大的体积稳定
- 因素# 5:增加烷基取代基邻碳正离子会稳定的正电荷
- 因素# 6:一个原子的电负性随着杂交提到的增加而增加;这造成正电荷
- 芳香性也可以稳定正电荷
- 捆绑在一起的因素稳定正电荷与负电荷稳定的因素
1。稳定正电荷在有机化学的重要性
任何时候你有一个正电荷形成的反应,是有用的问:这个新的正电荷会有多稳定?什么因素可能有助于稳定吗?正电荷的更稳定,更有利的反应。
相反,当你看到一个正电荷被摧毁的反应,是有用的问同样的问题。如果你看到一个特别不稳定的正电荷被摧毁了,这将是特别有利的。
与负电荷,有值得记住的几个主要因素:
- 相反电荷的吸引,所以正电荷稳定通过捐赠邻近原子的电子密度。
- 高电荷密度是不稳定的。如果费用可以“分散”或“扩散”不知怎么的,这是稳定。同样,如果相邻组删除从原子带正电的电子密度,这将破坏它(导致更高的电荷密度)。
好的,我们开始吧!
2。因素# 1:正电荷的增加来增加不稳定
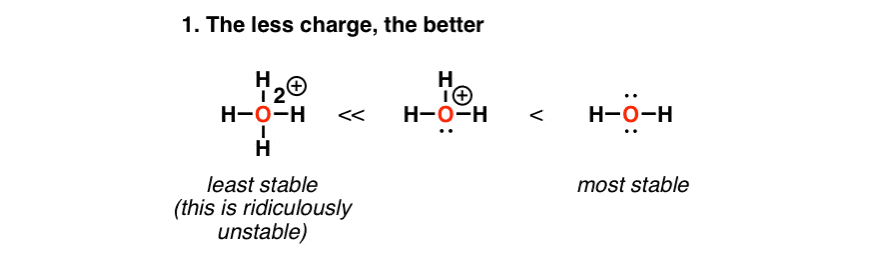
简单的说,电荷密度越低,正电荷会更稳定。因为这个原因(可笑)的H4O(2 +)比H更不稳定3O(+)这比中性H更加不稳定2O。
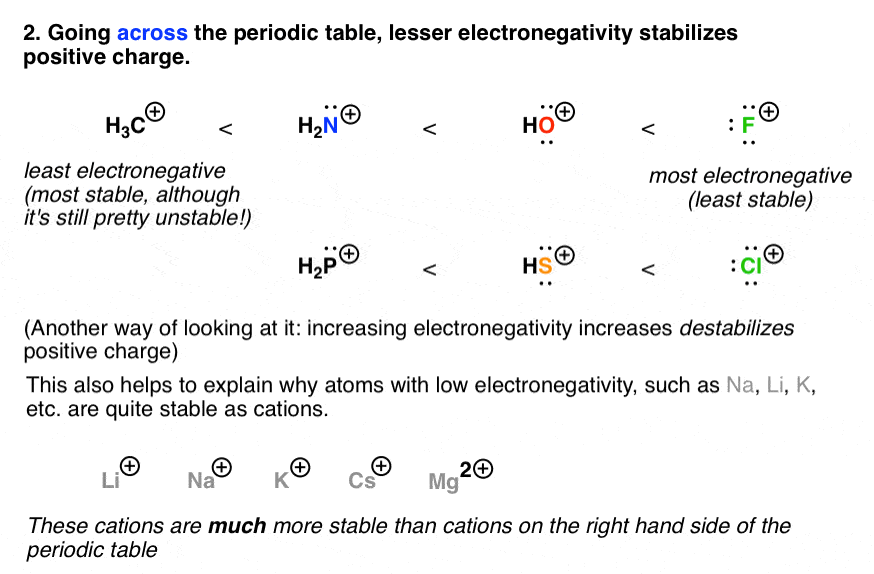
3所示。因素# 2:原子的电负性越低,就越能更好稳定正电荷
就像高电负性稳定负电荷,情况恰恰相反:低电负性将导致一个更稳定的正电荷。这有助于解释为什么像Na +阳离子,李+,和K +相当无害的稳定,而F +和Cl +。
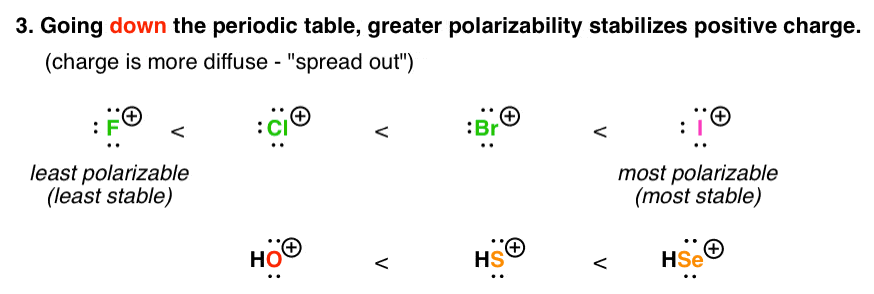
4所示。因素# 3:原子的极化率越大越好它可以稳定正电荷
当我们沿着一个列的元素周期表,原子半径将会增加,这意味着电荷密度降低。(高体积=低密度)。由于电荷是更多的“宋”,正电荷的稳定性将会增加。
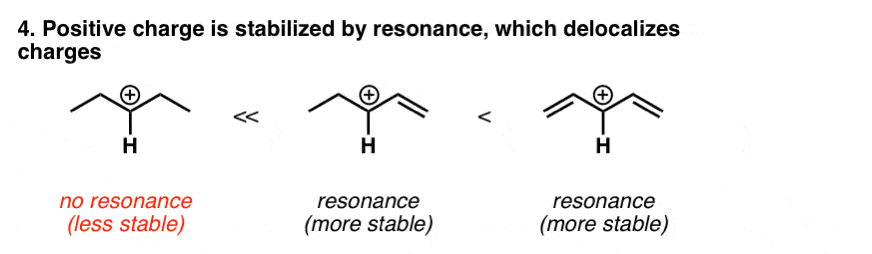
5。因素# 4:共振稳定——将正电荷分配在一个更大的体积稳定
“扩散”正电荷,这是可能的邻近的p轨道可以参与共振时,是一个稳定因素。共振稳定正电荷。
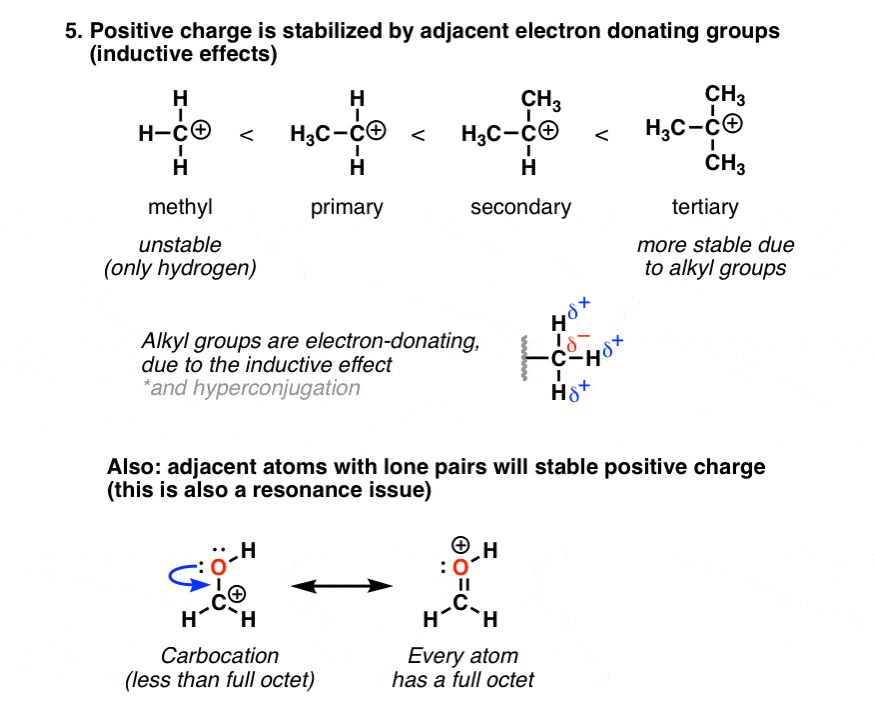
6。因素# 5:增加烷基取代基邻碳正离子会稳定的正电荷
如果你(电子)贫穷,(电子)起到了丰富的邻居。自相反电荷吸引正电荷将稳定邻居可以给出电子。典型的例子是碳正离子的稳定性,增加相邻碳原子数量的增加。另一个例子是π捐赠,邻近的原子与孤电子可以捐赠他们electron-poor物种如碳正离子。
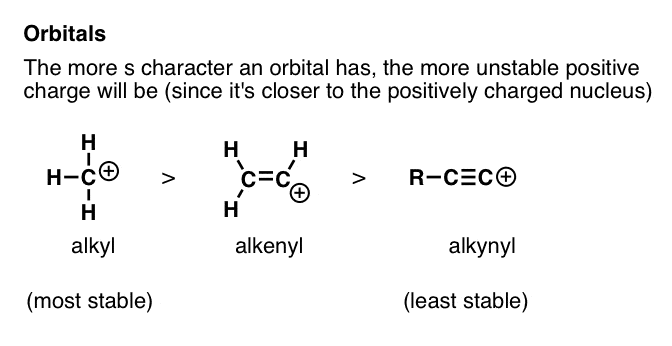
7所示。因素# 6:一个原子的电负性随着杂交提到的增加而增加;这造成正电荷
负电荷和从sp稳定3对sp2对sp杂交(烷基烯炔),由于负电荷在轨道随着提到——接近带正电的原子核。
为正电荷正好相反!拥有一个正电荷的sp轨道将意味着更加紧密的正电荷是带正电的原子核,这是不好的!所以稳定性的正电荷会增加我们从sp sp2对sp3。
8。芳香性也可以稳定正电荷
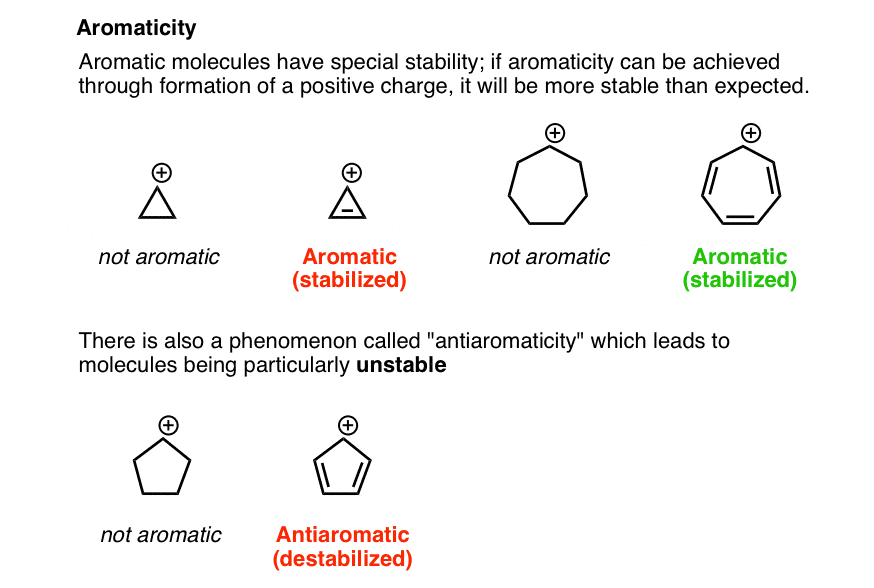
这是一个特殊的情况下,你通常在早期的组织2。有某些类型的分子具有一种特殊的稳定称为“芳香性”(看到帖子:芳香性的介绍)。某些分子熊正电荷芳香:如果是这样的话,正电荷会非常稳定,cyclopropenium和卓鎓碳正离子。(你甚至可以买卓鎓碳正离子!)
相反,有一个相关的(但相反)的现象称为“antiaromaticity”(看到帖子:Antiaromaticity)某些分子特别是在哪里不稳定的。
如果一个分子轴承一个正电荷antiaromatic,这将是比平时更不稳定。
9。捆绑在一起的因素稳定正电荷与负电荷稳定的因素
你注意到稳定的因素正电荷与负电荷稳定的因素?
1。“传播”稳定正面和负面的指控。共振,极化率,减少电荷密度和芳香性因素会稳定吗这两个积极的和消极的。
2。相邻的正电荷,负电荷是稳定的如电负性(增加),越来越多的提到,电子撤回组,不稳定通过相邻的负电荷。(相反电荷吸引,同种电荷相互排斥)。
3所示。正电荷由相邻稳定负电荷——如电子捐赠团体- - - - - -和由于相邻的正电荷如电负性(增加),越来越提到的轨道。(相反电荷吸引,同种电荷相互排斥)。
这七个因素将帮助我们非常理解为什么某些反应和其他不发生。
(CH3) +,不该sp3的杂交sp2,而不是因为数量的空间(CH3) + 3吗?
我认为稳定的正电荷并不解释,正电荷意味着缺乏电子,原子核附近没有任何真正的正电荷。你的声明”为正电荷正好相反!拥有一个正电荷的sp轨道将意味着更加紧密的正电荷是带正电的原子核,这是不好的!所以稳定性的正电荷会增加我们从sp sp2 sp3。”
不是令人满意的。
我有点困惑,我的书说,H2S比水更好的酸,因为SH -比哦更稳定同样我们可以说H2S比水更好的基础,因为h3 +比H3O +更稳定。现在这怎么可能,硫化氢是更好的酸以及更好的基础。
我不会说H2S是比水更好的基础。我从来没有见过的pKa值h3 +
一个正电荷由相邻稳定电子捐赠团体(例如甲基)。但是像氧的电负性更强,所以不会是一个电子的退出群,把更多的电子密度已经electron-poor区域,使其更积极和更不稳定?或者这是一个共振的情况比感应稳定作用,即氧孤,毗邻一个正电荷,可以resonante和正电荷的“重新分配”吗?
我知道比酮醛反应更大,因为他们有更少的CH /电子捐赠组织稳定部分正电荷羰基c .但酯有两个羰基碳氧键;我的心告诉我“不应该酯氧气破坏/把更多的电荷/使羰基C更积极?”。我的心告诉我的另一部分“O-CH3电子捐赠组织;不稳定部分积极羰基C吗?”。但是我想这是另一个共振比感应的事情吗?酮只有一个共振结构,将正电荷完全羰基碳,而酯有两个共振结构的时候,一个一个正电荷在哪里放置在酯氧(从而使正电荷集中)。
有疑问时,我总是提醒自己,“共振胜一切”,这是为什么,例如,卤素取代基苯,处于待发状态,通过感应,仍在昊图公司/ para董事通过共振。
嘿,
我很困惑杂交和电荷密度之间的关系。我我们学院教授告诉我们:“越是s轨道,destability或稳定减少”。也可以澄清之间的差别电荷密度和电负性及其对碳正离子的影响?
随着电负性的增加,一个负电荷的稳定性(如对电子)将会增加。你可以把从sp3 sp2 sp杂化,改变有效原子的电负性。
什么是相反的孤对电子的吗?一个空轨道。随着电负性增加,空轨道的* *不稳定性增加。这就是为什么我们看到碳正离子,但几乎从来没有看到氮,氧,和(尤其是)氟完全空轨道。
应用上面的比喻中,你可以把从sp3 sp2 sp,增加有效原子的电负性,其结果是一个空轨道将更不稳定。
另一种从的角度看它是势能。把一个对象1公里以上的地球表面。它有一定的潜在能量,地球的引力有关。如果你保持这个距离恒定,但增加行星的质量(比如地球- >天王星- >木星)增加物体的势能,正如增强电负性与势能增加。
当我们谈论“正电荷的扰动”由于杂交(或电负性)你可以认为它是减少电离能。
如果只有负电荷电子是如何可能的激进分子。
自由基是中性的,因为电子的负电荷相互抵消平衡原子核的正电荷。
总之任何因素降低了电荷稳定分子。阳离子苯的稳定性呢?
我认为苯阳离子被芳香性的情况下稳定。
环的π电子可以移动的正电荷苯环,因此扩散,因此赋予稳定分子。
这是一个常见的陷阱!在苯碳正离子(C6H5(+))空的p轨道与碳氢键是在同一个平面上,这是90度远离芳环的p轨道。所以共振稳定是不可能的。