烯醇、烯醇化物
脱酸
最后更新:2023年5月22日|
脱酸
在本文中,我们将讨论脱酸的上下文中,最常见的损失有限公司2从beta-keto酸(丙二酸和丙二酸酸)酯分别合成和乙酰乙酸合成。
我们将通过一些例子,展示如何不做箭头推(以及如何避免常见的错误),然后尝试解释为什么beta-keto酸脱羧容易发生,但不应该与“正常”的羧酸。我们也会有一些测试和练习。
表的内容
- 一些去工作
- 脱酸不工作!
- 怎么去工作?
- 脱酸是一种“1,2-Elimination”
- 的机制
- 脱乙酰乙酸和丙二酸酯的合成
- 一个不脱羧基的Beta-Keto酸
- 其他一些脱酸的例子
- 结论
- 笔记
- 测试你自己!
- (高级)引用和进一步阅读
1。一些去工作
在本文中,我们将讨论一些臭名昭著的有限公司2发射器:beta-keto酸和宝石二羧基的酸。
beta-keto酸羧酸,包含一个C = O组两个碳的吗羧酸。
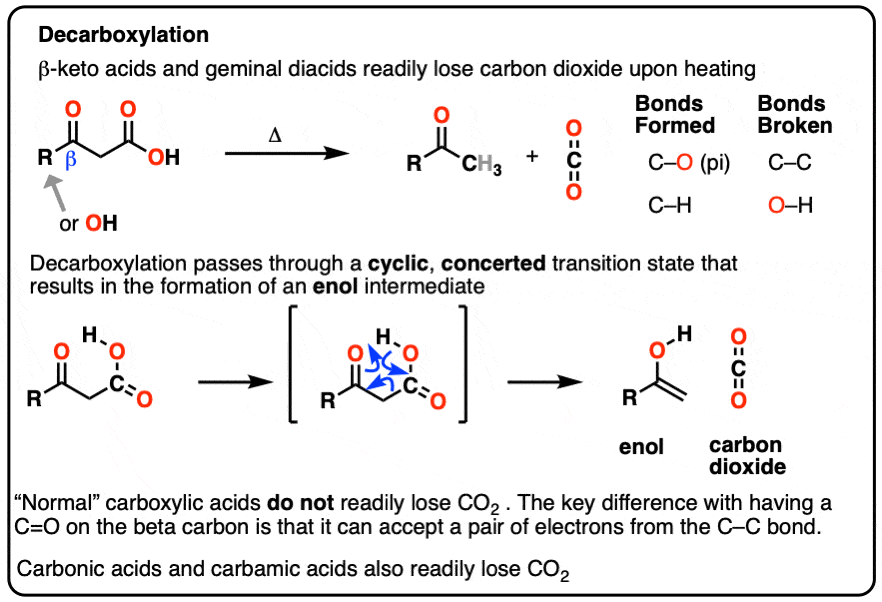
当beta-keto酸加热,他们自发地失去有限公司2给一个酮像这样:
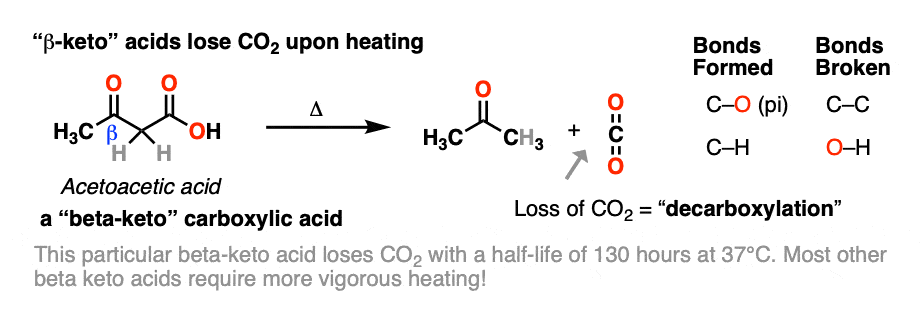
这就是所谓的“脱”。
脱羧通常需要加热时,乙酰乙酸,举个最简单的例子(上图),自然失去了有限公司2在室温下!(注1]
温室气体排放的另一个成员俱乐部是丙二酸(的衍生品宝石,二羧酸)[注2类似于一个beta-keto酸。技术上我猜你可能会认为“beta-acid酸”,但我从来没有听到任何人使用这个词。
丙二酸加热时,它发出有限公司2mono -羧酸(醋酸在这种情况下)。
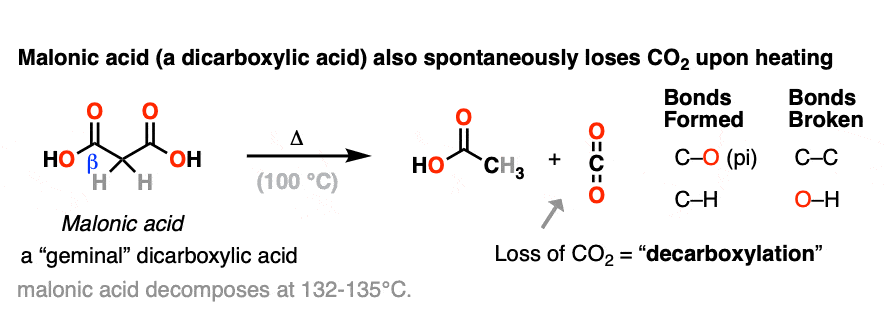
在每种情况下的脱羧碳碳键断裂和切断形成π键除了一个新的碳氢键。
这些反应主要的上下文中乙酰乙酸酯合成和丙二酸酯的合成前面提过的。(参见:丙二酸酯合成]
2。脱酸不工作
所以它真的那么容易吗?我们要做的就是加热羧酸一点,噗!关闭弹出有限公司2吗?
换句话说,我们可以任何旧热羧酸和失去公司2吗?
没有。当我们熟悉的朋友乙酸(的醋,遗憾的是未被充分认识的调味品炸薯条,顺便说一句)加热到100°C,它不会失去有限公司2。它只是沸腾。同样,长链羧酸丁酸和戊酸不要失去公司2容易在加热。他们只是沸腾。我个人不推荐沸腾他们没有一个运作良好的通风橱,然而,由于新鲜的气味吐(丁酸)和臭脚(戊酸)不会让你任何朋友。
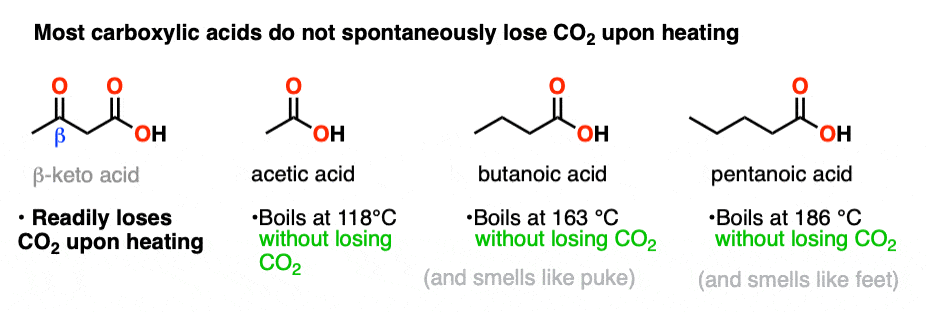
因为正常的长链酸不加热时自发失去二氧化碳,那么也许有一些特别的C = O的存在呢?
丙酮酸,CH3C (O)有限公司2H是一个α酮羧酸。乙酰丙酸,CH3C (O) CH2CH2羧基是一个γ酮羧酸。
所以这些分子如何脱羧基经加热,形成鲜明对比β酮羧酸吗?
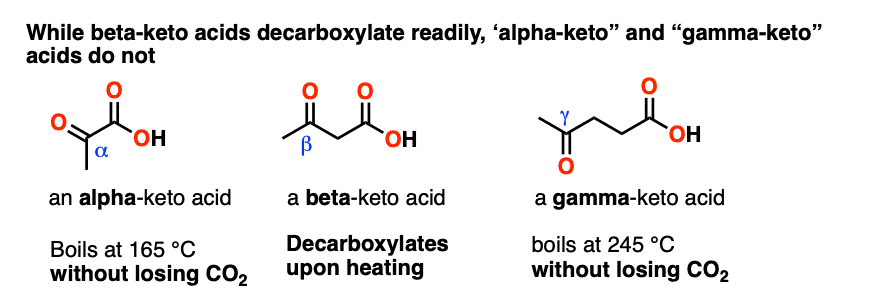
简短的回答是只有beta-keto羧酸脱羧基。其他的不喜欢。(这同样适用于α-和γ-二羧基的酸)(注3]
所以很明显这特别的C = O两个碳原子从公司2H,允许脱羧。
它是什么?
3所示。脱酸是如何工作的呢?
在上面的脱羧反应中,我们打破碳碳和成型有限公司2。
我们可以想象两种不同的方式,这可能发生,我们可以想象一个弯曲的箭头。
在第一个,我们画一个箭头显示了一对从碳碳键朝着电子有限公司2H和允许有限公司2H离开“离去基团”。
在第二个,我们画一个箭头显示碳碳键的一对电子远离有限公司2H和碳毗邻C = O。
哪一个是正确的?
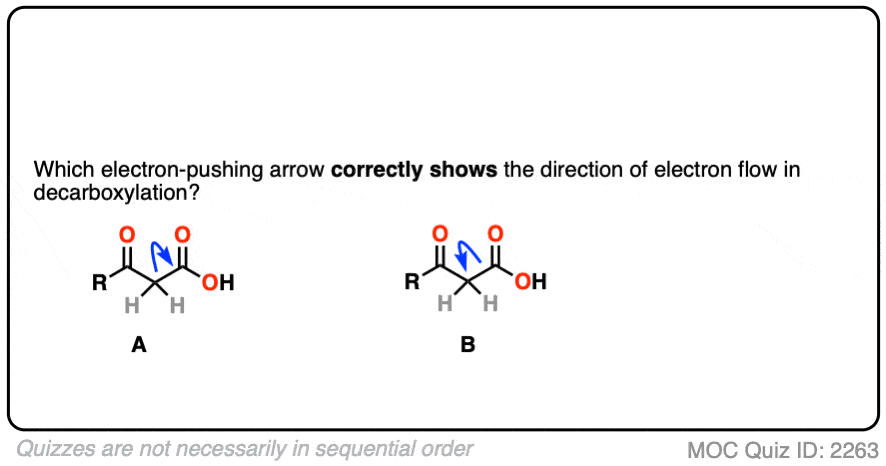 点击翻转
点击翻转
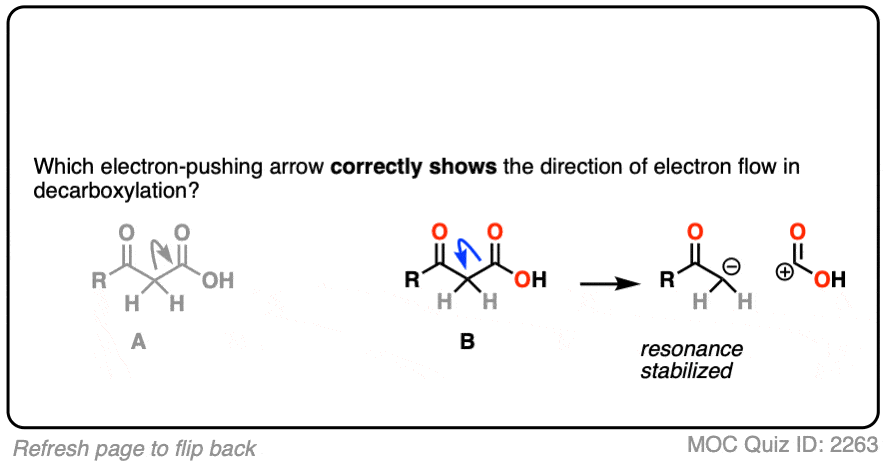
如果你选择了“A”,恭喜你!你犯了一个常见的错误,很多人之前,现在,你会在未来武装反对它。
虽然这样容易画出箭头,因为有限公司2是“离开”,这是不正确的。
为什么?密切关注碳碳键的断裂的后果这一方向。每一个曲线箭头使形式电荷在尾巴更多的正由1和形式电荷在头更多的负1。(看到的:反应的弯曲的箭头]
结果是一个碳正离子在碳,这带负电荷的有限公司2H (-)。这不是二氧化碳!(注意4]
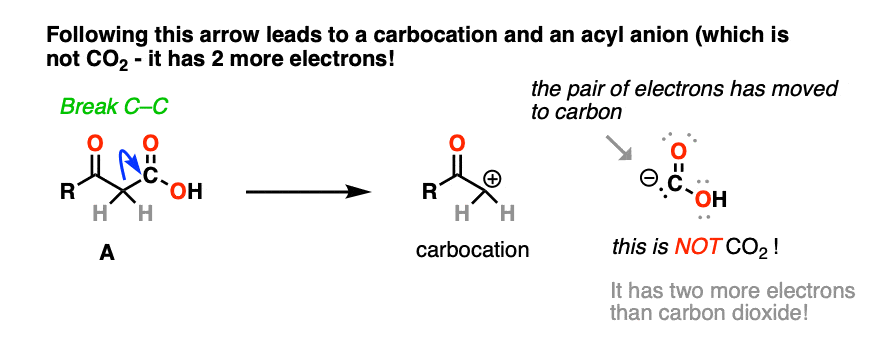
不,碳正离子不是共振稳定。(注5]
4所示。脱酸是一种“1,2-Elimination”
诀窍与脱看同样的方式你会看看其他1,2-elimination从羰基组。(看到帖子:1,2-elimination]
当这种情况发生时,我们形成切断(π)和中断LG (-)。
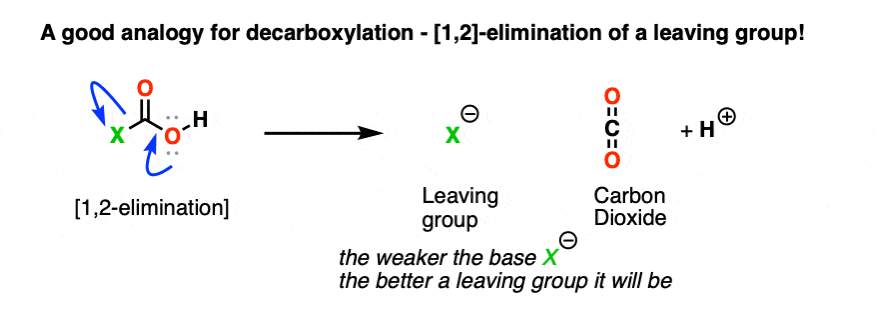
这意味着当脱酸发生时,我们应该看看任何连接到有限公司2H随着离去基团。
是这样的:
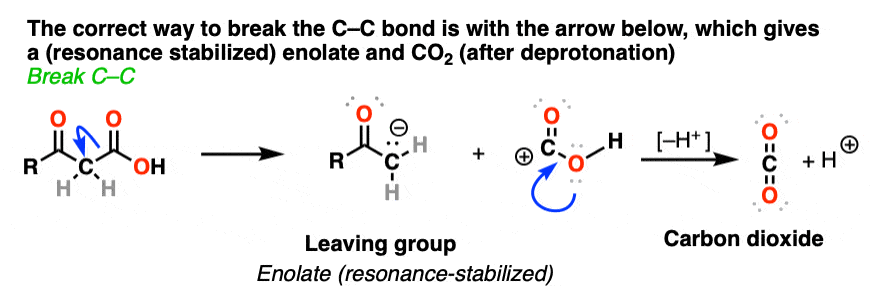
那么为什么脱羧beta-keto酸但的发生不发生在我们上面显示的例子(直链酸、α-和γ-酮酸,等等)。
好吧…所有这一切都归结到碱度(再一次)
你可能已经注意到现在,有机化学的特点之一是相同的旧课程以不同形式回到你的身边,重新包装。这是什么使它有趣!(你的意见可能不同)
阻止我如果你听过,但是,”较弱的基础,越好离去基团”。(参见:是什么让一个好的离去基团?]
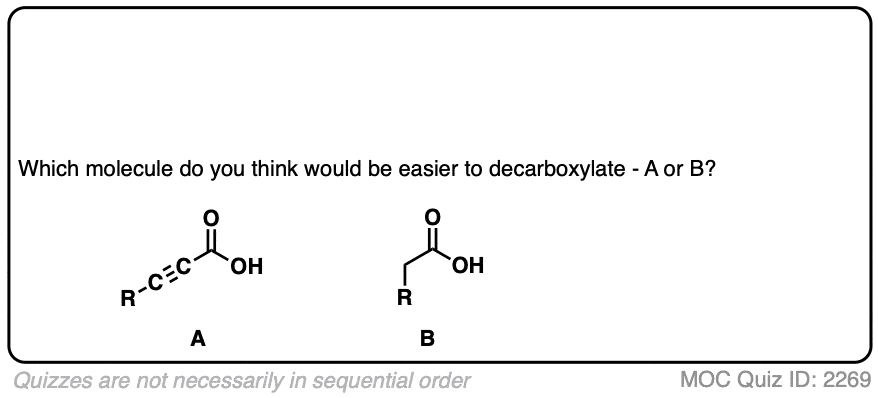
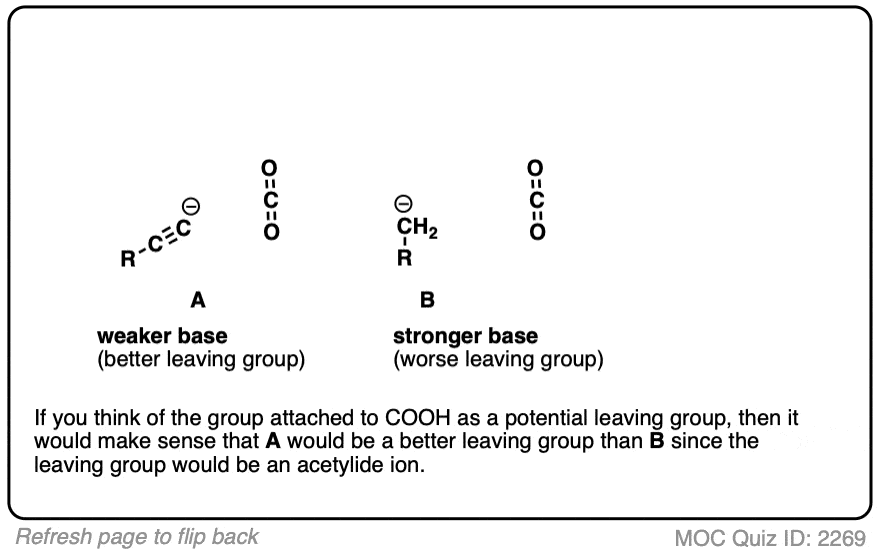
如果你看看这些脱酸开始离开团体,你注意到什么?
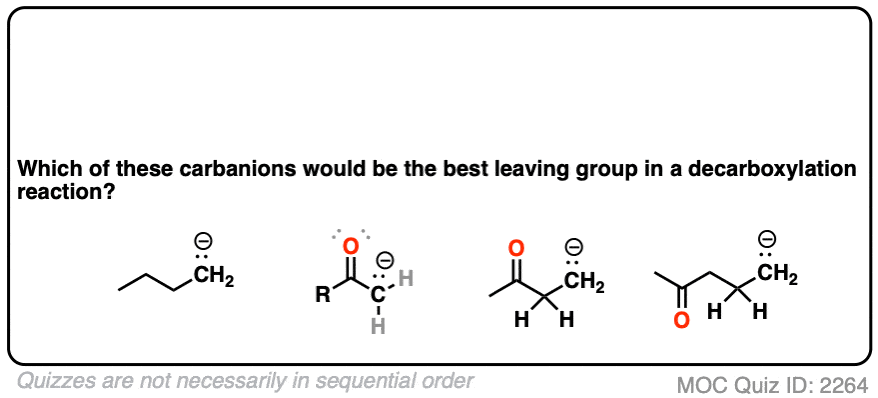 点击翻转
点击翻转
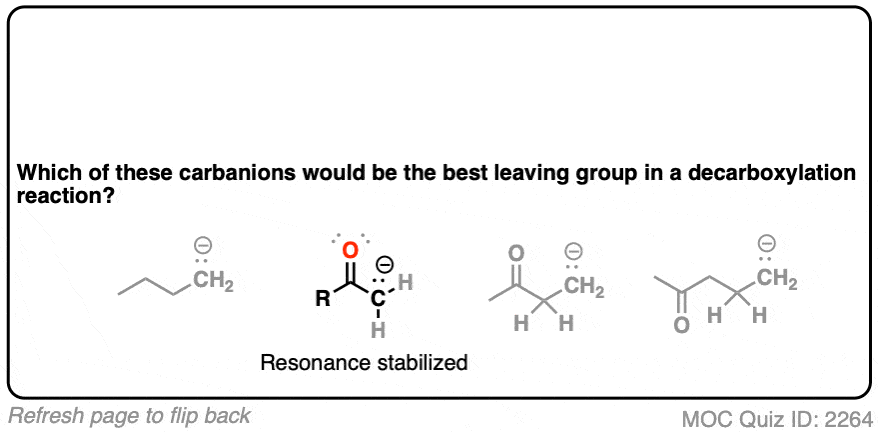
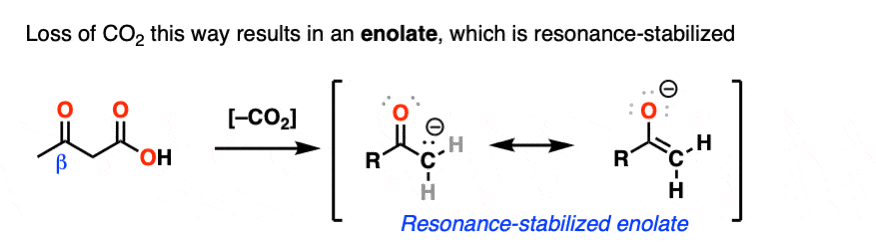
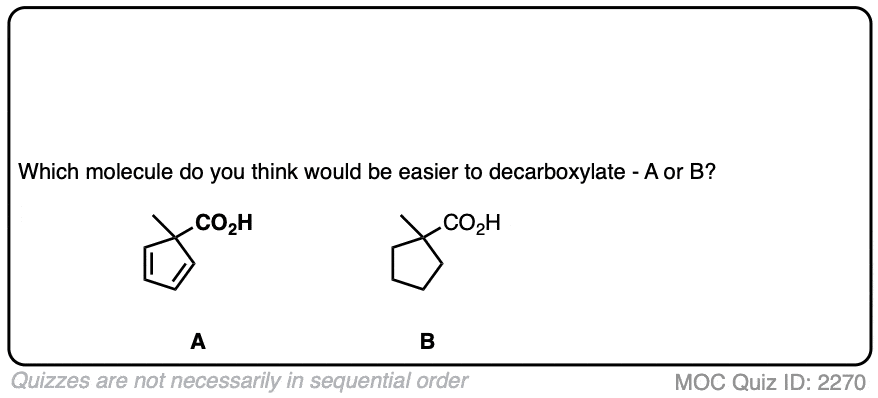
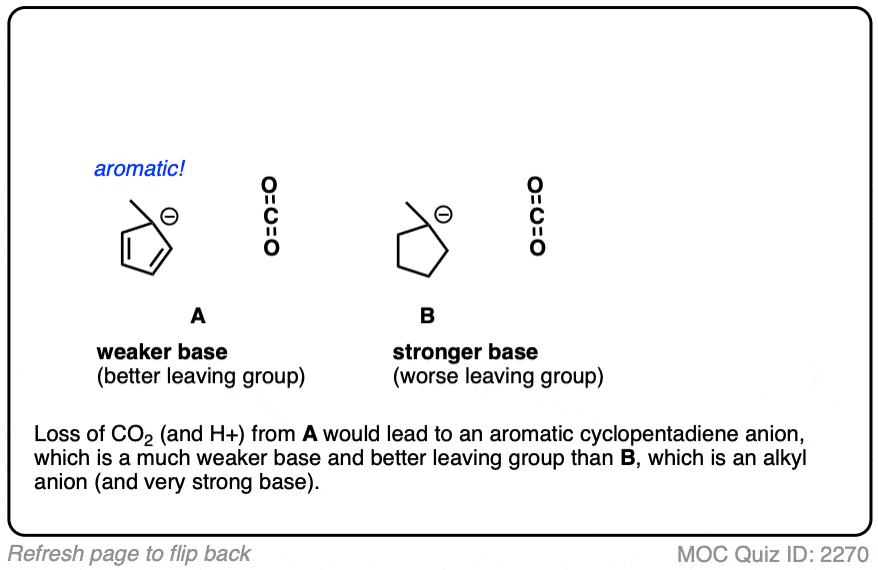
希望你像说:“啊哈!的烯醇化物是不同的,因为它带有一个负电荷,可离域的氧气共振,因此基础非常薄弱,因此更好离去基团!”
完全正确! ! !
这就是为什么C = O必须两个碳。我们会形成一个烯醇化物,负电荷可以搬到氧气。氧、电负性更强、更好的工作比碳稳定一个负电荷。
5。的机制
认为脱酸是一种消除的羰基集团是一个良好的开端。(脱羧、早期研究中提出了一种机制很像)。
实验证据描绘出一幅略微不同的图景。(注6更多的机制)
我们有我们最好的工作模型协调一致的机制与循环过渡态的碳碳键断裂同时地和碳碳形成π键。它发生一次没有指控中间体,类似于我们的老朋友单键转移的重组。
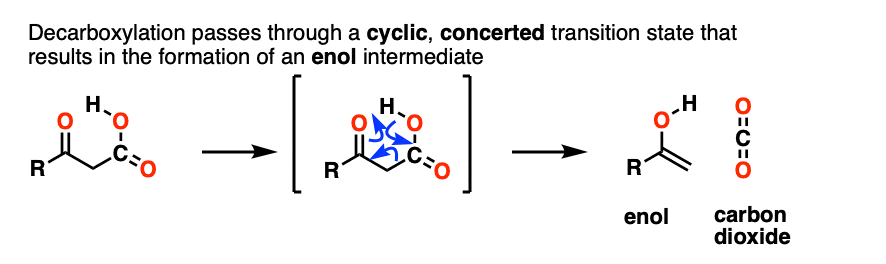
一个烯醇形成一个中间。的烯醇然后经历酮烯醇互变异构现象给我们酮
看到酮烯醇互变异构化机理,徘徊在这里和一个图像会弹出或单击链接。
6。脱乙酰乙酸酯和丙二酸的合成
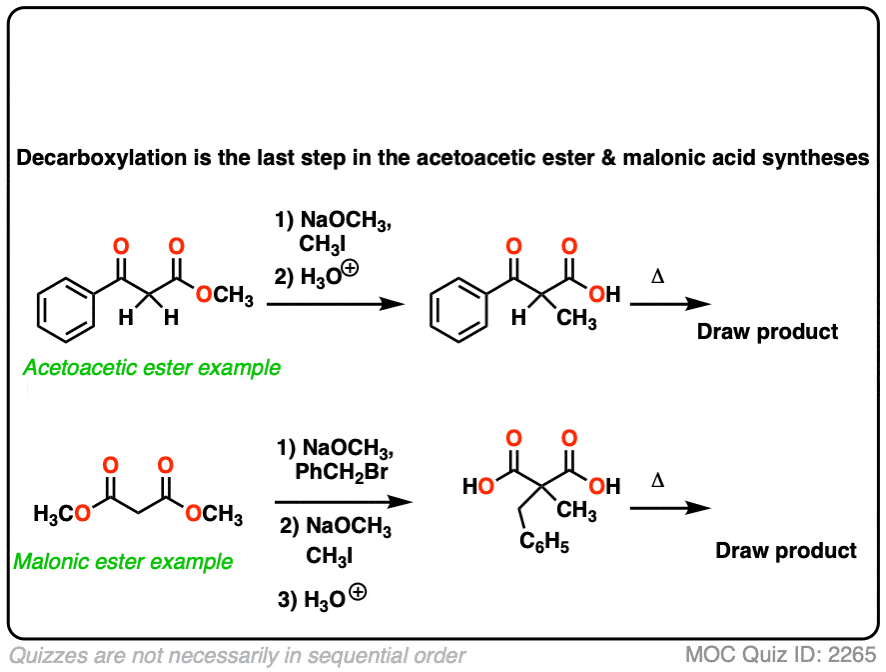
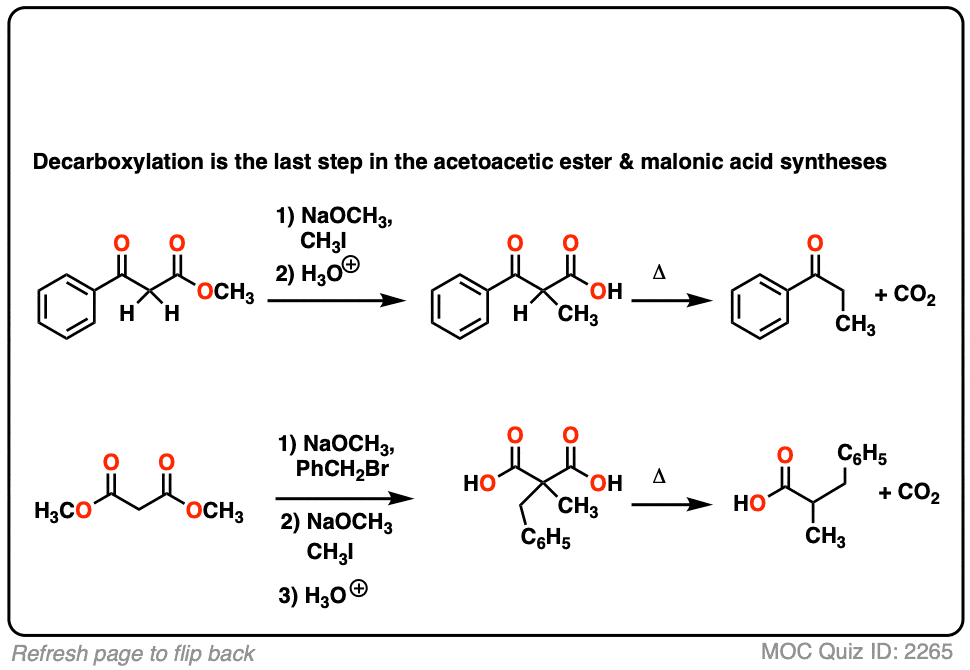
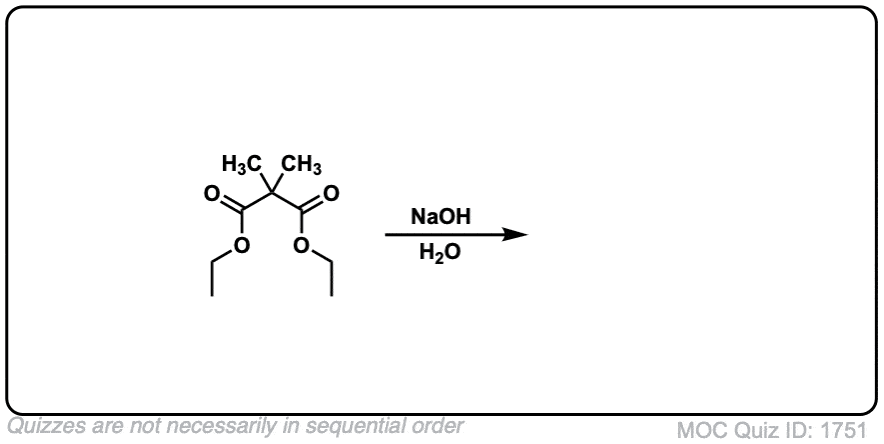
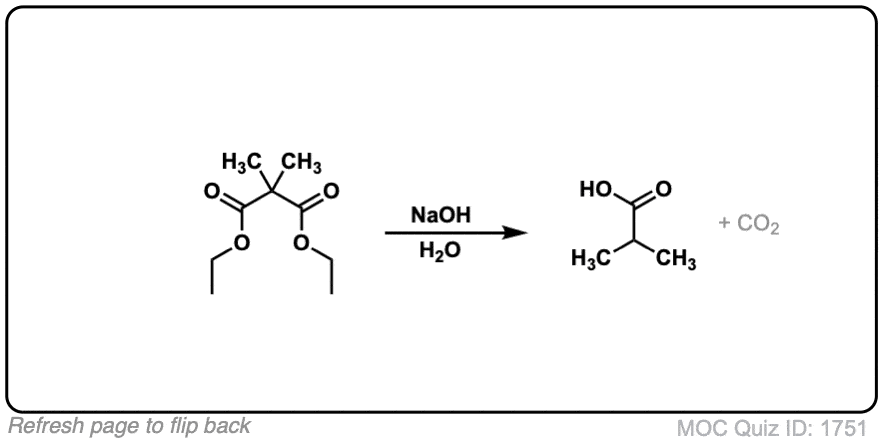
在丙二酸酯和乙酰乙酸酯合成,烯醇化物形成(例如NaOCH吗3),然后与一个烷基化烷基卤化物(例如CH3我),如果需要可以执行第二个烷基化。的酯然后水解,在基本(氢氧化钠)或酸性(H3O +)条件。
这里有一些例子的脱酸合成在野外发现。你能画出最终产品吗?
 点击翻转
点击翻转
7所示。一个不脱羧基的beta-keto酸
好吧。我们已经看到,C = O两个碳的羧酸是脱酸的关键。
让我们看一个有趣的例外。这是一个beta-keto的例子羧酸那不容易脱羧基在加热。
为什么不呢?
 点击翻转
点击翻转
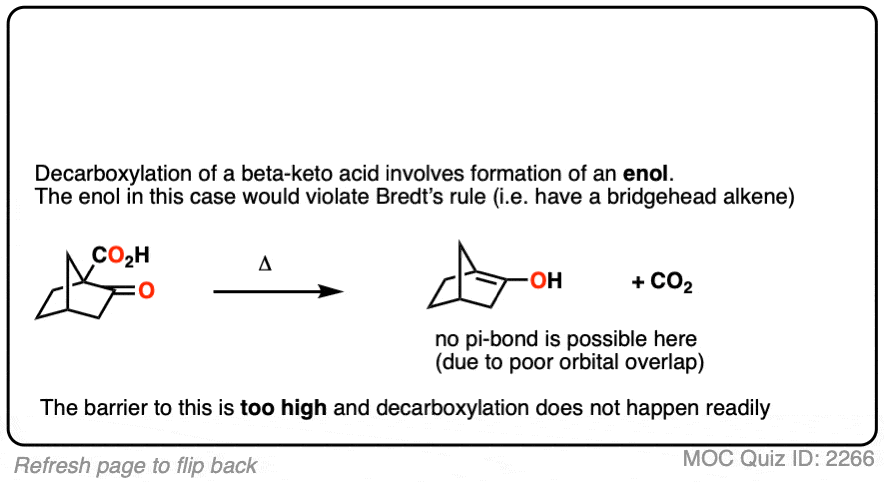
这是其中的一个小例子,帮助证明规则。
通过一个自反应所得烯醇中间,烯醇有一个碳碳键,结果表明烯醇形式不太好如果它意味着一个桥头堡双键形成。
8。其他一些脱酸的例子
到目前为止我已经没有覆盖脱酸的最熟悉的例子。
治疗与弱酸碳酸盐离子导致形成碳酸,这经历了自发的去水和有限公司2。
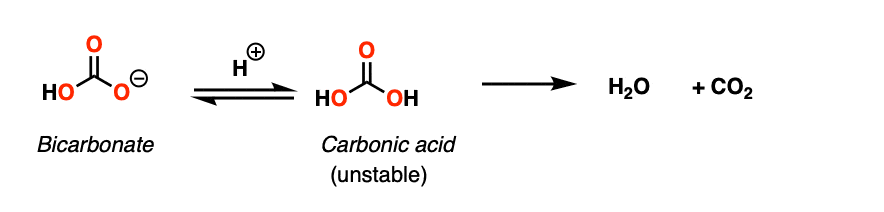
这是一个在实践中更加生动的例子,它是什么样子:
在这个紧要关头,几个类似的例子去让他们出现在后面的部分组织2。
想到的例子是表兄弟。(看到帖子:霍夫曼和库尔修斯重组]
在库尔修斯重排,酰基叠氮化加热,将异氰酸酯,失去N2在这个过程中。如果一个酒精加入我们吗氨基甲酸酯这个反应,这是更常见的应用。然而,如果水是补充说,这给了我们一个氨基甲酸(如碳酸)自发地脱羧基。
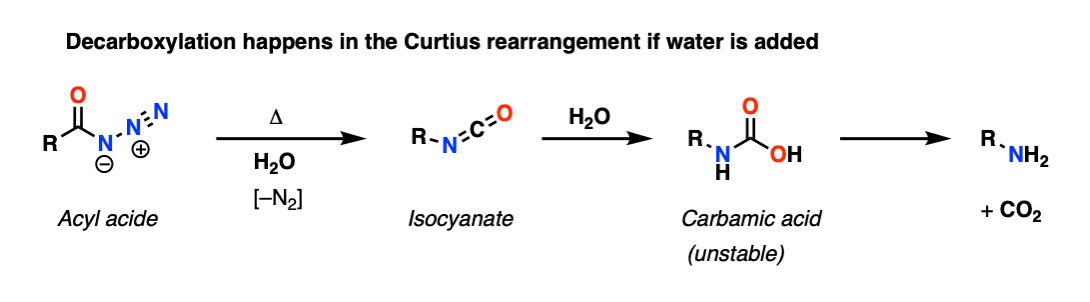
霍夫曼重排是一个类似酰胺与Br的重排2和氢氧化钠给一个中间氨基甲酸,同样失去了有限公司2给一个胺。
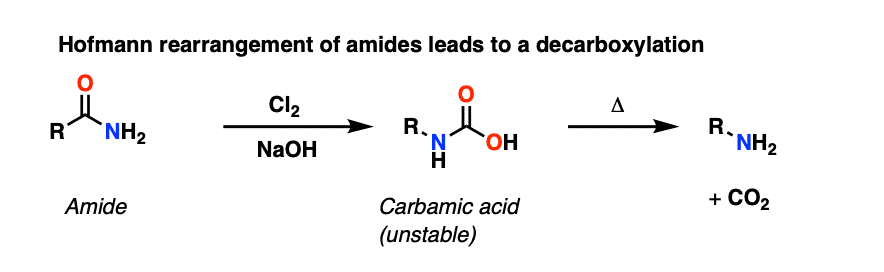
在脚注是一个简短的讨论有时遇到的两个脱介绍有机化学:科尔伯电解和脱羧Diels-Alder反应。(请注意7]
9。结论
让我们来总结一下:
- 脱酸容易发生在beta-keto酸和丙二酸衍生物。碳碳键断裂,切断(pi)债券形成。
- 通过循环反应收益,共同在一个过渡状态和结果烯醇中间,然后经历酮烯醇互变异构现象
- 小心的常见的错误处理有限公司2就像一个离去基团!最好的脱羧的类型1,2 -消去反应,形成新的碳碳π键”开始“碳碳键。
- 碳碳键是可以打破的,因为对电子可以通过共振delocalize氧气。这条路并不是“正常”的长链羧酸。
- 脱酸也自发地发生在碳酸和氨基甲酸。
笔记
注1-乙酰乙酸(pK一个= 3.5)的半衰期是140分钟37°C在水里。(裁判)其共轭碱乙酰乙酸盐,在体内生理条件下。在自然界中,乙酰乙酸盐的分解丙酮和二氧化碳是由酶催化的,乙酰乙酸脱羧酶。
有趣的历史注意这种酶,从维基百科:
乙酰乙酸脱羧酶是一种酶具有重要的历史意义,尤其是在第一次世界大战和建立以色列。[3]在战争期间盟军需要纯丙酮作为生物碱的一种溶剂,一个高度易燃化合物的主要成分是火药。[4]1916年,生物化学家和未来以色列第一任总统查魏茨曼是第一个孤立acetobutylicum梭状芽胞杆菌、革兰氏阳性厌氧菌乙酰乙酸盐脱羧酶的发现。魏茨曼能够利用生物产量的能力丙酮从淀粉以大规模生产炸药在战争期间。[3]这使得美国和英国政府安装过程由查魏茨曼几家大型工厂在英国,法国,加拿大,美国。通过魏茨曼科学贡献在第一次世界大战中,他成了亲密的有影响力的英国领导人教育他们的犹太复国主义的信仰。[5]其中一个是阿瑟·贝尔福贝尔福首先声明,该文档后那个人发音英国支持建立一个犹太人的家乡命名。
注2- - - - - -“偕的”(来自拉丁语双生子“孪生”)是指一个分子包含两个相同取代基(如宝石二醇为水合物,是另一个名字宝石-dihalides是通过增加HX的两倍炔烃)。顺丁烯二酸是一种宝石有两个公司以来二酸2H取代基的碳。
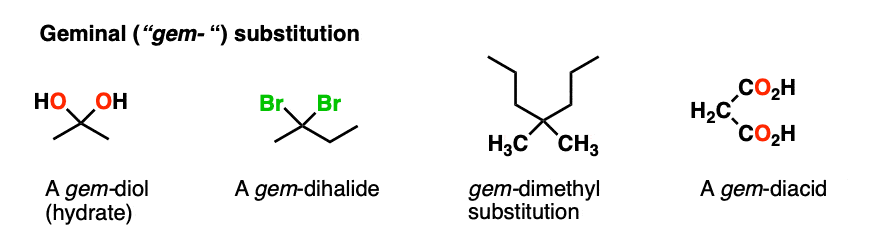
注3——相当于二酸将草酸(没有分解融化在190°C)和琥珀酸(融化在184 - 190°C)。这两种分子没有脱地融化。
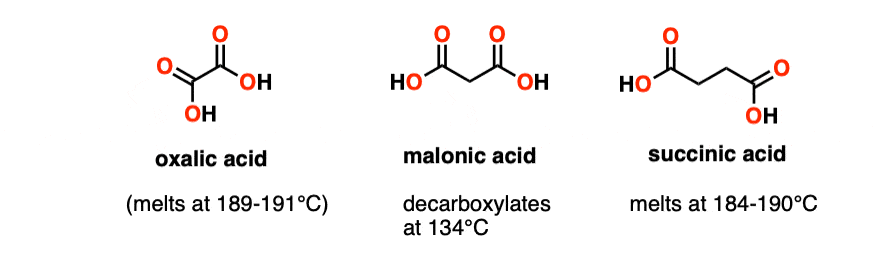
注意4——物种(-)有限公司2H是技术上共轭碱甲酸(HCO2H)通过aldehydic氢的去质子化。(到目前为止)甲酸更稳定更常见离子HCO2(-)。
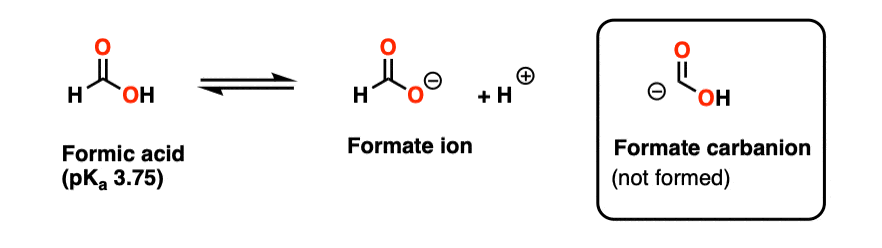
甲酸是一种碳氧化态+ 2,+ 4价的对比碳有限公司2。所以这个物种需要失去两个电子有限公司为了形式2。(事实证明,甲酸是一个有用的来源的H(-)在某些过渡金属催化反应)。
注5——为什么这不是碳“共轭”上?这似乎是一个不错的机会,一个测验。
 点击翻转
点击翻转
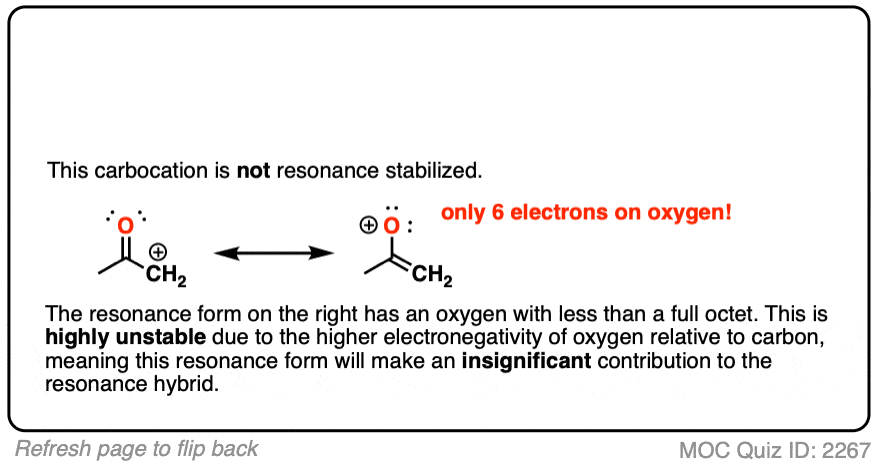
移动的一对电子形成新的碳碳π键会导致一个氧原子不到一个完整的八隅体。
不到一个完整的八隅体原子的稳定性大大降低,一个从左到右从硼沿着周期表(最稳定的)碳、氮、氧、氟(最不稳定)。
随着原子核的电负性增加,其也是如此电子亲和能。而碳正离子是众所周知的在某些情况下,甚至可以是孤立的,没有办法,氧原子电负性(3.4)将放弃其对电子像碳(2.5电负性)一个懦夫。
什么样的娱乐品味的化学氧原子不到一个完整的八隅体可能会执行,我强烈推荐这篇文章,德里克。劳:“我不会使用的东西:双氧二氟化物”,涵盖了化学FOOF。
假设1941年,脱酸的机理不明确,但有两个假设如何发生的。
所以你进行一系列的实验测量速率常数的各种不同极性的溶剂。
利率基本上是常数。你能得出什么结论呢?
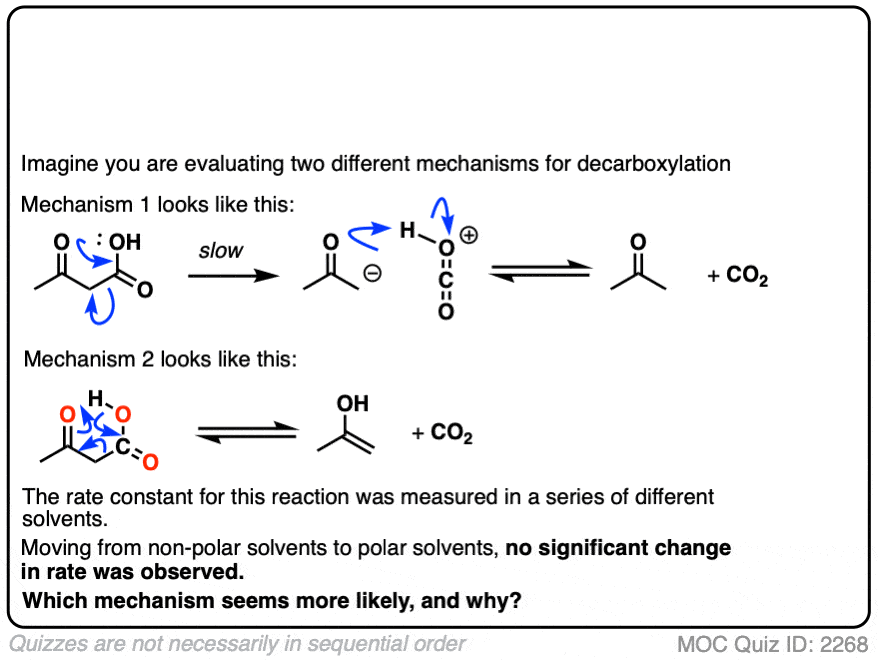 点击翻转
点击翻转
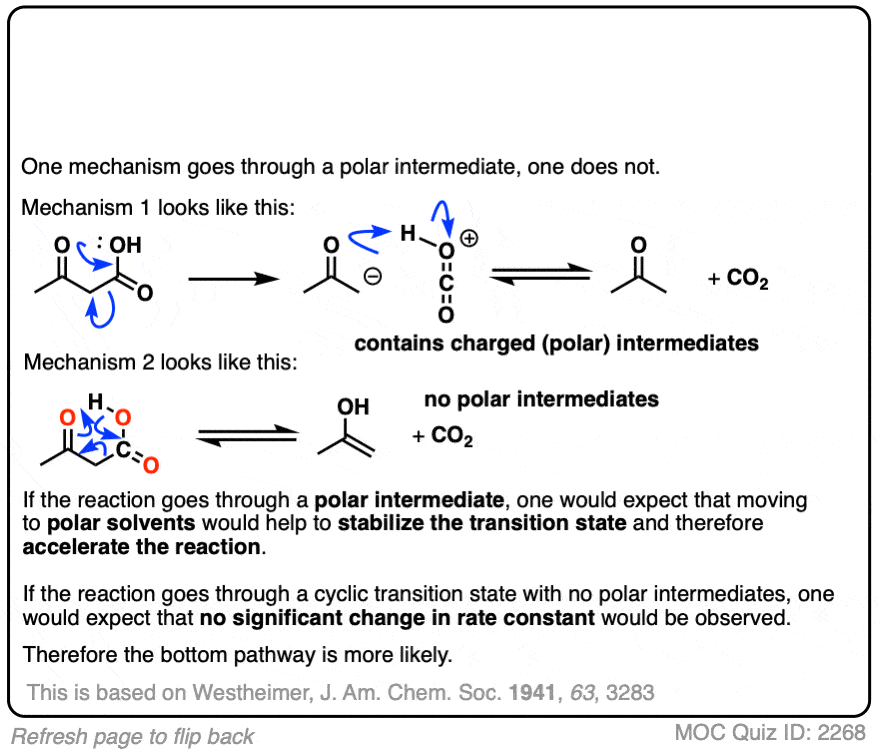
这是一个重要的脱酸实验建立循环机制。
整个故事更有趣。(裁判]
在科尔伯合成,一个羧酸接受电子,导致公司的损失2和两个分子耦合在一起通过一个激进的过程。
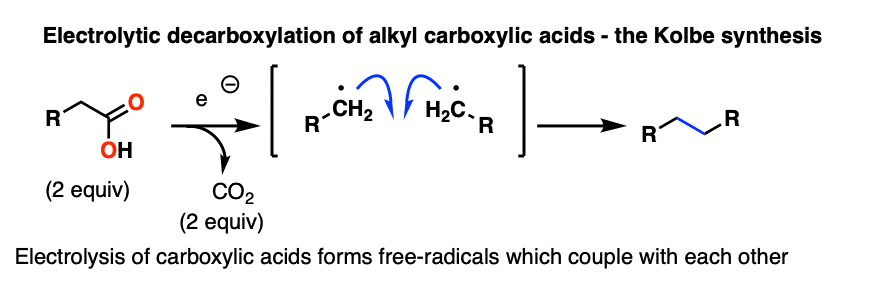
这是一个地区未来的有机化学教科书将重写。后基本上忽略了几十年来,电化学正在复兴。一个非常有趣的有机化学的前沿在羧酸和通过电化学过程耦合在一起的金属添加剂,会节省很多中间氧化/还原步骤。请继续关注。
这是一个非常好的现代(例子裁判]。
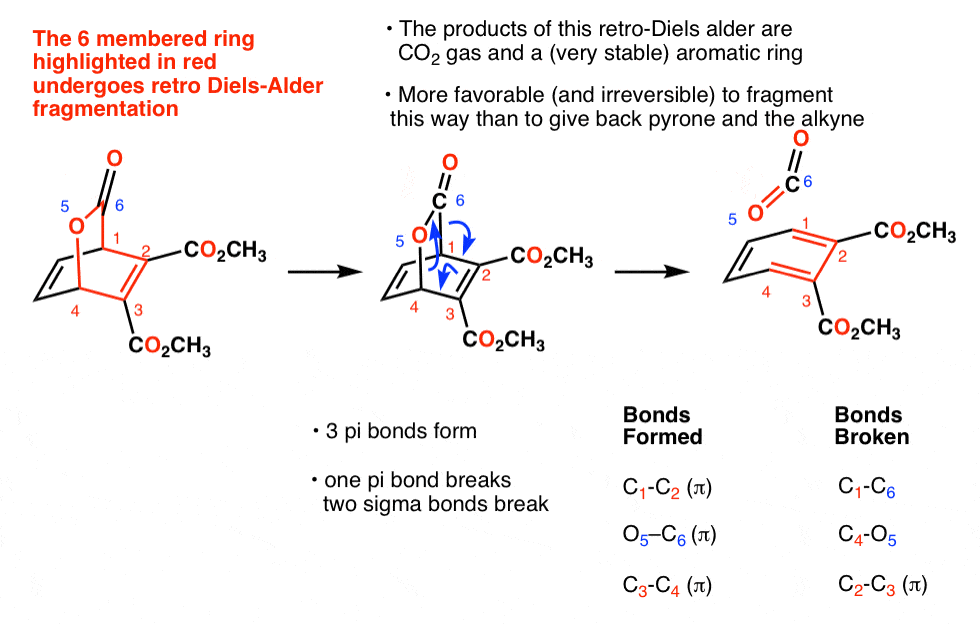
另一个上下文,脱羧出现在复古Diels-Alder吡喃酮的反应。吡喃酮的治疗像electron-poor亲二烯体炔烃其次是复古Diels-Alder导致公司的损失2加一个新芳环。
测试你自己!
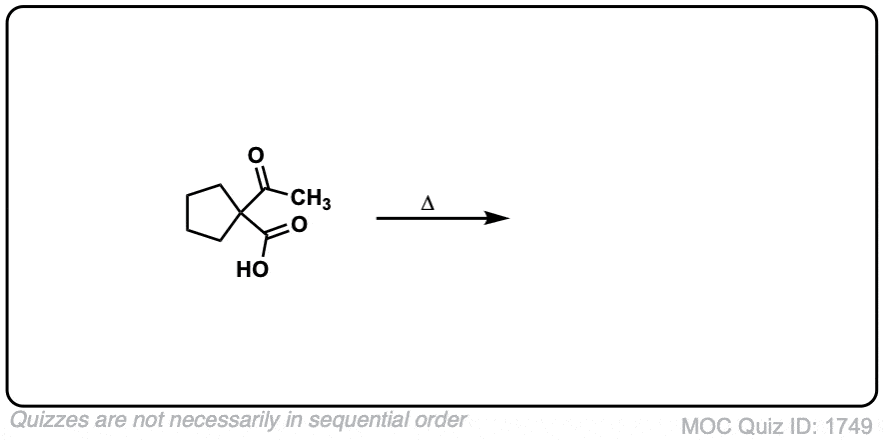 点击翻转
点击翻转
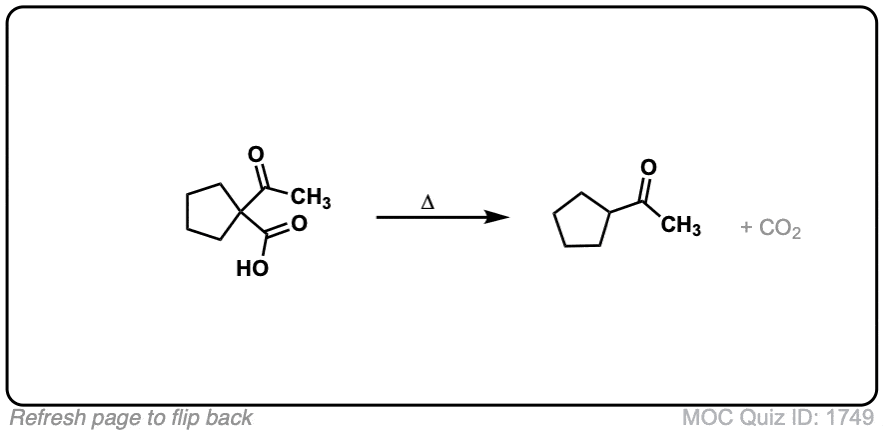
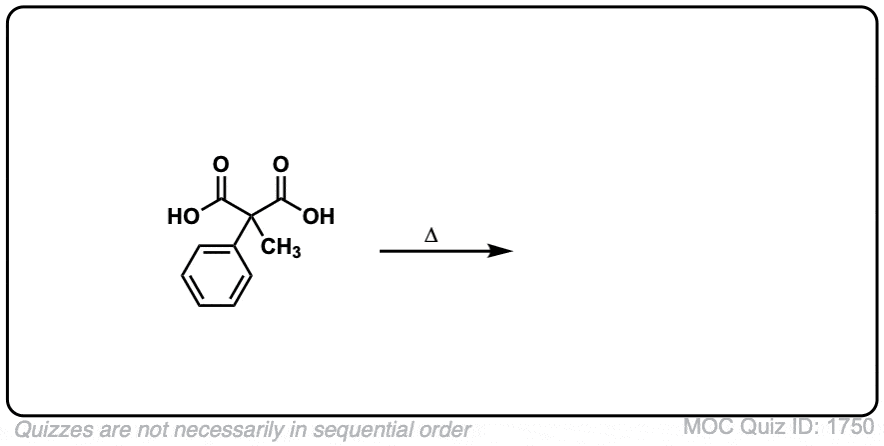 点击翻转
点击翻转
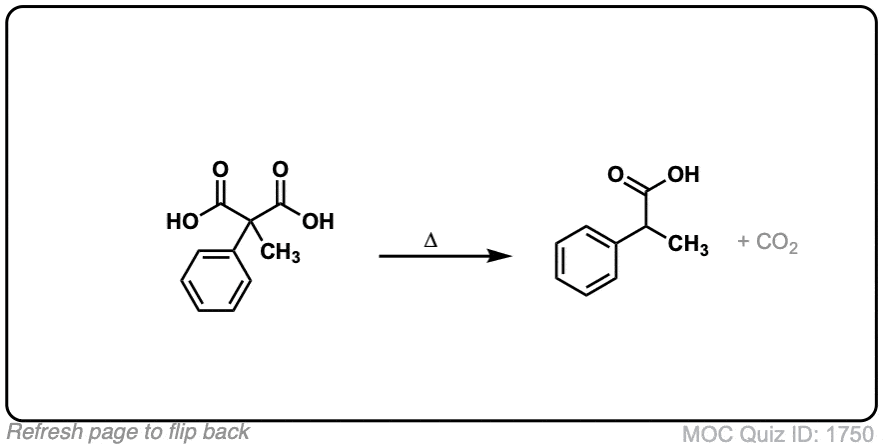
 点击翻转
点击翻转
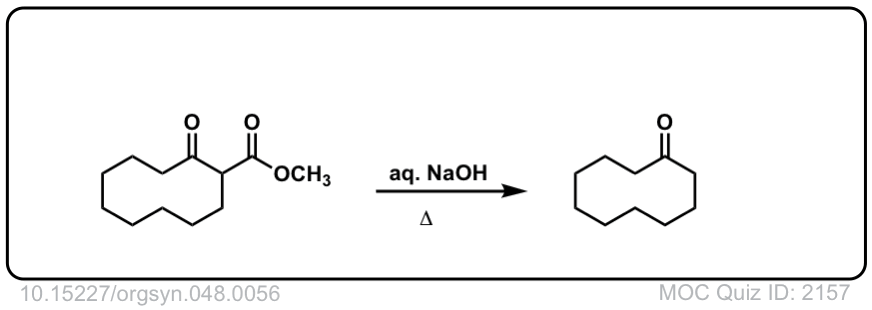
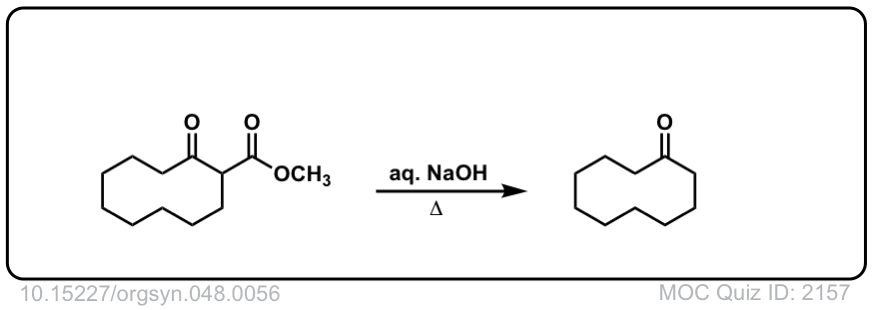
Org。Synth。1968年,48岁,56
链接DOI: 10.15227 / orgsyn.048.0056
 点击翻转
点击翻转
Org。Synth。1965年,45岁,25岁
链接DOI: 10.15227 / orgsyn.045.0025
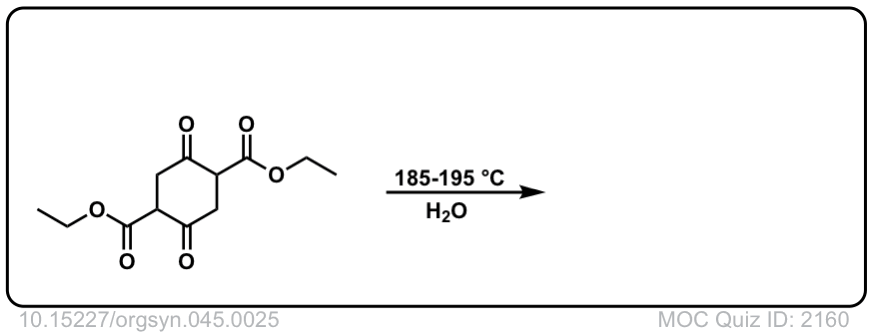 点击翻转
点击翻转
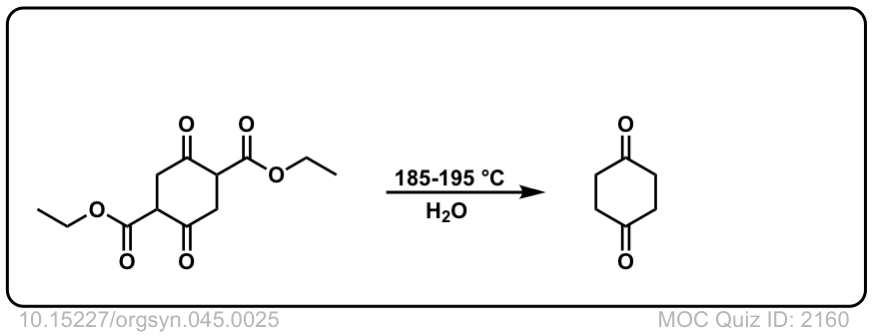
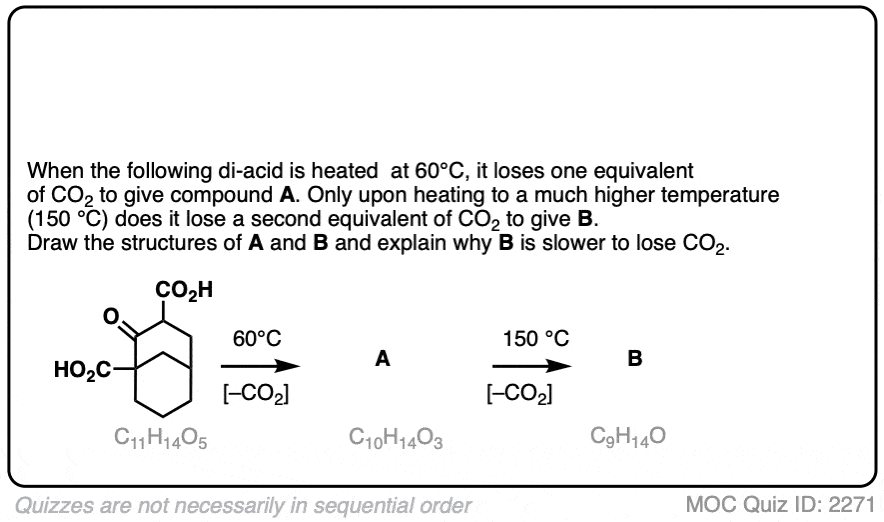 点击翻转
点击翻转
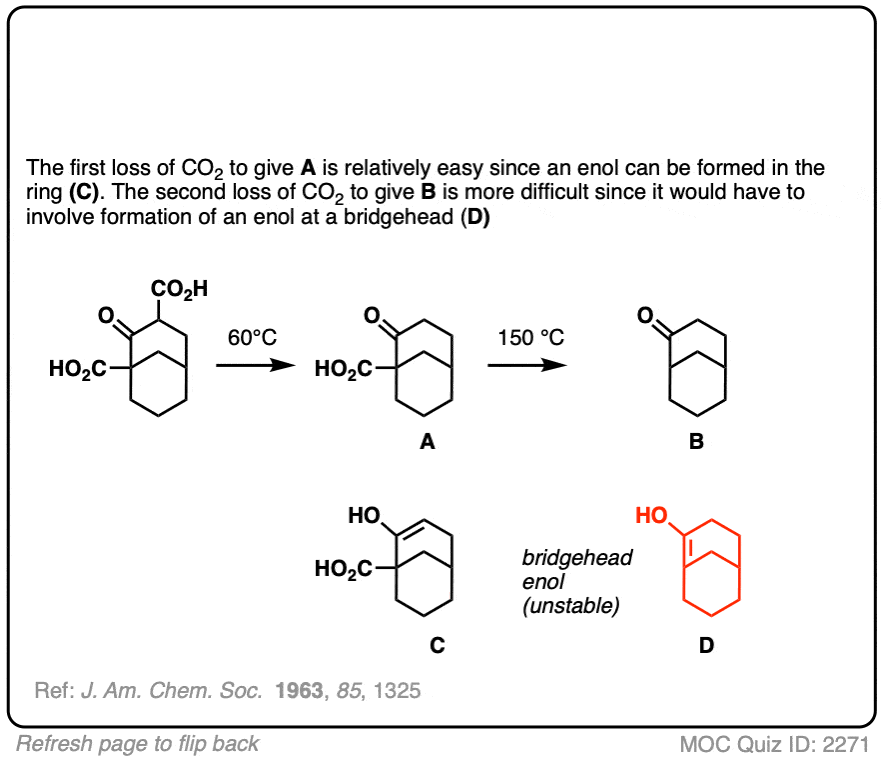
 点击翻转
点击翻转
 点击翻转
点击翻转
(高级)引用和进一步阅读
1。乙酰乙酸进行脱羧反应的酶动力学
r·w·干草和m·a·邦德
澳大利亚化学杂志1967年20岁,1823 - 1828
DOI:10.1071% 2 fch9671823
从文摘:乙酰乙酸CH进行脱羧反应的酶3COCH2有限公司2H→CH3COCH3+有限公司2及其研究了离子在溶液温度的范围。虽然酸分解大约50倍的阴离子37°,活化能酸(23.7千卡的摩尔1)是类似与阴离子(22.9千卡摩尔1)和大反应性的差异是由于一个熵效应。这些结果的意义进行了探讨,比较了与其它β-keto酸脱羧。
2。互变异构平衡乙酰乙酸
凯伦·d·格兰德和斯图亚特·m·罗森菲尔德
有机化学杂志1980年45 (9),1626 - 1628
DOI:10.1021 / jo01297a017
乙酰乙酸的比例烯醇形式是最高的非极性溶剂(CCl 49%4比极性溶剂(2%)2O)。质子溶剂破坏内部氢键中发现的烯醇的形式。
3所示。溶剂对反应速率的影响
f·h·韦斯特海默和w·a·琼斯
j。化学。Soc。1941年,63年,3283年
DOI:10.1021 / ja01857a017
韦斯特海默调查各溶剂的脱酸率。如果脱羧通过收取中间收益,那么它将速度加速度会观察到溶剂具有高介电常数。没有发现明显的速度加速度。这使得韦斯特海默提出脱酸的环状过渡态模型。
4所示。沿着边缘音乐会:动力学和边界的性质一般和特定的酸碱催化
汉娜·r·阿齐兹和丹尼尔·a .单例
美国化学学会杂志》上2017年,139年,5965 - 5972
DOI:10.1021 / jacs.7b02148
一个非常有趣的实验和理论研究beta-keto酸脱羧。研究支持循环机制的存在,质子转移快,但重原子(即C和O)运动缓慢,导致一个动态的“中间”,实际上不是一个能量最低。
这项研究也有一个有趣的回答韦斯特海默的1941年的研究;一致的计算偶极矩(8.40 D)和“逐步”(8.35 D)质子转移事件并不是非常不同的,这意味着我们不应该期望看到显著的加速率的极性溶剂。
5。脱酸的过渡态的性质β-keto酸
马歇尔w·罗格,拉尔夫·m·波拉克维克多p . Vitullo
j。化学。Soc。1975年,97年,6868 - 6869
DOI:10.1021 / ja00856a047
的研究氘同位素效应beta-keto酸进行脱羧反应的酶。
6。过渡态的脱酸β-keto酸和βγ-unsaturated酸
抓绑架J.C.Thurman
四面体的信1967年,8,2377 - 2380
DOI:10.1016 / s0040 - 4039 (00) 71610 - 8
7所示。β-Keto酸进行脱羧反应的酶。二世。调查Bicyclo Bredt规则的[3.2.1]辛烷系统
詹姆斯·p·费里斯和内森·c·米勒
美国化学学会杂志》上1966年88年(15),3522 - 3527
DOI:10.1021 / ja00967a011
脱beta-keto酸的有趣的研究bicyclo[3.2.1]辛烷系统,它在哪里发现脱酸率与离开之间的二面角有限公司2H的π键酮(按预期理想二面角= 90°)。
你好!
§8你讨论库尔修斯重排的酰基叠氮化加热和重新排列成异氰酸酯,在这个过程中失去了N2。
然而,在相应的图,你画一个分子副标题为“酸酰基”…这是一个监督或有另一种解释吗?
你好,是的,这是一个错误!应该“叠氮化”而不是“现在”:-)
假设我合成出一个计划,涉及的形成β酮羧酸作为一个产品(如诺文葛耳Doebner修改的凝结),有什么方法来确保这个不脱羧基酸吗?将低温(如室温)诀窍吗?或者我需要选择一个特定的溶剂系统吗?
取决于结构,但在最后,有很多温和室温协议基本酯水解(LiOH H2O /四氢呋喃)会给你最后羧酸。酸性水解一般包括加热和热脱酸。